文档内容
2025 年下期祁阳一中高一第一次段考化学试题
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、
准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:必修一第一章(人教版2019)。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 K 39 Mn 55 Fe 56
一、选择题(本题共16小题,每小题3分,共48分,每小题只有1个选项符合题意)
1. 逻辑推理是化学学习中常用的科学思维方法,以下四项推理中正确的是( )
A. 电解质在溶液里的复分解反应都是离子反应,离子反应都是电解质在溶液里的复分解反应
B. 酸类物质都有酸性,使溶液呈酸性的化合物都是酸
C. 氧化还原反应的实质是发生电子转移,凡是有电子转移的化学反应都是氧化还原反应
D. 碱类物质都有碱性,使溶液呈碱性的化合物都是碱
【答案】C
【解析】
【详解】A. 电解质溶液之间可以发生复分解反应,也可以发生氧化还原反应,如离子反应2I-+2Fe3+=2Fe2
++I 是氧化还原反应,A错误;
2
的
B. 使溶液呈酸性 化合物不一定是酸,如NaHSO 在水中发生电离:NaHSO=Na++H++SO ,溶液呈
4 4
酸性,但NaHSO 是一种盐,B错误;
4
C. 化合价有变化的反应都是氧化还原反应,化合价变化由电子转移引起的,故氧化还原反应的实质是发
生电子转移,凡是有电子转移的化学反应都是氧化还原反应,故C正确;
D. 使溶液呈碱性的化合物未必是碱,例如NaCO 溶液显碱性,但NaCO 是一种盐,D错误;
2 3 2 3
答案选C。
2. 当光束通过下列物质时,不会出现丁达尔效应的是
① 溶液 ②蔗糖溶液 ③泥水 ④云、雾 ⑤ 胶体 ⑥有色玻璃
A. ①②③④ B. ①②③ C. ②③⑤ D. ④⑤⑥
【答案】B【解析】
【分析】胶体能产生丁达尔效应,据此解答。
【详解】④云、雾、⑤ 胶体、⑥有色玻璃属于胶体,① 溶液、②蔗糖溶液、③泥水不会出
现丁达尔效应,答案选B。
3. 分类对于数以于万计化学物质的作用几乎是无可替代的。下列物质分类的正确组合是
纯净
选项 混合物 酸性氧化物 碱 盐
物
石灰
A 空气 盐酸 CO KAl(SO )
2 水 4 2
B 豆浆 Cu SO 烧碱 NaHCO
3 3
C 稀硫酸 石墨 CO 氨气 CuSO ∙5H O
4 2
生石
D 冰水混合物 SO 纯碱 Cu (OH) CO
灰 2 2 2 3
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.盐酸不是纯净物,石灰水是混合物不是碱,A错误;
B.所有物质的分类都正确,B正确;
C.CO不是酸性氧化物,氨气是碱性气体,不是碱,一水合氨是碱,C错误;
D.冰水混合物是纯净物,纯碱不是碱是盐,D错误;
答案选B。
4. 下列叙述错误的是( )
①溶液是电中性的,胶体是带电的
②使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
③将饱和FeCl 溶液长时间加热,得到的一定是Fe(OH) 胶体
3 3
④溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
⑤江河入海口三角洲的形成通常与胶体的聚沉有关
⑥医疗上的血液透析利用了胶体的性质,而土壤保肥与胶体的性质无关
⑦工厂中常用的静电除尘装置是利用胶体粒子的带电性而设计的
A. ①③④⑥ B. ①②⑤⑥⑦ C. ②③⑤⑥ D. ②⑤⑦
【答案】A【解析】
【详解】①溶液和胶体均为电中性,胶粒能吸附电荷,所以胶粒带电,但胶体不带电,①错误;
②血液属于胶体,使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血,应用了胶体聚
沉的原理,②正确;
③将饱和FeCl 溶液加热,待溶液变为红褐色时即得氢氧化铁胶体,但若长时间加热,由于加热能使胶体
3
聚沉,所以得到的将是氢氧化铁沉淀,③错误;
④溶液中溶质微粒不断无规律的运动,④错误;
⑤河水是胶体,河水胶体遇到海水中的电解质发生了聚沉,日积月累,形成了三角洲,⑤正确;
⑥血液透析原理即为渗析原理,涉及胶体性质,土壤的保肥作用是由于土壤胶粒通常带负电荷,吸附氮肥
中的铵根离子等植物生长所需的营养阳离子,而达到保肥效果,⑥错误;
⑦胶体粒子带电,能向着电场的某一极移动,可以用于工厂的除尘,⑦正确;故答案为:A。
【点睛】Fe(OH) 胶体的制备:向沸水中加入饱和FeCl 溶液,继续加热,待溶液变为红褐色时即得氢氧化
3 3
铁胶体。
5. 下列各选项最后的物质是要制取的物质,其中不可能得到的是
A. 溶液
B. 溶液 沉淀
C.
D. 溶液 HCl溶液
【答案】C
【解析】
【详解】A.碳酸钙高温生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠
反应生成氢氧化钠,A正确;
B.铜在氧气中加热能生成氧化铜,CuO能与硫酸反应生成硫酸铜,硫酸铜能与氢氧化钠反应生成氢氧化
铜沉淀,B正确;
C.高锰酸钾加热会生成氧气,硫在氧气中点燃生成二氧化硫,二氧化硫与水反应生成亚硫酸,而不是硫
酸,C错误;
D.碳酸钡与盐酸反应生成氯化钡,氯化钡与硫酸会反应生成硫酸钡沉淀,D正确;
故选C。6. 下列有关氧化还原反应的叙述正确的是
A. 氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
B. 某金属元素M由化合态变为游离态,M一定被还原
C. 用双线桥表示下列反应的电子转移
D. 非金属单质在反应中只能作氧化剂
【答案】B
【解析】
【详解】A. 氧化还原反应中有一种元素被氧化时,不一定有另一种元素被还原,可能发生自身氧化还原反
应,同种元素化合价既升高,又降低,故A错误;
B. 金属元素只有正价,某金属元素M由化合态变为游离态,M一定被还原,故B正确;
C. 6molHCl中只有5mol作还原剂,用双线桥表示下列反应的电子转移
,故C错误;
D. 非金属元素既有负价也有正价,非金属单质在反应中可能作氧化剂,也可能作还原剂,故D错误;
故选B。
7. 下列条件的溶液中,各组离子一定能够大量共存的是
A. 使酚酞试液变红的溶液: 、 、 、
B. 无色透明溶液中: 、 、 、
C. 可与Mg反应放出氢气的溶液中: 、 、 、
D. pH>7的溶液中: 、 、 、
【答案】D
【解析】
【详解】A.使酚酞溶液变红的溶液中含有大量的OH-,因3OH-+Fe3+=Fe(OH) ↓而不能大量共存,A不合
3
题意;B. 为紫红色离子,无色透明溶液中不可能含有大量的 ,B不合题意;
C.可与Mg反应放出氢气的溶液中含有大量的H+,因H++ =H O+CO↑而不能大量共存,C不合题意;
2 2
D.pH>7的溶液中含有大量的OH-,各离子之间不能发生反应,能大量共存,D符合题意;
故答案为:D。
8. 下列物质转化中,一定需要加入氧化剂才能实现的是
.
A B. C. D.
【答案】B
【解析】
【详解】A. , 的化合价降低,需要加入还原剂,A项错误;
B. , 的化合价升高,需要加入氧化剂,B项正确;
C. ,高锰酸钾既是氧化剂又是还原剂,不需要加入氧化剂,C项
错误;
D. , 的化合价降低,需要加入还原剂,D项错误;
故选B 。
9. 下列离子方程式正确的是
A. 用醋酸清洗铁锈:
B. 向Ba(OH) 溶液中滴加稀硫酸:
2
C. 稀硫酸与铁丝制取氢气:
D. 实验室制备二氧化碳气体:
【答案】D
【解析】
【详解】A.醋酸为弱电解质,不能拆成离子,A错误;
B . Ba(OH) 溶 液 中 钡 离 子 和 氢 氧 根 的 比 为 1∶2 , 正 确 离 子 方 程 式 为 :
2,B错误;
C.稀硫酸与铁丝反应生成硫酸亚铁,生成Fe2+而不是Fe3+,C错误;
D.实验室制备二氧化碳气体的离子方程式为: ,D正确;
故选:D。
10. 酸性溶液中分子或离子的还原性强弱顺序为SO >I->Fe2+>HO>Cl-,据此判断下列反应不可能发生
2 2 2
的是
A. 2Fe3++2H O+SO =2Fe2++SO +4H+
2 2
B. 2Fe2++Cl=2Fe3++2Cl-
2
C. I+SO+2H O=4H++SO +2I-
2 2 2
D. HO+H SO =SO↑+O ↑+2H O
2 2 2 4 2 2 2
【答案】D
【解析】
【分析】
【详解】A.反应2Fe3++2H O+SO =2Fe2++SO +4H+中,S元素的化合价升高,Fe元素的化合价降低,则
2 2
SO 为还原剂,还原性强弱为SO >Fe2+,与已知的还原性强弱一致,故A能发生;
2 2
B.反应2Fe2++Cl=2Fe3++2Cl-中,Fe元素的化合价升高,Cl元素的化合价降低,则Fe2+为还原剂,还原性
2
强弱为Fe2+>Cl-,与已知的还原性强弱一致,故B能发生;
C.反应I+SO+2H O=4H++SO +2I-中,S元素的化合价升高,I元素的化合价降低,则SO 为还原剂,还
2 2 2 2
原性强弱为SO >I-,与已知的还原性强弱一致,故C能发生;
2
D.反应HO+H SO =SO↑+O ↑+2H O中,S元素的化合价降低,O元素的化合价升高,则HO 为还原剂,
2 2 2 4 2 2 2 2 2
还原性强弱为HO>SO ,与已知的还原性强弱矛盾,故D不可能发生;
2 2 2
答案选D。
11. ClO 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO :
2 2
。下列说法正确的是
A. 在反应中失去电子 B. 被氧化C. 在反应中被还原 D. 1个 参加反应有1个电子转移
【答案】D
【解析】
【分析】在反应 中,KClO 中的Cl由
3
+5价降低到+4价,化合价降低,得电子作氧化剂,发生还原反应;HC O 中的C由+3价升高到+4价,化
2 2 4
合价升高,失电子作还原剂,发生氧化反应。
【详解】A.Cl元素的化合价由 价降低为 价,则 在反应中得到电子,故A错误;
B.Cl元素的化合价由 价降低为 价,作氧化剂,被还原,故B错误;
C.C元素的化合价由 价升高到 价,被氧化,则 在反应中被氧化,故C错误;
D.因反应中Cl元素的化合价由 价降低为 价,则1个 参加反应有1个电子转移,故D正确;
故选D。
12. 下列几种导电性变化图像,符合要求的是
A. 图A是向饱和石灰水中不断通入
B. 图B是向 溶液中滴加少量 溶液
C. 图C是向NaOH溶液中通入少量HCl气体
D. 图D是向 溶液中通入适量HCl气体
【答案】C
【解析】【详解】A.向饱和石灰水中不断通入CO,先生成CaCO 沉淀,使溶液的导电性降低,CaCO 再和CO
2 3 3 2
反应生成可溶于水的Ca(HCO ),使溶液的导电性增大,与图中变化不符合,选项A错误;
3 2
B.向 溶液中滴入少量 溶液,反应生成硫酸钡沉淀和水,离子浓度减小,导电能力减小,
与图中变化不符,选项B错误;
C.向NaOH溶液中通入少量HCl气体,发生中和反应生成氯化钠和水,反应前后离子浓度不变,溶液的
导电性不变,选项C正确;
D.向AgNO 溶液通入适量HCl,发生反应生成氯化银沉淀和硝酸,减少的银离子由氢离子补充,溶液中
3
离子浓度基本不变,导电性基本不变,选项D错误;
答案选C。
13. 某地区的雾霾中可能含有 、 、 、 、 、Cl、 、 等离子。某同学
收集雾霾样品,经必要的预处理配成试样溶液,设计如下实验探究其中含有的离子。
①取一定体积的溶液,加入足量 溶液,产生白色沉淀,继续滴加足量盐酸,沉淀不溶解,同时得到
无色气体。
②另取一定体积的溶液,加入足量 溶液,产生白色沉淀,继续滴加足量稀盐酸,沉淀全部溶解。
下列判断不正确的是
A. 操作①中产生的无色气体为 B. 可能含有 、
C. 肯定含有 、 、 D. 一定不存在 、 、
【答案】B
【解析】
【分析】①取一定体积的溶液,加入足量 溶液,产生白色沉淀,可能为BaCO 、BaSO,继续滴加
3 4
足量盐酸,沉淀不溶解,则说明是BaSO、无BaCO ,则无 ,则有 ,则无Ba2+,同时得到无色
4 3
气体为二氧化碳,则说明有 。
②另取一定体积的溶液,加入足量 溶液,产生白色沉淀,可能是Mg(OH) ,则无Fe3+,继续滴加足
2
量稀盐酸,沉淀全部溶解,说明白色沉淀为Mg(OH) ,则有 ,综上可知,一定有 、 、
2,一定无Ba2+、 、 ,可能有Na+、Cl-。
【详解】A.据分析,操作①中产生的无色气体为 ,由碳酸氢根和氢离子反应生成,A正确;
B.据分析,可能含有 ,一定无 ,B不正确;
C.据分析,肯定含有 、 、 ,C正确;
D.据分析,一定不存在 、 、 ,D正确;
选B。
14. 硫化氢的转化是资源利用和环境保护的重要研究课题。将HS和空气的混合气体通入FeCl 、FeCl 和
2 3 2
CuCl 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,不正确的是( )
2
A. 过程①中,生成CuS的反应为HS+Cu2+=CuS↓+2H+
2
B. 过程②中,Fe3+作氧化剂
C. 转化图中化合价不变的元素只有铜和氯
D. 回收S的总反应为2HS+O=2H O+2S↓
2 2 2
【答案】C
【解析】
【分析】由图可知:一共发生的有三个反应①HS+Cu2+=CuS↓+2H+;②CuS+2Fe3+=2Fe2++Cu2++S;③4Fe2+
2
+4H++O =4Fe3++2H O,由此可以推出总反应 2HS+O=2S↓+2H O,再结合氧化还原反应中的基本概念解题。
2 2 2 2 2
【详解】A.根据图中转化可知,生成CuS的反应为HS + Cu2+=CuS↓+ 2H+,A正确;
2
B.过程②中,Fe3+转化为Fe2+,Fe3+为氧化剂,B正确;
C.结合分析中的三个方程式,转化过程中化合价不变的元素除了有铜、氯之外还有氢,C错误;
D.根据图中转化可知,反应物为HS和O,生成物为S,根据原子守恒,还有水生成,总反应是
2 2
2HS+O=2H O+2S↓,D正确;
2 2 2
故选C。15. 已知反应:① ;② ;
③ 。下列说法错误的是
A. 还原性:
B. 反应①中氧化产物和还原产物的个数比为5∶2
C. 已知XO 能将 氧化,当溶液中XO 与 数目之比为1∶6时, 恰好被氧化为 ,X
2 2
在还原产物中的化合价为+4价
D. 可以发生反应:
【答案】C
【解析】
【详解】A.还原剂为在反应中所含元素化合价升高的物质,根据还原剂的还原性大于还原产物,则还原
性由强到弱的顺序为 ,故A正确;
B.反应①中氧化产物为Cl,还原产物为Mn2+,氧化产物和还原产物的个数比为5∶2,故B正确;
2
C.根据题意和得失电子数守恒设X在还原产物中的化合价为m,则2×(6-m)=6×(3-2),解得m=3,
即 对应还原产物中X的化合价为+3价,故C错误;
D.根据选项A中的还原性顺序 ,可以发生 ,故D
正确;
故答案为C。
16. 由铁及其化合物可制得铁红 、氯化铁、绿矾 、高铁酸钾 等物质。
高铁酸钾是一种既能杀菌、消毒,又能絮凝净水的水处理剂,能与水反应生成氢氧化铁和氧气。铁黄可用
作生产磁性材料、颜料的原料。工业制备 的离子方程式为
(未配平)。下列说法不正确的是
A. 每 与水反应,产生B. 中Fe显+6价
C. 的氧化性大于
D. 上述反应中氧化剂和还原剂的化学计量数之比为3:2
【答案】A
【解析】
【分析】 中Fe显+6价,Fe(OH) 变为 升高3价,ClO-变为Cl-降低2价,根据电子守恒,
3
Fe(OH) 与ClO-的计量数之比为2:3,根据元素守恒,电荷守恒,配平该离子方程式为
3
;
【详解】A.KFeO 与水反应的方程式为:4KFeO+10H O=4Fe(OH) ↓+8KOH+3O ↑, 的物质
2 4 2 4 2 3 2
的量为 ,产生0.75molO,质量为0.75mol =24g,故A错误;
2
B.KFeO 中,铁元素的化合价为x,则x+2+4×(-2)=0,解得x=+6,则高铁酸钾中铁显+6价,故B正确;
2 4
C.反应中 是氧化剂, 是氧化产物,故氧化性 > ,故C正确;
D.反应中 是氧化剂,Fe(OH) 是还原剂,由方程式
3
可知,氧化剂和还原剂的化学计量数之比为3:2,
故D正确;
答案选A。
二、非选择题(本题共6小题,每空2分,共58分)
17. 下列物质:① ② ③ ④ ⑤ ⑥酒精⑦ 溶液⑧ ⑨熔融
,请回答下面问题。
(1)属于电解质且能导电的是(填序号)_________。
(2)写出②溶于水的电离方程式:_________。
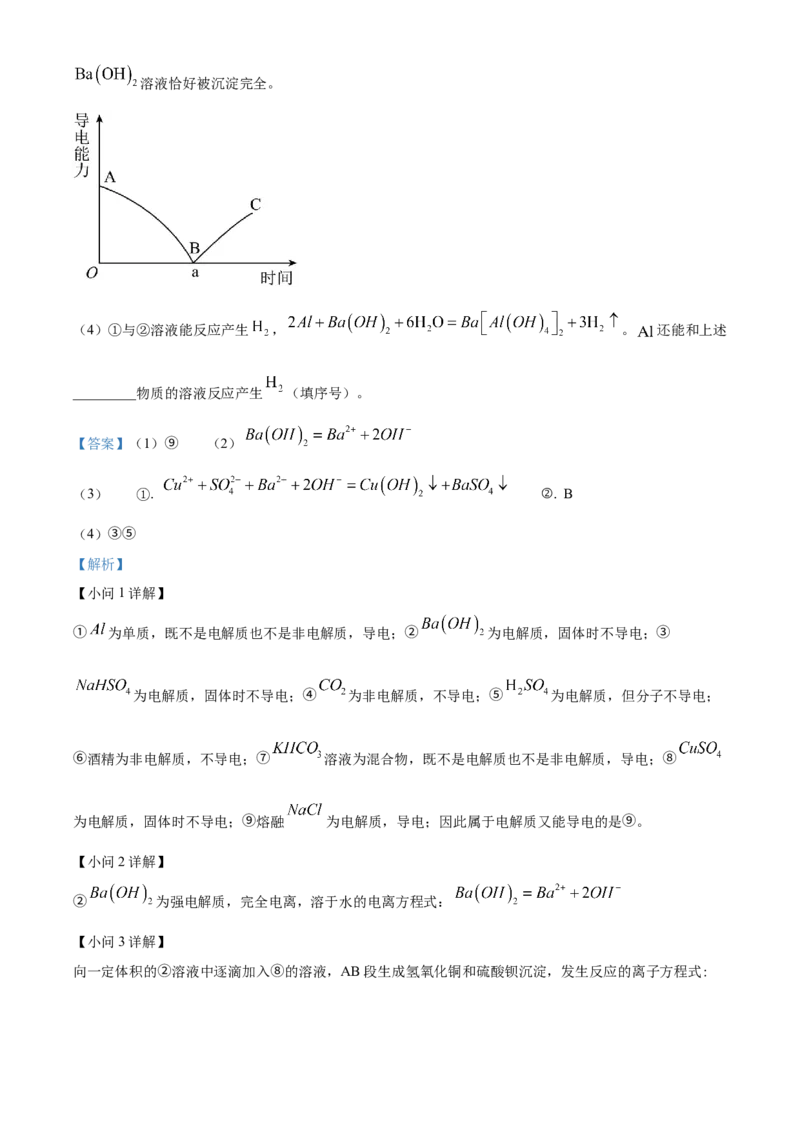
(3)向一定体积的②溶液中逐滴加入⑧的溶液,并测得混合溶液的导电能力随时间变化的曲线如图所示。
写出AB段发生反应的离子方程式:_________;图中_________处(填“A”或“B”或“C”)表示溶液恰好被沉淀完全。
(4)①与②溶液能反应产生 , 。 还能和上述
_________物质的溶液反应产生 (填序号)。
【答案】(1)⑨ (2)
(3) ①. ②. B
(4)③⑤
【解析】
【小问1详解】
① 为单质,既不是电解质也不是非电解质,导电;② 为电解质,固体时不导电;③
为电解质,固体时不导电;④ 为非电解质,不导电;⑤ 为电解质,但分子不导电;
⑥酒精为非电解质,不导电;⑦ 溶液为混合物,既不是电解质也不是非电解质,导电;⑧
为电解质,固体时不导电;⑨熔融 为电解质,导电;因此属于电解质又能导电的是⑨。
【小问2详解】
② 为强电解质,完全电离,溶于水的电离方程式:
【小问3详解】
向一定体积的②溶液中逐滴加入⑧的溶液,AB段生成氢氧化铜和硫酸钡沉淀,发生反应的离子方程式:;图中B表示 溶液恰好被沉淀完全,
导电能力最弱,因为硫酸铜过量以后溶液中有自由移动的离子导电能力增强。
【小问4详解】
还能和③ 反应生成硫酸铝、硫酸钠和氢气;与⑤ 溶液反应产生 和硫酸铝。
18. 分类是认识和研究物质及其变化的一种常用的科学方法,通过分类可以设计物质间的转化途径。“生
活离不开化学”。现有厨房中的下列调味品:①食盐;②小苏打;③面碱(主要成分为 );④食
醋(主要成分为醋酸 );⑤白酒(主要成分为乙醇);⑥白砂糖(主要成分为蔗糖)
(1)主要成分属于酸的是_________(填序号)。
(2) 在水溶液中的电离方程式是_________。
(3)面碱中含有少量 。检验此混合物中 的实验步骤如下:将少量混合物加水溶解后,加入足量
稀硝酸,再加入_________溶液(填化学式),可观察到白色沉淀,说明溶液中存在 ,生成白色沉淀的
离子方程式为_________。
(4)保温瓶中水垢的主要成分之一是 ,利用食醋可以浸泡除去,反应的离子方程式为_________。
【答案】(1)④ (2)
(3) ①. AgNO ②. Ag++Cl-=AgCl↓
3
(4)
【解析】
【小问1详解】
电离时生成的阳离子全部是H+的化合物是酸,则属于酸的为醋酸,即④;
【小问2详解】
NaCO 在溶液中能完全电离,故电离方程式为: ;
2 3
【小问3详解】
面碱中含有少量NaCl,检验此混合物中的Cl-的实验操作步骤如下,将少量混合物加水溶解后,置于试管
中,向试管中先加入足量稀硝酸,无明显现象,再加入AgNO 溶液,可观察到白色沉淀,说明溶液中存在
3Cl-,该反应的离子方程式为:Ag++Cl-=AgCl↓;
【小问4详解】
保温瓶中水垢的主要成分之一是CaCO ,利用食醋可以浸泡除去,醋酸为弱酸,不可拆,应以CHCOOH
3 3
分子形式参与反应,离子方程式为: 。
19. 经检测,某化工厂排出的废水呈酸性,且其中含有大量 Na+、Cu2+、SO 、Cl-、NO 。回答下列问题:
(1)下列离子中,能大量存在于该废水中的是_______(填标号)
A. Ag+ B. Mg2+ C. OH- D. HCO
(2)取100mL该废水于烧杯,逐滴加入NaOH溶液至呈碱性过程中,原废水中存在的离子的量会发生变
化的是Na+、_______(用离子符号表示)。
(3)某化学社团小组成员欲除去废水样品中的Cu2+和SO ,最终得到中性溶液,设计的方案流程如图:
①试剂c为_______(写化学式);溶液3所含溶质离子有Cl-、_______。
②“分离操作”需用到的玻璃仪器主要有_______。
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为_______。
【答案】(1)B (2)H+、Cu2+
(3) ①. NaCO ②. Na+、NO ③. 漏斗、烧杯、玻璃棒 ④. BaCO +2H+=Ba2++H O+CO↑
2 3 3 2 2
【解析】
【小问1详解】
A.Ag+与SO 、Cl-反应生成沉淀,Ag+在指定溶液中大量存在,故A不符合题意;
B.Mg2+在指定溶液中大量存在,故B符合题意;
C.OH-与Cu2+生成蓝色沉淀氢氧化铜,废水显酸性,H+与OH-发生中和反应,不能大量共存,故C不符合
题意;
D.废水显酸性,H+与HCO 反应生成二氧化碳,不能大量共存,故D不符合题意;答案为B;
【小问2详解】
废水显酸性,加入NaOH,H+与OH-发生中和反应,OH-与Cu2+生成蓝色沉淀氢氧化铜,原废水中存在离子
的量发生变化的是Na+、H+、Cu2+;故答案为H+、Cu2+;
【小问3详解】
根据流程,加入试剂a分离操作得到蓝色沉淀和溶液1,则试剂a为NaOH,溶液1中含有离子是Na+、SO
、Cl-、NO ,除去SO 应加入BaCl 或Ba(NO ),试剂b为BaCl 或Ba(NO ),除去过量的Ba2+,不引
2 3 2 2 3 2
入新杂质,应加入碳酸钠,即试剂c为碳酸钠,过滤,向滤液中加入盐酸,除去过量CO ;
①根据上述分析,试剂c为NaCO;溶液3中含有离子是Cl-、Na+、NO ;故答案为NaCO;Na+、NO
2 3 2 3
;
②分离操作的名称为过滤,需要用的玻璃仪器是(普通)漏斗、烧杯、玻璃棒;故答案为(普通)漏斗、烧杯、
玻璃棒;
为
③根据上述分析,白色沉淀 BaCO ,加入盐酸,发生BaCO +2H+=Ba2++H O+CO↑;故答案为
3 3 2 2
BaCO +2H+=Ba2++H O+CO↑。
3 2 2
20. 浓盐酸可以用于实验室制取氯气,其中一种制备方法的化学方程式为
。
(1) 中 的化合价为________。
(2)________(填化学式,下同)是氧化产物,________发生还原反应。
(3)用双线桥法标明电子转移的方向和数目:________。
【答案】(1)+6 (2) ①. Cl ②. K Cr O
2 2 2 7
(3)
【解析】
【小问1详解】
根据化合物中元素化合价代数和为零,铬元素的化合价为+6;
【小问2详解】Cl元素化合价从-1价升高到0价,失去1个电子,氯元素被氧化;Cr元素化合价从+6价降低到+3价,得
到3个电子,被还原,因此KCr O 是氧化剂,发生还原反应,HCl是还原剂,发生氧化反应,则Cl 是氧
2 2 7 2
化产物;KCr O 发生还原反应;
2 2 7
【小问3详解】
根据氧化还原反应中电子转移守恒可知反应中转移6个电子,则用双线桥法标明电子转移的方向和数目可
表示为: 。
21. 某反应中反应物与生成物有: 、 、 、 、 、 和一种未知物
质X。
(1)已知 在反应中得到电子,则该反应的还原剂是___________;
(2)已知2个 在反应中得到10个电子生成X,则X的化学式为___________。
(3)根据上述反应可推知___________。
A. 氧化性: B. 氧化性:
C. 还原性: D. 还原性:
(4)请配平下面反应的反应方程式,并用单线桥法标出转移电子的方向和数目___________。
【答案】(1)
(2)Br (3)AC
2
(4)
【解析】
【小问1详解】
已知 在反应中得到电子,则溴元素化合价降低,根据所给物质可知,As元素化合价升高,故该反应的还原剂是 ;
【
小问2详解】
已知2个 在反应中得到10个电子生成一个X,则溴元素的化合价降低5,溴化合价变为0,故X为
溴单质,化学式为Br ;
2
【小问3详解】
氧化剂氧化性大于氧化产物、还原剂还原性大于还原产物,由化合价可知,氧化剂、氧化产物分别为
、 ,还原剂、还原产物分别为 、Br ;故氧化性:KBrO >H AsO ,还原性:
2 3 3 4
;故选AC;
【小问4详解】
铜与稀硝酸反应生成硝酸铜、水和一氧化氮,根据守恒关系配平:
。
22. 双氧水 和水都是极弱电解质,但 溶液显极弱酸性,若把 看成是二元弱酸,它在水
中的电离方程式: 、 ;医疗上利用它有杀菌消毒作用来清洗伤口。
请回答下列问题:
(1)鉴于 显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”。请写出
与 作用形成的“正盐”的化学方程式:________。
(2)对于下列A∼D涉及 的反应,填写空白:
A.
B.
C.D.
E. (未配平)
① 仅体现还原性的反应是________(填代号)。
②上述反应说明 、 、 氧化性由弱到强的顺序是________。
(3)在 的参与下, 可以与 反应制备 纳米颗粒。若 与 的个数之比为 ,
配平该反应的离子方程式:________。
____ ____ ____ ____ ____ ____ ____
(4)奥运会期间,由于工作人员将84消毒液(NaClO)与双氧水混用,导致游泳池藻类快速生长,池水
变绿。一种可能的原因是 与 反应产生 促进藻类快速生长。该反应的离子反应方程式为:
________。
【答案】(1)HO+Ba(OH) =BaO +2H O
2 2 2 2 2
(2) ①. CE ②. KCrO