文档内容
2024—2025 学年高二期中考试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案字母涂黑,如需改动,
用橡皮擦干净后,再选涂其他答案字母。回答非选择题时,将答案写在答题卡上,写在本试卷
上无效。
3.考试结束后,将本试卷和答题卡一并交回。
考试时间为75分钟,满分100分
可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求。
1.下列物质属于弱电解质的是( )
A. B. C. D.
2.已知反应: ,其他相关数据如下表。
物质
分子中的化学键断裂时吸收的能量 4 3 6
下列说法正确的是( )
A. B. 和 的总能量小于
C. 完全反应放出 热量 D.生成 能量变化小于
3.实现化学反应 可以有以下两条途径,其中 ,
,则 为( )
A. B. C. D.
4.下列说法正确的是( )A. 的反应一定可以自发进行
B.根据反应的自发性可以预测该反应发生的快慢
C.可逆反应正向进行时,正反应具有自发性,则 一定小于零
D.常温下,反应 不能自发进行,则该反应的
5.在反应 中,表示该反应速率最快的是( )
A. B.
C. D.
6.在一固定容积的密闭容器中,充入 和 发生如下化学反应。
,其化学平衡常数(K)与温度(T)的关系如下表。
700 800 830 1000 1200
K
关于该反应的说法正确的是( )
A.
B.在 反应达到平衡时, 气体的转化率约为
C.其他条件不变,降低温度,反应达到新平衡前:
D.在 ,当 时,该反应向逆反应方向进行
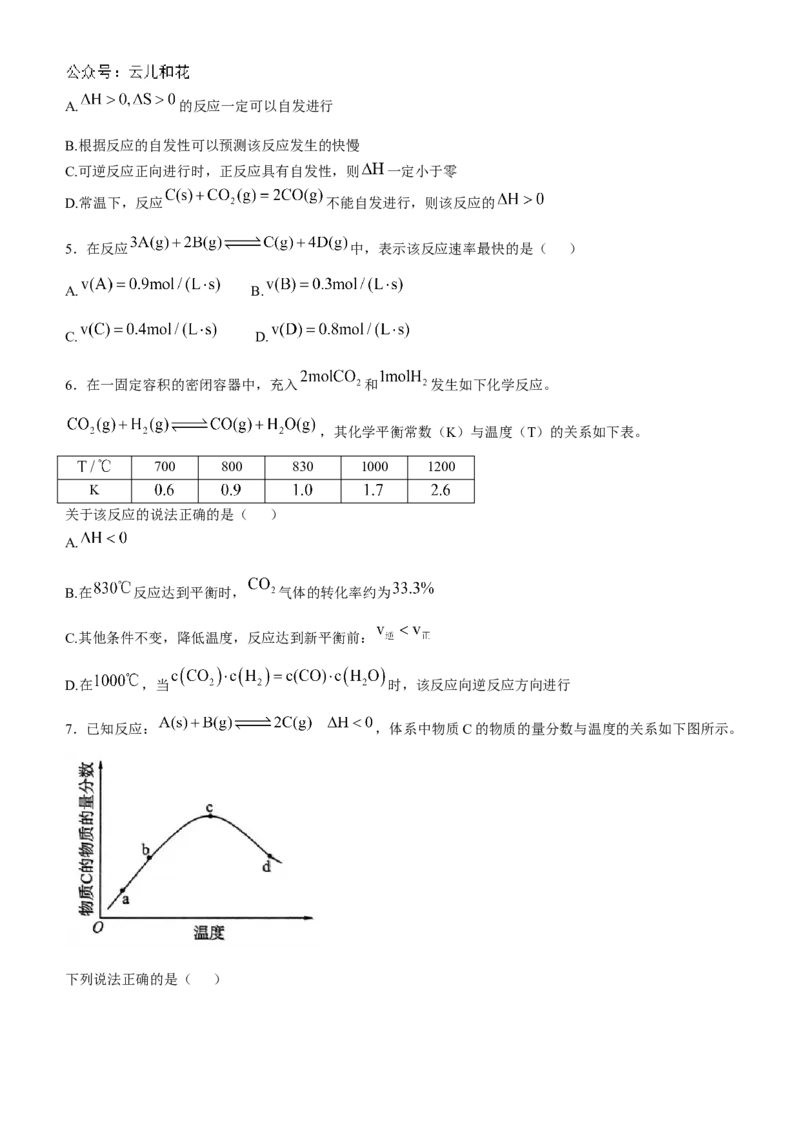
7.已知反应: ,体系中物质C的物质的量分数与温度的关系如下图所示。
下列说法正确的是( )A.其他条件不变时,增大压强,平衡不移动 B.该反应的平衡常数表达式
C.由图可知,b点已达到化学平衡状态 D.化学平衡常数
8. 时,在等体积的① 的 溶液、②0 的 溶液、③ 的
溶液、④ 的 溶液中,发生电离的水的物质的量之比是( )
A. B. C. D.
9.常温时,下列混合溶液的 一定小于7的是( )
A. 的盐酸和 的氨水等体积混合
B. 的盐酸和 的氢氧化钡溶液等体积混合
C. 的醋酸溶液和 的氢氧化钡溶液等体积混合
D. 的硫酸溶液和 的氨水等体积混合
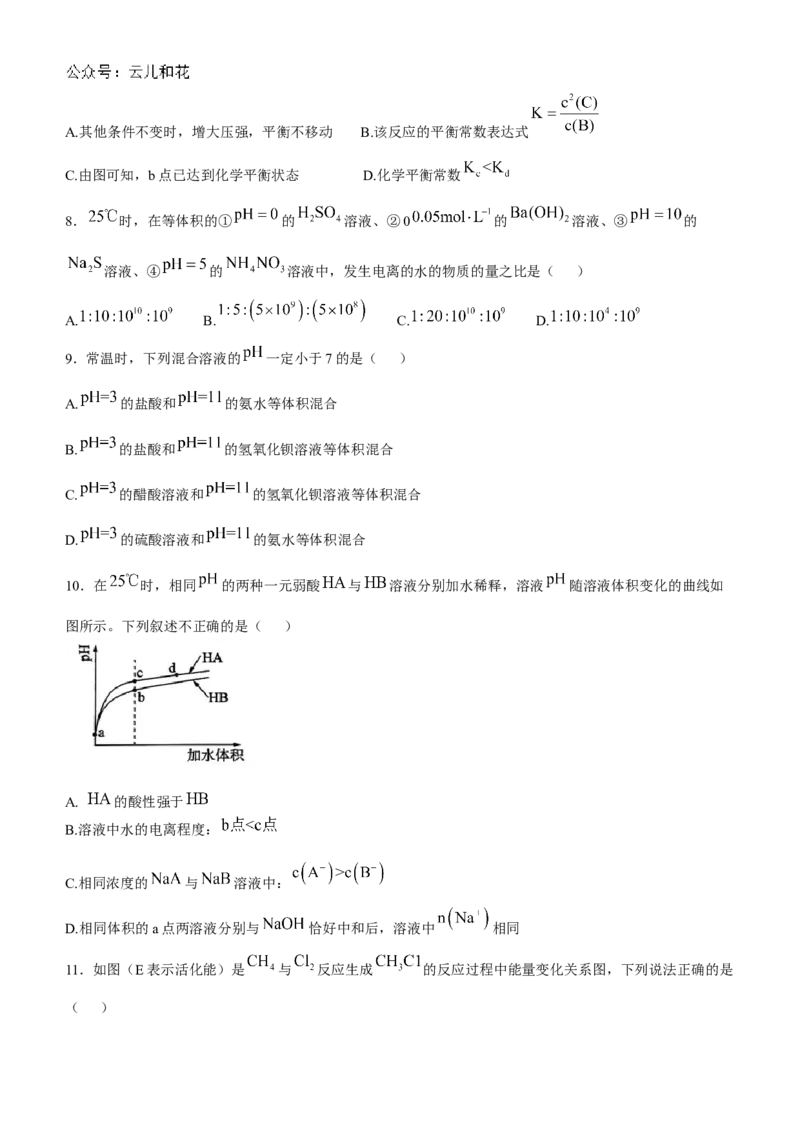
10.在 时,相同 的两种一元弱酸 与 溶液分别加水稀释,溶液 随溶液体积变化的曲线如
图所示。下列叙述不正确的是( )
A. 的酸性强于
B.溶液中水的电离程度:
C.相同浓度的 与 溶液中:
D.相同体积的a点两溶液分别与 恰好中和后,溶液中 相同
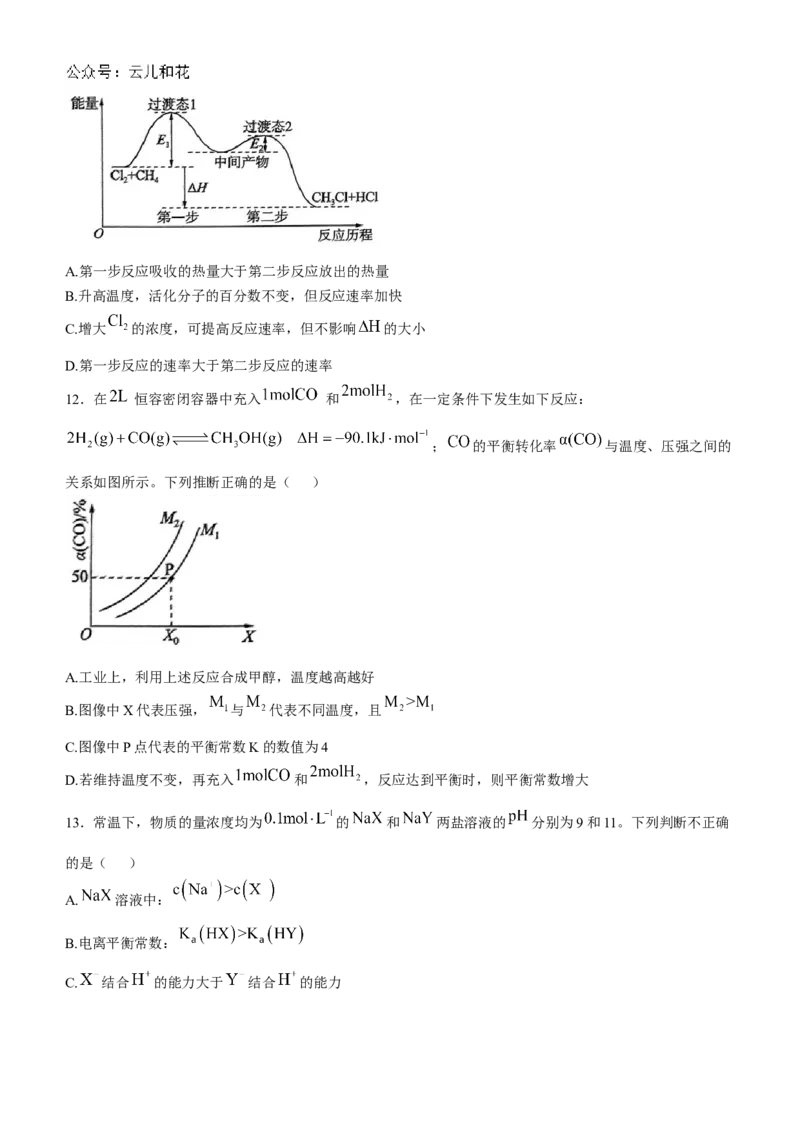
11.如图(E表示活化能)是 与 反应生成 的反应过程中能量变化关系图,下列说法正确的是
( )A.第一步反应吸收的热量大于第二步反应放出的热量
B.升高温度,活化分子的百分数不变,但反应速率加快
C.增大 的浓度,可提高反应速率,但不影响 的大小
D.第一步反应的速率大于第二步反应的速率
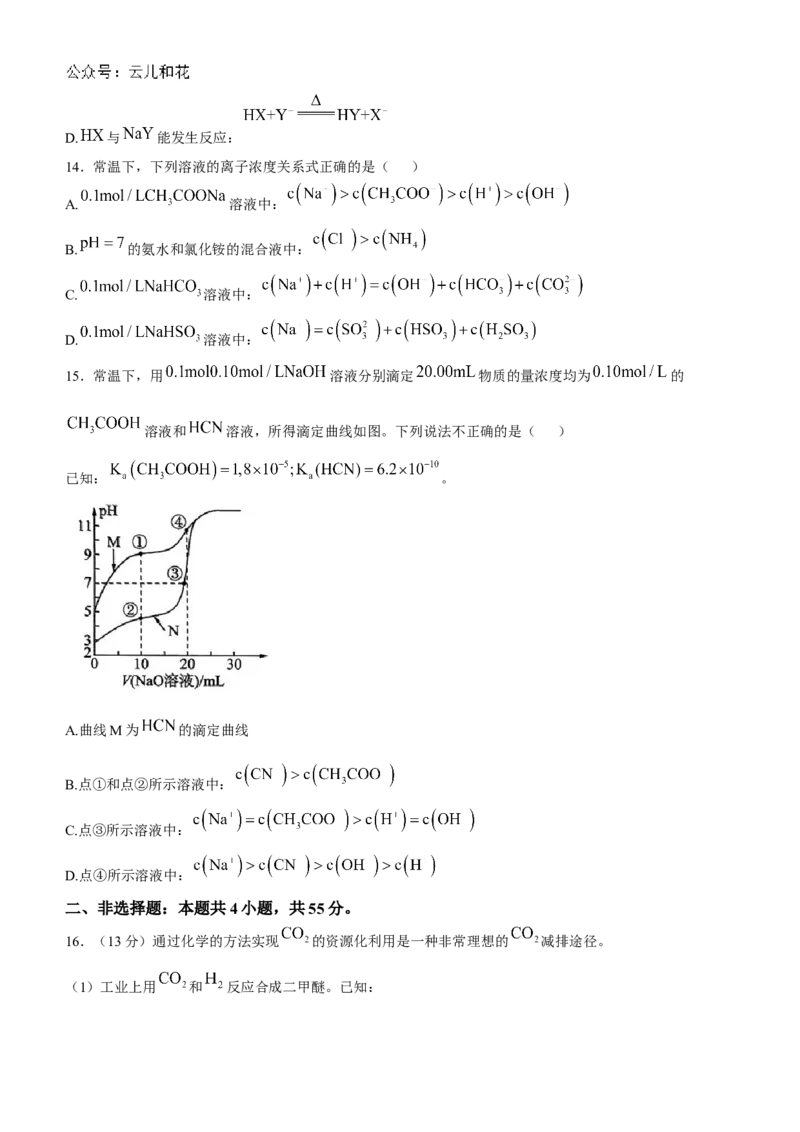
12.在 恒容密闭容器中充入 和 ,在一定条件下发生如下反应:
; 的平衡转化率 与温度、压强之间的
关系如图所示。下列推断正确的是( )
A.工业上,利用上述反应合成甲醇,温度越高越好
B.图像中X代表压强, 与 代表不同温度,且
C.图像中P点代表的平衡常数K的数值为4
D.若维持温度不变,再充入 和 ,反应达到平衡时,则平衡常数增大
13.常温下,物质的量浓度均为 的 和 两盐溶液的 分别为9和11。下列判断不正确
的是( )
A. 溶液中:
B.电离平衡常数:
C. 结合 的能力大于 结合 的能力D. 与 能发生反应:
14.常温下,下列溶液的离子浓度关系式正确的是( )
A. 溶液中:
B. 的氨水和氯化铵的混合液中:
C. 溶液中:
D. 溶液中:
15.常温下,用 溶液分别滴定 物质的量浓度均为 的
溶液和 溶液,所得滴定曲线如图。下列说法不正确的是( )
已知: 。
A.曲线M为 的滴定曲线
B.点①和点②所示溶液中:
C.点③所示溶液中:
D.点④所示溶液中:
二、非选择题:本题共4小题,共55分。
16.(13分)通过化学的方法实现 的资源化利用是一种非常理想的 减排途径。
(1)工业上用 和 反应合成二甲醚。已知:①
②
写出 和 转化为 和 的热化学方程式:
__________________________________________________________________。
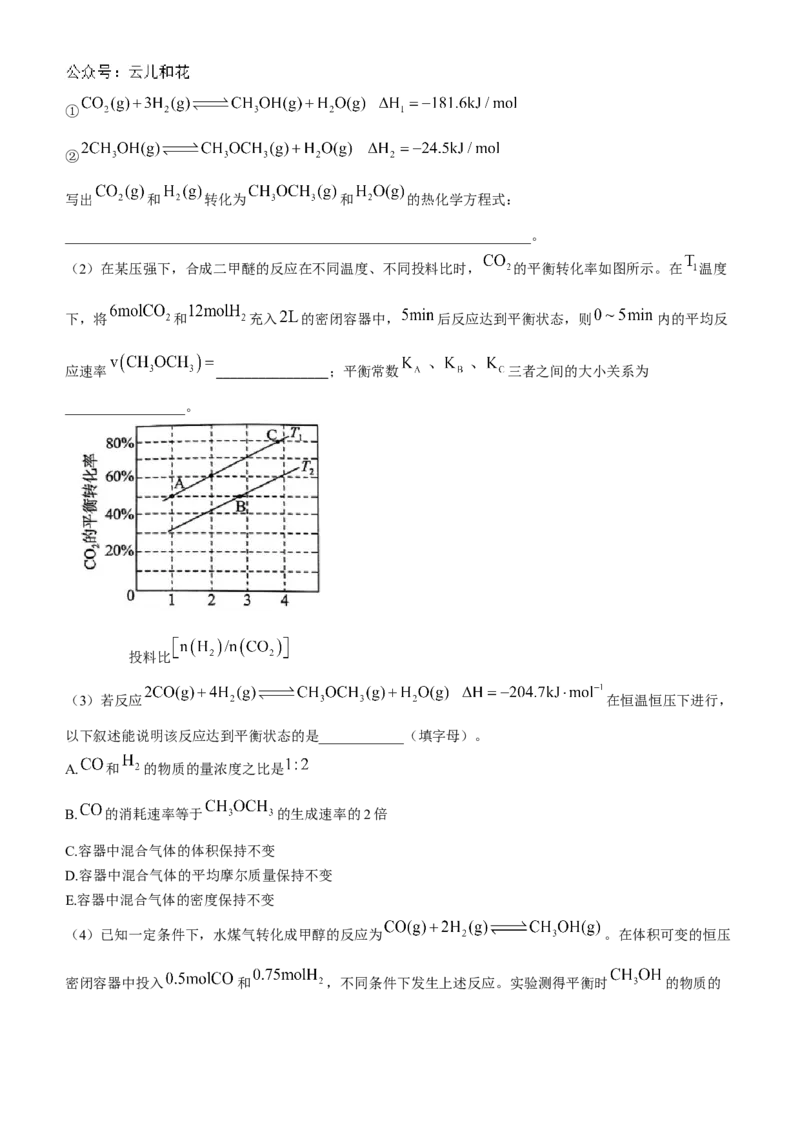
(2)在某压强下,合成二甲醚的反应在不同温度、不同投料比时, 的平衡转化率如图所示。在 温度
下,将 和 充入 的密闭容器中, 后反应达到平衡状态,则 内的平均反
应速率 ________________;平衡常数 三者之间的大小关系为
_________________。
投料比
(3)若反应 在恒温恒压下进行,
以下叙述能说明该反应达到平衡状态的是____________(填字母)。
A. 和 的物质的量浓度之比是
B. 的消耗速率等于 的生成速率的2倍
C.容器中混合气体的体积保持不变
D.容器中混合气体的平均摩尔质量保持不变
E.容器中混合气体的密度保持不变
(4)已知一定条件下,水煤气转化成甲醇的反应为 。在体积可变的恒压
密闭容器中投入 和 ,不同条件下发生上述反应。实验测得平衡时 的物质的量 随温度 、压强 的变化如图所示。
① _________ (填“<”或“>”)。
②M点对应的平衡混合气体的体积为 ,则 时,该反应的平衡常数 ____________, 的转化率
为__________(计算结果保留1位小数)。
17.(14分)研究 在海洋中的转移和归宿是当今海祥科学研究的前沿领域。
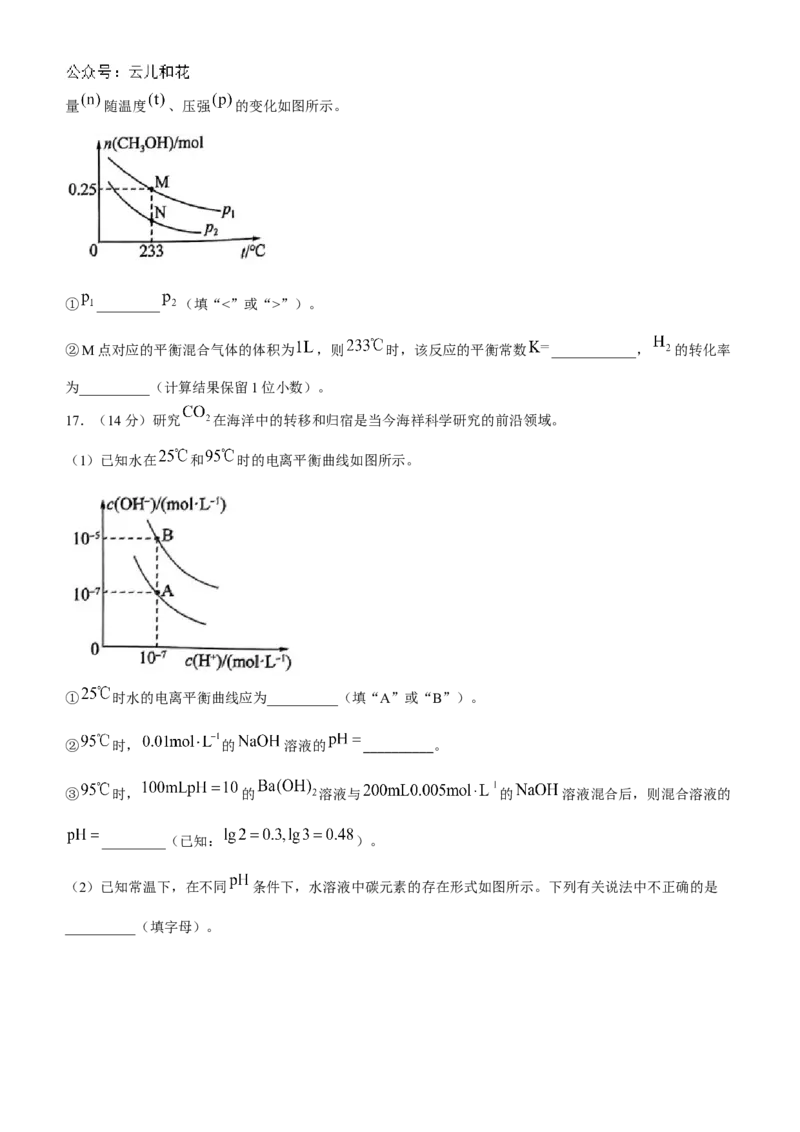
(1)已知水在 和 时的电离平衡曲线如图所示。
① 时水的电离平衡曲线应为__________(填“A”或“B”)。
② 时, 的 溶液的 __________。
③ 时, 的 溶液与 的 溶液混合后,则混合溶液的
_________(已知: )。
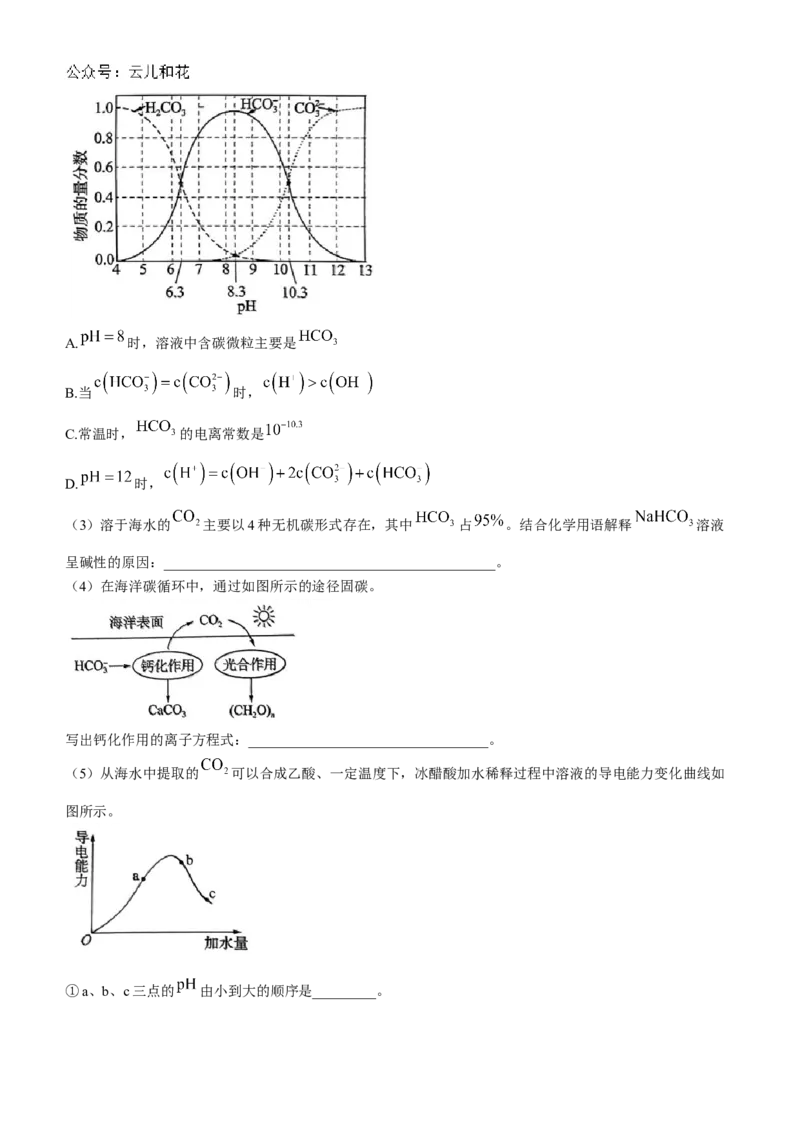
(2)已知常温下,在不同 条件下,水溶液中碳元素的存在形式如图所示。下列有关说法中不正确的是
__________(填字母)。A. 时,溶液中含碳微粒主要是
B.当 时,
C.常温时, 的电离常数是
D. 时,
(3)溶于海水的 主要以4种无机碳形式存在,其中 占 。结合化学用语解释 溶液
呈碱性的原因:_______________________________________________。
(4)在海洋碳循环中,通过如图所示的途径固碳。
写出钙化作用的离子方程式:__________________________________。
(5)从海水中提取的 可以合成乙酸、一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如
图所示。
①a、b、c三点的 由小到大的顺序是_________。②若使c点溶液中的 增大,可以采取下列措施中的_________(填字母)。
A加热 B.加很稀的 溶液 C.加 固体 D.加水
E.加入 固体 F.加入锌粒
18.(14分)Ⅰ.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(1)实验室在保存 溶液时,常在溶液中加少量的________,以抑制其水解;把 溶液蒸干并灼烧,
最后得到的固体主要产物的名称是_________。
(2)在日常生活中经常用 和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
______________________________。
Ⅱ.已知,常温下几种物质的电离平衡常数如下表。
化学式
电离平衡常数
(3) 时, 溶液显________性, 溶液的 _________7(填“大于”或“小
于”)。
(4)物质的量浓度均为 的这4种溶液:① 溶液,② 溶液、③
溶液、④ 溶液,按要求从大到小排序:
________________(填序号,下同); ___________________。
(5) 时,若氨水的浓度为 ,则溶液中的 ____________ 。将 通入该
氨水中,当 降至 时,溶液中的 ___________。
19.(14分) 应用广泛。利用工业废碱渣(主要成分 )吸收硫酸厂尾气中的 制备无水
的成本低、优势明显,其流程如下所示。已知:① 溶液的 约为 ;
②吸收过程中,当吸收塔中 约为5时,吸收液进入中和器。
(1) 的第一步电离方程式为______________________________________。
(2)中和器中发生的主要反应的离子方程式为____________________________________。
(3)为了促进 结晶,中和器中加入过量的 。请结合化学用语,从平衡移动的角度解释:
____________________________________。
(4)写出 溶液中离子浓度由大到小的顺序:__________________________________________。
(5)检验成品质量。①取少量成品溶解,_______________,说明成品中含 。请补全操作与现象。
②可用碘量法测定成品中 的含量,过程如下:
ⅰ.将 成品溶于水配成 溶液,取 于碘量瓶中,并调至弱酸性;
ii.加入 的碘标准液 ,盖上瓶塞,缓慢振荡使其充分反应;
iii.用 的 标准液滴定至溶液呈淡黄色时,加入 淀粉指示剂,继续滴定至终点,消耗
标准液 。(已知: )
a.滴定终点的现象是_________________________________________________。
b.成品中 的质量分数是______________。2024—2025 学年高二期中考试
化学参考答案及评分意见
1.C 【解析】氯化钠在水溶液中完全电离,属于强电解质,故A不符合题意;氢氧化钠在水溶液中完全电
离,属于强电解质,故B不符合题意;一水合氨在水溶液中部分电离,属于弱电解质,故C符合题意;硫酸
在水溶液中完全电离,属于强电解质,故D不符合题意。
2.A 【解析】断键时吸热、成键时放热,则 ,得 ,A正确;反应物具
有的总能量大于生成物具有的总能量,该反应为放热反应,则 和 的总能量大于 ,B错
误; 与 完全反应生成 时放出 热量,C错误; 的能量
比 的能量高,则生成 的能量变化大于 ,D错误。
3.B 【解析】根据盖斯定律
;B正确。
4.D 【解析】 ,反应自发进行,若 ,则在低温下 可能大于0,反应非自发,A
项错误;反应的自发性不能确定反应的快慢,B项错误;可逆反应正向进行时,若 ,则 且高
温条件下正反应具有自发性,C项错误;反应非自发进行, ,反应 ,要满足
,则 ,D项正确。
5.C 【解折】A. ,转化为 ;
B. ,转化为 ;
C. ;
D. ,转化为
C中数值最大,反应速率最快。
6.B 【解析】由题干表中数据可知,升高温度,平衡常数增大,说明升高温度,化学平衡正向移动,故,A错误;设在 反应达平衡时, 气体转化的物质的量为 ,容器的体积为V,则
起始量 2 1 0 0
转化量 x x x x
平衡量 x x
由表中数据可知,在 时 ,故反应达到平衡时, ,解得 ,故
气体的
转化率约为 ,B正确;由A项分析知,该反应的正反应是一个吸热反应,故其他条
件不变,降低温度,反应达到新平衡前,平衡逆向移动,故有: ,C错误;由表中数据知,在
时 ,当 时,即 ,该反应向正反
应方向进行,D错误。
7.B 【解析】该反应的正反应是气体体积增大的反应,在其他条件不变时,增大压强,化学平衡向气体体
积减小的逆反应方向移动,A错误;该反应的平衡常数表达式 ,B正确;在b点以后随着温度的升
高,C的物质的量分数还在增大,说明反应正向进行,b点未达到平衡状态,C错误;在其他条件不变时,升
高温度,化学平衡向吸热的逆反应方向移动,导致化学平衡常数减小。由于温度: ,所以化学平衡常数:
,D错误。
8.A 【解析】 与 均抑制水的电离, 与 均促进水的电离。 的
溶液中:; 的 溶液中:
; 的 溶液中:
; 的 溶液中: ,
由于是等体积,则其物质的量之比为 ,故A正确。
9.C 【解析】 的盐酸中 , 的氨水中 ,
是弱电解质,两溶液等体积混合后,氨水剩余,所得溶液呈碱性, ,A错误; 的
盐酸和 的氢氧化钡溶液等体积混合,恰好完全反应,所得溶液呈中性, ,B错误;
的醋酸溶液和 的氢氧化钡溶液等体积混合,醋酸剩余,所得溶液呈酸性, ,C正确;
的硫酸溶液和 的氨水等体积混合,氨水剩余,所得溶液呈碱性, ,D错误。
10D 【解析】 的酸性强于 ,A正确;b点表示酸电离出氢离子浓度更大,对水的电离抑制作用更大,
则溶液中水的电离程度:b点 点,B正确; 的酸性强于 ,根据越弱越水解可知,相同浓度的
与 溶液中 的水解程度更大,则 ,C正确; 的酸性强于 ,相同 的
两种一元弱酸 与 溶液中, 溶液的浓度大于 溶液的,则相同体积的a点两溶液分别与
恰好中和后,由 所得溶液中的 大,D错误。
11.C 【解析】反应物的总能量高于生成物的总能量,该反应为放热反应,所以第一步反应吸收的热量小
于第二步反应放出的热量,A项错误;升高温度,活化分子的百分数增加,反应速率加快,B项错误;反应
的焓变和反应的途径无关,只与反应的始态和终态有关,则增大反应物的浓度,不改变焓变大小,但提高反
应速率,C项正确;第一步反应的活化能大于第二步反应的活化能,所以第一步反应的速率小于第二步反应
的速率,D项错误。
12.C 【解析】该反应的正反应为放热反应,升高温度,虽然化学反应速率加快,但平衡逆向移动,甲醇
的产率减小,A项错误;图像中X代表压强, 与 代表温度且 ,B项错误;图像中P点表示
的平衡转化率为 ,列三段式可得,平衡常数 ,C项正确;
若温度不变,则平衡常数不变,D项错误。l3.C 【解析】浓度均为 的 溶液的 为9,则说明 为强碱弱酸盐,即 发生水解,
故 溶液中有: ,A正确;浓度均为 的 和 两盐溶液的 分别
为9和11,说明 的水解程度小于 ,根据越弱越水解规律可知,酸性 ,即电离常数:
,B正确;由B项可知,酸性 ,故 结合 的能力小于 结合 的能力,
C错误;由B项分析可知,酸性 ,根据强酸制弱酸的规律可知, 与 能发生反应:
,D正确。
14.D 【解析】醋酸钠溶液中存在醋酸根离子的水解,溶液显碱性,则 ,A错误;混合
液中存在电荷守恒 ,溶液的 为7,则 ,则
,B错误;溶液中存在电荷守恒 ,
C错误;溶液中存在物料守恒: ,即 ,D正确。
15.B 【解析】由题干已知信息可知 ,则等浓度的 溶液和
溶液的 , 溶液的更小,故曲线M为 的滴定曲线,A正确;点①和点②所示溶液
加入的 溶液体积相等,点①溶液呈碱性,溶质为等物质的量的 和 ,且 的水解程度
大于 的电离程度,点②溶液呈酸性,溶质为等物质的量的 和 ,且
的电离程度大于 的水解程度,故有 ,B错误;点③溶液呈
中性,则 ,根据电荷守恒得 ,故溶液中有
,C正确;点④溶液中溶质为 ,溶液的 ,溶液
呈碱性,则 ,根据电荷守恒得 ,故溶液中有:
,D正确。16.(13分)
(1) (2分)
(2) (2分) (2分)
(3)CDE(2分)
(4)①>(1分) ②16(2分) (2分)
【解析】(1)根据盖斯定律可知, ,
热化学方程式: 。
(2)根据图像可知, 温度下,当 的投料比为2时,二氧化碳的转化率为 ,反应的
二氧化碳的量为 ,生成二甲醚的量为 ,则 内的平均反应速率
;合成二甲醚的反应为放热反应,温度越高,二氧化碳的
转化率越低,故 。温度越高,平衡常数越小;温度相同,平衡常数相同,故 三者之间
的大小关系为 。
(3)当 和 的物质的量浓度之比是 ,无法说明正、逆反应速率相等,A错误; 的消耗速率与
的生成速率都为正反应速率,不能说明反应达到平衡状态,B错误;反应为气体分子数减少的反
应,在恒压条件下,容器中混合气体的体积保持不变,能说明反应达到平衡状态,C正确;气体的总质量不
变,反应为气体分子数减少的反应,故容器中混合气体的平均摩尔质量保持不变,能说明反应达到平衡状态,
D正确;气体的总质量不变,反应为气体分子数减少的反应,在恒压条件下当达到平衡时,气体的体积不再
改变,混合气体的密度不再改变,能说明反应达到平衡状态,E正确。
(4)①根据 可知,该反应的正反应是气体分子数减小的反应,增大压强,
平衡正向进行,平衡时 的物质的量较大,由图可知, ;
起始 0②根据三段式,转化 可知:
平衡
; 的转化率为 ;
17.(14分)
(1)①A(1分) ②10(1分) ③ (2分)
(2)BD(2分)
(3) 既发生水解,又发生电离,水解使溶液显碱性,电离使溶液显酸性,且水解程度大于电离程度,
所以 溶液呈碱性(2分)
(4) (2分)
(5)① (2分)
②ACEF(2分)
【解析】(1)①水的电离过程为吸热过程,根据图示数据分析,温度越高,水的电离程度越大,故曲线A
对应的温度为 。
②曲线B为 时水的电离平衡曲线,水的离子积为 , 的 溶液中,
,则 。
③ 时, 的 溶液中 ;
的 溶液中 ,
混合后 ,
则 。
(2)由图可知, 时,溶液中含碳微粒主要是 ,A项正确;由图可知,当
时,此时 ,说明 ,B项错误;电离平衡常数只与温度有关,取图中 的点,此时 , ,则常温时 的电离
常数为 ,C项正确; 时,该溶液主要为碳酸盐溶液,根据电荷守
恒可知还有其他阳离子,D项错误。
(4)反应物中含有碳酸氢根离子,生成物为碳酸钙,依据元素守恒以及电荷守恒得出方程式为:
(5)① 的大小与 有关, 大则 小。导电能力与离子浓度有关,在醋酸溶液中离子主要来
源于醋酸的电离,醋酸溶液的导电能力越强,说明 越大,a、b、c三点的 由小到大的顺序是
。
②若使 增大,即促进 的电离平衡向电离方向移动,A、B、C、D、F选项均可以
达到使电离平衡向电离方向移动的目的。B、D项虽然能使 的电离平衡向电离方向移动,但是稀
释占据了主导作用,导致 减小。E项中虽然 的电离受到抑制,但加入的
固体能使 增大,故ACEF符合。
18.(14分)
(1)盐酸(1分) 氧化铝(1分)
(2) (2分)
(3)中(1分) 大于(2分)
(4)④③①②(1分) ②①③④(2分)
(5) (2分) (2分)
【解析】Ⅰ.(1) 是强酸弱碱盐,水解呈酸性,保存 溶液时应加入盐酸抑制其水解。 也
属于强酸弱碱盐, 水解生成 和 ,在溶液蒸干时, 易挥发,生成的氢氧化铝在灼烧时
分解成氧化铝和水,所以最后得到的固体主要产物是氧化铝。
(2) 和 混合溶液中, 和 会相互促进水解生成氢氧化铝沉淀和二氧化碳气体,离子方程式为 。
Ⅱ.(3)从表格中的几种物质的电离平衡常数可知, 的 和 的 是相等的,则
和 的水解程度是一样的,故 溶液显中性。
的 的 , ,即 的水解程度大于 的,故
溶液的 大于7。
(4)① 是强酸弱碱盐,溶液显酸性;② 也是强酸弱碱盐,溶液也显酸性,由于 完
全电离,故酸性比①强;③ 是弱酸弱碱盐,由于 的 和 的 是相
等的,故溶液显中性;④ 是弱碱,溶液显碱性,所以它们的 从大到小顺序是④③①②。题述
四种溶液的物质的量浓度均为 ,其中① 、② 、③ 都是强电解
质,都是完全电离的,④ 是弱碱,是部分电离的,且① 溶液中的 部分水解,②
溶液的酸性会抑制 的水解,③ 是弱酸弱碱盐, 和 相互促进
水解,④ 是弱碱,电离出的 浓度最小,故四种溶液中 的浓度由大到小的顺序为
②①③④。
(5) 时,氨水的 ,若氨水的浓度为 ,则 ,
因为
氨水中 ,所以 。
时, ,若 ,则
,已知 的 ,
则 。
19.(14分)(1) (2分)
(2) (2)
(3) 存在溶解平衡: , 过量使 增大,上
述平衡逆向移动(2分)
(4) (2分)
(5)①滴加过量的盐酸酸化的氯化钡溶液,若产生白色沉淀(2分)
②滴入最后半滴 标准液,溶液由蓝色变为无色,且半分钟内不恢复蓝色(2分)
(2分)
【解析】(1) 为弱酸,第一步电离方程式为 ;
(2)根据题意可知,中和器中主要是将亚硫酸氢钠转化为硫酸钠,同时碳酸氢钠反应得到碳酸钠,主要反应
的离子方程式为: ;(3) 存在溶解平衡:
, 过量使 增大,上述平衡逆向移动;
(4) 溶液中主要为 和 ,由于 在水中既发生电离,也发生水解,但电离程度大
于水解程度,溶液显酸性,则离子浓度由大到小为: ;
(5)①为检验硫酸根离子的存在,需加入盐酸酸化的氯化钡溶液,若产生白色沉淀,证明含有硫酸根离子。
②本实验最后是用 标准液滴定至溶液呈淡黄色时,加入 淀粉指示剂,由于 遇到淀粉溶液显
蓝色,故滴定终点的现象是滴入最后半滴 标准液,溶液由蓝色变为无色,且半分钟内不恢复蓝色;
步骤ii中加入的碘标准液中含有的 ,步骤iii中
标准液消耗的 ,
故与 反应的 ,根据反应方程式 可知,
,
故成品中 的质量分数是