文档内容
2021 年河南省中考化学试卷
注意事项:
1.本试卷共4页,四个大题,25个小题,满分50分,考试时间50分钟。
2.本试卷上不要答题,请按答题卡上注意事项的要求直接把答案填写在答题卡上,答在试
卷上的答案无效。
相对原子质量 H:1 C:12 N:14 0:16 Na:23 Mg:24 Al:27 Cl:35. 5 K:39 Ca:40 Fe:56 Cu:64 Zn:65
Ag: 108
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
1. 河南博物院馆藏丰富。下列相关制作过程中一定发生了化学变化的是
A.玉柄雕琢 B.骨笛打孔 C.彩陶烧制 D.金简刻字
2. 日常生活中,用得最多的材料是有机合成材料。下列不属于有机合成材料的是
A.合金 B.塑料 C.合成橡胶 D.合成纤维
3. 侯德榜是我国制碱工业的先驱。侯氏制碱法中的“碱”是指其化学式为
A. Na C0 B.NaHC0 C. NaOH D. NaCl
2 3 3
4. “84”消毒液的主要辟分是次氯酸钠(NaCIO)。NaCIO中氯元素的化合价为
A. -1 B.+1 C. +5 D. +7
5. 下列物质在氧气里燃烧,能生成有刺激性气味气体的是
A.木炭 B.硫粉 C.铁丝 D.镁条
6. 古籍记载“曾青得铁则化为铜”,指可溶性的铜的化合物与铁反应得到铜,该反应为
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
7. 规范的操作方法是实验安全和成功的保证。下列图示的实验操作的是
A.点燃酒精灯 B.加热液体 C.收集氢气 D.稀释浓硫酸
8. 2021年世界水日主题是“珍惜水、爱护水“。下列说法正确的是
A.地球上的淡水资源十分丰富 B.部分结冰的蒸馏水属于混合物
C.水是由氢分子和氧原子构成的 D.硬水中含有较多可溶性钙、镁化合物
9. 黑火药爆炸时的反应为:S + 2KNO + 3C点燃X + N ↑ + 3C0 ↑。则X是
3 2 2
A.K S B.K SO C. K SO D. K S O
2 2 3 2 4 2 2 3
10. 右图是KNO 和NaCl的溶解度曲线。下列说法正确的是
3
A.KNO 溶解度大于NaCl的溶解度
3
B.t℃时,两种物质的饱和溶液中溶质的质量分数相等
C.30 ℃时,30g NaCl加入到100g水中可得到饱和溶液
D.将40℃时一定质量的KNO 的饱和溶液降温到20 ℃,该溶液 中
3
溶质的质量保持不变
MnO
11. 现有下列反应:①2KMn0 4 Δ K 2 Mn0 4 + Mn0 2 + 0 2 ↑ ;②2KCl0 3 Δ 2 2KCI + 30 2↑ ;
Δ
2NH NO 4H 0 + 2N ↑+〇 ↑。其中适用于实验室制取氧气的是
4 3 2 2 2
A. ①② B. ②③ C. ①③ D.①②③
12. 下列根据某些性质区分一些常见物质的方法错误的是
A.羊毛和涤纶:灼烧闻气味 B.硫酸铵和氯化铵:加熟石灰研磨
C.铜片和黄铜片:相互刻画 D.氧气和二氧化碳:伸入燃着的木条
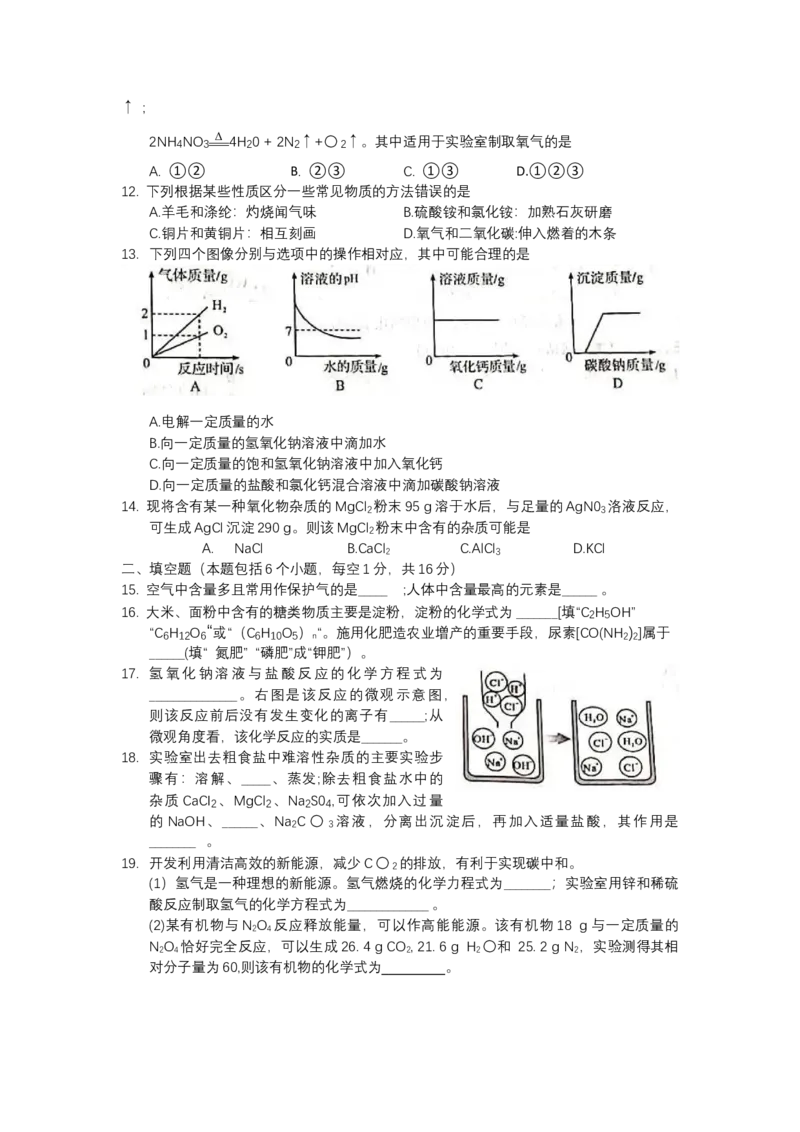
13. 下列四个图像分别与选项中的操作相对应,其中可能合理的是
A.电解一定质量的水
B.向一定质量的氢氧化钠溶液中滴加水
C.向一定质量的饱和氢氧化钠溶液中加入氧化钙
D.向一定质量的盐酸和氯化钙混合溶液中滴加碳酸钠溶液
14. 现将含有某一种氧化物杂质的MgCl 粉末95 g溶于水后,与足量的AgN0 洛液反应,
2 3
可生成AgCl沉淀290 g。则该MgCl 粉末中含有的杂质可能是
2
A. NaCl B.CaCl C.AlCl D.KCl
2 3
二、填空题(本题包括6个小题,每空1分,共16分)
15. 空气中含量多且常用作保护气的是_____ ;人体中含量最高的元素是______ 。
16. 大米、面粉中含有的糖类物质主要是淀粉,淀粉的化学式为_______[填“C H OH”
2 5
“C H O “或“(C H O ) “。施用化肥造农业増产的重要手段,尿素[CO(NH ) ]属于
6 12 6 6 10 5 n 2 2
______(填“ 氮肥” “磷肥”成“钾肥”)。
17. 氢氧化钠溶液与盐酸反应的化学方程式为
_______________。右图是该反应的微观示意图,
则该反应前后没有发生变化的离子有______;从
微观角度看,该化学反应的实质是_______。
18. 实验室出去粗食盐中难溶性杂质的主要实验步
骤有:溶解、_____、蒸发;除去粗食盐水中的
杂质 CaCI 、MgCl 、Na S0 ,可依次加入过量
2 2 2 4
的 NaOH、______、Na C 〇 溶液,分离出沉淀后,再加入适量盐酸,其作用是
2 3
________ 。
19. 开发利用清洁高效的新能源,减少C〇 的排放,有利于实现碳中和。
2
(1)氢气是一种理想的新能源。氢气燃烧的化学力程式为________;实验室用锌和稀硫
酸反应制取氢气的化学方程式为______________。
(2)某有机物与N O 反应释放能量,可以作高能能源。该有机物18 g与一定质量的
2 4
N O 恰好完全反应,可以生成26. 4 g CO , 21. 6 g H 〇和 25. 2 g N ,实验测得其相
2 4 2 2 2
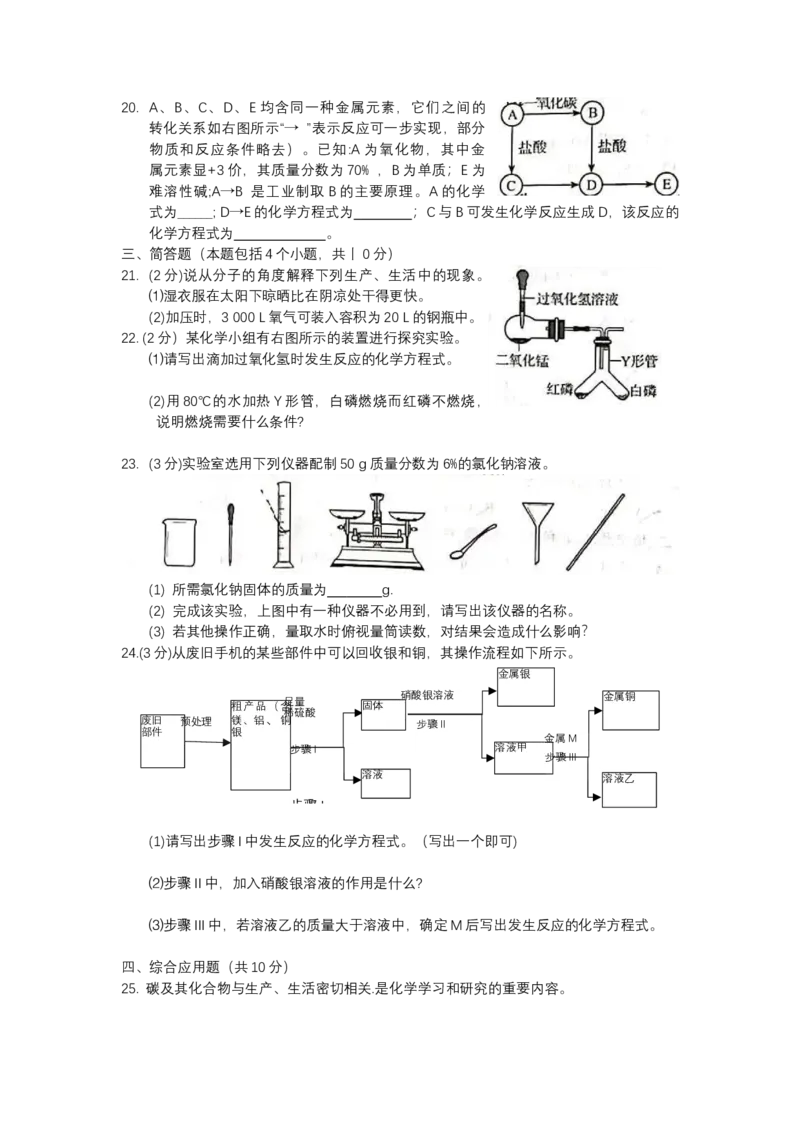
对分子量为60,则该有机物的化学式为 。20. A、B、C、D、E均含同一种金属元素,它们之间的
转化关系如右图所示“→ ”表示反应可一步实现,部分
物质和反应条件略去)。已知:A为氧化物,其中金
属元素显+3价,其质量分数为70% ,B为单质;E为
难溶性碱;A→B 是工业制取B的主要原理。A的化学
式为______; D→E的化学方程式为 ;C与B可发生化学反应生成D,该反应的
化学方程式为 。
三、简答题(本题包括4个小题,共丨0分)
21. (2分)说从分子的角度解释下列生产、生活中的现象。
⑴湿衣服在太阳下晾晒比在阴凉处干得更快。
(2)加压时,3 000 L氧气可装入容积为20 L的钢瓶中。
22. (2分)某化学小组有右图所示的装置进行探究实验。
⑴请写出滴加过氧化氢时发生反应的化学方程式。
(2)用80℃的水加热Y形管,白磷燃烧而红磷不燃烧,
说明燃烧需要什么条件?
23. (3分)实验室选用下列仪器配制50 g质量分数为6%的氯化钠溶液。
(1) 所需氯化钠固体的质量为 g.
(2) 完成该实验,上图中有一种仪器不必用到,请写出该仪器的名称。
(3) 若其他操作正确,量取水时俯视量筒读数,对结果会造成什么影响?
24.(3分)从废旧手机的某些部件中可以回收银和铜,其操作流程如下所示。
金属银
硝酸银溶液 金属铜
粗产品(含 足量 固体
稀硫酸
废旧 预处理 镁、铝、铜 步骤II
部件 银
金属M
步骤I 溶液甲
步骤III
溶液 溶液乙
步骤I
(1)请写出步骤I中发生反应的化学方程式。(写出一个即可)
⑵步骤II中,加入硝酸银溶液的作用是什么?
⑶步骤III中,若溶液乙的质量大于溶液中,确定M后写出发生反应的化学方程式。
四、综合应用题(共10分)
25. 碳及其化合物与生产、生活密切相关.是化学学习和研究的重要内容。(1) 请将右边虚线框内碳原子的结构示意图补画完整。
(2) 金刚石和石墨都属于碳单质,它们的化学性质相似,物理性质
却有很大差异,其原因是 (填字母代号)
a.构成它们的原子大小不同b.两种物质由不同种原子构成
c.构成它们的原子数目不同 d.两种物质里碳原子的排列方式不同.
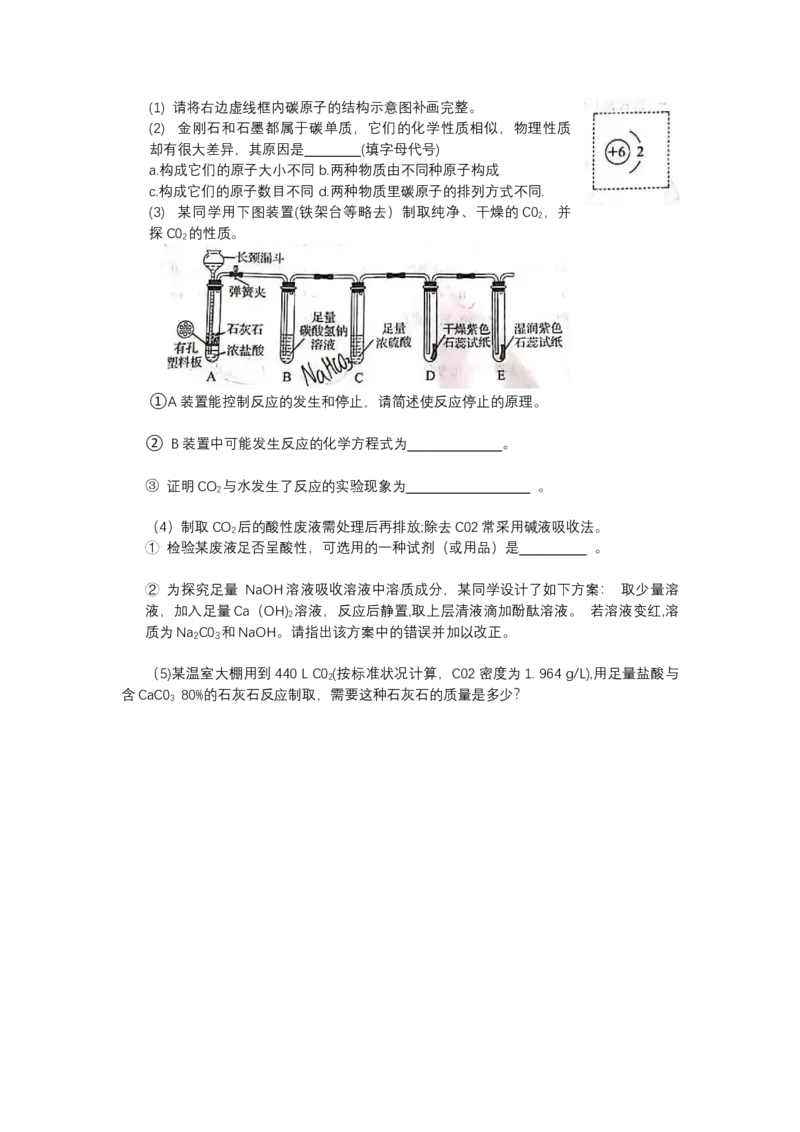
(3) 某同学用下图装置(铁架台等略去)制取纯净、干燥的C0 ,并
2
探C0 的性质。
2
①A装置能控制反应的发生和停止,请简述使反应停止的原理。
② B装置中可能发生反应的化学方程式为 。
③ 证明CO 与水发生了反应的实验现象为 。
2
(4)制取CO 后的酸性废液需处理后再排放;除去C02常采用碱液吸收法。
2
① 检验某废液足否呈酸性,可选用的一种试剂(或用品)是 。
② 为探究足量 NaOH溶液吸收溶液中溶质成分,某同学设计了如下方案: 取少量溶
液,加入足量Ca(OH) 溶液,反应后静置,取上层清液滴加酚酞溶液。 若溶液变红,溶
2
质为Na C0 和NaOH。请指出该方案中的错误并加以改正。
2 3
(5)某温室大棚用到440 L C0 (按标准状况计算,C02密度为1. 964 g/L),用足量盐酸与
2
含CaC0 80%的石灰石反应制取,需要这种石灰石的质量是多少?
32021 年河南省中考化学试卷
参考答案
一、选择题
题 1 2 3 4 5 6 7 8 9 10 11 12 13 14
号
答 C A A B B C D D A B A B D C
案
二、填空题
15、N ; 0
2
16、(C H 〇 ) ;氮肥
6 10 5n
17、HCl+NaOH=NaCl+H 0; Na +、Cl- ;H ++OH-= H O(或 H+与 OH-反应生成 H 0
2 2 2
18、过滤:BaCl ;除去溶液中过滤的NaOH和Na C0
2 2 3
19、⑴ 2H +O 点燃 2H 0; Zn+H S04=ZnS0 +H ↑
2 2 2 2 4 2
(2) C H N :
2 8 2
20、Fe O : 2NaOH+FeCl =Fe(OH) +2NaCl; 2FeCI +Fe= 3FeCl
2 3 2 2 3 2
三、简答题
21、(1)分子在不停的做无规则运动,温度越高,分子匀速速率越快
(2)分子间有间隔,压强越大,分子之间间隔越小
22、⑴ 2H 2 0 2 MnO 2 2H 2 0+0 2 ↑
(2)温度达到可燃物的着火点
23、(1) 3.0g
(2)漏斗
(3)会使量取的水的量偏小,溶质质量分数偏大
24、(1) Mg+H S0 =MgS0 +H ↑或2Al+3H S0 =Al (SO ) +3H ↑
2 4 4 2 2 4 2 4 3 2
(2) 把Cu和Ag固体进行分离(3) Zn+Cu(N0 ) =Zn(N0 ) +Cu
3 2 3 2
四、综合应用题
(2) d
(3) ①当用弹簧夹加紧橡皮管时,继续产生的气体导致压强变大,液体被压回长颈漏斗
固液分离, 反应停止。
②HCI+NaHCO =NaCl+H O+CO ↑
3 2 2
③D中干燥紫色石蕊试纸不变红,E中湿润的紫色石蕊试纸变红
(4)①紫色石蕊(或Zn)
②错误,加入过量的Ca(OH) ;改正取少量的待测液,加入足量的CaCI 溶液,看有
2 2
白色沉淀生成,反应后静置取上层清液滴加无色酚酞,若溶液变红,则溶液中含有
Na C0 和NaOH。
2 3
(5) 解:设需要石灰石的质量为X
CaCO +2HCl=CaCl +H 0+C0 ↑
3 2 2 2
100 44
X×80% (440X1.964) g
则: x=24.55g
答:需要这种石灰石的质量为24.55g。