文档内容
2015年湖北省黄石市中考化学试卷
一、选择题(共16小题,每小题3分,满分48分)
1.(3分)(2015•黄石)下列变化中,发生了化学变化的是( )
A.干冰气化 B.蔗糖溶于水 C.大理石破碎 D.粮食酿酒
2.(3分)(2015•黄石)根据我国环保部颁布的《环境空气质量标准》.下列项目不属于监测范
围的是( )
A.PM B.N C.SO D.NO
2.5 2 2 2
3.(3分)(2015•黄石)下列物质属于纯净物的是( )
A.加碘食盐 B.铅笔芯 C.硫酸铜 D.大冶劲酒
4.(3分)(2015•黄石)下列各种物质中,由分子构成的是( )
A.铝 B.金刚石 C.NaOH D.NH
3
5.(3分)(2015•黄石)高铁酸钠(NaFeO)是一种新型净水剂,高铁酸钠中铁元素的化合价
2 4
为( )
A.+2 B.+3 C.+4 D.+6
6.(3分)(2015•黄石)下列关于自然界中的水的说法正确的是( )
A.地球上的淡水资源取之不尽,用之不竭
B.水体污染的来源主要有工业污染、农业污染和生活污染
C.水分解可以得到氢气,因此水是廉价且清洁的能源物质
D.水的软化是将海水变成可饮用的淡水
7.(3分)(2015•黄石)锌元素的相关信息如图,下列有关锌的说法错误的是( )
A.原子的核电荷数是30 B.黄铜合金中通常含有锌元素
C.锌不能置换稀硫酸中的氢 D.相对原子质量为65.38
8.(3分)(2015•黄石)量筒中盛有一定量的液体.如果将量筒举过头顶读数,则读取的体积
读数与液体实际体积相比( )
A.偏小 B.偏大
C.没有影响 D.与人的身高有关
9.(3分)(2015•黄石)下列物质在空气中强热(或点燃)不能生成CO 的是( )
2
A.石墨 B.石灰石 C.CuO D.CO
10.(3分)(2015•黄石)下列关于金属的说法正确的是( )
A.人类使用金属铝的年代早于铜、铁
1B.“真金不怕火炼”表明金(Au)在高温条件下也很难与氧气反应
C.武德合金的熔点高,可用于制造保险丝
D.将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈
11.(3分)(2015•黄石)对下列日常生活中的现象解释不合理的是( )
生活中的现象 解释
A墙内开花墙外香 分子在不断运动
B乙醇、油漆需要密闭保存 分子质量很小,故液体均易挥发
C湿衣服在阳光下比阴凉处干得快温度升高,分子运动速度加快
D石油气加压可贮存在钢瓶中 分子间有间隔,加压使得间隔缩小
A.A B.B C.C D.D
12.(3分)(2015•黄石)下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
物质所含杂质除去杂质的方法
AO CO 点燃混合气体
2
BNaOHNaCl 加入适量的稀盐酸
CCuO Cu 在纯氢气流中加热
DH 水蒸气 通过盛有浓硫酸的洗气瓶
2
A.A B.B C.C D.D
13.(3分)(2015•黄石)为了验证镁、铜两种金属活动性大小,某同学设计了如图所示的实验,
为了达到试验目的,溶液应该选择( )
A.稀硫酸 B.硫酸镁溶液 C.氯化钠溶液 D.植物油
14.(3分)(2015•黄石)KCl的部分溶解度数值如表,下列说法正确的是( )
温度溶解度(g)
20℃34
30℃37
A.常温下,KCl微溶于水
B.20℃时,100g饱和溶液含有34g溶质
C.将30℃的饱和KCl溶液降温至20℃,会有KCl晶体析出
D .相同质量的水中加入不同质量的KCl,所得溶液的溶质质量分数一定不同
15.(3分)(2015•黄石)下表所列的各基本反应类型对应的化学方程式实例正确的是( )
基本反应类型化学方程式实例
A化合反应 CO+HO═HCO
2 2 3
B分解反应
2KClO 2KCl+3O
2 2
2↑
C复分解反应 KOH+NaCl═KCl+NaOH
D置换反应 Zn+HSO═ZnSO+2H↑
2 4 4 2
A.A B.B C.C D.D
16.(3分)(2015•黄石)“类推”是学习化学的常用方法,下列推理正确的是( )
A.酸和碱生成盐和水的反应属于中和反应,故盐酸和氢氧化钠溶液能发生中和反应
B.酸的溶液pH<7,故pH<7的溶液一定是酸的溶液
C.镁条在空气中燃烧生成白色固体,故铜片在空气中的灼烧也生成白色固体
D.碳可用于炼铁,故碳可用于冶炼所有的金属
二、填空题(共6小题,每小题6分,满分36分)
17.(6分)(2015•黄石)用下列物质的字母序号填空:
A.活性碳 B.二氧化硫 C.高分子材料 D.食醋 E.金属铝 F.氯化钾
(1)可形成酸雨的是 ;
(2)可用于生产食品包装袋的是 ;
(3)可用作钾肥的是 ;
(4)可用于填充防毒面具的是 ;
(5)可用于生产炊具的是 ;
(6)可用于除去水垢的是 .
18.(6分)(2015•黄石)(1)请用化学符号填空:
①2个双氧水分子 ;
②3个氢氧根离子 ;
③标出BaO中Ba元素的化合价 ;
(2)如图表示在一定条件下,物质转化过程的围观示意图,请根据图形信息回答问题:
①CO分子中C、O元素的质量比为 ;
②O2﹣核外电子数为 ;
③该过程的化学反应方程式为 .
19.(6分)(2015•黄石)向100g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量
与生成沉淀的质量之间的关系如图所示,请回答下列问题:
(1)将A点所对应的混合物过滤,滤液中所含溶质为 ;
(2)图中A点所对应的溶液总质量为 g;
(3)求(1)中所得滤液的溶质质量分数(请写出计算过程).
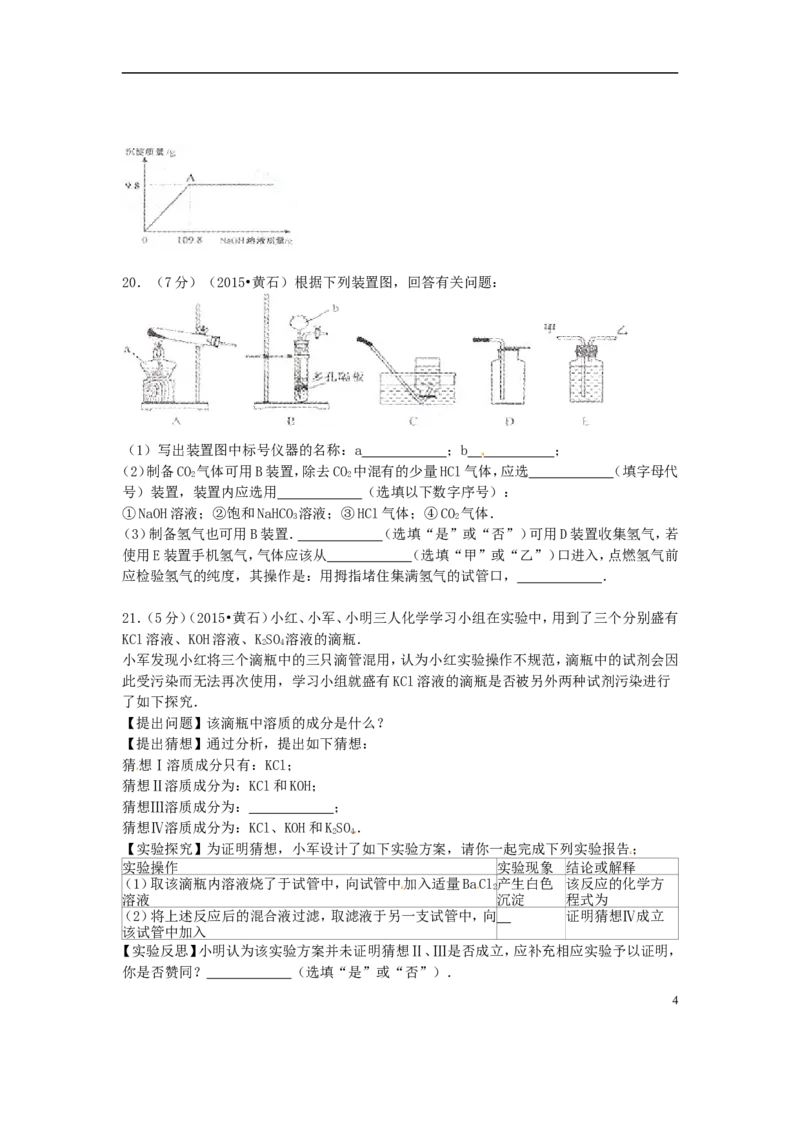
320.(7分)(2015•黄石)根据下列装置图,回答有关问题:
(1)写出装置图中标号仪器的名称:a ;b ;
(2)制备CO 气体可用B装置,除去CO 中混有的少量HCl气体,应选 (填字母代
2 2
号)装置,装置内应选用 (选填以下数字序号):
①NaOH溶液;②饱和NaHCO 溶液;③HCl气体;④CO 气体.
3 2
(3)制备氢气也可用B装置. (选填“是”或“否”)可用D装置收集氢气,若
使用E装置手机氢气,气体应该从 (选填“甲”或“乙”)口进入,点燃氢气前
应检验氢气的纯度,其操作是:用拇指堵住集满氢气的试管口, .
21.(5分)(2015•黄石)小红、小军、小明三人化学学习小组在实验中,用到了三个分别盛有
KCl溶液、KOH溶液、KSO 溶液的滴瓶.
2 4
小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因
此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行
了如下探究.
【提出问题】该滴瓶中溶质的成分是什么?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ溶质成分只有:KCl;
猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为: ;
猜想Ⅳ溶质成分为:KCl、KOH和KSO .
2 4
【实验探究】为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
实验操作 实验现象 结论或解释
(1)取该滴瓶内溶液烧了于试管中,向试管中加入适量BaCl产生白色 该反应的化学方
2
溶液 沉淀 程式为
(2)将上述反应后的混合液过滤,取滤液于另一支试管中,向 证明猜想Ⅳ成立
该试管中加入
【实验反思】小明认为该实验方案并未证明猜想Ⅱ、Ⅲ是否成立,应补充相应实验予以证明,
你是否赞同? (选填“是”或“否”).
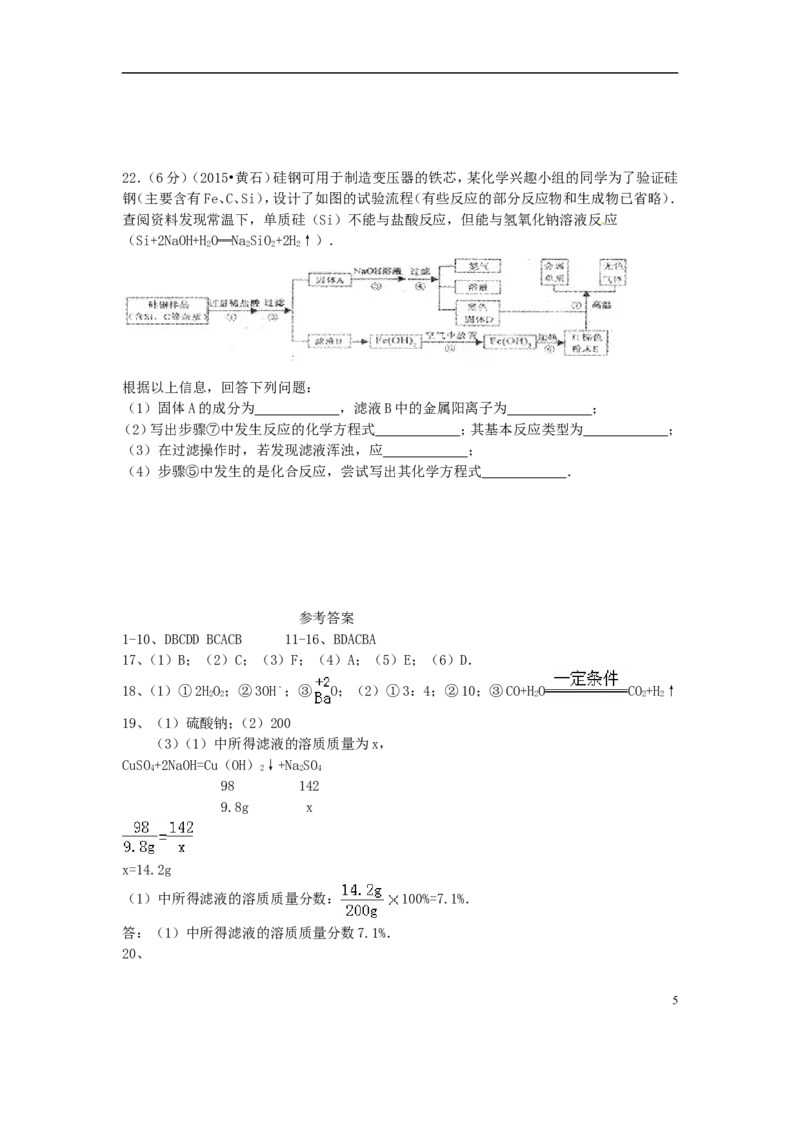
422.(6分)(2015•黄石)硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅
钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).
查阅资料发现常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应
(Si+2NaOH+HO═NaSiO+2H↑).
2 2 2 2
根据以上信息,回答下列问题:
(1)固体A的成分为 ,滤液B中的金属阳离子为 ;
(2)写出步骤⑦中发生反应的化学方程式 ;其基本反应类型为 ;
(3)在过滤操作时,若发现滤液浑浊,应 ;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 .
参考答案
1-10、DBCDD BCACB 11-16、BDACBA
17、(1)B;(2)C;(3)F;(4)A;(5)E;(6)D.
18、(1)①2HO;②3OH﹣;③ O;(2)①3:4;②10;③CO+HO CO+H↑
2 2 2 2 2
19、(1)硫酸钠;(2)200
(3)(1)中所得滤液的溶质质量为x,
CuSO+2NaOH=Cu(OH)↓+NaSO
4 2 2 4
98 142
9.8g x
x=14.2g
(1)中所得滤液的溶质质量分数: 100%=7.1%.
答:(1)中所得滤液的溶质质量分数7.1%.
20、
521 、
22 、
6