文档内容
五年(2021-2025)高考化学真题分类汇编
专题10 元素推断与元素周期律
考向 五年考情(2021-2025) 命题趋势
2025·浙江1月卷、2025·广东卷、2024·江苏卷、
考点01 元素周期律 2023·天津卷、2023·江苏卷、2022·江苏卷、2022·辽
宁卷、2022·海南卷、2021·湖北卷、2021·北京卷
试题命制时主要是以原子
2025·安徽卷、2025·湖南卷、2025·河南卷、2025·陕
(或离子)结构、核外电子排
晋青宁卷、2025·湖北卷、2025·河北卷、2025·甘肃
布、元素化合物的性质为
卷、2025·云南卷、2025·黑吉辽蒙卷、2024·广西
突破口,进行元素的推
卷、2024·福建卷、2024·重庆卷、2024·江西卷、
断,然后分项考查粒子半
2024·贵州卷、2024·广东卷、2024·甘肃卷、2024·浙 径大小的比较,金属性、
江卷、2024·河北卷、2024·全国甲卷、2024·湖北 非金属性强弱的比较,气
卷、2024·吉林卷、2024·新课标卷、2023·河北卷、 态氢化物的稳定性强弱最
2024·浙江卷、2023·福建卷、2023·重庆卷、2023·广 高价氧化物对应水化物的
考点03 元素推断 东卷、2023·浙江卷、2023·湖南卷、2023·湖北卷、 酸性强弱等元素周期律知
2023·辽宁卷、2023·全国乙卷、2023·全国甲卷、 识,有时还涉及化学键与
2022·天津卷、2022·重庆卷、2022·福建卷、2023·浙 物质类别关系的判断。解
题时抓住这些关键特性,
江卷、2022·河北卷、2022·辽宁卷、2022·海南卷、
首先确定其为何种元素,
2022·湖南卷、2022·广东卷、2022·全国乙卷、2022·
然后以此为突破口,推知
全国甲卷、2021·重庆卷、2022·浙江卷、2021·江苏
其他未知元素。
卷、2021·福建卷、2021·湖北卷、2021·辽宁卷、
2021·天津卷、2021·山东卷、2021·广东卷、2021·全
国甲卷、2021·湖南卷、2021·全国乙卷
考点一 元素周期律
1.(2025·浙江1月卷)根据元素周期律,下列说法不正确的是
A.第一电离能:N>O>S B.化合物中键的极性:SiCl >PCl
4 3
C.碱性:LiOH>KOH D.化合物中离子键百分数:MgO>Al O
2 3
【答案】C
【解析】A.根据同一周期从左往右元素的第一电离能呈增大趋势,ⅡA与ⅢA,ⅤA与ⅥA反常,
故第一电离能:N>O>S,A正确;
B.已知同一周期从左往右元素的电负性依次增大,电负性Si<P<Cl,电负性差值越大,键的极性越
大,故化合物中键的极性:SiCl >PCl ,B正确;
4 3
C.同一主族从上往下元素的金属性依次增大,金属性Li<K,故碱性:LiOH<KOH,C错误;
D.已知同一周期从左往右元素的电负性依次增大,即电负性Mg<Al,故Mg与O的电负性差值>Al
1 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司与O的电负性差值,电负性差值越大离子键百分数越大,故化合物中离子键百分数:MgO>Al O,D
2 3
正确;
故答案为:C。
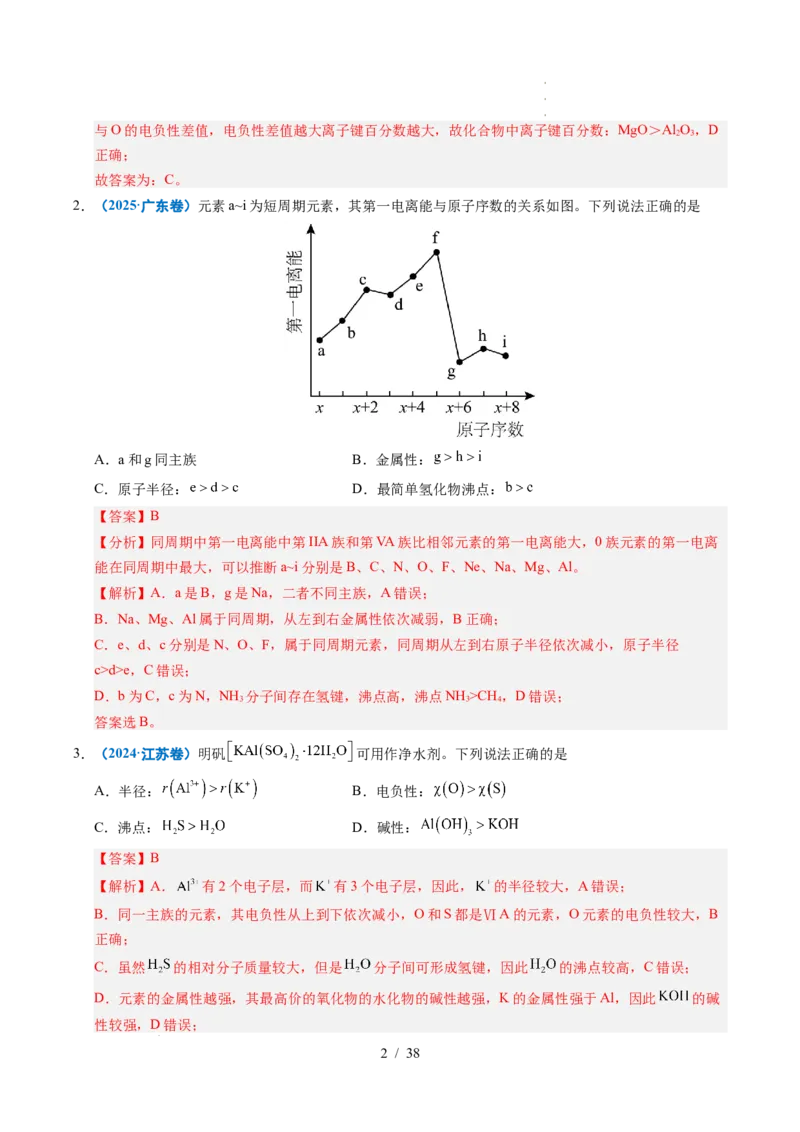
2.(2025·广东卷)元素a~i为短周期元素,其第一电离能与原子序数的关系如图。下列说法正确的是
A.a和g同主族 B.金属性:
C.原子半径: D.最简单氢化物沸点:
【答案】B
【分析】同周期中第一电离能中第IIA族和第VA族比相邻元素的第一电离能大,0族元素的第一电离
能在同周期中最大,可以推断a~i分别是B、C、N、O、F、Ne、Na、Mg、Al。
【解析】A.a是B,g是Na,二者不同主族,A错误;
B.Na、Mg、Al属于同周期,从左到右金属性依次减弱,B正确;
C.e、d、c分别是N、O、F,属于同周期元素,同周期从左到右原子半径依次减小,原子半径
c>d>e,C错误;
D.b为C,c为N,NH 分子间存在氢键,沸点高,沸点NH >CH ,D错误;
3 3 4
答案选B。
3.(2024·江苏卷)明矾 可用作净水剂。下列说法正确的是
A.半径: B.电负性:
C.沸点: D.碱性:
【答案】B
【解析】A. 有2个电子层,而 有3个电子层,因此, 的半径较大,A错误;
B.同一主族的元素,其电负性从上到下依次减小,O和S都是ⅥA的元素,O元素的电负性较大,B
正确;
C.虽然 的相对分子质量较大,但是 分子间可形成氢键,因此 的沸点较高,C错误;
D.元素的金属性越强,其最高价的氧化物的水化物的碱性越强,K的金属性强于Al,因此 的碱
性较强,D错误;
2 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司综上所述,本题选 B。
4.(2023·天津卷)下列性质不能用于判断C、 的非金属性强弱的是
A.元素的电负性
B.最高价氧化物的熔点
C.简单氢化物的热稳定性
D.最高价氧化物对应的水化物的酸性
【答案】B
5.(2023·江苏卷)元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是
A.原子半径: B.第一电离能:
C.碳单质、晶体硅、SiC均为共价晶体 D.可在周期表中元素Si附近寻找新半导体材料
【答案】D
【解析】A.同主族元素原子半径从上往下原子半径增大,故原子半径: ,A错
误;
B.同周期主族元素,从上往下原子半径增大,更易失电子,第一电离能: ,B
错误;
C.晶体硅、SiC均为共价晶体,碳单质中金刚石为共价晶体,而石墨为混合晶体,C 为分子晶体,C
60
错误;
D.周期表中元素Si附近存在许多准金属,可在其周围寻找半导体材料,D正确。
故选D。
6.(2022·江苏卷)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
【答案】A
【解析】A.核外电子数相同时,核电荷数越大半径越小,故半径大小为 ,故A正确;
B.同周期元素核电荷数越大电负性越大,故 ,故B错误;
C.同周期从左往右第一电离能呈增大趋势,同主族从上往下第一电离能呈减小趋势,故电离能大小为
,故C错误;
D.元素金属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为 ,故D
错误;
故选A。
7.(2022·辽宁卷)下列类比或推理合理的是
3 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司方
已知 结论
法
类
A 沸点: 沸点:
比
类
B 酸性: 酸性:
比
推
C 金属性: 氧化性:
理
推
D : 溶解度:
理
【答案】A
【解析】A. 、 、 的相对分子质量逐渐增大,沸点逐渐升高,可推知分子晶体的相对分子质
量越大,分子间作用力越大,沸点越高,由于相对分子质量: ,所以沸点:
,故A正确;
B.非金属元素最高价含氧酸的酸性与非金属性有关,元素的非金属性越强,最高价含氧酸的酸性越
强,所以酸性: ,酸性: ,故B错误;
C.由金属性: ,可推出氧化性 ;由离子方程式 可得,氧化
性: ,故C错误;
D. 和 的阴、阳离子个数比不相同,不能通过 大小来比较二者在水中的溶解度,故D
错误;
选A。
8.(2022·海南卷)钠和钾是两种常见金属,下列说法正确的是
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
【答案】A
【解析】A.同一主族元素的第一电离能从上到下依次减小,金属性越强的元素,其第一电离能越小,
因此,钠元素的第一电离能大于钾,A说法正确;
B.基态钾原子价层电子为4s1,其轨道表示式为 ,B说法不正确;
C.钾和钠均能与水发生置换反应,因此,钾不能置换出 NaC1溶液中的钠,C说法不正确;
D.钠元素与钾元素的原子序数分别为11和19,两者相差8,D说法不正确;
综上所述,本题选A。
9.(2021·湖北卷)金属Na溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配体L,得
4 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司到首个含碱金属阴离子的金黄色化合物[NaL]+Na-。下列说法错误的是
A.Na-的半径比F-的大 B.Na-的还原性比Na的强
C.Na-的第一电离能比H-的大 D.该事实说明Na也可表现出非金属性
【答案】C
【解析】A. 核外有3个电子层、 核外有2个电子层,故 的半径比 的大,A项正确;
B. 的半径比Na的大, 中原子核对最外层电子的引力更小,更易失电子,故 的还原性比
Na的强,B项正确;
C. 和 最外层均是2个电子,但Na-的半径更大,原子核对最外层电子的吸引力更小,故 更
易失去一个电子,即Na-的第一电离能比 的小,C项错误;
D.该事实说明Na可以形成 ,即Na也可在一定条件下得电子、表现出非金属性,D项正确;
故选C。
10.(2021·北京卷)下列性质的比较,不能用元素周期律解释的是
A.酸性:HClO>HSO >HSiO B.碱性:KOH>NaOH>LiOH
4 2 3 2 3
C.热稳定性:HO>HS>PH D.非金属性:F>O>N
2 2 3
【答案】A
【解析】A.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,由于S元素最高价
含氧酸是HSO ,不是HSO ,因此不能根据元素周期律判断酸性:HClO>HSO >HSiO,A错
2 4 2 3 4 2 3 2 3
误;
B.同一主族元素的金属性随原子序数的增大而增强。元素的金属性越强,其最高价氧化物对应的水
化物的碱性就越强。元素的金属性:K>Na>Li,所以碱性:KOH>NaOH>LiOH,B正确;
C.同一周期元素的非金属性随原子序数的增大而增强;同一主族元素的非金属性随原子序数的增大
而减弱。元素的非金属性越强,其简单氢化物的稳定性就越强。元素的非金属性:O>S>P,所以氢
化物的热稳定性:HO>HS>PH ,C正确;
2 2 3
D.同一周期元素的非金属性随原子序数的增大而增强,所以元素的非金属性:F>O>N,D正确;
故合理选项是A。
考点二 元素推断
11.(2025·安徽卷)某化合物的结构如图所示。W、X、Y、Z是原子序数依次增大的短周期元素,其中
X、Z位于同一主族。下列说法错误的是
A.元素电负性: B.该物质中Y和Z均采取 杂化
C.基态原子未成对电子数: D.基态原子的第一电离能:
【答案】D
5 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【分析】W、X、Y、Z是原子序数依次增大的短周期元素,其中X、Z位于同一主族,且X、Z均形
成2个共价键,则X为O,Z为S;Y形成5个共价键且原子序数位于O、S之间,则Y为P;W形成
1个共价键,原子序数最小,则W为H;
【解析】A.同周期从左向右电负性逐渐增大,同主族从上向下电负性逐渐减小,故元素电负性
O>S>P,即X>Z>Y,A项正确;
B.该物质中,P原子的价层电子对数为 ,为sp3杂化,S原子的价层电子对数为
,为sp3杂化,B项正确;
C.基态H原子未成对电子数为1,基态O原子的价电子排布式为2s22p4,未成对电子数为2,基态P
原子的价电子排布式为3s23p3,未成对电子数为3,则基态原子未成对电子数 ,即 ,C
项正确;
D.基态原子的第一电离能同周期从左向右逐渐增大,由于VA族原子的p轨道处于半充满状态,第一
电离能大于同周期相邻主族元素,即P>S,D项错误;
故选D。
12.(2025·湖南卷) 浓溶液中含有的 具有酸性,能溶解金属氧化物。元素X、Y、Z、
M的原子序数依次增大,分别位于不同的前四周期。Y的最外层电子数是内层的3倍,X和Y的最外
层电子数之和等于Z的最外层电子数,M的价层电子排布是 。下列说法正确的是
A.电负性:
B.Y形成的两种单质均为非极性分子
C.由X、Y、Z形成的化合物均为强电解质
D.铁管上镶嵌M,铁管不易被腐蚀
【答案】D
【分析】Y的最外层电子数是内层的3倍,则Y的最外层电子数为6,Y为O,X和Y的最外层电子
数之和等于Z的最外层电子数,则X的最外层电子数应为1,原子序数小于氧元素,则X为H,Z的
最外层电子数为7,则Z为Cl,M的价层电子排布是 ,M是Zn,综上所述:X为H、Y为O、
Z为Cl、M是Zn,据此解答;
【解析】A.非金属性越强,电负性越大, 中O为负化合价,因此X(H)的电负性小于Y
(O),A错误;
B.Y(O)的单质O 是非极性分子,但O 是极性分子(V形结构导致偶极矩不为零),B错误;
2 3
C.X(H)、Y(O)、Z(Cl)形成的化合物如HClO,属于弱电解质,并非全部为强电解质,C错
误;
D.M为Zn,比Fe活泼,镶嵌Zn会通过牺牲阳极保护铁管,使其不易被腐蚀,D正确;
故选D。
13.(2025·河南卷)我国科研人员合成了一种深紫外双折射晶体材料,其由原子序数依次增大的五种短周
6 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司期元素 和Z组成。基态X原子的s轨道中电子总数比p轨道中电子数多 所在族的
族序数等于Q的质子数,基态Y和Z原子的原子核外均只有1个未成对电子,且二者核电荷数之和为
Q的4倍。下列说法正确的是
A. 为极性分子 B. 为共价晶体
C.原子半径: D.1个 分子中有2个 键
【答案】D
【分析】Q、W、X、Y和Z为原子序最依次增大的短周期元素,基态X原子的s轨道中电子总数比P
轨道中电子数多1,X是N;X所在族的族序数等于Q的质子数,Q是B,所以W是C;基态Y和Z
原子的原子核外均只有1个未成对电子,且二者核电荷数之和为Q的4倍,即质子数之和为20,所以
Y是F,Z是Na。
【解析】A.BF 为平面正三角形结构,结构对称,属于非极性分子,A错误;
3
B.NaF是离子晶体,B错误;
C.同周期自左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,则原子半径C<Li<
Na,C错误;
D.N 分子中含有三键,所以含有2个π键,D正确;
2
答案选D。
14.(2025·陕晋青宁卷)一种高聚物 被称为“无机橡胶”,可由如图所示的环状三聚体制备。
X、Y和Z都是短周期元素,X、Y价电子数相等,X、Z电子层数相同,基态Y的 轨道半充满,Z
的最外层只有1个未成对电子,下列说法正确的是
A.X、Z的第一电离能: B.X、Y的简单氢化物的键角:
C.最高价含氧酸的酸性: D.X、Y、Z均能形成多种氧化物
【答案】D
【分析】X、Y价电子数相等,X、Y属于同一主族,且X形成5个键,Y形成3个键,基态Y的
轨道半充满,则X为P元素,Y为N元素,X、Z电子层数相同, Z的最外层只有1个未成对电子,
Z形成1个键,Z为Cl元素,以此分析。
【解析】A.第一电离能同周期从左到右有增大趋势,第一电离能:Cl>P,A错误;
B.X、Y的简单氢化物分别为:PH 和NH ,电负性:N>P,共用电子对距N近,成键电子对斥力N-
3 3
H大于P-H,键角:NH >PH,B错误;
3 3
C.元素的非金属性越强,其最高价含氧酸酸性越强,非金属性:Cl>N>P,酸性:
7 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司HClO>HNO >H PO ,C错误;
4 3 3 4
D.P、N、Cl均能形成多种氧化物,D正确;
答案选D。
15.(2025·湖北卷)某化合物的分子式为 。X、Y、Z三种元素位于同一短周期且原子序数依次增
大,三者的原子核外电子层数之和与未成对电子数之和相等,Z是周期表中电负性最大的元素。下列
说法正确的是
A.三者中Z的原子半径最大 B.三者中Y的第一电离能最小
C.X的最高化合价为 D. 与 键角相等
【答案】B
【分析】Z是周期表中电负性最大的元素,Z为F,电子层数为2,未成对电子数为1;X、Y、Z三种
元素位于同短周期且原子序数依次增大,三者的原子核外电子层数之和与未成对电子数之和相等,则
X和Y未成对电子数之和为5,X为C和Y为N或X为N和Y为O;化合物分子式为XY Z,则X和
2
2个Y总化合价为+1价,NO F符合,故X为N,Y为O,Z为F。
2
【解析】A.X为N,Y为O,Z为F,N、O、F位于同周期,F在最右边,F的原子半径最小,A错
误;
B.X为N,Y为O,Z为F,同周期从左往右,第一电离能呈增大趋势,N的2p轨道半充满,第一电
离能大于O,故三者中O的第一电离能最小,B正确;
C.X为N,N的最高正化合价为+5,C错误;
D.X为N,Z为F,NF 和NH 的中心原子均为sp3杂化,孤电子对数均为1,前者成键电子对离中心
3 3
N较远,成键电子对之间的斥力较小,键角较小,D错误;
答案选B。
16.(2025·河北卷)W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高
能级中的电子数相等,X与W同族,Y与X相邻且Y原子比X原子多一个未成对电子,Z位于W的
对角线位置。下列说法错误的是
A.第二电离能: B.原子半径:
C.单质沸点: D.电负性:
【答案】A
【分析】W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级中的
电子数相等,则W价电子排布式可能是:1s22s22p2或1s22s22p63s23p4,若W是C,X与W同族,则X
是Si,Y与X相邻且Y原子比X原子多一个未成对电子,则Y是P,Z位于W的对角线位置,则满足
条件的Z是P,与Y重复;故W是S;X与W同族,则X是O;Y与X相邻且Y原子比X原子多一
个未成对电子,则Y是N;Z位于W的对角线位置,则Z是F。
【解析】A.O的第二电离能高于N,因为O+的电子构型为2p3(半充满),失去电子需更高能量,而
N+的电子构型为2p2,失去电子相对容易,因此X(O)的第二电离能大于Y(N),A错误;
B.同主族从上到下,原子半径变大,同周期,从左到右原子半径变小,F(Z)位于第二周期,S
8 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司(W)位于第三周期,原子半径S>O>F,即: ,B正确;
C.N 与F 都是分子晶体,F 范德华力大,沸点高,C正确;
2 2 2
D.同主族从上到下,电负性逐渐减小,O的电负性大于S,D正确;
故选A。
17.(2025·甘肃卷)X、Y、Z、W、Q分别为原子序数依次增大的短周期主族元素。Y、Q基态原子的价
电子数相同,均为其K层电子数的3倍,X与Z同族,W为金属元素,其原子序数等于X与Z的原子
序数之和。下列说法错误的是
A.X与Q组成的化合物具有还原性 B.Y与Q组成的化合物水溶液显碱性
C.Z、W的单质均可在空气中燃烧 D.Z与Y按原子数 组成的化合物具有氧化性
【答案】B
【分析】X、Y、Z、W、Q分别为原子序数依次增大的短周期主族元素。Y、Q基态原子的价电子数
相同,说明Y、Q为同主族元素,均为其K层电子数的3倍,说明价电子数为6,为氧元素和硫元
素;X与Z同族,W为金属元素,其原子序数等于X与Z的原子序数之和,所以只能推出W为镁,
则Z为Na,X为H,据此解答。
【解析】A.X与Q组成的化合物如H与S形成的HS,这些化合物中S处于最低价,具有还原性,A
2
正确;
B.Y与Q形成的化合物为SO 或SO ,溶于水生成亚硫酸或硫酸,溶液显酸性,B错误;
2 3
C.Z为Na,W为Mg,都可以在空气中燃烧生成过氧化钠和氧化镁,C正确;
D.Z与Y按1:1组成的化合物为过氧化钠,其中O为-1价,有氧化性,D正确;
故选B。
18.(2025·云南卷)钙霞石是一种生产玻璃陶瓷的原料,所含M、Q、R、T、X、Y、Z为原子序数依次
增大的前20号主族元素,M是原子半径最小的元素,Q是形成物质种类最多的元素,R是地壳中含量
最高的元素,T、X、Y同周期,Q、X均与Y相邻,Z的原子序数等于M、R和T的原子序数之和。
下列说法正确的是
A.M与Z可形成离子化合物 B.原子半径:
C. 是极性分子 D.电负性:
【答案】A
【分析】M是原子半径最小的为H,Q是形成物质种类最多,则为C, R是地壳中含量最高,为O,
T、X、Y同周期且原子序数递增。Q(C)和X均与Y相邻,结合Z的原子序数Z = M + R + T = 1 + 8
+ T,Z ≤ 20,得T = 11(Na),Z = 20(Ca)。又因为T、X、Y同周期,Q、X均与Y相邻,可推出
Q(C)与Y(Si)同主族相邻,X(Al)与Y(Si)相邻且T(Na)、X(Al)、Y(Si)同属第三周
期, 故推出M为H、Q为C、R为O、T为Na、X为Al、Y为Si、Z为Ca,据此解答。
【解析】A.H与Ca形成CaH,为活泼金属形成的氢化物,为离子化合物,A正确;
2
B.同周期原子半径从左到右逐渐减小,同主族原子半径从上到下逐渐增大,R为O、T为Na、X为
Al,则它们的原子半径大小为O<Al<Na,即R<X<T,B错误;
9 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C. 为CO,为直线型的非极性分子,C错误;
2
D.同周期电负性从左到右逐渐增大,同主族电负性从下到上逐渐增大,Q为C、R为O、Y为Si,则
电负性Si<C<O,正确顺序为Y<Q<R,D错误;
故选A。
19.(2025·黑吉辽蒙卷)化学家用无机物甲 成功制备了有机物乙 ,开创了有机化
学人工合成的新纪元。其中W、X、Y、Z原子序数依次增大,X、Y、Z同周期,基态X、Z原子均有
2个单电子。下列说法正确的是
A.第一电离能:Z>Y>X B.甲中不存在配位键
C.乙中 键和 键的数目比为 D.甲和乙中X杂化方式分别为 和
【答案】D
【分析】(YW )XZ为有机物,基态X、Z原子均有2个单电子,X、Z分别为IVA族和VIA族元素,
2 2
X、Y、Z同周期、原子序数依次增大,若X、Y、Z为第三周期元素,则X、Y、Z分别为Si、P、S;
若X、Y、Z为第二周期元素,则X、Y、Z分别为C、N、O;又YWZXY为无机物,(YW )XZ为有
4 2 2
机物,所以X、Y、Z分别为C、N、O,W、X、Y、Z原子序数依次增大,能形成YWZXY,则W
4
为H,综上所述,W、X、Y、Z分别为H、C、N、O。
【解析】A.C、N、O同周期,同一周期主族元素,从左到右第一电离能有逐渐增大的趋势,第VA
族的第一电离能大于同周期相邻的两种元素,则第一电离能N>O>C,故A错误;
B.甲为NH OCN, 中有N原子提供孤对电子、H+提供空轨道形成的N→H配位键,故B错误;
4
C.乙为 ,其中有4个N-H、2个C-N、碳氧原子之间1个σ键,则一个
中有7个 键、1个π键, 键与π键的数目比为7:1,故C错误;
D.甲为NH OCN,其中的C原子与N原子形成三键、与O原子形成单键, 键电子对数为2,无孤
4
对电子,C原子采取sp杂化,乙为 ,其中的C原子形成3个 键,即 键电子对数
为3,无孤对电子,C原子采取sp2杂化,故D正确;
故答案为:D。
20.(2024·广西卷)如图所示的铼配合物离子能电催化还原 。短周期元素 的原子序数
依次增大。标准状况下,WY和 是等密度的无色气体, 是黄绿色气体。下列说法错误的是
10 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.第一电离能: B.图中X原子的杂化方式为
C. 元素以原子的形态与 配位 D.Y的电负性大于 中的化学键是极性键
【答案】C
【分析】短周期元素 的原子序数依次增大。 是黄绿色气体,Z为氯;X形成3个共用
电子对,X与Re2+之间为配位键,推测X为氮,标准状况下,WY和 是等密度的无色气体,则WY
为一氧化碳、 为氮气,故W为碳、X为氮、Y为氧、Z为氯;
【解析】A.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,第一电
离能大于同周期相邻元素,故第一电离能大小:N>O,A正确;
B.图中X原子处于环中,且存在平面大π键,则其杂化方式为 ,B正确;
C.由图可知,整个离子带1个单位正电荷,而其中 带2个单位正电荷,则氯元素以Cl-的形态与
配位,C错误;
D.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;O的电负性大于C,则CO中
的化学键是极性键,D正确;
故选C。
21.(2024·福建卷)某电解质阴离子的结构如图。X、Y、Z、Q为原子序数依序增大的同周期元素,Z的
单质为空气的主要成分之一。下列说法错误的是
A.第一电离能:
B.最简单氢化物沸点:
C.键长:
D.Y的最高价氧化物对应水化物在水中电离:
【答案】A
【分析】由该阴离子结构可知Z形成2条共价键,Z的单质为空气的主要成分之一,可知Z为O;Y
形成4条共价键,Y为C,Q形成1条共价键,Q为F,X得1个电子后形成4条共价键,则X最外层
电子数为3,X为B,据此分析解答。
【解析】A.B、C、O为同周期元素,从左到右,第一电离能呈增大趋势,则第一电离能:BO>F,原子半径越小键长越短,则键长:C-C>C-O>C-F,故C正确;
D.Y为C,其最高价氧化物的水化物为HCO,碳酸为二元弱酸,分步电离,电离方程式为:
2 3
11 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司,故D正确;
故选A。
22.(2024·重庆卷)R、X、Y和Z为短周期元素, 的分子结构如下所示。R中电子只有一种自旋
取向,X、Y和Z处于同一周期,X的核外电子数等于Y的最高能级电子数,且等于Z的最外层电子
数。下列说法正确的是
A.原子半径: B.非金属性:
C.单质的沸点: D.最高正化合价:
【答案】A
【分析】R、X、Y和Z为短周期元素,R中电子只有一种自旋取向,R为H元素;X、Y和Z处于同
一周期,X的核外电子数等于Y的最高能级电子数,且等于Z的最外层电子数,XY ZR 的分子中X、
3 3
Z均形成4个共价键,则X为B元素、Z为N元素;Y只形成1个共价键,结合位置可知Y为F元
素,以此来解答。
【解析】A.X为B元素、Z为N元素,同周期主族元素从左向右原子半径减小,则原子半径:Z<
X,故A正确;
B.Y为F元素、Z为N元素,同周期主族元素从左向右非金属性增强,则非金属性:Y>Z,故B错
误;
C.X为B元素、Y为F元素,X的单质为共价晶体,Y的单质为分子晶体,单质的沸点:X>Y,故
C错误;
D.R为H元素、X为B元素,最高正化合价:X(+3)>R(+1),故D错误;
故选:A。
23.(2024·江西卷)某新材料阳离子为W X YZM+。W、X、Y、Z和M是原子序数依次增大的前20号
36 18 2 6
主族元素,前四周期中M原子半径最大,X、Y、Z同周期。XW 分子含有大π键( ),XZ 分子呈
6 6 2
直线形。下列说法正确的是
A.WYZ 是强酸 B.MZW是强碱 C.MZ 是共价化合物D.XW 是离子化合物
2 2 2 2 2
【答案】B
【分析】W、X、Y、Z和M是原子序数依次增大的前20号主族元素,前四周期中M原子半径最大,
M为K元素,X、Y、Z同周期,XW 分子含有大π键( ),说明XW 是苯,X为C元素,W为H
6 6 6 6
元素,XZ 分子呈直线形,为CO,Z为O元素,Y为N元素,以此解答。
2 2
【解析】A.由分析可知,W为H元素、Y为N元素、Z为O元素,HNO 是弱酸,不是强酸,A错
2
12 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司误;
B.由分析可知,M为K元素、Z为O元素,W为H元素,KOH是强碱,B正确;
C.由分析可知,M为K元素、Z为O元素,KO 中存在K+和 ,属于离子化合物,C错误;
2 2
D.由分析可知,X为C元素、W为H元素,C H 为乙炔的分子式,乙炔中没有离子键,属于共价化
2 2
合物,D错误;
故选B。
24.(2024·贵州卷)某化合物由原子序数依次增大的短周期主族元素W、X、Y、Z、Q组成(结构如图)。
X的最外层电子数等于内层电子数,Y是有机物分子骨架元素,Q和W能形成两种室温下常见的液态
化合物。下列说法错误的是
A.第一电离能: B.该化合物中Q和W之间可形成氢键
C.X与Al元素有相似的性质 D.W、Z、Q三种元素可形成离子化合物
【答案】A
【分析】X的最外层电子数等于内层电子数,则X的核外电子排布式为 ,X为Be元素,W只能
形成一条共价键,结合W的位置可知W为H元素,Y是有机物分子骨架元素,则Y为C元素,Q和
W能形成两种室温下常见的液态化合物,则Q为O元素,则Z为N元素,据此解答。
【解析】A.同一周期,从左到右,元素的第一电离能呈增大的趋势,N原子中2p能级上电子为半满
结构,较为稳定,第一电离能大于同周期与之相邻的元素,则第一电离能:CH,A不正确;
B. 是中强酸,而 是强酸,因此,在相同条件下,后者的酸性较强,B不正确;
C.H只有1个电子,O的2p轨道上有4个电子,O有2个未成对电子,因此,基态原子的未成对电
子数 O>H,C不正确;
D.K的氧化物溶于水且与水反应生成强碱 ,S的氧化物溶于水且与水反应生成 或
,因此,氧化物溶于水所得溶液的pH的大小关系为 K>S,D正确;
综上所述,本题选D。
31.(2024·吉林卷)如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,基态X原
子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试验呈
绿色。下列说法错误的是
A.单质沸点: B.简单氢化物键角:
C.反应过程中有蓝色沉淀产生 D. 是配合物,配位原子是Y
【答案】D
【分析】Q是ds区元素,焰色试验呈绿色,则Q为Cu元素;空间运动状态数是指电子占据的轨道
数,基态X原子的核外电子有5种空间运动状态,则X为第2周期元素,满足此条件的主族元素有
N(1s22s22p3)、O(1s22s22p4)、F(1s22s22p5);X、Y、Z为原子序数依次增大,基态Y、Z原子有两个未成
对电子,若Y、Z为第2周期元素,则满足条件的可能为C(1s22s22p2)或O(1s22s22p4),C原子序数小于
N,所以Y不可能为C,若Y、Z为第3周期元素,则满足条件的可能为Si(1s22s22p63s23p2)或
S(1s22s22p63s23p4),Y、Z可与Cu形成CuZY ,而O、Si、S中只有O和S形成的 才能形成
4
CuZY ,所以Y、Z分别为O、S元素,则X只能为N;W能与X形成XW,则W为IA族或VIIA族
4 3
元素,但W原子序数小于N,所以W为H元素,综上所述,W、X、Y、Z、Q分别为H、N、O、
S、Cu。
【解析】A.W、Y、Z分别为H、O、S,S单质常温下呈固态,其沸点高于氧气和氢气,O 和H 均
2 2
17 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司为分子晶体,O 的相对分子质量大于H,O 的范德华力大于 H,所以沸点O>H,即沸点S>O>
2 2 2 2 2 2 2
H,故A正确;
2
B.Y、X的 简单氢化物分别为HO和NH ,HO的中心原子O原子的价层电子对数为2+ ×(6-
2 3 2
2×1)=4、孤电子对数为2,空间构型为V形,键角约105º,NH 的中心原子N原子的价层电子对数为
3
3+ ×(5-3×1)=4、孤电子对数为1,空间构型为三角锥形,键角约107º18´,所以键角: ,故B
正确;
C.硫酸铜溶液中滴加氨水,氨水不足时生成蓝色沉淀氢氧化铜,氨水过量时氢氧化铜溶解,生成
Cu(NH )SO ,即反应过程中有蓝色沉淀产生,故C正确;
3 4 4
D. 为Cu(NH )SO ,其中铜离子提供空轨道、NH 的N原子提供孤电子对,两者形成配
3 4 4 3
位键,配位原子为N,故D错误;
故答案为:D。
32.(2024·新课标卷)我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离
子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。
W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成
对电子数为4。下列叙述错误的是
A.W、X、Y、Z四种元素的单质中Z的熔点最高
B.在X的简单氢化物中X原子轨道杂化类型为
C.Y的氢氧化物难溶于NaCl溶液,可以溶于 溶液
D. 中 提供电子对与 形成配位键
【答案】A
【分析】W、X 、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电
子数是其内层电子数的2倍,则W为C元素;每个周期的ⅡA和ⅤA的元素的第一电离能都比左右
相邻元素的高,由于配合物 中Y在外界,Y可形成简单阳离子,则Y属于金属元素,故
X和Y分别为N和Mg;Z的M层未成对电子数为4,则其3d轨道上有4个不成对电子,其价电子排
布式为 ,Z为Fe元素, 为 。
【解析】A.W、X、 Y、Z四种元素的单质中,N元素的单质形成分子晶体,Mg和Fe均形成金属晶
体,C元素既可以形成金刚石又可以形成石墨,石墨的熔点最高,A不正确;
B.X的简单氢化物是 ,其中心N原子价层电子对数为3+ ,N原子轨道杂化类型
为 ,B正确;
C.Y的氢氧化物是 ,其属于中强碱,其难溶于水,难溶于 溶液,但是,由于 电
18 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司离产生的 可以破坏 的沉淀溶解平衡,因此 可以溶于 溶液,C正确;
D. 中 的C原子提供孤电子对与 形成配位键,D正确;
综上所述,本题选A。
33.(2023·河北卷)下图所示化合物是制备某些药物的中间体,其中 均为短周期元素,
且原子序数依次增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一
半。下列说法正确的是
A.简单氢化物的稳定性: B.第一电离能:
C.基态原子的未成对电子数: D.原子半径:
【答案】A
【分析】由 均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有
气体的稳定电子构型,Z原子的电子数是Q的一半,图中W含有1个化学键,原子序数最小,故W
为H,X含有4个共价键,故X为C,Z和Q都含2个共价键,且Z原子的电子数是Q的一半,故Z
为O,Q为S,Y含3个共价键,而且原子序数介于C和O之间,故Y为N,据此回答
【解析】A.非金属性:O>S,故简单氢化物的稳定性: ,A正确;
B.同一周期从左到右第一电离能呈现增大的趋势,故第一电离能: ,B错误;
C.基态原子中C的未成对电子数为2个,S的未成对电子数也为2个,故基态原子的未成对电子数:
,C错误;
D.原子半径为O>H,故原子半径: ,D错误;
故选A。
34.(2024·浙江卷)X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最小,短周期中
M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不正确的是
A.沸点:
B.M与Q可形成化合物 、
C.化学键中离子键成分的百分数:
D. 与 离子空间结构均为三角锥形
【答案】D
【分析】X半径最小为H,短周期电负性最小则M为Na,Z原子的s能级与p能级的电子数相等,则
Z为O,Z与Y、Q相邻,Y为N,Q为S,以此分析;
19 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【解析】A.HO中含有氢键,则沸点高于HS,A正确;
2 2
B.Na与O形成NaO、NaO,则O与S同族化学性质性质相似,B正确;
2 2 2
C.NaO的电子式为 ,NaS的电子式为 ,离子键百分比 =
2 2
(电负性差值 / 总电负性差值),O的电负性大于S,则NaO离子键成分的百分数大于NaS,C正确;
2 2
D. 为sp2杂化,孤电子对为0,为平面三角形, 为sp3杂化,孤电子对为1,三角锥形,D错
误;
故选D。
35.(2023·福建卷)某含锰着色剂的化学式为 ,Y、X、Q、Z为原子序数依次增大的短周期
元素,其中 具有正四面体空间结构, 结构如图所示。下列说法正确的是
A.键角: B.简单氢化物沸点:
C.第一电离能: D.最高价氧化物对应的水化物酸性:
【答案】C
【分析】由题意,Y、X、Q、Z为原子序数依次增大的短周期元素,其中 具有正四面体空间结
构,可知 为 ,故Y为H,X为N;同时分析 结构,可知Q正常情况应该成两根键,Q
为ⅥA的元素,同时Z也成5根键,Z为ⅤA的元素,故Q为O,Z为P。
【解析】A. 和 都是sp3杂化,但是 中有一对孤电子对,孤电子对对成键电子对的排斥
作用更大,在一个 是三角锥形结构,而 是正四面体结构,故键角: < ,A错误;
B.X、Q、Z分别为N、O、P,沸点顺序为 ,正确顺序为Q>X>Z,B错误;
C.同主族元素从上到下第一电离能减小,同周期从左到右第一电离能有增大的趋势,故第一电离
能:N>O>Mn,C正确;
D.Z的最高价氧化物对应的水化物为 ,X最高价氧化物对应的水化物为 ,前者为中强酸而
后者为强酸,D错误;
故选C。
36.(2023·重庆卷)化合物XYWR和XZWR所含元素相同,相对分子质量相差7,1molX YWR含
3 7 3 7 3 7
40mol质子,X、W和R三种元素位于同周期,X原子最外层电子数是R原子核外电子数的一半。下
列说法正确的是
A.原子半径:W>R B.非金属性:X>R
C.Y和Z互为同素异形体 D.常温常压下X和W的单质均为固体
20 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【答案】A
【分析】化合物XYWR和XZWR所含元素相同,相对分子质量相差7,说明Y、Z为氢元素的两种
3 7 3 7
核素,由题干信息可知,1molX YWR含40mol质子,X、W和R三种元素位于同周期,X原子最外
3 7
层电子数是R原子核外电子数的一半,则X、W、R的内层电子数为2,设X的最外层电子数为a,则
R的核外电子数为2a,W的核外电子数为b,Y的质子数为1,则有:3(a+2)+ 2a+b+7=40(a、b均为整
数),5a+b=27,解得a=5,b=2(X、R不在同周期,舍去);a=4,b=7;a=3,b=12(X、R不在同周期,
舍去);则X为C,R为O,W为N。
【解析】A.同周期从左到右原子半径逐渐减小,则原子半径:W>R,故A正确;
B.同周期从左到右非金属性逐渐增强,则非金属性: R>X,故B错误;
C.Y和Z是氢的两种核素,两者互为同位素,故C错误;
D.常温常压下X的单质为固体,W的单质是气体,故D错误。
综上所述,答案为A。
37.(2023·广东卷)化合物 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅
有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周
期,E在地壳中含量最多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
【答案】A
【分析】E在地壳中含量最多为氧元素,X的基态原子价层电子排布式为 ,所以 , ,
X为镁或者 ,X为锂,Y的基态原子价层p轨道半充满所以可能为氮或磷,Y和M同族所以为氮
或磷,根据X与M同周期、 化合价之和为零,可确定Z为氢元素、M为磷元素、X为镁元
素、E为氧元素、Y氮元素。
【解析】A.元素电负性:氧大于氮大于氢,A正确;
B.磷化氢、氨气、水固体均是分子晶体,氨气、水固体中都存在氢键沸点高,磷化氢没有氢键沸点
低,所以氢化物沸点:冰大于氨大于磷化氢,B错误;
C.同周期第一电离能自左向右总趋势逐渐增大,当出现第ⅡA族和第ⅤA族时比左右两侧元素电离
能都要大,所以氮大于氧大于镁 ,C错误;
D. 价层电子对为 ,有一对孤电子对,空间结构为三角锥形, 价层电子对为 ,
没有孤电子对, 空间结构为平面三角形,D错误;
故选A。
38.(2023·浙江卷)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,
且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列
说法不正确的是
21 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.第一电离能:
B.电负性:
C.Z、W原子形成稀有气体电子构型的简单离子的半径:
D. 与水反应生成产物之一是非极性分子
【答案】A
【分析】X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有
X、 Y元素相邻。X基态原子核外有2个未成对电子,则X为C,Y为N,Z为F,W原子在同周期
中原子半径最大,则W为Na。
【解析】A.根据同周期从左到右第一电离能呈增大趋势,但第IIA族大于第IIIA族,第VA族大于第
VIA族,则第一电离能: ,故A错误;
B.根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则电负性:
,故B正确;
C.根据同电子层结构核多径小,则Z、W原子形成稀有气体电子构型的简单离子的半径: ,故
C正确;
D. 与水反应生成产物之一为乙炔,乙炔是非极性分子,故D正确。
综上所述,答案为A。
39.(2023·湖南卷)日光灯中用到的某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、Z和W为
3 4 2 2
原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数
相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XX>Z>W,A错误;
B.同一周期原子半径从左到右依次减小,同一主族原子半径从上到下依次增大,故四种原子的原子
22 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司半径大小为:YO>C,B正确;
C.Q为Al,Al O 为两性氧化物,C正确;
2 3
D.该阴离子中L与Q之间形成配位键,D正确;
故答案选A。
42.(2023·全国乙卷)一种矿物由短周期元素W、X、Y组成,溶于稀盐酸有无色无味气体生成。W、
X、Y原子序数依次增大。简单离子 与 具有相同的电子结构。下列叙述正确的是
A.X的常见化合价有 、 B.原子半径大小为
C.YX的水合物具有两性 D.W单质只有4种同素异形体
【答案】A
【分析】W、X、Y为短周期元素,原子序数依次增大,简单离子X2-与Y2+具有相同的电子结构,则
它们均为10电子微粒, X为O,Y为Mg,W、X、Y组成的物质能溶于稀盐酸有无色无味的气体产
生,则W为C,产生的气体为二氧化碳,据此解答。
【解析】A.X为O,氧的常见价态有-1价和-2价,如HO 和HO,A正确;
2 2 2
B.W为C,X为O,Y为Mg,同主族时电子层数越多,原子半径越大,电子层数相同时,原子序数
越小,原子半径越大,所以原子半径大小为:Y>W>X,B错误;
C.Y为Mg,X为O,他们可形成MgO,水合物为Mg(OH) ,Mg(OH) 只能与酸反应生成盐和水,不
2 2
能与碱反应,所以YX的水合物没有两性,C错误;
D.W为C,碳的同素异形体有:金刚石、石墨、石墨烯、富勒烯、碳纳米管等,种类不止四种,D
错误;
故选A。
43.(2023·全国甲卷)W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。
Y的最外层电子数与其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是
2
A.原子半径: B.简单氢化物的沸点:
C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
【答案】C
【分析】W、X、Y、Z为短周期主族元素,原子序数依次增大,WX 是形成酸雨的物质之一,根据原
2
子序数的规律,则W为N,X为O,Y的最外层电子数与其K层电子数相等,又因为Y的原子序数大
于氧的,则Y电子层为3层,最外层电子数为2,所以Y为Mg,四种元素最外层电子数之和为19,
则Z的最外层电子数为6,Z为S,据此解答。
24 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【解析】A.X为O,W为N,同周期从左往右,原子半径依次减小,所以半径大小为W>X,A错
误;
B.X为O,Z为S,X的简单氢化物为HO,含有分子间氢键,Z的简单氢化物为HS,没有氢键,
2 2
所以简单氢化物的沸点为X>Z,B错误;
C.Y为Mg,X为O,他们可形成MgO,为离子化合物,C正确;
D.Z为S,硫的最高价含氧酸为硫酸,是强酸,D错误;
故选C。
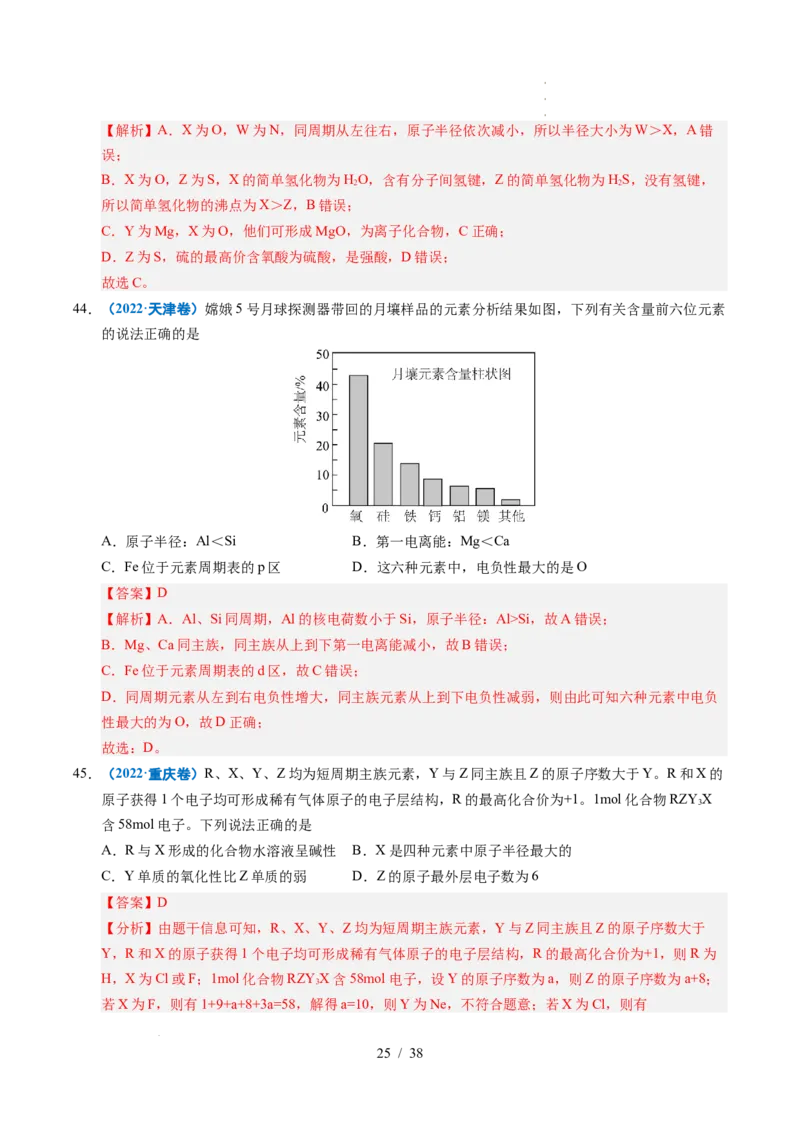
44.(2022·天津卷)嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素
的说法正确的是
A.原子半径:Al<Si B.第一电离能:Mg<Ca
C.Fe位于元素周期表的p区 D.这六种元素中,电负性最大的是O
【答案】D
【解析】A.Al、Si同周期,Al的核电荷数小于Si,原子半径:Al>Si,故A错误;
B.Mg、Ca同主族,同主族从上到下第一电离能减小,故B错误;
C.Fe位于元素周期表的d区,故C错误;
D.同周期元素从左到右电负性增大,同主族元素从上到下电负性减弱,则由此可知六种元素中电负
性最大的为O,故D正确;
故选:D。
45.(2022·重庆卷)R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于Y。R和X的
原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1。1mol化合物RZY X
3
含58mol电子。下列说法正确的是
A.R与X形成的化合物水溶液呈碱性 B.X是四种元素中原子半径最大的
C.Y单质的氧化性比Z单质的弱 D.Z的原子最外层电子数为6
【答案】D
【分析】由题干信息可知,R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于
Y,R和X的原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1,则R为
H,X为Cl或F;1mol化合物RZY X含58mol电子,设Y的原子序数为a,则Z的原子序数为a+8;
3
若X为F,则有1+9+a+8+3a=58,解得a=10,则Y为Ne,不符合题意;若X为Cl,则有
25 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司1+17+a+8+3a=58,解得a=8,则Y为O,Z为S;故R为H、X为Cl、Y为O、Z为S,据此分析解
题。
【解析】A.由分析可知,R为H、X为Cl,故R与X形成的化合物即HCl水溶液呈酸性,A错误;
B.由分析可知,R为H、X为Cl、Y为O、Z为S,故S是四种元素中原子半径最大的,B错误;
C.由分析可知,Y为O、Z为S,由于O的非金属性比S强,故O 的氧化性比S强,C错误;
2
D.由分析可知,Z为S,是16号元素,S原子最外层电子数为6,D正确;
故答案为:D。
46.(2022·福建卷)某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短周期元素
组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳中
含量最多的元素。下列说法正确的是
A.简单氢化物沸点: B. 分子的空间构型为三角锥形
C.原子半径: D.最高价氧化物对应水化物的碱性:
【答案】A
【分析】X的核外电子总数为最外层电子数的2倍,X为Be;Z为地壳中含量最多的元素,Z为O,X
与Y、Z与W均为同周期相邻元素,Y为B,W为F,据此解答。
【解析】A. 常温下为液态,HF常温下为气体,沸点 ,故A正确;
B. 为BF,中心B原子有3对价电子且没有孤电子对,空间构型为平面三角形,故B错误;
3
C.四种元素为同周期元素,随核电荷数增大原子半径减小,原子半径:Be>B>O>F,故C错误;
D.Be最高价氧化物水化物为Be(OH) ,溶液显两性,B最高价氧化物的水化物为HBO,溶液显酸
2 3 3
性,故D错误;
故选:A。
47.(2023·浙江卷)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,Y的s
能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法不正
确的是
A.电负性:
B.最高正价:
C.Q与M的化合物中可能含有非极性共价键
D.最高价氧化物对应水化物的酸性:
【答案】B
【分析】Y的s能级电子数量是p能级的两倍,Y为C,X的 轨道全充满,原子序数XX,A正确;
B.N最高正价为+5价,O无最高正价,最高正价N大于O,B错误;
26 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.Na和O形成的过氧化钠中含有非极性共价键,C正确;
D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性N大于C,硝酸酸性强于碳酸,
D正确;
故选B。
48.(2022·河北卷)两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依次增大的五种短周期主
族元素,下列说法错误的是
A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
【答案】A
【分析】X、Y、Z、R、Q是原子序数依次增大的五种短周期主族元素,由两种化合物的结构示意图
可知,X、Y、Z、R、Q形成共价键的数目分别为4、3、2、1、5,则五种元素分别为C元素、N元
素、O元素、F元素、P元素。
【解析】A.由两种化合物的结构示意图可知,化合物中磷原子的最外层电子数为10,不满足最外层
8电子稳定结构,故A错误;
B.C元素、N元素、O元素、F元素、P元素中位于元素周期表右上角的氟元素的非金属性最强,元
素的非金属性越强,简单氢化物的稳定性最强,故B正确;
C.红棕色二氧化氮转化为无色四氧化二氮的反应为放热反应,降低温度,平衡向正反应方向移动,
气体的颜色变浅,则将装有二氧化氮气体的透明密闭容器浸入冰水中,气体颜色变浅,故C正确;
D.氧气和臭氧是氧元素形成的不同种单质,互为同素异形体,臭氧层破坏会造成环境污染,则臭氧
在大气中的含量与环境污染密切相关,故D正确;
故选A。
49.(2022·辽宁卷)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电
子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
【答案】B
【分析】短周期元素X、Y、Z、W、Q原子序数依次增大,W简单离子在同周期离子中半径最小,说
明W为第三周期元素Al。短周期元素的基态原子中有两个单电子,可分类讨论:①为第二周期元素
时,最外层电子排布为2s22p2或2s22p4,即C或O;②为第三周期元素时,最外层电子排布为3s23p2或
27 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司3s23p4,即Si或S。Q与Z同主族,结合原子序数大小关系可知,则X、Z、Q分别为C、O和S,则Y
为N。
【解析】A.X为C,能与多种元素(H、O、N、P、S等)形成共价键,A正确;
B.Z和Q形成的简单氢化物为HO和HS,由于HO分子间能形成氢键,故HO沸点高于HS,B错
2 2 2 2 2
误;
C.Y为N,Z为O,N的最外层p轨道电子为半充满结构,比较稳定,故其第一电离能比O大,C正
确;
D.W为Al,Z为O,O的电负性更大,D正确;
故选B。
50.(2022·海南卷)短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成
水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列
判断正确的是
A. 是非极性分子
B.简单氢化物沸点:
C.Y与Z形成的化合物是离子化合物
D.X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且Y是组成水
的元素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,则Z为Na元素,W
原子在同周期主族元素中原子半径最小,则W为Cl元素,据此分析解答。
【解析】A.由分析,X为N元素,W为Cl元素,NCl 分子的空间构型为三角锥形,其正负电荷的中
3
心不重合,属于极性分子,A错误;
B.常温下HO为液态,NH 为气态,故沸点HO>NH ,即简单氢化物沸点:X<Y,B错误;
2 3 2 3
C.Y为O元素,Z为Na元素,两者形成的化合物为NaO、NaO 均为离子化合物,C正确;
2 2 2
D.N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
3 2
答案选C。
51.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增
大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径: B.非金属性:
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
【答案】C
28 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【分析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,
X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X
为C元素、Y为O元素、Z为F元素、W为Si元素。
【解析】A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>
F,故A正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减
弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
52.(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对
应的水化物为强酸。下列说法不正确的是
甲 乙
丙 丁 戊
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【分析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若
是高氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙
为Si、丁为P。
【解析】A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲
烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。
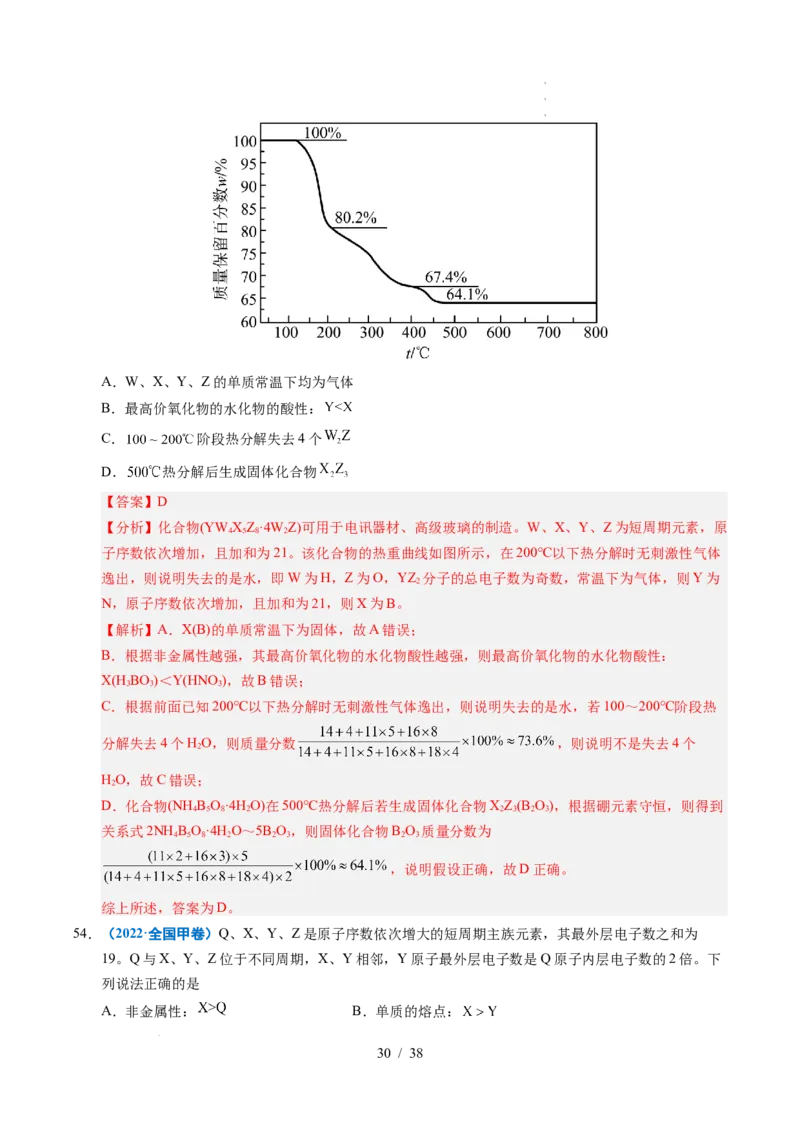
53.(2022·全国乙卷)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短
周期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数,常温下为气体。该化合物
的热重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
29 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物的酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物
【答案】D
【分析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原
4 5 8 2
子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体
逸出,则说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为
2
N,原子序数依次增加,且加和为21,则X为B。
【解析】A.X(B)的单质常温下为固体,故A错误;
B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:
X(H BO)<Y(HNO ),故B错误;
3 3 3
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段热
分解失去4个HO,则质量分数 ,则说明不是失去4个
2
HO,故C错误;
2
D.化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元素守恒,则得到
4 5 8 2 2 3 2 3
关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。
综上所述,答案为D。
54.(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为
19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下
列说法正确的是
A.非金属性: B.单质的熔点:
30 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.简单氢化物的沸点: D.最高价含氧酸的酸性:
【答案】D
【分析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子
最外层电子数为Q原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最
外层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、
Y、Z的最外层电子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子
数最多为7,若Q的最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层
电子数为6,为O元素,则Z的最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元
素,Z的最外层电子数为7,为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S
或P,据此分析解题。
【解析】A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上往
下依次减弱,故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即
Y>X,B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为
2 3
Cl或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不
2 3
存在,故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价
含氧酸酸性:Z>Y,D正确;
故答案为:D。
55.(2021·重庆卷)元素X、Y和Z可形成化合物XYZ, X的原子序数是Z的原子序数的5倍,1 mol
3 3 6
XYZ 含42mol质子,下列叙述正确的是
3 3 6
A.X位于周期表的第二周期第VA族
B.Y的原子半径大于X的原子半径
C.Y的氧化物为无色气体
D.Z的单质与Cl 反应可生成共价化合物
2
【答案】D
【分析】设Z的原子序数为a,Y的原子序数为b,则X的原子序数为5a,1 mol X YZ 含42mol质
3 3 6
子,可得15a+3b+6a=21a+3b=42,即7a+b=14,因原子序数只能是整数,则a只能为1,b=7,Z为
H,Y为N,X为B,据此解答
【解析】A.X为B,原子序数为5,位于周期表的第二周期第IIIA族,故A错误;
B.Y为N,X为B,两者同周期,原子序数越小半径越大,原子半径:X>Y,故B错误;
C.Y为N,其氧化物二氧化氮为红棕色气体,故C错误;
D.Z为H,其单质氢气与氯气反应生成HCl,为共价化合物,故D正确;
故选:D。
31 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司56.(2022·浙江卷)W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y同族,Y的原子序数
是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是
A.非金属性:Y>W B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸 D.X与Y可形成化合物XY
2 3
【答案】D
【分析】X是地壳中含量最多的金属元素,X为Al元素,W和Y同族,Y的原子序数是W的2倍,
W为O元素,Y为S元素,Z为Cl元素,据此分析解题。
【解析】A.非金属性同主族从上至下逐渐减弱:Y<W,A错误;
B.氯化铝是共价化合物,B错误;
C.Y、Z的最高价氧化物对应的水化物分别硫酸和高氯酸,两者均为强酸,次氯酸也是氯的氧化物对
应的水化合物,但次氯酸为弱酸,C错误;
D.根据化合物的化合价代数和为0可知,铝与硫元素形成的化合物化学式为Al S,D正确;
2 3
答案选D。
57.(2021·江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元
素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下
列说法正确的是
A.原子半径:r(X)Y
C.该阴离子中X不满足8电子稳定结构D.最简单氢化物水溶液的pH:X>M
【答案】D
【分析】根据W是有机分子的骨架元素,知W为C元素:由图可如,Y形成1个双键,则其最外层
有6个电子,结合原子序数关系知,Y为O元素,则X为N元素;Z形成1个单键,则Z为F元素;
M的成键总数为6,则M为S元素。以此解答。
【解析】A.根据上述分析可知:Z为F元素,无正化合价,故A错误;
B.根据上述分析可知:W为C元素,Y为O元素。C原子的电子排布式为 ,未成对电子数
为2,O原子的电子排布式为 ,未成对电子数也为2,故B错误;
C.根据上述分析可知:X为N元素,该阴离子中N形成2个单键,有2对孤对电子,满足8电子稳定
结构,故C错误:
D.根据上述分析可知:X为N元素, 最简单氢化物 , 的水溶液星碱性;M为S元素, 最简单
氢化物 , 的水溶液呈酸性,故水溶液的 ,故D正确;
故答案:D。
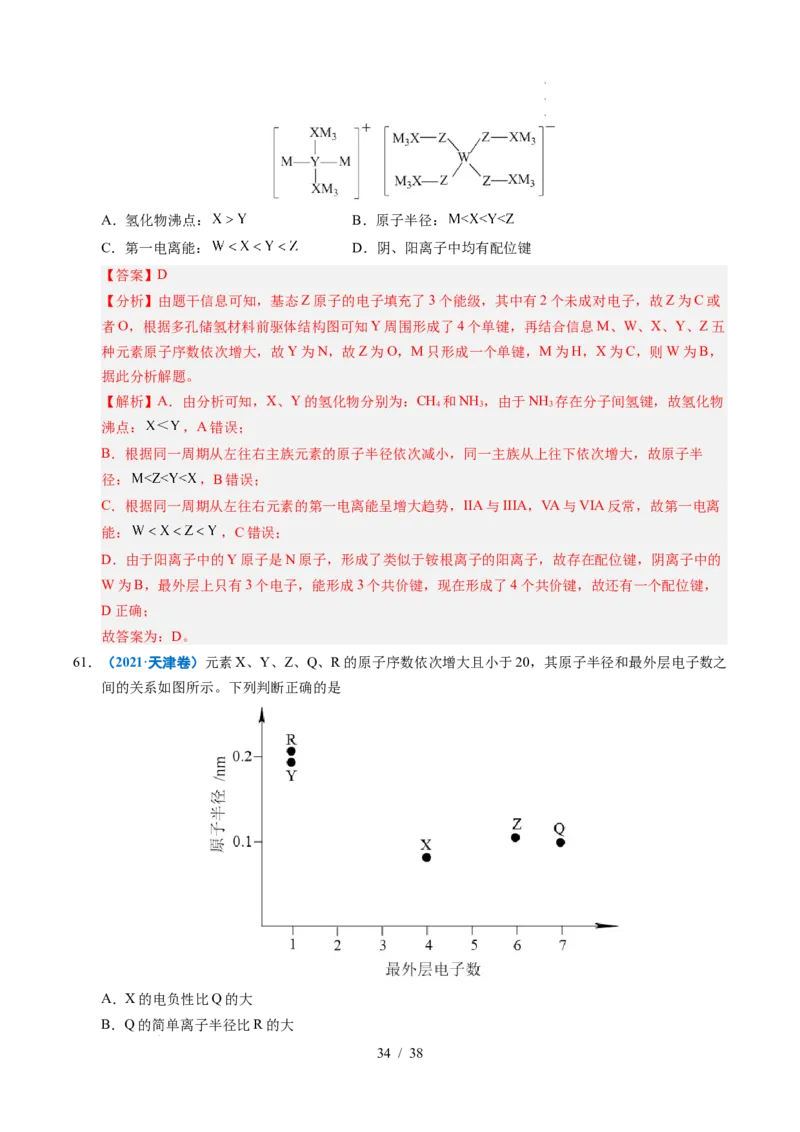
60.(2021·辽宁卷)某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,
基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是
33 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.氢化物沸点: B.原子半径:
C.第一电离能: D.阴、阳离子中均有配位键
【答案】D
【分析】由题干信息可知,基态Z原子的电子填充了3个能级,其中有2个未成对电子,故Z为C或
者O,根据多孔储氢材料前驱体结构图可知Y周围形成了4个单键,再结合信息M、W、X、Y、Z五
种元素原子序数依次增大,故Y为N,故Z为O,M只形成一个单键,M为H,X为C,则W为B,
据此分析解题。
【解析】A.由分析可知,X、Y的氢化物分别为:CH 和NH ,由于NH 存在分子间氢键,故氢化物
4 3 3
沸点: ,A错误;
B.根据同一周期从左往右主族元素的原子半径依次减小,同一主族从上往下依次增大,故原子半
径: ,B错误;
C.根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA,VA与VIA反常,故第一电离
能: ,C错误;
D.由于阳离子中的Y原子是N原子,形成了类似于铵根离子的阳离子,故存在配位键,阴离子中的
W为B,最外层上只有3个电子,能形成3个共价键,现在形成了4个共价键,故还有一个配位键,
D正确;
故答案为:D。
61.(2021·天津卷)元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之
间的关系如图所示。下列判断正确的是
A.X的电负性比Q的大
B.Q的简单离子半径比R的大
34 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.Z的简单气态氢化物的热稳定性比Q的强
D.Y的最高价氧化物对应的水化物的碱性比R的强
【答案】B
【分析】X、Y、Z、Q、R的原子序数依次增大且小于20,由图象中最外层电子数和原子半径的关系
可知,X为C、Y为Na、Z为S、Q为Cl、R为K。
【解析】A.C的电负性比Cl的小,故A错误;
B.核外电子数相同时质子数越大半径越小,故Q的简单离子半径比R的大,故B正确;
C.同周期元素,原子序数越大非金属性越强,则简单氢化物更稳定,则Z的简单气态氢化物的热稳
定性比Q的弱,故C错误;
D.同主族元素,原子序数越大金属性越强,则最高价氧化物对应水化物的碱性越强,则Y的最高价
氧化物对应的水化物的碱性比R的弱,故D错误;
故选B。
62.(2021·山东卷)X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合
物能以[XY ]+[XY ]-的形式存在。下列说法错误的是
4 6
A.原子半径:X>Y B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强 D.同周期中第一电离能小于X的元素有4种
【答案】D
【分析】Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴
离子和阳离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。
【解析】A.P与Cl在同一周期,则P半径大,即X>Y,A项不符合题意;
B.两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH 的失电子能力强,还原性强,
3 3
即X>Y,B项不符合题意;
C.同周期元素从左往右,金属性减弱,非金属性增强,各元素对应的金属单质还原性减弱,非金属
单质的氧化性增强,所以Cl 的氧化性最强,C项不符合题意;
2
D.同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素的
第一电离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5种,D
项符合题意;
故选D。
63.(2021·广东卷)一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元素 、 、
原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列说法不正
确的是
35 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A. 是一种强酸
B.非金属性:
C.原子半径:
D. 中, 的化合价为+2价
【答案】C
【分析】题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。
的原子核只有1个质子,则X为H元素;元素 、 、 原子序数依次增大,且均位于 的下一
周期,即第二周期元素,则Y为C元素,Z为O元素,W为F元素;元素 的原子比 原子多8个电
子,则E为Cl元素,综合以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。
据此分析解答。
【解析】A.氯元素非金属性较强,其最高价氧化物的水化物HClO 是一种强酸,故A正确;
4
B.同一周期元素从左到右非金属性逐渐增强,所以非金属性:F>O>C,故B正确;
C.同一周期从左到右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,电子层越多半径越
大,所以原子半径:Cl>C>F,故C错误;
D.OF 中,F为-1价,则O的化合价为+2价,故D正确;
2
答案选C。
64.(2021·全国甲卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和
X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正
确的是
A.原子半径:
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【分析】W.X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外
层电子数之和,也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X的单质
常温下均为气体,则推知W和X为非金属元素,所以可判断W为H元素,X为N元素,Z的最外层
电子数为1+5=6,Y的最外层电子数为 =3,则Y为Al元素,Z为S元素,据此结合元素及其化合物
的结构与性质分析解答。
【解析】根据上述分析可知,W为H元素,X为N元素,Y为Al元素,Z为S元素,则
A.电子层数越多的元素原子半径越大,同周期元素原子半径依次减小,则原子半径:Y(Al)>Z(S)>
X(N)>W(H),A错误;
B.W为H元素,X为N元素,两者可形成NH 和NH,B错误;
3 2 4
C.Y为Al元素,其氧化物为两性氧化物,可与强酸、强碱反应,C错误;
36 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.W、X和Z可形成(NH )S、NH HS,两者既含有离子键又含有共价键,D正确。
4 2 4
故选D。
65.(2021·湖南卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的
原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的 分子。下
列说法正确的是
A.简单离子半径:
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:
D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
【答案】B
【分析】Z的最外层电子数为K层的一半,则Z的核外有3个电子层,最外层电子数为1,即为Na,
W与X能形成原子个数比为2:1的18电子的分子,则形成的化合物为NH,所以W为H,X为N,Y
2 4
的原子序数是W和X的原子序数之和,则Y为O。据此分析解答。
【解析】由分析可知,W为H,X为N,Y为O,Z为Na。
A.离子的电子层数相同时,原子序数越小,半径越大,即离子半径大小为:N3->O2->Na+,即简单
离子半径为:X>Y>Z,故A错误;
B.W为H,Y为O,能形成HO,含有极性共价键和非极性共价键,故B正确;
2 2
C.X的最简单氢化物为氨气,Y的最简单氢化物为水,水的沸点高于氨气,即最简单氢化物的沸点
为Y>X,故C错误;
D.由W、X、Y三种元素形成的化合物有硝酸,硝酸铵,氨水等,硝酸,硝酸铵显酸性,氨水显碱
性,故由W、X、Y三种元素形成的化合物不一定都是酸性,故D错误;
故选B。
66.(2021·全国乙卷)我国嫦娥五号探测器带回 的月球土壤,经分析发现其构成与地球土壤类似
土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15。X、Y、Z为
同周期相邻元素,且均不与W同族,下列结论正确的是
A.原子半径大小顺序为
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
【答案】B
【分析】由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、Y、Z为同
周期相邻元素,可知W所在主族可能为第ⅢA族或第ⅥA族元素,又因X、Y、Z为同周期相邻元
素,且均不与W同族,故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已知可
推知W、X、Y、Z依次为O、Mg、Al、Si,据此答题。
【解析】A.O原子有两层,Mg、Al、Si均有三层且原子序数依次增大,故原子半径大小顺序为Mg
37 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司>Al>Si>O,即 ,A错误;
B.化合物XW即MgO为离子化合物,其中的化学键为离子键,B正确;
C.Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性介于导体和
绝缘体之间,故Y单质的导电性能强于Z单质的,C错误;
D.Z的氧化物的水化物为硅酸,硅酸酸性弱于碳酸,D错误;
故选B。
38 / 38
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司