文档内容
广东省 2018 年中考化学试题
可能用到的相对原子质量: H-1 Li-7 C-12 0-16 P-31 S-32 C1-35.5 Ca-40 Fe-56
一、选择题
1. 下图属“用后必须洗手”标志(贴在微毒或有毒的试剂瓶上)的是
A. B.
C. D.
【答案】B
【解析】
【详解】A、是节约用水的标志,错误;B、是“用后必须洗手”标志,正确;C、是禁止饮用的标志,错误;
D、是腐蚀品标志,错误。故选B。
点睛:熟悉各种标志表示的含义是解题关键。
2. 中华传统文化博大精深,下列古诗中不涉及化学变化的是
A. 梅须逊雪三分白,雪却输梅一段香 B. 爆竹声中一岁除,春风送暖入屠苏
C. 爝火燃回春浩浩,洪炉照破夜沉沉 D. 千锤万凿出深山,烈火焚烧若等闲
【答案】A
【解析】
A、梅须逊雪三分白,雪却输梅一段香的意思是梅花须逊让雪花三分晶莹洁白,雪花却输给梅花一段清香
(即梅不如雪白,雪没有梅香),无新物质生成,属于物理变化,符合题意;B、爆竹爆炸过程中有新物
质二氧化碳等生成,属于化学变化,不符合题意;C、煤炭燃烧过程中有新物质二氧化碳等生成,属于化
学变化,不符合题意;D、高温煅烧石灰石过程中有新物质氧化钙等生成,属于化学变化,不符合题意。
故选A。
点睛:物理变化和化学变化的根本区别在于是否有新物质生成。如果有新物质生成,则属于化学变化;反
之,则是物理变化。
3. 下列水果中酸度最强的是A. 菠萝pH=4.1 B. 木瓜pH-5.5
C. 草莓pH=3.2 D. 柠檬pH=2.3
【答案】D
【解析】
pH越小,酸性越强。2.3<3.1<4.1<5.5。故选D。
4. 下列说法正确的是
A. 溶液都是均一、稳定、无色透明的
B. 金刚石、石墨、活性炭性质相同
C. 排放CO 是引起酸雨的主要原因
2
D. 空气中O 的体积约占21%
2
【答案】D
【解析】
A、溶液不一定都是无色的,如硫酸铜溶液是蓝色的,错误;B、金刚石、石墨、活性炭化学性质相同,物
理性质不同,错误;C、排放SO 是引起酸雨的主要原因,错误;D、空气中O 的体积约占21%,正确。
2 2
故选D。
5. 下列物质不属于复合材料的是
A. 塑料 B. 玻璃钢 C. 碳素陶瓷 D. 钢筋混凝土
【答案】A
【解析】
A、塑料属于合成材料,正确;B、玻璃钢属于复合材料,错误;C、碳素陶瓷属于复合材料,错误;D、
钢筋混凝土属于复合材料,错误。故选A。
6. 下列操作正确的是A. 滴加溶液 B. 加入固体C. 量取液体 D.
加入酒精
【答案】D
【解析】
A、用胶头滴管滴加溶液时,胶头滴管应垂直悬空于容器口的正上方进行滴加,不能伸入试管内,错误;
B、试管中加入固体时,应将试管横放,将固体放在试管口,然后将试管慢慢竖起来,错误;C、量取液体
时,瓶塞应倒放在桌面上,错误;D、向酒精灯加入酒精时,应用漏斗进行添加,瓶塞倒放,标签向着手
心,禁止向燃着的酒精灯添加酒精,正确。故选D。
点睛:熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
7. 下列属于分解反应的是
A. 2HO 2H↑+O ↑ B. CO+2NaOH=Na CO+H O
2 2 2 2 2 3 2
C. C+H O CO+H D. NH +CO +H O=NH HCO
2 2 3 2 2 4 3
【答案】A
【解析】
A、反应物一种,生成物两种,符合“一变多”的形式,属于分解反应,正确;B、反应物有两种,生成物
两种,不符合“一变多”的形式,不属于分解反应,错误;C、反应物有两种,生成物两种,不符合“一
变多”的形式,不属于分解反应,错误;D、反应物有两种,生成物有三种,不符合“一变多”的形式,
不属于分解反应,错误。故选A。点睛:掌握分解反应的特征是解题关键。
8. 有一混合气体通过澄清石灰水无明显现象,剩余气体经浓硫酸洗气后点燃,在火焰上方罩上干冷烧杯,
内壁出现水雾。符合上述现象的气体组合是
A. H、CO、CO B. N、O、CO C. H、CH、CO D. H、CH、CO
2 2 2 2 2 2 4 2 4 2
【答案】C
【解析】
·
通过澄清石灰水无明显现象,说明无二氧化碳;经浓硫酸洗气后点燃,在火焰上方罩上干冷烧杯,内壁出
现水雾,说明该气体组合中含有氢元素。故选C。
9. 下表中知识的归纳正确的是
有机物都易燃,都要远离火源
2O表示两个氧元素
A用语 B安全 安全封闭房间烧含 碳燃料要防CO
2O 表示两个氧分子
2 中毒
生活垃圾集中焚烧用于发电 儿童需补钙是因为缺乏微量元素钙
C环保
新制木家具通风放置让甲醛
D生活
糖类、 脂肪、蛋白质和水都是营
挥发 养素
A. A B. B C. C D. D
【答案】C
【解析】
A、2O表示两个氧原子,错误;B、有机物不一定都易燃,如CCl ,错误;C、生活垃圾集中焚烧,用于
4
发电;新制木家具通风放置,让甲醛挥发,正确;D、钙是人体内的常量元素,错误。故选C。
10. 区别下列物质的方法错误的是
A. 羊绒与棉花(灼烧) B. 醋酸与盐酸(滴入酚酞)
C. 硬水与软水(加入肥皂水) D. 氯化钾与氯化铵(加熟石灰研磨)
【答案】B
【解析】
A、灼烧羊毛有烧焦羽毛的气味,灼烧棉花没有,可以区别,正确;B、醋酸与盐酸都显酸性,滴入酚酞溶
液,都不变色,错误;C、硬水加肥皂水,起浮渣、泡沫少,软水加肥皂水无浮渣、泡沫丰富,可以区别,
正确;D、氯化铵加熟石灰研磨产生氨气,有刺激性气味,氯化钾加熟石灰研磨,无刺激性气味,可以区
别,正确。故选B。
11. 下列说法正确的是
A. 催化剂的作用是加快反应速率 B. 石油是有机物,也是纯净物C. 铁器在干燥的空气中不易生锈 D. 节约用水对沿海城市意义不大
【答案】C
【解析】
A、催化剂的作用是改变反应速率,错误;B、石油是有机物,也是混合物,错误;C、铁生锈的条件是铁
与空气中的氧气和水共同作用。故铁器在干燥的空气中不易生锈,正确;D、海水中盐含量很高,不能直
接饮用,海水淡化成本高,且节约用水是每个公民应尽责任义务,错误。故选C。
12. 下表物质中含有少量杂质,其中除杂方法正确的是
物质 杂质 除去杂质的方法
A CaCl 溶液 HCl 滴入碳酸钠溶液
2
B CO O 通过灼热的铜网
2 2
C NaOH NaCO 加入稀盐酸至不再产生气泡
2 3
D CuO Cu 加足量稀盐酸,充分搅拌后再过滤
A. A B. B C. C D. D
【答案】B
【解析】
A、碳酸钠溶液与盐酸反应生成氯化钠,氯化钠是新的杂质,违背除杂原则,错误;B、氧气与灼热的铜网
反应生成氧化铜,能除去氧气且不引入新的杂质,正确;C、稀盐酸与氢氧化钠溶液反应,违背除杂原则,
错误;D、稀盐酸与氧化铜反应,违背除杂原则,错误。故选B。
点睛:解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)
是正确解题的关键。
13. 向一定质量的水中加入生石灰,下列曲线错误的是
A. B. C. D.
【答案】D
【解析】
A、氧化钙与水反应生成氢氧化钙,溶液质量增加。当溶液饱和后溶液质量最大,继续加入氧化钙,氧化
钙与水继续反应,当水反应完后,溶液质量为0,正确;B、氧化钙与水反应生成氢氧化钙,溶质质量分数增大。当溶液饱和后,溶质质量分数最大;继续加入氧化钙,氧化钙与水继续反应,溶液温度升高,氢氧
化钙溶解度变小,溶质质量分数减小,当水反应完后,溶液质量分数为0,正确;C、氧化钙与水反应生成
氢氧化钙,当加入氧化钙达到一定量时恰好与水完全反应,此时水的质量为 0,正确;D、氧化钙与水反
应温度升高,当氧化钙恰好与水完全反应后温度最高,此后温度开始降低,但不会低于反应前的温度,错
误。故选D。
点睛:要准确解答此类题,关键要对化学反应 的知识熟练掌握,并能结合图象的数学意义,综合考虑;图
象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程。
14. 利用盐酸和硝酸银探究铁、铜、银的金属活动顺序,下列实验可以不需要进行的是
A. 铁+稀盐酸 B. 铜+稀盐酸 C. 银+稀盐酸 D. 铜+硝酸银溶液
【答案】C
【解析】
由金属活动顺序表的应用,验证实验的设计思路为:根据三种金属与盐酸反应情况,可验证铁的活动性比
铜、银强;然后利用金属铜和硝酸银的置换结果,验证铜的活动性比银强;对比四个实验,实验A证明金
属铁能置换出酸中的氢;B证明金属铜不能置换出酸中的氢,而实验D可以证明银的活动性小于铜,所以
不做实验C也不影响三种金属活动性的判断。故选C。
二、非选择题
15. “下图”是部分元素的离子结构示意图和元素周期表的一部分。 请回答:
(1)图①、②中属于阴离子的是___(填序号),该元素的质子数为_____;13号元素原子的最外层电子数为
_____。
(2)由表中原子序数为1、8、13的元素组成物质的化学式为_____。
【答案】 (1). ② (2). 17 (3). 3 (4). Al(OH)
3
【解析】
(1)根据质子数小于电子数解答;根据原子中质子数等于电子数解答;(2)根据1、8、13号元素分析解答。
(1)图①中质子数大于电子数,属于阳离子;图②中质子数小于电子数,属于阴离子,故选②;该元素的质
子数为17;13号元素原子的最外层电子数为13-2-8=3;(2)1、8、13号元素分别为H、O、Al,它们组成物
质的化学式为Al(OH)。
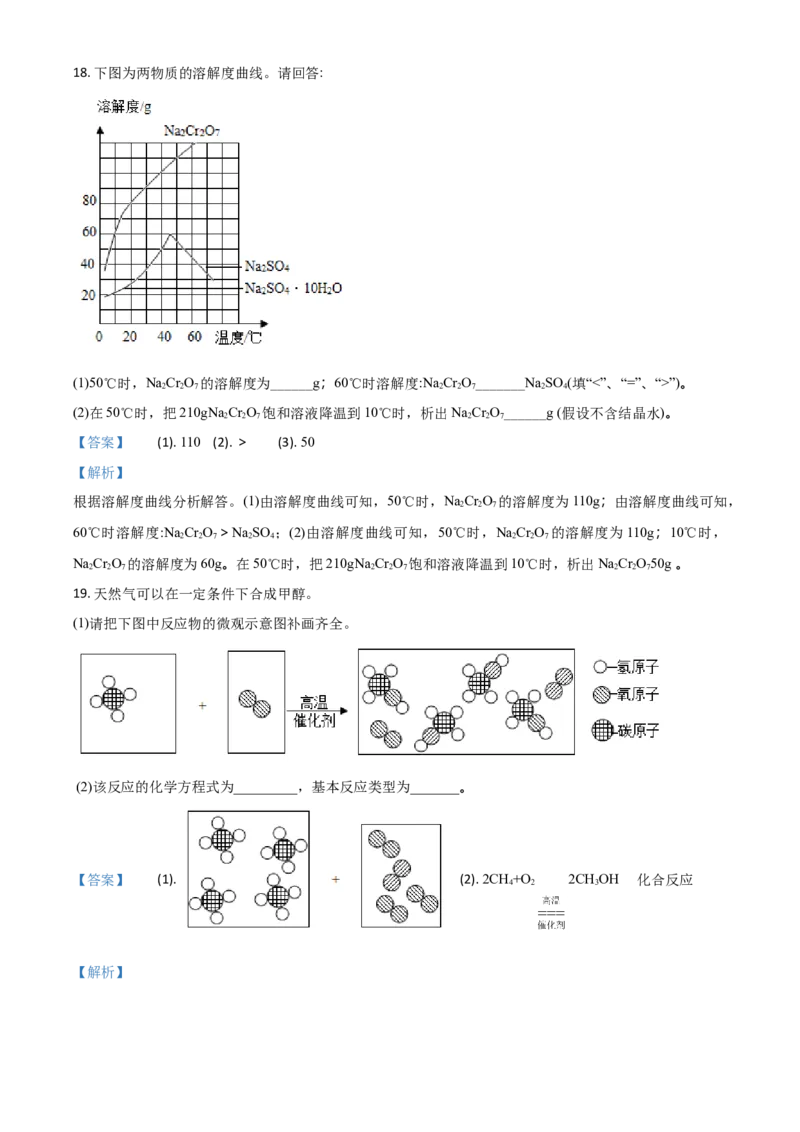
316. “如图”表示元素的化合价与物质类别关系。若它表示氮元素的部分关系图。则:
(1)A点对应的物质类别是_____;B点表示物质的化学式为______。
(2)某化合物的化学式为KNO,它代表的点是_______(填字母);写出由D点表示的物质与水发生反应生成
3
E的化学方程式___________。
【答案】 (1). 单质 (2). NO (3). F (4). NO+H O=2HNO
2 5 2 3
【解析】
(1)根据单质的化合价为0解答;根据B点中氮的氧化物中氮元素的化合价为+2价解答;(2)根据KNO 属于
3
盐及KNO 中氮元素的化合价分析解答;根据D点中氮的氧化物中氮元素显+5价及E点表示的酸中氮元素
3
的化合价为+5价分析解。(1)A点时氮元素的化合价为0,对应的物质类别是单质;B点中氮的氧化物中氮
元素的化合价为+2价,氧元素通常显-2价,故B点表示物质的化学式为NO;(2)KNO 属于盐;KNO 中钾
3 3
元素显+1价,氧元素显-2价,根据化合物中各元素正负化合价代数和为0可得氮元素的化合价为+5价,
故它代表的点是F;D点表示+5价氮的氧化物NO ,E点表示的酸中氮元素显+5价,即为HNO ;NO 与
2 5 3 2 5
HO反应生成HNO,反应的化学方程式为NO+H O=2HNO 。
2 3 2 5 2 3
17. 2017年冬天,某小伙子为了取暖在卫生间里贴满了“暖宝宝”(该产品的部分说明书为:“暖身更暖心,升
温快。发热成分:高纯度铁粉、水、盐……;发热时间: 10小时;平均温度:52℃),他把门窗关闭以防暖气
泄漏。几分钟后,他失去意识而倒地,幸而被门外的朋友及时救起。请回答:
(1)铁氧化发热,主要生成物的化学式为______;盐是催化剂,其质量和_____不变。
(2)该小伙子失去意识并不是温度过高和身体本身的原因,而是_____。
【答案】 (1). Fe O (2). 化学性质 (3). 铁氧化消耗氧气,导致缺氧
2 3
【解析】
(1)根据铁与氧气和水反应生成氧化铁解答;根据催化剂在化学反应中质量和化学性质都不变解答;(2)根据
铁氧化发热需要消耗氧气解答。(1)铁与氧气和水反应生成氧化铁,化学式为Fe O ;盐是催化剂,其质量
2 3
和化学性质不变;(2)该小伙子失去意识并不是温度过高和身体本身的原因,而是铁氧化消耗氧气,导致缺
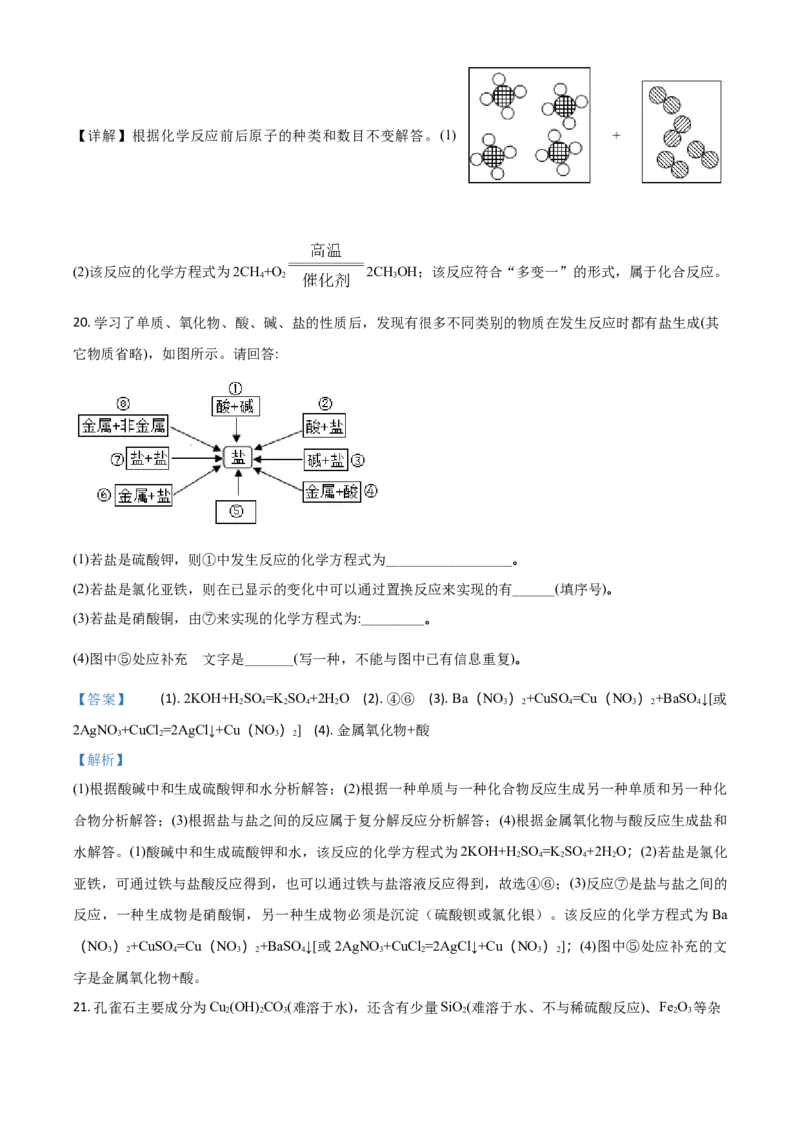
氧。18. 下图为两物质的溶解度曲线。请回答:
(1)50℃时,NaCr O 的溶解度为______g;60℃时溶解度:Na Cr O_______NaSO (填“<”、“=”、“>”)。
2 2 7 2 2 7 2 4
(2)在50℃时,把210gNaCr O 饱和溶液降温到10℃时,析出NaCr O______g (假设不含结晶水)。
2 2 7 2 2 7
【答案】 (1). 110 (2). > (3). 50
【解析】
根据溶解度曲线分析解答。(1)由溶解度曲线可知,50℃时,NaCr O 的溶解度为110g;由溶解度曲线可知,
2 2 7
60℃时溶解度:Na Cr O >NaSO ;(2)由溶解度曲线可知,50℃时,NaCr O 的溶解度为110g;10℃时,
2 2 7 2 4 2 2 7
NaCr O 的溶解度为60g。在50℃时,把210gNaCr O 饱和溶液降温到10℃时,析出NaCr O50g 。
2 2 7 2 2 7 2 2 7
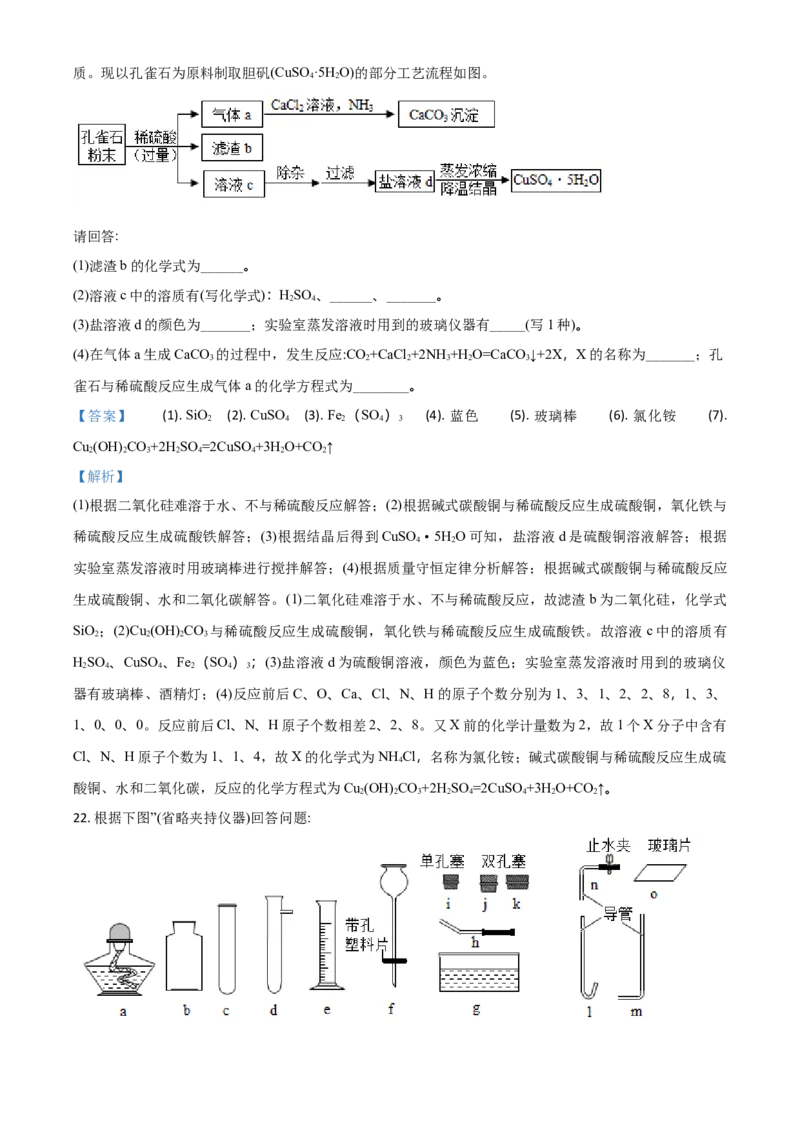
19. 天然气可以在一定条件下合成甲醇。
(1)请把下图中反应物的微观示意图补画齐全。
(2)该反应的化学方程式为_________,基本反应类型为_______。
【答案】 (1). (2). 2CH+O 2CHOH 化合反应
4 2 3
【解析】【详解】根据化学反应前后原子的种类和数目不变解答。(1)
(2)该反应的化学方程式为2CH+O 2CHOH;该反应符合“多变一”的形式,属于化合反应。
4 2 3
20. 学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其
它物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为__________________。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有______(填序号)。
(3)若盐是硝酸铜,由⑦来实现的化学方程式为:_________。
的
(4)图中⑤处应补充 文字是_______(写一种,不能与图中已有信息重复)。
【答案】 (1). 2KOH+H SO =K SO +2H O (2). ④⑥ (3). Ba(NO ) +CuSO=Cu(NO ) +BaSO ↓[或
2 4 2 4 2 3 2 4 3 2 4
2AgNO+CuCl =2AgCl↓+Cu(NO )] (4). 金属氧化物+酸
3 2 3 2
【解析】
(1)根据酸碱中和生成硫酸钾和水分析解答;(2)根据一种单质与一种化合物反应生成另一种单质和另一种化
合物分析解答;(3)根据盐与盐之间的反应属于复分解反应分析解答;(4)根据金属氧化物与酸反应生成盐和
水解答。(1)酸碱中和生成硫酸钾和水,该反应的化学方程式为2KOH+H SO =K SO +2H O;(2)若盐是氯化
2 4 2 4 2
亚铁,可通过铁与盐酸反应得到,也可以通过铁与盐溶液反应得到,故选④⑥;(3)反应⑦是盐与盐之间的
反应,一种生成物是硝酸铜,另一种生成物必须是沉淀(硫酸钡或氯化银)。该反应的化学方程式为Ba
(NO ) +CuSO=Cu(NO ) +BaSO ↓[或2AgNO+CuCl =2AgCl↓+Cu(NO ) ];(4)图中⑤处应补充的文
3 2 4 3 2 4 3 2 3 2
字是金属氧化物+酸。
21. 孔雀石主要成分为Cu (OH) CO(难溶于水),还含有少量SiO(难溶于水、不与稀硫酸反应)、Fe O 等杂
2 2 3 2 2 3质。现以孔雀石为原料制取胆矾(CuSO ·5H O)的部分工艺流程如图。
4 2
请回答:
(1)滤渣b的化学式为______。
(2)溶液c中的溶质有(写化学式):HSO 、______、_______。
2 4
(3)盐溶液d的颜色为_______;实验室蒸发溶液时用到的玻璃仪器有_____(写1种)。
(4)在气体a生成CaCO 的过程中,发生反应:CO +CaCl +2NH+H O=CaCO ↓+2X,X的名称为_______;孔
3 2 2 3 2 3
雀石与稀硫酸反应生成气体a的化学方程式为________。
【答案】 (1). SiO (2). CuSO (3). Fe (SO ) (4). 蓝色 (5). 玻璃棒 (6). 氯化铵 (7).
2 4 2 4 3
Cu (OH) CO+2H SO =2CuSO+3H O+CO↑
2 2 3 2 4 4 2 2
【解析】
(1)根据二氧化硅难溶于水、不与稀硫酸反应解答;(2)根据碱式碳酸铜与稀硫酸反应生成硫酸铜,氧化铁与
稀硫酸反应生成硫酸铁解答;(3)根据结晶后得到CuSO ·5HO可知,盐溶液d是硫酸铜溶液解答;根据
4 2
实验室蒸发溶液时用玻璃棒进行搅拌解答;(4)根据质量守恒定律分析解答;根据碱式碳酸铜与稀硫酸反应
生成硫酸铜、水和二氧化碳解答。(1)二氧化硅难溶于水、不与稀硫酸反应,故滤渣b为二氧化硅,化学式
SiO ;(2)Cu (OH) CO 与稀硫酸反应生成硫酸铜,氧化铁与稀硫酸反应生成硫酸铁。故溶液c中的溶质有
2 2 2 3
HSO 、CuSO 、Fe (SO ) ;(3)盐溶液d为硫酸铜溶液,颜色为蓝色;实验室蒸发溶液时用到的玻璃仪
2 4 4 2 4 3
器有玻璃棒、酒精灯;(4)反应前后C、O、Ca、Cl、N、H的原子个数分别为1、3、1、2、2、8,1、3、
1、0、0、0。反应前后Cl、N、H原子个数相差2、2、8。又X前的化学计量数为2,故1个X分子中含有
Cl、N、H原子个数为1、1、4,故X的化学式为NH Cl,名称为氯化铵;碱式碳酸铜与稀硫酸反应生成硫
4
酸铜、水和二氧化碳,反应的化学方程式为Cu (OH) CO+2H SO =2CuSO+3H O+CO↑。
2 2 3 2 4 4 2 2
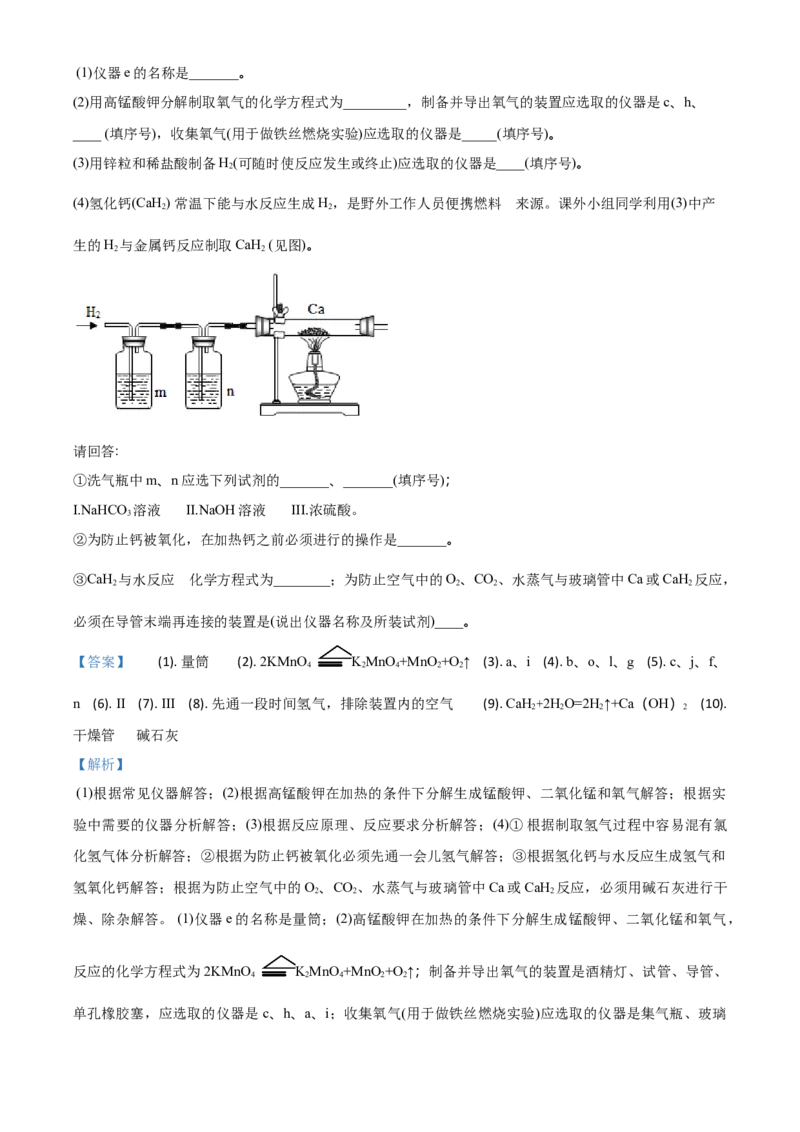
22. 根据下图”(省略夹持仪器)回答问题:(1)仪器e的名称是_______。
(2)用高锰酸钾分解制取氧气的化学方程式为_________,制备并导出氧气的装置应选取的仪器是c、h、
____ (填序号),收集氧气(用于做铁丝燃烧实验)应选取的仪器是_____(填序号)。
(3)用锌粒和稀盐酸制备H(可随时使反应发生或终止)应选取的仪器是____(填序号)。
2
的
(4)氢化钙(CaH) 常温下能与水反应生成H,是野外工作人员便携燃料 来源。课外小组同学利用(3)中产
2 2
生的H 与金属钙反应制取CaH (见图)。
2 2
请回答:
①洗气瓶中m、n应选下列试剂的_______、_______(填序号);
I.NaHCO 溶液 II.NaOH溶液 III.浓硫酸。
3
②为防止钙被氧化,在加热钙之前必须进行的操作是_______。
的
③CaH 与水反应 化学方程式为________;为防止空气中的O、CO、水蒸气与玻璃管中Ca或CaH 反应,
2 2 2 2
必须在导管末端再连接的装置是(说出仪器名称及所装试剂)____。
【答案】 (1). 量筒 (2). 2KMnO KMnO +MnO+O ↑ (3). a、i (4). b、o、l、g (5). c、j、f、
4 2 4 2 2
n (6). II (7). III (8). 先通一段时间氢气,排除装置内的空气 (9). CaH+2HO=2H↑+Ca(OH) (10).
2 2 2 2
干燥管 碱石灰
【解析】
(1)根据常见仪器解答;(2)根据高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气解答;根据实
验中需要的仪器分析解答;(3)根据反应原理、反应要求分析解答;(4)①根据制取氢气过程中容易混有氯
化氢气体分析解答;②根据为防止钙被氧化必须先通一会儿氢气解答;③根据氢化钙与水反应生成氢气和
氢氧化钙解答;根据为防止空气中的O 、CO 、水蒸气与玻璃管中Ca或CaH 反应,必须用碱石灰进行干
2 2 2
燥、除杂解答。 (1)仪器e的名称是量筒;(2)高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气,
反应的化学方程式为2KMnO KMnO +MnO+O ↑;制备并导出氧气的装置是酒精灯、试管、导管、
4 2 4 2 2
单孔橡胶塞,应选取的仪器是c、h、a、i;收集氧气(用于做铁丝燃烧实验)应选取的仪器是集气瓶、玻璃片、导管l、及水槽(集气瓶底要留有少量水),故选b、o、l、g;(3)用锌粒和稀盐酸制备H(可随时使反
2
应发生或终止)应选取的仪器是c、j、f、n;(4)①制取氢气过程中容易混有氯化氢气体,应用氢氧化钠溶
液除去,故m为氢氧化钠溶液,故选II,n为浓硫酸,故选III;②为防止钙被氧化,在加热钙之前必须进
行的操作是先通一段时间氢气,排除装置内的空气;③氢化钙与水反应生成氢气和氢氧化钙,反应的化学
方程式为CaH+2HO=2H↑+Ca(OH) ;为防止空气中的O 、CO 、水蒸气与玻璃管中Ca或CaH 反应,
2 2 2 2 2 2 2
必须在导管末端再连接的装置是装有碱石灰的干燥管。
23. 请参与下列探究实验:
【实验探究】
步
实验操作 实验现象 结论或解释
骤
用玻棒分别蘸取95%的酒精、 酒精_______,蒸馏 结论:酒精是可燃物,水
(1)
蒸馏水置于火焰上。 水_______。 不是可燃物。
在铁片两端放大小相同的硬纸 结论:乒乓球碎片的
乒乓球碎片先燃烧、
(2) 片、乒乓球碎片,在铁片中间 ________比硬纸片的
硬纸片后燃烧。
加热。 低。
在右图中打开分液漏斗的旋塞
①溶液中产生气泡;
②蜡烛火焰a_____填 现象②的原因是:CO 不
(3) 2
“先于”“后于”)b熄 助燃;___________。
灭。
用大烧杯罩住高低两支点燃的
①烧杯底部变黑;② CO 不助燃,蜡烛不完
2
(4) 蜡烛火焰d比c先熄 全燃烧;d 先熄灭的原
蜡烛。
灭。 因是:_______。
【拓展】堆积的面粉不容易点燃,即使少量点燃也只是小火燃烧;如果把面粉撒向空中遇火星可能会发生
爆炸。“小火燃烧”和“发生爆炸”的原因分别是:_______________。
【答案】 (1). 燃烧 不燃烧 (2). 着火点 (3). 先于 (4). CO 密度比空气大 (5). 燃烧生成的
2
热气体密度小,占据烧杯的上方,上方氧气含量较低 (6). “小火燃烧”的原因是:因为堆积的面粉与
空气接触不充分 (7). “发生爆炸”的原因是:与空气接触面积大,燃烧比较剧烈,空气受热膨胀,发
生爆炸
【解析】
(1)根据酒精是可燃物,水不是可燃物解答;(2)根据乒乓球碎片先燃烧、硬纸片后燃烧解答;(3)根据二氧
化碳的密度比空气大解答;(4)根据氧气的密度比空气大,上方氧气含量较低解答;【拓展】根据面粉与空气的接触面积不同分析解答。(1)由于酒精是可燃物,水不是可燃物,所以能观察到的实验现象是酒精燃烧,
蒸馏水不燃烧;(2)根据乒乓球碎片先燃烧、硬纸片后燃烧可知,乒乓球碎片的着火点比硬纸片的低;(3)打
开分液漏斗的旋塞,分液漏斗中的盐酸注入烧杯中,与烧杯中的碳酸钠溶液反应,生成二氧化碳,CO 不
2
助燃且密度比空气大。故能观察到蜡烛火焰a先于b熄灭。(4)d 先熄灭的原因是燃烧生成的热气体密度小,
占据烧杯的上方,氧气的密度比空气大,上方氧气含量较低;【拓展】“小火燃烧”的原因是因为堆积的
面粉与空气接触不充分;“发生爆炸”的原因是与空气接触面积大,燃烧比较剧烈,空气受热膨胀,发生
爆炸。
24. 大型电动车使用的磷酸亚铁锂(LiFePO )电池,具有“体积小、成本低、充电快、输出功率高、循环寿命
4
长”等优点。回答问题:
(1)磷酸亚铁锂中非金属元素的原子个数比为_______。
(2)磷酸亚铁锂中锂、磷元素的质量比为_______。
(3)磷酸亚铁锂中铁元素的质量分数为________(精确到0.1%)。
【答案】(1)P:O=1:4(2)7:31(3)35.4%
【解析】
【详解】根据磷酸亚铁锂的化学式计算解答。(1)根据磷酸亚铁锂的化学式为LiFePO ,其中P、O属于非金
4
属元素,故磷酸亚铁锂中非金属元素的原子个数比为P:O=1:4;(2)磷酸亚铁锂中锂、磷元素的质量比为
7:31;(3)磷酸亚铁锂中铁元素的质量分数为 ×100%=35.4%。
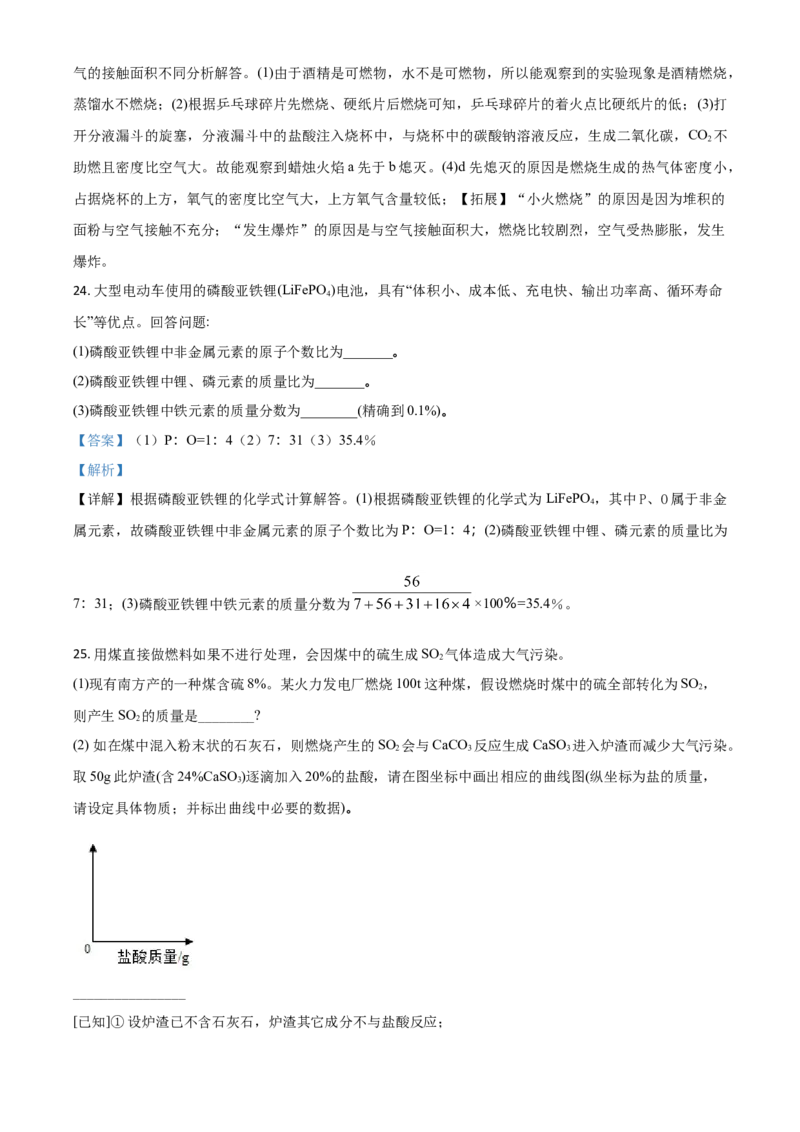
25. 用煤直接做燃料如果不进行处理,会因煤中的硫生成SO 气体造成大气污染。
2
(1)现有南方产的一种煤含硫8%。某火力发电厂燃烧100t这种煤,假设燃烧时煤中的硫全部转化为SO ,
2
则产生SO 的质量是________?
2
(2) 如在煤中混入粉末状的石灰石,则燃烧产生的SO 会与CaCO 反应生成CaSO 进入炉渣而减少大气污染。
2 3 3
取50g此炉渣(含24%CaSO)逐滴加入20%的盐酸,请在图坐标中画出相应的曲线图(纵坐标为盐的质量,
3
请设定具体物质;并标出曲线中必要的数据)。
________________
[已知]①设炉渣已不含石灰石,炉渣其它成分不与盐酸反应;②CaSO 和盐酸反应类似于CaCO
3 3
(3)向燃烧后的烟气喷洒石灰浆也可吸收SO 生成CaSO。现用一万元分别购买两种原料来除去SO ,相关
2 3 2
数据如下表:
方法 物质 相对分子质量 纯度 价格 (元/t) 除SO 的量 (t)
2
A 石灰石 100 90% 200 14.4
B 熟石灰 74 94% 500 14.6
方法B比方法A除SO 的量略大,而且工业上多数采用方法B。其原因分别是:_________。
2
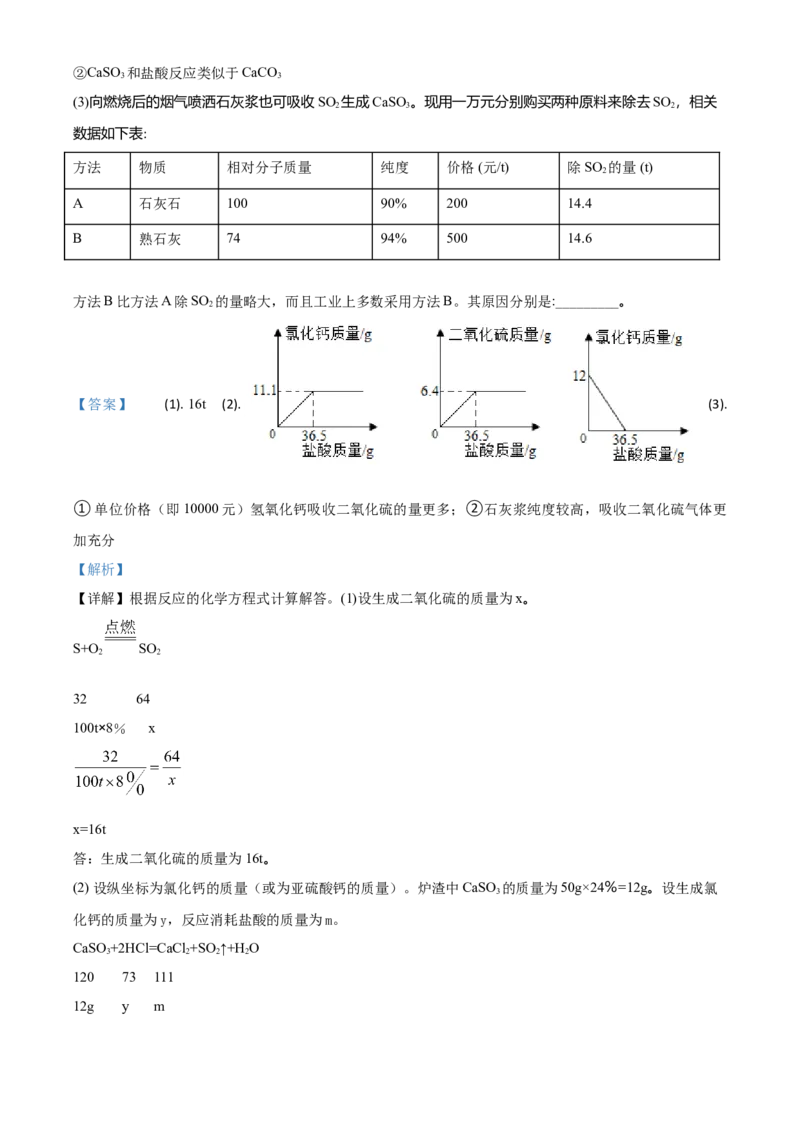
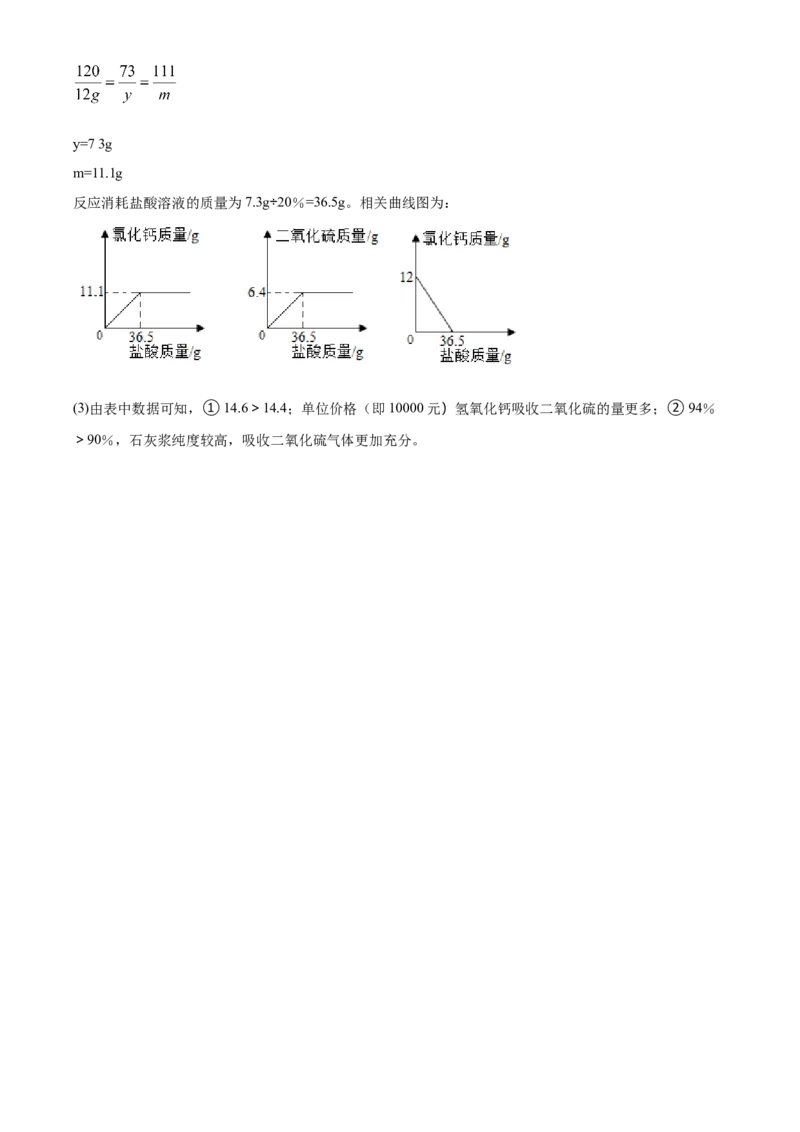
【答案】 (1). 16t (2). (3).
①单位价格(即10000元)氢氧化钙吸收二氧化硫的量更多;②石灰浆纯度较高,吸收二氧化硫气体更
加充分
【解析】
【详解】根据反应的化学方程式计算解答。(1)设生成二氧化硫的质量为x。
S+O SO
2 2
32 64
100t×8% x
x=16t
答:生成二氧化硫的质量为16t。
(2) 设纵坐标为氯化钙的质量(或为亚硫酸钙的质量)。炉渣中CaSO 的质量为50g×24%=12g。设生成氯
3
化钙的质量为y,反应消耗盐酸的质量为m。
CaSO+2HCl=CaCl +SO↑+H O
3 2 2 2
120 73 111
12g y m.
y=73g
m=11.1g
反应消耗盐酸溶液的质量为7.3g÷20%=36.5g。相关曲线图为:
(3)由表中数据可知,①14.6>14.4;单位价格(即10000元)氢氧化钙吸收二氧化硫的量更多;②94%
>90%,石灰浆纯度较高,吸收二氧化硫气体更加充分。