文档内容
考阅评·大联考
2024 年秋季广西示范性高中高一期中考调研测试
化学科试卷
本试卷满分100分,考试时间75分钟
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写清楚,将条形码准确粘贴在条形码区域内。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工
整、笔迹清楚。
3.请按照题号顺序在各题目的答题区域内作答,超出答题区书写的答案无效;在草稿纸、试题
卷上答题无效。
4.保持卡面清洁,不要折叠、不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H—l C—12 O—16 S—32 Na—23 Cl—35.5
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个正确选项)
1.化学贯穿古今,下列对古诗词所涉及化学知识的解读不正确的是( )
A.“错把陈醋当成墨,写尽半生纸上酸”,陈醋是混合物
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“熬胆矾铁斧,久之亦化为铜”,其中铜能导电,所以铜是电解质
D.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中发生的变化过程涉及电子转移
2.下列各组物质的分类正确的是( )
A.混合物:漂白粉、氯水、冰水混合物 B.酸:NaHSO、HCl、HClO
4
C.酸性氧化物:CO、CO、NaO D.同素异形体:C 、金刚石、石墨
2 2 60
3.下列离子方程式书写正确的是( )
A.用醋酸除水垢:
B.氢氧化钡溶液与稀硫酸反应:
C.钠与水反应:
D.澄清石灰水与过量碳酸氢钠反应:
4.下列变化过程中,必须加入氧化剂才能实现的是( )
A.CuO→Cu B.C→CO C.FeCl →FeCl D.(NH )SO →NH
2 3 2 4 2 4 3
5.关于反应 ,下列说法正确的是( )
A.水是氧化剂,LiH是还原剂 B.该反应属于置换反应
C.LiH既是氧化剂又是还原剂 D.该反应每生成1mol H,转移的电子数为2mol
2
6.用N 代表阿伏加德罗常数的值,下列说法正确的是( )
AA.常温常压下,11.2L甲烷气体含有的分子数为0.5 N
A
B.0.1mol OH-中含有的电子数为N
A
C.通常情况下,7.8g过氧化钠所含阴离子数为0.2 N
A
D.将4.0g NaOH溶于1L水中可得0.1mol/L NaOH溶液
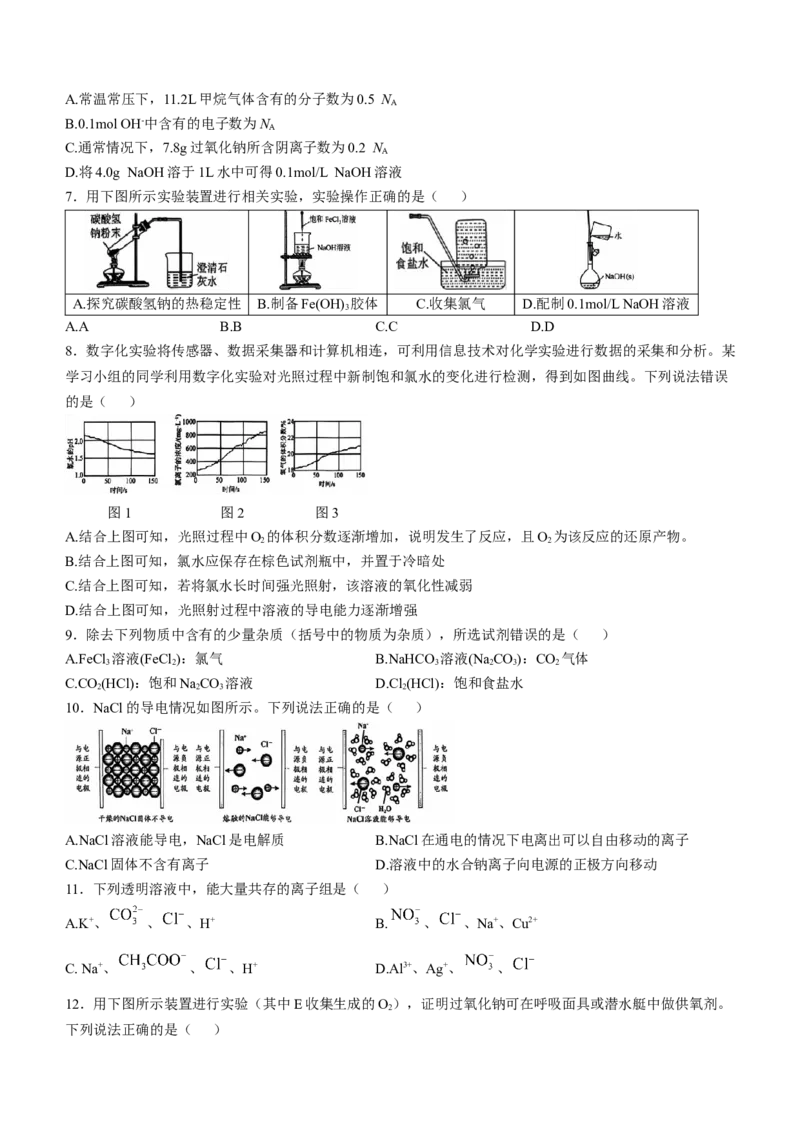
7.用下图所示实验装置进行相关实验,实验操作正确的是( )
A.探究碳酸氢钠的热稳定性 B.制备Fe(OH) 胶体 C.收集氯气 D.配制0.1mol/L NaOH溶液
3
A.A B.B C.C D.D
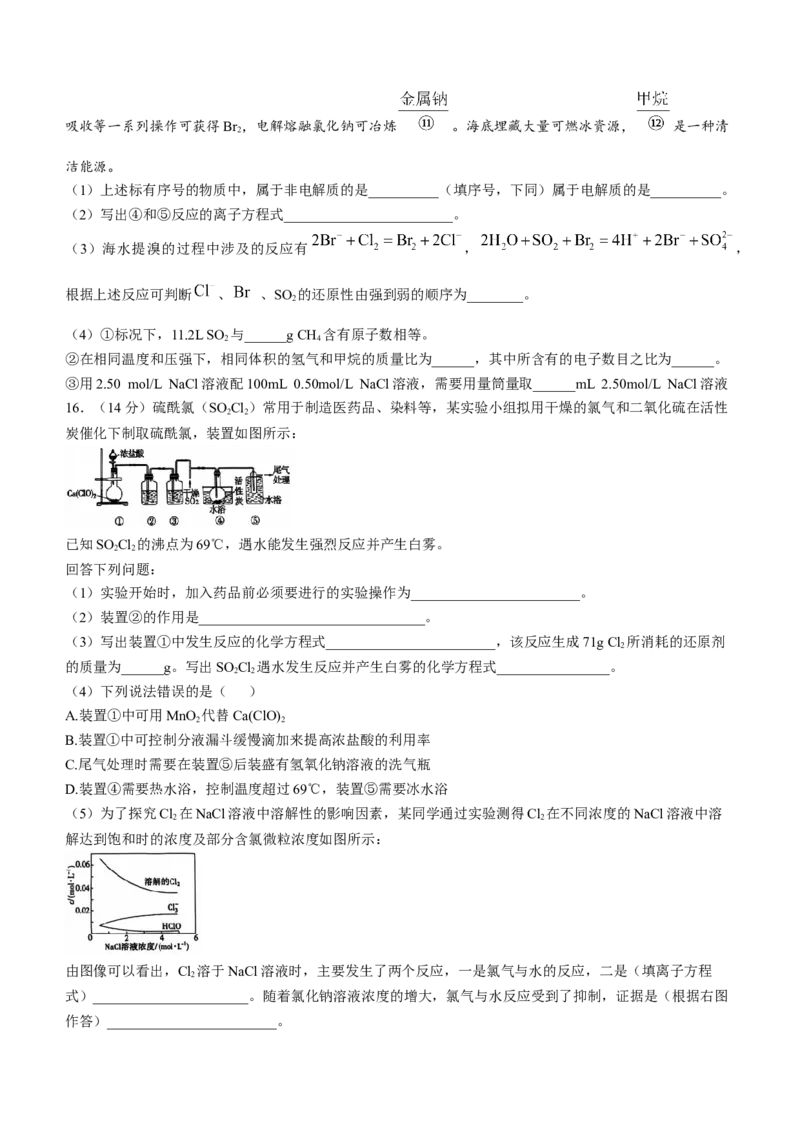
8.数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。某
学习小组的同学利用数字化实验对光照过程中新制饱和氯水的变化进行检测,得到如图曲线。下列说法错误
的是( )
图1 图2 图3
A.结合上图可知,光照过程中O 的体积分数逐渐增加,说明发生了反应,且O 为该反应的还原产物。
2 2
B.结合上图可知,氯水应保存在棕色试剂瓶中,并置于冷暗处
C.结合上图可知,若将氯水长时间强光照射,该溶液的氧化性减弱
D.结合上图可知,光照射过程中溶液的导电能力逐渐增强
9.除去下列物质中含有的少量杂质(括号中的物质为杂质),所选试剂错误的是( )
A.FeCl 溶液(FeCl ):氯气 B.NaHCO 溶液(NaCO):CO 气体
3 2 3 2 3 2
C.CO (HCl):饱和NaCO 溶液 D.Cl (HCl):饱和食盐水
2 2 3 2
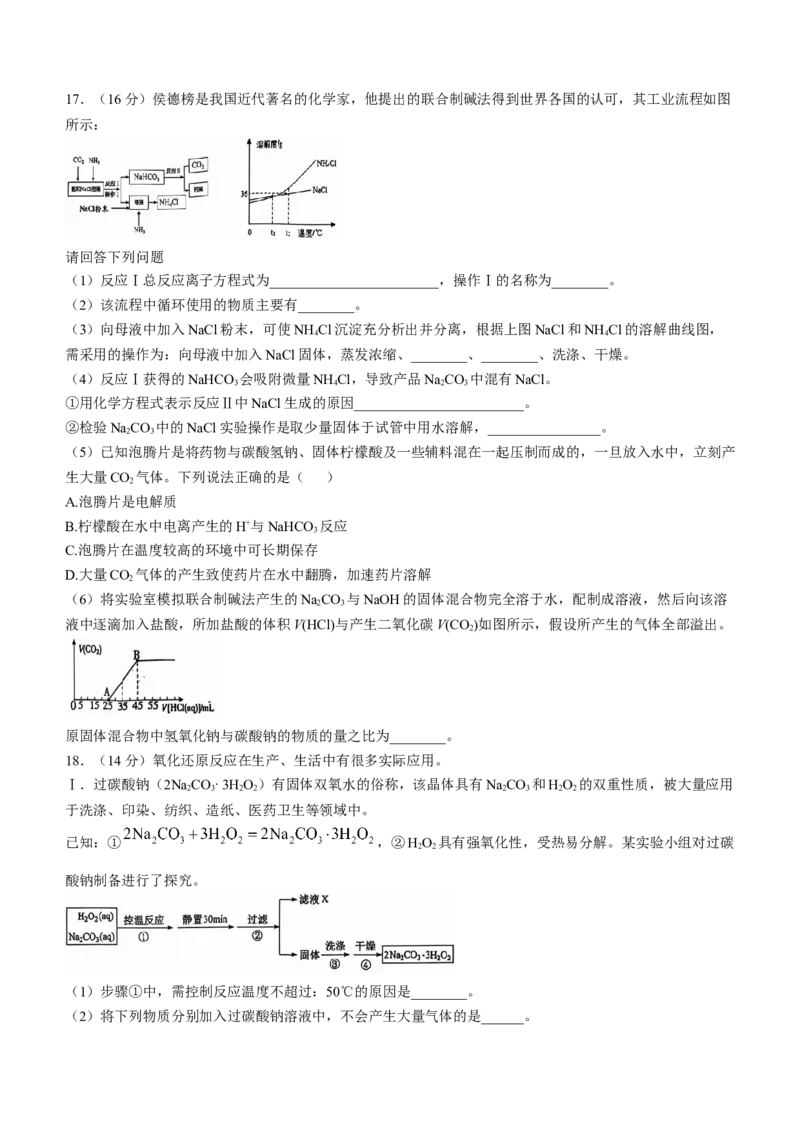
10.NaCl的导电情况如图所示。下列说法正确的是( )
A.NaCl溶液能导电,NaCl是电解质 B.NaCl在通电的情况下电离出可以自由移动的离子
C.NaCl固体不含有离子 D.溶液中的水合钠离子向电源的正极方向移动
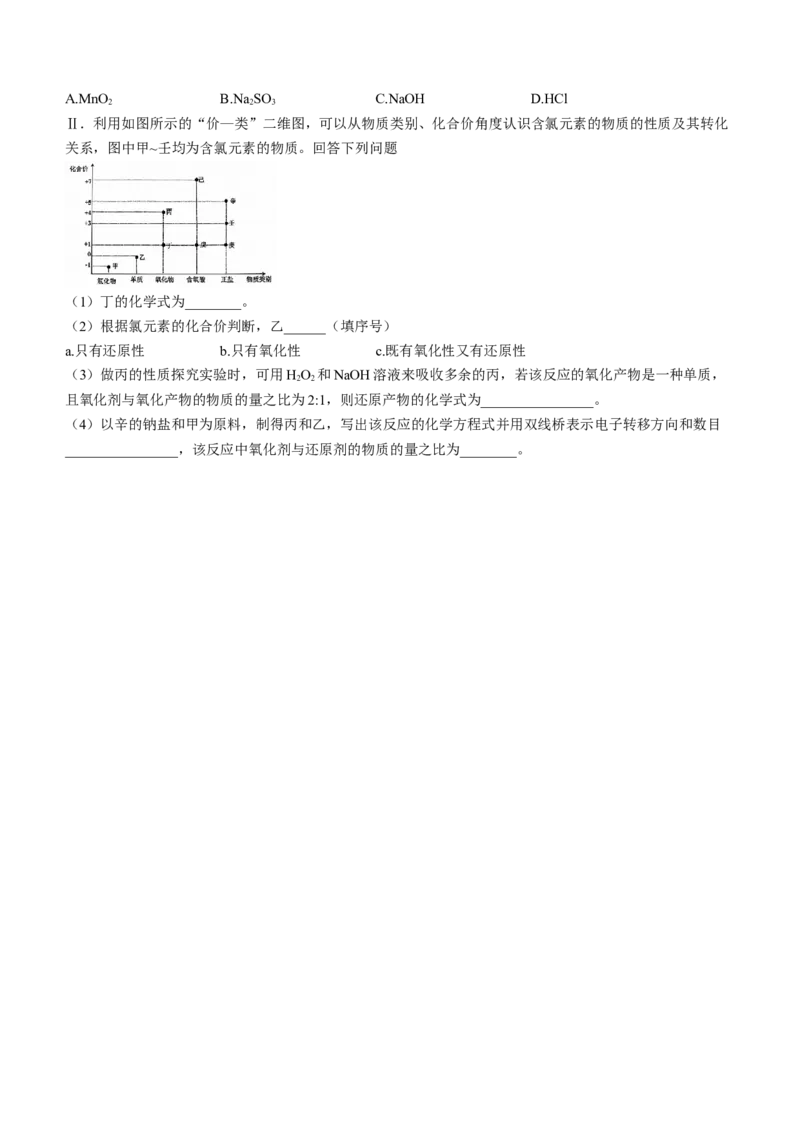
11.下列透明溶液中,能大量共存的离子组是( )
A.K+、 、 、H+ B. 、 、Na+、Cu2+
C. Na+、 、 、H+ D.Al3+、Ag+、 、
12.用下图所示装置进行实验(其中E收集生成的O),证明过氧化钠可在呼吸面具或潜水艇中做供氧剂。
2
下列说法正确的是( )A.C中的反应每转移0.4 mol电子,产生0.1 mol O
2
B.在B、C之间最好加装一个装有浓硫酸的洗气瓶
C.可用稀硫酸代替稀盐酸制备CO
2
D.D装置的作用是除去CO
2
13.配制450mL 1mol/L的NaCl溶液,部分实验操作示意图如下:
下列说法正确的是( )
A.实验中需用的仪器有天平、450mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为②①④③
C.用托盘天平称量NaCl固体的质量为29.25g
D.定容时,俯视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
14.研究人员提出利用含硫物质热化学循环实现太阳能的转化与储存,过程如图所示。设N 为阿伏伽德罗常
A
数的值,下列说法正确的是( )
A.反应Ⅰ中化合价发生改变的仅有硫元素
B.22.4L SO 所含的原子数为3 N
2 A
C.利用该含硫物质循环反应,可实现太阳能转化为电能
D.“SO 催化歧化”反应中,S是氧化产物
2
二、非选择题(本题共4小题,共58分)
15.(14分)阅读下列科普短文并填空。
海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,
如 、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用于
生产 、 、 、 、 、 等。苦卤 经过氯气氧化,热空气吹出,吸收等一系列操作可获得Br ,电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源, 是一种清
2
洁能源。
(1)上述标有序号的物质中,属于非电解质的是__________(填序号,下同)属于电解质的是__________。
(2)写出④和⑤反应的离子方程式________________________。
(3)海水提溴的过程中涉及的反应有 , ,
根据上述反应可判断 、 、SO 的还原性由强到弱的顺序为________。
2
(4)①标况下,11.2L SO 与______g CH 含有原子数相等。
2 4
②在相同温度和压强下,相同体积的氢气和甲烷的质量比为______,其中所含有的电子数目之比为______。
③用2.50 mol/L NaCl溶液配100mL 0.50mol/L NaCl溶液,需要用量筒量取______mL 2.50mol/L NaCl溶液
16.(14分)硫酰氯(SO Cl)常用于制造医药品、染料等,某实验小组拟用干燥的氯气和二氧化硫在活性
2 2
炭催化下制取硫酰氯,装置如图所示:
已知SO Cl 的沸点为69℃,遇水能发生强烈反应并产生白雾。
2 2
回答下列问题:
(1)实验开始时,加入药品前必须要进行的实验操作为________________________。
(2)装置②的作用是________________________________。
(3)写出装置①中发生反应的化学方程式________________________,该反应生成71g Cl 所消耗的还原剂
2
的质量为______g。写出SO Cl 遇水发生反应并产生白雾的化学方程式________________。
2 2
(4)下列说法错误的是( )
A.装置①中可用MnO 代替Ca(ClO)
2 2
B.装置①中可控制分液漏斗缓慢滴加来提高浓盐酸的利用率
C.尾气处理时需要在装置⑤后装盛有氢氧化钠溶液的洗气瓶
D.装置④需要热水浴,控制温度超过69℃,装置⑤需要冰水浴
(5)为了探究Cl 在NaCl溶液中溶解性的影响因素,某同学通过实验测得Cl 在不同浓度的NaCl溶液中溶
2 2
解达到饱和时的浓度及部分含氯微粒浓度如图所示:
由图像可以看出,Cl 溶于NaCl溶液时,主要发生了两个反应,一是氯气与水的反应,二是(填离子方程
2
式)______________________。随着氯化钠溶液浓度的增大,氯气与水反应受到了抑制,证据是(根据右图
作答)________________________。17.(16分)侯德榜是我国近代著名的化学家,他提出的联合制碱法得到世界各国的认可,其工业流程如图
所示:
请回答下列问题
(1)反应Ⅰ总反应离子方程式为________________________,操作Ⅰ的名称为________。
(2)该流程中循环使用的物质主要有________。
(3)向母液中加入NaCl粉末,可使NH Cl沉淀充分析出并分离,根据上图NaCl和NH Cl的溶解曲线图,
4 4
需采用的操作为:向母液中加入NaCl固体,蒸发浓缩、________、________、洗涤、干燥。
(4)反应Ⅰ获得的NaHCO 会吸附微量NH Cl,导致产品NaCO 中混有NaCl。
3 4 2 3
①用化学方程式表示反应Ⅱ中NaCl生成的原因________________________。
②检验NaCO 中的NaCl实验操作是取少量固体于试管中用水溶解,________________。
2 3
(5)已知泡腾片是将药物与碳酸氢钠、固体柠檬酸及一些辅料混在一起压制而成的,一旦放入水中,立刻产
生大量CO 气体。下列说法正确的是( )
2
A.泡腾片是电解质
B.柠檬酸在水中电离产生的H+与NaHCO 反应
3
C.泡腾片在温度较高的环境中可长期保存
D.大量CO 气体的产生致使药片在水中翻腾,加速药片溶解
2
(6)将实验室模拟联合制碱法产生的NaCO 与NaOH的固体混合物完全溶于水,配制成溶液,然后向该溶
2 3
液中逐滴加入盐酸,所加盐酸的体积V(HCl)与产生二氧化碳V(CO)如图所示,假设所产生的气体全部溢出。
2
原固体混合物中氢氧化钠与碳酸钠的物质的量之比为________。
18.(14分)氧化还原反应在生产、生活中有很多实际应用。
Ⅰ.过碳酸钠(2NaCO·3HO)有固体双氧水的俗称,该晶体具有NaCO 和HO 的双重性质,被大量应用
2 3 2 2 2 3 2 2
于洗涤、印染、纺织、造纸、医药卫生等领域中。
已知:① ,②HO 具有强氧化性,受热易分解。某实验小组对过碳
2 2
酸钠制备进行了探究。
(1)步骤①中,需控制反应温度不超过:50℃的原因是________。
(2)将下列物质分别加入过碳酸钠溶液中,不会产生大量气体的是______。A.MnO B.Na SO C.NaOH D.HCl
2 2 3
Ⅱ.利用如图所示的“价—类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化
关系,图中甲~壬均为含氯元素的物质。回答下列问题
(1)丁的化学式为________。
(2)根据氯元素的化合价判断,乙______(填序号)
a.只有还原性 b.只有氧化性 c.既有氧化性又有还原性
(3)做丙的性质探究实验时,可用HO 和NaOH溶液来吸收多余的丙,若该反应的氧化产物是一种单质,
2 2
且氧化剂与氧化产物的物质的量之比为2:1,则还原产物的化学式为________________。
(4)以辛的钠盐和甲为原料,制得丙和乙,写出该反应的化学方程式并用双线桥表示电子转移方向和数目
________________,该反应中氧化剂与还原剂的物质的量之比为________。