文档内容
3.2.2 物质的量在化学方程式计算中的应用 练习(解析版)
1.将足量铁粉放入100 mL 0.1 mol·L-1的CuSO 溶液中,充分反应后析出的铜的质量为( )
4
A.32 g B.6.4 g C.0.64 g D.3.2 g
【答案】C
【 解 析 】 n(CuSO )=0.100 L×0.1 mol·L-1=0.01 mol , 由 CuSO +Fe FeSO +Cu , 可 知
4 4 4
n(Cu)=n(CuSO )=0.01 mol,m(Cu)=0.01 mol×64 g·mol-1=0.64 g。
4
2.等物质的量的常见金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为 V 、
A
V 、V ,已知V =2V ,且V =V +V ,则在金属C的生成物中,该金属的化合价为( )
B C B C A B C
A.+1价 B.+2价 C.+3价 D.+4价
【答案】A
【解析】V =2V ,V =V +V =3V ,根据得失电子守恒,A失去的电子数为C的3倍,金属最外
B C A B C C
层电子数一般小于4,故A的化合价为C的3倍,C的化合价只能为+1价。
3.把一小块钠放入足量水中,会发生如下反应:2Na+2H O 2NaOH+H ↑。有关该反应的下列
2 2
说法正确的是( )
A.反应中Na与NaOH的质量相等
B.反应中HO和H 的质量相等
2 2
C.反应中HO和H 的质量之比为2∶1
2 2
D.反应中Na与NaOH的物质的量之比为1∶1
【答案】D
【解析】该反应中,Na与NaOH的物质的量之比为1∶1,质量之比为23∶40,所以A项错误,
D项正确;H O与H 的物质的量之比为2∶1,质量之比为18∶1,所以B项、C项均错误。
2 2
4.2 mol·L-1的盐酸和硫酸各100 mL,分别加入等质量的铁粉,反应后生成的气体质量之比为
2∶3,则向盐酸中加入的铁粉的物质的量为( )
A.0.05 mol B.0.075 mol C.0.15 mol D.0.2 mol
【答案】C
【解析】n(HCl)=0.2 mol,n(H SO )=0.2 mol。
2 4
若酸均不足,即完全反应生成H 的质量之比为1∶2;
2
若酸均过量,即金属不足,则生成H 的质量之比为1∶1。
2
现生成H 的质量之比为2∶3,则说明盐酸不足,硫酸过量;根据盐酸中HCl的物质的量可求出
2
生成H 0.1 mol,则HSO 反应生成0.15 mol H,则铁粉为0.15 mol。
2 2 4 2
5.将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积
比是( )A.1∶2∶3 B.6∶3∶2 C.3∶1∶1 D.1∶1∶1
【答案】C
【解析】根据金属与酸反应的实质2M+2nH+ 2Mn++nH↑可知三种金属都过量,而铝、镁都
2
不与HO反应,按盐酸计算,两者产生气体的物质的量都为0.05 mol,金属钠可继续与HO反应最
2 2
终产生0.15 mol H,即同温同压下产生气体的体积比为0.15 mol∶0.05 mol∶0.05 mol=3∶1∶1。
2
6.一块表面已被氧化为NaO的钠块10.8 g,将其投入100 g 水中,产生H 0.2 g,则被氧化
2 2
的钠的质量是( )
A.9.2 g B.10.6 g C.6.2 g D.4.6 g
【答案】D
【解析】由于钠块放入水中发生反应:2Na+2H O 2NaOH+H ↑,由产生H 的质量可求出Na
2 2 2
的质量,进而可求出钠块中NaO的质量,最后根据关系式:Na O~2Na才能求出被氧化的钠的质量。
2 2
7.将铁加入到100 mL某浓度的盐酸中恰好完全反应,反应后生成的气体为V L(标准状况下),
将铝加入到100 mL 2 mol·L-1 NaOH溶液中恰好完全反应,充分反应后生成的气体为3V L。下列说
法正确的是( )
A.铁和铝的物质的量相等
B.原盐酸的浓度为2 mol·L-1
C.铁加入盐酸中的离子方程式为2Fe+6H+ 2Fe3++3H ↑
2
D.盐酸与NaOH溶液中溶质的物质的量浓度之比为1∶3
【答案】B
【解析】Al与NaOH溶液的反应为
2Al + 2NaOH+2H O 2NaAlO +3H ↑
2 2 2
2 mol 2 mol 3 mol
n(Al) 0.1 L×2 mol·L-1 n(H )
2
2mol 3mol
列比例式 = 解得n(H )=0.3 mol
0.1 L×2mol·L-1 n(H ) 2
2
2mol 2mol
= ,解得n(Al)=0.2 mol
0.1 L×2mol·L-1 n(Al)
由Al与NaOH溶液反应生成的气体为3V L,
3V L
得 =0.3 mol 则V=2.24。
22.4mol·L-1
再根据反应Fe+2HCl FeCl +H ↑,可求出反应的Fe的物质的量为0.1 mol,HCl的物质的量
2 2
0.2mol
为0.2 mol,则c(HCl)= =2 mol·L-1,B正确;由上述数据分析知铁、铝物质的量不相等,A
0.1 L错误;Fe与盐酸反应生成Fe2+,C错误;盐酸与NaOH溶液中溶质的物质的量浓度之比为1∶1,D
错误。
8.已知m g Al在足量氯气中燃烧,生成固体的质量为(m+21.3) g,若将m g Al投入总质量为
95.2 g的NaOH水溶液中恰好完全反应,则所得溶液中溶质的质量分数为( )
A.5.4% B.8.0% C.16.3% D.16.4%
【答案】D
【解析】设生成 NaAlO 的质量为 x,生成氢气的质量为 y。由 2Al+3Cl 2AlCl 和
2 2 3
2Al+2NaOH+2H O 2NaAlO +3H ↑得关系式
2 2 2
2Al~2AlCl ~ 2NaAlO ~3H
3 2 2
54 267 164 6
mg (m+21.3)g x y
54 267 164 6
= = =
mg (m+21.3) g x y
解得:m=5.4,x=16.4g,y=0.6g
m(NaAlO ) 16.4g
w(NaAlO )= 2 ×100%= ×100%=16.4%。
2 m(溶液) (5.4+95.2-0.6) g
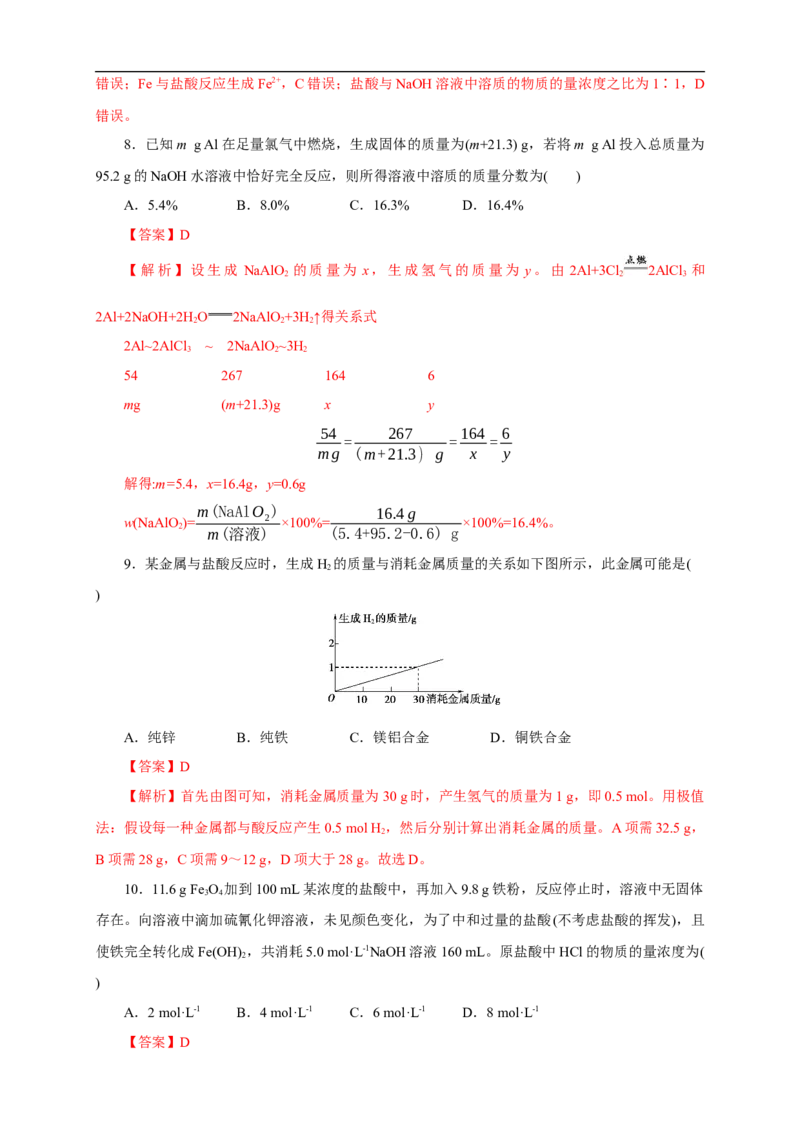
9.某金属与盐酸反应时,生成H 的质量与消耗金属质量的关系如下图所示,此金属可能是(
2
)
A.纯锌 B.纯铁 C.镁铝合金 D.铜铁合金
【答案】D
【解析】首先由图可知,消耗金属质量为30 g时,产生氢气的质量为1 g,即0.5 mol。用极值
法:假设每一种金属都与酸反应产生0.5 mol H,然后分别计算出消耗金属的质量。A项需32.5 g,
2
B项需28 g,C项需9~12 g,D项大于28 g。故选D。
10.11.6 g Fe O 加到100 mL某浓度的盐酸中,再加入9.8 g铁粉,反应停止时,溶液中无固体
3 4
存在。向溶液中滴加硫氰化钾溶液,未见颜色变化,为了中和过量的盐酸(不考虑盐酸的挥发),且
使铁完全转化成Fe(OH) ,共消耗5.0 mol·L-1NaOH溶液160 mL。原盐酸中HCl的物质的量浓度为(
2
)
A.2 mol·L-1 B.4 mol·L-1 C.6 mol·L-1 D.8 mol·L-1
【答案】D【解析】由题意可知,经过一系列反应后,最终得到的物质是Fe(OH) 和NaCl,根据元素守恒
2
160 mL
得:c(HCl)×V(HCl)=c(NaOH)×V(NaOH),c(HCl)=5.0 mol·L-1× =8 mol·L-1。
100 mL
11.将Fe和Al按一定的质量比组成合金。
(1)取一定量的该合金,向其中加入足量NaOH溶液,生成气体n L(标准状况),则反应的离子
方程式是 ,合金中Al的物质的量是 。
[来源:学。科。网Z。X。X。K]
(2)另取相同质量的该合金,向其中加入足量稀硫酸,固体全部溶解,生成气体 m L(标准状况),
则反应中转移电子的物质的量是 mol,合金中Fe的质量是 。
n m 56(m-n)
【答案】(1)2Al+2OH-+2H O 2AlO- +3H ↑ mol (2) g
2 2 2 33.6 11.2 22.4
【解析】合金中Al既能与NaOH反应,也能与稀硫酸反应,且等量Al与足量的NaOH溶液或
稀硫酸反应生成等量的H;而Fe只能与稀硫酸反应;由2Al+2OH-+2H O 2Al +3H ↑可知,合金
2 2 O- 2
2
2 nL n
中Al的物质的量为 × = mol;Fe、Al与稀硫酸反应生成m L H ,由2H+
3 22.4 L·mol-1 33.6 2
m (m-n)L
H 可知转移电子物质的量为 mol;由Fe置换出的H 体积为(m-n) L,故m(Fe)=
2 11.2 2 22.4 L·mol-1
56(m-n)
×56 g·mol-1即 g。
22.4
12.在标准状况下进行甲、乙、丙三组实验。三组实验各取 30 mL同浓度的盐酸,加入同一种
镁铝混合物粉末,产生气体,有关数据列表如下:
实验序号 甲 乙 丙
混合物质量/mg 255 385 459
生成气体/mL 280 336 336
(1)甲、乙两组实验中,哪一组盐酸是不足量的? (填“甲”或“乙”)。理由是
。
(2)要算出盐酸中HCl的物质的量浓度,题中可作计算依据的数据是 ,求得盐酸
中HCl的物质的量浓度为 。
(3)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是 ,
求得Mg、Al的物质的量之比为 。 [【答案】(1)乙 因甲、乙生成H 的体积不等,则产生H 体积小的,说明还有酸未反应,因
2 2
280
此甲中盐酸过量,混合物反应完全;若乙中盐酸过量,则可产生H: ×385 mL≈423 mL,而实际为
2
255
336 mL,说明乙中盐酸不足,合金过量 (2)336 mL 1 mol·L-1 (3)255 mg和280 mL 1∶1
【解析】(2)在乙或丙中,因盐酸反应完全,则可根据
2HCl ~ H
2
2 1
n(HCl)= 336×10-3L ×2=3×10-2 mol c(HCl)=3×10-2mol=1 mol·L-1
22.4 L·mol-1 0.03 L
(3)在甲中,混合物完全反应,盐酸有剩余,则可根据混合物质量255 mg,生成气体280 mL计
3
算。根据Mg~H,Al~ H 得:n(Mg)×24 g·mol-1+n(Al)×27 g·mol-1=255×10-3 g
2 2
2
n(Mg)+3n(Al)= 280×10-3L
2 22.4 L·mol-1
求得:n(Mg)=0.005 mol,n(Al)=0.005 mol,n(Mg)∶n(Al)=1∶1。