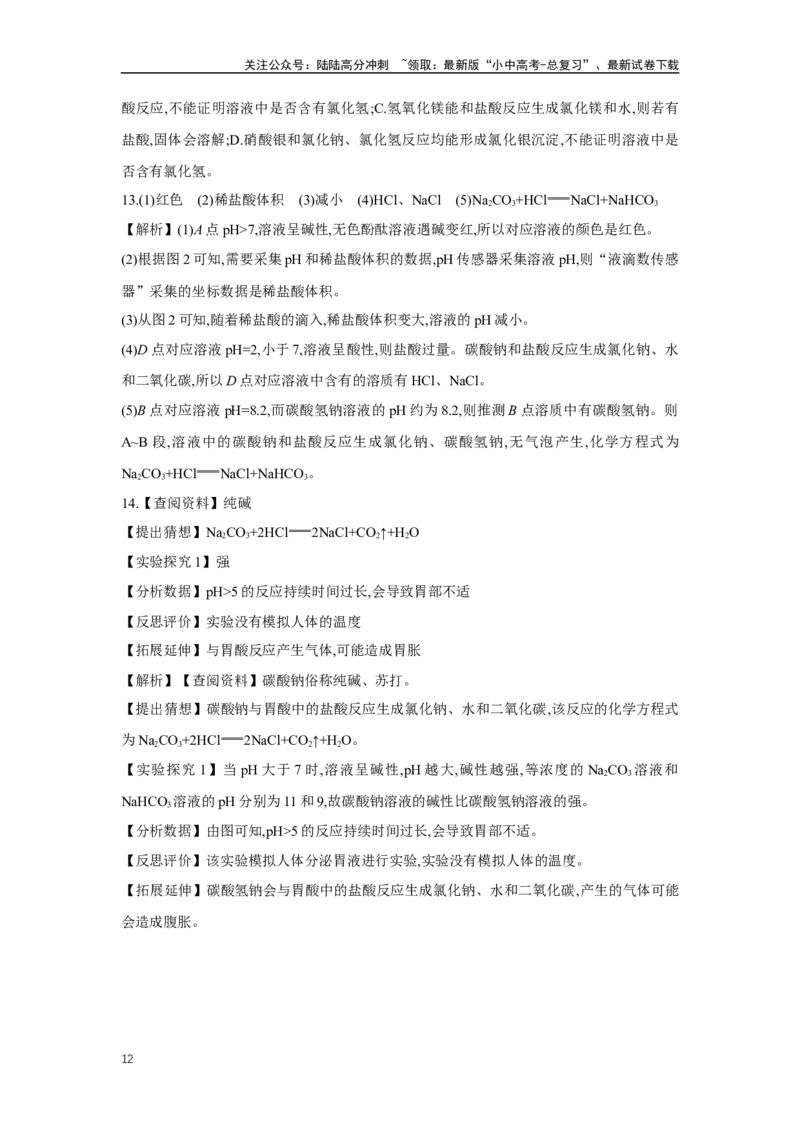文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.2.2 盐 化肥
【基础作业】
1.下列有关纯碱的认识错误的是( )
A.组成:由碳、氧和钠三种元素组成
B.性质:能与BaCl 、NaCl等盐溶液反应
2
C.用途:用于玻璃、造纸、纺织等生产工业
D.生产:侯氏制碱法
2.部分盐和酸的溶解性(20 ℃)如表所示。下列说法不正确的是 ( )
离子 Cl- SO2− CO2−
4 3
H+ 溶、挥 溶 溶
Ca2+ 溶 微 不
Mg2+ 溶 溶 微
A.盐酸是挥发性酸
B.MgSO 是可溶性盐
4
C.常温下的溶解度:CaCO >CaSO
3 4
D.常温下,MgSO 溶液与稀盐酸不发生反应
4
3.(改编)碳酸氢铵是一种重要的化工原料和食品添加剂,可用于饼干、糕点的制作。碳酸氢
铵在60 ℃以上会发生反应:NHHCO NH ↑+H O+CO↑,碳酸氢铵可溶于水。下列说法不
4 3 3 2 2
合理的是 ( )
A.碳酸氢铵要保存在阴凉干燥处
B.碳酸氢铵属于盐
C.使用碳酸氢铵可使糕点更加松软
D.烤制后的饼干中还有碳酸氢铵
4.(原创·生活情境)“舌尖上的安全”是各级政府义不容辞之责,下列做法中不会危及人体健康
的是 ( )
A.食品腌制时大量使用亚硝酸盐
B.用碳酸钡代替硫酸钡做钡餐
C.烘焙蛋糕时添加少量小苏打
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.用硫酸铜溶液作自来水生产过程中的净水剂
5.施肥是使农业增产的重要手段。下列关于化肥的说法不正确的是 ( )
A.尿素[CO(NH)]属于氮肥
2 2
B.植物的叶片发黄,应施用磷肥来改善其生长状况
C.铵态氮肥不能与碱性物质混用
D.硝酸钾属于复合肥
6.我国化学家侯德榜发明了“侯氏制碱法”,为纯碱和氮肥工业技术的发展作出了杰出贡献。
生产过程涉及的主要化学反应如下:
①NH +CO +H O+NaCl NH Cl+NaHCO ↓
3 2 2 4 3
②2NaHCO NaCO+H O+CO↑
3 2 3 2 2
实验室称取含有氯化钠的纯碱样品12.5 g,加入95 g一定溶质质量分数的稀盐酸,恰好完全反
应,得到氯化钠溶液103.1 g。下列分析不正确的是 ( )
A.若反应①中得到53.5 g氯化铵,它与30 g尿素[CO(NH)]所含的氮元素的质量相等
2 2
B.若NaCO 粉末中混有少量的NaHCO ,可用加热的方法除杂
2 3 3
C.所得氯化钠溶液中溶质的质量分数为11.3%
D.纯碱样品中碳酸钠的质量分数为84.8%
7.(改编)化学在粮食生产中发挥着重要作用。
(1)清澈透明的湖水可以灌溉农田,想知道湖水是硬水还是软水,可向湖水的水样中加入
进行检验。
(2)粮食安全是“国之大者”,小麦是我国重要的粮食作物。合理施肥是小麦增产的最有力措
施,下列肥料中属于复合肥的是 (填字母)。
A.CO(NH )
2 2
B.KNO
3
C.Ca (PO )
3 4 2
D.(NH )HPO
4 2 4
(3)我国的盐碱地面积大,盐碱地是主要受氯化钠和碳酸钠等影响的土壤。某同学欲选用合适
的试剂来逐一检验出土壤中含NaCl、NaCO 两种钠盐,他加入下列两种试剂的先后顺序是
2 3
(填字母)。
A.硝酸银溶液 B.稀硝酸
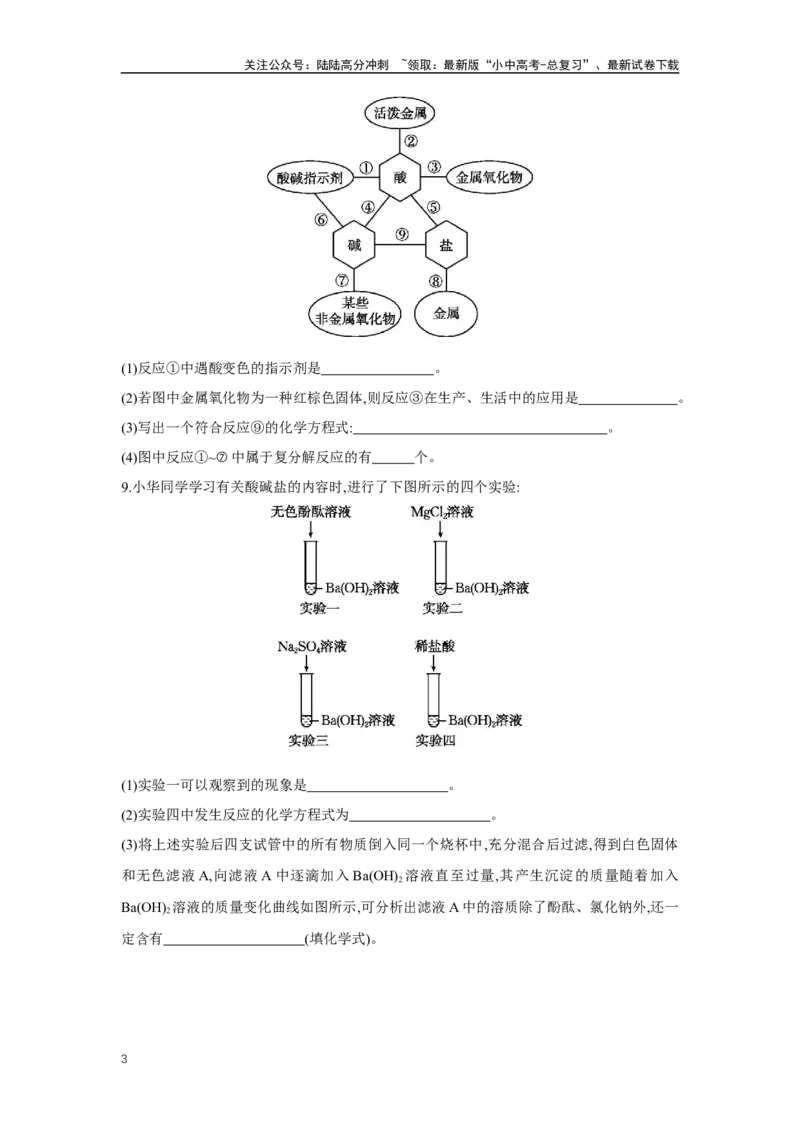
8.(改编)我国航天员使用的“飞天”舱外服是目前世界上最先进的航天服之一。学习小组同
学模仿航天服的外形,建立了下图所示常见物质类别之间化学反应的思维导图。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)反应①中遇酸变色的指示剂是 。
(2)若图中金属氧化物为一种红棕色固体,则反应③在生产、生活中的应用是 。
(3)写出一个符合反应⑨的化学方程式: 。
(4)图中反应①~⑦中属于复分解反应的有 个。
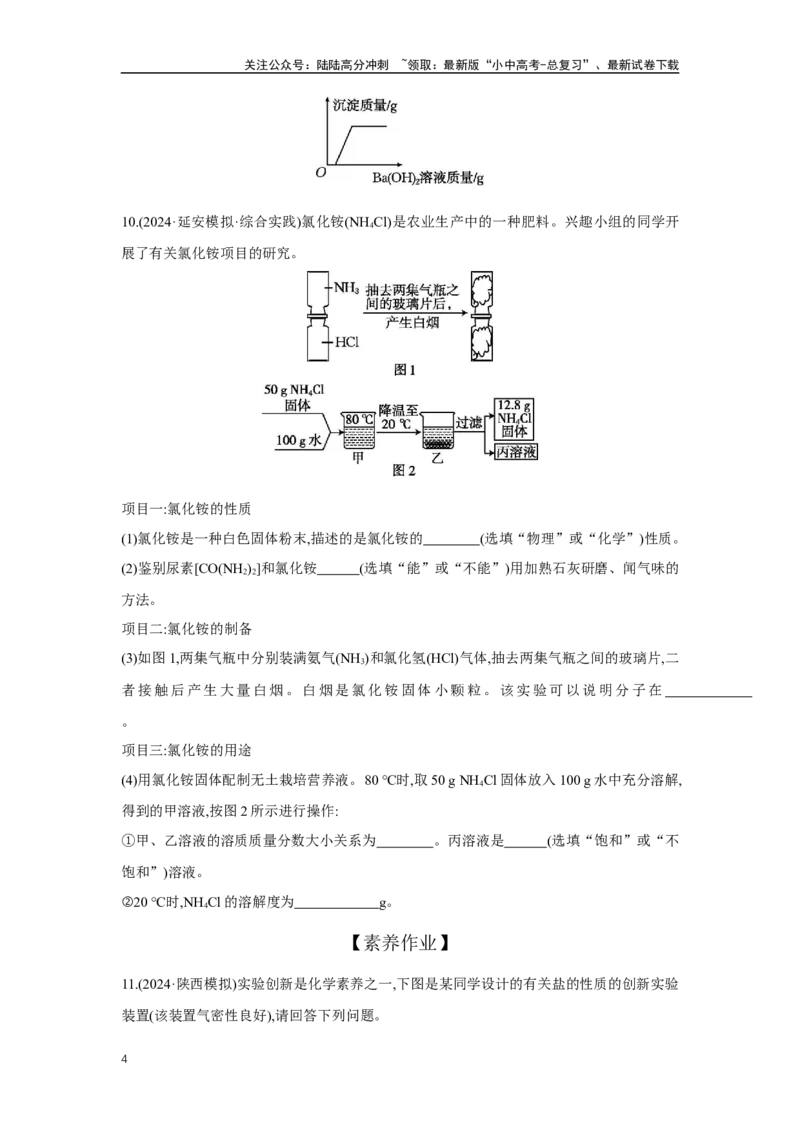
9.小华同学学习有关酸碱盐的内容时,进行了下图所示的四个实验:
(1)实验一可以观察到的现象是 。
(2)实验四中发生反应的化学方程式为 。
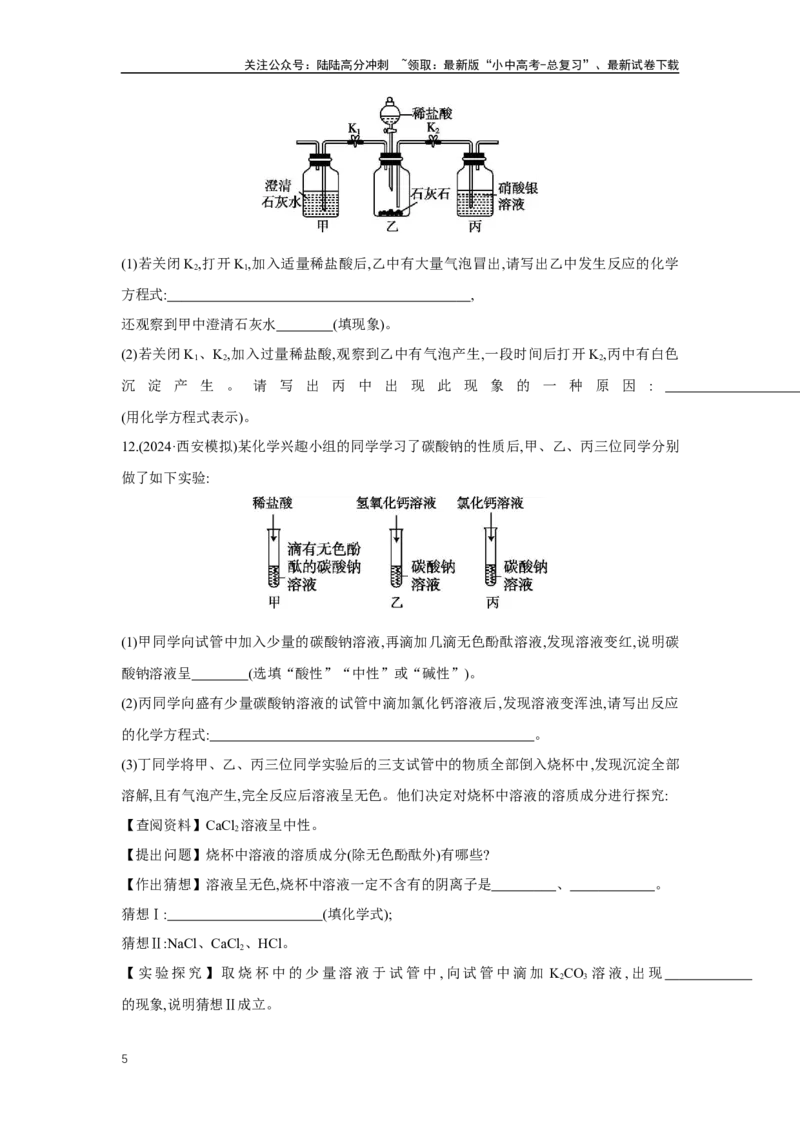
(3)将上述实验后四支试管中的所有物质倒入同一个烧杯中,充分混合后过滤,得到白色固体
和无色滤液A,向滤液A中逐滴加入Ba(OH) 溶液直至过量,其产生沉淀的质量随着加入
2
Ba(OH) 溶液的质量变化曲线如图所示,可分析出滤液A中的溶质除了酚酞、氯化钠外,还一
2
定含有 (填化学式)。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
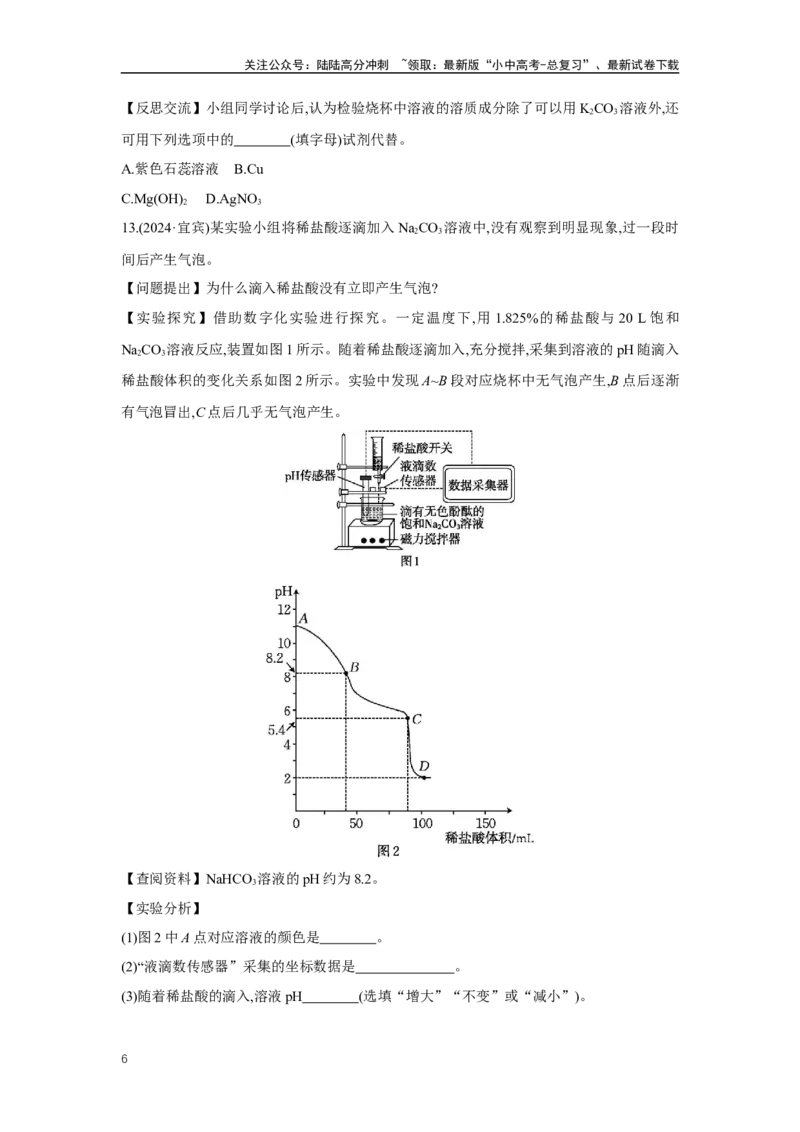
10.(2024·延安模拟·综合实践)氯化铵(NH Cl)是农业生产中的一种肥料。兴趣小组的同学开
4
展了有关氯化铵项目的研究。
项目一:氯化铵的性质
(1)氯化铵是一种白色固体粉末,描述的是氯化铵的 (选填“物理”或“化学”)性质。
(2)鉴别尿素[CO(NH)]和氯化铵 (选填“能”或“不能”)用加熟石灰研磨、闻气味的
2 2
方法。
项目二:氯化铵的制备
(3)如图1,两集气瓶中分别装满氨气(NH )和氯化氢(HCl)气体,抽去两集气瓶之间的玻璃片,二
3
者接触后产生大量白烟。白烟是氯化铵固体小颗粒。该实验可以说明分子在
。
项目三:氯化铵的用途
(4)用氯化铵固体配制无土栽培营养液。80 ℃时,取50 g NH Cl固体放入100 g水中充分溶解,
4
得到的甲溶液,按图2所示进行操作:
①甲、乙溶液的溶质质量分数大小关系为 。丙溶液是 (选填“饱和”或“不
饱和”)溶液。
②20 ℃时,NHCl的溶解度为 g。
4
【素养作业】
11.(2024·陕西模拟)实验创新是化学素养之一,下图是某同学设计的有关盐的性质的创新实验
装置(该装置气密性良好),请回答下列问题。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)若关闭K,打开K,加入适量稀盐酸后,乙中有大量气泡冒出,请写出乙中发生反应的化学
2 1
方程式: ,
还观察到甲中澄清石灰水 (填现象)。
(2)若关闭K 、K,加入过量稀盐酸,观察到乙中有气泡产生,一段时间后打开K,丙中有白色
1 2 2
沉 淀 产 生 。 请 写 出 丙 中 出 现 此 现 象 的 一 种 原 因 :
(用化学方程式表示)。
12.(2024·西安模拟)某化学兴趣小组的同学学习了碳酸钠的性质后,甲、乙、丙三位同学分别
做了如下实验:
(1)甲同学向试管中加入少量的碳酸钠溶液,再滴加几滴无色酚酞溶液,发现溶液变红,说明碳
酸钠溶液呈 (选填“酸性”“中性”或“碱性”)。
(2)丙同学向盛有少量碳酸钠溶液的试管中滴加氯化钙溶液后,发现溶液变浑浊,请写出反应
的化学方程式: 。
(3)丁同学将甲、乙、丙三位同学实验后的三支试管中的物质全部倒入烧杯中,发现沉淀全部
溶解,且有气泡产生,完全反应后溶液呈无色。他们决定对烧杯中溶液的溶质成分进行探究:
【查阅资料】CaCl 溶液呈中性。
2
【提出问题】烧杯中溶液的溶质成分(除无色酚酞外)有哪些?
【作出猜想】溶液呈无色,烧杯中溶液一定不含有的阴离子是 、 。
猜想Ⅰ: (填化学式);
猜想Ⅱ:NaCl、CaCl 、HCl。
2
【实验探究】取烧杯中的少量溶液于试管中,向试管中滴加 KCO 溶液,出现
2 3
的现象,说明猜想Ⅱ成立。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【反思交流】小组同学讨论后,认为检验烧杯中溶液的溶质成分除了可以用KCO 溶液外,还
2 3
可用下列选项中的 (填字母)试剂代替。
A.紫色石蕊溶液 B.Cu
C.Mg(OH) D.AgNO
2 3
13.(2024·宜宾)某实验小组将稀盐酸逐滴加入NaCO 溶液中,没有观察到明显现象,过一段时
2 3
间后产生气泡。
【问题提出】为什么滴入稀盐酸没有立即产生气泡?
【实验探究】借助数字化实验进行探究。一定温度下,用1.825%的稀盐酸与20 L饱和
NaCO 溶液反应,装置如图1所示。随着稀盐酸逐滴加入,充分搅拌,采集到溶液的pH随滴入
2 3
稀盐酸体积的变化关系如图2所示。实验中发现A~B段对应烧杯中无气泡产生,B点后逐渐
有气泡冒出,C点后几乎无气泡产生。
【查阅资料】NaHCO 溶液的pH约为8.2。
3
【实验分析】
(1)图2中A点对应溶液的颜色是 。
(2)“液滴数传感器”采集的坐标数据是 。
(3)随着稀盐酸的滴入,溶液pH (选填“增大”“不变”或“减小”)。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)图2中D点对应溶液中含有的溶质有 (填化学式)。
【实验结论】
(5)稀盐酸滴入NaCO 溶液,反应分两段进行。
2 3
A~B段:发生反应的化学方程式是 。
B~C段:A~B段的生成物继续与稀盐酸反应转化为CO 逸出。
2
14.(2024·湖北)NaHCO 是治疗胃酸过多症的一种抗酸药。某学习小组在室温下,对NaCO
3 2 3
是否适合作为抗酸药进行了如下探究。
【查阅资料】
①NaHCO 俗称小苏打,Na CO 俗称 。
3 2 3
②人体胃液(含有盐酸)通常约为100 mL,pH约为1.5。人体温度约为37 ℃。
③抗酸药的标准之一:药物发生疗效时,胃液的pH保持在3~5之间最好,pH过高会导致胃痛
等不适症状。
【提出猜想】
猜想甲:Na CO 适合作为抗酸药。其理由是 (用化学
2 3
方程式表示)。
猜想乙:Na CO 不适合作为抗酸药。其原因可能是碱性较强。
2 3
【实验探究1】探究NaCO 与NaHCO 碱性的强弱
2 3 3
依次测量等浓度的NaCO 溶液和NaHCO 溶液的pH,结果分别为11和9。NaCO 溶液的碱
2 3 3 2 3
性比NaHCO 溶液的 (选填“强”或“弱”)。
3
【实验探究2】探究NaCO 作为抗酸药的适应性
2 3
先向500 mL烧杯中加入100 mL pH=1.5的盐酸,用自动注射器向烧杯中以1 mL/min的速率
滴入pH=1.5的盐酸(模拟人体分泌胃液),再加入1.0 g Na CO 固体,并持续搅拌。用pH传感
2 3
器记录溶液pH随时间的变化曲线。
将上述实验中NaCO 换成NaHCO ,重复实验过程,所得两条曲线如图所示。
2 3 3
【分析数据】由图可知,与NaHCO 相比:①Na CO 反应时造成胃液pH远大于5;②Na CO
3 2 3 2 3
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。
【得出结论】NaCO 不适合作为抗酸药,猜想乙正确。
2 3
【反思评价】有小组成员提出,从控制变量和对比实验的角度看,“实验探究2”设计不够严谨,
你认为不严谨之处是 。
【拓展延伸】Al(OH) 也是一种常用的抗酸药。相比 Al(OH) ,从与胃酸反应的产物分
3 3
析,NaHCO 抗酸药存在的不足是 。
3
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答案
1.B 2.C 3.D
4.C 【解析】A.亚硝酸盐有毒,食品腌制时不能使用亚硝酸盐,会危及人体健康,错误;B.不能
用碳酸钡代替硫酸钡做钡餐,碳酸钡能与胃液中的盐酸反应生成氯化钡、水和二氧化碳,氯化
钡有毒,会危害人体健康,错误;C.碳酸氢钠受热能生成二氧化碳,是发酵粉的主要成分,常用于
焙制糕点,不会危及人体健康,正确;D.硫酸铜属于重金属盐,有毒,硫酸铜溶液不能作自来水生
产过程中的净水剂,错误。
5.B
14
6.C 【解析】A.53.5 g氯化铵中氮元素的质量为53.5 g× ×100%=14 g,30
14+1×4+35.5
2×14
g尿素中氮元素的质量为30 g× ×100%=14 g,正确;B.Na CO 粉末受热
12+16+(14+2)×2 2 3
不分解,而NaHCO 受热分解成碳酸钠、二氧化碳和水,没有引入新的杂质,可用加热的方法
3
除去NaCO 粉末中混有的少量NaHCO ,正确;C.根据质量守恒定律可知,生成二氧化碳的质
2 3 3
量为12.5 g+95 g-103.1 g=4.4 g,
设碳酸钠的质量为x,生成氯化钠的质量为y,
NaCO+2HCl 2NaCl+CO ↑+H O
2 3 2 2
106 117 44
x y 4.4 g
106 x
=
44 4.4g
x=10.6 g
117 y
=
44 4.4g
y=11.7 g
则氯化钠的质量为 12.5 g-10.6 g+11.7 g=13.6 g,所得氯化钠溶液中溶质的质量分数为
13.6g 10.6g
×100%≈13.2%,错误;D.纯碱样品中碳酸钠的质量分数为 ×100%=84.8%,正确。
103.1g 12.5g
7.(1)肥皂水 (2)BD (3)BA
【解析】(1)常用肥皂水来区分硬水和软水,泡沫多、浮渣少的是软水,泡沫少、浮渣多的是
硬水。
(2)KNO 中同时含有氮元素和钾元素,属于复合肥,(NH)HPO 中同时含有氮元素和磷元素,属
3 4 2 4
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
于复合肥。
(3)碳酸钠与酸反应产生气体,加入足量的稀硝酸,有气泡产生,说明含有碳酸钠,再加入硝酸银,
产生沉淀(氯化银沉淀),说明含有氯化钠。
8.(1)紫色石蕊溶液 (2)用酸除铁锈 (3)Ca(OH) +Na CO CaCO ↓+2NaOH(合理即可)
2 2 3 3
(4)3
【解析】(1)紫色石蕊溶液遇酸性溶液变红,无色酚酞溶液遇酸性溶液不变色,则反应①中遇
酸变色的指示剂是紫色石蕊溶液。
(2)若图中金属氧化物为一种红棕色固体,则红棕色固体是氧化铁,与稀盐酸反应生成氯化铁
和水,反应③在生产、生活中的应用是用酸除铁锈。
(3)反应⑨是碱和盐的反应,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学
方程式为Ca(OH) +Na CO CaCO ↓+2NaOH。
2 2 3 3
(4)反应①~⑦中属于复分解反应的有③④⑤三个,②属于置换反应,⑦不是两种化合物相互交
换成分生成两种新的化合物的反应,不属于复分解反应。
9.(1)无色酚酞溶液变红 (2)2HCl+Ba(OH) BaCl +2H O (3)HCl、MgCl
2 2 2 2
【解析】(1)酚酞遇碱变红色,所以实验一中能够观察到的现象是溶液变红色。
(2)氢氧化钡和盐酸反应生成氯化钡和水,化学方程式为Ba(OH) +2HCl BaCl +2H O。
2 2 2
(3)实验二氯化镁与氢氧化钡反应生成氢氧化镁和氯化钡,实验三硫酸钠与氢氧化钡反应生成
硫酸钡和氢氧化钠,实验四盐酸与氢氧化钡反应生成氯化钡和水,将上述试管内溶液混合后,
得到白色固体和无色滤液A,向滤液A中逐滴加入Ba(OH) 溶液直至过量,在加入一定量的氢
2
氧化钡后才出现沉淀,说明混合后,盐酸过量,不含有硫酸钠。盐酸与氢氧化钠反应生成氯化
钠和水,盐酸与氢氧化钡反应生成氯化钡和水,盐酸与氢氧化镁反应生成氯化镁和水,而氯化
钡与硫酸钠反应可以生成硫酸钡和氯化钠,可分析出滤液A中的溶质除了酚酞、氯化钠外,
还一定含有HCl、MgCl 。
2
10.(1)物理 (2)能 (3)不断地运动 (4)甲>乙 饱和 37.2
【解析】(1)氯化铵是一种白色固体粉末,不需要通过化学变化表现出来,属于氯化铵的物理
性质。
(2)尿素不能和氢氧化钙反应,氯化铵和氢氧化钙反应生成氯化钙、水和氨气,产生刺激性气
味,鉴别尿素[CO(NH)]和氯化铵能用加熟石灰研磨、闻气味的方法。
2 2
(3)如图1所示,两集气瓶中分别装满氨气(NH )和氯化氢(HCl)气体,抽去两集气瓶之间的玻璃
3
片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。该实验可以说明分子在不断地运
动。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
50g 50g−12.8g
(4)①甲、乙溶液的溶质质量分数分别是 ×100%≈33.3%、
100g+50g 50g−12.8g+100g
×100%≈27.1%,溶质质量分数大小关系为甲>乙。丙溶液是饱和溶液。②20 ℃时,100 g水中
溶解37.2 g氯化铵恰好饱和,该温度下NH Cl的溶解度为37.2 g。
4
11.(1)CaCO +2HCl CaCl +H O+CO↑ 变 浑 浊 (2)CaCl +2AgNO
3 2 2 2 2 3
Ca(NO )+2AgCl↓(或HCl+AgNO HNO+AgCl↓)
3 2 3 3
【解析】(1)石灰石的主要成分是碳酸钙,关闭K,打开K,加入稀盐酸后,乙中盐酸和碳酸钙
2 1
反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO +2HCl CaCl +H O+CO↑;二
3 2 2 2
氧化碳气体沿着导管进入甲中,与氢氧化钙反应生成碳酸钙沉淀和水,则可观察到甲中澄清石
灰水变浑浊。
(2)关闭K 、K,加入稀盐酸,观察到乙中有气泡产生,盐酸与石灰石的主要成分碳酸钙反应生
1 2
成氯化钙、二氧化碳和水,一段时间后乙中二氧化碳气体增多,气压增大,打开K,乙中液体沿
2
着导管进入丙中,乙中液体中含有氯化钙和稀盐酸,其进入丙中与硝酸银反应,反应的化学方
程式为CaCl +2AgNO Ca(NO )+2AgCl↓、HCl+AgNO HNO+AgCl↓。
2 3 3 2 3 3
12.(1)碱性 (2)CaCl +Na CO CaCO ↓+2NaCl (3)OH- C NaCl、CaCl 有气泡产
2 2 3 3 O2− 2
3
生 AC
【解析】(1)无色酚酞溶液遇碱性溶液变红,碳酸钠溶液能使无色酚酞溶液变红,说明碳酸钠
溶液呈碱性。
(2)碳酸钠和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为CaCl +Na CO
2 2 3
CaCO ↓+2NaCl。
3
【作出猜想】乙试管中,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,而氢氧化钠溶液
和碳酸钠溶液均能使无色酚酞溶液变红,但最终溶液显无色,则说明溶液中不含碳酸钠和氢氧
化钠,则溶液中一定不含的阴离子为OH-、C ;盐酸和氢氧化钠反应生成氯化钠和水,盐酸
O2−
3
和碳酸钙反应生成氯化钙、水和二氧化碳,沉淀全部溶解,且有气泡产生,则说明溶液中一定
含有氯化钠和氯化钙,可能含有氯化氢,猜想Ⅱ为NaCl、CaCl 、HCl,则猜想Ⅰ为NaCl、
2
CaCl 。
2
【实验探究】猜想Ⅱ成立,即溶液中含有盐酸,碳酸钾和盐酸反应生成氯化钠、水和二氧化碳,
则观察到有气泡产生。
【反思交流】A.盐酸能使紫色石蕊溶液变红色,能证明溶液中是否含有氯化氢;B.铜不能和盐
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
酸反应,不能证明溶液中是否含有氯化氢;C.氢氧化镁能和盐酸反应生成氯化镁和水,则若有
盐酸,固体会溶解;D.硝酸银和氯化钠、氯化氢反应均能形成氯化银沉淀,不能证明溶液中是
否含有氯化氢。
13.(1)红色 (2)稀盐酸体积 (3)减小 (4)HCl、NaCl (5)Na CO+HCl NaCl+NaHCO
2 3 3
【解析】(1)A点pH>7,溶液呈碱性,无色酚酞溶液遇碱变红,所以对应溶液的颜色是红色。
(2)根据图2可知,需要采集pH和稀盐酸体积的数据,pH传感器采集溶液pH,则“液滴数传感
器”采集的坐标数据是稀盐酸体积。
(3)从图2可知,随着稀盐酸的滴入,稀盐酸体积变大,溶液的pH减小。
(4)D点对应溶液pH=2,小于7,溶液呈酸性,则盐酸过量。碳酸钠和盐酸反应生成氯化钠、水
和二氧化碳,所以D点对应溶液中含有的溶质有HCl、NaCl。
(5)B点对应溶液pH=8.2,而碳酸氢钠溶液的pH约为8.2,则推测B点溶质中有碳酸氢钠。则
A~B段,溶液中的碳酸钠和盐酸反应生成氯化钠、碳酸氢钠,无气泡产生,化学方程式为
NaCO+HCl NaCl+NaHCO 。
2 3 3
14.【查阅资料】纯碱
【提出猜想】NaCO+2HCl 2NaCl+CO ↑+H O
2 3 2 2
【实验探究1】强
【分析数据】pH>5的反应持续时间过长,会导致胃部不适
【反思评价】实验没有模拟人体的温度
【拓展延伸】与胃酸反应产生气体,可能造成胃胀
【解析】【查阅资料】碳酸钠俗称纯碱、苏打。
【提出猜想】碳酸钠与胃酸中的盐酸反应生成氯化钠、水和二氧化碳,该反应的化学方程式
为NaCO+2HCl 2NaCl+CO ↑+H O。
2 3 2 2
【实验探究 1】当pH大于7时,溶液呈碱性,pH越大,碱性越强,等浓度的NaCO 溶液和
2 3
NaHCO 溶液的pH分别为11和9,故碳酸钠溶液的碱性比碳酸氢钠溶液的强。
3
【分析数据】由图可知,pH>5的反应持续时间过长,会导致胃部不适。
【反思评价】该实验模拟人体分泌胃液进行实验,实验没有模拟人体的温度。
【拓展延伸】碳酸氢钠会与胃酸中的盐酸反应生成氯化钠、水和二氧化碳,产生的气体可能
会造成腹胀。
12