文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题一 物质的化学变化
专题 02 燃料的燃烧
01考情透视·目标导航
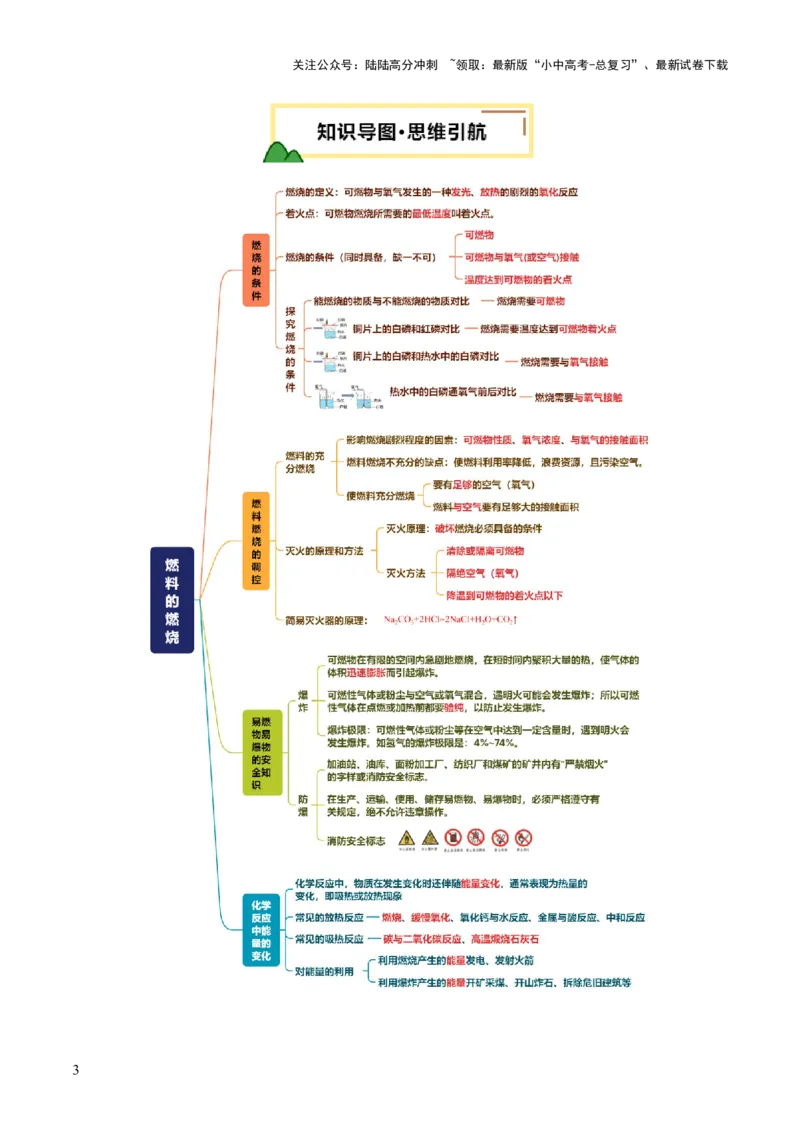
02知识导图·思维引航
03考点突破·考法探究
考点一 燃烧的条件
考点二 燃料燃烧的调控
考点三 易燃物易爆物的安全知识
考点四 化学反应中的能量变化
实验•燃烧条件的探究
04题型精研·考向洞悉
题型一 燃烧的条件
►考向01 燃烧的定义
►考向02 燃烧的条件
►考向03 实验探究燃烧的条件
►考向04 控制变量法在实验中的应用
题型二 燃料燃烧的调控
►考向01 燃料充分燃烧的方法及重要性
►考向02 灭火的原理与方法
►考向03 火灾的预防与自救
►考向04 常用的灭火器相关知识
题型三 易燃物易爆物的安全知识
►考向01 易燃易爆物的使用和储存
►考向02 消防安全标志
题型四 化学反应中的能量变化
►考向01 常见的吸热放热反应
►考向02 化学变化中能量变化的应用
实验 燃烧条件的探究
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点要求 课标要求 命题预测
常见的考向有:燃烧的条件、燃烧条
件的探究、灭火的原理、燃料的充分燃
通过实验探究燃烧的条
烧、易燃物易爆物的安全知识等。燃烧的
件,理解燃烧的原理及其在生活
燃烧的条件 条件考查一般以选择、填空或实验探究的
中的应用;能运用变量控制思想
形式进行,可直接考查,也常结合生活生
设计燃烧条件的实验探究方案。
产实际中常出现的各种形式的燃烧情境,
如火炬、酒精灯、燃气灶、柴火灶燃烧
理解灭火的原理及其在
等;燃料燃烧的调控考查一般从灭火的原
生活中的应用。初步体会调控化
理、燃料的充分燃烧、易燃物易爆物的安
燃料燃烧的调控 学反应的重要意义,结合实例认
全知识三个方面进行。灭火的原理可单独
识合理利用、调控化学反应的重
在选择题中考查,也可结合其他知识点在
要性。
填空题中考查;燃料的充分燃烧和易燃易
爆物的安全知识一般是穿插在填空题中考
了解各种燃烧和爆炸现
查。考查形式可结合各种燃烧和爆炸现象
易燃物易爆物的 象,了解易燃易爆物的生产、运
及灭火方法,家庭用电、用气及不同材料
安全知识 输、使用和储存中的防燃防爆措
燃烧引起的火灾与施救,面粉厂、煤粉
施。
厂、加油站、矿井等的防燃防爆措施等。
化学反应中的能量变化一般是穿插在选择
题、填空题等题型中考查。
化学反应中的能 认识物质变化过程中伴
量变化 随着能量的变化
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 燃烧的条件
一、燃烧的定义
1.燃烧:通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
2.注意:发光放热的反应不一定是燃烧,如灯泡发光
3.着火点:可燃物燃烧所需要的最低温度叫着火点。着火点是物质的性质,一般不改变。
【特别提醒】燃烧不一定需要氧气,如:
① H 在 C l 中的燃烧生成氯化氢,化学方程式: H + Cl 点燃 2HCl
2 2 2 2
②Na 在 Cl 中的燃烧生成氯化氢,化学方程式: 2Na + C l 点燃 2NaCl
2 2
③ Mg 在 CO 中的燃烧生成氧化镁和碳,化学方程式: 2Mg + CO 点燃 2MgO + C
2 2
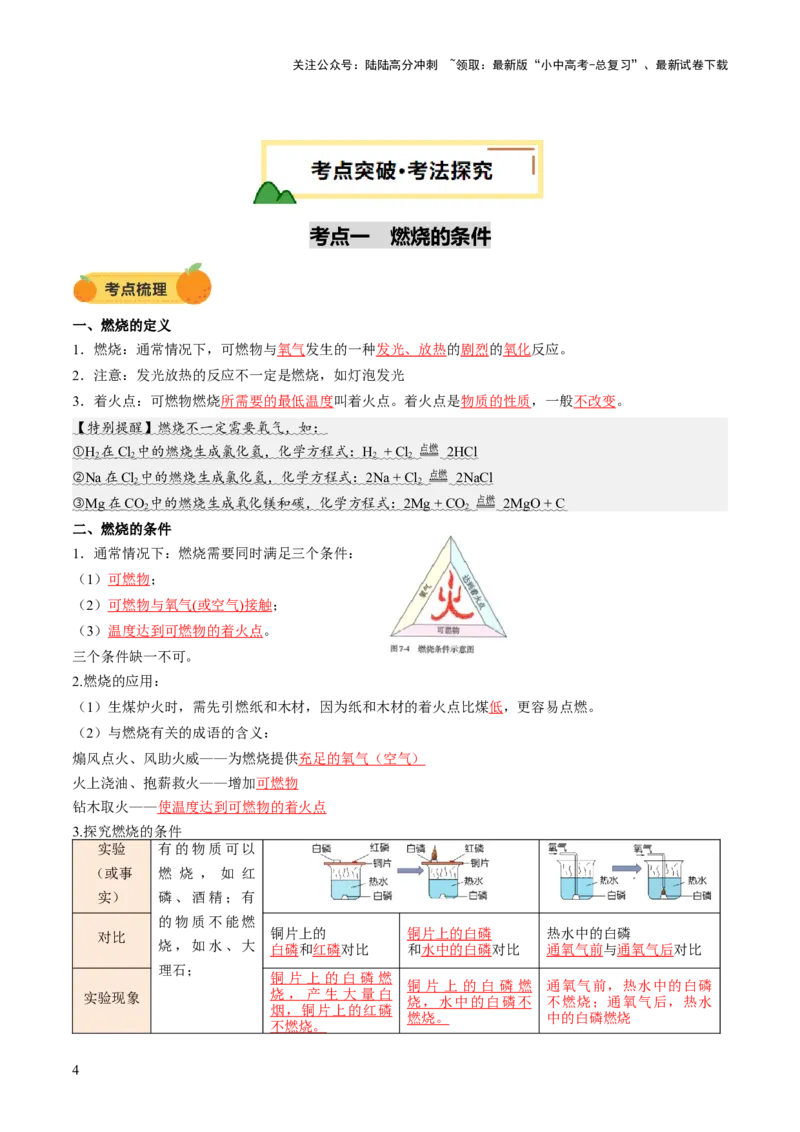
二、燃烧的条件
1.通常情况下:燃烧需要同时满足三个条件:
(1)可燃物;
(2) 可燃物与氧气 ( 或空气 ) 接触 ;
(3)温度达到可燃物的着火点。
三个条件缺一不可。
2.燃烧的应用:
(1)生煤炉火时,需先引燃纸和木材,因为纸和木材的着火点比煤低,更容易点燃。
(2)与燃烧有关的成语的含义:
煽风点火、风助火威——为燃烧提供充足的氧气(空气)
火上浇油、抱薪救火——增加可燃物
钻木取火——使温度达到可燃物的着火点
3.探究燃烧的条件
实验 有的物质可以
(或事 燃 烧 , 如 红
实) 磷、酒精;有
的物质不能燃
对比 铜片上的 铜片上的白磷 热水中的白磷
烧,如水、大 白磷和红磷对比 和水中的白磷对比 通氧气前与通氧气后对比
理石;
铜片上的白磷燃
铜 片 上 的 白 磷 燃 通氧气前,热水中的白磷
实验现象 烧,产生 大量白 烧,水中的白磷不 不燃烧;通氧气后,热水
烟 ,铜片上的红磷
燃烧。 中的白磷燃烧
不燃烧。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
可燃物是燃烧 燃烧需要温度达到 燃烧需要与氧气接
燃烧需要与氧气接触
的条件之一 可燃物的着火点 触
结论 通常情况下:燃烧需要同时满足三个条件:
① 可燃物 ; ② 可燃物与氧气 ( 或空气 ) 接触 ; ③温度达到可燃物的着火
点。
铜片的作用 导热、放置药品;
实验分析
热水的作用 ① 使水中白磷与空气隔绝 ②为薄铜片上的药品提供热量
3.教材实验改进
改进原因 现象
试管中的白磷燃烧,产生大量白烟,左边气球
PO 有毒,排放到空气中污染空
2 5
先胀大后变瘪。
气;实验用药品较多。
试管中的红磷和水中白磷不燃烧。
气球的作用是形成密闭环境防污染。
1.有发光、放热现象的变化一定是燃烧( )
错误。有发光、放热现象的变化不一定是燃烧,如灯泡通电发光、放热不是燃烧。
2.可燃物燃烧必须同时具备三个条件( )
正确。燃烧必须同时满足三个条件,缺一不可:可燃物;要与氧气接触;温度要达到着火点。
3.可燃物与氧气反应时都会发生燃烧( )
错误。可燃物与氧气反应时,不一定会发生燃烧,如铝在常温下便可与氧气反应产生氧化铝。
4.燃烧一定有火焰产生,并放出热量( )
错误。燃烧是一种剧烈的有氧反应,并放出热量,不一定有火焰产生,故错误。
1.【新考法】(2024·江苏徐州·中考真题)为探究燃烧的条件,向粘有蜡烛的烧杯中加入水并点燃蜡烛,
装置如图。蜡烛燃烧至水面处时熄灭,其主要原因是
A.蜡烛与氧气隔绝 B.蜡烛的着火点降低C.蜡烛没有可燃性 D.燃烧产生
二氧化碳
【答案】A
【详解】可燃物燃烧的条件:温度达到可燃物的着火点、与氧气接触,蜡烛燃烧至水面处时熄灭,其主要
原因是水使蜡烛与氧气隔绝,故选:A。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点二 燃料燃烧的调控
1.燃料的充分燃烧
(1)影响燃烧剧烈程度的因素:可燃物的性质、氧气的浓度、与氧气的接触面积 。
(2)燃料燃烧不充分的缺点:产生黑烟,生成CO等。使燃料利用率降低,浪费资源,且污染空气。
(3)使燃料充分燃烧,需要考虑两点:
①要有足够的空气(氧气);
②燃料与空气要有足够大的接触面积。
(4)生活应用
①烧柴火时,不停的向炉膛扇风,增大氧气的量;篝火晚会,架空木材, 增
大与空气的接触面积,燃烧更旺。
②天然气灶做饭时,火焰呈黄色或橙色,锅底有黑色固体出现,氧气不足,燃烧不充分,此时应该
将炉具的进风口“调大”,增大空气的进气量。
【特别提醒】
氧气的浓度越大,燃烧就越剧烈,可燃物与氧气接触面积越大,燃烧就越剧烈。
2.灭火的原理和方法
(1)灭火的原理:破坏燃烧必须具备的条件;
(2)灭火的方法:
①清除或隔离可燃物;如森林着火砍掉树木,开辟隔离带;煤气罐着,火关闭阀门等;
② 隔绝 O ;如油锅着火,盖锅盖;酒精在桌面上燃烧,用湿抹布扑盖;熄灭酒精灯,灯帽盖灭等;
2
③降温到可燃物的着火点以下;如油锅着火,放青菜;水灭火;吹灭蜡烛等;
(3)应用:
釜底抽薪——清除可燃物
杯水车薪——水太少了,不能使温度降至可燃物着火点以下
3.简易灭火器的原理
(1)利用饱和碳酸钠溶液与浓盐酸反应,瞬间产生大量的
二氧化碳使装置中的压强增大,喷出混有二氧化碳的液体,
有降温和隔绝空气的作用。
(2)反应的化学方程式:NaCO+2HCl=2NaCl+H O+CO↑
2 3 2 2
4.常见灭火器
灭火器 灭火原理 适用范围
隔绝空气 扑灭一般的失火外,还可以扑灭电器、油、气等燃烧引起的失火
干粉灭火器
(电器着火,先断电再灭火)
降温;隔绝空气 扑灭图书、档案、贵重设备、精密仪器等物的失火
二氧化碳灭火器
(灭火时不留下任何痕迹而使物体损坏)
隔绝空气 扑灭汽油、柴油、木材、棉布等的失火
水基型灭火器
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.为什么用扇子扇炉火,越扇越旺;用扇子扇蜡烛火焰,一扇就灭?
用扇子扇煤炉火,虽然降低了温度,但没有降至着火点以下,反而增加了空气的流通,所以
越扇越旺。用扇子扇蜡烛火焰,虽然增加了空气的流通,但却降低了温度至着火点以下,所
以一扇就灭。
2.判断对错:
(1)电器着火,应先切断电源,再灭火。(√)
(2)室内起火,打开门窗。(ⅹ)
打开门窗,会增加空气的流通,增加氧气的浓度,反应剧烈,燃烧更旺。
(3)吹灭蜡烛,是隔绝了氧气。(ⅹ)
吹灭蜡烛,是空气流动带走热量,使蜡烛火焰温度降低到着火点以下。
1.【新素材】(2024·湖南·中考真题)花鼓戏《补锅》中唱到“手拉风箱呼呼响,火炉烧得红旺旺”。下
列说法最合理的是
A.风箱拉动过程中增加了可燃物
B.手拉风箱为煤的燃烧提供了充足氧气
C.火炉烧得旺是因为降低了煤的着火点
D.氧气能支持燃烧,说明氧气具有可燃性
【答案】B
【详解】A、风箱拉动过程中提供了充足的氧气,而氧气并不是可燃物,故选项说法不正确;
B、风箱拉动过程中提供了充足的氧气,有利于煤充分燃烧,故选项说法正确;
C、着火点是物质的固有属性,一般不会改变,故选项说法不正确;
D、氧气能支持燃烧,说明氧气具有助燃性,不具有可燃性,故选项说法不正确。
故选B。
考点三 易燃物易爆物的安全知识
1.爆炸
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)概念:可燃物在有限的空间内急剧地燃烧,在短时间内聚积大量的热,使气体的体积迅速膨胀而引
起爆炸。
(2)爆炸极限:可燃性气体或粉尘等在空气中达到一定含量时,遇到明火会发生爆炸。
(3)可燃性气体或粉尘与空气或氧气混合,遇到明火可能会发生爆炸;所以可燃性气体在点燃或加热前
都要验纯,以防止发生爆炸。
(4)常见的可燃性气体有:氢气、一氧化碳、甲烷、天然气、煤气、液化石油气;
常见的可燃性粉尘有:面粉、煤粉、纺织厂的粉尘等
2.防爆注意事项
(1)加油站、油库、面粉加工厂、纺织厂和煤矿的矿井内有“严禁烟火”的字样或消防安全标志。
(2)在生产、运输、使用、储存易燃物、易爆物时,必须严格遵守有关规定,绝不允许违章操作。
(3)部分消防安全标志
1.煤气泄漏需要立即关闭阀门并打开窗户通风。(不能用火种照明;不用用电设备,如不在室内拨打电话、
不能开电灯、不能开排气扇等)
2.若燃气管道泄漏,不能用燃着的蜡烛检査,可用涂肥皂水的方法去检查或用仪器检查。
3.爆炸的条件是:可燃性气体与助燃性气体充分混合,且有明火。
4.几种可燃性气体混合,遇明火不会发生爆炸,而是安静的燃烧。只有可燃性气体与空气或氧气混合后,
遇明火才会发生爆炸。
1.【新考向】(2024·北京·中考真题)下列标志表示“禁止烟火”的是
A. B. C. D.
【答案】B
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【详解】A、该标志是腐蚀品标志,不符合题意;
B、该标志是禁止烟火标志,符合题意;
C、该标志是爆炸品标志,不符合题意;
D、该标志是禁止放易燃物标志,不符合题意。
故选B。
考点四 化学反应中的能量变化
1.化学反应中,物质在发生变化时还伴随能量变化,通常表现为热量的变化,即吸热或放热现象。还可以
转化为其他形式的能量,如电能。
2.人类生活对能量的利用
利用燃烧产生的能量 利用爆炸产生的能量
做饭、取暖、发电、烧制陶瓷、冶炼金 开矿采煤、开山炸石、定向爆炸、拆除
属、发射火箭等 危旧建筑等
1.化学反应中一定有能量的变化,只是有些明显,有些不易察觉。
2.条件为加热或高温的反应很多是吸热反应,但也有的不是,加热或高温不是判断吸热反应的依据。
1.【新考向】(2024·广西南宁·模拟预测)下列有关化学反应与能量的说法,正确的是
A.化学反应伴随着能量变化 B.化学反应不一定遵循质量守恒定律
C.在化学反应中只有燃烧反应才能放出热量 D.人类利用的能量都是通过化学反应获得的
【答案】A
【详解】A、化学反应中伴随着能量变化,常表现为吸热或放热现象,正确;
B、化学反应一定遵循质量守恒定律,错误;
C、除燃烧外,还有很多反应也放热,例如缓慢氧化,生石灰与水的反应,金属和酸的反应等,错误;
D、人类利用的能量还可以通过做功的方法获得,错误;
故选 A。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实验 燃烧条件的探究
1.实验目的:
(1)加深对燃烧条件的认识,进一步了解灭火的原理。
(2)学会控制变量方法在科学探究中的运用
2.实验用品:烧杯、镊子、坩埚钳、酒精灯、火柴、酒精、小木块、煤块、蜡烛……
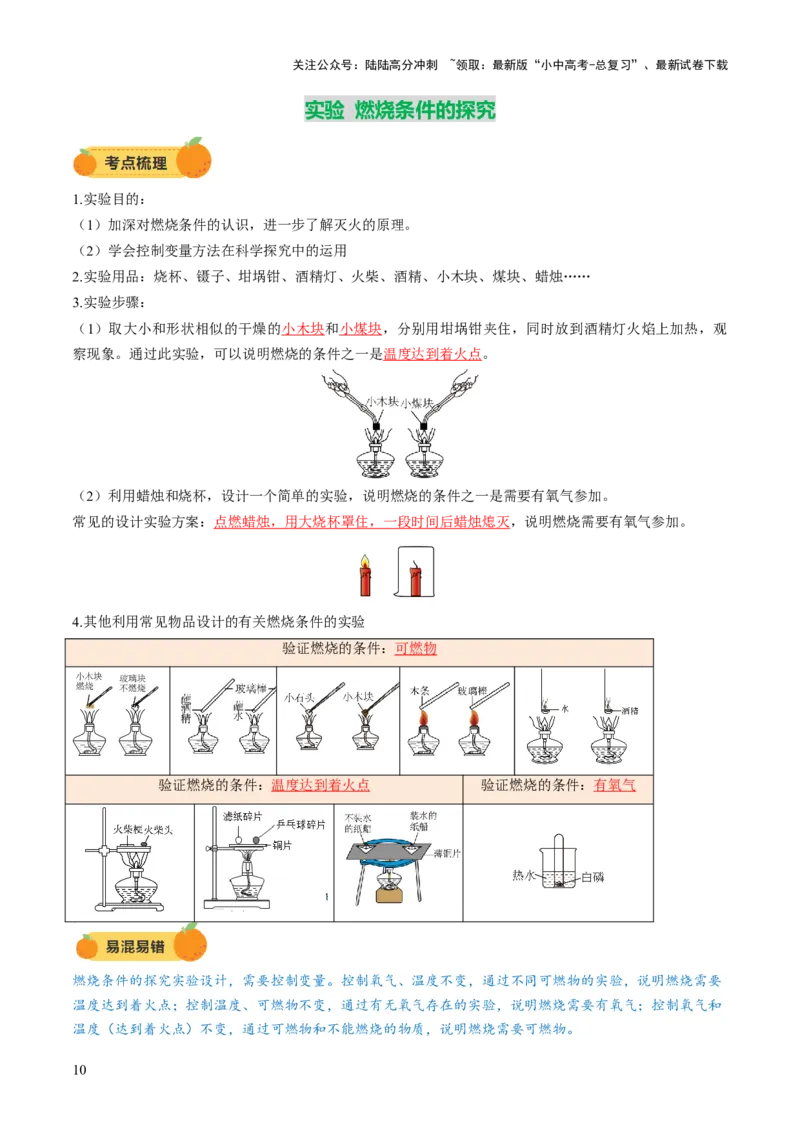
3.实验步骤:
(1)取大小和形状相似的干燥的小木块和小煤块,分别用坩埚钳夹住,同时放到酒精灯火焰上加热,观
察现象。通过此实验,可以说明燃烧的条件之一是温度达到着火点。
(2)利用蜡烛和烧杯,设计一个简单的实验,说明燃烧的条件之一是需要有氧气参加。
常见的设计实验方案:点燃蜡烛,用大烧杯罩住,一段时间后蜡烛熄灭,说明燃烧需要有氧气参加。
4.其他利用常见物品设计的有关燃烧条件的实验
验证燃烧的条件:可燃物
验证燃烧的条件:温度达到着火点 验证燃烧的条件:有氧气
燃烧条件的探究实验设计,需要控制变量。控制氧气、温度不变,通过不同可燃物的实验,说明燃烧需要
温度达到着火点;控制温度、可燃物不变,通过有无氧气存在的实验,说明燃烧需要有氧气;控制氧气和
温度(达到着火点)不变,通过可燃物和不能燃烧的物质,说明燃烧需要可燃物。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
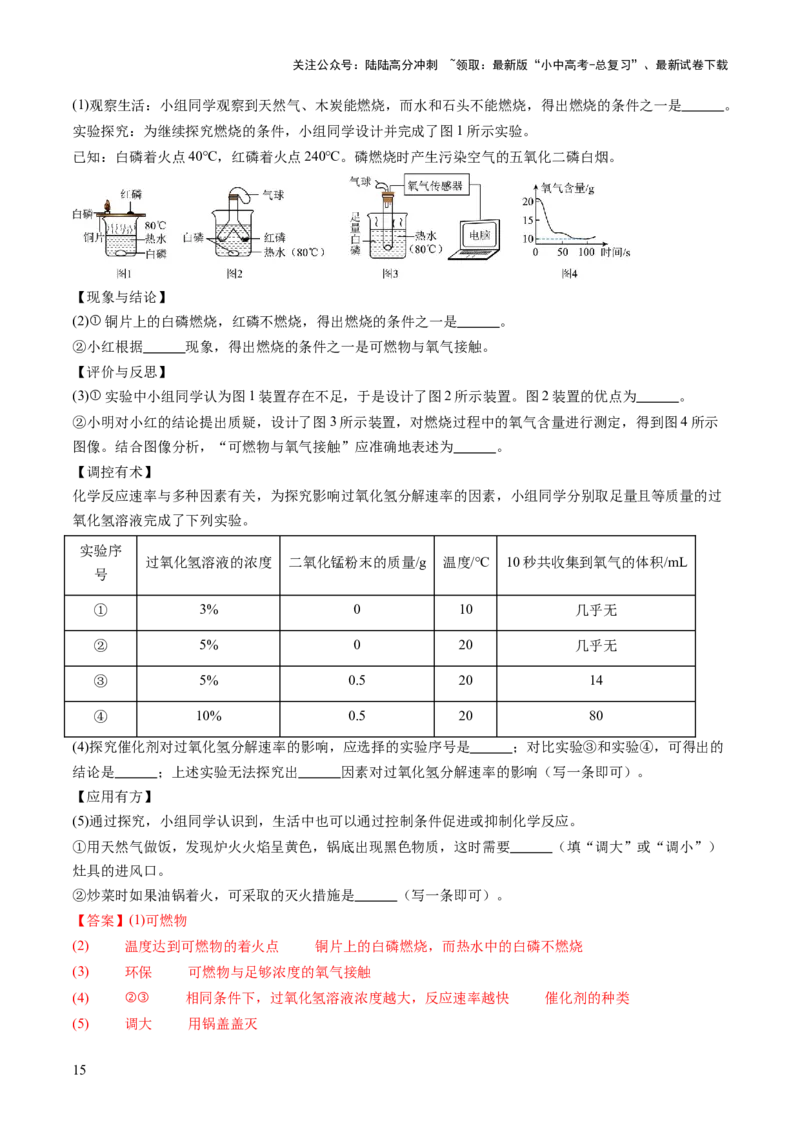
1.化学学习小组同学想通过实验探究燃烧的条件。
(1)图甲是探究燃烧需要 。
(2)如图乙所示:在燃着的蜡烛上扣一个烧杯,过一会观察到蜡烛熄灭,可以得出燃烧的条件之一是
。
(3)将装有某气体的试管管口朝下插入热水中,使试管罩住白磷(如图丙所示),结果观察到了白磷在水中
燃烧的“水火相容”奇观。则试管中所装气体可能是 。
【答案】(1)可燃物(或物质具有可燃性)
(2)燃烧需要充足的氧气
(3)氧气/O /空气
2
【详解】(1)图甲中小石头不燃烧,小木块燃烧,探究燃烧需要可燃物,故填:可燃物(或物质具有可
燃性)。
(2)如图乙所示:在燃着的蜡烛上扣一个烧杯,氧气消耗后,蜡烛便熄灭,可以得出燃烧的条件之一是:
燃烧需要充足的氧气,故填:燃烧需要充足的氧气。
(3)如图丙所示,结果观察到了白磷在水中燃烧的“水火相容”奇观,则试管所装气体可能是氧气或空
气,故答案为:氧气或O 或空气;
2
题型一 燃烧的条件
►考向01 燃烧的定义
1.(2024·四川广元·中考真题)逻辑推理是一种重要的化学思维方法。下列推理合理的是
A.金刚石、石墨都是由碳元素组成的单质,因此它们的性质相同
B.在化学变化中分子可以分成原子,因此原子是化学变化中最小的粒子
C.化合物是由多种元素组成的物质,因此由多种元素组成的物质一定是化合物
D.燃烧是物质与氧气发生的发光放热的剧烈的氧化反应,因此燃烧必须要有氧气参与
【答案】B
【详解】A、金刚石、石墨都是由碳元素组成的单质,它们的化学性质相同,但碳原子的排列方式不同,
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
它们的物理性质差异很大,故选项推理错误;
B、在化学变化中分子可以分成原子,原子在重新组合成新分子,因此原子是化学变化中最小的粒子,故
选项推理正确;
C、化合物是由多种元素组成的物质,但由多种元素组成的物质不一定是化合物,也可能是混合物,如过
氧化氢与水的混合物,故选项推理错误;
D、燃烧是物质与氧气发生的发光放热的剧烈的氧化反应,但燃烧不一定要有氧气参与,如镁在二氧化碳
燃烧,故选项推理错误。
故选B。
2.(2024·甘肃临夏·中考真题)推理是学习化学时常用的一种科学思维,下列说法中错误的是
A.酸雨的pH<7,但pH<7的雨水不一定是酸雨
B.某物质在氧气中燃烧生成SO ,该物质组成中一定含硫元素
2
C.溶液具有均一性、稳定性,但均一、稳定的液体不一定是溶液
D.燃烧伴随着发光、放热现象,所以有发光、放热现象的变化一定是燃烧
【答案】D
【详解】A、pH<5.6的降雨称为酸雨,所以pH<7的雨水不一定是酸雨。A正确;
B、根据质量守恒定律,化学反应前后元素质量不变,所以某物质在氧气中燃烧生成SO ,该物质组成中一
2
定含硫元素。B正确;
C、溶液是一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。水是均一、稳定的液体,
但水是纯净物,所以水不是溶液。即溶液具有均一性、稳定性,但均一、稳定的液体不一定是溶液。C正
确;
D、燃烧伴随着发光、放热现象,但电灯通电也有发光、放热,则不是燃烧。所以有发光、放热现象的变
化不一定是燃烧。D错误。
综上所述:选择D。
►考向02 燃烧的条件
3.【新考向】(2023·湖南湘潭·中考真题)古代用“木燧”(钻木取火)的方法引燃易燃物。下列说法错误
的是
A.“木燧”中的“木”是可燃物 B.钻木是机械能转化为热能的过程
C.钻木生热改变了可燃物的着火点 D.在钻木取火的过程中,空气提供了助燃物
【答案】C
【详解】A、“木燧”是指摩擦生热,使木柴燃烧,其中的“木”是可燃物,选项正确;
B、钻木过程中摩擦生热,机械能转化为热能,选项正确;
C、钻木生热,使木柴温度达到着火点以上,而不是改变了可燃物的着火点,选项错误;
D、在钻木取火的过程中,空气提供了氧气,氧气是助燃物,选项正确。
故选C。
4.【新考法】(2023·辽宁·中考真题)取一张光滑的厚纸,做成一个如图所示的小纸锅,用纸锅盛水在火上
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
加热,锅里的水烧开了,纸锅却没有燃烧,其主要原因是
A.纸的着火点变低 B.水隔绝了氧气
C.温度低于纸的着火点 D.纸锅与氧气的接触面积太小
【答案】C
【详解】水在沸腾过程中,尽管继续吸热,但温度总保持在沸点不变,而纸盒没有燃烧,说明水沸腾时的
温度没有达到纸燃烧时的温度,即水的沸点低于纸的着火点;故选C。
►考向03 实验探究燃烧的条件
5.【教材素材题】(2024·重庆·中考真题)利用红磷和白磷进行燃烧条件探究,实验装置如下图所示。下列
说法不正确的是
A.a处物质为白磷 B.红磷的着火点高于80℃
C.a、b两点对比说明燃烧需要氧气 D.c处通入氧气白磷能燃烧
【答案】C
【分析】白磷、红磷的着火点分别为40℃、240℃。
【详解】A、a处物质能燃烧,为白磷,故说法正确;
B、b处物质没有燃烧,是红磷,跟氧气接触,没有燃烧说明红磷的着火点高于80℃,故说法正确;
C、铜片上的白磷燃烧,红磷不燃烧,能说明燃烧时温度需达到着火点,故说法错误;
D、c处通入氧气,水中的白磷燃烧,故说法正确。
故选C。
6.【创新实验】(2024·江苏无锡·中考真题)用如图所示装置进行“探究燃烧条件”的对比实验:a处通
入氧气,管①中白磷未燃烧,b处通入氧气,管②中白磷燃烧。下列叙述错误的是
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.生料带起隔离作用
B.实验推知燃烧只需要氧气
C.实验推知白磷着火点(T)的范围:20℃