文档内容
2008 年普通高等学校招生全国统一考试(化学)
选择题 共21小题,第小题6分,共126分。
以下数据可供解题时参考:
相对原子质量(原子量):H l C 12 O 16 Na 23 K 39
Mn 55 Cu 64 Zn 65 Ag 108 Pb 207
一、 选择题(本题共13小题,在每小题给出的四个选项中,只有一项是符合题目要求
的。)
6.在溶液中加入中量NaO 后仍能大量共存的离子组是
2 2
A.NH+、Ba2+、Cl-、NO- B.K+、AlO-、Cl-、SO2-
4 3 2 4
C.Ca2+、Mg2+、NO-、HCO- D.Na+、Cl-、CO2-、SO2-
3 3 3 3
7.下列化合物,按其品体的熔点由高到低排列正确的是
A.SiO CaCl CBr CF B.SiO CsCl CF CBr
2 4 2 2 4 4
C.CsCl SiO CBr CF D.CF CBr CsCl SiO
2 4 4 4 4 2
8.下列各组物质不属于同分异构体的是
A.2,2-二甲基丙醇和2-甲基丁醇 B.邻氯甲苯和对氯甲苯
C.2-甲基丁烷和戊烷 D.甲基丙烯酸和甲酸丙酯
9.下列各组给定原子序数的元素,不能形成原子数之比为1∶1稳定化合物的是
A.3和17 B.1和8 C.1和6 D.7和12
10.下列叙述中正确的是
A. NH 、CO、CO 都是极性分子
3 2
B. CH、CCl 都是含有极性键的非极性分子
4 4
C. HF、HCl、HBr、Hl的稳定性依次增强
D. CS、HO、C H 都是直线型分子
2 2 2 2
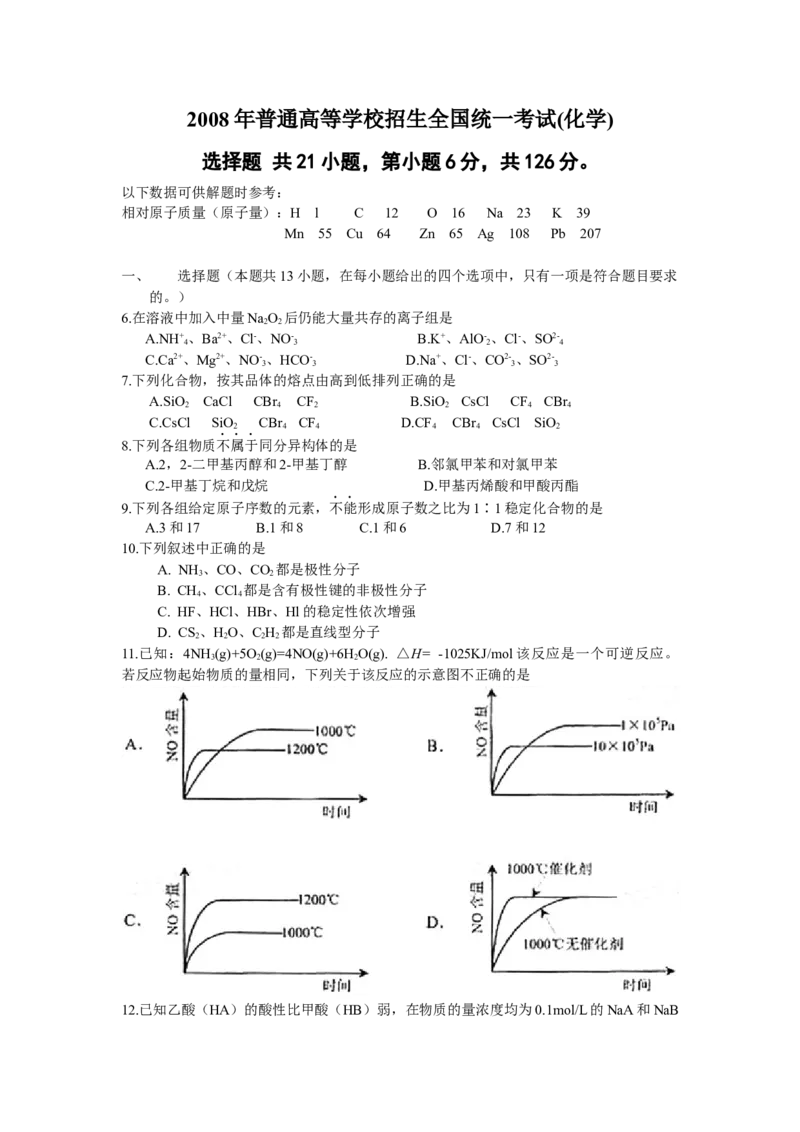
11.已知:4NH (g)+5O(g)=4NO(g)+6H O(g). △H= -1025KJ/mol该反应是一个可逆反应。
3 2 2
若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
12.已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1mol/L的NaA和NaB混合溶液中,下列排序正确的是
A.c(OH)>c(HA)>c(HB)>c(H+) B. c(OH-)>c(A-)>c(B-)>c(H+)
C. c(OH-)>c(B-)>c(A-)>c(H+) D. c(OH-)>c(HB)>c(HA)>c(H+)
13.电解100mL含 c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论
上析出金属质量最大的是
A. 0.10mol/LAg+ B. 0.20mol/L Zn2+
C. 0.20mol/L Cu2+ D. 0.20mol/L Pb2+
26.(16分)
实验室可由软锰矿(主要成分为MnO )制备KMnO ,方法如下:软锰矿与过量固体
2 4
KOH和KClO 在高温下反应,生成锰酸钾(KMnO )和KCl;用水溶解,滤去残渣,滤
3 2 4
液酸化后,KMnO 转变为MnO 和KMnO ;滤去MnO 沉淀,浓缩滤液,结晶得到深紫
2 4 2 4 2
色的针状KMnO 。请回答:
4
(1) 软锰矿制备KMnO 的化学方程式是
2 4
;
(2)KMnO 制备KMnO 的离子方程式是 ;
2 4 4
(3)若用2.5g软锰矿(含MnO 80%)进行上述实验,计算KMnO 的理论产量;
2 4
(4)KMnO 能与热的经硫酸酸化的NaC O 反应生成Mn2+和CO ,该反应的化学方
4 2 2 4 2
程式是
;
(5)上述制得的KmnO 产品0.165g,恰好与0.335g纯NaC O 反应完全,计算该
4 2 2 4
KMnO 的纯度。
4
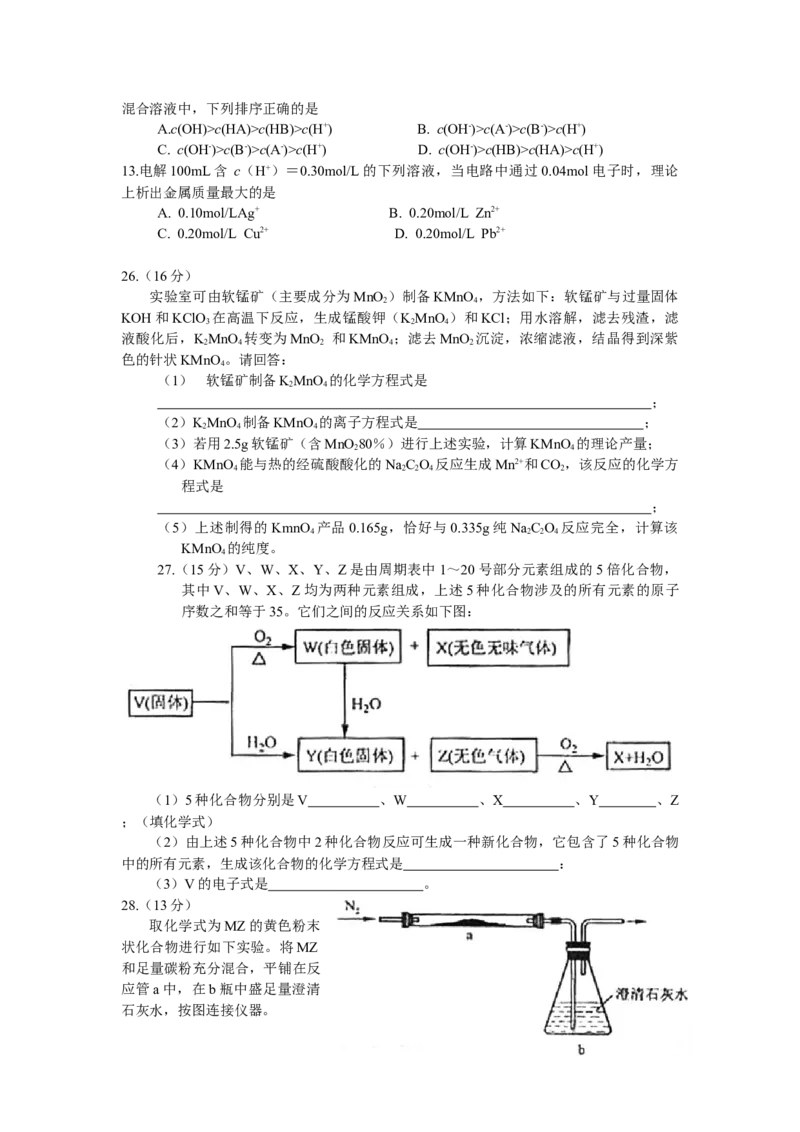
27.(15分)V、W、X、Y、Z是由周期表中1~20号部分元素组成的5倍化合物,
其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子
序数之和等于35。它们之间的反应关系如下图:
(1)5种化合物分别是V 、W 、X 、Y 、Z
;(填化学式)
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物
中的所有元素,生成该化合物的化学方程式是 :
(3)V的电子式是 。
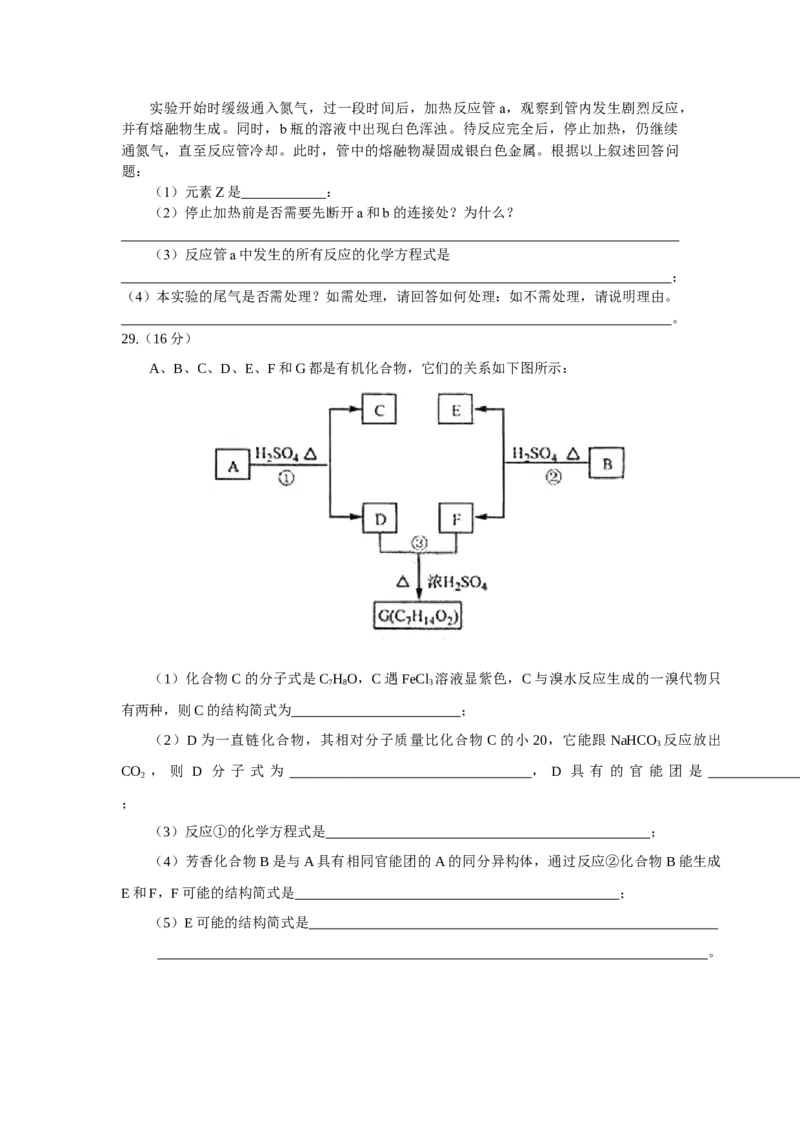
28.(13分)
取化学式为MZ的黄色粉末
状化合物进行如下实验。将MZ
和足量碳粉充分混合,平铺在反
应管a中,在b瓶中盛足量澄清
石灰水,按图连接仪器。实验开始时缓级通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,
并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续
通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。根据以上叙述回答问
题:
(1)元素Z是 :
(2)停止加热前是否需要先断开a和b的连接处?为什么?
(3)反应管a中发生的所有反应的化学方程式是
;
(4)本实验的尾气是否需处理?如需处理,请回答如何处理:如不需处理,请说明理由。
。
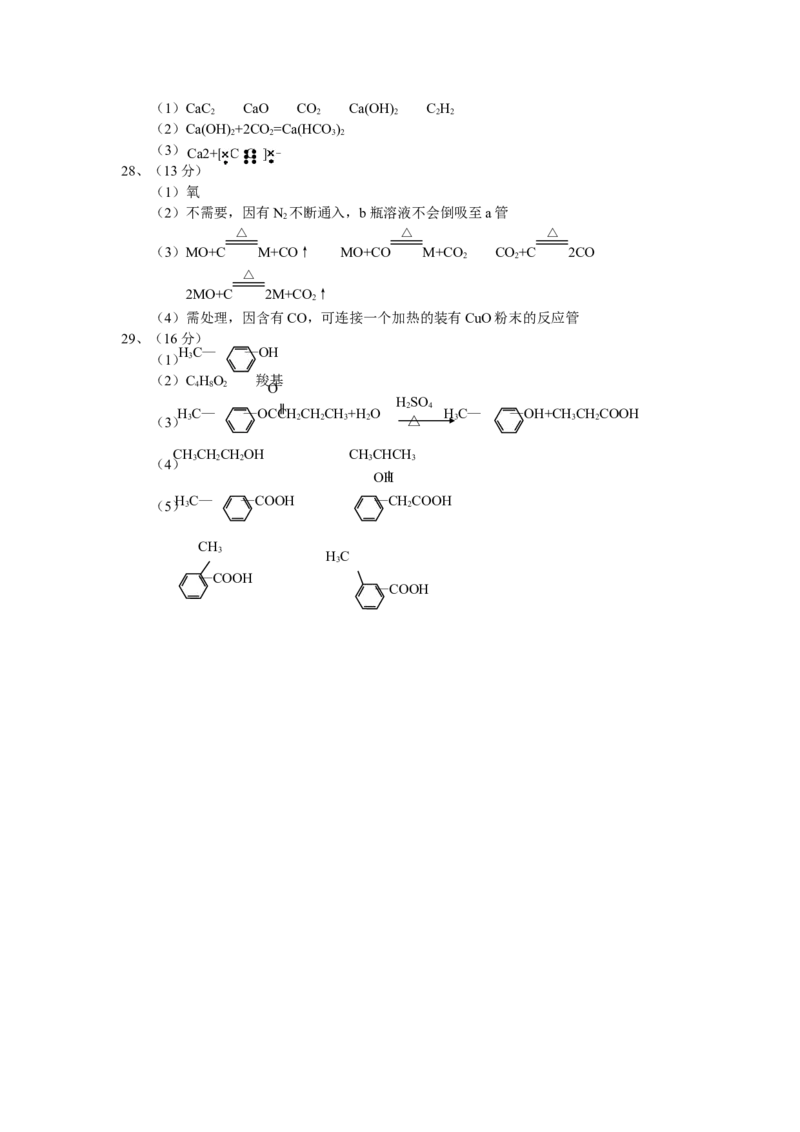
29.(16分)
A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:
(1)化合物C的分子式是C HO,C遇FeCl 溶液显紫色,C与溴水反应生成的一溴代物只
7 8 3
有两种,则C的结构简式为 ;
(2)D为一直链化合物,其相对分子质量比化合物 C的小20,它能跟NaHCO 反应放出
3
CO , 则 D 分 子 式 为 , D 具 有 的 官 能 团 是
2
;
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成
E和F,F可能的结构简式是 ;
(5)E可能的结构简式是
。参考答案
第Ⅰ卷共21小题,每小题6分,共126分。
一、选择题:选对的给6分,选错或未选的给0分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案 A C D C D B A D D B C A C
26、(16分)
△
(1)3MnO +6KOH+KClO 3KMnO +KCl+3H O
2 3 2 4 2
O2- O−
(2)3Mn 4 +4H+ = MnO ↓+2Mn 4 +2H O
2 2
(3)由上述两个化学方程式可知,反应物和生成物间的计量关系为:
2
3
MnO KMnO KMnO
2 2 4 4
2
3
87 158×
2.5×80% x
2
158g/mol× ×2.5g×80%
3
x= =2.4g
87g/mol
答:KMnO 的理论产量是2.4g
4
△
(4)2KMnO +5Na C O+8H SO KSO +2MnSO +5Na SO +10CO ↑+8H O
4 2 2 4 2 4 2 4 4 2 4 2 2
(5)设该KMnO 的纯度为y,根据化学方程式可知
4
2
5
KMnO ———NaC O
4 2 2 4
2
5
×158 134
0.165 × y 0.335
0.335g 2
× ×158g/mol
134g/mol 5
y= ×100%=95.8%
0.165g
27、(15分)(1)CaC CaO CO Ca(OH) C H
2 2 2 2 2
(2)Ca(OH) +2CO =Ca(HCO )
2 2 3 2
(3) Ca2+[ C C ]2-
28、(13分)
(1)氧
(2)不需要,因有N 不断通入,b瓶溶液不会倒吸至a管
2
△ △ △
(3)MO+C M+CO↑ MO+CO M+CO CO+C 2CO
2 2
△
2MO+C 2M+CO↑
2
(4)需处理,因含有CO,可连接一个加热的装有CuO粉末的反应管
29、(16分)
HC— —OH
(1)3
(2)C HO 羧基
4 8 2 O
HSO
2 4
HC— —OCCH CHCH+H O HC— —OH+CH CHCOOH
(3)3 2 2 3 2 △ 3 3 2
CHCHCHOH CHCHCH
(4) 3 2 2 3 3
OH
HC— —COOH —CHCOOH
(5)3 2
CH
3 HC
3
—COOH
—COOH