文档内容
2010 年全国统一高考化学试卷(全国卷Ⅰ)
一、选择题
1.(3分)下列判断错误的是( )
A.熔点:Si N >NaCl>SiI
3 4 4
B.沸点:NH >PH >AsH
3 3 3
C.酸性:HClO >H SO >H PO
4 2 4 3 4
D.碱性:NaOH>Mg(OH) >Al(OH)
2 3
2.(3分)下列叙述正确的是( )
A.Li在氧气中燃烧主要生成Li O
2 2
B.将 CO 通入次氯酸钙溶液可生成次氯酸
2
C.将 SO 通入 BaCl 溶液可生成BaSO 沉淀
2 2 3
D.将NH 通入热的CuSO 溶液中能使Cu2+还原成 Cu
3 4
3.(3分)能正确表示下列反应的离子方程式是( )
A.将铁粉加入稀硫酸中2Fe+6H+═2Fe3++3H ↑
2
B.将磁性氧化铁溶于盐酸Fe O +8H+═3Fe3++4H O
3 4 2
C.将氯化亚铁溶液和稀硝酸混合Fe2++4H++NO ﹡═Fe3++2H O+NO↑
3 2
D.将铜屑加Fe3+溶液中2Fe3++Cu═2Fe2++Cu2+
4.(3分)下列叙述正确的是( )
A.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.在滴有酚酞溶液的氨水中,加入NH Cl的溶液恰好无色,则此时溶液
4
pH<7
C.常温下,1.0×10﹡3mol/L 盐酸的pH=3.0,1.0×10﹡8mol/L 盐酸pH=8.0
D.若1mLpH=1盐酸与100mLNaOH溶液混合后,溶液 pH=7,则NaOH 溶
液的pH=11
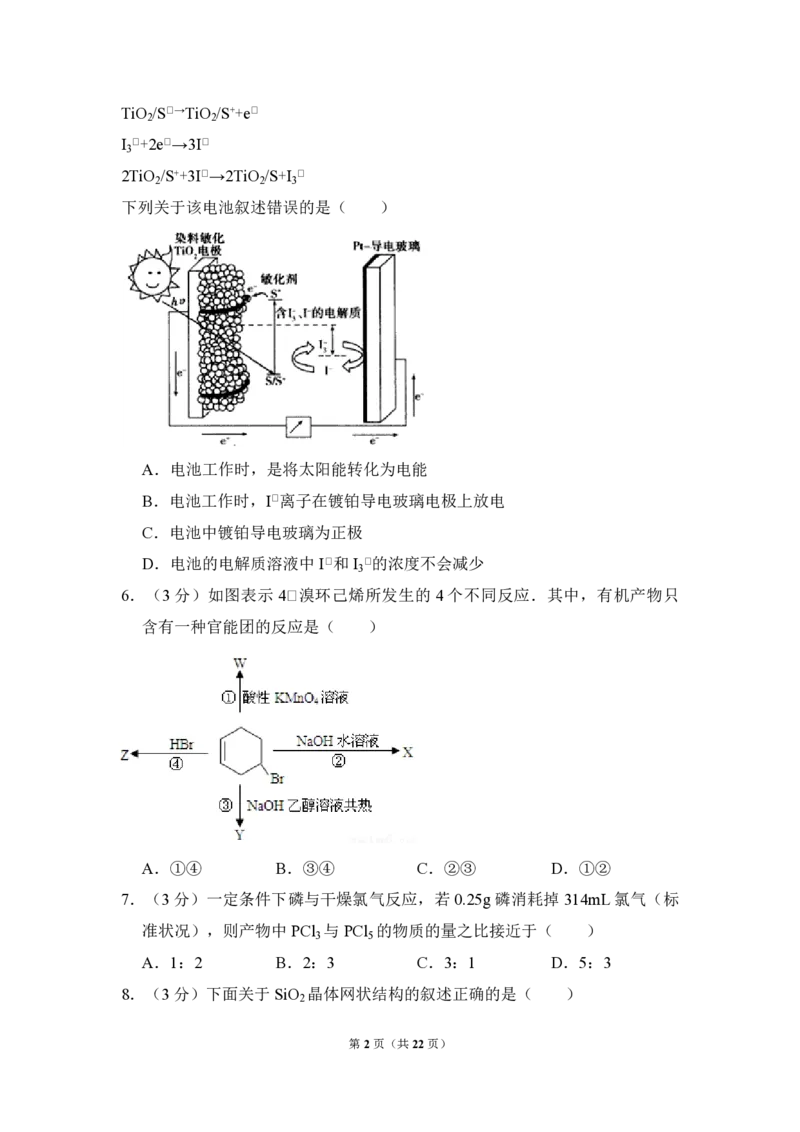
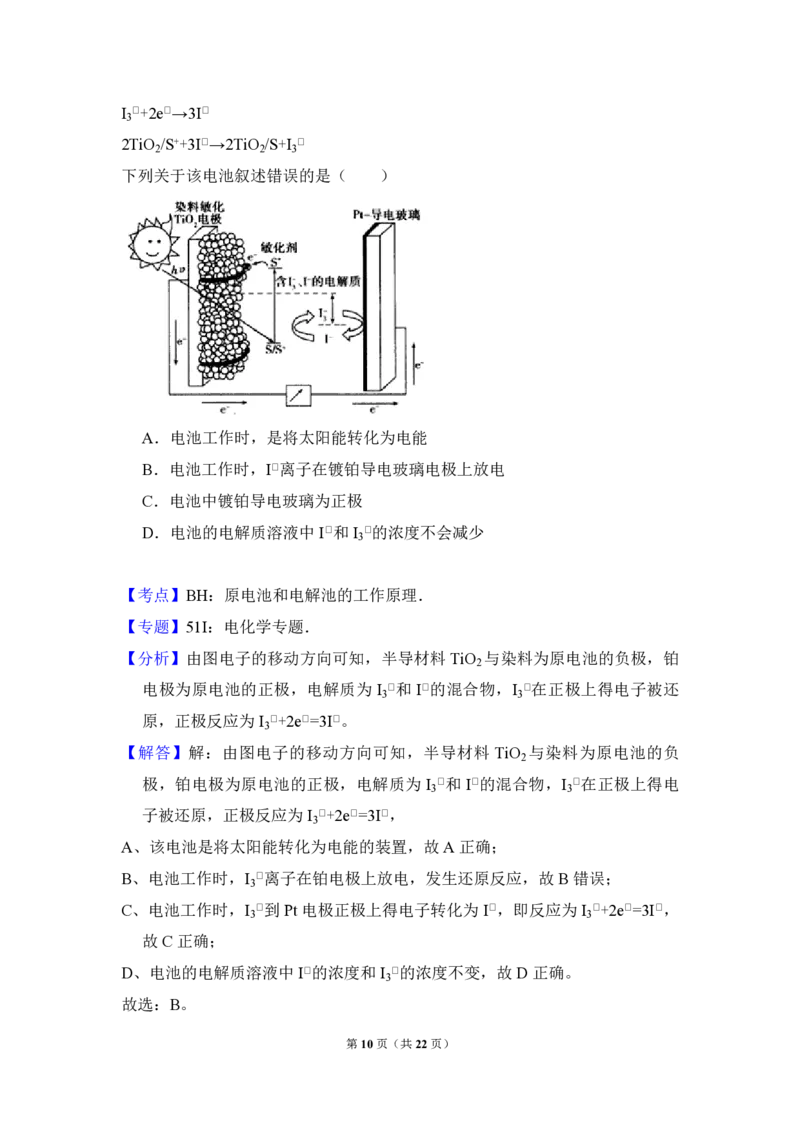
5.(3 分)如图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机
光敏燃料(S)涂覆在 TiO 纳米晶体表面制成,另一电极由导电玻璃镀铂构
2
成,电池中发生的反应为:
TiO /s→TiO /S﹡(激发态)
2 2
第1页(共22页)TiO /S﹡→TiO /S++e﹡
2 2
I ﹡+2e﹡→3I﹡
3
2TiO /S++3I﹡→2TiO /S+I ﹡
2 2 3
下列关于该电池叙述错误的是( )
A.电池工作时,是将太阳能转化为电能
B.电池工作时,I﹡离子在镀铂导电玻璃电极上放电
C.电池中镀铂导电玻璃为正极
D.电池的电解质溶液中I﹡和I ﹡的浓度不会减少
3
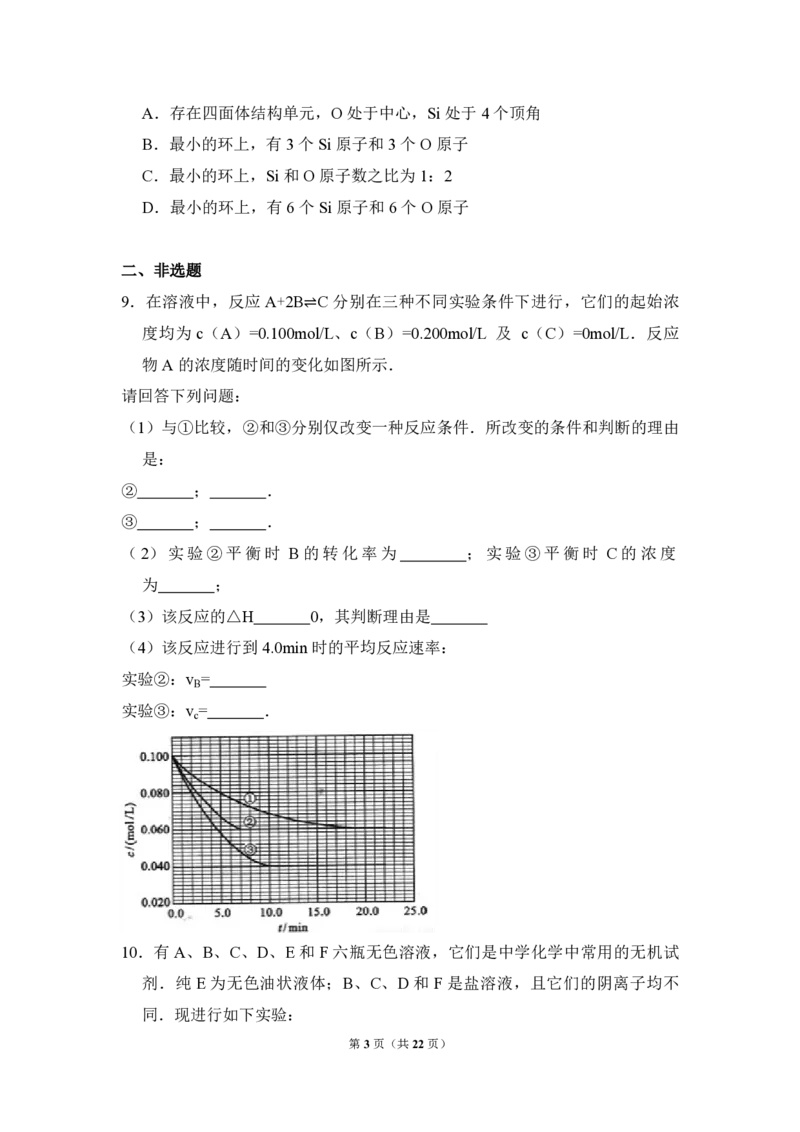
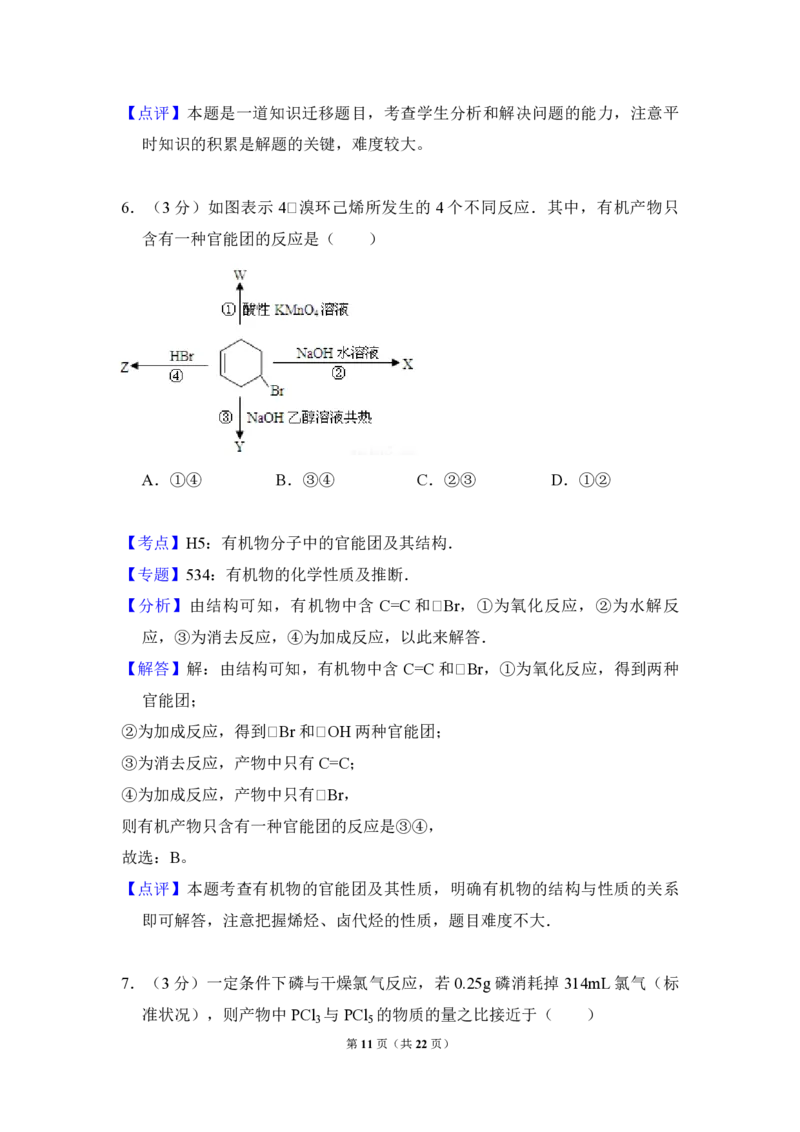
6.(3分)如图表示 4﹡溴环己烯所发生的 4个不同反应.其中,有机产物只
含有一种官能团的反应是( )
A.①④ B.③④ C.②③ D.①②
7.(3分)一定条件下磷与干燥氯气反应,若 0.25g磷消耗掉 314mL氯气(标
准状况),则产物中PCl 与PCl 的物质的量之比接近于( )
3 5
A.1:2 B.2:3 C.3:1 D.5:3
8.(3分)下面关于SiO 晶体网状结构的叙述正确的是( )
2
第2页(共22页)A.存在四面体结构单元,O 处于中心,Si处于4个顶角
B.最小的环上,有3个 Si原子和3个O 原子
C.最小的环上,Si 和O 原子数之比为1:2
D.最小的环上,有6个Si原子和6个O 原子
二、非选题
9.在溶液中,反应 A+2B⇌C分别在三种不同实验条件下进行,它们的起始浓
度均为 c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应
物A 的浓度随时间的变化如图所示.
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由
是:
② ; .
③ ; .
(2)实验②平衡时 B的转化率为 ;实验③平衡时 C的浓度
为 ;
(3)该反应的△H 0,其判断理由是
(4)该反应进行到4.0min时的平均反应速率:
实验②:v =
B
实验③:v = .
c
10.有 A、B、C、D、E和 F 六瓶无色溶液,它们是中学化学中常用的无机试
剂.纯 E为无色油状液体;B、C、D 和 F 是盐溶液,且它们的阴离子均不
同.现进行如下实验:
第3页(共22页)①A 有刺激性气味,用沾有浓盐酸的玻璃棒接近A 时产生白色烟雾;
②将 A 分别加入其它五种溶液中,只有 D、F 中有沉淀产生;继续加入过量 A
时,D 中沉淀无变化,F 中沉淀完全溶解;
③将 B分别加入 C、D、E、F 中,C、D、F 中产生沉淀,E中有无色、无味气
体逸出;
④将C 分别加入D、E、F 中,均有沉淀生成,再加入稀 HNO ,沉淀均不溶.
3
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方
法: .
11.请设计CO 在高温下与木炭反应生成CO 的实验.
2
(1)在下面方框中,A 表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题
卡上的 A 后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理
不分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下
方标出字母 B、C…;其他可选用的仪器(数量不限)简易表示如下:
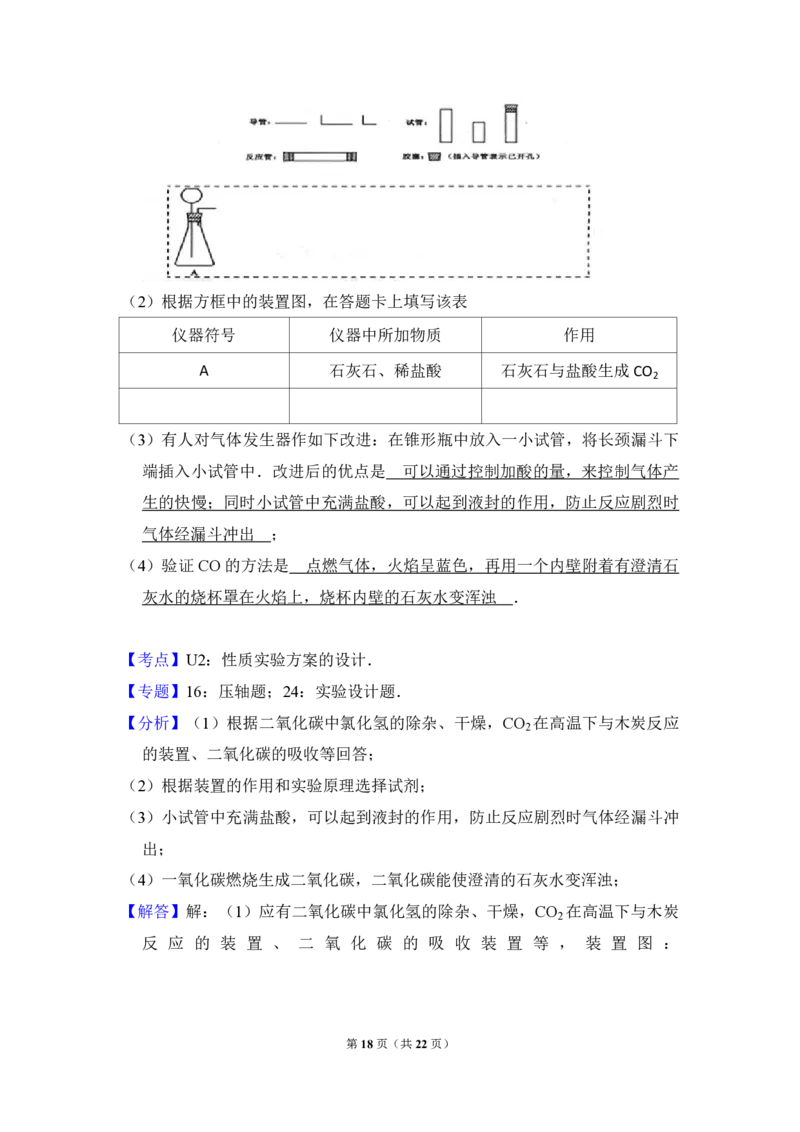
(2)根据方框中的装置图,在答题卡上填写该表
仪器符号 仪器中所加物质 作用
A 石灰石、稀盐酸 石灰石与盐酸生成 CO
2
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下
端插入小试管中.改进后的优点是 ;
(4)验证CO 的方法是 .
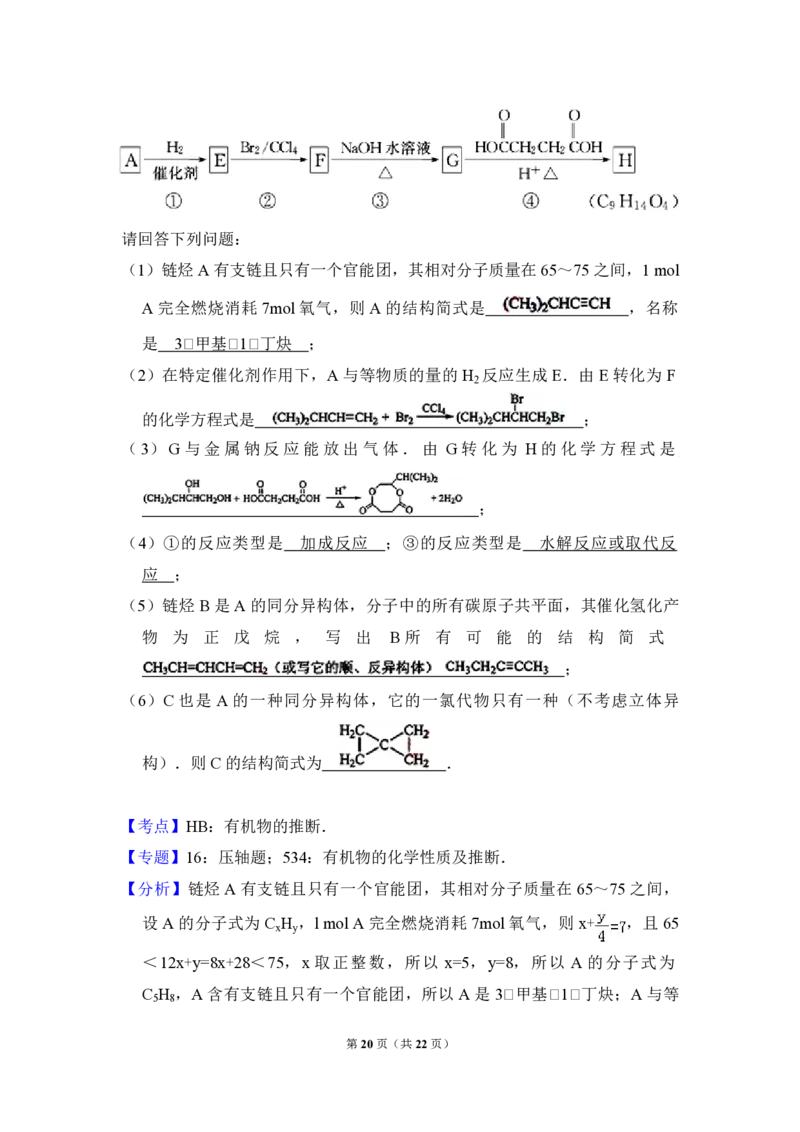
第4页(共22页)12.有机化合物A~H 的转换关系如下所示:
请回答下列问题:
(1)链烃 A 有支链且只有一个官能团,其相对分子质量在 65~75之间,1 mol
A 完全燃烧消耗7mol氧气,则A 的结构简式是 ,名称是 ;
(2)在特定催化剂作用下,A 与等物质的量的 H 反应生成 E.由 E转化为 F
2
的化学方程式是 ;
(3)G 与金属钠反应能放出气体.由G 转化为H 的化学方程式是 ;
(4)①的反应类型是 ;③的反应类型是 ;
(5)链烃 B 是 A 的同分异构体,分子中的所有碳原子共平面,其催化氢化产
物为正戊烷,写出B所有可能的结构简式 ;
(6)C也是 A 的一种同分异构体,它的一氯代物只有一种(不考虑立体异
构).则C 的结构简式为 .
第5页(共22页)2010 年全国统一高考化学试卷(全国卷Ⅰ)
参考答案与试题解析
一、选择题
1.(3分)下列判断错误的是( )
A.熔点:Si N >NaCl>SiI
3 4 4
B.沸点:NH >PH >AsH
3 3 3
C.酸性:HClO >H SO >H PO
4 2 4 3 4
D.碱性:NaOH>Mg(OH) >Al(OH)
2 3
【考点】75:金属在元素周期表中的位置及其性质递变的规律;76:非金属在
元素周期表中的位置及其性质递变的规律;77:元素周期律的作用;9H:晶
体熔沸点的比较.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题;51D:化学键与晶体结构.
【分析】A、从晶体的类型比较;
B、从是否含有氢键的角度比较;
C、从非金属性强弱的角度比较;
D、从金属性强弱的角度比较;
【解答】解:A、Si N 为原子晶体,NaCl为离子晶体,SiI 为分子晶体,一般
3 4 4
来说,不同晶体的熔点高低按照原子晶体>离子晶体>分子晶体的顺序,故
有Si N >NaCl>SiI ,故A 正确;
3 4 4
B、NH 含有氢键,沸点最高,PH 和 AsH 不含氢键,沸点的高点取决于二者
3 3 3
的相对分子质量大小,相对分子质量越大,沸点越高,应为 AsH >PH ,故
3 3
顺序为NH >AsH >PH ,故B错误;
3 3 3
C、元素的非金属性越强,其对应的最高价氧化物的水化物的酸性就越强,由
于非金属性 Cl>S>P,所以最高价氧化物的水化物的酸性的强弱顺序为:
HClO >H SO >H PO ,故 C正确;
4 2 4 3 4
D、元素的金属性越强,其对应的最高价氧化物的水化物的碱性就越强,由于
第6页(共22页)金属性 Na>Mg>Al,所以最高价氧化物的水化物的碱性的强弱顺序为:
NaOH>Mg(OH) >Al(OH) ,故D 正确。
2 3
故选:B。
【点评】本题考查不同晶体的熔沸点的高低以及物质酸性、碱性的强弱比较,
本题难度不大,注意积累相关基础知识,本题中注意氢键的问题以及晶体类
型的判断.
2.(3分)下列叙述正确的是( )
A.Li在氧气中燃烧主要生成Li O
2 2
B.将 CO 通入次氯酸钙溶液可生成次氯酸
2
C.将 SO 通入 BaCl 溶液可生成BaSO 沉淀
2 2 3
D.将NH 通入热的CuSO 溶液中能使Cu2+还原成 Cu
3 4
【考点】EB:氨的化学性质;F5:二氧化硫的化学性质;GG:碱金属的性
质.
菁优网版权所有
【专题】523:氧族元素;524:氮族元素;526:金属概论与碱元素.
【分析】A、锂的性质不同于钠,与镁的性质相似;
B、碳酸的酸性比次氯酸强,反应可以发生;
C、根据盐酸和亚硫酸的酸性强弱判断反应能否进行;
D、在溶液中发生离子反应,生成氢氧化铜沉淀.
【解答】解:A、锂在空气中燃烧生成氧化锂,故A 错误;
B、碳酸的酸性比次氯酸强,反应可以发生,故B正确;
C、盐酸的酸性比亚硫酸强,将 SO 通入 BaCl 溶液不会生成 BaSO 沉淀,故
2 2 3
C错误;
D、将 NH 通入热的 CuSO 溶液中生成氢氧化铜沉淀,而在加热条件下,氨气
3 4
可和氧化铜反应生成铜,故 D 错误。
故选:B。
【点评】本题考查物质的性质,涉及锂的性质、盐酸和亚硫酸的酸性强弱、碳
酸和次氯酸的酸性强弱以及氨气和硫酸铜溶液的反应,本题难度不大,注意
第7页(共22页)D 选项为易错点.
3.(3分)能正确表示下列反应的离子方程式是( )
A.将铁粉加入稀硫酸中2Fe+6H+═2Fe3++3H ↑
2
B.将磁性氧化铁溶于盐酸Fe O +8H+═3Fe3++4H O
3 4 2
C.将氯化亚铁溶液和稀硝酸混合Fe2++4H++NO ﹡═Fe3++2H O+NO↑
3 2
D.将铜屑加Fe3+溶液中2Fe3++Cu═2Fe2++Cu2+
【考点】49:离子方程式的书写.
菁优网版权所有
【专题】516:离子反应专题.
【分析】A、铁和非氧化性的酸反应生成亚铁盐;
B、磁性氧化铁中的铁元素有正二价和正三价两种;
C、离子反应要遵循电荷守恒;
D、铜和三价铁反应生成亚铁离子和铜离子.
【解答】解:A、铁和稀硫酸反应生成亚铁盐,Fe+2H+=Fe2++H ↑,故A 错误;
2
B、磁性氧化铁溶于盐酸发生的反应为:Fe O +8H+=2Fe3++Fe2++4H O,故 B错
3 4 2
误;
C、氯化亚铁溶液能被稀硝酸氧化,3Fe2++4H++NO ﹡=3Fe3++2H O+NO↑,故 C
3 2
错误;
D、铜和三价铁反应生成亚铁离子和铜离子,铜不能置换出铁,即
2Fe3++Cu=2Fe2++Cu2+,故D 正确。
故选:D。
【点评】本题主要考查学生离子方程时的书写知识,要注意原子守恒、电荷守
恒、得失电子守恒的思想,是现在考试的热点.
4.(3分)下列叙述正确的是( )
A.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.在滴有酚酞溶液的氨水中,加入NH Cl的溶液恰好无色,则此时溶液
4
pH<7
第8页(共22页)C.常温下,1.0×10﹡3mol/L 盐酸的pH=3.0,1.0×10﹡8mol/L 盐酸pH=8.0
D.若1mLpH=1盐酸与100mLNaOH溶液混合后,溶液 pH=7,则NaOH 溶
液的pH=11
【考点】D5:弱电解质在水溶液中的电离平衡;DA:pH 的简单计算.
菁优网版权所有
【专题】51G:电离平衡与溶液的pH 专题.
【分析】A、根据弱电解质的电离平衡来分析稀释后的pH;
B、根据离子对氨水的电离平衡的影响来分析平衡移动及溶液的pH;
C、根据常温下酸溶液的pH 一定小于7来分析;
D、根据酸碱混合及溶液的pH=7 来分析NaOH 溶液的 pH。
【解答】解:A、因醋酸是弱电解质,稀释时促进电离,但氢离子的浓度减
小,则pH 变大,即b>a,故A 错误;
B、在氨水中存在电离平衡,当加入 NH Cl,平衡逆向移动,氢氧根离子的浓
4
度减小,由酚酞的变色范围 8.2~10可知,此时溶液的 pH 可能小于 8.2,不
一定小于7,故B错误;
C、因常温下,中性溶液的 pH=7,则酸的 pH 一定小于 7,即盐酸溶液的 pH 不
会为8,故C错误;
D、因酸碱混合后 pH=7,即恰好完全反应,设碱的浓度为 c,则 1×
0.1mol/L=100×c,c=0.001mol/L,则NaOH 溶液的PH=11,故D 正确;
故选:D。
【点评】本题考查了电离平衡及 pH 的有关计算,学生应注意酸的溶液的 pH 在
常温下一定小于 7,能利用影响平衡的因素及酸碱反应的实质来分析解答即
可。
5.(3 分)如图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机
光敏燃料(S)涂覆在 TiO 纳米晶体表面制成,另一电极由导电玻璃镀铂构
2
成,电池中发生的反应为:
TiO /s→TiO /S﹡(激发态)
2 2
TiO /S﹡→TiO /S++e﹡
2 2
第9页(共22页)I ﹡+2e﹡→3I﹡
3
2TiO /S++3I﹡→2TiO /S+I ﹡
2 2 3
下列关于该电池叙述错误的是( )
A.电池工作时,是将太阳能转化为电能
B.电池工作时,I﹡离子在镀铂导电玻璃电极上放电
C.电池中镀铂导电玻璃为正极
D.电池的电解质溶液中I﹡和I ﹡的浓度不会减少
3
【考点】BH:原电池和电解池的工作原理.
菁优网版权所有
【专题】51I:电化学专题.
【分析】由图电子的移动方向可知,半导材料 TiO 与染料为原电池的负极,铂
2
电极为原电池的正极,电解质为 I ﹡和 I﹡的混合物,I ﹡在正极上得电子被还
3 3
原,正极反应为I ﹡+2e﹡=3I﹡。
3
【解答】解:由图电子的移动方向可知,半导材料 TiO 与染料为原电池的负
2
极,铂电极为原电池的正极,电解质为 I ﹡和 I﹡的混合物,I ﹡在正极上得电
3 3
子被还原,正极反应为 I ﹡+2e﹡=3I﹡,
3
A、该电池是将太阳能转化为电能的装置,故A 正确;
B、电池工作时,I ﹡离子在铂电极上放电,发生还原反应,故B错误;
3
C、电池工作时,I ﹡到 Pt 电极正极上得电子转化为I﹡,即反应为 I ﹡+2e﹡=3I﹡,
3 3
故C正确;
D、电池的电解质溶液中I﹡的浓度和I ﹡的浓度不变,故 D 正确。
3
故选:B。
第10页(共22页)【点评】本题是一道知识迁移题目,考查学生分析和解决问题的能力,注意平
时知识的积累是解题的关键,难度较大。
6.(3分)如图表示 4﹡溴环己烯所发生的 4个不同反应.其中,有机产物只
含有一种官能团的反应是( )
A.①④ B.③④ C.②③ D.①②
【考点】H5:有机物分子中的官能团及其结构.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】由结构可知,有机物中含 C=C和﹡Br,①为氧化反应,②为水解反
应,③为消去反应,④为加成反应,以此来解答.
【解答】解:由结构可知,有机物中含 C=C和﹡Br,①为氧化反应,得到两种
官能团;
②为加成反应,得到﹡Br和﹡OH 两种官能团;
③为消去反应,产物中只有C=C;
④为加成反应,产物中只有﹡Br,
则有机产物只含有一种官能团的反应是③④,
故选:B。
【点评】本题考查有机物的官能团及其性质,明确有机物的结构与性质的关系
即可解答,注意把握烯烃、卤代烃的性质,题目难度不大.
7.(3分)一定条件下磷与干燥氯气反应,若 0.25g磷消耗掉 314mL氯气(标
准状况),则产物中PCl 与PCl 的物质的量之比接近于( )
3 5
第11页(共22页)A.1:2 B.2:3 C.3:1 D.5:3
【考点】5A:化学方程式的有关计算.
菁优网版权所有
【专题】16:压轴题;1A:计算题.
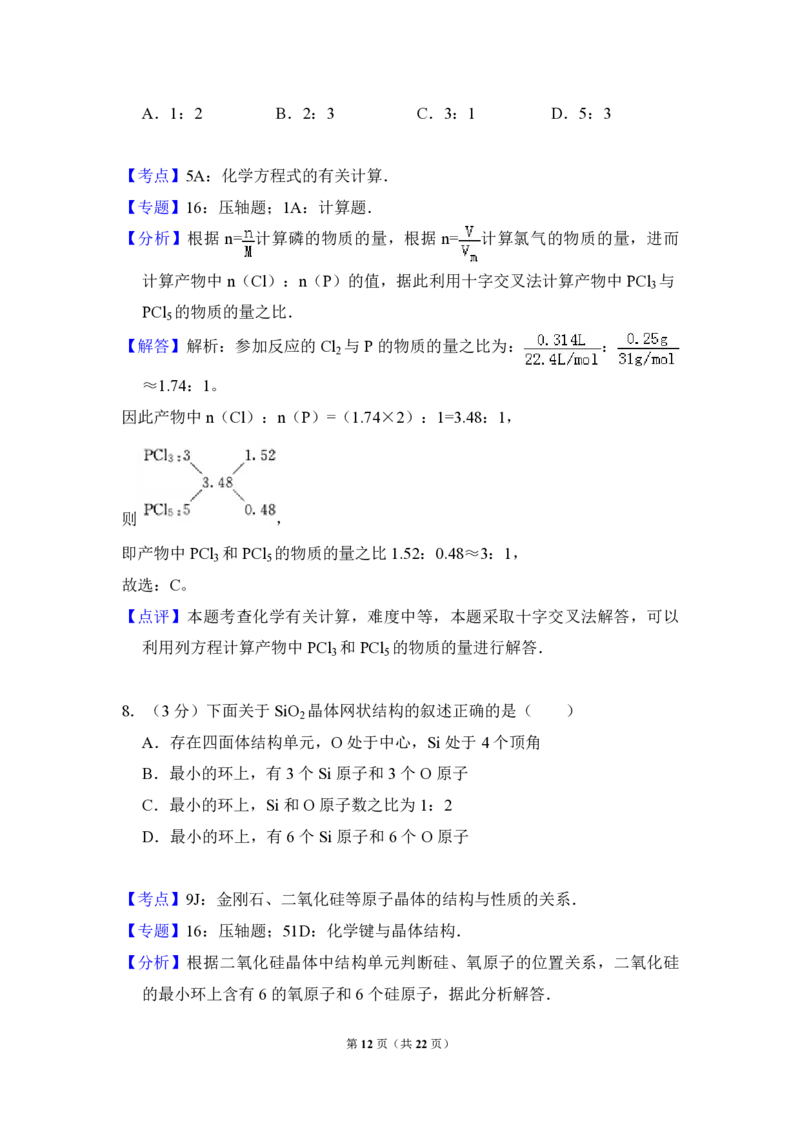
【分析】根据 n= 计算磷的物质的量,根据 n= 计算氯气的物质的量,进而
计算产物中 n(Cl):n(P)的值,据此利用十字交叉法计算产物中 PCl 与
3
PCl 的物质的量之比.
5
【解答】解析:参加反应的 Cl 与 P 的物质的量之比为: :
2
≈1.74:1。
因此产物中n(Cl):n(P)=(1.74×2):1=3.48:1,
则 ,
即产物中PCl 和PCl 的物质的量之比1.52:0.48≈3:1,
3 5
故选:C。
【点评】本题考查化学有关计算,难度中等,本题采取十字交叉法解答,可以
利用列方程计算产物中 PCl 和PCl 的物质的量进行解答.
3 5
8.(3分)下面关于SiO 晶体网状结构的叙述正确的是( )
2
A.存在四面体结构单元,O 处于中心,Si处于4个顶角
B.最小的环上,有3个 Si原子和3个O 原子
C.最小的环上,Si 和O 原子数之比为1:2
D.最小的环上,有6个Si原子和6个O 原子
【考点】9J:金刚石、二氧化硅等原子晶体的结构与性质的关系.
菁优网版权所有
【专题】16:压轴题;51D:化学键与晶体结构.
【分析】根据二氧化硅晶体中结构单元判断硅、氧原子的位置关系,二氧化硅
的最小环上含有6的氧原子和 6个硅原子,据此分析解答.
第12页(共22页)【解答】解:A、二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四
个共价键,每个氧原子能形成 2个共价键,Si处于中心,O 处于 4个顶角,
故A 错误;
B、最小的环上,有6个 Si原子和6个O 原子,故 B错误;
C、最小的环上,有 6个 Si原子和 6个 O 原子,所以最小的环上硅氧原子数之
比为1:1,故C错误;
D、最小的环上,有 6个 Si原子和 6个 O 原子,Si处于中心,O 处于 4个顶
角,故D 正确。
故选:D。
【点评】本题考查了二氧化硅的结构单元,难度不大,注意教材中基础知识的
掌握.
二、非选题
9.在溶液中,反应 A+2B⇌C分别在三种不同实验条件下进行,它们的起始浓
度均为 c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应
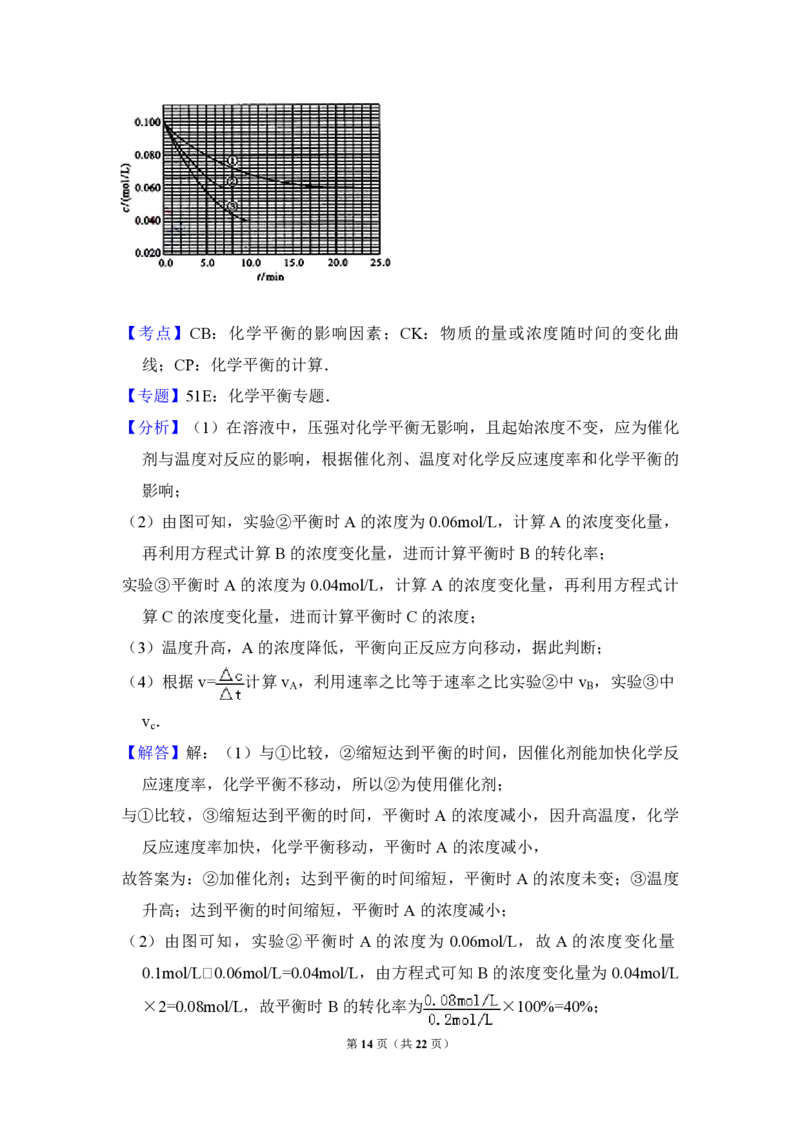
物A 的浓度随时间的变化如图所示.
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由
是:
② 加催化剂 ; 达到平衡的时间缩短,平衡时A 的浓度未变 .
③ 温度升高 ; 达到平衡的时间缩短,平衡时A 的浓度减小 .
(2)实验②平衡时 B的转化率为 40% ;实验③平衡时 C的浓度为
0.06mol/L ;
(3)该反应的△H > 0,其判断理由是 温度升高,平衡向正反应方向移
动,
(4)该反应进行到4.0min时的平均反应速率:
实验②:v = 0.014mol(L•min)﹡1
B
实验③:v = 0.009mol(L•min)﹡1 .
c
第13页(共22页)【考点】CB:化学平衡的影响因素;CK:物质的量或浓度随时间的变化曲
线;CP:化学平衡的计算.
菁优网版权所有
【专题】51E:化学平衡专题.
【分析】(1)在溶液中,压强对化学平衡无影响,且起始浓度不变,应为催化
剂与温度对反应的影响,根据催化剂、温度对化学反应速度率和化学平衡的
影响;
(2)由图可知,实验②平衡时 A 的浓度为 0.06mol/L,计算 A 的浓度变化量,
再利用方程式计算B的浓度变化量,进而计算平衡时 B的转化率;
实验③平衡时 A 的浓度为 0.04mol/L,计算 A 的浓度变化量,再利用方程式计
算C的浓度变化量,进而计算平衡时 C的浓度;
(3)温度升高,A 的浓度降低,平衡向正反应方向移动,据此判断;
(4)根据 v= 计算 v ,利用速率之比等于速率之比实验②中 v ,实验③中
A B
v .
c
【解答】解:(1)与①比较,②缩短达到平衡的时间,因催化剂能加快化学反
应速度率,化学平衡不移动,所以②为使用催化剂;
与①比较,③缩短达到平衡的时间,平衡时 A 的浓度减小,因升高温度,化学
反应速度率加快,化学平衡移动,平衡时 A 的浓度减小,
故答案为:②加催化剂;达到平衡的时间缩短,平衡时 A 的浓度未变;③温度
升高;达到平衡的时间缩短,平衡时 A 的浓度减小;
(2)由图可知,实验②平衡时 A 的浓度为 0.06mol/L,故 A 的浓度变化量
0.1mol/L﹡0.06mol/L=0.04mol/L,由方程式可知 B的浓度变化量为 0.04mol/L
×2=0.08mol/L,故平衡时 B的转化率为 ×100%=40%;
第14页(共22页)实 验 ③ 平 衡 时 A 的 浓 度 为 0.04mol/L, 故 A 的 浓 度 变 化 量
0.1mol/L﹡0.04mol/L=0.06mol/L, 由 方 程 式 可 知 C的 浓 度 变 化 量 为
0.06mol/L,故平衡时 C的浓度为0.06mol/L,
故答案为:40%;0.06mol/L;
(3)因③温度升高,平衡时 A 的浓度减小,化学平衡向吸热的方向移动,说
明正反应方向吸热,即△H>0,
故答案为:>;温度升高,平衡向正反应方向移动;
( 4) 实 验 ② 中 , v = =0.007mol( L•min) ﹡1, 所 以
A
v =2v =0.014mol(L•min)﹡1;
B A
实 验 ③ 中 , v = =0.009mol( L•min) ﹡1, 所 以
A
v =v =0.009mol(L•min)﹡1,
C A
故答案为:0.014mol(L•min)﹡1;0.009mol(L•min)﹡1.
【点评】本题考查化学平衡浓度﹡时间图象、化学反应速率计算、化学平衡影
响因素等,注意细心读取图象中物质的浓度,难度不大.
10.有 A、B、C、D、E和 F 六瓶无色溶液,它们是中学化学中常用的无机试
剂.纯 E为无色油状液体;B、C、D 和 F 是盐溶液,且它们的阴离子均不
同.现进行如下实验:
①A 有刺激性气味,用沾有浓盐酸的玻璃棒接近A 时产生白色烟雾;
②将 A 分别加入其它五种溶液中,只有 D、F 中有沉淀产生;继续加入过量 A
时,D 中沉淀无变化,F 中沉淀完全溶解;
③将 B分别加入 C、D、E、F 中,C、D、F 中产生沉淀,E中有无色、无味气
体逸出;
④将C 分别加入D、E、F 中,均有沉淀生成,再加入稀 HNO ,沉淀均不溶.
3
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式): A:NH •H O
3 2
或NH ;E:H SO ;F:AgNO ;C:BaCl
3 2 4 3 2
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
B:Na CO 或 K CO ,用洁净的铂丝蘸取少量 B,在酒精灯火焰中灼烧,若
2 3 2 3
第15页(共22页)焰色呈黄色则 B 为 Na CO 溶液;若透过蓝色钴玻璃观察焰色呈紫色,则 B
2 3
为K CO 溶液;
2 3
D:Al (SO ) 或 MgSO 取少量 D,向其中滴加 NaOH 溶液有沉淀生成,继
2 4 3 4
续滴加过量的 NaOH 溶液,若沉淀溶解,则 D 为 Al (SO ) 溶液,若沉淀
2 4 3
不溶解,则D 为MgSO 溶液. .
4
【考点】GS:无机物的推断.
菁优网版权所有
【专题】11:推断题;524:氮族元素;527:几种重要的金属及其化合物.
【分析】①A 有刺激性气味,用沾有浓盐酸的玻璃棒接近 A 时产生白色烟雾,
说明A 为NH •H O 或NH ;
3 2 3
②将 A 分别加入其它五种溶液中,只有 D、F 中有沉淀产生;继续加入过量 A
时,D 中沉淀无变化,可能为 Al(OH) 或 Mg(OH) ,F 中沉淀完全溶
3 2
解,则F 为AgNO ,
3
D 可能为Al (SO ) 或MgSO ;
2 4 3 4
③将 B分别加入 C、D、E、F 中,C、D、F 中产生沉淀,E中有无色、无味气
体逸出,该气体为CO ,说明 E为酸溶液,且纯E为无色油状液体,说明E
2
为H SO ;
2 4
④将 C分别加入 D、E、F 中,均有沉淀生成,再加入稀 HNO ,沉淀均不溶,
3
则该沉淀可能为 BaSO 或 AgCl,则 C应为 BaCl ,B可能为 Na CO 或
4 2 2 3
K CO .以此解答该题.
2 3
【解答】解:(1)①A 有刺激性气味,用沾有浓盐酸的玻璃棒接近 A 时产生
白色烟雾,说明A 为 NH •H O 或NH ;
3 2 3
②将 A 分别加入其它五种溶液中,只有 D、F 中有沉淀产生;继续加入过量 A
时,D 中沉淀无变化,可能为 Al(OH) 或 Mg(OH) ,F 中沉淀完全溶
3 2
解,则F 为AgNO ;
3
③将 B分别加入 C、D、E、F 中,C、D、F 中产生沉淀,E中有无色、无味气
体逸出,该气体为CO ,说明 E为酸溶液,且纯E为无色油状液体,说明E
2
为H SO ,B可能为Na CO 或K CO ;
2 4 2 3 2 3
④将 C分别加入 D、E、F 中,均有沉淀生成,再加入稀 HNO ,沉淀均不溶,
3
第16页(共22页)则该沉淀可能为BaSO 或 AgCl,则C应为BaCl ,.
4 2
根据 B、C、D 和 F 是盐溶液,且它们的阴离子均不同,D 可能为 Al (SO )
2 4 3
或MgSO ,
4
所以,能确定的是 A:NH •H O 或 NH ;E:H SO ; F:AgNO ; C:
3 2 3 2 4 3
BaCl ,
2
故答案为:A:NH •H O 或NH ;E:H SO ; F:AgNO ; C:BaCl ;
3 2 3 2 4 3 2
(2)不能确定的是 D 可能为 Al (SO ) 或 MgSO ,B可能为 Na CO 或
2 4 3 4 2 3
K CO ,
2 3
检验方法是:用洁净的铂丝蘸取少量 B,在酒精灯火焰中灼烧,若焰色呈黄色
则 B 为 Na CO 溶液;若透过蓝色钴玻璃观察焰色呈紫色,则 B为 K CO 溶
2 3 2 3
液;取少量 D,向其中滴加 NaOH 溶液有沉淀生成,继续滴加过量的 NaOH
溶液,若沉淀溶解,则 D 为 Al (SO ) 溶液,若沉淀不溶解,则 D 为
2 4 3
MgSO 溶液.
4
故答案为:B:Na CO 或 K CO ,用洁净的铂丝蘸取少量 B,在酒精灯火焰中
2 3 2 3
灼烧,若焰色呈黄色则 B为 Na CO 溶液;若透过蓝色钴玻璃观察焰色呈紫
2 3
色,则B 为K CO 溶液;
2 3
D:Al (SO ) 或 MgSO 取少量 D,向其中滴加 NaOH 溶液有沉淀生成,继
2 4 3 4
续滴加过量的 NaOH 溶液,若沉淀溶解,则 D 为 Al (SO ) 溶液,若沉淀
2 4 3
不溶解,则D 为MgSO 溶液.
4
【点评】本题考查物质的推断,题目难度中等,注意根据反应显现进行推断,
题中注意B、C、D 和F 是盐溶液,且它们的阴离子均不同.
11.请设计CO 在高温下与木炭反应生成CO 的实验.
2
(1)在下面方框中,A 表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题
卡上的 A 后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理
不分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下
方标出字母 B、C…;其他可选用的仪器(数量不限)简易表示如下:
第17页(共22页)(2)根据方框中的装置图,在答题卡上填写该表
仪器符号 仪器中所加物质 作用
A 石灰石、稀盐酸 石灰石与盐酸生成 CO
2
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下
端插入小试管中.改进后的优点是 可以通过控制加酸的量,来控制气体产
生的快慢;同时小试管中充满盐酸,可以起到液封的作用,防止反应剧烈时
气体经漏斗冲出 ;
(4)验证 CO 的方法是 点燃气体,火焰呈蓝色,再用一个内壁附着有澄清石
灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊 .
【考点】U2:性质实验方案的设计.
菁优网版权所有
【专题】16:压轴题;24:实验设计题.
【分析】(1)根据二氧化碳中氯化氢的除杂、干燥,CO 在高温下与木炭反应
2
的装置、二氧化碳的吸收等回答;
(2)根据装置的作用和实验原理选择试剂;
(3)小试管中充满盐酸,可以起到液封的作用,防止反应剧烈时气体经漏斗冲
出;
(4)一氧化碳燃烧生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
【解答】解:(1)应有二氧化碳中氯化氢的除杂、干燥,CO 在高温下与木炭
2
反 应 的 装 置 、 二 氧 化 碳 的 吸 收 装 置 等 , 装 置 图 :
第18页(共22页),
故答案为: ;
(2)B 中装有饱和碳酸氢钠溶液,其作用是除去 CO 气体中混有的少量 HCl
2
气体.C中装有浓硫酸,干燥气体,在 D 中二氧化碳与碳反应产生一氧化
碳,E中装入氢氧化钠溶液吸收多余的二氧化碳,故答案为:
仪器标号 仪器中所加物质 作用
B 饱和碳酸氢钠溶液 除去CO 中的 HCl 气体
2
C 浓硫酸 除去CO 中的水气
2
D 干燥木炭粉 与CO 反应产生 CO
2
E 氢氧化钠溶液 吸收未反应的 CO
2
;
(3)小试管中充满盐酸,可以起到液封的作用,防止反应剧烈时气体经漏斗冲
出,可以通过控制加酸的量,来控制气体产生的快慢,
故答案为:可以通过控制加酸的量,来控制气体产生的快慢;同时小试管中充
满盐酸,可以起到液封的作用,防止反应剧烈时气体经漏斗冲出;
(4)一氧化碳燃烧有蓝色火焰,生成二氧化碳,二氧化碳能使澄清的石灰水变
浑浊,
故答案为:点燃气体,火焰呈蓝色,再用一个内壁附着有澄清石灰水的烧杯罩
在火焰上,烧杯内壁的石灰水变浑浊;
【点评】本题考查性质实验方案的设计,难度不大,注意掌握实验的原理是解
题的关键.
12.有机化合物A~H 的转换关系如下所示:
第19页(共22页)请回答下列问题:
(1)链烃 A 有支链且只有一个官能团,其相对分子质量在 65~75之间,1 mol
A 完全燃烧消耗 7mol氧气,则 A 的结构简式是 ,名称
是 3﹡甲基﹡1﹡丁炔 ;
(2)在特定催化剂作用下,A 与等物质的量的 H 反应生成 E.由 E转化为 F
2
的化学方程式是 ;
(3)G 与金属钠反应能放出气体.由 G 转化为 H 的化学方程式是
;
(4)①的反应类型是 加成反应 ;③的反应类型是 水解反应或取代反
应 ;
(5)链烃 B 是 A 的同分异构体,分子中的所有碳原子共平面,其催化氢化产
物 为 正 戊 烷 , 写 出 B所 有 可 能 的 结 构 简 式
;
(6)C也是 A 的一种同分异构体,它的一氯代物只有一种(不考虑立体异
构).则C 的结构简式为 .
【考点】HB:有机物的推断.
菁优网版权所有
【专题】16:压轴题;534:有机物的化学性质及推断.
【分析】链烃 A 有支链且只有一个官能团,其相对分子质量在 65~75之间,
设 A 的分子式为 C H ,l mol A 完全燃烧消耗 7mol氧气,则 x+ ,且 65
x y
<12x+y=8x+28<75,x取正整数,所以 x=5,y=8,所以 A 的分子式为
C H ,A 含有支链且只有一个官能团,所以 A 是 3﹡甲基﹡1﹡丁炔;A 与等
5 8
第20页(共22页)物质的量的 H 反应生成 E,则 E是 3﹡甲基﹡1﹡丁烯;E和溴发生加成反应
2
生成 F,所以 F 的结构简式为: ,F 和氢氧化钠的水溶液发
生取代反应生成 G,G 的结构简式为 ,G 和 1,4﹡丁二酸反应
生成H,H 的结构简式为: .
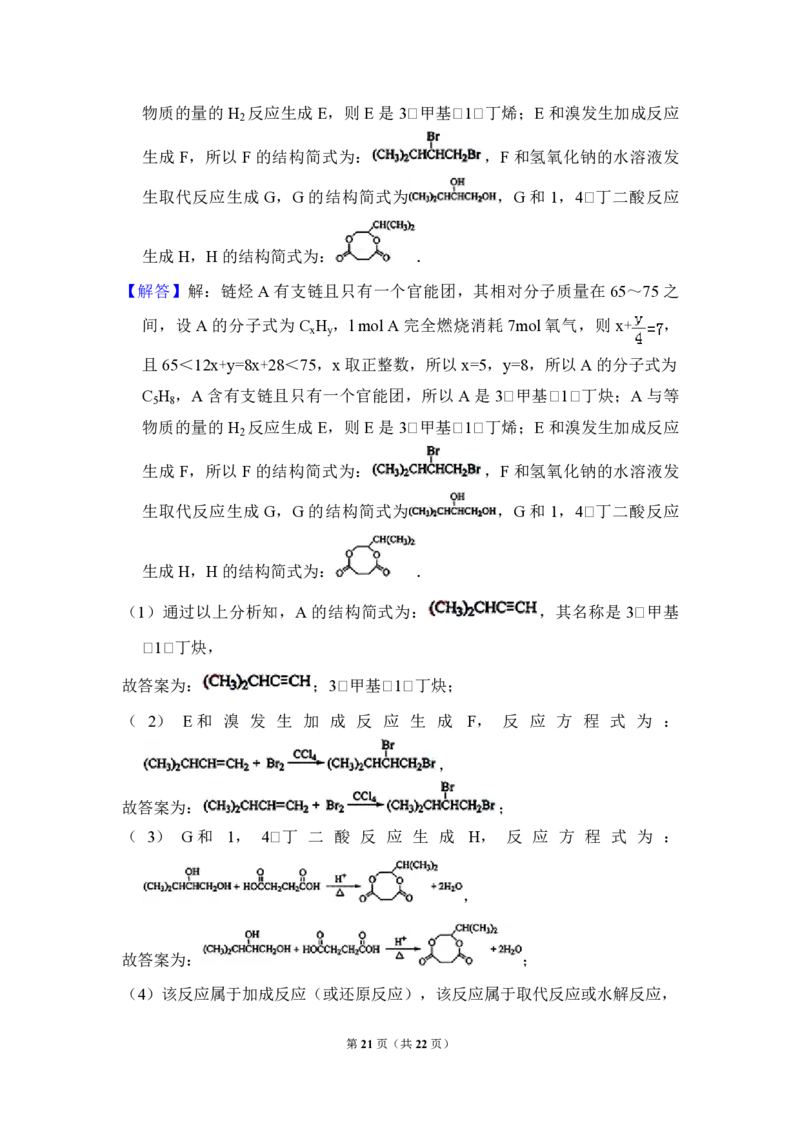
【解答】解:链烃 A 有支链且只有一个官能团,其相对分子质量在 65~75之
间,设 A 的分子式为 C H ,l mol A 完全燃烧消耗 7mol氧气,则 x+ ,
x y
且65<12x+y=8x+28<75,x取正整数,所以x=5,y=8,所以A 的分子式为
C H ,A 含有支链且只有一个官能团,所以 A 是 3﹡甲基﹡1﹡丁炔;A 与等
5 8
物质的量的 H 反应生成 E,则 E是 3﹡甲基﹡1﹡丁烯;E和溴发生加成反应
2
生成 F,所以 F 的结构简式为: ,F 和氢氧化钠的水溶液发
生取代反应生成 G,G 的结构简式为 ,G 和 1,4﹡丁二酸反应
生成H,H 的结构简式为: .
(1)通过以上分析知,A 的结构简式为: ,其名称是 3﹡甲基
﹡1﹡丁炔,
故答案为: ;3﹡甲基﹡1﹡丁炔;
( 2) E和 溴 发 生 加 成 反 应 生 成 F, 反 应 方 程 式 为 :
,
故答案为: ;
( 3) G 和 1, 4﹡丁 二 酸 反 应 生 成 H, 反 应 方 程 式 为 :
,
故答案为: ;
(4)该反应属于加成反应(或还原反应),该反应属于取代反应或水解反应,
第21页(共22页)故答案为:加成反应(或还原反应),该反应属于取代反应或水解反应;
(5)链烃 B 是 A 的同分异构体,分子中的所有碳原子共平面,其催化氢化产
物为正戊烷,则 B 中含有一个碳碳三键或两个碳碳双键,根据乙烯和乙炔的
结 构 知 , B所 有 可 能 的 结 构 简 式
,
故答案为: ;
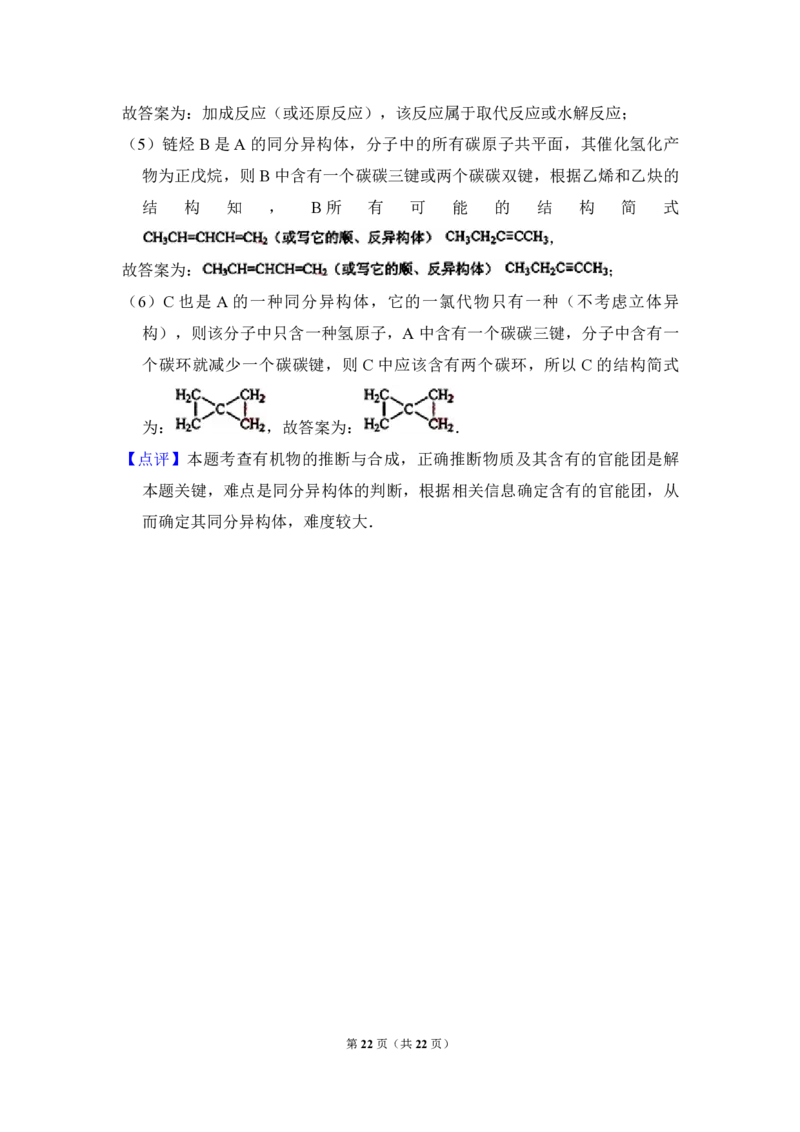
(6)C也是 A 的一种同分异构体,它的一氯代物只有一种(不考虑立体异
构),则该分子中只含一种氢原子,A 中含有一个碳碳三键,分子中含有一
个碳环就减少一个碳碳键,则 C中应该含有两个碳环,所以 C的结构简式
为: ,故答案为: .
【点评】本题考查有机物的推断与合成,正确推断物质及其含有的官能团是解
本题关键,难点是同分异构体的判断,根据相关信息确定含有的官能团,从
而确定其同分异构体,难度较大.
第22页(共22页)