文档内容
2013 年天津市高考化学试卷
一、本卷共6题,每题6分,共36分.在每题给出的四个选项中,只有一项是最符合题
目要求的.
1.(6分)运用有关概念判断下列叙述正确的是( )
A.1 mol H 燃烧放出的热量为H 的燃烧热
2 2
B.Na SO 与H O 的反应为氧化还原反应
2 3 2 2
C. 和 互为同系物
D.BaSO 的水溶液不易导电,故BaSO 是弱电解质
4 4
2.(6分)以下食品化学知识的叙述不正确的是( )
A.食盐可作调味剂,也可作食品防腐剂
B.新鲜蔬菜做熟后,所含维生素C会有损失
C.纤维素在人体内可水解为葡萄糖,故可作人类的营养物质
D.葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒
3.(6分)下列有关元素的性质及其递变规律正确的是( )
A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
4.(6分)下列实验误差分析错误的是( )
A.用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
5.(6分)下列有关电解质溶液的说法正确的是( )
A.在蒸馏水中滴加浓H SO ,K 不变
2 4 w
B.CaCO 难溶于稀硫酸,也难溶于醋酸
3
C.在Na S稀溶液中,c(H+)=c(OH﹣)﹣2c(H S)﹣c(HS﹣)
2 2
D.NaCl溶液和CH COONH 溶液均显中性,两溶液中水的电离程度相同
3 4
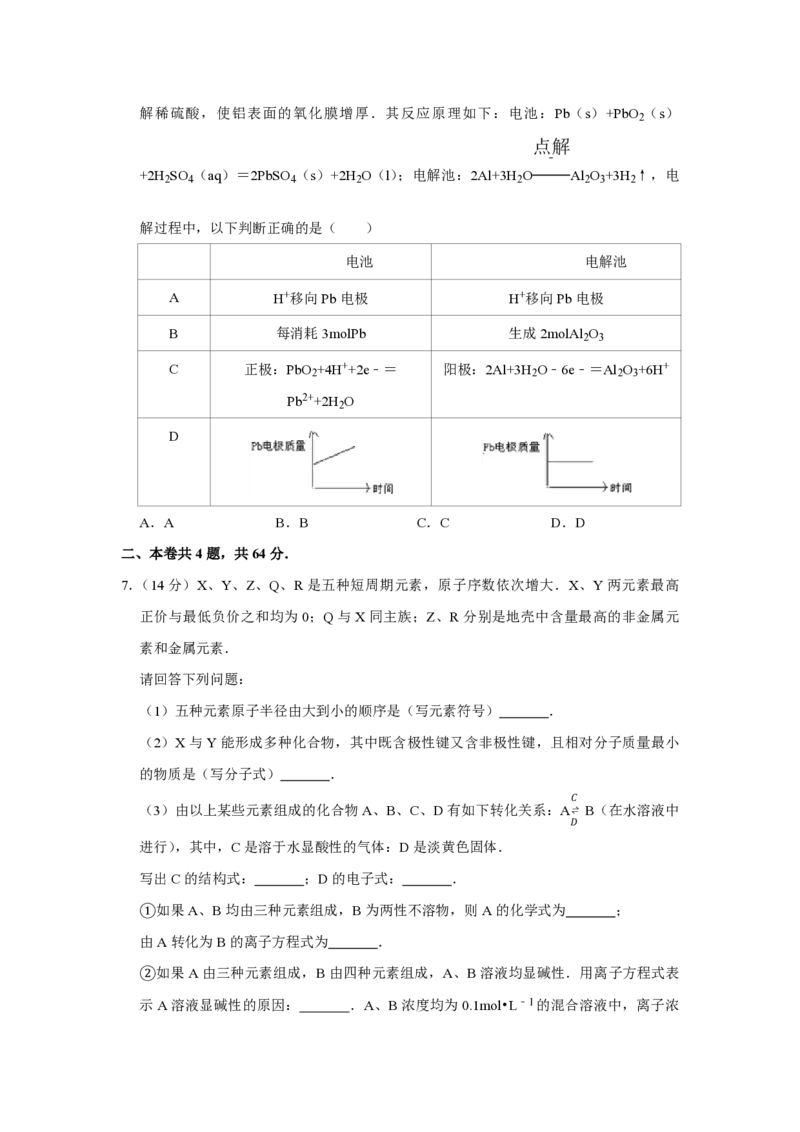
6.(6分)为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.其反应原理如下:电池:Pb(s)+PbO (s)
2
点解
¯
+2H SO (aq)=2PbSO (s)+2H O(l);电解池:2Al+3H O Al O +3H ↑,电
2 4 4 2 2 2 3 2
解过程中,以下判断正确的是( )
电池 电解池
A H+移向Pb电极 H+移向Pb电极
B 每消耗3molPb 生成2molAl O
2 3
C 正极:PbO +4H++2e﹣= 阳极:2Al+3H O﹣6e﹣=Al O +6H+
2 2 2 3
Pb2++2H O
2
D
A.A B.B C.C D.D
二、本卷共4题,共64分.
7.(14分)X、Y、Z、Q、R是五种短周期元素,原子序数依次增大.X、Y两元素最高
正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元
素和金属元素.
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) .
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小
的物质是(写分子式) .
𝐶
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A⇌ B(在水溶液中
𝐷
进行),其中,C是溶于水显酸性的气体:D是淡黄色固体.
写出C的结构式: ;D的电子式: .
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;
由A转化为B的离子方程式为 .
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性.用离子方程式表
示A溶液显碱性的原因: .A、B浓度均为0.1mol•L﹣1的混合溶液中,离子浓度由大到小的顺序是 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要
成分有 .
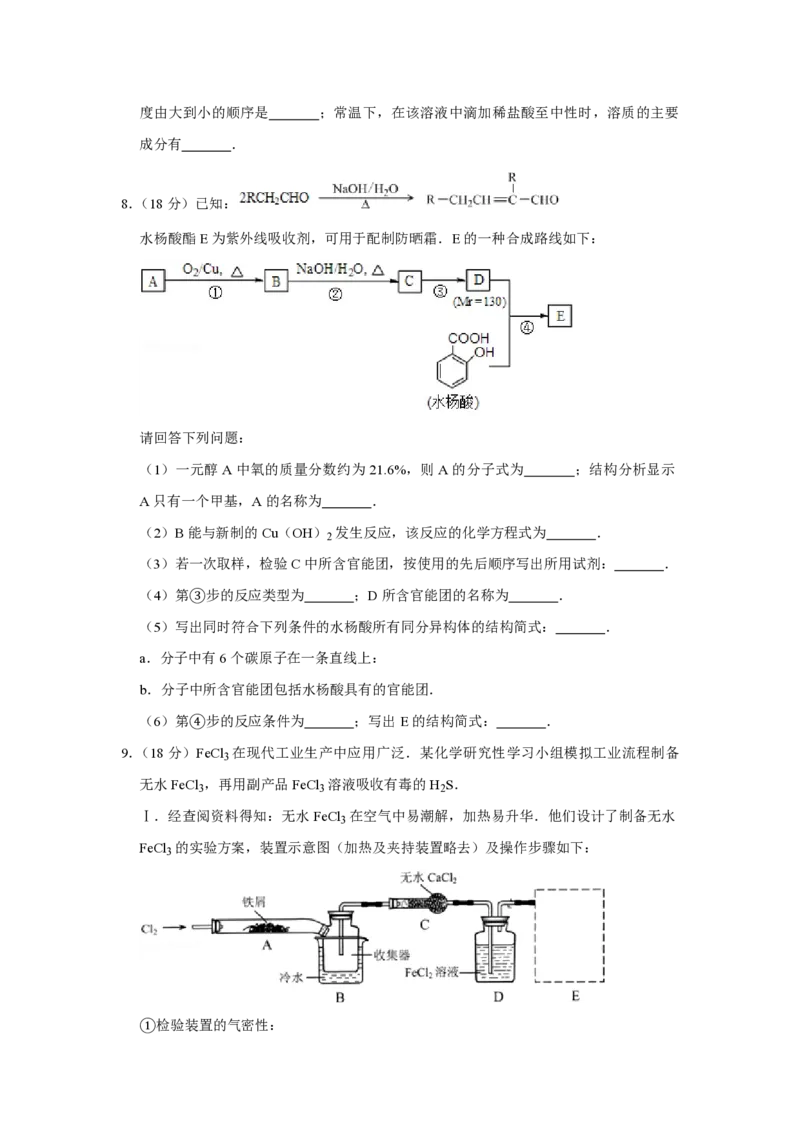
8.(18分)已知:
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为 ;结构分析显示
A只有一个甲基,A的名称为 .
(2)B能与新制的Cu(OH) 发生反应,该反应的化学方程式为 .
2
(3)若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂: .
(4)第③步的反应类型为 ;D所含官能团的名称为 .
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式: .
a.分子中有6个碳原子在一条直线上:
b.分子中所含官能团包括水杨酸具有的官能团.
(6)第④步的反应条件为 ;写出E的结构简式: .
9.(18分)FeCl 在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备
3
无水FeCl ,再用副产品FeCl 溶液吸收有毒的H S.
3 3 2
Ⅰ.经查阅资料得知:无水FeCl 在空气中易潮解,加热易升华.他们设计了制备无水
3
FeCl 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
3
①检验装置的气密性:②通入干燥的Cl ,赶尽装置中的空气;
2
⑨用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl ,并用干燥的N 赶尽Cl ,将收集器密封.
2 2 2
请回答下列问题:
(1)装置A中反应的化学方程式为 .
(2)第③步加热后,生成的烟状 FeCl 大部分进入收集器,少量沉积在反应管 A右
3
端.要使沉积的FeCl 进入收集器,第④步操作是 .
3
(3)操作步骤中,为防止FeCl 潮解所采取的措施有(填步骤序号) .
3
(4)装置B中冷水浴的作用为 ;装置C的名称为 ;装置D中FeCl 全
2
部反应后,因失去吸收Cl 的作用而失效,写出检验FeCl 是否失效的试剂: .
2 2
(5)在虚线框中画出尾气吸收装置E并注明试剂.
Ⅱ.该组同学用装置D中的副产品FeCl 溶液吸收H S,得到单质硫;过滤后,再以石
3 2
墨为电极,在一定条件下电解滤液.
(6)FeCl 与H S反应的离子方程式为 .
3 2
(7)电解池中H+在阴极放电产生H ,阳极的电极反应式为 .
2
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:
①H S的原子利用率为100%;② .
2
10.(14分)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM (直径小于
2.5
等于 2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对 PM 、
2.5
SO 、NO 等进行研究具有重要意义。
2 x
请回答下列问题:
(1)将PM 样本用蒸馏水处理制成待测试样。
2.5
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 K+ Na+ NH + SO 2﹣ NO ﹣ Cl﹣
4 4 3
浓度/mol•L﹣1 4×10﹣6 6×10﹣6 2×10﹣5 4×10﹣5 3×10﹣5 2×10﹣5
根据表中数据判断PM 的酸碱性为 ,试样的pH= 。
2.5
(2)为减少SO 的排放,常采取的措施有:
2
①将煤转化为清洁气体燃料。1
已知:H (g) + O (g)=H O(g);△H=﹣241.81kJ•mol﹣1
2 2 2
2
1
C (s) + O (g)=CO (g);△H=﹣110.51kJ•mol﹣1
2
2
写出焦炭与水蒸气反应的热化学方程式: 。
②洗涤含SO 的烟气。以下物质可作洗涤剂的是 。
2
a.Ca(OH) b.Na CO c.CaCl d.NaHSO
2 2 3 2 3
(3)汽车尾气中NO 和CO的生成及转化
x
①已知汽缸中生成NO的反应为:N (g)+O (g)⇌2NO (g);△H>0
2 2
若 1mol空气含 0.8mol N 和 0.2mol O ,1300℃时在密闭容器内反应达到平衡,测得
2 2
NO为:8×10﹣4 mol.计算该温度下的平衡常数:K= 。
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
②汽车燃油不完全燃烧时产生 CO,有人设想按下列反应除去 CO:2CO (g)=2C
(s)+O (g)
2
已知该反应的△H>0,简述该设想能否实现的依据: 。
③目前,在汽车尾气系统中安装催化转化器可减少CO和NO的污染,其化学反应方程
式为 。