文档内容
2016年普通高等学校招生全国统一考试(四川卷)
理科综合化学部分
1.化学与生产和生活密切相关。下列过程中没有发生化学变化的是
A.氯气作水杀菌消毒剂
B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂
D.肥皂水作蚊虫叮咬处的清洗剂
2.根据下列实验操作和现象得出的结论正确的是
选项 实验操作 现象 结论
A 将某溶液与稀盐酸反应产生的 石灰水变浑浊 该溶液中一定含有
气体通入澄清石灰水 CO 2-
3
B 常温下,将铁片浸入足量浓硫 铁片不溶解 常温下,铁与浓硫酸
酸中 钠一定没有发生化学
反应
C 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 该食盐中一定没有添
加碘化钾
D 向苯酚钠溶液中滴加乙酸溶液 溶液变浑浊 相同条件下,乙酸的
酸性一定比苯酚强
3.下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在H+、Cl-、MnO -
4
B.pH=2的溶液中可能大量存在Na+、NH +、SiO 2-
4 3
C.Fe2+与H O 在酸性溶液中的反应:2Fe2++H O +2H+=2Fe3++2H O
2 2 2 2 2
D.稀硫酸和氢氧化钡溶液反应:H++SO 2-+Ba2++OH-=BaSO ↓+H O
4 4 2
4.N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.2.4g镁在足量的氧气中燃烧,转移的电子数为0.1N
A
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5N
A
C.氢原子数为0.4N 的甲醇分子中含有的σ键数为0.4N
A A
D.0.1L0.5mol/LCH COOH溶液中含有的氢离子数为0.05N
3 A
5.某电动汽车配载一种可充放电的锂离子电池。放电时电池的总反应为: Li
1-
CoO +LiC =LiCoO + C (x<1)。下列关于该电池的说法不正确的是
x 2 x 6 2 6
A.放电时,Li+在电解质中由负极向正极迁移B.放电时,负极的电极反应式为LiC -xe-= xLi++ C
x 6 6
C.充电时,若转移1mole-,石墨C 电极将增重7xg
6
D.充电时,阳极的电极反应式为LiCoO -xe-=Li CoO +Li+
2 1-x 2
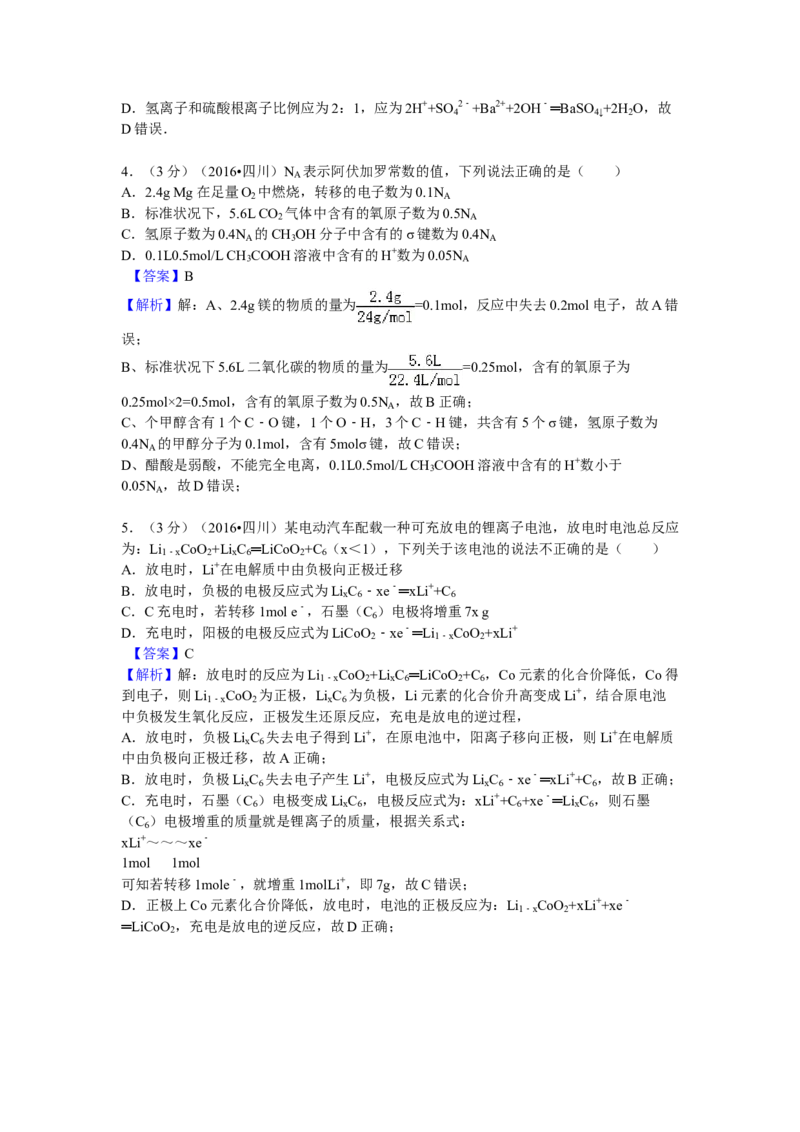
6.一定条件下,CH 与H O(g)发生反应:CH (g)+H O(g) CO(g)+3H (g)设起始
4 2 4 2 2
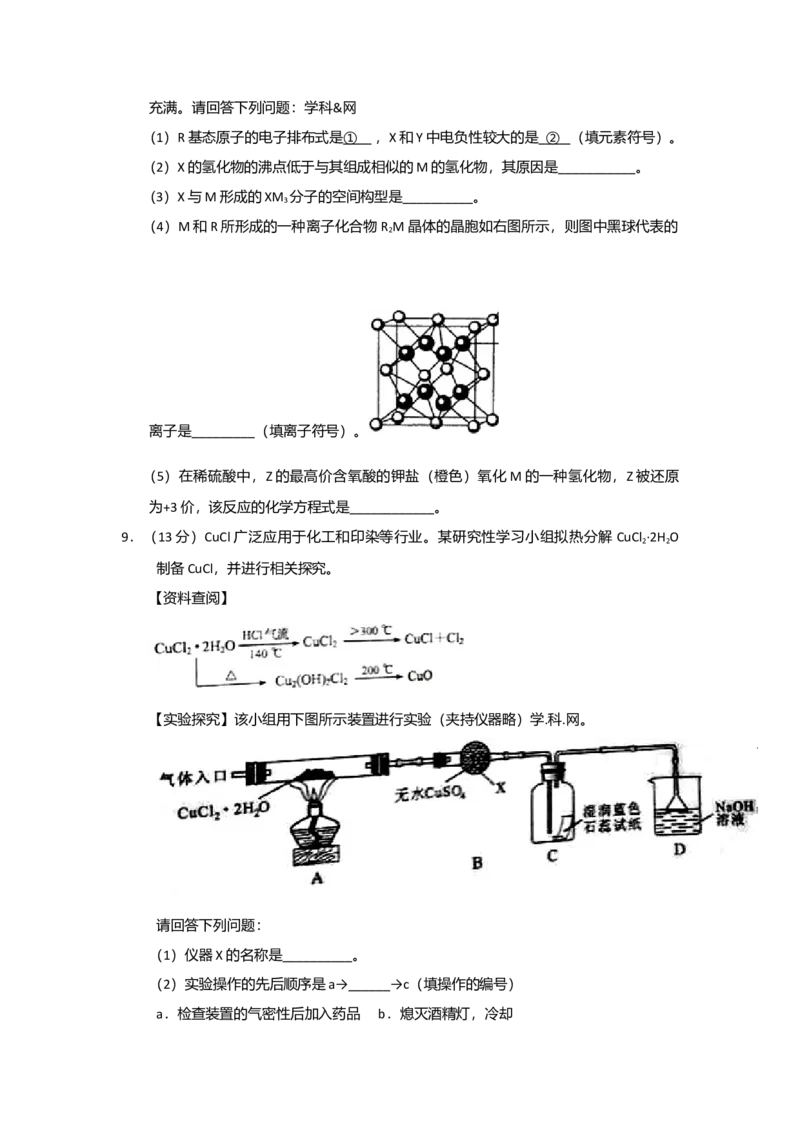
=Z,在恒压下,平衡时 (CH )的体积分数与Z和T(温度)的关系如图所示。下列说
4
法正确的是
A.该反应的焓变△H>0
B..图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中 =3
D.温度不变时,图中X点对应的平衡在加压后 (CH )减小
4
7.向1L含0.01molNaAlO 和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO )增大,先
2 2
后发生三个不同的反应,当0.01molc(AlO -)+c(OH-)
2
B 0.01 c(Na+)>c(AlO -)> c(OH-)>c(CO 2-)
2 3
C 0.015 c(Na+)> c(HCO -)>c(CO 2-)> c(OH-)
3 3
D 0.03 c(Na+)> c(HCO -)> c(OH-)>c(H+)
3
8.(13分)M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M
基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,
X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:学科&网
(1)R基态原子的电子排布式是 ① ,X和Y中电负性较大的是 ② (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________。
(3)X与M形成的XM 分子的空间构型是__________。
3
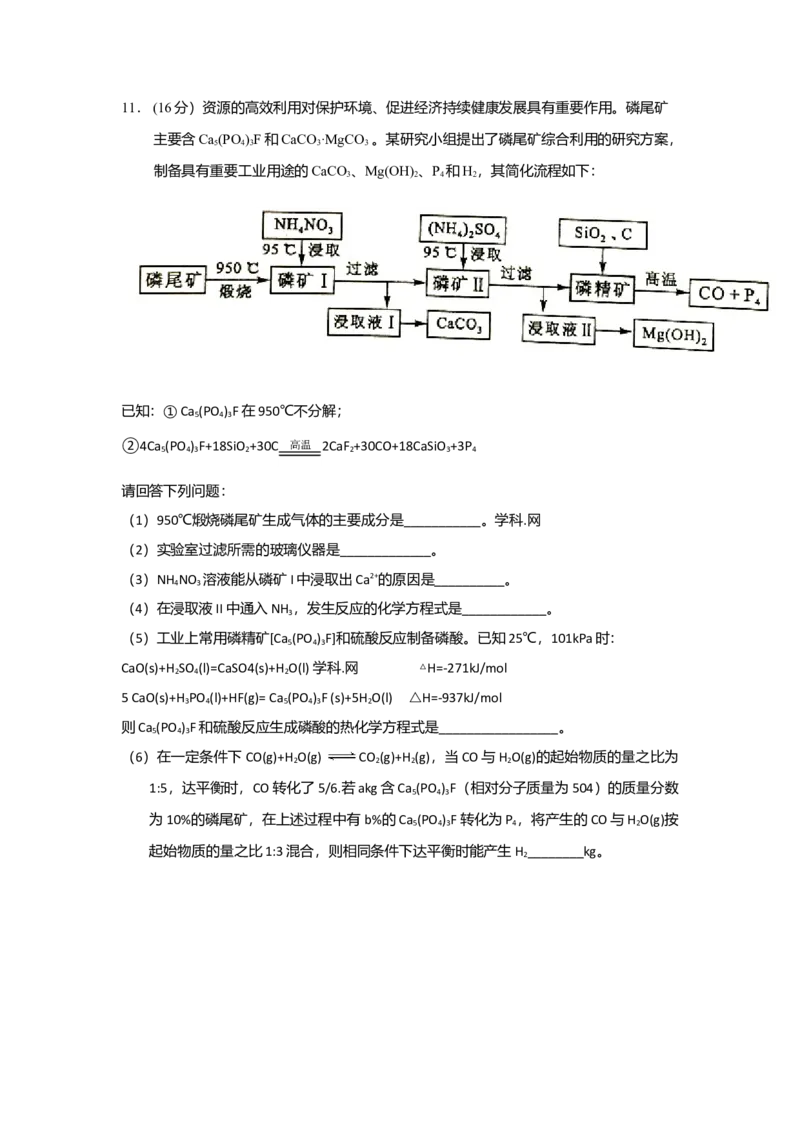
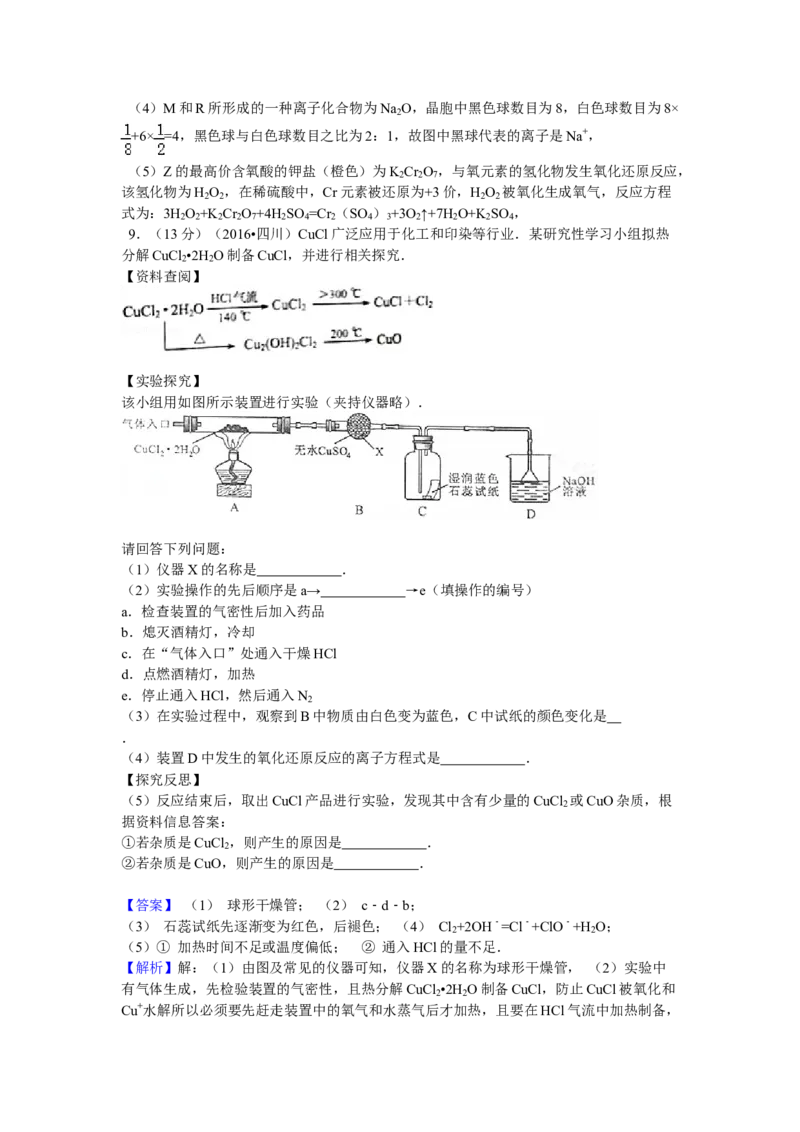
(4)M和R所形成的一种离子化合物R M晶体的晶胞如右图所示,则图中黑球代表的
2
离子是_________(填离子符号)。
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原
为+3价,该反应的化学方程式是____________。
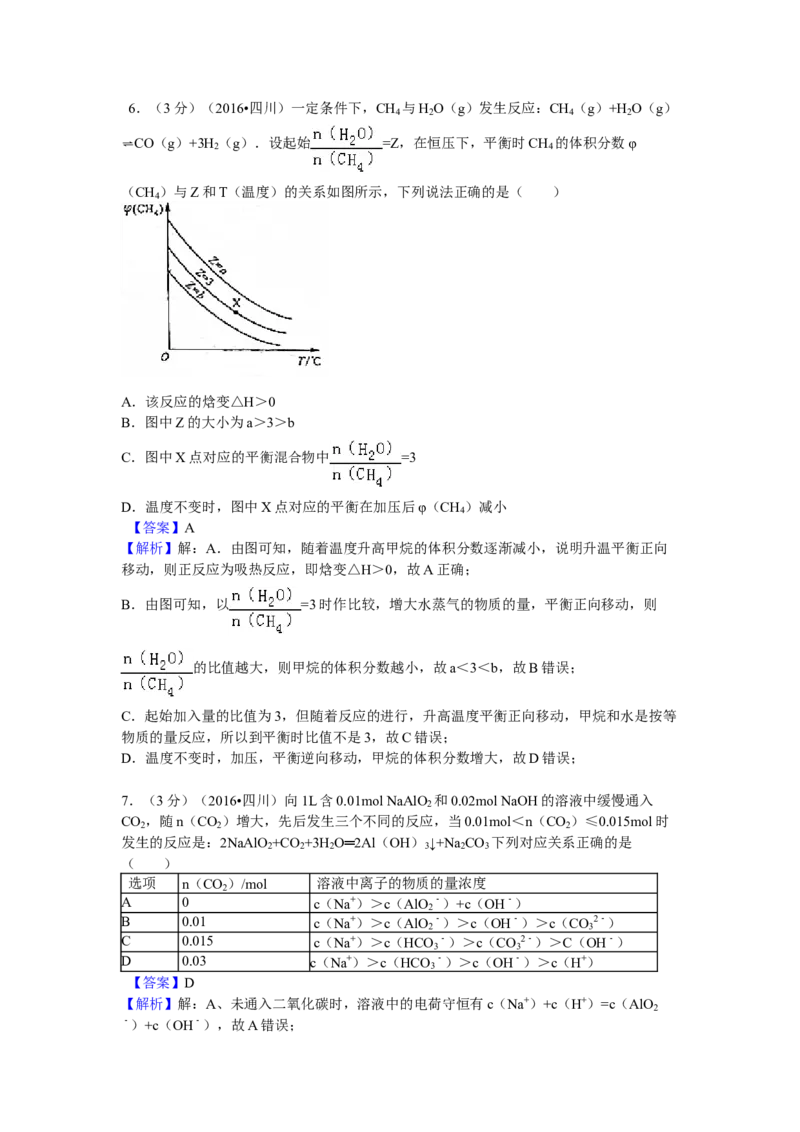
9.(13分)CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解 CuCl ·2H O
2 2
制备CuCl,并进行相关探究。
【资料查阅】
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)学.科.网。
请回答下列问题:
(1)仪器X的名称是__________。
(2)实验操作的先后顺序是a→______→c(填操作的编号)
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却c.在“气体入口”处干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N
2
(3)在实验过程中,观察到 B 中物质由白色变为蓝色,C 中试纸的颜色变化是
_______。
(4)装置D中发生的氧化还原反应的离子方程式是________________。
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl 或CuO杂质,
2
根据资料信息分析:
①若杂质是CuCl ,则产生的原因是________________。
2
②若杂质是CuO,则产生的原因是________________。
10.(16分)高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合
成路线如下(部分反应条件和试剂略):学.科.网
请回答下列问题:
(1)试剂I的名称是____a____,试剂II中官能团的名称是____b___,第② 步的反应类型
是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH(CH)OH。若X含有羧基和苯
3 2 4
环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所
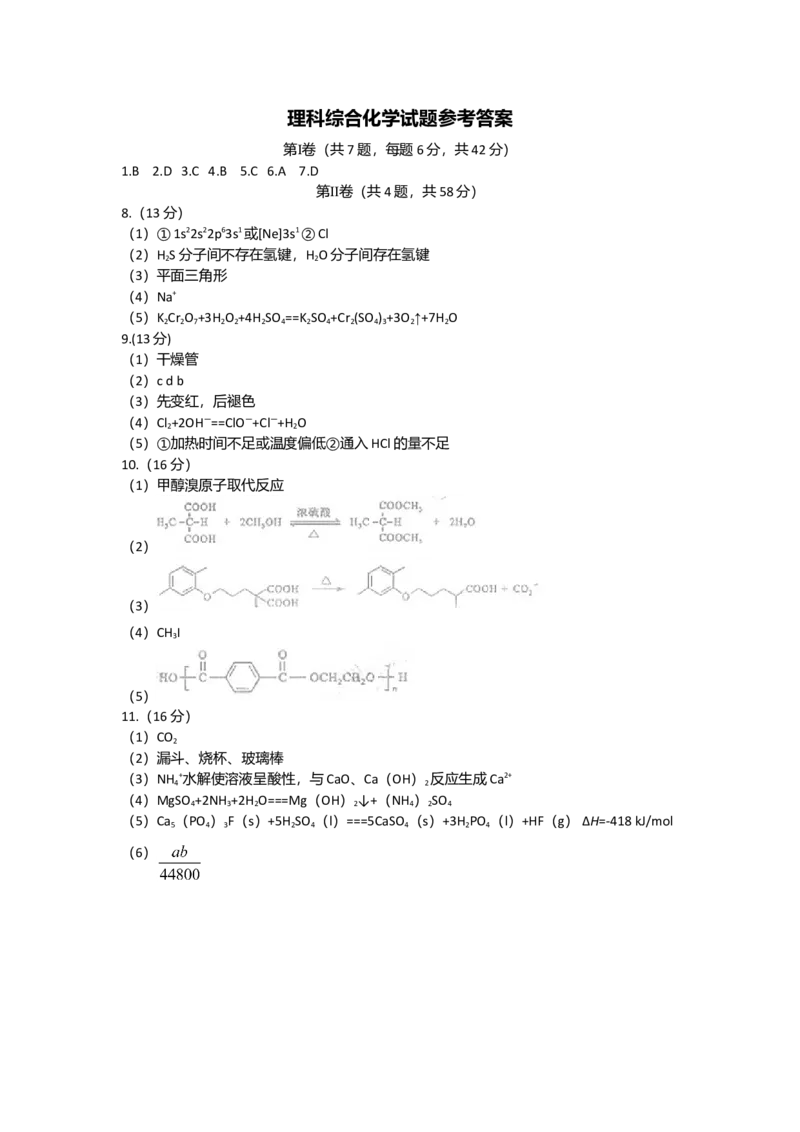
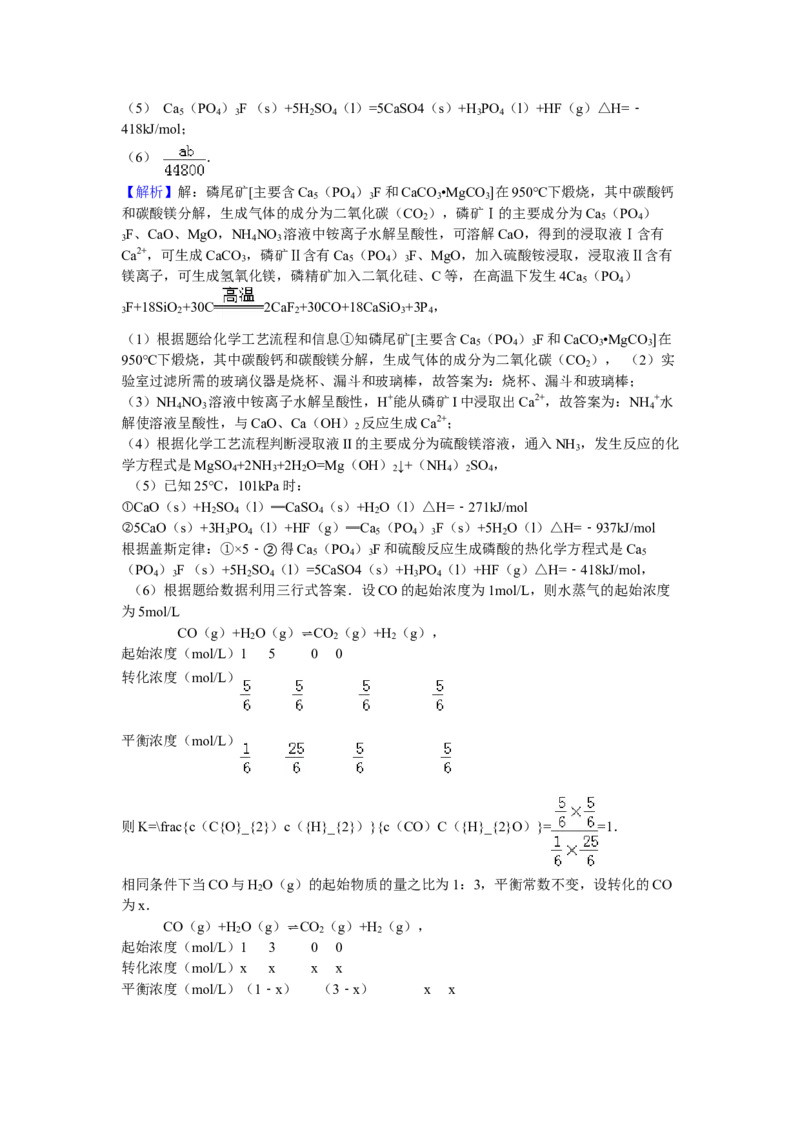
得缩聚物的结构简式是___________。11. (16分)资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿
主要含Ca (PO )F和CaCO ·MgCO 。某研究小组提出了磷尾矿综合利用的研究方案,
5 4 3 3 3
制备具有重要工业用途的CaCO 、Mg(OH) 、P 和H,其简化流程如下:
3 2 4 2
已知:①Ca (PO ) F在950℃不分解;
5 4 3
②4Ca (PO ) F+18SiO +30C 高温 2 CaF +30CO+18CaSiO +3P
5 4 3 2 2 3 4
请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是___________。学科.网
(2)实验室过滤所需的玻璃仪器是_____________。
(3)NH NO 溶液能从磷矿I中浸取出Ca2+的原因是__________。
4 3
(4)在浸取液II中通入NH ,发生反应的化学方程式是____________。
3
(5)工业上常用磷精矿[Ca (PO ) F]和硫酸反应制备磷酸。已知25℃,101kPa时:
5 4 3
CaO(s)+H SO (l)=CaSO4(s)+H O(l) 学科.网 △H=-271kJ/mol
2 4 2
5 CaO(s)+H PO (l)+HF(g)= Ca (PO ) F (s)+5H O(l) △H=-937kJ/mol
3 4 5 4 3 2
则Ca (PO ) F和硫酸反应生成磷酸的热化学方程式是_________________。
5 4 3
(6)在一定条件下CO(g)+H O(g) CO (g)+H (g),当CO与H O(g)的起始物质的量之比为
2 2 2 2
1:5,达平衡时,CO转化了5/6.若akg含Ca (PO ) F(相对分子质量为504)的质量分数
5 4 3
为10%的磷尾矿,在上述过程中有b%的Ca (PO ) F转化为P ,将产生的CO与H O(g)按
5 4 3 4 2
起始物质的量之比1:3混合,则相同条件下达平衡时能产生H ________kg。
2理科综合化学试题参考答案
第Ⅰ卷(共7题,每题6分,共42分)
1.B 2.D 3.C 4.B 5.C 6.A 7.D
第Ⅱ卷(共4题,共58分)
8.(13分)
(1)①1s22s22p63s1或[Ne]3s1②Cl
(2)H S分子间不存在氢键,H O分子间存在氢键
2 2
(3)平面三角形
(4)Na+
(5)K Cr O +3H O +4H SO ==K SO +Cr (SO ) +3O ↑+7H O
2 2 7 2 2 2 4 2 4 2 4 3 2 2
9.(13分)
(1)干燥管
(2)c d b
(3)先变红,后褪色
(4)Cl +2OH—==ClO—+Cl—+H O
2 2
(5)①加热时间不足或温度偏低②通入HCl的量不足
10.(16分)
(1)甲醇溴原子取代反应
(2)
(3)
(4)CH I
3
(5)
11.(16分)
(1)CO
2
(2)漏斗、烧杯、玻璃棒
(3)NH +水解使溶液呈酸性,与CaO、Ca(OH) 反应生成Ca2+
4 2
(4)MgSO +2NH +2H O===Mg(OH) ↓+(NH ) SO
4 3 2 2 4 2 4
(5)Ca (PO ) F(s)+5H SO (l)===5CaSO (s)+3H PO (l)+HF(g) ΔH=-418 kJ/mol
5 4 3 2 4 4 2 4
(6)2016 年四川省高考化学试卷
一、选择题(共7小题,每小题3分,满分21分)
1.(3分)(2016•四川)化学与生产和生活密切相关,下列过程中没有发生化学变化的是
( )
A.氯气作水的杀菌消毒剂 B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂 D.肥皂水作蚊虫叮咬处的清洗剂
【答案】 B
【解析】解:A、氯气和水反应生成盐酸和次氯酸,次氯酸具有强氧化性,能杀菌消毒,
属于化学变化,故A错误;
B、硅胶做干燥剂是吸水,没有发生化学变化,故B正确;
C、二氧化硫和有色物质化合使之生成无色物质,发生了化学反应,属于化学变化,故C
错误;
D、肥皂水显碱性,与蚊虫叮咬处释放的酸发生中和反应,发生了化学反应,故D错误.
2.(3分)(2016•四川)根据下列实验操作和现象得出的结论正确的是( )
选项 实验操作 现象 结论
A 将某溶液与稀盐酸反应产生的 石灰水变浑浊 该溶液中一定含有CO 2﹣
3
气体通入澄清石灰水
B 常温下,将铁片浸入足量浓硫 铁片不溶解 常温下,铁与浓硫酸一定没有发生化
酸中 学反应
C 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 该食盐中一定没有添加KIO
3
D 向苯酚钠溶液滴加乙酸溶液 溶液变浑浊 相同条件下,乙酸的酸性一定比苯酚
强
【答案】D
【解析】解:A.和稀盐酸反应生成能使澄清石灰水变浑浊的气体的离子还有HCO ﹣等,
3
所以该实验不一定含有CO 2﹣,故A错误;
3
B.铁在常温下和浓硫酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步反应,
该现象为钝化,发生了化学反应,故B错误;
C.碘酸钾和淀粉不反应,碘单质遇到淀粉显蓝色,故C错误;
D.强酸能和弱酸盐反应生成弱酸,苯酚在常温下溶解度很小,向苯酚钠溶液滴加乙酸溶
液,溶液变浑浊,说明生成苯酚,则乙酸酸性大于苯酚,故D正确;
3.(3分)(2016•四川)下列关于离子共存或离子反应的说法正确的是( )
A.某无色溶液中可能大量存在H+、Cl﹣、MnO ﹣
4
B.pH=2的溶液中可能大量存在Na+、NH +、SiO 2﹣
4 3
C.Fe2+与H O 在酸性溶液中的反应:2Fe2++H O +2H+═2Fe3++2H O
2 2 2 2 2
D.稀硫酸与Ba(OH) 溶液的反应:H++SO 2﹣+Ba2++OH﹣═BaSO +2H O
2 4 4↓ 2
优网版权所有
【答案】C
【解析】解:A.MnO ﹣是紫色,不可能存在无色溶液中,故A错误;
4
B.pH=2的溶液呈酸性,硅酸根离子和氢离子反应生成硅酸沉淀,故B错误;
C.Fe2+与H O 在酸性溶液中发生氧化还原反应,生成铁离子和水,反应的离子方程式
2 2
2Fe2++H O +2H+═2Fe3++2H O满足电子守恒和电荷守恒,故C正确;
2 2 2D.氢离子和硫酸根离子比例应为2:1,应为2H++SO 2﹣+Ba2++2OH﹣═BaSO +2H O,故
4 4↓ 2
D错误.
4.(3分)(2016•四川)N 表示阿伏加罗常数的值,下列说法正确的是( )
A
A.2.4g Mg在足量O 中燃烧,转移的电子数为0.1N
2 A
B.标准状况下,5.6L CO 气体中含有的氧原子数为0.5N
2 A
C.氢原子数为0.4N 的CH OH分子中含有的σ键数为0.4N
A 3 A
D.0.1L0.5mol/L CH COOH溶液中含有的H+数为0.05N
3 A
【答案】B
【解析】解:A、2.4g镁的物质的量为 =0.1mol,反应中失去0.2mol电子,故A错
误;
B、标准状况下5.6L二氧化碳的物质的量为 =0.25mol,含有的氧原子为
0.25mol×2=0.5mol,含有的氧原子数为0.5N ,故B正确;
A
C、个甲醇含有1个C﹣O键,1个O﹣H,3个C﹣H键,共含有5个σ键,氢原子数为
0.4N 的甲醇分子为0.1mol,含有5molσ键,故C错误;
A
D、醋酸是弱酸,不能完全电离,0.1L0.5mol/L CH COOH溶液中含有的H+数小于
3
0.05N ,故D错误;
A
5.(3分)(2016•四川)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应
为:Li CoO +Li C ═LiCoO +C (x<1),下列关于该电池的说法不正确的是( )
1﹣x 2 x 6 2 6
A.放电时,Li+在电解质中由负极向正极迁移
B.放电时,负极的电极反应式为Li C ﹣xe﹣═xLi++C
x 6 6
C.C充电时,若转移1mol e﹣,石墨(C )电极将增重7x g
6
D.充电时,阳极的电极反应式为LiCoO ﹣xe﹣═Li CoO +xLi+
2 1﹣x 2
【答案】C
【解析】解:放电时的反应为Li CoO +Li C ═LiCoO +C ,Co元素的化合价降低,Co得
1﹣x 2 x 6 2 6
到电子,则Li CoO 为正极,Li C 为负极,Li元素的化合价升高变成Li+,结合原电池
1﹣x 2 x 6
中负极发生氧化反应,正极发生还原反应,充电是放电的逆过程,
A.放电时,负极Li C 失去电子得到Li+,在原电池中,阳离子移向正极,则Li+在电解质
x 6
中由负极向正极迁移,故A正确;
B.放电时,负极Li C 失去电子产生Li+,电极反应式为Li C ﹣xe﹣═xLi++C ,故B正确;
x 6 x 6 6
C.充电时,石墨(C )电极变成Li C ,电极反应式为:xLi++C +xe﹣═Li C ,则石墨
6 x 6 6 x 6
(C )电极增重的质量就是锂离子的质量,根据关系式:
6
xLi+~~~xe﹣
1mol 1mol
可知若转移1mole﹣,就增重1molLi+,即7g,故C错误;
D.正极上Co元素化合价降低,放电时,电池的正极反应为:Li CoO +xLi++xe﹣
1﹣x 2
═LiCoO ,充电是放电的逆反应,故D正确;
26.(3分)(2016•四川)一定条件下,CH 与H O(g)发生反应:CH (g)+H O(g)
4 2 4 2
⇌CO(g)+3H
2
(g).设起始 =Z,在恒压下,平衡时CH
4
的体积分数φ
(CH )与Z和T(温度)的关系如图所示,下列说法正确的是( )
4
A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中 =3
D.温度不变时,图中X点对应的平衡在加压后φ(CH )减小
4
【答案】A
【解析】解:A.由图可知,随着温度升高甲烷的体积分数逐渐减小,说明升温平衡正向
移动,则正反应为吸热反应,即焓变△H>0,故A正确;
B.由图可知,以 =3时作比较,增大水蒸气的物质的量,平衡正向移动,则
的比值越大,则甲烷的体积分数越小,故a<3<b,故B错误;
C.起始加入量的比值为3,但随着反应的进行,升高温度平衡正向移动,甲烷和水是按等
物质的量反应,所以到平衡时比值不是3,故C错误;
D.温度不变时,加压,平衡逆向移动,甲烷的体积分数增大,故D错误;
7.(3分)(2016•四川)向1L含0.01mol NaAlO 和0.02mol NaOH的溶液中缓慢通入
2
CO ,随n(CO )增大,先后发生三个不同的反应,当0.01mol<n(CO )≤0.015mol时
2 2 2
发生的反应是:2NaAlO +CO +3H O═2Al(OH) ↓+Na CO 下列对应关系正确的是
2 2 2 3 2 3
( )
选项 n(CO )/mol 溶液中离子的物质的量浓度
2
A 0 c(Na+)>c(AlO ﹣)+c(OH﹣)
2
B 0.01 c(Na+)>c(AlO ﹣)>c(OH﹣)>c(CO 2﹣)
2 3
C 0.015 c(Na+)>c(HCO ﹣)>c(CO 2﹣)>C(OH﹣)
3 3
D 0.03 c(Na+)>c(HCO ﹣)>c(OH﹣)>c(H+)
3
【答案】D
【解析】解:A、未通入二氧化碳时,溶液中的电荷守恒有c(Na+)+c(H+)=c(AlO
2
﹣)+c(OH﹣),故A错误;B、当二氧化碳为0.01mol,所得溶液为0.01mol碳酸钠和0.01mol偏铝酸钠,因为碳酸酸
性强于氢氧化铝,所以偏铝酸根离子水解程度比碳酸根离子强,则偏铝酸根离子浓度小于
碳酸根离子浓度,所以溶液中离子的物质的量浓度大小为:c(Na+)>c(OH﹣)>c
(CO 2﹣)>c(AlO ﹣),故B错误;
3 2
C、当二氧化碳为0.015mol时,所以得溶液为0.015mol碳酸钠,溶液中离子浓度的关系为
c(Na+)>c(CO 2﹣)>c(OH﹣)>c(HCO ﹣),故C错误;
3 3
D、当二氧化碳的量为0.03mol时,所得溶质为碳酸氢钠,水解程度大于电离程度,溶液显
碱性,所以离子浓度大小顺序为:c(Na+)>c(HCO ﹣)>c(OH﹣)>c(H+),D正确;
3
二、解答题(共4小题,满分13分)
8.(2016•四川)M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元
素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元
素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道
半充满.请回答下列问题:
(1)R基态原子的电子排布式是 ,X和Y中电负性较大的是
(填元素符号).
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是 .
(3)X与M形成的XM 分子的空间构型是 .
3
(4)M和R所形成的一种离子化合物R M晶体的晶胞如图所示,则图中黑球代表的离子
2
是 (填离子符号).
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3
价,该反应的化学方程式是 .
【答案】(1) 1s22s22p63s1;Cl; (2) H O分子能形成氢键,而H S不能形成氢键;
2 2
(3) 平面三角形; (4) Na+;
(5) 3H O +K Cr O +4H SO =Cr (SO ) +3O ↑+7H O+K SO .
2 2 2 2 7 2 4 2 4 3 2 2 2 4
【解析】解:M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.
M基态原子L层中p轨道电子数是s电子数的2倍,核外电子排布式为1s22s22p4,故M为
O元素;由原子序数可知R、X、Y均处于第三周期,R是同周期元素中最活泼的金属元素,
则R为Na;X和M形成的一种化合物是引起酸雨的主要大气污染物,则X为S元素,可
知Y为Cl;Z的基态原子4s和3d轨道半充满,外围电子排布式为3d54s1,处于VIB族,
故Z为Cr.
(1)R为Na,基态原子的电子排布式是1s22s22p63s1,同周期自左而右电负性增大,故Cl
元素电负性大于S的,
(2)H O分子能形成氢键,使水的沸点升高,而H S不能形成氢键,故硫化氢的沸点低
2 2
于水的,
(3)X与M形成的SO 分子中S原子孤电子对数= =0,价层电子对数为
3
3+0=3,故其空间构型为平面三角形,(4)M和R所形成的一种离子化合物为Na O,晶胞中黑色球数目为8,白色球数目为8×
2
+6× =4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+,
(5)Z的最高价含氧酸的钾盐(橙色)为K Cr O ,与氧元素的氢化物发生氧化还原反应,
2 2 7
该氢化物为H O ,在稀硫酸中,Cr元素被还原为+3价,H O 被氧化生成氧气,反应方程
2 2 2 2
式为:3H O +K Cr O +4H SO =Cr (SO ) +3O ↑+7H O+K SO ,
2 2 2 2 7 2 4 2 4 3 2 2 2 4
9.(13分)(2016•四川)CuCl广泛应用于化工和印染等行业.某研究性学习小组拟热
分解CuCl •2H O制备CuCl,并进行相关探究.
2 2
【资料查阅】
【实验探究】
该小组用如图所示装置进行实验(夹持仪器略).
请回答下列问题:
(1)仪器X的名称是 .
(2)实验操作的先后顺序是a→ →e(填操作的编号)
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N
2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是
.
(4)装置D中发生的氧化还原反应的离子方程式是 .
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl 或CuO杂质,根
2
据资料信息答案:
①若杂质是CuCl ,则产生的原因是 .
2
②若杂质是CuO,则产生的原因是 .
【答案】 (1) 球形干燥管; (2) c﹣d﹣b;
(3) 石蕊试纸先逐渐变为红色,后褪色; (4) Cl +2OH﹣=Cl﹣+ClO﹣+H O;
2 2
(5)① 加热时间不足或温度偏低; ② 通入HCl的量不足.
【解析】解:(1)由图及常见的仪器可知,仪器X的名称为球形干燥管, (2)实验中
有气体生成,先检验装置的气密性,且热分解CuCl •2H O制备CuCl,防止CuCl被氧化和
2 2
Cu+水解所以必须要先赶走装置中的氧气和水蒸气后才加热,且要在HCl气流中加热制备,反应结束后先熄灭酒精灯,应该要继续通入氮气直至装置冷切,所以操作顺序为:a﹣c﹣d
﹣b﹣e,
(3)B中有白色变为蓝色,说明有水生成,产物中还有Cl ,所以C中石蕊试纸先逐渐变
2
为红色,后褪色,
(4)D中是Cl 和NaOH反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl +2OH
2 2
﹣=Cl﹣+ClO﹣+H O,
2
(5)①由2CuCl 2CuCl+Cl ↑,杂质是CuCl 说明CuCl 没有反应完全,分
2 2 2 2
解温度不高,故答案为:加热时间不足或温度偏低;
②杂质是氧化铜,说明CuCl被氧气氧化才产生了CuO,说明装置中有氧气,可能是没有
在HCl的氛围中加热或者未等试管冷却就停止通入HCl气体,
11.(2016•四川)资源的高效利用对保护环境.促进经济持续健康发展具有重要作用.磷
尾矿主要含Ca (PO ) F和CaCO •MgCO .某研究小组提出了磷尾矿综合利用的研究方
5 4 3 3 3
案,制备具有重要工业用途的CaCO 、Mg(OH) 、P 和H 其简化流程如图:
3 2 4 2
已知:①Ca (PO ) F在950℃不分解
5 4 3
②4Ca
5
(PO
4
)
3
F+18SiO
2
+30C 2CaF
2
+30CO+18CaSiO
3
+3P
4
请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是
(2)实验室过滤所需的玻璃仪器是
(3)NH NO 溶液能从磷矿Ⅰ中浸取出Ca2+的原因是
4 3
(4)在浸取液Ⅱ中通入NH ,发生反应的化学方程式是
3
(5)工业上常用磷精矿[Ca PO ) F 和硫酸反应制备磷酸.已知25℃,101kPa时:
5 4 3
CaO(s)+H SO (l)═CaSO (s)+H O(l)△H=﹣271kJ/mol
2 4 4 2
]
5CaO(s)+3H PO (l)+HF(g)═Ca (PO ) F(s)+5H O(l)△H=﹣937kJ/mol
3 4 5 4 3 2
则Ca (PO ) F和硫酸反应生成磷酸的热化学方程式是
5 4 3
(6)在一定条件下CO(g)+H
2
O(g) ⇌CO
2
(g)+H
2
(g),当CO与H
2
O(g)的起始
物质的量之比为1:5,达平衡时,CO转化了 .若a kg含Ca (PO ) F(相对分子质量
5 4 3
为504)的质量分数为10%的磷尾矿,在上述过程中有b%的Ca (PO ) F转化为P ,将
5 4 3 4
产生的CO与H O(g)按起始物质的量之比1:3混合,则在相同条件下达平衡时能产生
2
H kg.
2
【答案】 (1) 二氧化碳(CO );
2
(2) 烧杯、漏斗和玻璃棒;
(3) NH +水解使溶液呈酸性,与CaO、Ca(OH) 反应生成Ca2+;
4 2
(4) MgSO +2NH +2H O=Mg(OH) ↓+(NH ) SO ;
4 3 2 2 4 2 4(5) Ca (PO ) F (s)+5H SO (l)=5CaSO4(s)+H PO (l)+HF(g)△H=﹣
5 4 3 2 4 3 4
418kJ/mol;
(6) .
【解析】解:磷尾矿[主要含Ca (PO ) F和CaCO •MgCO 在950℃下煅烧,其中碳酸钙
5 4 3 3 3
和碳酸镁分解,生成气体的成分为二氧化碳(CO ),磷矿Ⅰ的主要成分为Ca (PO )
2 5 4
]
F、CaO、MgO,NH NO 溶液中铵离子水解呈酸性,可溶解CaO,得到的浸取液Ⅰ含有
3 4 3
Ca2+,可生成CaCO ,磷矿Ⅱ含有Ca (PO ) F、MgO,加入硫酸铵浸取,浸取液Ⅱ含有
3 5 4 3
镁离子,可生成氢氧化镁,磷精矿加入二氧化硅、C等,在高温下发生4Ca (PO )
5 4
F+18SiO +30C 2CaF +30CO+18CaSiO +3P ,
3 2 2 3 4
(1)根据题给化学工艺流程和信息①知磷尾矿[主要含Ca (PO ) F和CaCO •MgCO 在
5 4 3 3 3
950℃下煅烧,其中碳酸钙和碳酸镁分解,生成气体的成分为二氧化碳(CO ), (2)实
2
]
验室过滤所需的玻璃仪器是烧杯、漏斗和玻璃棒,故答案为:烧杯、漏斗和玻璃棒;
(3)NH NO 溶液中铵离子水解呈酸性,H+能从磷矿I中浸取出Ca2+,故答案为:NH +水
4 3 4
解使溶液呈酸性,与CaO、Ca(OH) 反应生成Ca2+;
2
(4)根据化学工艺流程判断浸取液II的主要成分为硫酸镁溶液,通入NH ,发生反应的化
3
学方程式是MgSO +2NH +2H O=Mg(OH) ↓+(NH ) SO ,
4 3 2 2 4 2 4
(5)已知25℃,101kPa时:
①CaO(s)+H
2
SO
4
(l)═CaSO
4
(s)+H
2
O(l)△H=﹣271kJ/mol
②5CaO(s)+3H
3
PO
4
(l)+HF(g)═Ca
5
(PO
4
)
3
F(s)+5H
2
O(l)△H=﹣937kJ/mol
根据盖斯定律:①×5﹣②得Ca (PO ) F和硫酸反应生成磷酸的热化学方程式是Ca
5 4 3 5
(PO ) F (s)+5H SO (l)=5CaSO4(s)+H PO (l)+HF(g)△H=﹣418kJ/mol,
4 3 2 4 3 4
(6)根据题给数据利用三行式答案.设CO的起始浓度为1mol/L,则水蒸气的起始浓度
为5mol/L
CO(g)+H
2
O(g) ⇌CO
2
(g)+H
2
(g),
起始浓度(mol/L)1 5 0 0
转化浓度(mol/L)
平衡浓度(mol/L)
则K=\frac{c(C{O}_{2})c({H}_{2})}{c(CO)C({H}_{2}O)}= =1.
相同条件下当CO与H O(g)的起始物质的量之比为1:3,平衡常数不变,设转化的CO
2
为x.
CO(g)+H
2
O(g) ⇌CO
2
(g)+H
2
(g),
起始浓度(mol/L)1 3 0 0
转化浓度(mol/L)x x x x
平衡浓度(mol/L)(1﹣x) (3﹣x) x x则 =1,解得x= ,即达平衡时,CO转化了 ,转化为P 的Ca
4 5
(PO ) F质量为a×10%×b%kg,
4 3
根据反应4Ca (PO ) F+18SiO +30C 2CaF +30CO+18CaSiO +3P 知生成CO的质
5 4 3 2 2 3 4
量为 kg,
则转化的CO的质量为 × kg,
根据反应:CO(g)+H
2
O(g) ⇌CO
2
(g)+H
2
(g)知相同条件下达平衡时能产生H
2
= kg.