文档内容
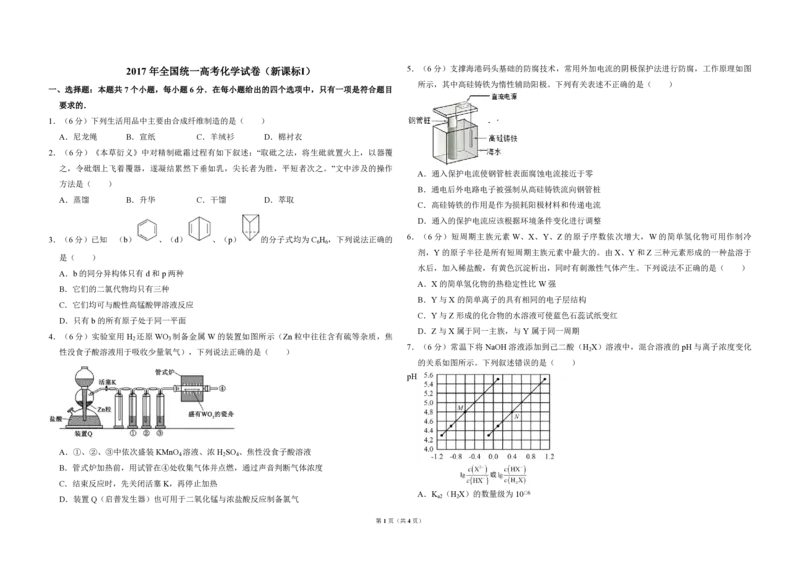
2017 年全国统一高考化学试卷(新课标Ⅰ) 5.(6分)支撑海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图
所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
一、选择题:本题共 7个小题,每小题 6分.在每小题给出的四个选项中,只有一项是符合题目
要求的.
1.(6分)下列生活用品中主要由合成纤维制造的是( )
A.尼龙绳 B.宣纸 C.羊绒衫 D.棉衬衣
2.(6分)《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆
之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作
A.通入保护电流使钢管桩表面腐蚀电流接近于零
方法是( )
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
A.蒸馏 B.升华 C.干馏 D.萃取
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
6.(6分)短周期主族元素 W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷
3.(6分)已知 (b) 、(d) 、(p) 的分子式均为 C H ,下列说法正确的
6 6
剂,Y 的原子半径是所有短周期主族元素中最大的。由 X、Y 和 Z三种元素形成的一种盐溶于
是( )
水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是( )
A.b的同分异构体只有d和p两种
A.X 的简单氢化物的热稳定性比W强
B.它们的二氯代物均只有三种
B.Y 与X 的简单离子的具有相同的电子层结构
C.它们均可与酸性高锰酸钾溶液反应
C.Y 与Z形成的化合物的水溶液可使蓝色石蕊试纸变红
D.只有b的所有原子处于同一平面
D.Z与X 属于同一主族,与 Y 属于同一周期
4.(6 分)实验室用 H 还原 WO 制备金属 W的装置如图所示(Zn粒中往往含有硫等杂质,焦
2 3
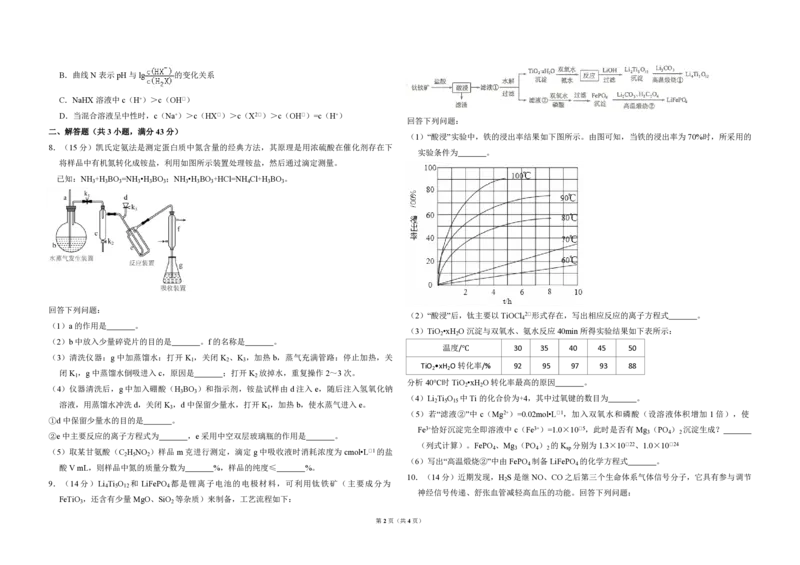
7.(6分)常温下将 NaOH 溶液添加到己二酸(H X)溶液中,混合溶液的 pH 与离子浓度变化
性没食子酸溶液用于吸收少量氧气),下列说法正确的是( ) 2
的关系如图所示。下列叙述错误的是( )
pH
A.①、②、③中依次盛装KMnO 溶液、浓H SO 、焦性没食子酸溶液
4 2 4
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度
C.结束反应时,先关闭活塞K,再停止加热
A.K (H X)的数量级为10﹣6
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 a2 2
第1页(共4页)B.曲线 N 表示pH 与lg 的变化关系
C.NaHX 溶液中 c(H+)>c(OH﹣)
D.当混合溶液呈中性时,c(Na+)>c(HX﹣)>c(X2﹣)>c(OH﹣)=c(H+)
回答下列问题:
二、解答题(共 3小题,满分 43分)
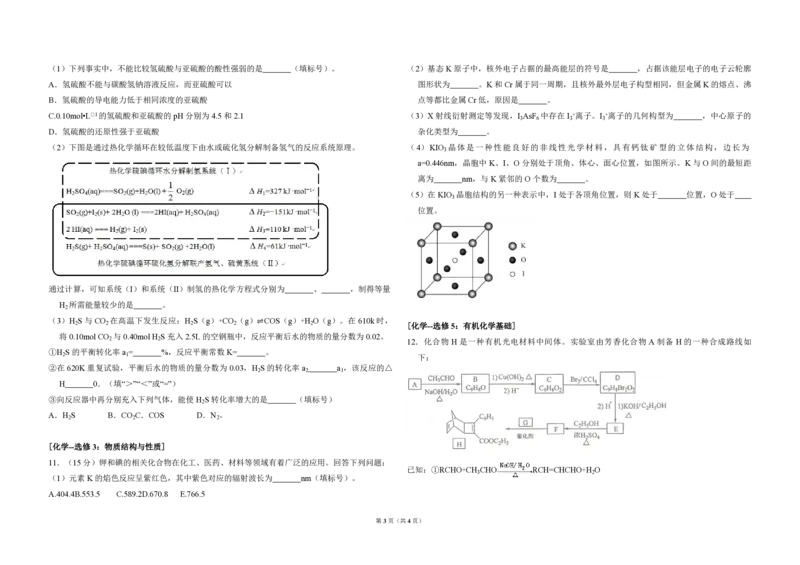
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的浸出率为 70%时,所采用的
8.(15 分)凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下
实验条件为 。
将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。
已知:NH +H BO =NH •H BO ;NH •H BO +HCl=NH Cl+H BO 。
3 3 3 3 3 3 3 3 3 4 3 3
回答下列问题:
(2)“酸浸”后,钛主要以TiOCl 2﹣形式存在,写出相应反应的离子方程式 。
4
(1)a的作用是 。
(3)TiO •xH O 沉淀与双氧水、氨水反应 40min所得实验结果如下表所示:
2 2
(2)b中放入少量碎瓷片的目的是 。f 的名称是 。
温度/℃ 30 35 40 45 50
(3)清洗仪器:g中加蒸馏水:打开 K ,关闭 K 、K ,加热 b,蒸气充满管路:停止加热,关
1 2 3
TiO •xH O 转化率/% 92 95 97 93 88
2 2
闭K ,g中蒸馏水倒吸进入 c,原因是 ;打开K 放掉水,重复操作2~3次。
1 2
分析40℃时 TiO •xH O 转化率最高的原因 。
2 2
(4)仪器清洗后,g中加入硼酸(H BO )和指示剂,铵盐试样由 d注入 e,随后注入氢氧化钠
3 3
(4)Li Ti O 中Ti的化合价为+4,其中过氧键的数目为 。
2 5 15
溶液,用蒸馏水冲洗d,关闭K ,d中保留少量水,打开K ,加热b,使水蒸气进入e。
3 1
(5)若“滤液②”中 c(Mg2+)=0.02mol•L﹣1,加入双氧水和磷酸(设溶液体积增加 1倍),使
①d中保留少量水的目的是 。
Fe3+恰好沉淀完全即溶液中 c(Fe3+)=1.0×10﹣5,此时是否有 Mg (PO ) 沉淀生成?
3 4 2
②e中主要反应的离子方程式为 ,e采用中空双层玻璃瓶的作用是 。
(列式计算)。FePO 、Mg (PO ) 的K 分别为1.3×10﹣22、1.0×10﹣24
4 3 4 2 sp
(5)取某甘氨酸(C H NO )样品 m克进行测定,滴定 g中吸收液时消耗浓度为 cmol•L﹣1的盐
2 5 2
(6)写出“高温煅烧②”中由FePO 制备LiFePO 的化学方程式 。
4 4
酸V mL,则样品中氮的质量分数为 %,样品的纯度≤ %。
10.(14分)近期发现,H S 是继 NO、CO 之后第三个生命体系气体信号分子,它具有参与调节
2
9.(14分)Li Ti O 和 LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
4 5 12 4
神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
FeTiO ,还含有少量MgO、SiO 等杂质)来制备,工艺流程如下:
3 2
第2页(共4页)(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是 (填标号)。 (2)基态 K 原子中,核外电子占据的最高能层的符号是 ,占据该能层电子的电子云轮廓
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 图形状为 。K 和 Cr属于同一周期,且核外最外层电子构型相同,但金属 K 的熔点、沸
B.氢硫酸的导电能力低于相同浓度的亚硫酸 点等都比金属Cr低,原因是 。
C.0.10mol•L﹣1的氢硫酸和亚硫酸的pH 分别为4.5 和2.1 (3)X 射线衍射测定等发现,I AsF 中存在 I +离子。I +离子的几何构型为 ,中心原子的
3 6 3 3
D.氢硫酸的还原性强于亚硫酸 杂化类型为 。
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。 (4)KIO 晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为
3
a=0.446nm,晶胞中 K、I、O 分别处于顶角、体心、面心位置,如图所示。K 与 O 间的最短距
离为 nm,与K 紧邻的O 个数为 。
(5)在 KIO 晶胞结构的另一种表示中,I处于各顶角位置,则 K 处于 位置,O 处于
3
位置。
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为 、 ,制得等量
H 所需能量较少的是 。
2
(3)H S 与 CO 在高温下发生反应:H S(g)+CO (g)⇌COS(g)+H O(g)。在 610k时,
2 2 2 2 2 [化学--选修 5:有机化学基础]
将0.10mol CO 与0.40mol H S 充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
2 2 12.化合物 H 是一种有机光电材料中间体。实验室由芳香化合物 A 制备 H 的一种合成路线如
①H S 的平衡转化率a = %,反应平衡常数K= 。
2 1 下:
②在 620K 重复试验,平衡后水的物质的量分数为 0.03,H S 的转化率 a a ,该反应的△
2 2 1
H 0.(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H S 转化率增大的是 (填标号)
2
A.H S B.CO C.COS D.N 。
2 2 2
[化学--选修 3:物质结构与性质]
11.(15分)钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
已知:①RCHO+CH CHO RCH=CHCHO+H O
3 2
(1)元素K 的焰色反应呈紫红色,其中紫色对应的辐射波长为 nm(填标号)。
A.404.4B.553.5 C.589.2D.670.8 E.766.5
第3页(共4页)② +
回答下列问题:
(1)A 的化学名称为 。
(2)由C 生成D 和E生成F 的反应类型分别为 、 。
(3)E的结构简式为 。
(4)G 为甲苯的同分异构体,由F 生成H 的化学方程式为 。
(5)芳香化合物 X 是 F 的同分异构体,X 能与饱和碳酸氢钠溶液反应放出 CO ,其核磁共振氢
2
谱显示有 4种不同化学环境的氢,峰面积比为 6:2:1:1,写出 2种符合要求的 X 的结构简
式 。
(6)写出用环戊烷和 2﹣丁炔为原料制备化合物 的合成路线 (其他试剂任
选)。
第4页(共4页)