文档内容
2023 年普通高等学校招生考试化学科目(天津卷)
一、选择题
1. 近年来我国航天事业发展迅速,下列对所涉及化学知识的叙述错误的是
A. “嫦娥五号”取回的月壤样品中含有天然玻璃物质,玻璃是晶体
B. “天舟六号”壳体使用了铝合金,合金是金属材料
C. “长征七号”采用了液氧煤油发动机,煤油是混合物
D. “天宫”空间站新补充了一批氙推进剂,氙是稀有气体
【答案】A
【解析】
【详解】A.玻璃是非晶体,A错误;
B.合金和金属单质是金属材料,B正确;
C.煤油为碳原子数C11-C17的高沸点烃类混合物,主要成分是饱和烃类,还含有不饱和烃和芳香烃,煤
油为混合物,C正确;
D.氙是第5周期0族元素,属于稀有气体,D正确;
故答案为:A。
2. 下列化学常识,错误的是
A. 淀粉是一种多糖 B. 葡萄糖有还原性 C. 油脂是一种高分子 D. 氨基酸具有两性
【答案】C
【解析】
【详解】A.淀粉本身属于糖类,淀粉属于糖类中的多糖,故A正确;
B.葡萄糖中含有醛基,具有还原性,故B正确;
C.油脂相对分子质量较小,不属于高分子化合物,故C错误;
D.氨基酸中含有氨基和羧基,既可以和酸反应也可以和碱反应,具有两性,故D正确;
故选C。
3. 下列方法(试剂)中,无法鉴别 和 两种物质的是
A. 焰色试验 B. 试纸 C. 稀氨水 D.
【答案】C
【解析】
【详解】A.钠元素、钡元素的焰色不同,可以用焰色试验鉴别碳酸钠和氯化钡,A不符合;
B.NaCO 溶液显碱性,BaCl 溶液显中性,故可以用pH试纸检验NaCO 和BaCl ,B不符合;
2 3 2 2 3 2C.NaCO 溶液和BaCl 溶液与氨水都不反应,都无现象,C符合;
2 3 2
D.NaCO 溶液与NaSO 溶液不反应,BaCl 溶液与NaSO 反应生成白色沉淀硫酸钡, D不符合;
2 3 2 4 2 2 4
故答案为:C。
4. 下列常见物质及用途,错误的是
A. 氢氧化铝可用于治疗胃酸过多
B. SiO 可用于制造光导纤维
2
C. Fe O 是铁红,可以用作染料
2 3
D. 钠起火,可以使用水基灭火器扑灭
【答案】D
【解析】
【详解】A.胃酸中含有HCl,氢氧化铝可以与HCl反应,能用于治疗胃酸过多,A正确;
B.SiO 具有良好的光学特性,可用于制造光导纤维,B正确;
2
C.Fe O 是一种红色粉末,俗称铁红,常用作红色染料,C正确;
2 3
D.钠能与水反应生成易燃性气体氢气,不能使用水基灭火器扑灭,D错误;
故选D。
5. 下列性质不能用于判断C、 的非金属性强弱的是
A. 元素的电负性
B. 最高价氧化物的熔点
C. 简单氢化物的热稳定性
D. 最高价氧化物对应的水化物的酸性
【答案】B
【解析】
【详解】A.电负性越大,元素的非金属性越强,故不选A;
的
B.最高价氧化物 熔点,与化学键或分子间作用力有关,与元素非金属性无关,故选B;
C.简单氢化物的越稳定,元素非金属性越强,故不选C;
D.最高价氧化物对应的水化物的酸性越强,元素非金属性越强,故不选D;
选B。
6. 常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国卫生组织(WTO)列为Al级高效
2
安全消毒剂。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠反应,其反应的化学
方程式:CHOH+6NaClO +3H SO =CO ↑+6ClO ↑+3Na SO +5H O,则下列说法正确的是
3 3 2 4 2 2 2 4 2
A. CO 是非极性分子
2B. 键角:ClO ClO ,B错误;
C.该反应中,碳元素化合价由−2价变为+4价,氯元素化合价由+5价变为+4价,所以氧化剂是NaClO,
3
还原剂是甲醇,C错误;
D.ClO 中Cl原子提供1对电子,有一个O原子提供1个电子,另一个O原子提供1对电子,这5个电子
2
处于互相平行的轨道中形成大π键,Cl提供孤电子对与其中一个O形成配位键,Cl与另一个O形成的是
普通的共价键(σ键,这个O只提供了一个电子参与形成大π键),Cl的价层电子对数3,则Cl原子的轨
道杂化方式为sp2,ClO 分子空间构型为V形,D错误;
2
故选A。
7. 利用18O示踪技术研究HO 与Cl 的反应历程,结果如下:
2 2 2
①
②
下列叙述正确的是
A. 反应①是置换反应
B. 18O的核电荷数是18
C. 18O与16O互为同素异形体
D. 反应历程中 中的O-O键未发生断裂
【答案】D
【解析】【详解】A.反应①生成两种化合物,不是置换反应,故A错误;
B.核电荷数等于核内质子数,所以18O的核电荷数是8,故B错误;
C.18O与16O是质子数相同、中子数不同的原子,互为同位素,故C错误;
D.反应历程中 、H-O-O-Cl、O 都含O-O键,所以 中O-O键没有发生断裂,故D正确;
2
选D。
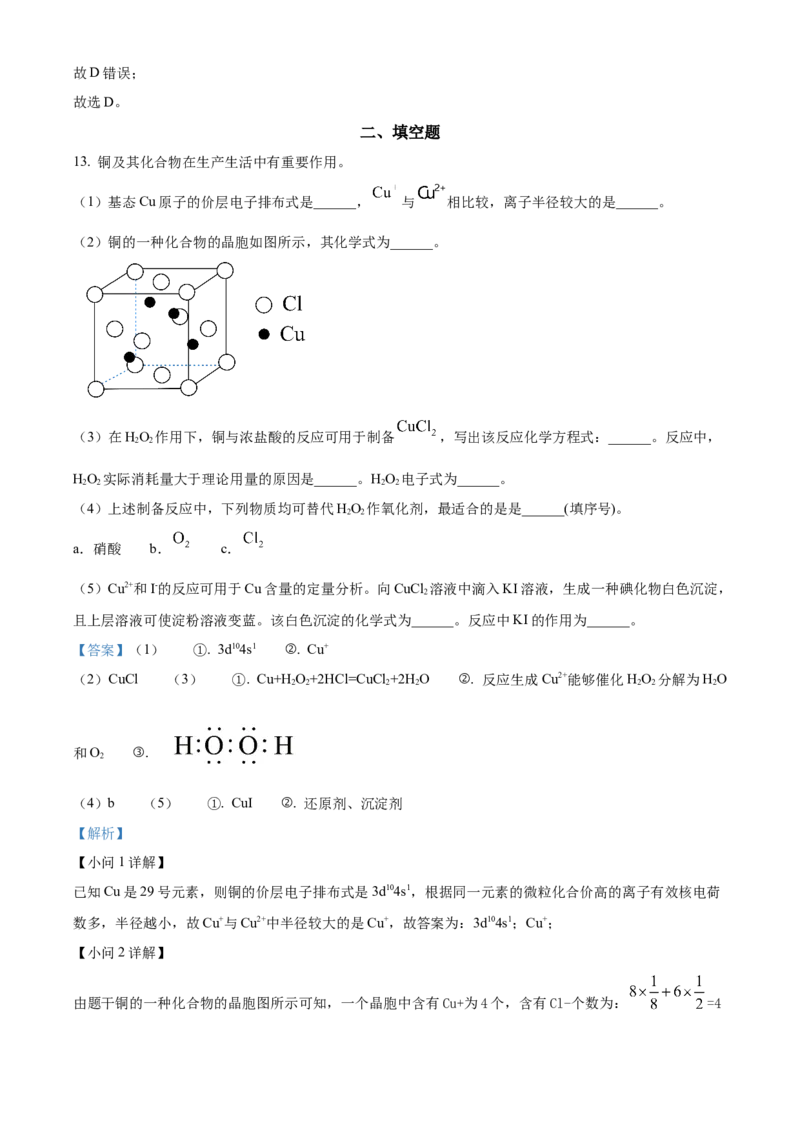
8. 如图所示,是芥酸的分子结构,关于芥酸,下列说法正确的是
A. 芥酸是一种强酸 B. 芥酸易溶于水 C. 芥酸是顺式结构 D. 分子式为
【答案】C
【解析】
【详解】A.芥酸中含有羧基,烃基较大,则芥酸的酸性小于醋酸,属于弱酸,故A错误;
B.虽然芥酸中含有的羧基是亲水基团,但疏水基——烃基较大,其难溶于水,故B错误;
C.芥酸中存在碳碳双键,且H原子在碳碳双键的同一侧,是一种顺式不饱和脂肪酸,故C正确;
D.由结构简式可知,芥酸的分子式为C H O,故D错误;
22 42 2
故选C。
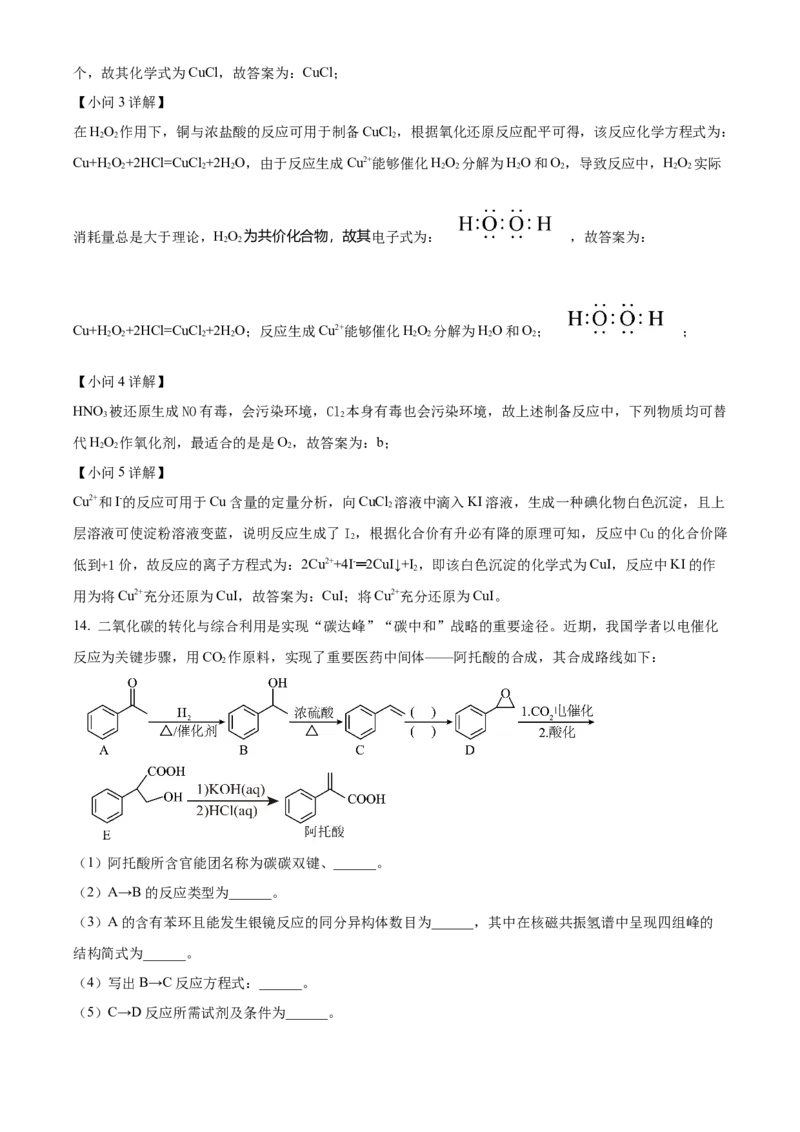
9. 实验室制备和收集相应气体可使用下图装置的是
A. Fe与稀硝酸反应制NO
B. MnO 与浓盐酸共热制备Cl
2 2
C. NaOH与浓氨水制备NH
3
D. NaSO 与浓硫酸制备SO
2 3 2
【答案】D【解析】
【详解】A.NO与O 反应生成NO ,不能用排空气法收集NO,故不选A;
2 2
B.二氧化锰与浓盐酸共热制备Cl,反应需要吸热,缺少加热装置,故不选B;
2
C.氨气的密度比空气小,需要用向下排空气法收集NH ,故不选C;
3
D.NaSO 与浓硫酸反应生成SO ,SO 密度比空气大,用向上排空气法收集SO ,故选D;
2 3 2 2 2
选D。
10. 在浓度为 的 溶液中,如下说法正确的是
A. 溶液中浓度最大的离子是
B.
C.
D. 磷酸第二步电离平衡的平衡常数表达式为
【答案】B
【解析】
【详解】A. 在水溶液中完全电离生成Na+和 , 又发生电离和水解,则溶液中浓
度最大的离子是Na+,故A错误;
B.根据NaH PO 溶液中的物料守恒可得:c(Na+)=c( )+c(PO )+c(HPO )+c(H PO )=0.1mol/L,故
2 4 3 4
B正确;
C.根据NaH PO 溶液中的电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(H PO )+2c(HPO )+3c(PO ),故C错
2 4 2
误;
D.磷酸第二步电离方程式为: ,电离平衡的平衡常数表达式为
,故D错误;
故选B。故选:B。
11. 下表列出25℃时不同羧酸的 (即 )。根据表中的数据推测,结论正确的是羧酸
pK 4.76 2.59 2.87 2.90
a
A. 酸性强弱:
B. 对键合电子的吸引能力强弱:FCl>Br,对键合电子的吸引能力强弱:
F>Cl>Br,B错误;
C.F是吸电子基团,F原子个数越多,吸电子能力越强,使得羧基中O—H键极性增强,更易电离,酸性
增强,则25℃时的pK 大小:CHF COOH