文档内容
山东省 2023 年普通高中学业水平等级考试
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Si-28 S-32 C1-35.5 K-39
Cu-64
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归为一类的是
A. 泰山墨玉 B. 龙山黑陶 C. 齐国刀币 D. 淄博琉璃
2. 实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
.
A 稀盐酸:配制 溶液
B. 稀硫酸:蔗糖和淀粉的水解
C. 稀硝酸:清洗附有银镜的试管
D. 浓硫酸和浓硝酸的混合溶液:苯的磺化
3. 下列分子属于极性分子的是
A. B. C. D.
4. 实验室安全至关重要,下列实验室事故处理方法错误的是
A. 眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗
B. 皮肤溅上碱液,先用大量水冲洗,再用 的硼酸溶液冲洗
C. 电器起火,先切断电源,再用二氧化碳灭火器灭火
D. 活泼金属燃烧起火,用灭火毛(石棉布)灭火
5. 石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF) ,该物质仍具润滑性,其单层局部结
2 x
构如图所示。下列关于该化合物的说法正确的是
A. 与石墨相比,(CF) 导电性增强
x
B. 与石墨相比,(CF) 抗氧化性增强
xC. (CF) 中 的键长比 短
x
D. 1mol(CF) 中含有2xmol共价单键
x
6. 鉴别浓度均为 的 、 三种溶液,仅用下列一种方法不可行的
是
A. 测定溶液 B. 滴加酚酞试剂
C. 滴加 溶液 D. 滴加饱和 溶液
7. 抗生素克拉维酸的结构简式如图所示,下列关于克拉维酸的说法错误的是
A. 存在顺反异构
B. 含有5种官能团
C. 可形成分子内氢键和分子间氢键
D. 1mol该物质最多可与1molNaOH反应
8. 一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定有机醇
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸酐
完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用甲醇标准溶液滴定至终点,消耗标准溶液 。对于上述实验,下列做法正确的是
A. 进行容量瓶检漏时,倒置一次即可
B. 滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
.
C 滴定读数时,应单手持滴定管上端并保持其自然垂直
D. 滴定读数时,应双手一上一下持滴定管
9. 一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定有机醇
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸酐
完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
甲醇标准溶液滴定至终点,消耗标准溶液 。 样品中羟基含量(质量分数)计
算正确的是
A. B.
C. D.
10. 一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定有机醇
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸酐
完全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
甲醇标准溶液滴定至终点,消耗标准溶液 。根据上述实验原理,下列说法正确的
是
A. 可以用乙酸代替乙酸酐进行上述实验
B. 若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C. 步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D. 步骤④中,若加水量不足,将导致测定结果偏大
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
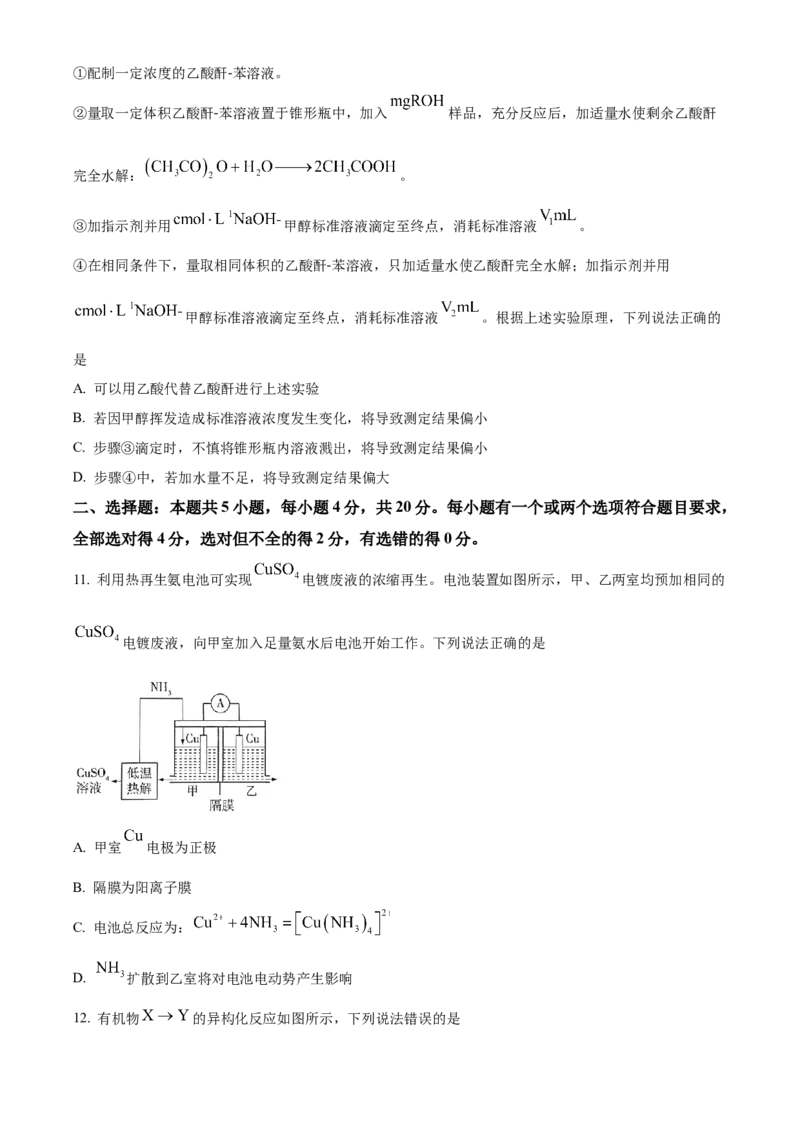
11. 利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的
电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A. 甲室 电极为正极
B. 隔膜为阳离子膜
C. 电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
12. 有机物 的异构化反应如图所示,下列说法错误的是A. 依据红外光谱可确证X、Y存在不同的官能团
B. 除氢原子外,X中其他原子可能共平面
C. 含醛基和碳碳双键且有手性碳原子的Y的同分异构体有4种(不考虑立体异构)
D. 类比上述反应, 的异构化产物可发生银镜反应和加聚反应
的
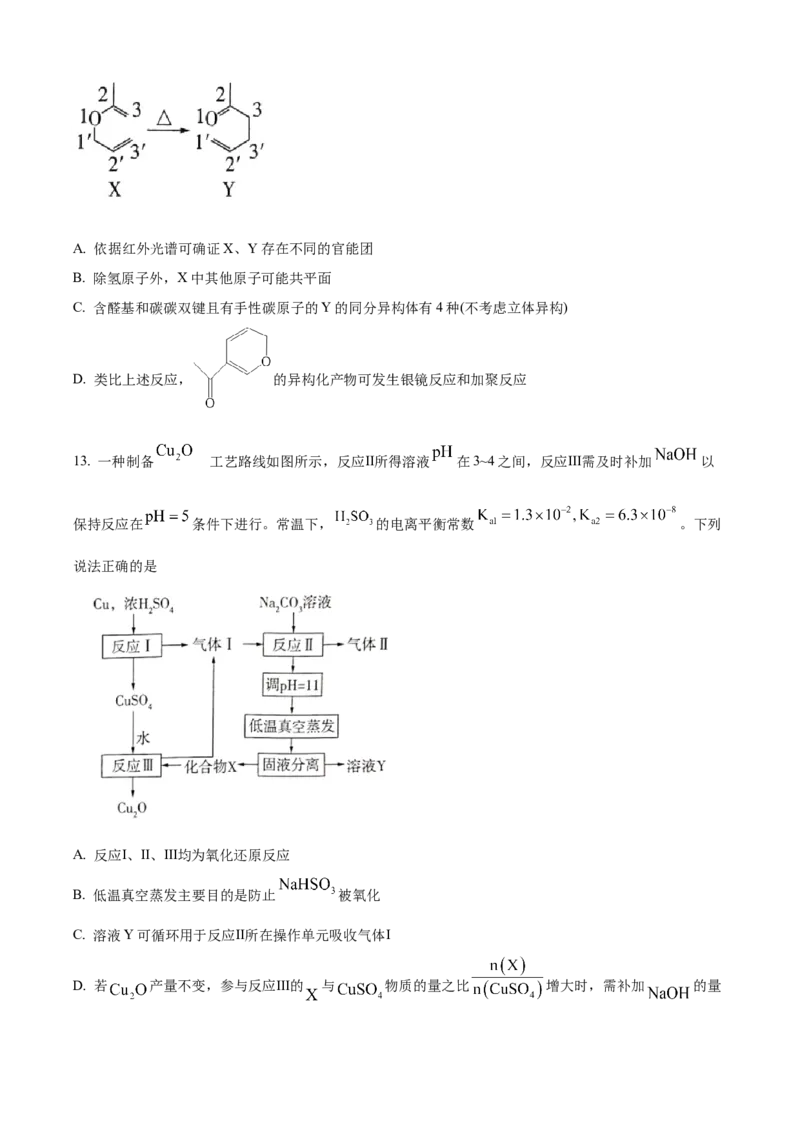
13. 一种制备 工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及时补加 以
保持反应在 条件下进行。常温下, 的电离平衡常数 。下列
说法正确的是
A. 反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B. 低温真空蒸发主要目的是防止 被氧化
C. 溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
D. 若 产量不变,参与反应Ⅲ的 与 物质的量之比 增大时,需补加 的量减少
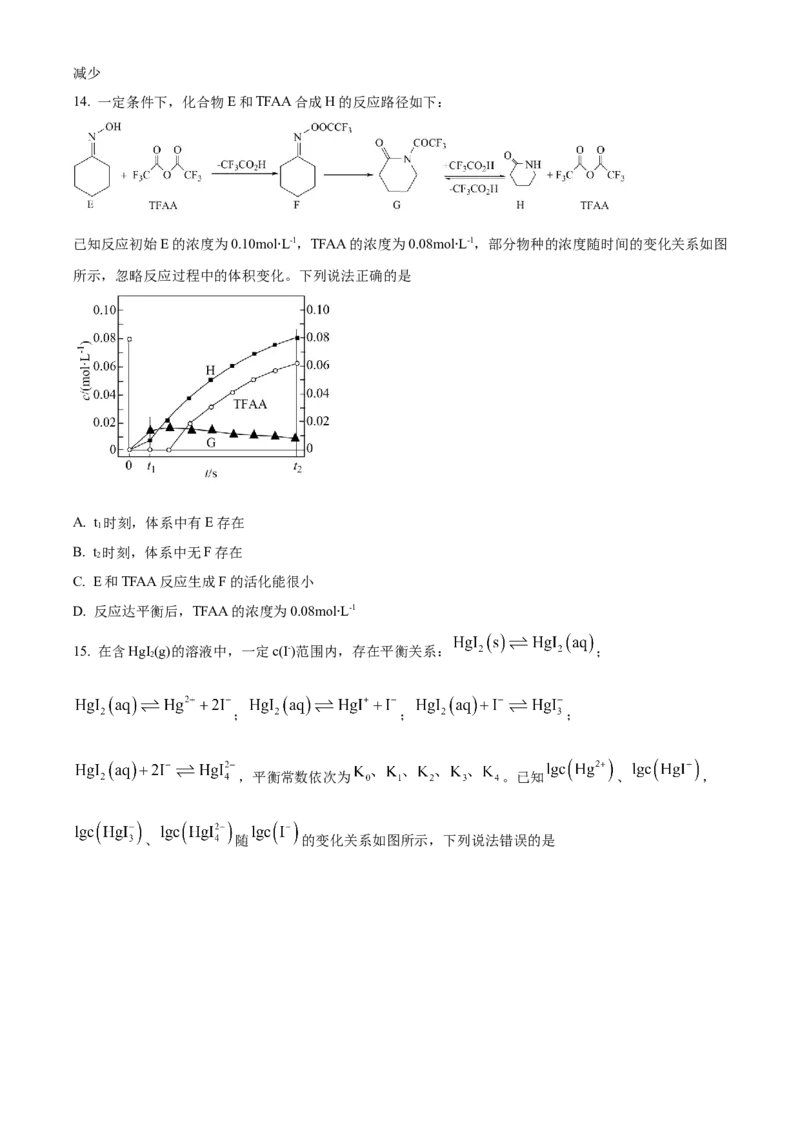
14. 一定条件下,化合物E和TFAA合成H的反应路径如下:
已知反应初始E的浓度为0.10molL-1,TFAA的浓度为0.08molL-1,部分物种的浓度随时间的变化关系如图
所示,忽略反应过程中的体积变化∙。下列说法正确的是 ∙
A. t 时刻,体系中有E存在
1
B. t 时刻,体系中无F存在
2
C. E和TFAA反应生成F的活化能很小
D. 反应达平衡后,TFAA的浓度为0.08molL-1
∙
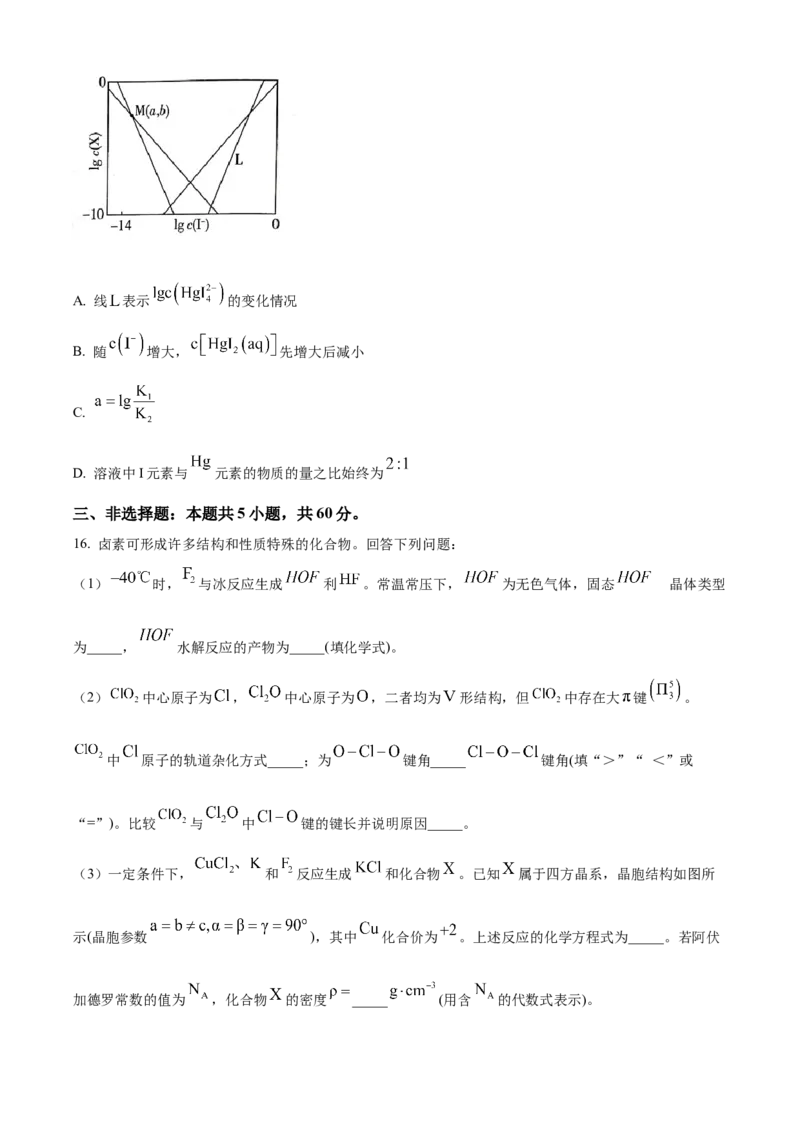
15. 在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ;
,平衡常数依次为 。已知 、 ,
、 随 的变化关系如图所示,下列说法错误的是A. 线 表示 的变化情况
B. 随 增大, 先增大后减小
C.
D. 溶液中I元素与 元素的物质的量之比始终为
三、非选择题:本题共5小题,共60分。
16. 卤素可形成许多结构和性质特殊的化合物。回答下列问题:
的
(1) 时, 与冰反应生成 利 。常温常压下, 为无色气体,固态 晶体类型
为_____, 水解反应的产物为_____(填化学式)。
(2) 中心原子为 , 中心原子为 ,二者均为 形结构,但 中存在大 键 。
中 原子的轨道杂化方式_____;为 键角_____ 键角(填“>”“ <”或
“=”)。比较 与 中 键的键长并说明原因_____。
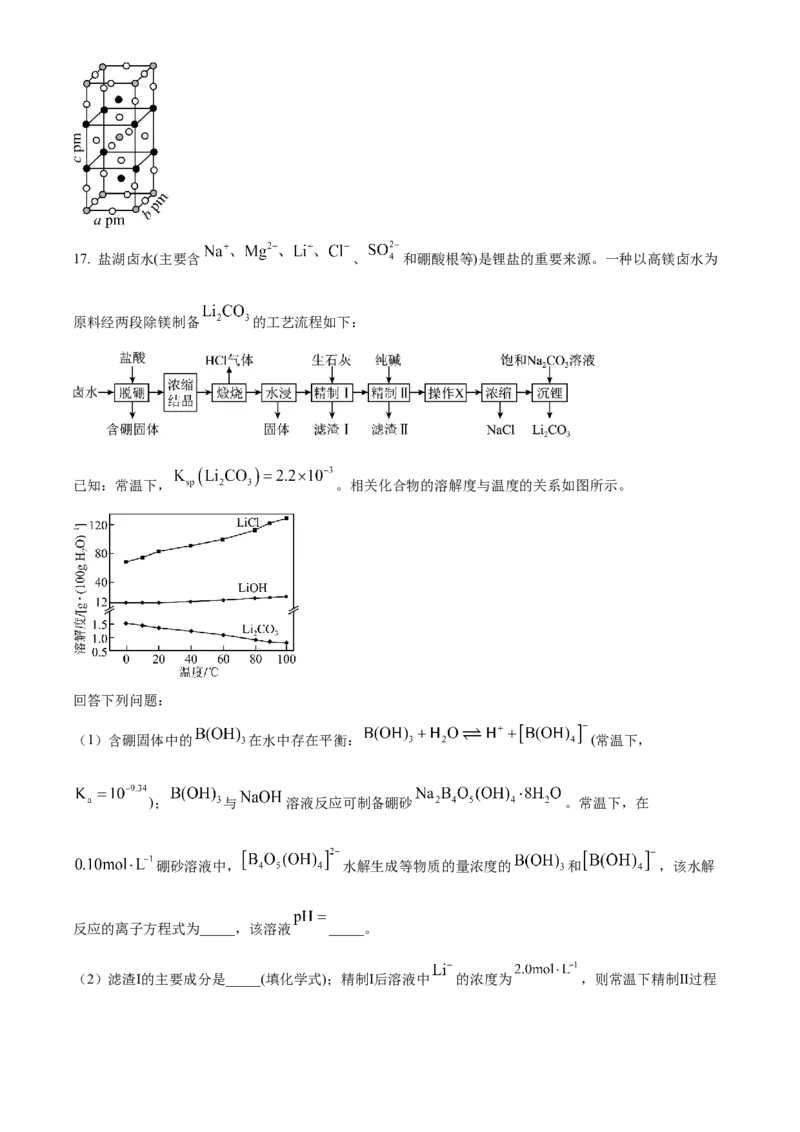
(3)一定条件下, 和 反应生成 和化合物 。已知 属于四方晶系,晶胞结构如图所
示(晶胞参数 ),其中 化合价为 。上述反应的化学方程式为_____。若阿伏
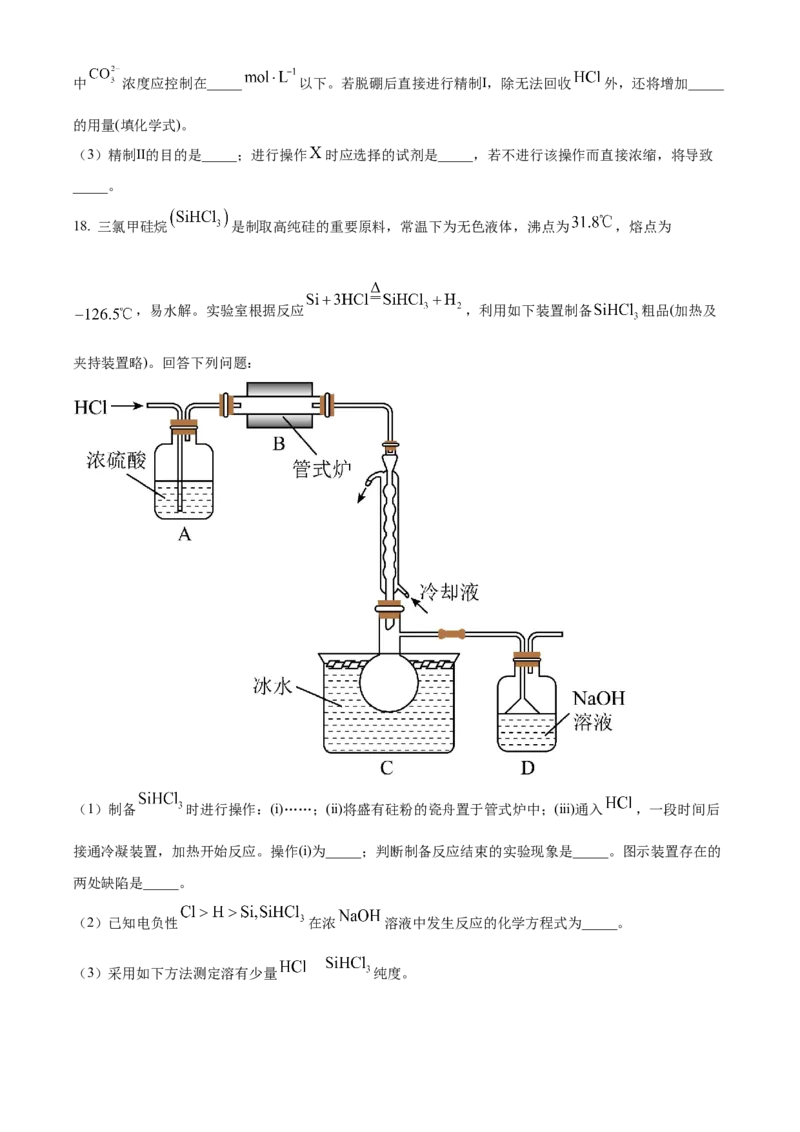
加德罗常数的值为 ,化合物 的密度 _____ (用含 的代数式表示)。17. 盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为
原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下,
); 与 溶液反应可制备硼砂 。常温下,在
硼砂溶液中, 水解生成等物质的量浓度的 和 ,该水解
反应的离子方程式为_____,该溶液 _____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过程中 浓度应控制在_____ 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加_____
的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作 时应选择的试剂是_____,若不进行该操作而直接浓缩,将导致
_____。
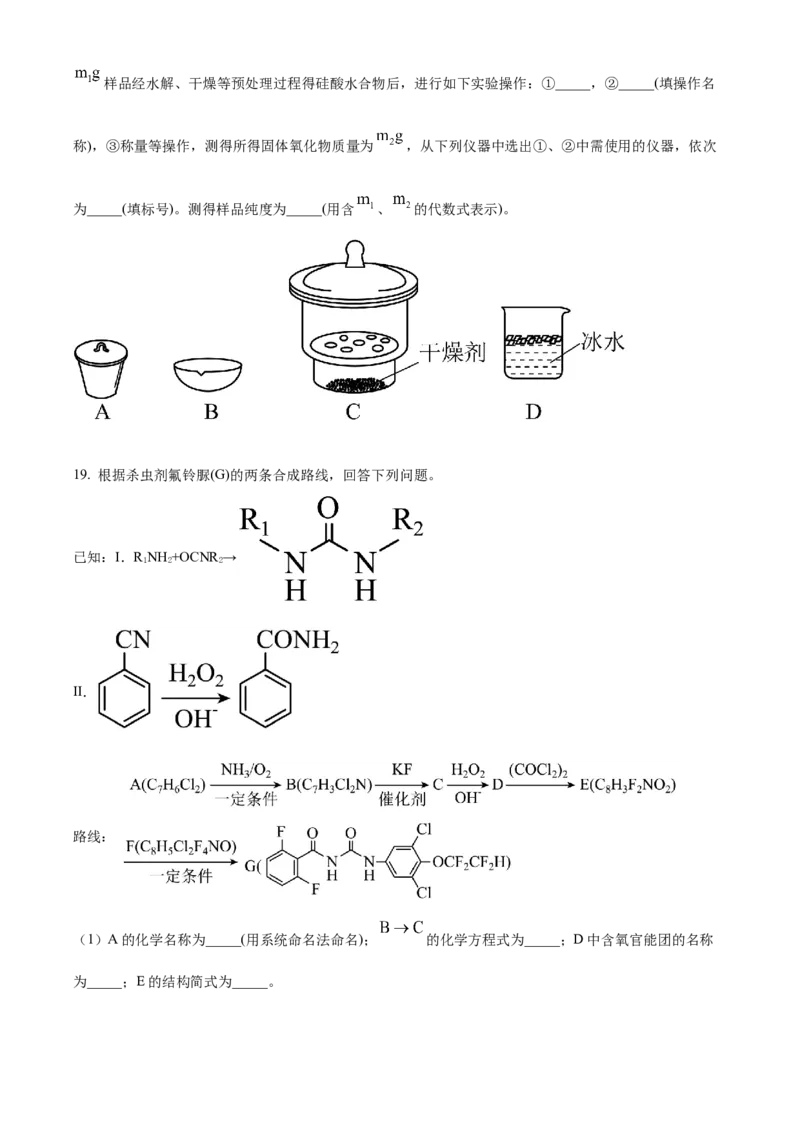
18. 三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,易水解。实验室根据反应 ,利用如下装置制备 粗品(加热及
夹持装置略)。回答下列问题:
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后
接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结束的实验现象是_____。图示装置存在的
两处缺陷是_____。
(2)已知电负性 在浓 溶液中发生反应的化学方程式为_____。
的
(3)采用如下方法测定溶有少量 纯度。样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,②_____(填操作名
称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次
为_____(填标号)。测得样品纯度为_____(用含 、 的代数式表示)。
19. 根据杀虫剂氟铃脲(G)的两条合成路线,回答下列问题。
已知:Ⅰ.R NH +OCNR →
1 2 2
Ⅱ.
路线:
(1)A的化学名称为_____(用系统命名法命名); 的化学方程式为_____;D中含氧官能团的名称
为_____;E的结构简式为_____。路线二:
(2)H中有_____种化学环境的氢,①~④属于加成反应的是_____(填序号);J中原子的轨道杂化方式有
_____种。
20. 一定条件下,水气变换反应 的中间产物是 。为探究该反应过程,
研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡
后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变 _____(用
含 的代数式表示)。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。 温度下, 电
离平衡常数为 ,当 平衡浓度为 时, 浓度为_____ ,此时反应Ⅰ应速率
_____ (用含 和k的代数式表示)。
(3) 温度下,在密封石英管内完全充满 水溶液,使 分解,分解产物均
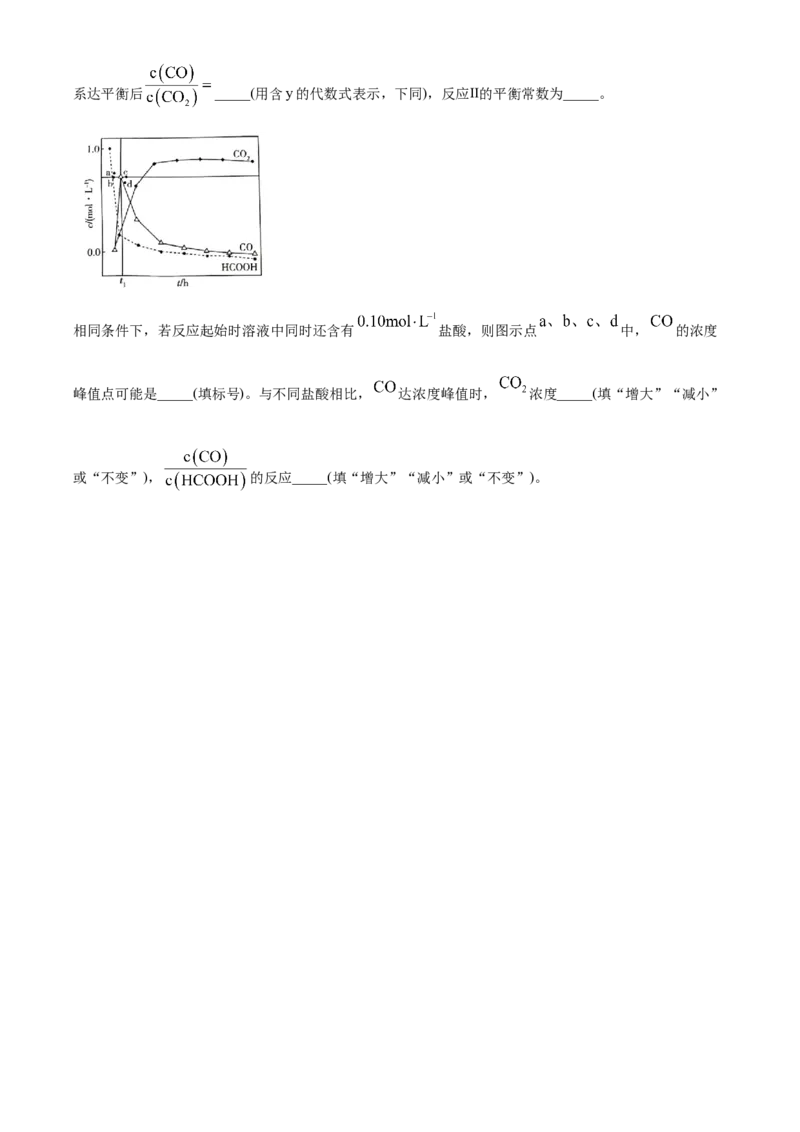
完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得
的浓度分别为 ,反应Ⅱ达平衡时,测得 的浓度为 。体系达平衡后 _____(用含y的代数式表示,下同),反应Ⅱ的平衡常数为_____。
相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点 中, 的浓度
峰值点可能是_____(填标号)。与不同盐酸相比, 达浓度峰值时, 浓度_____(填“增大”“减小”
或“不变”), 的反应_____(填“增大”“减小”或“不变”)。