文档内容
2023 年重庆市高考卷·化学
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 重庆市战略性新兴产业发展“十四五”规划(2021-2025年)涉及的下列物质中,属于金属材料的是
A.重组蛋白 B.高性能铜箔 C.氮化镓半导体 D.聚氨酯树脂
A. A B. B C. C D. D
2. 下列离子方程式中,错误的是
A. 通入水中:
B. 通入石灰乳中:
C. 放入 溶液中:
D. 放入 溶液中:
3. 下列叙述正确的是
A. 分别与空气和氧气反应,生成的产物相同
B. 分别与 和 反应,反应的类型相同
C. 分别与 和 反应,生成的气体相同
D. 浓 分别与 和 反应,生成的酸性气体相同
4. 已知反应: , 为阿伏加德罗常数的值,若消耗 (标准状
况) ,下列叙述错误的是A. 转移的电子数为 B. 生成的 质量为
C. 乙生成的氧化产物分子数为 D. 生成的 含有孤电子对数为
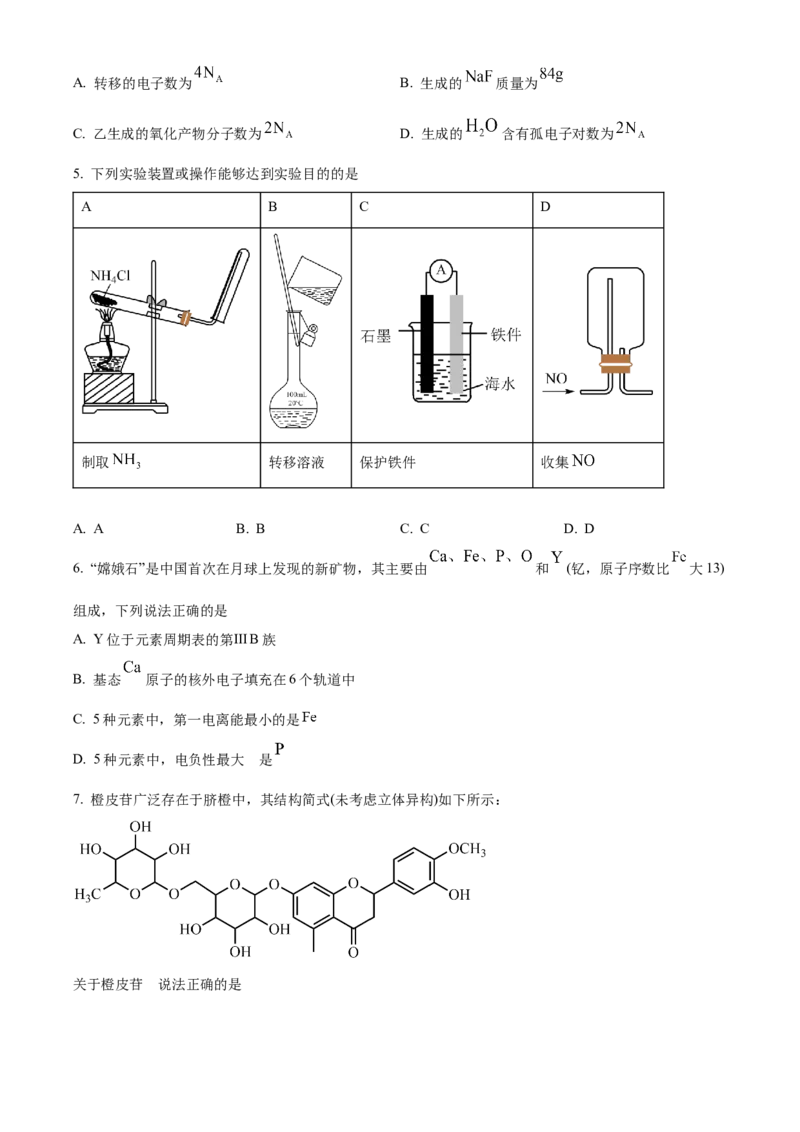
5. 下列实验装置或操作能够达到实验目的的是
A B C D
制取 转移溶液 保护铁件 收集
A. A B. B C. C D. D
6. “嫦娥石”是中国首次在月球上发现的新矿物,其主要由 和 (钇,原子序数比 大13)
组成,下列说法正确的是
A. Y位于元素周期表的第ⅢB族
B. 基态 原子的核外电子填充在6个轨道中
C. 5种元素中,第一电离能最小的是
的
D. 5种元素中,电负性最大 是
7. 橙皮苷广泛存在于脐橙中,其结构简式(未考虑立体异构)如下所示:
关于橙皮苷 的说法正确的是A. 光照下与氯气反应,苯环上可形成 键
B. 与足量 水溶液反应, 键均可断裂
C. 催化剂存在下与足量氢气反应, 键均可断裂
D. 与 醇溶液反应,多羟基六元环上可形成 键
8. 下列实验操作和现象,得出的相应结论正确的是
选
实验操作 现象 结论
项
氧化性:
向盛有 和 的试 盛 的试管中产
A
管中分别滴加浓盐酸 生黄绿色气体
B 向 溶液中通入 气体 出现黑色沉淀(CuS) 酸性:
乙醇和浓硫酸共热至 ,将产生
C 溴水褪色 乙烯发生了加成反应
的气体通入溴水中
向 溶液中滴加 溶
D 出现黄色沉淀 发生了水解反应
液
A. A B. B C. C D. D
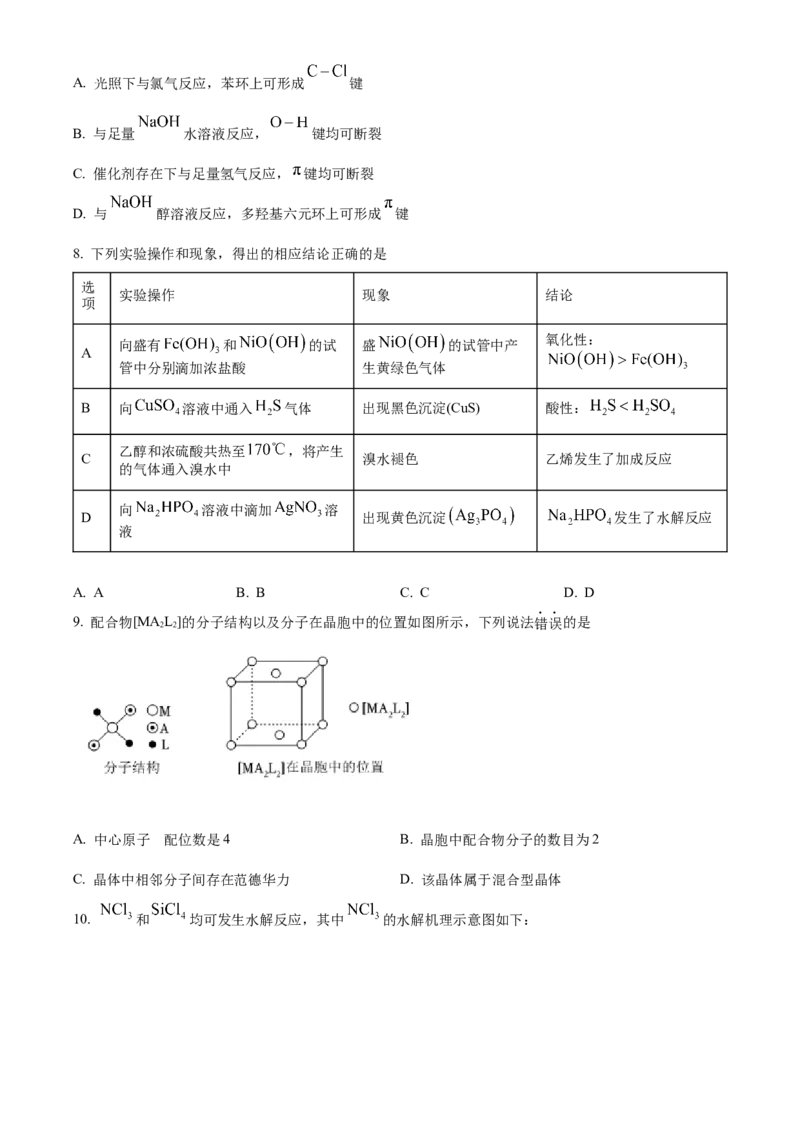
9. 配合物[MA L]的分子结构以及分子在晶胞中的位置如图所示,下列说法错误的是
2 2
的
A. 中心原子 配位数是4 B. 晶胞中配合物分子的数目为2
C. 晶体中相邻分子间存在范德华力 D. 该晶体属于混合型晶体
10. 和 均可发生水解反应,其中 的水解机理示意图如下:下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化
C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
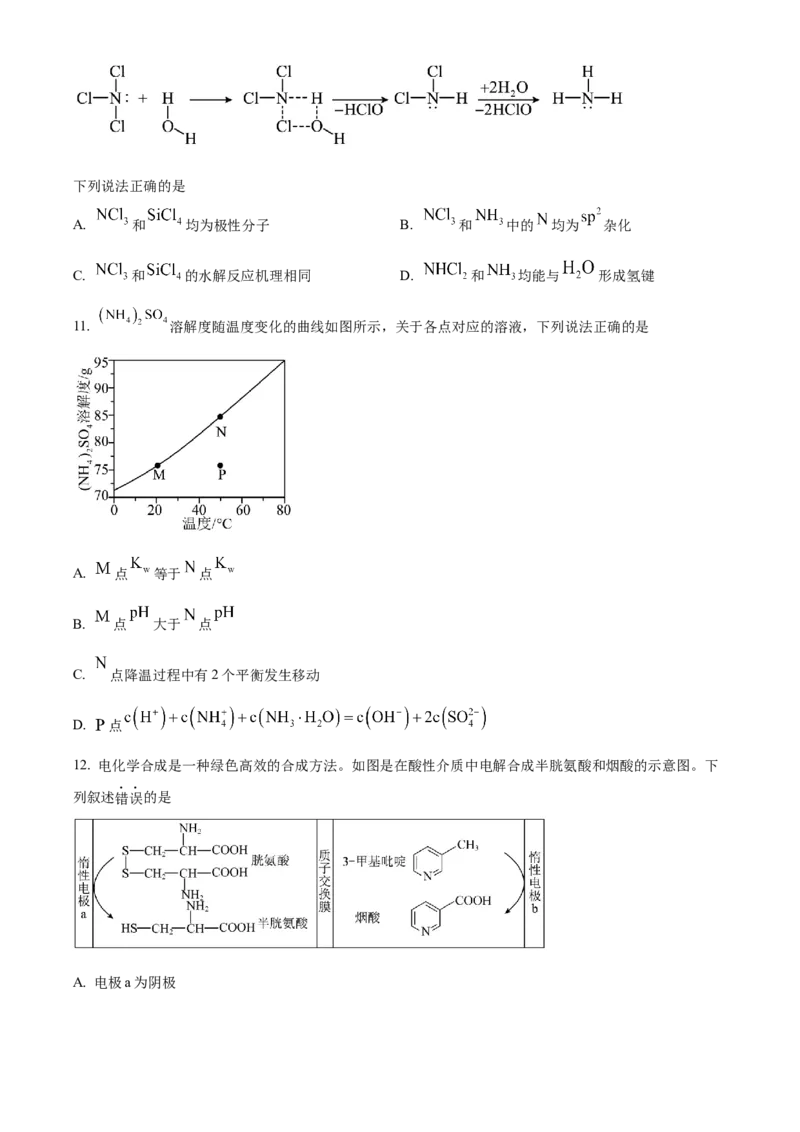
11. 溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列说法正确的是
A. 点 等于 点
B. 点 大于 点
C. 点降温过程中有2个平衡发生移动
D. 点
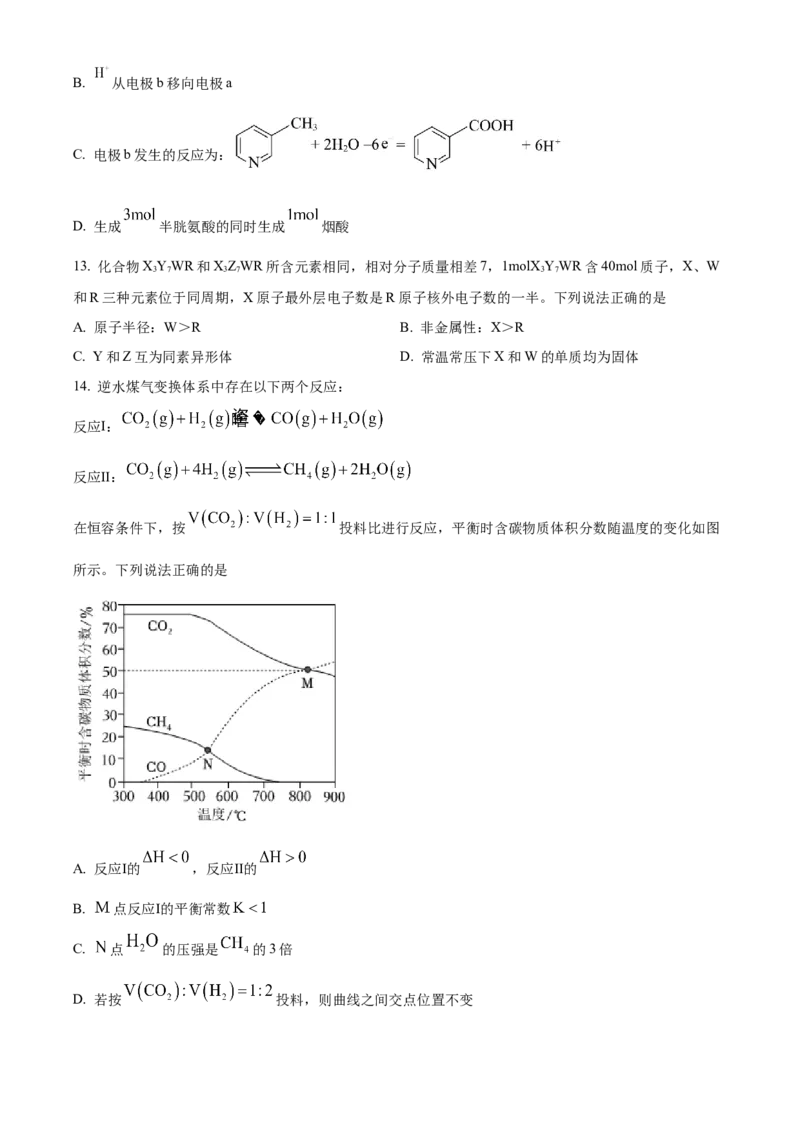
12. 电化学合成是一种绿色高效的合成方法。如图是在酸性介质中电解合成半胱氨酸和烟酸的示意图。下
列叙述错误的是
A. 电极a为阴极B. 从电极b移向电极a
C. 电极b发生的反应为:
D. 生成 半胱氨酸的同时生成 烟酸
13. 化合物XYWR和XZWR所含元素相同,相对分子质量相差7,1molX YWR含40mol质子,X、W
3 7 3 7 3 7
和R三种元素位于同周期,X原子最外层电子数是R原子核外电子数的一半。下列说法正确的是
A. 原子半径:W>R B. 非金属性:X>R
C. Y和Z互为同素异形体 D. 常温常压下X和W的单质均为固体
14. 逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:
反应Ⅱ:
在恒容条件下,按 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图
所示。下列说法正确的是
A. 反应Ⅰ的 ,反应Ⅱ的
B. 点反应Ⅰ的平衡常数
C. 点 的压强是 的3倍
D. 若按 投料,则曲线之间交点位置不变二、非选择题:本题共4小题,共58分。
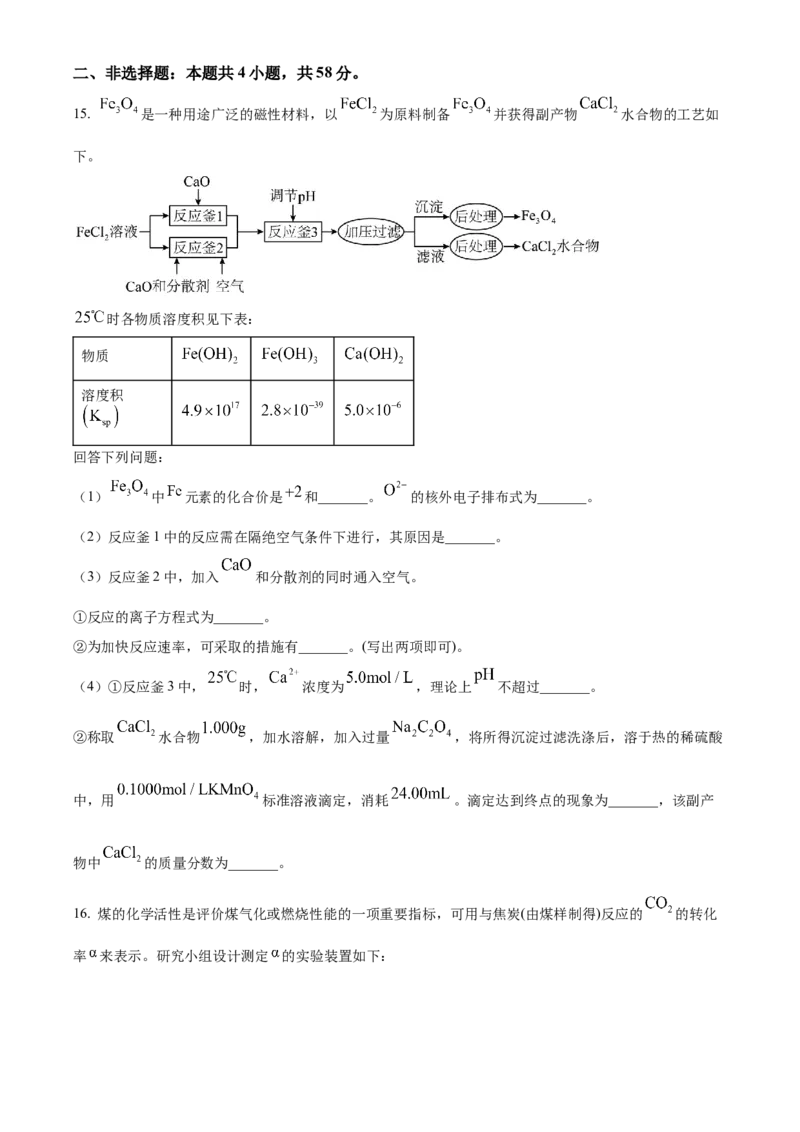
15. 是一种用途广泛的磁性材料,以 为原料制备 并获得副产物 水合物的工艺如
下。
时各物质溶度积见下表:
物质
溶度积
回答下列问题:
(1) 中 元素的化合价是 和_______。 的核外电子排布式为_______。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是_______。
(3)反应釜2中,加入 和分散剂的同时通入空气。
①反应的离子方程式为_______。
②为加快反应速率,可采取的措施有_______。(写出两项即可)。
(4)①反应釜3中, 时, 浓度为 ,理论上 不超过_______。
②称取 水合物 ,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸
中,用 标准溶液滴定,消耗 。滴定达到终点的现象为_______,该副产
物中 的质量分数为_______。
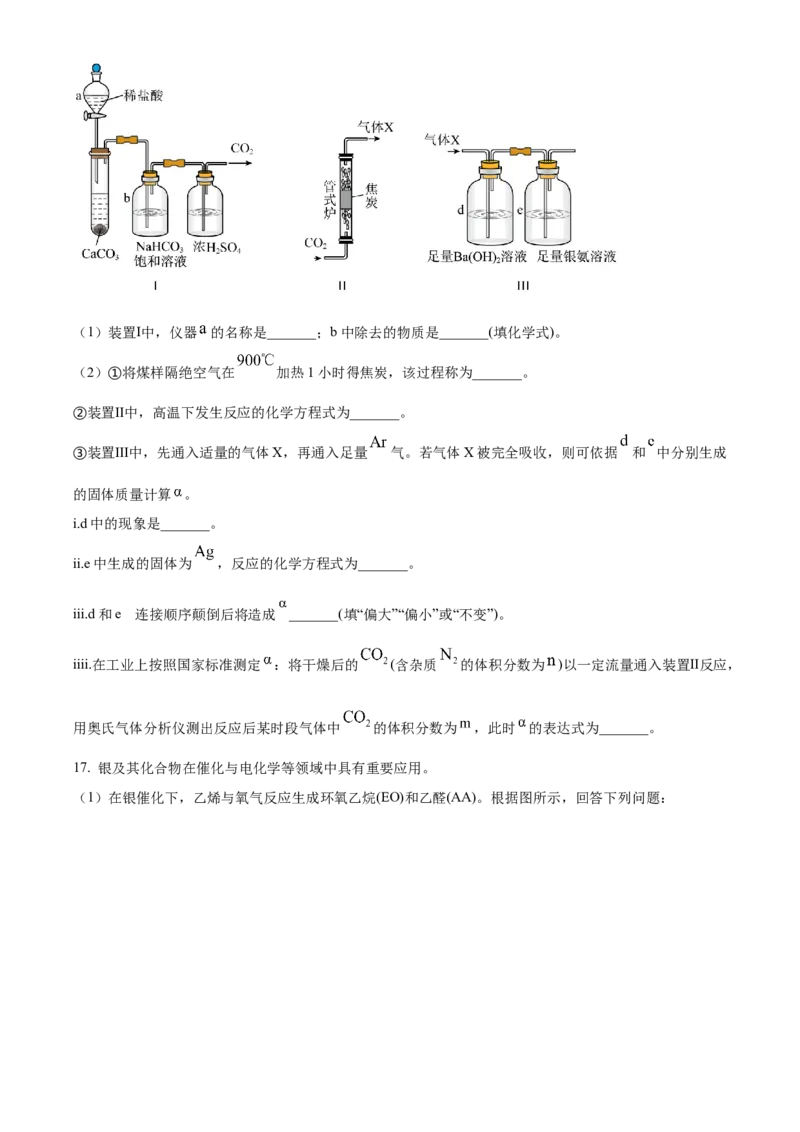
16. 煤的化学活性是评价煤气化或燃烧性能的一项重要指标,可用与焦炭(由煤样制得)反应的 的转化
率 来表示。研究小组设计测定 的实验装置如下:(1)装置Ⅰ中,仪器 的名称是_______;b中除去的物质是_______(填化学式)。
(2)①将煤样隔绝空气在 加热1小时得焦炭,该过程称为_______。
②装置Ⅱ中,高温下发生反应的化学方程式为_______。
③装置Ⅲ中,先通入适量的气体X,再通入足量 气。若气体X被完全吸收,则可依据 和 中分别生成
的固体质量计算 。
i.d中的现象是_______。
ii.e中生成的固体为 ,反应的化学方程式为_______。
的
iii.d和e 连接顺序颠倒后将造成 _______(填“偏大”“偏小”或“不变”)。
iiii.在工业上按照国家标准测定 :将干燥后的 (含杂质 的体积分数为 )以一定流量通入装置Ⅱ反应,
用奥氏气体分析仪测出反应后某时段气体中 的体积分数为 ,此时 的表达式为_______。
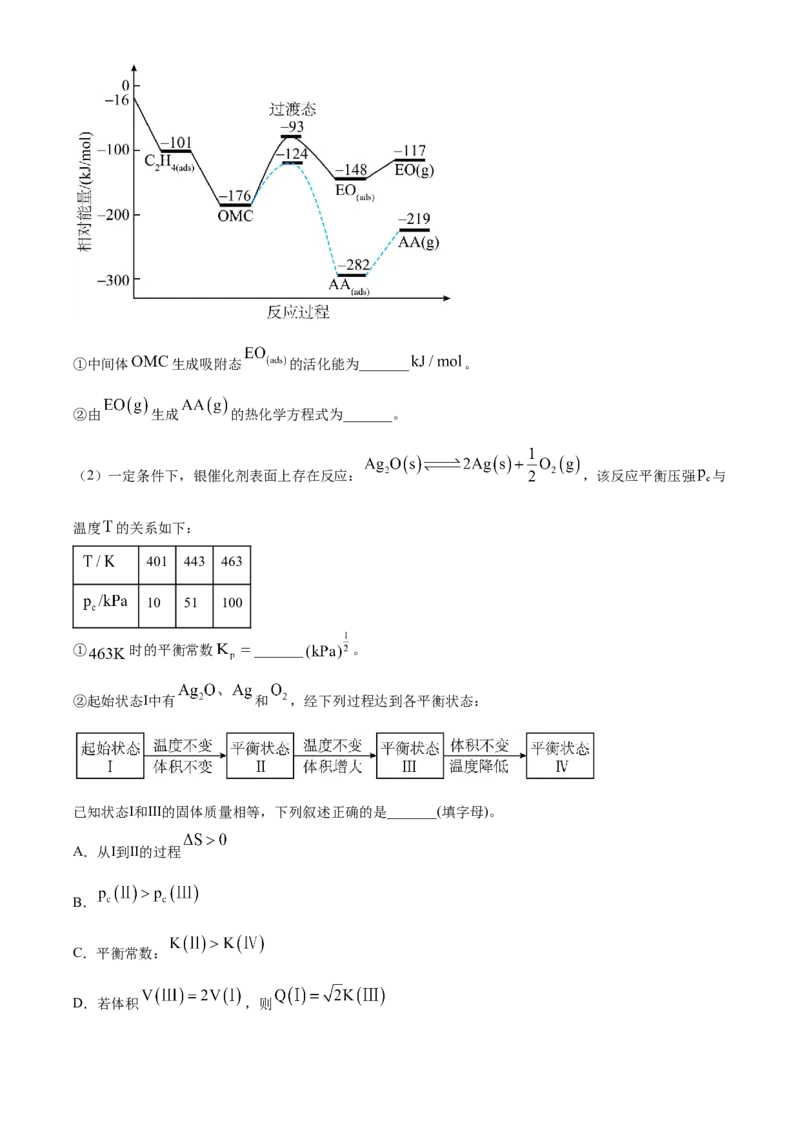
17. 银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:①中间体 生成吸附态 的活化能为_______ 。
②由 生成 的热化学方程式为_______。
(2)一定条件下,银催化剂表面上存在反应: ,该反应平衡压强 与
温度 的关系如下:
401 443 463
10 51 100
① 时的平衡常数 _______ 。
②起始状态Ⅰ中有 和 ,经下列过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是_______(填字母)。
A.从Ⅰ到Ⅱ的过程
B.
C.平衡常数:
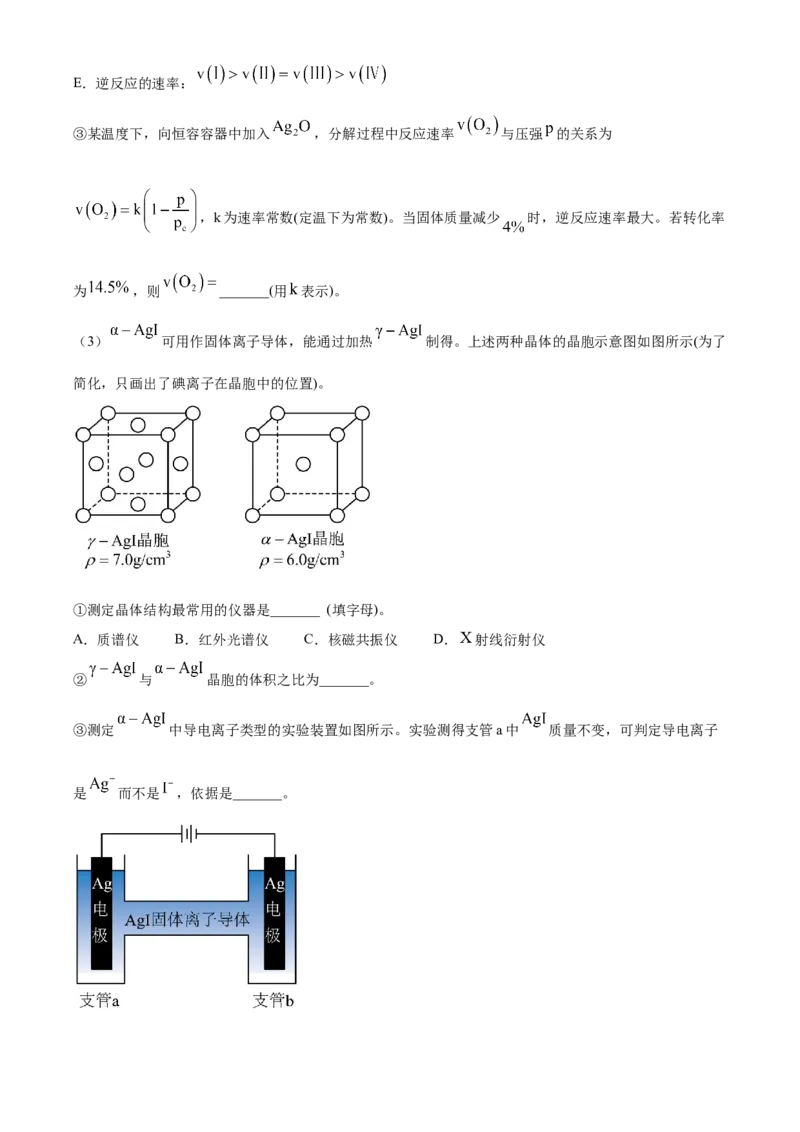
D.若体积 ,则E.逆反应的速率:
③某温度下,向恒容容器中加入 ,分解过程中反应速率 与压强 的关系为
,k为速率常数(定温下为常数)。当固体质量减少 时,逆反应速率最大。若转化率
为 ,则 _______(用 表示)。
(3) 可用作固体离子导体,能通过加热 制得。上述两种晶体的晶胞示意图如图所示(为了
简化,只画出了碘离子在晶胞中的位置)。
①测定晶体结构最常用的仪器是_______ (填字母)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D. 射线衍射仪
② 与 晶胞的体积之比为_______。
③测定 中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子
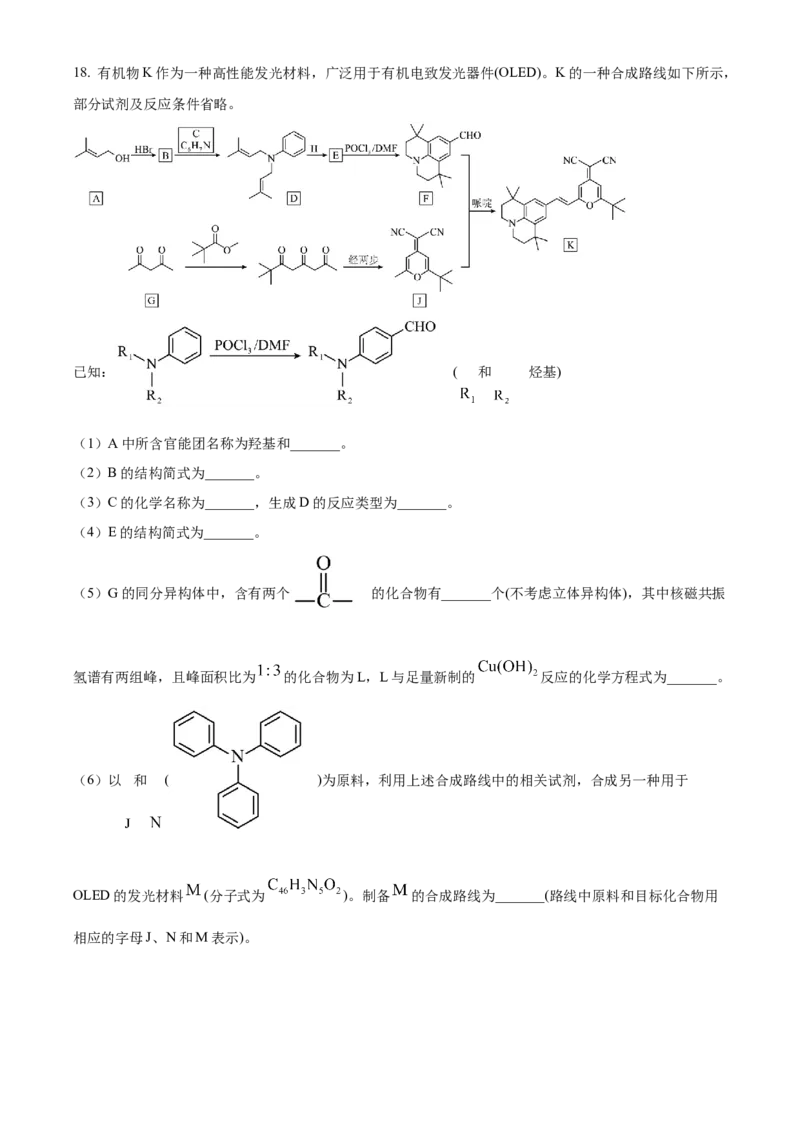
是 而不是 ,依据是_______。18. 有机物K作为一种高性能发光材料,广泛用于有机电致发光器件(OLED)。K的一种合成路线如下所示,
部分试剂及反应条件省略。
已知: ( 和 烃基)
为
(1)A中所含官能团名称为羟基和_______。
(2)B的结构简式为_______。
(3)C的化学名称为_______,生成D的反应类型为_______。
(4)E的结构简式为_______。
(5)G的同分异构体中,含有两个 的化合物有_______个(不考虑立体异构体),其中核磁共振
氢谱有两组峰,且峰面积比为 的化合物为L,L与足量新制的 反应的化学方程式为_______。
(6)以 和 ( )为原料,利用上述合成路线中的相关试剂,合成另一种用于
OLED的发光材料 (分子式为 )。制备 的合成路线为_______(路线中原料和目标化合物用
相应的字母J、N和M表示)。