文档内容
2025 届广东省省内两校十月第一次模拟
C. 纸的主要成分纤维素属于合成高分子化合物
2024.10
命题人:客路中学 龙门中学 教研组
注意事项:
D. 用工具打磨石材制砚台的过程是物理变化
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,
2.下列热化学方程式正确的是
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上
选
已知条件 热化学方程式
无效。 项
点燃
3.考试结束后,本试卷和答题卡一并交回。
A H 的燃烧热为akJ⋅mol-1 H +Cl ̲(cid:11) 2HClΔH=-akJ⋅mol-1
2 2 2 ̲(cid:11)
4.诚信考试,拒绝舞弊。
B 1molSO 2 、0.5molO 2 完全反应,2SO (g)+O (g)⇀2SO (g)ΔH=-98.3kJ⋅mol-1
2 2 3
一、单选题:本大题共16小题,共44分。 放出热量98.3kJ
↽
1.关于中国传统文化中的“文房四宝”,下列叙述中不正确的是( ) C H+ (aq)+OH- (aq)=H O(l)ΔH=H-5S7O.3k(Ja⋅q)m+oBla-1 (OH) (aq)=BaSO (s)+2H O(l)ΔH=-114.6kJ⋅mol-1
2 2 4 2 4 2
D
31g白磷(P
4
)比31g红磷能量多
P (白磷,s)=4P(红磷,s)ΔH=-4bkJ⋅mol-1
bkJ 4
A. 可用灼烧法鉴别毛笔笔头是否含蛋白质
A. A B. B C. C D. D
3.下列有关反应的离子方程式不正确的是
A. 氧化铁与稀盐酸混合:
B. 用墨写字利用了常温下碳的稳定性 Fe O +6H+=2Fe3++3H O
2 3 2
B. FeCl 溶解Cu:2Fe3++Cu=2Fe2++Cu2+
3
C. 碳酸氢钠溶液与稀 反应:
H SO CO2-+2H+=H O+CO ↑
2 4 3 2 2
学科网(北京)股份有限公司D. 氯气与碘化钾溶液: A. 无色溶液中: 、 、 、
2I-+Cl =I +2Cl- K+ N H+ SO2- Cl-
2 2 4 4
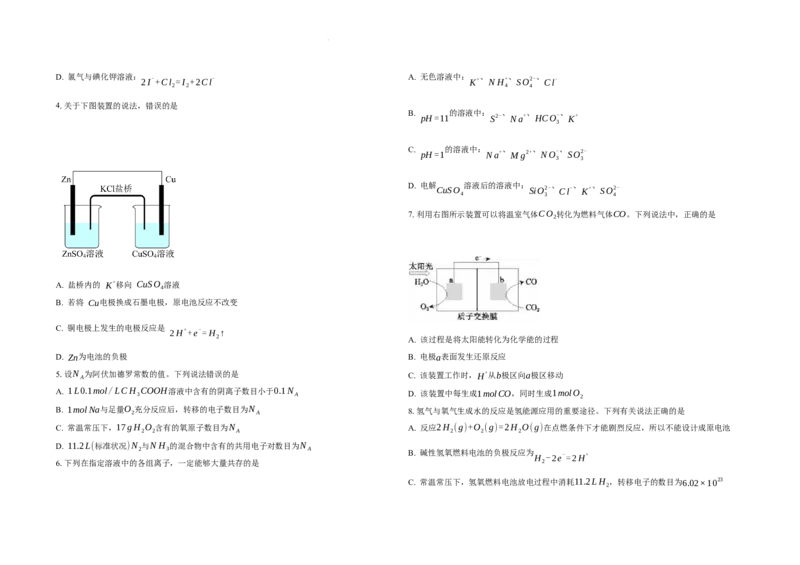
4.关于下图装置的说法,错误的是
B. 的溶液中: 、 、 、
pH=11 S2- Na+ HCO- K+
3
C. 的溶液中: 、 、 、
pH=1 Na+ M g2+ NO- SO2-
3 3
D. 电解 溶液后的溶液中: 、 、 、
CuSO SiO2- Cl- K+ SO2-
4 3 4
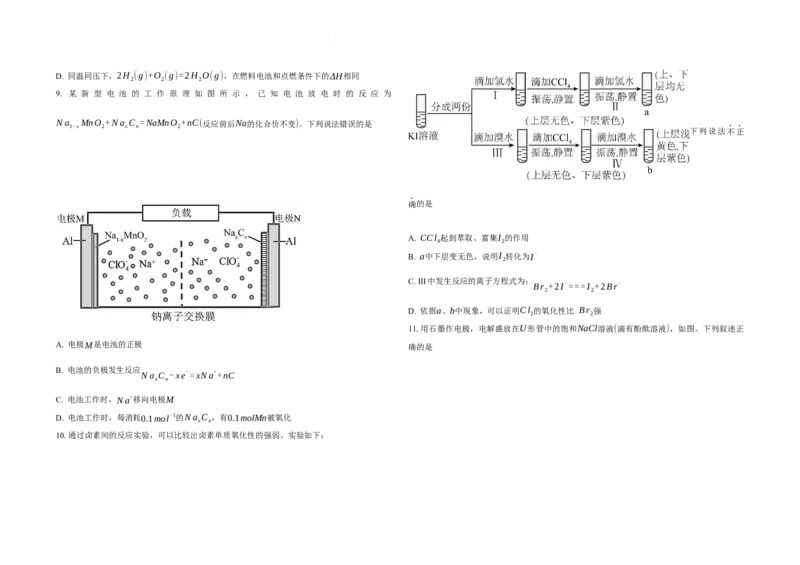
7.利用右图所示装置可以将温室气体CO 转化为燃料气体CO。下列说法中,正确的是
2
A. 盐桥内的 K+移向 CuSO 溶液
4
B. 若将 Cu电极换成石墨电极,原电池反应不改变
C. 铜电极上发生的电极反应是
2H++e-=H ↑
2 A. 该过程是将太阳能转化为化学能的过程
D. Zn为电池的负极 B. 电极a表面发生还原反应
5.设N 为阿伏加德罗常数的值。下列说法错误的是 C. 该装置工作时,H+从b极区向a极区移动
A
A. 1L0.1mol/LCH 3 COOH溶液中含有的阴离子数目小于0.1N A D. 该装置中每生成1molCO,同时生成1molO 2
B. 1molNa与足量O 充分反应后,转移的电子数目为N 8.氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
2 A
C. 常温常压下,17gH O 含有的氧原子数目为N A. 反应2H (g)+O (g)=2H O(g)在点燃条件下才能剧烈反应,所以不能设计成原电池
2 2 A 2 2 2
D. 11.2L(标准状况)N 与N H 的混合物中含有的共用电子对数目为N
2 3 A B. 碱性氢氧燃料电池的负极反应为
H -2e-=2H+
6.下列在指定溶液中的各组离子,一定能够大量共存的是 2
C. 常温常压下,氢氧燃料电池放电过程中消耗11.2LH ,转移电子的数目为6.02×1023
2
学科网(北京)股份有限公司D. 同温同压下,2H (g)+O (g)=2H O(g),在燃料电池和点燃条件下的ΔH相同
2 2 2
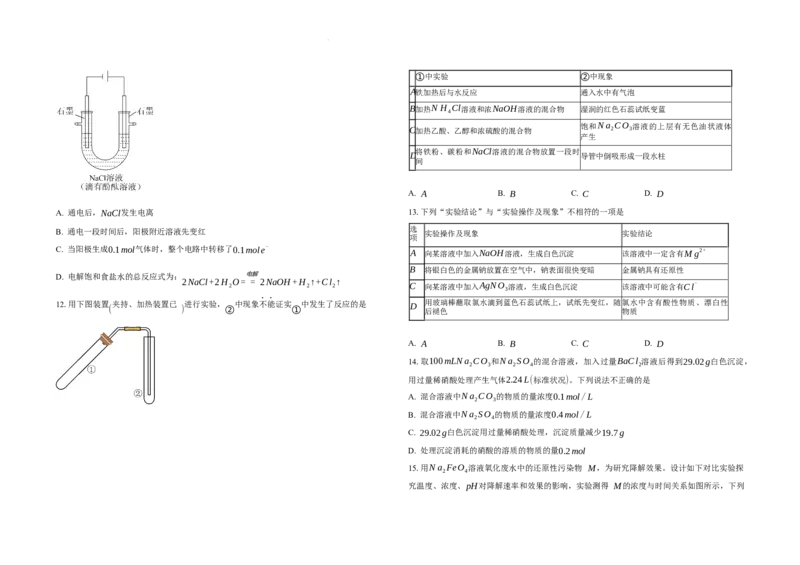
9. 某 新 型 电 池 的 工 作 原 理 如 图 所 示 , 已 知 电 池 放 电 时 的 反 应 为
Na MnO +Na C =NaMnO +nC(反应前后Na的化合价不变)。下列说法错误的是
1-x 2 x n 2
下列说法不正
确的是
A. CCl 起到萃取、富集I 的作用
4 2
B. a中下层变无色,说明I 转化为I-
2
C. Ⅲ中发生反应的离子方程式为:
Br +2I-===I +2Br-
2 2
D. 依据a、b中现象,可以证明Cl 的氧化性比 Br 强
2 2
11.用石墨作电极,电解盛放在U形管中的饱和NaCl溶液(滴有酚酞溶液),如图。下列叙述正
A. 电极M是电池的正极 确的是
B. 电池的负极发生反应
Na C -xe-=xNa++nC
x n
C. 电池工作时,Na+移向电极M
D. 电池工作时,每消耗0.1mol-1的Na C ,有0.1molMn被氧化
x n
10.通过卤素间的反应实验,可以比较出卤素单质氧化性的强弱。实验如下:
学科网(北京)股份有限公司①中实验 ②中现象
A铁加热后与水反应 通入水中有气泡
B加热N H Cl溶液和浓NaOH溶液的混合物 湿润的红色石蕊试纸变蓝
4
饱和Na CO 溶液的上层有无色油状液体
C加热乙酸、乙醇和浓硫酸的混合物 2 3
产生
将铁粉、碳粉和NaCl溶液的混合物放置一段时
D 导管中倒吸形成一段水柱
间
A. A B. B C. C D. D
A. 通电后,NaCl发生电离 13.下列“实验结论”与“实验操作及现象”不相符的一项是
选
B. 通电一段时间后,阳极附近溶液先变红 实验操作及现象 实验结论
项
C. 当阳极生成0.1mol气体时,整个电路中转移了0.1mole- A 向某溶液中加入NaOH溶液,生成白色沉淀 该溶液中一定含有M g2+
B 将银白色的金属钠放置在空气中,钠表面很快变暗 金属钠具有还原性
D. 电解饱和食盐水的总反应式为: 电解
2NaCl+2H O= = 2NaOH+H ↑+Cl ↑
2 2 2 C 向某溶液中加入AgNO 溶液,生成白色沉淀 该溶液中可能含有Cl-
3
12.用下图装置 夹持、加热装置已 进行实验, 中现象不能证实 中发生了反应的是 D 用玻璃棒蘸取氯水滴到蓝色石蕊试纸上,试纸先变红,随氯水中含有酸性物质、漂白性
( ) ② ① 后褪色 物质
A. A B. B C. C D. D
14.取100mLNa CO 和Na SO 的混合溶液,加入过量BaCl 溶液后得到29.02g白色沉淀,
2 3 2 4 2
用过量稀硝酸处理产生气体2.24L(标准状况)。下列说法不正确的是
A. 混合溶液中Na CO 的物质的量浓度0.1mol/L
2 3
B. 混合溶液中Na SO 的物质的量浓度0.4mol/L
2 4
C. 29.02g白色沉淀用过量稀硝酸处理,沉淀质量减少19.7g
D. 处理沉淀消耗的硝酸的溶质的物质的量0.2mol
15.用Na FeO 溶液氧化废水中的还原性污染物 M,为研究降解效果。设计如下对比实验探
2 4
究温度、浓度、pH对降解速率和效果的影响,实验测得 M的浓度与时间关系如图所示,下列
学科网(北京)股份有限公司说法错误的是
温 度
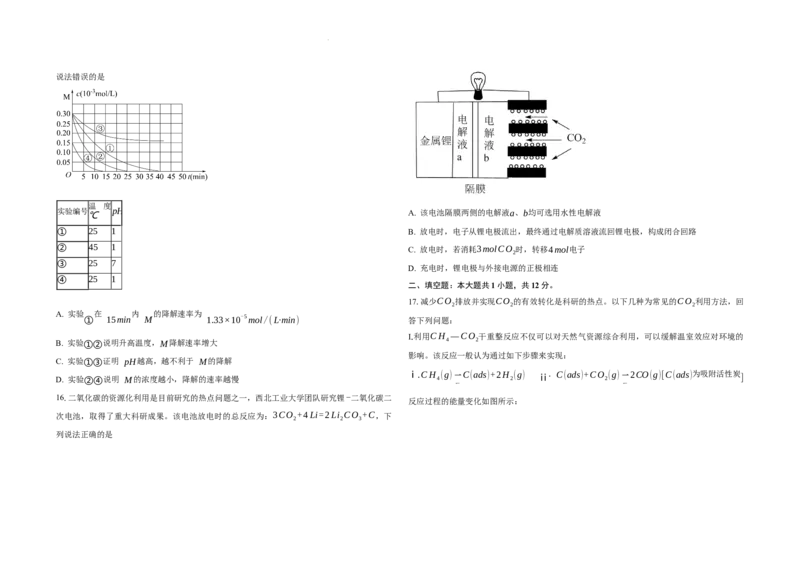
实验编号 pH A. 该电池隔膜两侧的电解液a、b均可选用水性电解液
℃
① 25 1 B. 放电时,电子从锂电极流出,最终通过电解质溶液流回锂电极,构成闭合回路
② 45 1 C. 放电时,若消耗3molCO 时,转移4mol电子
2
③ 25 7
D. 充电时,锂电极与外接电源的正极相连
④ 25 1
二、填空题:本大题共1小题,共12分。
17.减少CO 排放并实现CO 的有效转化是科研的热点。以下几种为常见的CO 利用方法,回
2 2 2
A. 实验 在 内 的降解速率为
① 15min M 1.33×10-5mol/(L·min) 答下列问题:
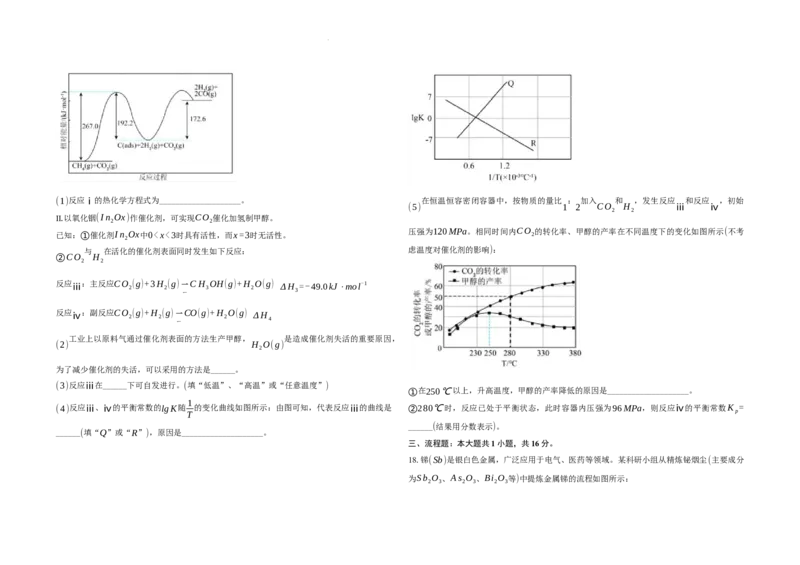
Ⅰ.利用CH —CO 干重整反应不仅可以对天然气资源综合利用,可以缓解温室效应对环境的
B. 实验①②说明升高温度,M降解速率增大 4 2
影响。该反应一般认为通过如下步骤来实现:
C. 实验①③证明 pH越高,越不利于 M的降解
D. 实验②④说明 M的浓度越小,降解的速率越慢
ⅰ.CH
4
(g)⇀C(ads)+2H
2
(g)
ⅱ
.C(ads)+CO
2
(g)⇀2CO(g)[C(ads)为吸附活性炭
]
↽ ↽
16.二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二
反应过程的能量变化如图所示:
次电池,取得了重大科研成果。该电池放电时的总反应为:3CO +4Li=2Li CO +C,下
2 2 3
列说法正确的是
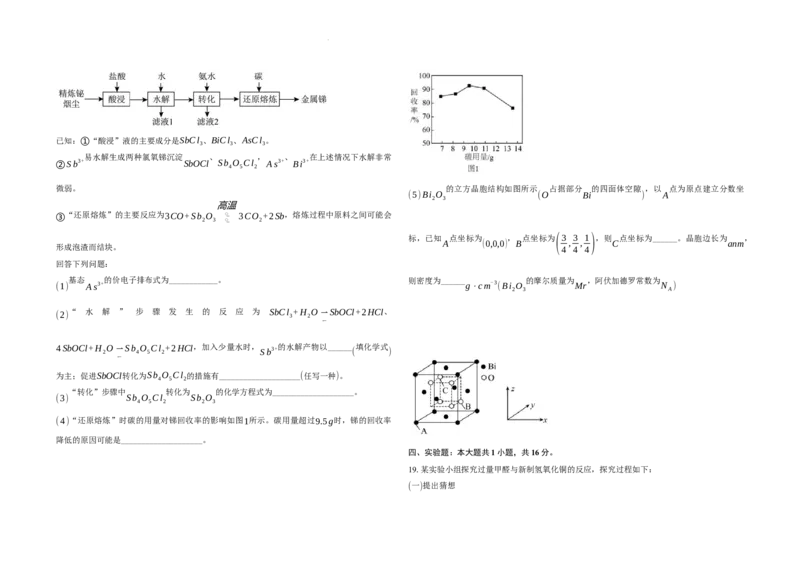
学科网(北京)股份有限公司(1)反应ⅰ的热化学方程式为____________________。 在恒温恒容密闭容器中,按物质的量比 : 加入 和 ,发生反应 和反应 ,初始
(5) 1 2 CO H ⅲ ⅳ
2 2
Ⅱ.以氧化铟(In Ox)作催化剂,可实现CO 催化加氢制甲醇。
2 2
已知:①催化剂In Ox中0Cu,因此Zn做负极,发生失电子的氧化反应,负极
H O 1mol
2 2
反应式为Zn-2e-=Zn2+;Cu做正极,CuSO 溶液中的Cu2+发生得电子的还原反应,其电极
4
B.根据1molSO 、0.5molO 完全反应后,放出热量98.3kJ可知,则2molSO 、1molO 完
2 2 2 2 反应式为Cu2++2e-=Cu;据此分析解答。
全反应后,放出热量
196.6kJ
,因此2SO (g)+O (g)⇀2SO (g)ΔH=-196.6kJ⋅mol-1, 【详解】A.在原电池中,阳离子移向正极,因此盐桥中的K+移向CuSO 4 溶液中,A正确;
2 2 3
↽ B.若将铜电极换成石墨电极,电极反应式没有变化,则原电池反应不改变,B正确;
故B错误; C.铜电极上是由CuSO 溶液中的Cu2+发生得电子的还原反应,其电极反应式为
4
C.根据 H+ (aq)+OH- (aq)=H O(l)ΔH=-57.3kJ⋅mol-1 ,生成 BaSO 沉淀,放出的热量 Cu2++2e-=Cu,C错误;
2 4
D.在该原电池中,由于金属性Zn>Cu,因此Zn做负极,D正确;
大 于 114.6kJ, 故 H
故答案选C。
,故C错误; 5.【答案】D
❑ SO (aq)+Ba(OH) (aq)=BaSO (s)+2H O(l)ΔH<-114.6kJ⋅mol-1
2 4 2 4 2
学科网(北京)股份有限公司【详解】A.CH COOH溶液中存在水的电离和醋酸的电离,水和CH COOH是弱电解质 1
3 3 D.根据得失电子守恒,该装置中每生成1molCO,同时生成 molO ,故D错误;
2 2
属于微弱电离,故1L0.1mol/LCH COOH溶液中含有的阴离子数目小于0.1N ,A正确;
3 A
故选A。
B.1molNa与足量O 充分反应,Na变为Na+转移1mole-,B正确;
2
8.【答案】D
m 17g
C.17gH O 的 物 质 的 量 为 = = =0.5mol, 含 有 的 氧 原 子 数 目 为
2 2 M 34g/mol 【详解】A.反应2H (g)+O (g)=2H O(g)是自发的氧化还原反应,能设计成原电池, A
2 2 2
2×0.5mol×N =N ,C正确; 错误;
A A
D. 与 分子中均含有 对共用电子对,故 标准状况 与 的混合物中含有的 B.碱性氢氧燃料电池的负极是氢气失去电子和氢氧根离子反应生成水,负极反应式为
N N H 3 11.2L( )N N H
2 3 2 3
,B错误;
H +2e-+2OH-=2H O
11.2L 2 2
共用电子对数目为 ×3×N =1.5N ,D错误;
22.4L/mol A A
C.常温常压下气体摩尔体积大于22.4/mol,氢氧燃料电池放电过程中消耗氢气11.2L,则氢
故选D。
气的物质的量小于0.5mol,反应转移电子小于0.5mol×2=1mol,故数目小于6.02×1023,C
6.【答案】A
错误;
【详解】A.该组离子之间不反应,离子可大量共存,且离子均为无色,故A正确;
D.反应的焓变与反应途径无关,在燃料电池和点燃条件下的ΔH相同, D正确;
B. 的溶液显碱性, 与 反应生成碳酸根离子和水,不能大量存在,故 B错误
pH=11 OH- HCO- 故选D。
3
9.【答案】D
C. 的溶液显酸性, 、 发生反应生成二氧化硫和水,不能大量共存,故 C错误;
pH=1 H+ SO2-
3 【分析】根据题给信息电池放电时的反应为Na MnO +Na C =NaMnO +nC(反应前
1-x 2 x n 2
D.电解 溶液生成铜、硫酸和氧气,反应后的溶液是硫酸, 与 反应生成硅酸, 后Na的化合价不变)可知,Mn元素化合价降低,发生得电子的还原反应,所以电极M为电池
CuSO H+ SiO2-
4 3
的正极,C元素化合价升高,Na C 在电极N发生失电子的氧化反应,据此分析解答。
x n
不能共存,故 D错误;
【 详 解 】 A.由 电 池 总 反 应 可 知 , 放 电 时 , M电 极 发 生 反 应
故选:A。
,所以电极 是电池的正极,故A正确;
7.【答案】A Na MnO +xe-+xNa+=NaMnO M
1-x 2 2
【详解】A.根据图示,该过程是将太阳能转化为化学能的过程,故A正确;
B.由电池总反应可知,放电时,电池的负极发生反应 ,故B正确;
Na C -xe-=xNa++nC
B.根据图示,电极a表面发生水转化为氧气的过程,反应中O元素的化合价升高,被氧化,发 x n
生氧化反应,故B错误; C.M是正极、N是负极,电池工作时,Na+移向电极M,故C正确;
C.根据图示,a为负极,b为正极,H+从a极区向b极区移动,故C错误; D.根据反应总方程式Na MnO +Na C =NaMnO +nC可知,每消耗0.1mol-1的Na C ,
1-x 2 x n 2 x n
学科网(北京)股份有限公司有0.1molMn被还原,故D错误;
电解 ,D正确;
2NaCl+2H O= = 2NaOH+H ↑+Cl ↑
2 2 2
答案选D。
故选;D。
10.【答案】B
【点睛】本题考查电解原理,为高频考点,侧重于学生的分析、计算能力的考查,难度一般,
【详解】A、碘单质和四氯化碳都是非极性分子,下层呈紫色,所以CCl 起到萃取、富集I
4 2
掌握离子放电顺序是解题的关键,注意基础知识的积累掌握。易错点是氢氧根离子在阴极产生
的作用,所以A选项是正确的;B、四氯化碳不溶于水,比水重,碘单质在四氯化碳中溶解度大
的判断。
于水中,四氯化碳层为紫红色,上层主要溶质是氯化钾,加氯水后,I 被氧化为碘酸根离子,
2
12.【答案】A
能溶解在水中,而不是将I 转化为I-,故B错误;C、溴单质的氧化性强于碘单质,所以溴单质
2
【详解】A.铁加热后不能与水发生反应,铁只能与水蒸气在高温条件下发生反应,②中有气
能将碘离子氧化成碘单质,发生了
Br +2I-=I +2Br-
,所以
C
选项是正确的
;D
、Ⅱ滴入氯水
泡是①中空气受热膨胀造成的,所以不能证实①中发生了反应,A符合题意;
2 2
B.加热时氯化铵与浓NaOH溶液反应生成氨气,氨气为碱性气体,遇到湿润的红色石蕊试纸会
能将碘单质氧化成无色的碘酸根离子,而Ⅳ滴入溴水下层仍呈紫色,所以氯气的氧化性强于溴
变蓝,B不符合题意;
单质,故D正确;答案:B。
C.加热乙酸、乙醇和浓硫酸的混合物,生成乙酸乙酯,饱和碳酸钠溶液可吸收乙醇、除去乙酸、
11.【答案】D
降低酯的溶解度,则充分振荡后,饱和Na CO 溶液的上层有无色油状液体乙酸乙酯析出,C
2 3
【分析】用石墨作电极电解饱和氯化钠溶液,阴极发生还原反应,电极反应式为:
不符合题意;
2H O+2e-=H ↑+2OH-
,生成
NaOH
,该极呈碱性;阳极发生氧化反应,电极反应式为: D.铁粉、碳粉和NaCl溶液的混合物,构成原电池,Fe发生吸氧腐蚀,则导管中倒吸形成一段
2 2
水柱,D不符合题意;
2Cl--2e-=Cl ↑ ,总反应为: 2NaCl+2H O= 电 = 解 2NaOH+H ↑+Cl ↑ ,以此解答该题。 故选A。
2 2 2 2
13.【答案】A
【详解】A.NaCl为强电解质,无论是否通电,在溶液中都发生电离,A错误;
【详解】A.白色沉淀可能为氢氧化铝或氢氧化镁等,由操作和现象可知,该溶液中不一定含
B.阳极生成氯气,阴极生成NaOH,则阴极附近溶液先变红,B错误;
有M g2+,故A错误;
C.阳极发生氧化反应,电极反应式为: ,生成 氯气时,转移电子为
2Cl--2e-=Cl ↑ 0.1mol B.将银白色的金属钠放置在空气中,钠表面很快变暗,说明Na与氧气发生氧化反应生成了氧
2
化钠,钠表现出还原性,故B正确;
0.2mol,C错误;
C.向某溶液中加入AgNO 溶液,生成的白色沉淀可能为Ag CO ,不一定为AgCl,则原溶
D.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠,总方程式为 3 2 3
液中可能含有Cl-,故C正确;
学科网(北京)股份有限公司D.氯水含盐酸、次氯酸,次氯酸具有漂白性,则蓝色石蕊试纸先变红,随后褪色,故D正确; A. 由 图 中 数 据 可 知 , 实 验 ①在 15min内
故选:A。
,
Δc(M)=(0.3mol/L-0.1mol/L)×10-3=2×10-4mol/L
14.【答案】A
【分析】用过量稀硝酸处理产生气体2.24L,该气体应为二氧化碳,其物质的量为:
△c 2×10-4mol/L
v(M)= = ≈1.33×10-5mol/(L⋅min),故A正确;
2.24L
△t 15min
=0.1mol;则碳酸钠的物质的量以及生成碳酸钡的物质的量均为0.1mol,生成碳
22.4L/mol
B.实验①②起始量相同,②中温度高,则说明升高温度,M降解速率增大,故B正确;
酸钡的质量为0.1mol×197g/mol=19.7g;则硫酸钡的质量为29.02-19.7=9.32g,其物质
C.实验①③中pH不同,图中曲线斜率大小证明pH越高,越不利于M的降解,故C正确;
D.实验②④中温度不同、浓度不同,不能说明浓度减小反应速率减小,故D错误;
9.32g
的量为 =0.04mol,可知Na SO 的物质的量为0.04mol,据此分析解答;
233g/mol 2 4
故选D。
【 详 解 】 A.由 以 上 分 析 可 知 Na CO 的 物 质 的 量 为 0.1mol, 则 其 浓 度 为 :
2 3 16.【答案】C
【详解】A.Li与水会反应,因此该电池隔膜左侧的电解液a不能选用水性电解液,故A错误;
0.1mol
=1mol⋅L-1,故 A错误;
0.1L B.电子不能通过电解质溶液,故B错误;
B.由以上分析可知Na
2
SO
4
的物质的量为0.04mol,混合溶液中Na
2
SO
4
的物质的量浓度 C.根据反应方程式3CO
2
+4Li=2Li
2
CO
3
+C,转移4mol电子,有3mol二氧化碳参与反应,
因此放电时,若消耗3molCO 时,转移4mol电子,故C正确;
0.04mol 2
==0.4mol/L,故B正确;
0.1L D.放电时Li为负极,因此充电时,锂电极与外接电源的负极相连,故D错误。
C.29.02g白色沉淀用过量稀硝酸处理,其中碳酸钡溶于硝酸,其质量为19.7g,故C正确; 综上所述,答案为C。
D.1mol碳酸钡消耗2mol硝酸,则0.1mol碳酸钡溶解消耗0.2mol硝酸,故D正确;
故选:A。
17.【答案】 (1) CH
4
(g)⇀C(ads)+2H
2
(g) ΔH=+74.8kJ⋅mol-1 (2) 及时将生成的
↽
15.【答案】D
H O(g)分离出来
【分析】 2
1
本题考查反应速率的计算及影响因素,为高频考点,把握图中信息及表中信息的分析、速率的 (3)低温 (4)Q 反应ⅲ的 ΔH <0 ,随温度升高,平衡常数K减小,故 lgK 随 的增大而
3 T
影响因素为解答的关键,侧重分析、计算与运用能力的考查,注意控制变量法的应用,题目难
增大
度不大。
(5)①250℃以上,反应ⅲ达到平衡,ⅲ是放热反应,升高温度,平衡逆向移动,甲醇产率
【解答】
学科网(北京)股份有限公司2
降低 ②
9
20.【答案】(1) (2分) 羧基、酯基(2分,每空1分) (2)取代反应,还原反应(2分,
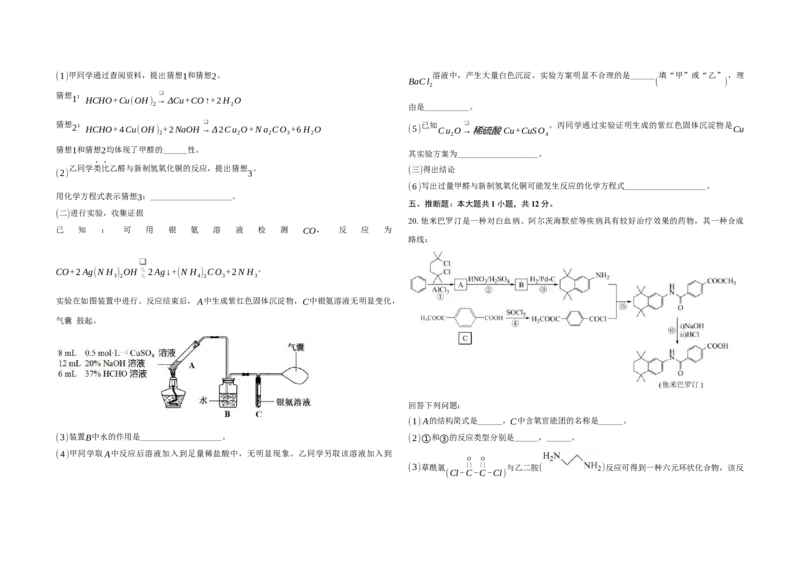
18.【答案】(1) 4s2 (2)SbOCl;加足量水、加热、用热水、加少量氨水等
每空1分,顺序写错不给分)
❑
(3) Sb O Cl +2N H ⋅H O ̲(cid:11) 2Sb O +2N H Cl+H O
4 5 2 3 2 ̲(cid:11) 2 3 4 2
(3) (2分)
碳的用量过大,会与 形成泡渣而结块,使得 与 的接触面积减小,还原效
(4) Sb O CO Sb O
2 3 2 3
率降低,回收率减小
(4)13(2分) (2分)
(1 3 3) 2Mr
(5) , ,
4 4 4 a3N ×10-21
A (5)
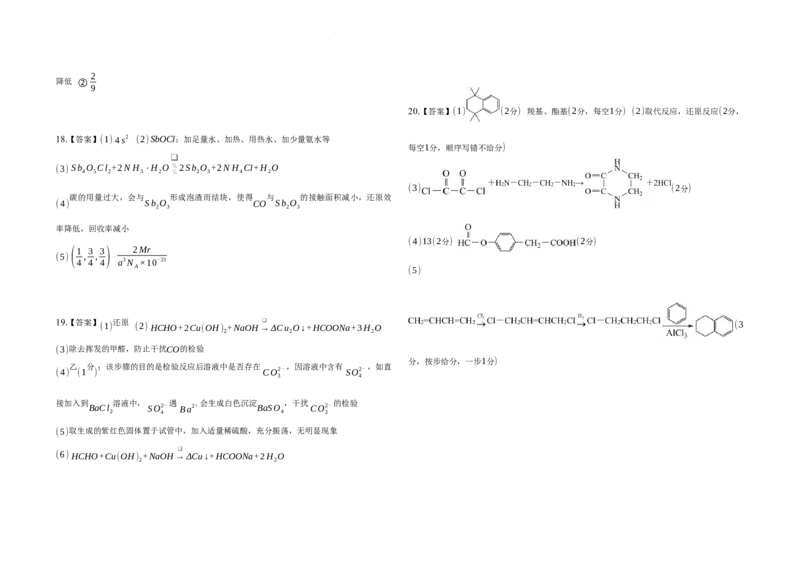
19.【答案】 (1) 还原 (2) HCHO+2Cu(OH) +NaOH→ ❑ ΔCu O↓+HCOONa+3H O (3
2 2 2
(3)除去挥发的甲醛,防止干扰CO的检验
分,按步给分,一步1分)
乙 分 ;该步骤的目的是检验反应后溶液中是否存在 ,因溶液中含有 ,如直
(4) (1 ) CO2- SO2-
3 4
接加入到 溶液中, 遇 会生成白色沉淀 ,干扰 的检验
BaCl SO2- Ba2+ BaSO CO2-
2 4 4 3
(5)取生成的紫红色固体置于试管中,加入适量稀硫酸,充分振荡,无明显现象
❑
(6) HCHO+Cu(OH) +NaOH→ΔCu↓+HCOONa+2H O
2 2
学科网(北京)股份有限公司