文档内容
房山区 2019—2020 学年度第一学期终结性检测试卷
九年级化学
考生须知:
1.本试卷共8页,共39道小题,满分90分。考试时间90分钟。
2.在试卷和答题卡上准确填写学校名称、班级和姓名。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束,将本试卷、答题卡和草稿纸一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40 Fe 56
第一部分 选择题(共40分)
一、填空题(每小题只有1个选项符合题意。每小题2分)
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
【答案】A
【解析】
空气的成分按体积计算,大约是:氮气占 78%、氧气占 21%、稀有气体占 0.94%、二氧化碳占
0.03%、其它气体和杂质占0.03%。
2.下列做法中,不符合“低碳”理念的是
A. 乱丢垃圾 B. 双面打印 C. 随手关灯 D. 公交出行
【答案】A
【解析】
【详解】A、乱丢垃圾,污染环境,增加处理环境问题的能耗,故选项不符合“低碳”理念;
B、双面使用纸张,可以减少森林的砍伐,树木可以通过光合作用吸收二氧化碳,同时还可以节约生产中
所消耗的能源,故选项符合“低碳”理念;
C、随手关灯,节约电能,能减少二氧化碳的排放,故选项符合“低碳”理念;
D、乘坐公交车出行,能减少交通工具的使用,从而减少二氧化碳的排放,故选项符合“低碳”理念。
故选:A。
【点睛】低碳理念已成为人们的共识,节能减排的措施和观念是化学考查的热点,要用低碳理念指导自己
的活动,把节能减排的措施运用到生产、生活中去.
3.蛋黄中含铁丰富。这里的“铁”指的是A. 原子 B. 分子 C. 元素 D. 单质
【答案】C
【解析】
【详解】这里的“铁”指的是不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,
与具体形态无关。
故选:C。
4.下列不属于二氧化碳(或干冰)用途的是
A. 人工降雨 B. 灭火 C. 火箭燃料 D. 制碳酸饮料
【答案】C
【解析】
A、固体二氧化碳升华吸热,能用于人工降雨,正确;B、二氧化碳既不燃烧也不支持燃烧,能用于灭火,
正确;C、二氧化碳不具有可燃性,不能用作火箭燃料,错误;D、二氧化碳能与水反应生成碳酸,可以用
于制碳酸饮料,正确。故选C。
5.下列物质中,属于溶液的是
A. 蔗糖水 B. 牛奶 C. 米粥 D. 豆浆
【答案】A
【解析】
【详解】A. 具有均一性、稳定性的混合物是溶液,蔗糖水具有均一性、稳定性,是混合物,属于溶液,此
选项符合题意;
B. 牛奶不具有均一性、稳定性,不是溶液,此选项不符合题意;
C. 米粥不具有均一性、稳定性,不是溶液,此选项不符合题意;
D. 豆浆不具有均一性、稳定性,不是溶液,此选项不符合题意。故选A。
【点睛】根据溶液是混合物,具有均一性、稳定性进行分析。
6.下列关于木炭在氧气中燃烧的说法中,不正确的是
A. 黑色固体减少 B. 燃烧时产生红光
C. 生成无色气体 D. 反应过程中放热
【答案】B
【解析】
【详解】A、木炭在氧气中充分燃烧生成二氧化碳,会观察到黑色固体减少,故选项说法正确;
B、木炭 在氧气中燃烧,发出白光,故选项说法错误;
C、木炭在氧气中充分燃烧生成二氧化碳,会观察到生成无色气体,故选项说法正确;
D、木炭在氧气中充分燃烧生成二氧化碳,反应过程中放出热量,故选项说法正确。
故选:B。7.下列实验基本操作正确的是
A. 将未用完的药品放回原试剂瓶中 B. 实验后将废液倒入下水道中
C. 将pH试纸直接放入待测液体中 D. 用镊子取用块状固体药品
【答案】D
【解析】
【详解】A、用剩的药品要做到“三不一要”:不放回原瓶;不随丢弃;不拿出实验室;要放入指定容器,
故操作错误;
B、实验产生的废液不能直接倒入下水道,以免腐蚀下水道,故操作错误;
C、用pH试纸测定未知溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃
棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能将pH试纸伸入待测液中,
以免污染待测液,故操作错误;
D、可用镊子取用块状固体药品,故操作正确。
故选:D。
8.下列中草药煎制步骤中,属于过滤操作的是
A. 冷水浸泡 B. 加热煎制 C. 箅渣取液 D. 灌装保存
【答案】C
【解析】
【详解】A、冷水浸泡属于物质的溶解,故错误;
B、加热煎制属于加热,故错误;
C、箅渣取液将固体和液体分离,属于 过滤操作,正确;
D、灌装保存是液体转移,故错误;
故选:C。
【点睛】过滤用于分离不溶性物质和液体的分离。
9.金被加工成金箔,说明金具有良好的
A. 延展性 B. 导电性 C. 导热性 D. 抗腐蚀性
【答案】A
【解析】
【详解】金被加工成金箔,说明金具有良好的延展性。故选A。
10. 下列物质中,含有氢分子的是
A. HSO B. HO C. H D. HO
2 4 2 2 2 2
【答案】C
【解析】试题分析:氢分子构成的物质是氢气;其他三种物质都含有氢元素。
考点:物质的构成微粒
11.下列金属不能与稀盐酸发生反应的是
A. 镁 B. 锌 C. 铜 D. 铁
【答案】C
【解析】
【详解】在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,镁、锌、铁均排在氢前面,铜排在
氢后面,不能与稀盐酸反应,故选:C。
12.下列方法能鉴别氧气和二氧化碳的是
A. 闻气味 B. 向集气瓶中倒入水
C. 观察颜色 D. 向集气瓶中倒入澄清石灰水
【答案】D
【解析】
【详解】A、两种气体都是没有气味的气体,用闻气体气味的方法无法鉴别,故选项错误;
B、向集气瓶中加适量水,氧气不易溶于水,二氧化碳能溶于水,无明显现象,无法鉴别,故选项错误;
C、两种气体都是没有颜色的气体,用观察颜色的方法无法鉴别,故选项错误;
D、二氧化碳能使澄清的石灰水变浑浊,氧气不能,能鉴别,故选项正确;
故选:D。
13.钛是一种广泛应用于航天和航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的
核外电子数为
A. 4 B. 22 C. 26 D. 48
【答案】B
【解析】
【详解】由题意一种Ti原子的原子核内有22个质子,根据核电荷数=质子数=电子数,故该钛原子核外的
电子数为22。
故选:B。
【点睛】本题难度不是很大,掌握原子中核电荷数=质子数=电子数是解答本题的关键。
14.为保证实验安全,下列使用酒精灯的实验操作合理的是A. 点燃酒精灯 B. 添加酒精 C.
加热液体 D. 熄灭酒精灯
【答案】C
【解析】
【详解】A、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所
示操作错误;
B、严禁给燃着的酒精灯添加酒精,图中所示操作错误;
C、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的三分之
一,图中所示操作正确;
D、酒精灯熄灭时要用灯帽盖灭,不能用嘴吹灭,图中所示操作错误。
故选:C。
【点睛】本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是
解答此类试题的关键。
15.乙醇俗称酒精,其完全燃烧的的化学方程式为:C HOH+3O 2CO+3H O,根据该化学方程式无法
2 5 2 2 2
获取的信息是
A. 反应物和生成物 B. 反应所需条件
C. 反应物 的颜色和状态 D. 生成物的分子个数比
【答案】C
【解析】【详解】A、反应物是甲醇和氧气,生成物是二氧化碳和水,故正确;
B、反应条件是点燃,故正确;
C、从该方程式中不能看出反应物的颜色和状态,故错误;
D、二氧化碳和水的分子个数比为2:3,故正确。
故选:C。
16.车载安全气囊使用了叠氮化钠(NaN )。在一定条件下NaN 迅速发生分解反应的化学方程式表示为:
3 3
2NaN 2Na+口↑,其中口表示
3
A. 5N B. N C. N D. 3N
3 2 2
【答案】D
【解析】
【详解】根据质量守恒定律,化学反应前后原子种类和数目不变,反应前有 2个钠原子,6个氮原子,反
应后2个钠原子,应该还有6个氮原子,可知空白处应该为3N,故选:D。
2
17.下列关于O 的实验室制法及性质实验的说法不正确的是
2
A制O 的药品 B发生装置 C收集装置 D验证O 的可燃性
2 2
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、实验室中用过氧化氢和二氧化锰制氧气,选项正确;
B、过氧化氢和二氧化锰制氧气属于固液常温型,可以采用B中装置制取,选项正确;
C、氧气密度比空气大,可以采用向上排空气法收集,选项正确;
D、氧气具有助燃性,不具可燃性,选项错误。
故选:D。
18.下列化学方程式书写正确的是A. CO+Ca(OH) =CaCO ↓+H O B. HO H↑+ O ↑
2 2 3 2 2 2 2 2
C. 3CO +Fe O 2Fe+3CO D. 3Fe + 4O Fe O
2 3 2 2 3 4
【答案】A
【解析】
【详解】A、该方程式书写完全正确;
B、水在通电的条件下生成氢气和氧气,方程式应为:2HO 2H↑+ O ↑,选项错误;
2 2 2
C、一氧化碳还原氧化铁,反应条件是高温,方程式应为:3CO +Fe O 2Fe+3CO ,选项错误;
2 3 2
D、选项中方程式没有配平,应该为:3Fe + 2O Fe O,选项错误。
2 3 4
故选:A。
19.不同温度时,NaCl固体的溶解度如下表所示。20℃时,将50g NaCl固体加入到盛有100g水的烧杯中,
充分溶解得到溶液。下列说法正确的是
温度/℃ 20 40 60 80 100
溶解度/g 36.0 36.6 37.3 38.4 39.8
A. 烧杯中溶液的质量为150g
B. 烧杯中剩余固体的质量为14g
C. 溶液中溶质质量分数的计算式为 ×100%D. 升高温度能将烧杯中的饱和溶液变为不饱和溶液
【答案】B
【解析】
【详解】A、20℃时氯化钠的溶解度为36g,20℃时,将50g NaCl固体加入到盛有100g水的烧杯中,烧杯
中溶液的质量为100g+36g=136g,故错误;
B、20℃时100g水中最多能溶解36g氯化钠,所以烧杯中剩余固体的质量为14g,正确;
C、溶液中溶质质量分数的计算式为 ,故错误;
D、由数据表格可以看出氯化钠的溶解度随温度的变化不大,所以升高温度不能将烧杯中的饱和溶液变为
不饱和溶液,故错误。
故选:B。
20.中国科学家成功将二氧化碳转化为乙烯(C H),其反应前后分子种类的微观示意图如图所示。下列
2 4
说法不正确的是
A. 反应中原子种类没有改变
B. 反应前后分子种类发生了改变
C. 丙和丁中的氢元素全部来自于乙中
D. 参加反应的甲与生成的丙质量比为11:7
【答案】D
【解析】
【分析】
由变化的微观示意图可知,该反应是二氧化碳和氢气在一定条件下反应生成乙烯和水,方程式是:
【详解】A、由示意图可知,反应中原子种类没有改变,故正确;
B、由方程式可以看出反应前后分子种类发生了改变,故正确;
C、甲是二氧化碳,不含氢元素,乙是氢气,由氢元素组成,所以丙和丁中的氢元素全部来自于乙中,正
确;D.由化学方程式可知,参加反应的甲与丙的质量比为88:28=22:7,故错误。
故选:D。
第二部分 非选择题(共50分)
二、填空题(每空1分)
〖生活现象解释〗
21.垃圾分类就是新时尚。在去博物馆的路上,小明将空饮料瓶投入到下列______(填序号)垃圾桶中。
【答案】A
【解析】
【详解】矿泉水空瓶属于可回收物,并且无毒无害,应放入可回收物垃圾桶中。
故选:A。
22.在饮料的配料中,有一种食品添加剂是苯甲酸钠(C HNaO )。其中碳氧原子的个数比为___________。
7 5 2
【答案】7:2
【解析】
【详解】由苯甲酸钠化学式(C HNaO )可知,碳、氧原子个数比为:7:2。
7 5 2
23.碳酸饮料需“避免阳光直晒及高温”贮存的原因之一是__________________(用化学方程式解释)。
【答案】HCO=H O+CO↑
2 3 2 2
【解析】【详解】二氧化碳和水生成碳酸,直晒或高温碳酸分解成水和二氧化碳,方程式为:HCO=H O+CO↑。
2 3 2 2
24.参观过程中,小明发现了一种陶瓷电容器(如图),主要材料为TiO 等。
2
(1)TiO 属于____________(填序号)。
2
A单质 B化合物 C氧化物
(2)TiO 中Ti的化合价为________。
2
【答案】 (1). BC (2). +4
【解析】
【详解】(1)TiO 由两种元素组成,其中一种为氧元素,属于化合物中的氧化物,故选:BC。
2
(2)TiO 中O化合价为-2价,设Ti的化合价为x,根据在化合物中,各元素正负化合价的代数和为零,
2
则有x+(-2)×2=0,解得x=+4。
25.如图是一款燃气灶的示意图。
(1)铸铁炉架表面经过四氧化三铁处理,四氧化三铁中铁、氧元素的质量比为__________。
(2)烹饪时,用铸铁炉架将锅架高,其主要原因是__________(填序号)。
A避免锅被烤坏 B避免食物被烤焦 C使用外焰加热
(3)燃气灶常用天然气、液化石油气等燃气,天然气主要成分燃烧的化学方程式为______________。
(4)燃气灶关火的方法是关闭燃气阀门,其灭火的原理是_________。
【答案】 (1). 21:8(168:64) (2). C (3). CH+2O 2HO + CO (4). 清除可燃物
4 2 2 2
【解析】【详解】(1)四氧化三铁中铁、氧元素的质量比为: 。
(2)外焰温度最高,适宜加热,烹饪时,用铸铁炉架将锅架高,其主要原因是使用外焰加热,故选:C。
(3)天然气主要成分是甲烷,甲烷燃烧生成二氧化碳和水,反应方程式为:CH+2O 2HO + CO 。
4 2 2 2
(4)燃气灶关火的方法是关闭燃气阀门,其灭火的原理是清除可燃物。
26.均衡饮食是健康的基础。
(1)如图是中国居民平衡膳食餐盘,其中富含维生素的食物有_________。
(2)牛奶中含丰富的钙,多喝牛奶可预防_______(填“骨质疏松”或“贫血”)。
【答案】 (1). 蔬菜水果 (2). 骨质疏松
【解析】
【详解】(1)其中富含维生素的食物有:蔬菜水果;
(2)牛奶中含丰富的钙,多喝牛奶可预防骨质疏松。
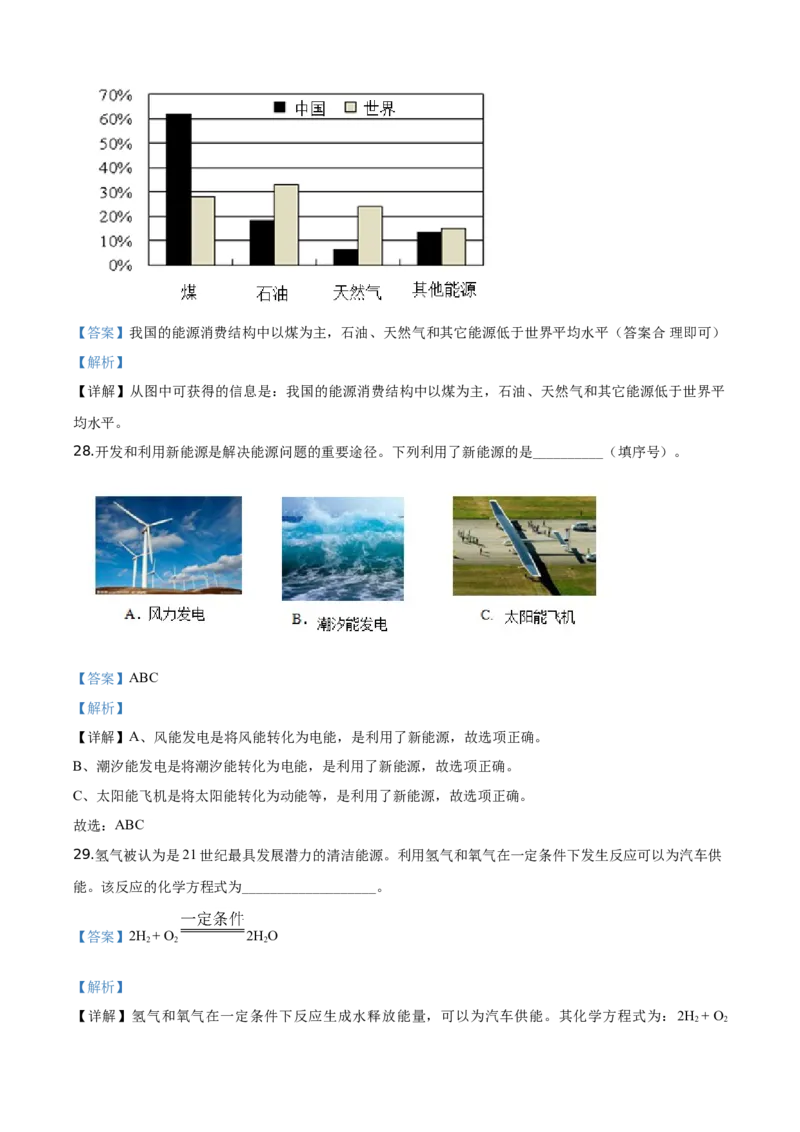
27.人类社会的发展离不开能源。如图是我国和世界能源消费结构的对比图。从图中可获得的信息是
____________________。【答案】我国的能源消费结构中以煤为主,石油、天然气和其它能源低于世界平均水平(答案合 理即可)
【解析】
【详解】从图中可获得的信息是:我国的能源消费结构中以煤为主,石油、天然气和其它能源低于世界平
均水平。
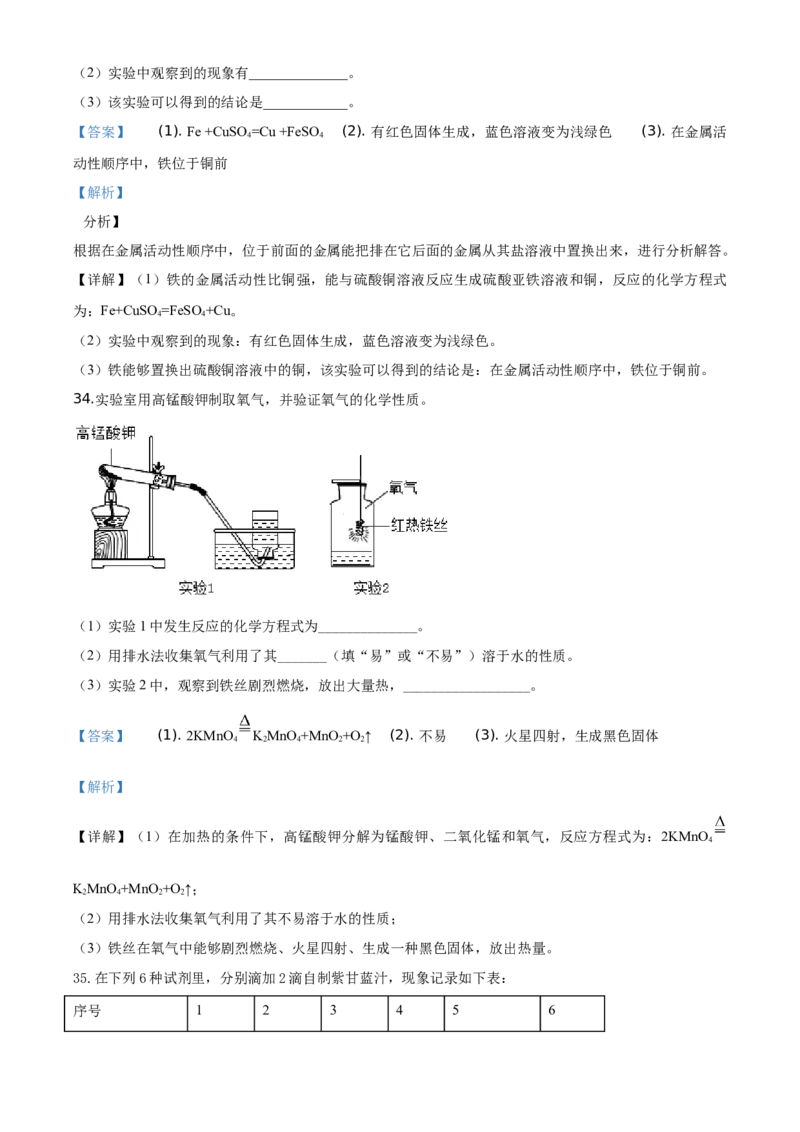
28.开发和利用新能源是解决能源问题的重要途径。下列利用了新能源的是__________(填序号)。
【答案】ABC
【解析】
【详解】A、风能发电是将风能转化为电能,是利用了新能源,故选项正确。
B、潮汐能发电是将潮汐能转化为电能,是利用了新能源,故选项正确。
C、太阳能飞机是将太阳能转化为动能等,是利用了新能源,故选项正确。
。
故选:ABC
29.氢气被认为是21世纪最具发展潜力的清洁能源。利用氢气和氧气在一定条件下发生反应可以为汽车供
能。该反应的化学方程式为___________________。
【答案】2H + O 2HO
2 2 2
【解析】
【详解】氢气和氧气在一定条件下反应生成水释放能量,可以为汽车供能。其化学方程式为:2H + O
2 22HO。
2
〖科普阅读理解〗
30.阅读下面科普短文。
俗话说:“过了腊八就是年”,因此泡制腊八蒜已成为一种过年的习俗。
腊八蒜的制作方法是将蒜瓣剥皮洗净,放到密封容器里,倒入陈醋或米醋,封口冷藏。一段时间后,蒜会
变得通体碧绿。
腊八蒜为什么会变绿?
腊八蒜呈现绿色是天然色素造成的。大蒜细胞中含有较多的含硫类生物活性物质,这些物质在蒜酶和醋酸
的作用下,经过一系列反应可生成两种大蒜色素——黄色素和蓝色素,从而使蒜呈现绿色。其中蓝色素性
质不稳定,温度略高就容易分解,光照会加速分解。而黄色素较稳定,在酸性环境中,升温和光照都不会
使其分解。因此存放一段时间后的腊八蒜,其颜色就会从蓝绿色慢慢变成黄绿色,再逐渐变成浅黄色。
腊八蒜为什么在“腊八”泡制?
实践中发现将6月初新收获的大蒜直接用于加工腊八蒜,是不会变绿的。在7至9 月这几个温度较高的月
份,常温贮存一段时间的新蒜用于加工腊八蒜也不能变绿。综上可得,温度对于大蒜绿变具有至关重要的
作用。低温可打破大蒜休眠、激活蒜酶、促使大蒜绿变。将刚采摘的新蒜在不同温度条件下贮存,测得其
绿变能力趋势如图。
一般情况下,腊八蒜里的蓝色素会在泡制25天左右达到峰值,到40天左右,腊八蒜基本上已经由绿色完
全变为黄色。而“腊八”距离除夕一般是21天或22天,这个时间间隔恰好使腊八蒜在过年时呈现出最巅
峰的色泽和味道。
怎样保持腊八蒜的绿色?
研究表明,保持4℃的低温,控制pH在4.0左右,并使用真空包装和避光条件,腊八蒜就能保存三个月以
上而不变黄。
依据文章内容回答下列问题。(1)泡制腊八蒜所用的醋中含有醋酸(CHCOOH),其组成元素有__________种。
3
(2)泡制腊八蒜最好选用____________条件下贮存的蒜(填序号,下同)。
A0~4℃、贮存20天左右 B0~4℃、贮存80天左右
C常温、贮存20天左右 D常温、贮存80天左右
(3)选在腊八节泡蒜的原因是______________________。
(4)下列说法正确的是_________。
A腊八蒜呈现绿色由于加入了人工色素
B较高的贮存温度不利于使大蒜具有绿变能力
C在腊八蒜的泡制过程中,避光处理可避免腊八蒜过早变黄
(5)生活中,延长腊八蒜绿色时间的措施有__________________。
【答案】 (1). 3 (2). B (3). 温度、时间适宜,能使蓝色素在春节达到峰值 (4). BC (5). 放
入冰箱内冷藏(答案合理即可)
【解析】
【详解】(1)由醋酸分子式(CHCOOH),可知醋酸由碳、氢、氧三种元素组成;
3
(2)由趋势图可知泡制腊八蒜最好选用0~4℃,可以贮存80天左右,故选:B。
(3)腊八蒜最好选用0~4℃条件下贮存,一般情况下,腊八蒜里的蓝色素会在泡制25天左右达到峰值,
而“腊八”距离除夕一般是21天或22天,这个时间间隔恰好使腊八蒜在过年时呈现出最巅峰的色泽和味道。
(4)A腊八蒜呈现绿色是天然色素造成的。大蒜细胞中含有较多的含硫类生物活性物质,这些物质在蒜
酶和醋酸的作用下,经过一系列反应可生成两种大蒜色素——黄色素和蓝色素,从而使蒜呈现绿色,故选
项说法错误;
B由图表可知,较高的贮存温度不利于使大蒜具有绿变能力,故选项说法正确;
C研究表明,保持4℃的低温,控制pH在4.0左右,并使用真空包装和避光条件,腊八蒜就能保存三个月
以上而不变黄,故选项说法正确;
故选:BC。
(5)生活中,延长腊八蒜绿色时间的措施有:放入冰箱内冷藏、使用避光容器贮存等。
〖生产实际分析〗
31.工业上常用“分离液态空气法”制氧气,此方法是以空气为原料,利用液氮与液氧沸点不同,将其分离。
其微观示意图如下:(1)“分离液态空气法”发生的是________(填“物理变化”或“化学变化”)。
(2)下列说法正确的是_______(填序号,下同)。
A洁净空气是纯净物 B此方法制氧气的原料来源广泛
C沸点属于物理性质 D利用此方法既可得到氧气又可得到氮气
(3)下列能表示液态空气微观示意图的是_____。
【答案】 (1). 物理变化 (2). BCD (3). B
【解析】
【详解】(1)“分离液态空气法”,只是将成分分离出来,没有新物质生成,属于物理变化;
(2)A 空气中有氮气、氧气、二氧化碳等,属于混合物,选项错误;
B此方法制氧气的原料是空气,来源广泛,故正确;
C沸点属于物理性质,正确;
D此方法是以空气为原料,利用液氮与液氧沸点不同,将其分离,利用此方法既可得到氧气又可得到氮气,
故选项正确;
故选:BCD。
(4)洁净的空气为气态。分子间隔大,冷却压缩成为液态空气,分子种类与数目不变,只是分子间隔变
小,故B能表示液态空气微观示意图。
32.氢氧化钙 [Ca(OH) ] 是重要的建筑材料,工业上常以石灰石(主要成分为CaCO )为原料生产氢氧化钙,
2 3
主要流程如下:(1)氢氧化钙[Ca(OH) ]的组成元素中,属于金属元素的是_______________。
2
(2)粉碎石灰石的目的是_____________。
(3)煅烧炉中,发生的反应为CaCO CaO + CO ↑,此反应属于基本反应类型中________反应。
3 2
(4)消化池中发生的反应为CaO +H O = Ca(OH) ,若56t CaO参加反应,可产生的Ca(OH) 质量为
2 2 2
________t。
【答案】 (1). 钙元素(Ca) (2). 增大反应物的受热面积,使反应更充分 (3). 分解 (4). 74
【解析】
【详解】(1)氢氧化钙[Ca(OH) ]的组成元素中,属于金属元素的是:钙元素。
2
(2)粉碎石灰石的目的是:增大反应物的受热面积,使反应更充分;
(3)该反应中反应物为一种,生成物为两种,属于分解反应;
(4)设生成氢氧化钙的质量为x:
x=74t
〖基本实验及其原理分析〗
33.利用如图所示实验,验证金属活动性顺序。
(1)发生反应的化学方程式为_____________。(2)实验中观察到的现象有______________。
(3)该实验可以得到的结论是____________。
【答案】 (1). Fe +CuSO =Cu +FeSO (2). 有红色固体生成,蓝色溶液变为浅绿色 (3). 在金属活
4 4
动性顺序中,铁位于铜前
【解析】
【分析】
根据在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,进行分析解答。
【详解】(1)铁的金属活动性比铜强,能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式
为:Fe+CuSO=FeSO+Cu。
4 4
(2)实验中观察到的现象:有红色固体生成,蓝色溶液变为浅绿色。
(3)铁能够置换出硫酸铜溶液中的铜,该实验可以得到的结论是:在金属活动性顺序中,铁位于铜前。
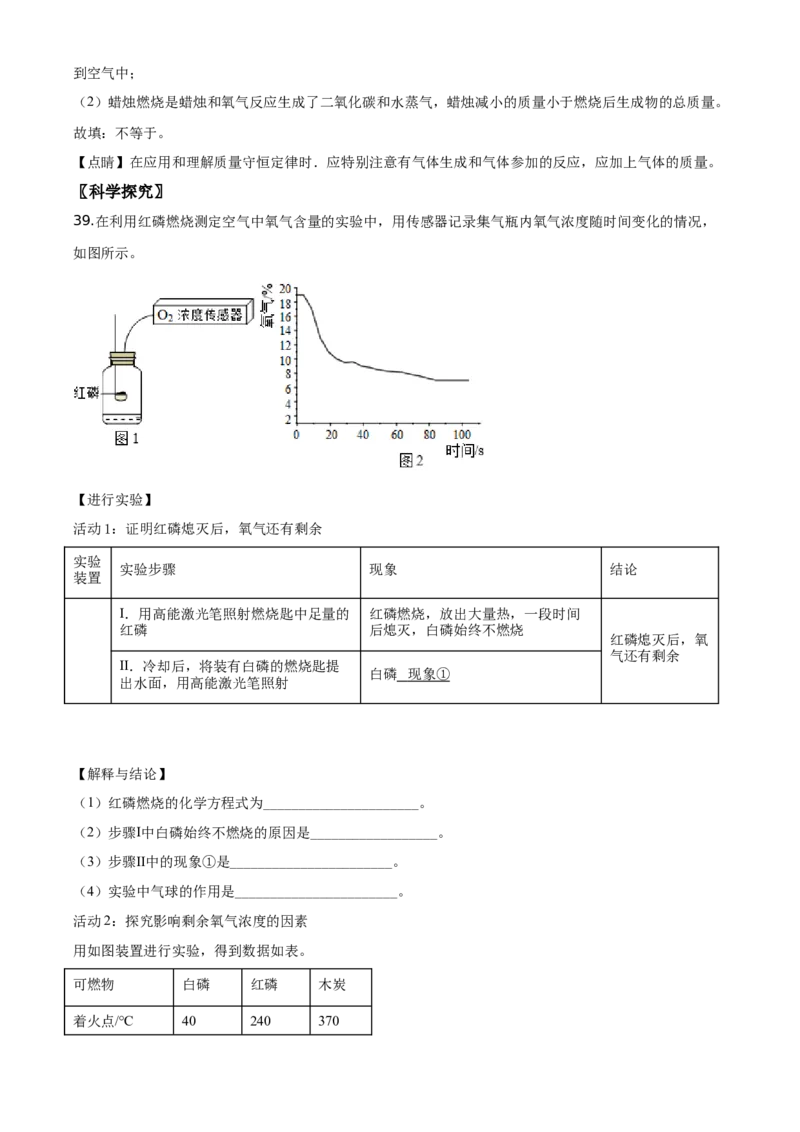
34.实验室用高锰酸钾制取氧气,并验证氧气的化学性质。
(1)实验1中发生反应的化学方程式为______________。
(2)用排水法收集氧气利用了其_______(填“易”或“不易”)溶于水的性质。
(3)实验2中,观察到铁丝剧烈燃烧,放出大量热,__________________。
【答案】 (1). 2KMnO KMnO +MnO+O ↑ (2). 不易 (3). 火星四射,生成黑色固体
4 2 4 2 2
【解析】
【详解】(1)在加热的条件下,高锰酸钾分解为锰酸钾、二氧化锰和氧气,反应方程式为:2KMnO
4
KMnO +MnO+O ↑;
2 4 2 2
(2)用排水法收集氧气利用了其不易溶于水的性质;
(3)铁丝在氧气中能够剧烈燃烧、火星四射、生成一种黑色固体,放出热量。
35.在下列6种试剂里,分别滴加2滴自制紫甘蓝汁,现象记录如下表:
序号 1 2 3 4 5 6试剂 稀盐酸 石灰水 蒸馏水 白醋 草木灰溶液 食盐水
滴加紫甘蓝汁后 红色 绿色 紫色 红色 绿色 紫色
(1)紫甘蓝汁_______(填“能”或“不能”)作酸碱指示剂。
(2)草木灰溶液显________(填“酸性”、“中性”或“碱性”)。
(3)作为空白对照实验的是______________(填序号)。
【答案】 (1). 能 (2). 碱性 (3). 3
【解析】
【详解】(1)稀盐酸显酸性,能使紫甘蓝汁由紫色变成红色;石灰水呈碱性,能使紫甘蓝汁由紫色变成
绿色,蒸馏水呈中性,紫甘蓝汁不变色,所以紫甘蓝汁可以做酸碱指示剂;
(2)草木灰溶液能使紫甘蓝汁变成绿色,所以草木灰溶液显碱性;
(3)向“蒸馏水中滴加紫甘蓝汁”的目的是检验不是水能使紫甘蓝汁变色,起到了空白对照实验的作用。
【点睛】掌握酸碱指示剂好的溶液酸碱性的关系的知识是解答本题的关键。
36.实验室配制100 g溶质质量分数为6%的氯化钠溶液。实验操作如下:
(1)正确的实验操作顺序是_______________(填序号)。
(2)操作②中托盘天平需要称量氯化钠的质量为__________g。
(3)操作④中玻璃棒起到的作用是_____________。
(4)操作⑤中量筒的量程是_____________(填“10mL”、“50mL”或“100mL”)。
【答案】 (1). ③②①⑤④ (2). 6 (3). 搅拌,加速氯化钠的溶解 (4). 100mL
【解析】
【详解】(1)配制该溶液的操作顺序为计算、称量、量取、溶解,所以序号为③②①⑤④;
(2)实验室配制100 g溶质质量分数为6%的氯化钠溶液,需要称量氯化钠的质量为:100g×6%=6g;
(3)操作④中玻璃棒起到的作用是:搅拌,加速氯化钠的溶解;
(4)需要水当当质量为100g-6g=94g,需要水94g÷1g/ml=94mL,所以应选用100mL的量筒。
【点睛】本题考查了配制溶质质量分数一定的溶液,要合理选择所用的实验仪器和实验步骤,并且注意实
验过程中正确实验操作的问题。。
37.用下图装置进行实验
(1)实验1中发生反应的化学方程式为_______。
(2)实验1中将燃着的木条放在集气瓶口,若观察到______________,说明二氧化碳已收集满。
(3)实验2中,a、b为润湿的紫色石蕊棉球,c、d为干燥的紫色石蕊棉球。实验中能说明二氧化碳密度
大于空气且能与水反应的现象有_____________________。
【答案】 (1). CaCO +2HCl=CaCl +H O+CO↑ (2). 木条熄灭 (3). c、d不变色,b比a先由紫色
3 2 2 2
变为红色
【解析】
【详解】(1)大理石主要成分是碳酸钙,盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,反应方程式为:
CaCO +2HCl=CaCl +H O+CO↑;
3 2 2 2
(2)二氧化碳不燃烧且不支持燃烧,所以实验1中将燃着的木条放在集气瓶口,若观察到木条熄灭,说明
二氧化碳已收集满;
(3)a、b为润湿的紫色石蕊棉球,c、d为干燥的紫色石蕊棉球。c、d不变色,a、b变色。证明二氧化碳
不能使紫色石蕊变色,二氧化碳与水反应生成碳酸,碳酸呈酸性,可以使紫色石蕊试剂变红;若b先变红,
说明二氧化碳先与下面棉球中水反应,证明二氧化碳的密度比空气大。
38.小明用电子秤进行如图所示的称量活动。经过一段时间后,活动1和活动2的电子秤示数都减小了。
(1)活动1的电子秤示数减小,从微粒的角度解释其原因是_________________________。
(2)活动2中电子秤示数减小的部分________(填“等于”或“不等于”)蜡烛燃烧后生成物的总质量。
【答案】 (1). 分子运动到空气中 (2). 不等于
【解析】
【详解】(1)酒精易挥发,所以,活动1的电子秤示数减小,从微粒的角度解释其原因是:酒精分子运动到空气中;
(2)蜡烛燃烧是蜡烛和氧气反应生成了二氧化碳和水蒸气,蜡烛减小的质量小于燃烧后生成物的总质量。
故填:不等于。
【点睛】在应用和理解质量守恒定律时.应特别注意有气体生成和气体参加的反应,应加上气体的质量。
〖科学探究〗
39.在利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶内氧气浓度随时间变化的情况,
如图所示。
【进行实验】
活动1:证明红磷熄灭后,氧气还有剩余
实验
实验步骤 现象 结论
装置
Ⅰ.用高能激光笔照射燃烧匙中足量的 红磷燃烧,放出大量热,一段时间
红磷 后熄灭,白磷始终不燃烧
红磷熄灭后,氧
气还有剩余
Ⅱ.冷却后,将装有白磷的燃烧匙提
白磷 现象①
出水面,用高能激光笔照射
【解释与结论】
(1)红磷燃烧的化学方程式为______________________。
(2)步骤Ⅰ中白磷始终不燃烧的原因是__________________。
(3)步骤Ⅱ中的现象①是_______________________。
(4)实验中气球的作用是_______________________。
活动2:探究影响剩余氧气浓度的因素
用如图装置进行实验,得到数据如表。
可燃物 白磷 红磷 木炭
着火点/℃ 40 240 370生成物状态 固态 固态 气态
剩余氧气浓度 3.1% 7.0% 14.0%
(5)通过对比右表中红磷和白磷的相关数据,可以得出影响剩余氧气浓度的因素可能是________。
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因
可能有________。
【答案】 (1). 4P+5O 2PO (2). 未与氧气接触 (3). 燃烧 (4). 防止污染物进入空气,
2 2 5
保护环境,还可以缓冲瓶内的压力 (5). 可燃物的着火点 (6). 木炭燃烧的生成物是气体,剩余氧气
浓度较大
【解析】
【详解】[解释与结论]
(1)红磷燃烧生成五氧化二磷,反应方程式为:4P+5O 2PO;
2 2 5
(2)步骤Ⅰ中白磷始终不燃烧的原因是:未与氧气接触;
(3)步骤Ⅱ中的现象①是:白磷燃烧,因为白磷提出水面与氧气接触,温度达到白磷着火点,所以白磷
燃烧。
(4)红磷燃烧生成的五氧化二磷会污染空气,气球的作用是:防止污染物进入空气,保护环境,还可以
缓冲瓶内的压力;
(5)由图表数据可知,白磷和红磷比较,白磷着火点最低,瓶内剩余氧气最少,红磷着火点最高,瓶内
剩余氧气最多,所以影响剩余氧气浓度的因素可能是可燃物的着火点;
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能
有:木炭燃烧生成物的气体,瓶中压强变化不大,无法测量消耗氧气的量,而且木炭燃烧完剩余氧气浓度
大,测量结果不准确。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635