文档内容
通州区 2022 一 2023 学年第一学期九年级期末质量检测
化学试卷
考生须知:
1.本试卷共8页,共两部分,37道小题,满分70分。考试时间为70分钟。
2.在试卷和答题卡(纸)上准确填写学校名称、班级、姓名。
3.试题答案一律填涂或书写在答题卡(纸)上,在试卷上作答无效。
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束后,请将答题卡交回。
可能用到的相对原子质量:H1 C12 O16 Mg24 C135.5
第一部分 选择题(共25分)
选择题(每个小题只有1个选项符合题意,每题1分。)
1. 在空气的成分中,体积分数约占21%的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
2. 地壳中含量最多的元素是
A. 硅 B. 氧 C. 铁 D. 铝
3. 下列物质能在空气中燃烧并产生白烟的是
A. 铁丝 B. 红磷 C. 木炭 D. 氢气
4. “高钙奶”、“低钠盐”中的“钙”、“钠”指的是
A. 分子 B. 原子 C. 元素 D. 单质
5. 碳元素与氧元素的本质区别是
A. 质子数不同 B. 电子数不同 C. 中子数不同 D. 最外层电子数不同
6. 吸烟有害健康,烟气中的一种有毒气体是( )
A. N B. CO C. O D. CO
2 2 2
7. 下列符号表示2个氢原子的是
A. 2H B. 2H+ C. H D. 2H
2 2
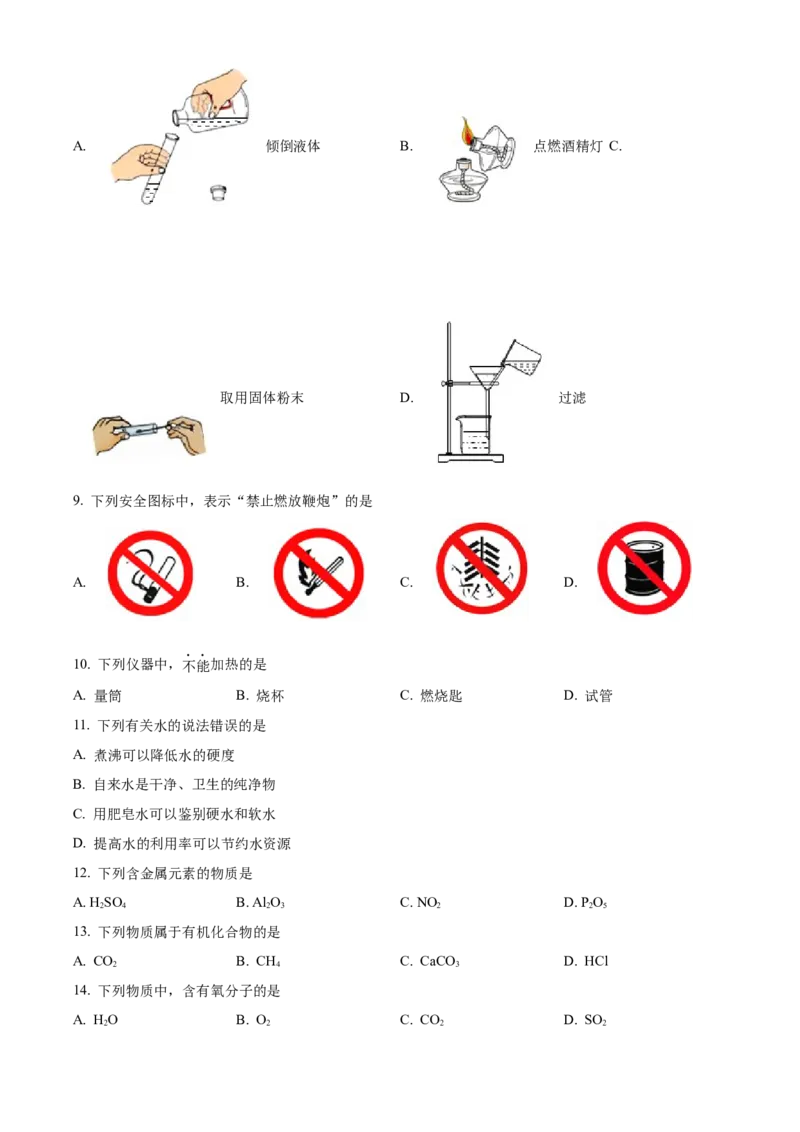
8. 下列实验操作中,正确的是A. 倾倒液体 B. 点燃酒精灯 C.
取用固体粉末 D. 过滤
9. 下列安全图标中,表示“禁止燃放鞭炮”的是
A. B. C. D.
10. 下列仪器中,不能加热的是
A. 量筒 B. 烧杯 C. 燃烧匙 D. 试管
11. 下列有关水的说法错误的是
A. 煮沸可以降低水的硬度
B. 自来水是干净、卫生的纯净物
C. 用肥皂水可以鉴别硬水和软水
D. 提高水的利用率可以节约水资源
12. 下列含金属元素的物质是
A. H SO B. Al O C. NO D. P O
2 4 2 3 2 2 5
13. 下列物质属于有机化合物的是
A. CO B. CH C. CaCO D. HCl
2 4 3
14. 下列物质中,含有氧分子的是
A. HO B. O C. CO D. SO
2 2 2 215. 检验二氧化碳是否收 集满的方法是( )
A. 将带火星的木条伸入集气瓶口 B. 将燃着的木条伸至集气瓶口
C. 向集气瓶中加入澄清石灰水 D. 将燃着的木条伸入集气瓶中
16. 下列操作中,最适宜鉴别空气和氧气两瓶气体的是
A. 观察气体颜色 B. 插入带火星的木条
C. 闻气体的气味 D. 加入澄清的石灰水
17. 下列物质中,属于氧化物的是
A. SiO B. KMnO C. O D. Ca(OH)
2 4 2 2
18. 依据如图实验,不能得到的二氧化碳的性质是
A. 不可燃 B. 不支持燃烧 C. 能溶于水 D. 密度大于空气
19. 下列关于物质用途的描述不正确的是
A. 氧气可用作燃料 B. 稀有气体可用作电光源
C. 干冰可用作制冷剂 D. 氮气可用作焊接金属时的保护气
20. 下列物质化学式书写不正确的是
A. 碳酸HCO B. 氯化钠NaCl C. 氧化镁MgO D. 硫酸铜CuSO
2 3 2 4
21. 已知硫化氢(HS)燃烧的化学方程式为: 。下列说法正确的是
2
A. 该反应体现了HS的可燃性 B. 表示硫化氢加氧气等于二氧化硫加水
2
C. 生成的SO 可以直接排入空气 D. 硫化氢由两个氢原子和一个硫原子构成
2
22. 赤铁矿(主要成分是Fe O)用于工业炼铁。Fe O 中铁元素的化合价为
2 3 2 3
A. +6 B. +5 C. +3 D. +1
23. 空间站中会配备一种手套状的灭火巾。如果火情小,可使用灭火巾抓握火苗灭火,其灭火的原理是
A. 隔绝可燃物 B. 降低可燃物的着火点
C. 隔绝空气 D. 降低温度至可燃物着火点以下
24. 空气中氧气含量测定实验如图所示。下列有关说法不正确的是A. 打开止水夹观察到烧杯中的水流入集气瓶约占集气瓶体积的五分之一
B. 所用红磷要足量
C. 待红磷熄灭并冷却至室温后,打开止水夹
D. 集气瓶底部的水可以起到吸热降温和吸收白烟的作用
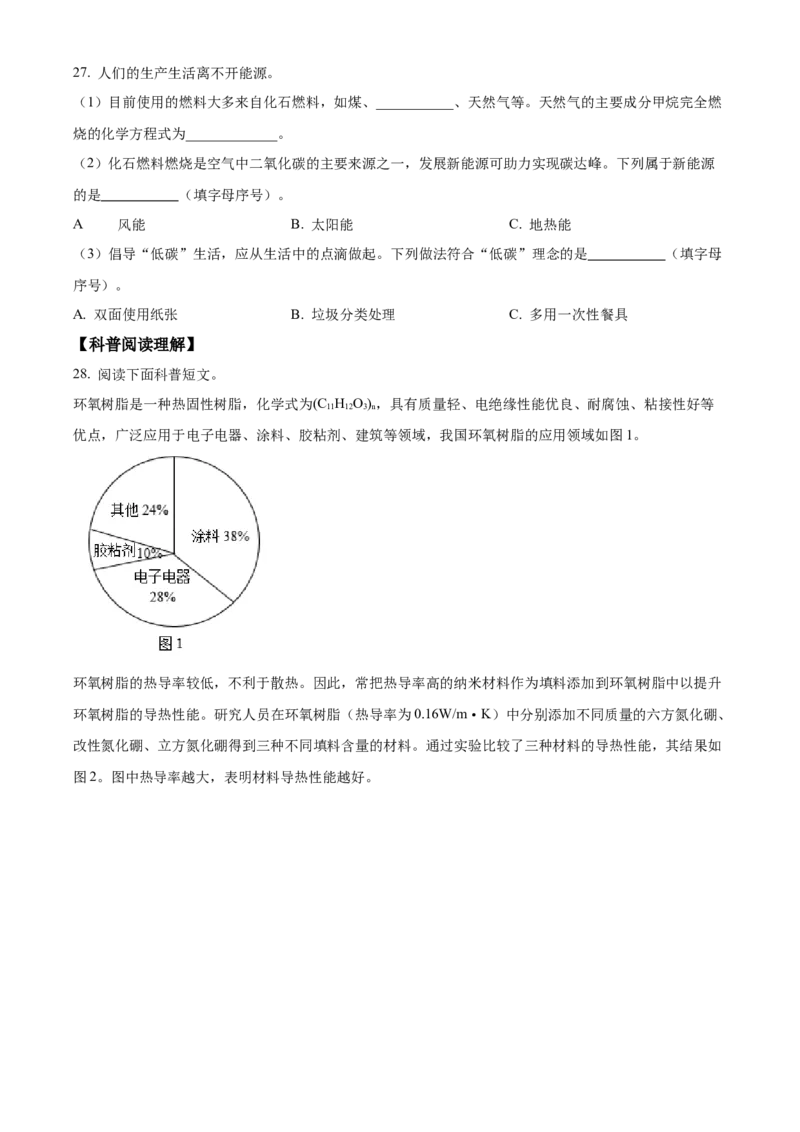
25. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解制氢的微观示意图如下:
下列说法正确的是
A. 反应前后氢原子的个数发生改变 B. 乙中碳元素和氧元素的质量分数相等
C. 反应前后分子种类发生改变 D. 该反应中生成的甲和乙的质量比为1:1
第二部分 非选择题(共45分)
【生活现象解释】
26. 航天梦照亮中国科技兴国路。在距离地球400多公里的“天宫”,三位航天员老师给我们带来了别开
生面的“科学实验课”。
(1)太空“冰雪”实验中用到乙酸钠(CHCOONa),CHCOONa中碳、氢原子个数比为___________。
3 3
(2)航天员在“天宫”中生活所需要的氧气来自水的电解,写出电解水发生反应的化学方程式
___________。
(3)航天员展示了“锆金属熔化与凝固”实验。锆在元素周期表中的信息如图所示,锆原子的核外电子
数为___________。
(4)航天员将泡腾片放在蓝色水球中,观察到水球中产生了很多小气泡,并闻到阵阵香气。“闻到香
气”说明分子具有的性质是___________。27. 人们的生产生活离不开能源。
(1)目前使用的燃料大多来自化石燃料,如煤、___________、天然气等。天然气的主要成分甲烷完全燃
烧的化学方程式为_____________。
(2)化石燃料燃烧是空气中二氧化碳的主要来源之一,发展新能源可助力实现碳达峰。下列属于新能源
的是 (填字母序号)。
.
A 风能 B. 太阳能 C. 地热能
(3)倡导“低碳”生活,应从生活中的点滴做起。下列做法符合“低碳”理念的是 (填字母
序号)。
A. 双面使用纸张 B. 垃圾分类处理 C. 多用一次性餐具
【科普阅读理解】
28. 阅读下面科普短文。
环氧树脂是一种热固性树脂,化学式为(C H O),具有质量轻、电绝缘性能优良、耐腐蚀、粘接性好等
11 12 3 n
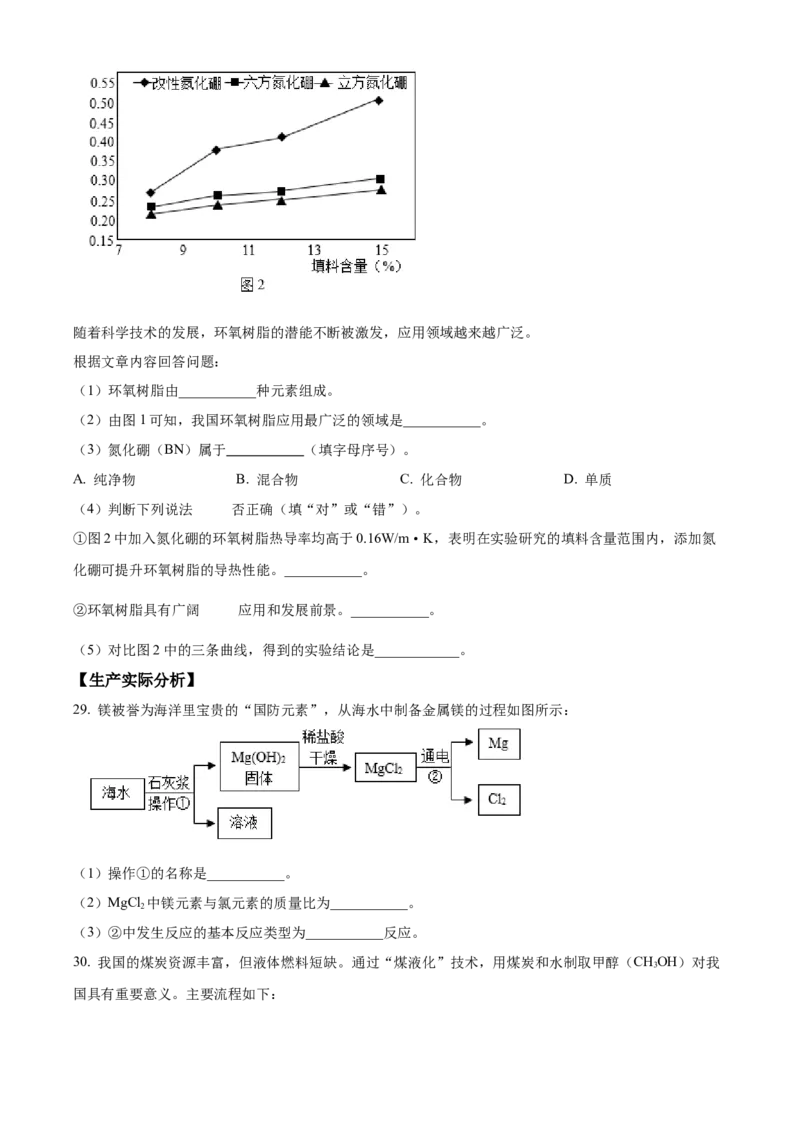
优点,广泛应用于电子电器、涂料、胶粘剂、建筑等领域,我国环氧树脂的应用领域如图1。
环氧树脂的热导率较低,不利于散热。因此,常把热导率高的纳米材料作为填料添加到环氧树脂中以提升
环氧树脂的导热性能。研究人员在环氧树脂(热导率为0.16W/m·K)中分别添加不同质量的六方氮化硼、
改性氮化硼、立方氮化硼得到三种不同填料含量的材料。通过实验比较了三种材料的导热性能,其结果如
图2。图中热导率越大,表明材料导热性能越好。随着科学技术的发展,环氧树脂的潜能不断被激发,应用领域越来越广泛。
根据文章内容回答问题:
(1)环氧树脂由___________种元素组成。
(2)由图1可知,我国环氧树脂应用最广泛的领域是___________。
(3)氮化硼(BN)属于 (填字母序号)。
A. 纯净物 B. 混合物 C. 化合物 D. 单质
(4)判断下列说法 是否正确(填“对”或“错”)。
①图2中加入氮化硼的环氧树脂热导率均高于0.16W/m·K,表明在实验研究的填料含量范围内,添加氮
化硼可提升环氧树脂的导热性能。___________。
的
②环氧树脂具有广阔 应用和发展前景。___________。
(5)对比图2中的三条曲线,得到的实验结论是____________。
【生产实际分析】
29. 镁被誉为海洋里宝贵的“国防元素”,从海水中制备金属镁的过程如图所示:
(1)操作①的名称是___________。
(2)MgCl 中镁元素与氯元素的质量比为___________。
2
(3)②中发生反应的基本反应类型为___________反应。
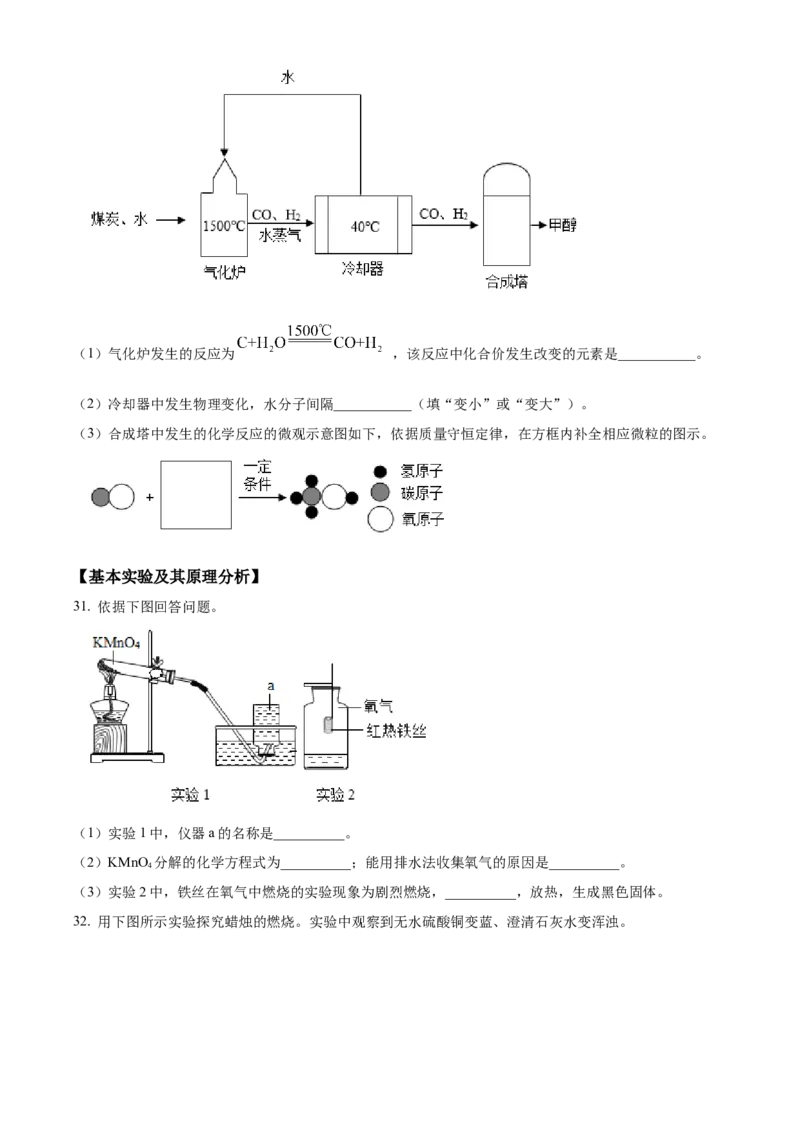
30. 我国的煤炭资源丰富,但液体燃料短缺。通过“煤液化”技术,用煤炭和水制取甲醇(CHOH)对我
3
国具有重要意义。主要流程如下:(1)气化炉发生的反应为 ,该反应中化合价发生改变的元素是___________。
(2)冷却器中发生物理变化,水分子间隔___________(填“变小”或“变大”)。
(3)合成塔中发生的化学反应的微观示意图如下,依据质量守恒定律,在方框内补全相应微粒的图示。
【基本实验及其原理分析】
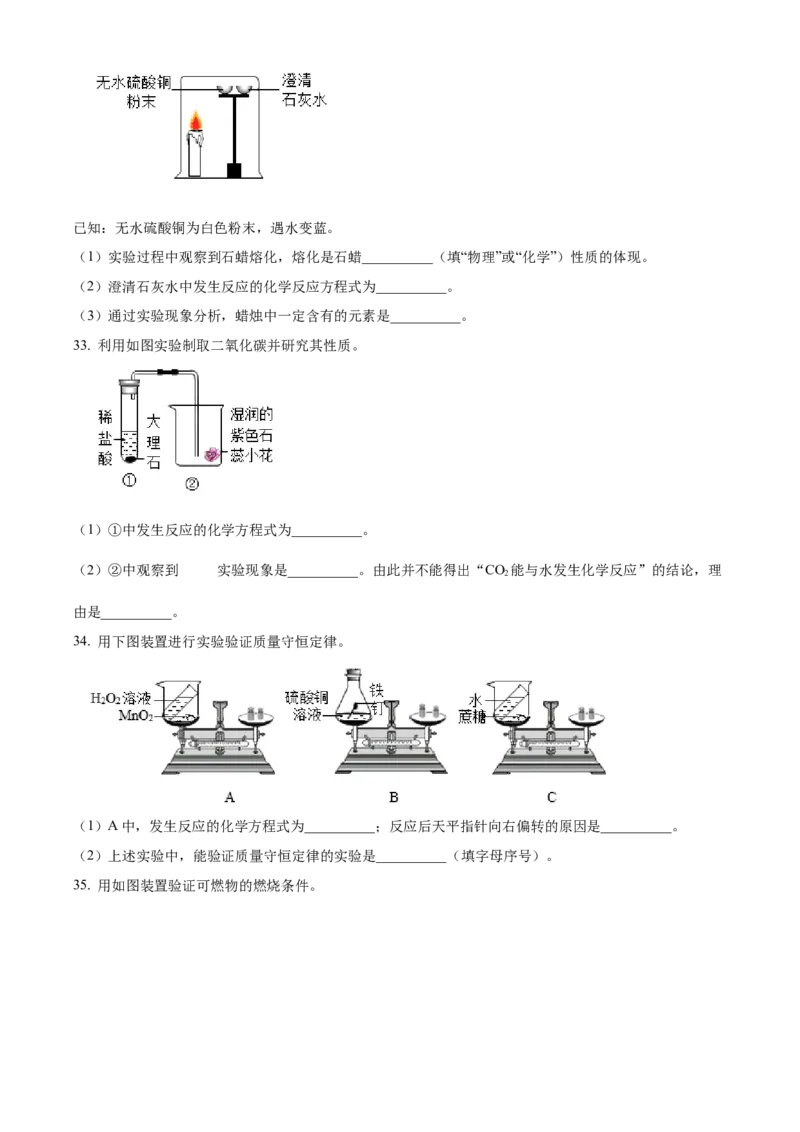
31. 依据下图回答问题。
(1)实验1中,仪器a的名称是__________。
(2)KMnO 分解的化学方程式为__________;能用排水法收集氧气的原因是__________。
4
(3)实验2中,铁丝在氧气中燃烧的实验现象为剧烈燃烧,__________,放热,生成黑色固体。
32. 用下图所示实验探究蜡烛的燃烧。实验中观察到无水硫酸铜变蓝、澄清石灰水变浑浊。已知:无水硫酸铜为白色粉末,遇水变蓝。
(1)实验过程中观察到石蜡熔化,熔化是石蜡__________(填“物理”或“化学”)性质的体现。
(2)澄清石灰水中发生反应的化学反应方程式为__________。
(3)通过实验现象分析,蜡烛中一定含有的元素是__________。
33. 利用如图实验制取二氧化碳并研究其性质。
(1)①中发生反应的化学方程式为__________。
的
(2)②中观察到 实验现象是__________。由此并不能得出“CO 能与水发生化学反应”的结论,理
2
由是__________。
34. 用下图装置进行实验验证质量守恒定律。
(1)A中,发生反应的化学方程式为__________;反应后天平指针向右偏转的原因是__________。
(2)上述实验中,能验证质量守恒定律的实验是__________(填字母序号)。
35. 用如图装置验证可燃物的燃烧条件。已知:白磷的着火点为40℃,红磷的着火点为240℃。
(1)铜片上的白磷燃烧,水中白磷不燃烧,说明可燃物燃烧的条件之一是__________。
(2)能验证可燃物燃烧需要温度达到可燃物着火点的现象是__________。
(3)关于实验下列说法正确的是 (填字母序号)。
A. 热水的作用只是提供温度
B. 实验中热水的温度应不低于40℃
C. 用导管对准热水中的白磷通入氧气,可使白磷燃烧
【科学探究】
36. 研究人员用硫酸亚铁(FeSO )和氯化铁(FeCl )等试剂制备了超顺磁性纳米四氧化三铁,并探究影
4 3
响产物纳米四氧化三铁尺寸的因素。
【查阅资料】
纳米四氧化三铁尺寸在20nm~30nm之间时呈现超顺磁性,在该范围内,纳米四氧化三铁尺寸越大,超顺
磁性越好。
【进行实验】
称取一定量的FeCl 和FeSO 充分溶解在水中,加热到一定温度并保持恒温,机械搅拌的同时逐滴加入氢
3 4
氧化钠溶液,溶液中有沉淀产生,进一步处理沉淀得到产物纳米四氧化三铁。
实验记录如下:
实验编号 铁元素含量/(g/L) 温度/(℃) 搅拌速度/(r/min) 产物颜色 产物尺寸/(nm)
① 8.4 70 1000 黑褐色 9
② 14 70 1000 黑色 21
③ 19.6 70 1000 黑色 32
④ 14 70 400 黑色 41
⑤ 14 70 700 黑色 34
⑥ 14 50 1000 黑色 23
⑦ 14 90 1000 黑褐色 33
【解释与结论】(1)实验过程中的主要反应如下,补全化学方程式: _______
。
(2)具有超顺磁性的产物颜色应为__________(填“黑色”或“黑褐色”)。
(3)依据实验①~③得出的结论是___________。
(4)探究温度、铁元素含量相同时,搅拌速度对纳米四氧化三铁尺寸的影响的实验是__________(填实
验编号)。
【反思与评价】
(5)依据实验数据,不能得出“铁元素含量、搅拌速度相同时,温度越高,纳米四氧化三铁尺寸越大”
的结论,其证据是__________。
(6)依据实验数据,制备超顺磁性纳米四氧化三铁的最佳实验条件是:铁元素含量、温度、搅拌速度分
别为 (填字母序号)。
A. 14g/L,50℃,1000r/min B. 8.4g/L,70℃,1000r/min
C. 14g/L,70℃,700r/min D. 14g/L,70℃,400r/min
【实际应用定量分析】
37. 矿物质碳化封存CO 是实现碳中和的途径之一。矿物质碳化封存主要反应的化学方程式为
2
。利用此方法计算20kg的MgO可以封存CO 的质量(写出计算过程及结
2
果)。