文档内容
第 9 讲 钠及其化合物
达标练习01.
★☆☆☆☆
(2020·北师大附中期中)钠与水反应的现象和钠的下列性质无关的是( )
A.钠的熔点较低 B.钠的密度小于水
C.钠的硬度较小 D.钠的还原性强
【考点】钠的性质
【答案】C
【解析】A. 因钠与水反应放热,钠的熔点低,所以看到钠熔成闪亮的小球,与
性质有关,故A不选。
B. 钠的密度比水小,所以钠浮在水面上,与性质有关,故B不选;
C. 硬度大小与反应现象无关,所以与性质无关,故C选;
D. 因钠的金属性强,所以与水反应剧烈,与性质有关,故D不选;故选:C。
达标练习02.
★★☆☆☆
(2020·广州二中期中)有关钠的叙述正确的是( )
(已知:氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水)
A.2.3g钠与97.7g水反应后,溶液中溶质的质量分数等于4%
B.钠和 溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出了金属铜
C.向金
�
属
�
钠
��
与�水反应后的溶液中通入适量氯气后,溶液中含有两种溶质
D.钠在空气中的缓慢氧化与其在空气中点燃所得的产物一样
【考点】钠和氯气的性质
【答案】C
【解析】A. 2.3g钠与97.7g水反应,依据 ,生成
氢氧化钠的质量为4g,但是因为反应消耗
2
了
N
水
a+
,
2
同
�
时2� 生
�
成
2
氢
Na
气
�
,
�
所
+
以 �2溶
�
液的质
量小于100g,溶质的质量分数大于4%,故A错误;
B.金属钠和硫酸铜溶液的反应先是和水的反应,生成氢氧化钠和氢气,然后是
氢氧化钠和硫酸铜之间的复分解反应,即 ,
, 2N 钠 a 跟 +2C�uS2�O 4� 溶 2 液 Na 反 � 应 � 生 + 成 �2的 � 蓝色沉
2
淀
N
上
aO
有
H
时
+
出
��
现
��
暗�斑
�
是
��
因
䁮�
为
�
钠 �2与
�+
水反
Na
应2� 放
�
热� ,使得氢氧化铜受热分解生成氧化铜的
第1页(共9页)缘故,故B 错误;
C.钠与水反应 ,反应后的溶液为 溶液,氯
气和 溶液 2 反 N 应 a+ 生 2 成 �2� � 、 2Na��+ 和 �H2 2�O,反应方程式为 NaOH
NaOH ,所 N 以 a 产 Cl 物 N 中 a 有 ClO 两种盐生成,故C 正确; 2NaOH+�2 �
NDa . � 钠 + 在空 Na 气 Cl 中 O+ 的 � 缓2慢 � 氧化生成氧化钠,其在空气中点燃生成过氧化钠,故D 错
误;故选:C。
达标练习03.
★★☆☆☆
(2020·石家庄二中期中)下列有关钠单质的事实对应解释不合理的是( )
选项 事实 解释
A 钠保存在煤油中 煤油不与钠发生反应,钠的密度比煤油大,
煤油可以隔绝空气和水蒸气
B 新切开的钠的光亮的 钠和空气中的氧气反应生成了
表面很快变暗 Na2�2
C 钠蒸汽充入灯泡中制 钠的焰色为黄色,穿透能力强
成高压钠灯
D 钠可以用小刀切割 钠质地柔软
【考点】钠单质的性质
【答案】B
【解析】A.钠与煤油不反应,且比煤油密度大,钠沉在底部,煤油可以使钠隔
绝空气和水蒸气,防止钠与氧气、水反应,故A正确;
B. 是活泼金属,易被氧气氧化,新切开的钠的光亮的表面很快变暗,是因为
钠和
N
空
a
气中的氧气反应生成了 ,故B错误;
C. 的焰色反应为黄色,钠蒸
Na
汽2O 充入灯泡中制成高压钠灯,会发出黄光,穿透
能力
N
强
a
,故C 正确;
D.钠的硬度小,质地柔软,可以用小刀切割,故D正确;故选:B。
第2页(共9页)达标练习04.
★★★☆☆
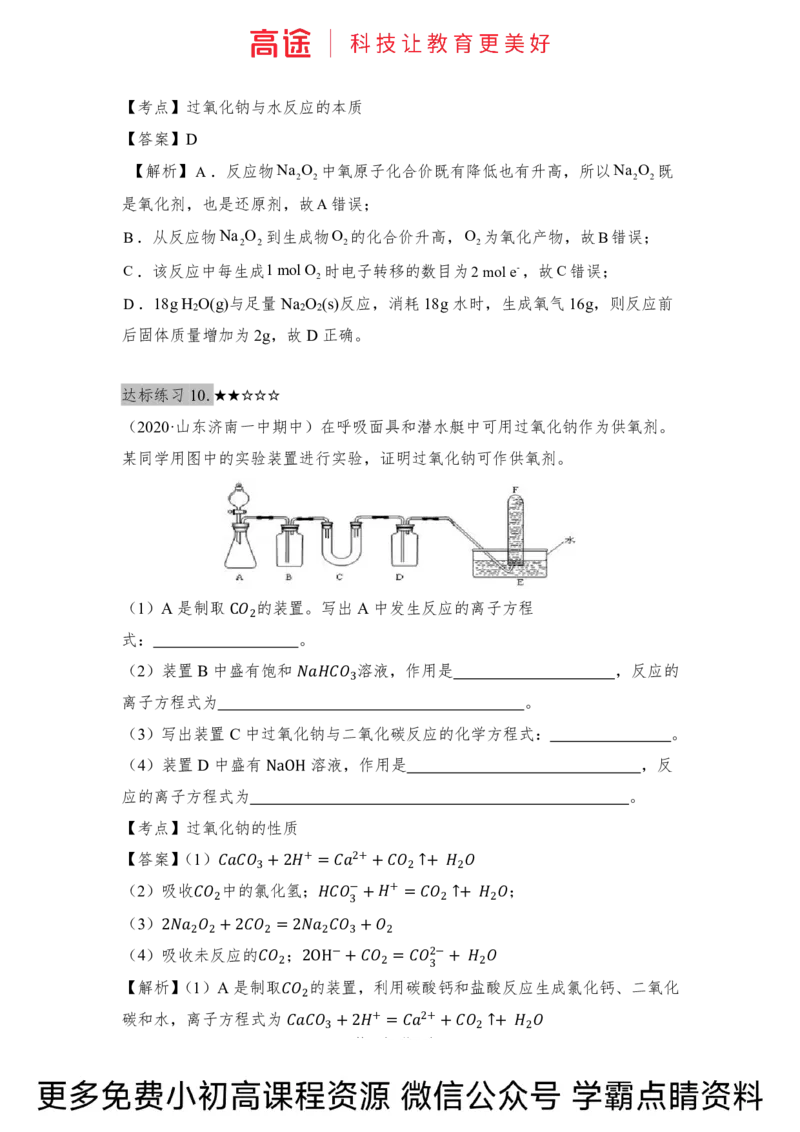
(2020·张家口市期末)如图装置,试管中盛有水,气球a中盛有干燥的Na O 颗
2 2
粒,U 形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口。实验时将气球中
的Na O 抖落到试管b的水中,将发生的现象是( )
2 2
A.U形管内红色褪去 B.试管内溶液变红
C.气球a变瘪 D.U形管水位:d c
【考点】过氧化钠的性质
【答案】D
【解析】由于发生反应2Na O + 2H O = 4NaOH + O ,产生O 使气球膨胀,
2 2 2 2 2
该反应放出大量热量,使锥形瓶中空气受热膨胀而出现U形管中水位d c,由
于浅红色的水是在U形管中而非试管中,则 U形管内的红水不褪色,水是无色
的,反应后试管内溶液也不变色,故选:D
达标练习05.
★★☆☆☆
(2020·湖南师大附中期中)下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因
果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
A 过氧化钠可为航天员供氧 与 反应生成O Ⅰ对,Ⅱ对,有
2
Na2�2 C�2
B 碳酸钠溶液可用于治疗胃病 可与盐酸反应 Ⅰ对,Ⅱ对,无
Na2C��
C 向 的水溶液中滴加酚 与水反应生成氢氧化 Ⅰ对,Ⅱ错,无
Na2�2酞变红色 Na2�2 钠
D 金属钠具有强还原性 高压钠灯发出透雾能力强的 Ⅰ对,Ⅱ对,有
黄光
第3页(共9页)【考点】钠及其化合物的性质
【答案】A
【解析】
A.过氧化钠与二氧化碳反应生成氧气和碳酸钠,所以过氧化钠可为航天员供氧,
故A正确;
B.碳酸钠碱性较强,一般用碳酸氢钠治疗胃酸过多,故B错误;
C. 与水反应生成氢氧化钠,同时过氧化钠具有强的氧化性,所以向
的水 N 溶 a2液 �2中滴加酚酞先变红后褪色,故C 错误; Na2�2
D.高压钠灯发出透雾能力强的黄光,与其强还原性无关,故D错误。
故选:A。
达标练习06.
★★☆☆☆
(2020·辽宁六校联考)将 投入 溶液中,可观察到的现象是( )
①生成白色沉淀 ②生 N 成 a 红2� 褐2 色沉 F 淀 e��
③有气泡产生 ④因为 具有漂白性,所以 溶液褪色
A.①④ B.② Na ③2�2 C.①③ Fe�� D.仅②
【考点】过氧化钠的性质
【答案】B
【解析】将 投入 溶液中,发生的反应为:
, N 与 a2氢 � 氧2 化钠 F 反 e� 应 �, 2Na2� ,2立 + 即 2� 生2成 � � 红 � 褐 N 色 a� 的 �+
�+ � �+
�2 � �t 沉淀,所以看到的现象 �� 是 � :有 + 大 �t 量气 � 泡 � 生 t䁮� 成 � , ��有 � 红褐色沉淀生成。故选:
�Bt 。 䁮����
达标练习07.
★★☆☆☆
(2020·湖北黄冈期中)将适量金属钠投入下列溶液中,有气体放出,但无沉淀
生成的是( )
A.盐酸 B.饱和氢氧化钠溶液
C.FeCl3 溶液 D.CuSO4 溶液
【考点】钠单质的性质
【答案】A
第4页(共9页)【解析】A. 钠与盐酸反应生成氯化钠和氢气,没有沉淀,故A正确;
B. 钠与饱和的氢氧化钠溶液反应生成氢气和氢氧化钠,消耗溶剂水,同时溶质
质量增加,溶液是过饱和溶液,有氢氧化钠沉淀析出,故B 错误;
C. 钠与氯化铁溶液反应有氢氧化铁沉淀和氢气生成,故C错误;
D. 钠与硫酸铜溶液反应有氢氧化铜沉淀和氢气生成,故D错误;故选:A。
达标练习08.
★★★☆☆
(2020·南昌市期末)(多选)下列关于氧化钠和过氧化钠的叙述正确的是( )
A.将Na O与Na O 分别加入滴有酚酞的水中,二者现象相同
2 2 2
B.在Na O 与水的反应中,水是还原剂
2 2
C.相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1
D. Na O 阴阳离子个数比为1:2
2 2
【考点】过氧化钠与氧化钠构成及性质
【答案】CD
【解析】选项A:过氧化钠与水反应生成氢氧化钠和氧气,具有强氧化性,与酚
酞反应先变红后褪色,氧化钠与水反应只生成氢氧化钠,与酚酞反应只变红色,
二者现象不相同,故A错误;
选项B:在Na O 与水的反应中过氧化钠既是氧化剂也是还原剂,水不是氧化剂
2 2
也不是还原剂,故B 错误;
选项C:氧化钠中阴离子是氧离子,过氧化钠中阴离子是过氧根离子,所以相同
物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1,故C正确;
选项D:Na O 阴阳离子个数比为1:2,故D 正确。故选:CD。
2 2
达标练习09.
★★☆☆☆
对于反应:2Na O + 2H O = 4NaOH + O ↑,下列说法中正确的是( )
2 2 2 2
A.Na O 是氧化剂,H O是还原剂
2 2 2
B.O 既是氧化产物,又是还原产物
2
C.该反应中每生成1molO 时电子转移的数目为4mole-
2
D.18gH O(g)与足量Na O (s)反应,反应前后固体质量增加2g
2 2 2
第5页(共9页)【考点】过氧化钠与水反应的本质
【答案】D
【解析】A.反应物Na O 中氧原子化合价既有降低也有升高,所以Na O 既
2 2 2 2
是氧化剂,也是还原剂,故A错误;
B.从反应物Na O 到生成物O 的化合价升高,O 为氧化产物,故B错误;
2 2 2 2
C.该反应中每生成1 mol O 时电子转移的数目为2 mol e-,故C错误;
2
D.18gH O(g)与足量Na O (s)反应,消耗18g水时,生成氧气16g,则反应前
2 2 2
后固体质量增加为2g,故D正确。
达标练习10.
★★☆☆☆
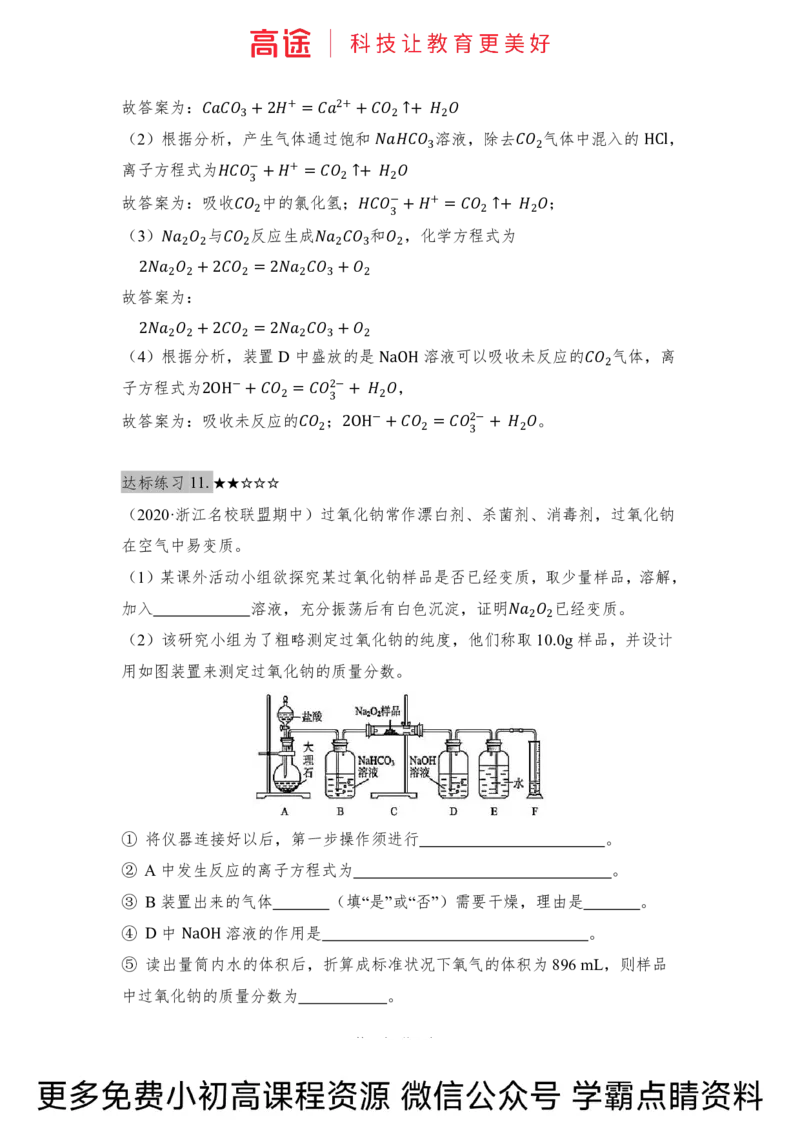
(2020·山东济南一中期中)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。
某同学用图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1)A是制取 的装置。写出A中发生反应的离子方程
式: C�2 。
(2)装置B 中盛有饱和 溶液,作用是 ,反应的
离子方程式为 Na���� 。
(3)写出装置C 中过氧化钠与二氧化碳反应的化学方程式: 。
(4)装置D中盛有 溶液,作用是 ,反
应的离子方程式为 。
NaOH
【考点】过氧化钠的性质
【答案】(1)
+ 2+
(2)吸收 � 中 a� 的 � 氯� + 化 2 氢 � ; � �a +��2 �+ �2� ;
� +
(3) ��2 ���� +� � ��2 �+ �2�
(4) 2 吸 N 收 a2未 �2反 + 应 2 的 ��2 � ; 2Na2��� +�2
� 2�
【解析】(1)A是制�取�2 2的OH装置+,��利2用�碳��酸�钙+和�盐2酸� 反应生成氯化钙、二氧化
碳和水,离子方程式为 ��2
第6+页(共92页+)
�a��� +2� � �a +��2 �+ �2�故答案为:
+ 2+
(2)根据分 � 析 a� , ��产 + 生 2 气 � 体 � 通 � 过 a 饱和 +��2 �+ � 溶2� 液,除去 气体中混入的 ,
离子方程式为 Na���� ��2 HCl
� +
故答案为:吸�收��� 中+的�氯�化�氢�2;�+ �2� ;
� +
(3) 与 ��反2 应生成 ��和�� +,�化学�方�程�2式�+为�2�
Na2�2 ��2 Na2��� �2
故答 2N 案 a2为 � :2 +2��2 � 2Na2��� +�2
(4 2 ) Na 根 2� 据 2 分 + 析 2� , �2 装 � 置 2 D Na 中 2� 盛 � 放 � + 的 � 是 2 溶液可以吸收未反应的 气体,离
子方程式为 Na , OH ��2
� 2�
故答案为:2吸O收H未+反�应�2的� ��;� + �2� 。
� 2�
��2 2OH +��2 � ��� + �2�
达标练习11.
★★☆☆☆
(2020·浙江名校联盟期中)过氧化钠常作漂白剂、杀菌剂、消毒剂,过氧化钠
在空气中易变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,
加入 溶液,充分振荡后有白色沉淀,证明 已经变质。
(2)该研究小组为了粗略测定过氧化钠的纯度,他们称
N
取 a2�102.0g样品,并设计
用如图装置来测定过氧化钠的质量分数。
① 将仪器连接好以后,第一步操作须进行 。
② A 中发生反应的离子方程式为 。
③ B 装置出来的气体 (填“是”或“否”)需要干燥,理由是 。
④ D中 溶液的作用是 。
⑤ 读出量
Na
筒
O
内
H
水的体积后,折算成标准状况下氧气的体积为896mL,则样品
中过氧化钠的质量分数为 。
第7页(共9页)【考点】过氧化钠的性质
【答案】
(1) 或 ;
(2)
�
①
a�
检 2查装
�a
置
�
的 2气密性;
② ;
+ 2+
③
�
否
a�
;
�
过�
+
氧
2
化
�
钠
�
与
�
水
a
和二
+
氧
��
化2碳
�+
反
�
应2生
�
成氧气的物质的量定量关系相同对测定
过氧化钠质量分数无影响,所以不需要干燥出去水蒸气;
④ 吸收未反应的 ;
⑤ 62.4%。 ��2
【解析】(1)过氧化钠在空气中变质会最后生成碳酸钠固体,探究一包过氧化钠
样品是否已经变质,可以利用碳酸根离子和钡离子或钙离子结合生成碳酸钡或碳
酸钙白色沉淀证明 已经变质,取少量样品,溶解,加入 或 溶
液,充分振荡后有 N 白 a 色2� 沉2淀,证明 已经变质,故答案为: �a�2 或 �a�2 ;
(2)装置图中 A为生成二氧化碳的
N
装 a2置 �2,碳酸钙和盐酸反应生成
�a
二
�
氧2 化
�
碳
a
、
�
水2
和氯化钙,反应的离子方程式为: ,B 为洗
+ 2+
气装置,吸收二氧化碳中混有的 �a , �� 防�止 +2� 与 � 过 �a 氧化 + 钠 � 反 �2应 � , +C� 为2� 二氧化碳
与过氧化钠反应的装置,D为吸收
H
多
Cl
余的二氧
HC
化
l
碳的装置,防止多余的二氧化碳
进入量气装置,导致测得的氧气的体积偏大,E 和F 是测量生成氧气的体积的装
置;
①实验探究测定方法是测定二氧化碳和过氧化钠反应生成的氧气,装置中必须是
气密性完好,将仪器连接好以后,必须进行的第一步操作是检查装置的气密性;
故答案为:检查装置的气密性;
②装置图中A为生成二氧化碳的装置,碳酸钙和盐酸反应生成二氧化碳、水和
氯化钙,反应的离子方程式为: ,故答案为:
+ 2+
�a���; +2� � �a +��2 �+ �2�
+ 2+
� ③ aB�� 装�置 + 出 2� 来的 � 气 �a 体不 + 需 � 要 �2干 � 燥 + , � 二2� 氧化碳、水蒸气和过氧化钠反应生成碳酸钠
和氧气的反应,反应的化学方程式为: ,
,过氧
2N
化
a
钠2� 反2应
+2
生
�
成 �2氧
�
气
2
的
Na
物2� 质
�
的�
+
量
�
定2量关系
相
2N
同
a
对2� 测2
+
定
2
过
�
氧2O 化
�
钠
�
质
Na
量
OH
分
+
数
�
无2影
�
响,所以不需要干燥出去水蒸气,故答案为:
否;过氧化钠与水和二氧化碳反应生成氧气的物质的量定量关系相同对测定过氧
第8页(共9页)化钠质量分数无影响,所以不需要干燥出去水蒸气;
④D为吸收多余的二氧化碳的装置,防止多余的二氧化碳进入量气装置,导致测
得的氧气的体积偏大,故答案为:吸收未反应的 ;
⑤测定出量筒内水的体积后,折算成标准状况下
�
氧
�
气2 的体积为896mL,物质的
量= =0.04mol,即氧气的质量为0.04mol×32g/mol=1.28g,由
���⎁��
22���Ͷ�ܮ , ,可得m(2Na2�2)+
2=�6�.224�g,2则N样a2品��中� +过�氧2化钠2N的a质2�量2 +分2数�为2O=� �Na×O10H0+%=�262�.4%,故答案N为a:26�22.4%。
��2��
�����
第9页(共9页)