文档内容
(5)化工生产中的重要非金属元素—高二化学人教版暑假作业本
1.下列有关实验室试剂的存放错误的是( )
A.用棕色试剂瓶存放浓硝酸 B.少量金属钠存放在煤油中
C.用玻璃试剂瓶盛装氢氟酸 D.用带橡胶塞的试剂瓶盛装NaOH溶液
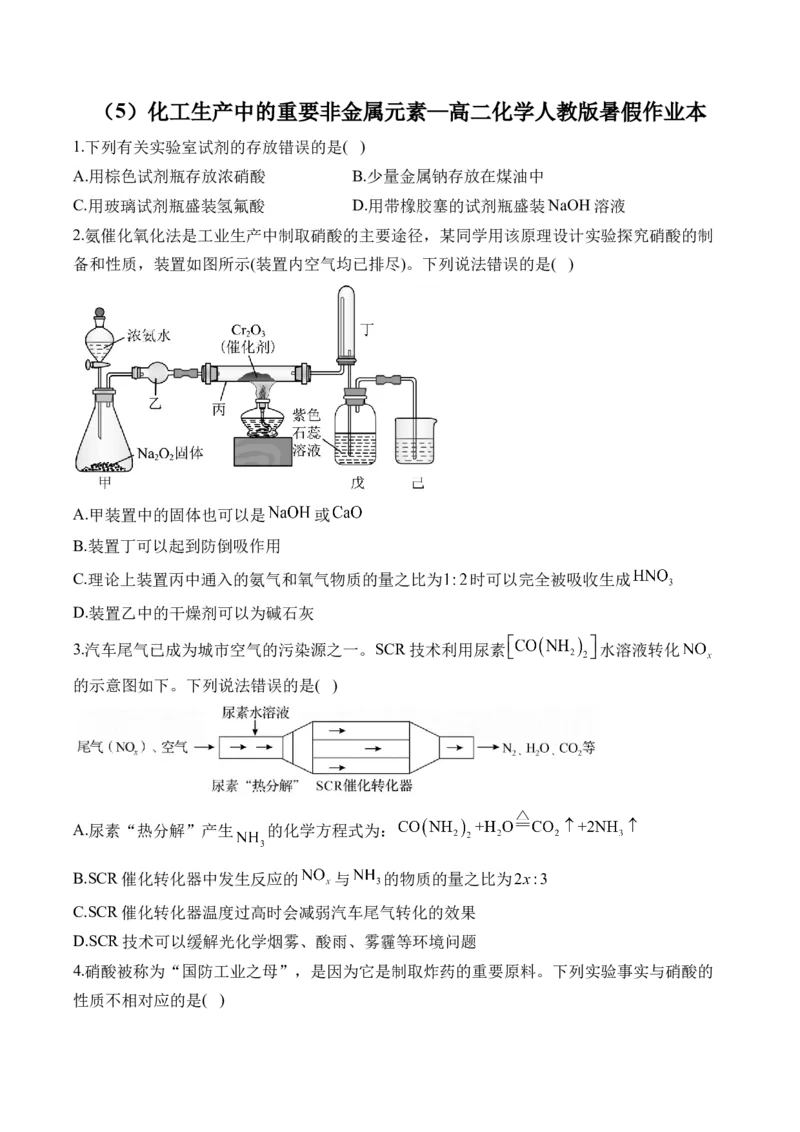
2.氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理设计实验探究硝酸的制
备和性质,装置如图所示(装置内空气均已排尽)。下列说法错误的是( )
A.甲装置中的固体也可以是 或
B.装置丁可以起到防倒吸作用
C.理论上装置丙中通入的氨气和氧气物质的量之比为 时可以完全被吸收生成
D.装置乙中的干燥剂可以为碱石灰
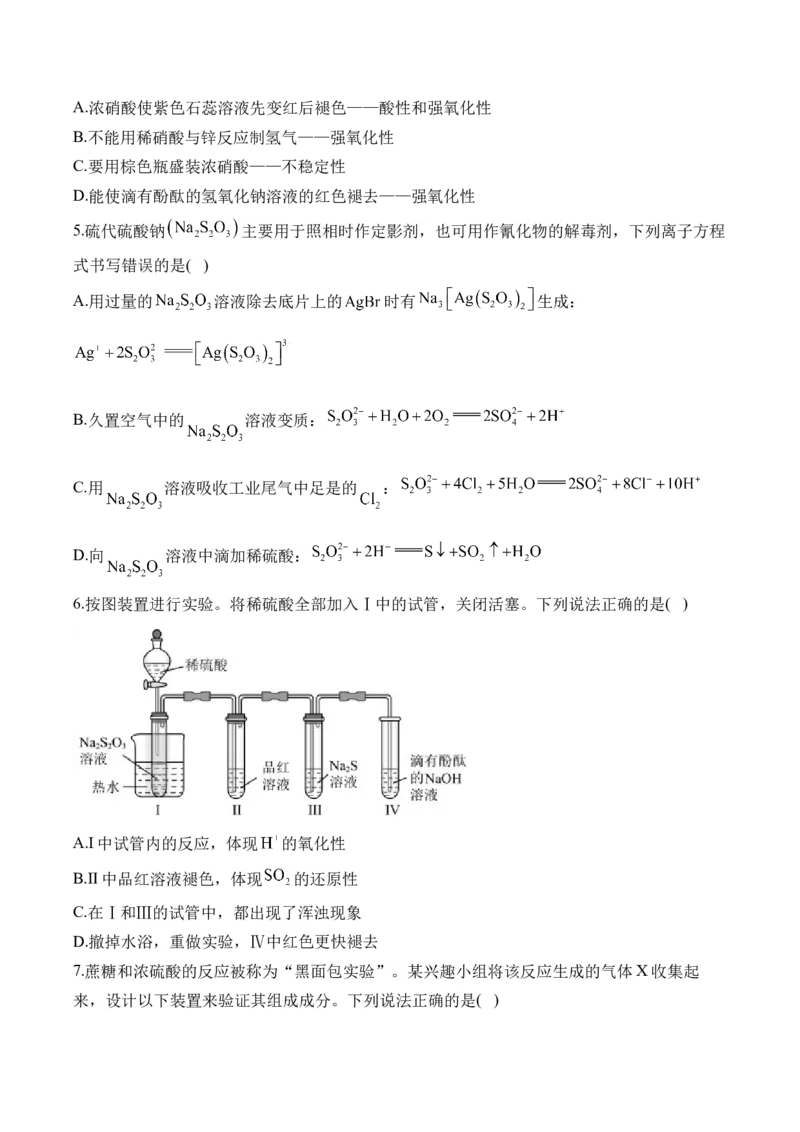
3.汽车尾气已成为城市空气的污染源之一。SCR技术利用尿素 水溶液转化
的示意图如下。下列说法错误的是( )
A.尿素“热分解”产生 的化学方程式为:
B.SCR催化转化器中发生反应的 与 的物质的量之比为
C.SCR催化转化器温度过高时会减弱汽车尾气转化的效果
D.SCR技术可以缓解光化学烟雾、酸雨、雾霾等环境问题
4.硝酸被称为“国防工业之母”,是因为它是制取炸药的重要原料。下列实验事实与硝酸的
性质不相对应的是( )A.浓硝酸使紫色石蕊溶液先变红后褪色——酸性和强氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液的红色褪去——强氧化性
5.硫代硫酸钠 主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程
式书写错误的是( )
A.用过量的 溶液除去底片上的 时有 生成:
B.久置空气中的 溶液变质:
C.用 溶液吸收工业尾气中足是的 :
D.向 溶液中滴加稀硫酸:
6.按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是( )
A.Ⅰ中试管内的反应,体现 的氧化性
B.Ⅱ中品红溶液褪色,体现 的还原性
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象
D.撤掉水浴,重做实验,Ⅳ中红色更快褪去
7.蔗糖和浓硫酸的反应被称为“黑面包实验”。某兴趣小组将该反应生成的气体X收集起
来,设计以下装置来验证其组成成分。下列说法正确的是( )A.蔗糖和浓硫酸反应,蔗糖固体由白变黑,体现浓硫酸的吸水性
B.物质a是碱石灰,用于检验生成的水
C.装置乙用于除去 , 被还原
D.装置丙中溶液不褪色,装置丁中溶液变浑浊,说明有 生成
8.普通玻璃的主要成分为 , 和 ,它是以纯碱、石灰石和石英砂(主要成
分为 )为原料,经混合、粉碎,在玻璃窑中熔融,发生复杂的物理变化和化学变化制得
的。下列说法正确的是( )
A.沸点:
B. 的VSEPR模型与空间结构均为平面三角形
C. 和 分别与足量的稀盐酸反应,反应后均无新的沉淀产生
D.0.1mol 的质量为6
9.接触法制硫酸、氨氧化法制硝酸、工业制备高纯硅分别经过下列主要变化:
下列说法符合事实的是( )
A.第8、9两步互为可逆反应
B.第3、6步都是直接用水吸收
C.第7步 过量,会发生:
D.第9步反应发生前,首先要对第8步反应产物进行蒸馏,得到纯净的
10.近日,香港理工大学戴建国教授团队通过使用硫酸钡和纳米二氧化硅微球对无机地质聚合物进行改性,合成了一种可常温制备的日间辐射制冷涂层。该新型无机涂层实现日间辐射制
冷降温8.9℃,解决城市热岛和气候变化挑战。下列有关说法错误的是( )
A. 中Si的杂化方式为
B. 的水溶液几乎不导电,所以为弱电解质
C.将纳米二氧化硅微球分散到蒸馏水中,能用渗析的方法将其分离出来
D.该涂层在恶劣环境下能保持良好的性能,包括高温、水浸泡、机械磨损和阳光照射等
11.高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路
线,其中一种工艺流程示意图及主要反应如下:
(1)工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为__________。
当有 参与反应时,该反应转移的电子数是__________。
(2)还原炉中发生的化学反应方程式为:__________。
(3)上述工艺生产中循环使用的物质除Si、 外,还有__________。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为__________。
(5)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻
璃和盐酸反应的离子方程式:__________。
(6)关于硅及其相关化合物的叙述正确的是__________。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO H O H CO ,用类比法得知,
2 2 2 3
C. 用氧化物形式表示为
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
E.SiO 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
2
F.玻璃、水泥、陶瓷都是传统的硅酸盐产品
12.连二亚硫酸钠( )俗称保险粉,广泛应用于有机合成,实验室常用 还原法制备连二亚硫酸钠。回答下列问题:
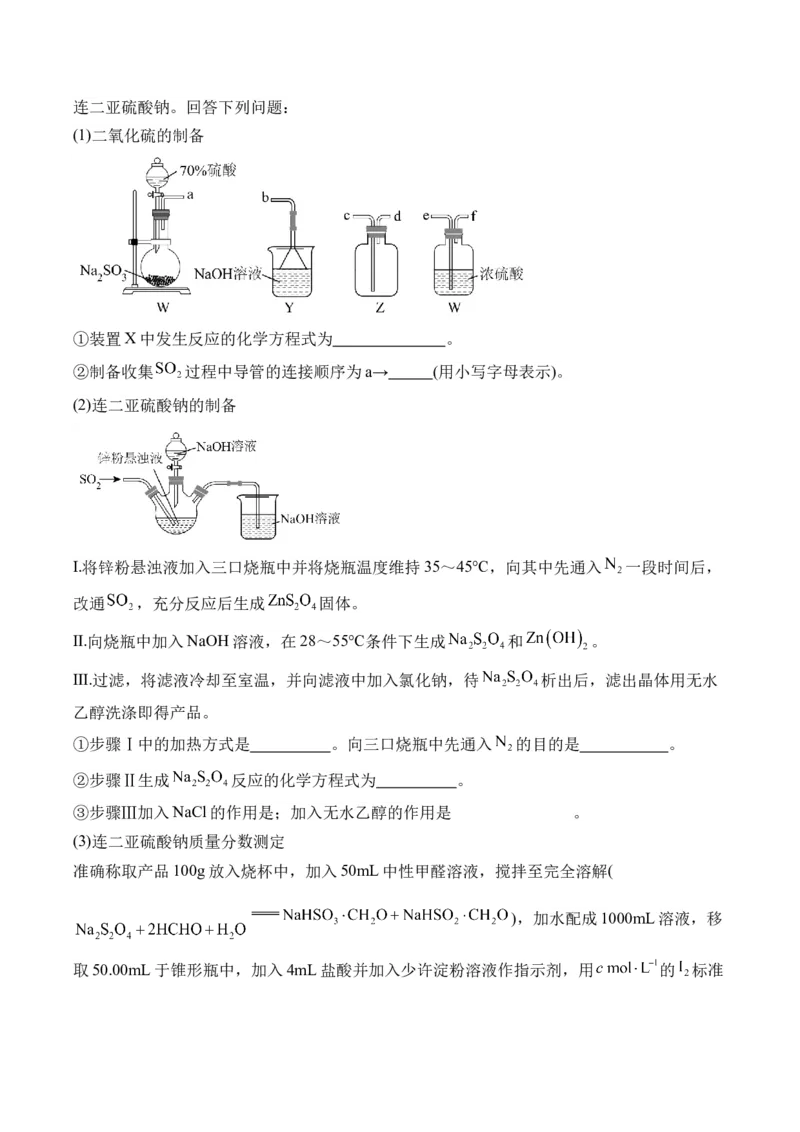
(1)二氧化硫的制备
①装置X中发生反应的化学方程式为 。
②制备收集 过程中导管的连接顺序为a→ (用小写字母表示)。
(2)连二亚硫酸钠的制备
Ⅰ.将锌粉悬浊液加入三口烧瓶中并将烧瓶温度维持35~45℃,向其中先通入 一段时间后,
改通 ,充分反应后生成 固体。
Ⅱ.向烧瓶中加入NaOH溶液,在28~55℃条件下生成 和 。
Ⅲ.过滤,将滤液冷却至室温,并向滤液中加入氯化钠,待 析出后,滤出晶体用无水
乙醇洗涤即得产品。
①步骤Ⅰ中的加热方式是 。向三口烧瓶中先通入 的目的是 。
②步骤Ⅱ生成 反应的化学方程式为 。
③步骤Ⅲ加入NaCl的作用是;加入无水乙醇的作用是 。
(3)连二亚硫酸钠质量分数测定
准确称取产品100g放入烧杯中,加入50mL中性甲醛溶液,搅拌至完全溶解(
),加水配成1000mL溶液,移
取50.00mL于锥形瓶中,加入4mL盐酸并加入少许淀粉溶液作指示剂,用 的 标准溶液滴定,( 、
)滴定至终点时,消耗碘溶液 。产
品中连二亚硫酸钠的质量分数 (列出计算表达式即可)。
13.依据下图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为________,从化合价上看,X具有________(填“氧化性”或
“还原性”)。
(2)回答下列关于 的问题:
①实验室常用 与 制取氨气,该反应的化学方程式为
________________________。
②下列试剂不能用于干燥 的是________(填字母)。
A.浓硫酸
B.碱石灰
C. 固体
D.
E.
③若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图。
④氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
________________________。(3)回答下列关于 、 的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体 和
反应可转化为无害气体排放,写出相关反应的化学方程式:
________________________________________________。
② 和 按一定比例混合可以被 溶液完全吸收,写出相关反应的化学方程式:
______________。
工业生产中利用氨水吸收 和 ,原理如图所示。
被吸收过程的离子方程式为
________________________________________________________。
答案以及解析
1.答案:C
解析:A.浓硝酸具有强氧化性,且见光容易分解,所以浓硝酸应该保存在棕色试剂瓶中,故
A正确
B.因金属钠能与空气中的氧气和水蒸气反应,煤油的密度小于钠,钠沉在煤油下面,所以少
量的金属钠存放在煤油中隔离空气,故B正确;
C.氢氟酸能与玻璃中二氧化硅反应,能腐蚀玻璃,所以不能用玻璃瓶盛放氢氟酸,故C错
误;
D.氢氧化钠呈强碱性,能和二氧化硅反应生成硅酸钠,硅酸钠具有黏性,能把玻璃塞黏住,
故D正确;
故选:C。
2.答案:A
解析:甲中浓氨水与过氧化钠反应制备氨气和氧气,经过干燥后在丙中发生氨气的催化氧化生
成一氧化氮,一氧化氮可生成二氧化氮,过量的氧气与二氧化氮在戊中可生成硝酸,己为尾
气吸收装置,据此分析解答;A.甲装置需要提供氨气和氧气,如果甲装置中的固体是NaOH或CaO,只能提供氨气,不能
提供氧气,A错误;
B.若发生倒吸,水先进入丁试管中,所以装置丁可以起到防倒吸作用,B正确;
C.根据反应: 、 可知,装置丙
中通入的氨气和氧气物质的量之比为1:2时可以完全被吸收生成 ,C正确;
D.乙用于干燥氨气、氧气,可用碱石灰干燥,D正确;
答案选A。
3.答案:C
解析:A.尿素[ ]水溶液热分解为 和 ,根据原子守恒可得反应的化学方程式
为: ,故A正确;
B. 与 反应的化学方程式为 ,发生反应的
与 的物质的量之比为 ,故B正确;
C.由于不知道该反应的催化剂的活性温度,无法判断温度过高是否会影响尾气的转化效果,
故C错误;
D.该技术可以处理氮氧化物尾气,可以缓解光化学烟雾、酸雨、雾霾等环境问题,故D正
确。
答案选C。
4.答案:D
解析:向滴有酚酞的NaOH溶液中滴入硝酸,溶液红色褪去,利用的是硝酸的酸性。
5.答案:A
解析:A.用过量的 溶液除去底片上的 时有 生成,反应的离子
方程式为: ,选项A错误;
B.久置空气中的 溶液变质,被空气中的氧气氧化为硫酸钠,反应的离子方程式为:
,选项B正确;C.用 溶液吸收工业尾气中足量的 ,生成硫酸钠、氯化钠和盐酸,反应的离子方程
式为: ,选项C正确;
D.向 溶液中滴加稀硫酸,生成硫和二氧化硫,反应的离子方程式为:
,选项D正确;
答案选A。
6.答案:C
解析::A.Ⅰ中试管内发生反应S O2 2H SSO H O,氢元素化合价不变,H不
2 3 2 2
体现氧化性,故A错误;Ⅱ中品红溶液褪色,体现 的漂白性,故B错误;Ⅰ试管内发生
反应S O2 2H SSO H O,Ⅲ试管内发生反应
2 3 2 2
,Ⅰ和Ⅲ的试管中都出现了浑浊现象,故C正确;撤掉水浴,重做实验,反应速率减慢,Ⅳ
中红色褪去的速率减慢,故D错误。
7.答案:D
解析:蔗糖与浓硫酸反应,蔗糖脱水后生成的碳和浓硫酸在加热条件下反应生成二氧化硫、
二氧化碳和水。气体X的成分为 、 、 。浓硫酸使蔗糖变黑,体现了浓硫酸的脱
水性,A错误;
用无水硫酸铜检验水的生成,B错误;
用酸性高锰酸钾溶液除去二氧化硫,二氧化硫被氧化,C错误;
装置丙中品红不褪色,说明二氧化硫已除尽,装置丁中澄清石灰水变浑浊,说明有二氧化碳
产生,D正确。
8.答案:B
解析:沸点: ,A项错误; 与足量的稀盐酸反应会生成 沉淀,
C项错误;0.1mol 的质量为6g,D项错误。
9.答案:D
10.答案:B
解析:A.二氧化硅中硅原子形成4个σ键无孤电子对,所以Si的杂化方式为 ,故A正确;B.硫酸钡难溶于水,但溶于水的硫酸钡完全电离,所以硫酸钡是强电解质,故B错误;
C.纳米二氧化硅微球是胶体,能透过滤纸.但不能透过半透膜,所以将纳米二氧化硅微球分散
到蒸馏水中,能用渗析的方法将其分离出来,故C正确:D.该涂层在恶劣环境下能保持良好
的性能,包括高温、水浸泡、机械磨损和阳光照射等,故D正确。
11.答案:(1) ;
(2)
(3)
(4)
(5)
(6)CDF
解析:(1)用石英砂和过量焦炭高温加热生成粗硅的化学方程式为:
, 当有 参与反应时,该反应转移的电子数是
;
(2)还原炉中用 还原 ,生成高纯度的 单质,发生的化学反应方程式为:
;
(3)流化床反应器中发生反应: ,还原炉中发生反应:
,所以可以循环的物质还有 ;
(4)氢氟酸来雕刻玻璃,氢氟酸和 反应,化学方程式为: ;
(5)水玻璃和盐酸反应制取硅酸的离子方程式为:SiO2 2H H SiO ;
3 2 3(6)A.自然界中不存在天然游离的硅单质,硅是以二氧化硅和硅酸盐存在于自然界中,A错
误;
B. 不溶于水,也不与水反应,B错误;
C.根据氧化物的表示方法,NaAlSi O 用氧化物形式表示为 ,C正确;
3 8
D.在周期表中,硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半
导体材料,D正确;
E. 既能和NaOH溶液反应,又能和氢氟酸反应,但SiO 不能与其他酸反应,为酸性氧化
2
物,E错误;
F.玻璃、水泥、陶瓷都是传统的硅酸盐产品,F正确。
故选CDF。
12.答案:(1) ;e→f→c→d→b
(2)水浴加热排出装置内空气,防止 被氧化
降低 的溶解度,便于析出洗去杂质离
子且加快脱水干燥
(3)
解析:(1)①装置X中硫酸和亚硫酸钠反应生成二氧化硫和水、硫酸钠,方程式为:
;
②二氧化硫生成后首先用浓硫酸干燥,随后收集,二氧化硫密度大于空气,应该用向上排空
气的方法收集,最后要尾气处理,故顺序为:a→e→f→c→d→b;
(2)①由于加热温度维持35~45℃,则步骤Ⅰ中的加热方式是水浴加热;由于产物容易被
氧化,装置含有空气,故通入氮气的目的是:排出装置内空气,防止 被氧化;
②根据题意可知,通入 ,充分反应后生成 ,随后加入氢氧化钠反应生成产物,方
程式为: ;
③根据题意向滤液中加入氯化钠则析出产物,故加入氯化钠的目的是:降低 的溶解
度,便于析出;乙醇容易挥发,便于干燥,则加入乙醇的目的是:洗去杂质离子且加快脱水干燥;
(3)根据方程式 ,
、
可知, ,则
,则
。
13.答案:(1) ;氧化性
(2)① ;②ADE;③ ;④
;
(3)① ;② ;
;
解析:(1)X中氮元素化合价是 价,则其氧化物的化学式为 ,氮元素处于最高价,
因此X具有氧化性。
(2)①实验室常用 与 制取氨气,该反应的化学方程式为
②A.氨气为碱性气体,浓硫酸具有酸性,会与氨气发生反应,故不能用浓硫酸干燥;B.碱石灰可以干燥氨气;C. 固体可以干燥氨气;D. 是酸性氧化物,能与 反应;E.
能和 反应。
③氨气极易溶于水,比空气轻,收集方法只能用向下排空气法收集,导气管位置应该是“短
进长出”: 。
④氨气催化氧化的化学方程式为 。
(3)①汽车尾气中的有害气体 和 反应可转化为无害气体( 、 )排放, 中
C元素的化合价升高2,而 中N元素的化合价降低2,根据化合价升降守恒和原子守恒可
知,其化学方程式为 。
② 中N为 价, 中N为 价,归中反应只能都转化为 价,故其化学方程式为
;反应物是亚硫酸铵、二氧化氮,生成物是硫酸铵和
氮气,则 被吸收过程的离子方程式为 。