文档内容
(6)化学反应与能量—高二化学人教版暑假作业本
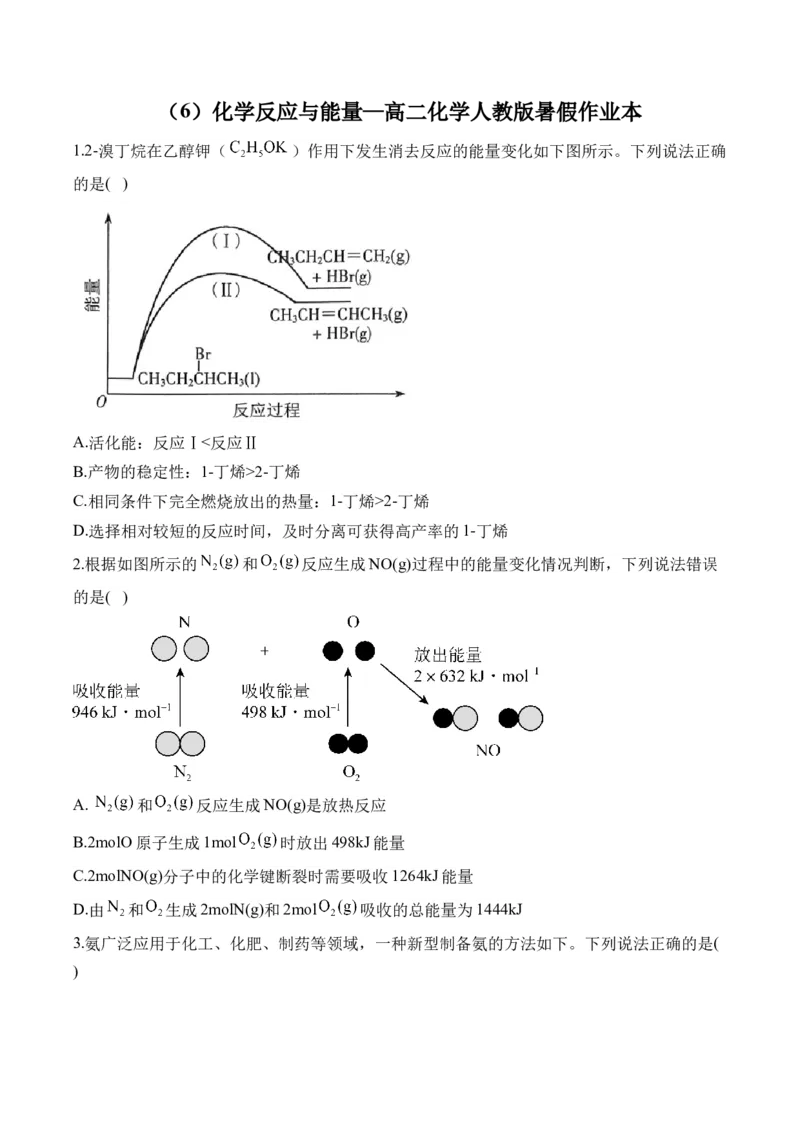
1.2-溴丁烷在乙醇钾( )作用下发生消去反应的能量变化如下图所示。下列说法正确
的是( )
A.活化能:反应Ⅰ<反应Ⅱ
B.产物的稳定性:1-丁烯>2-丁烯
C.相同条件下完全燃烧放出的热量:1-丁烯>2-丁烯
D.选择相对较短的反应时间,及时分离可获得高产率的1-丁烯
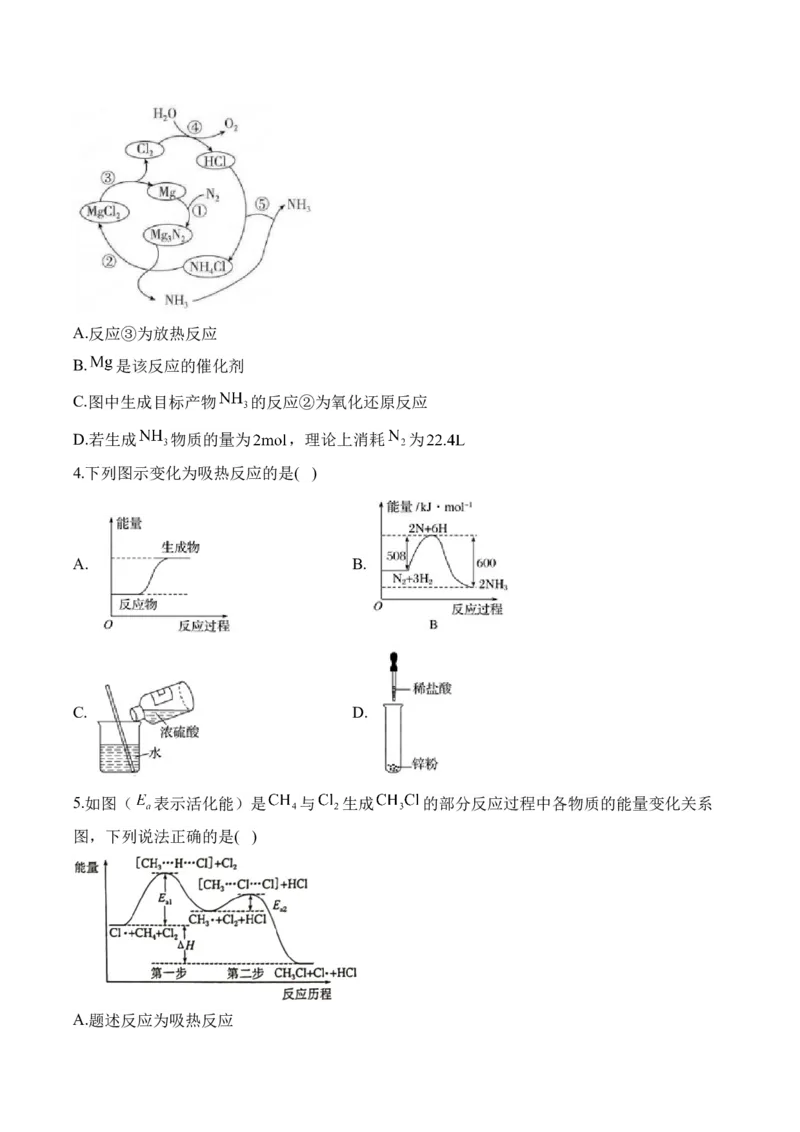
2.根据如图所示的 和 反应生成NO(g)过程中的能量变化情况判断,下列说法错误
的是( )
A. 和 反应生成NO(g)是放热反应
B.2molO原子生成1mol 时放出498kJ能量
C.2molNO(g)分子中的化学键断裂时需要吸收1264kJ能量
D.由 和 生成2molN(g)和2mol 吸收的总能量为1444kJ
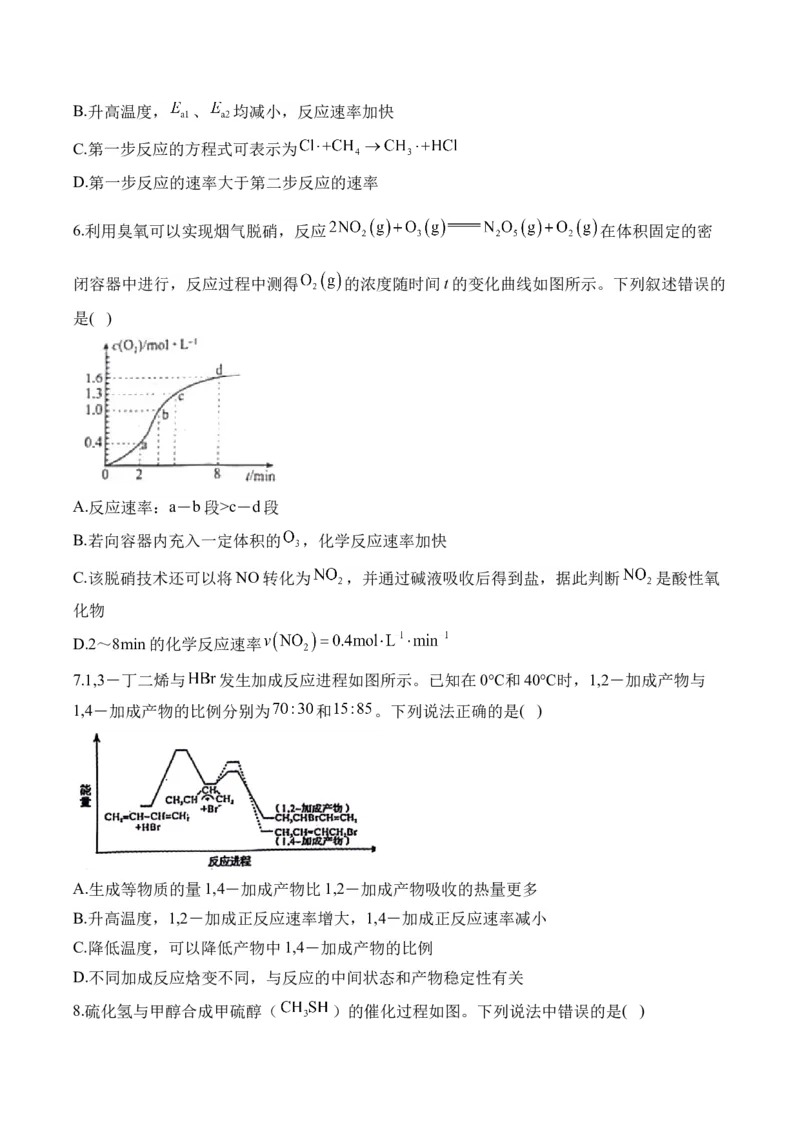
3.氨广泛应用于化工、化肥、制药等领域,一种新型制备氨的方法如下。下列说法正确的是(
)A.反应③为放热反应
B. 是该反应的催化剂
C.图中生成目标产物 的反应②为氧化还原反应
D.若生成 物质的量为 ,理论上消耗 为
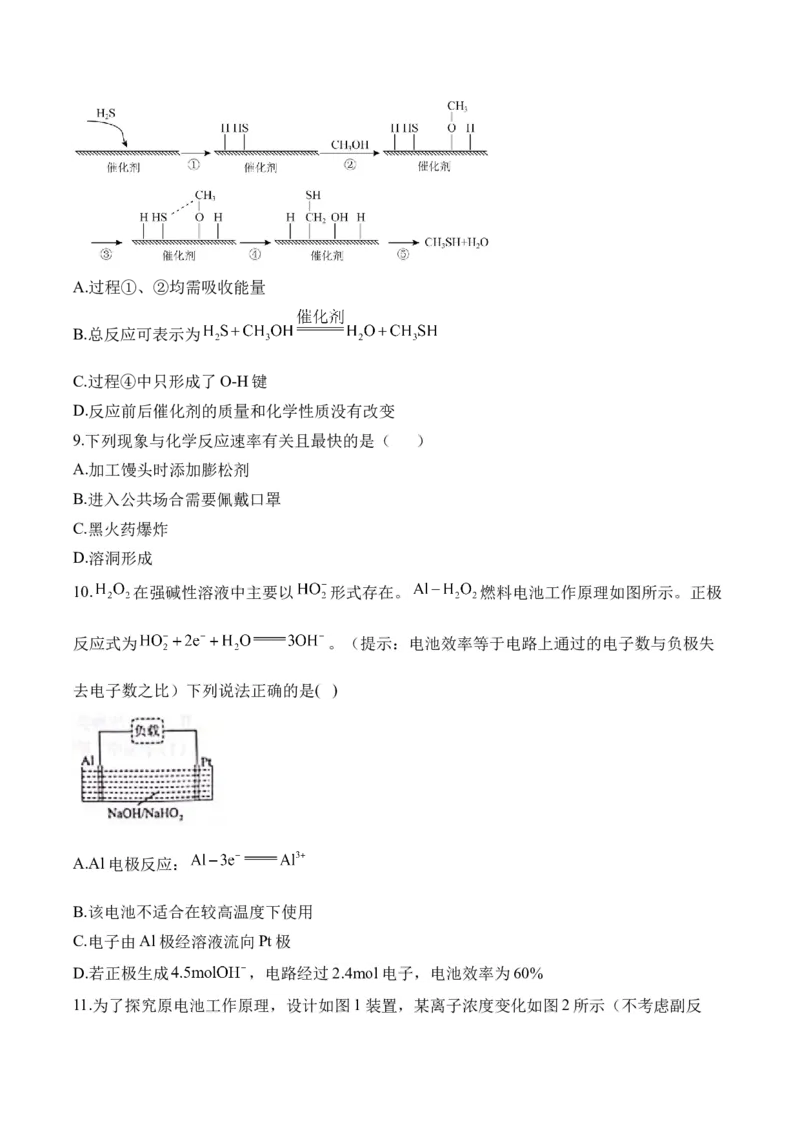
4.下列图示变化为吸热反应的是( )
A. B.
C. D.
5.如图( 表示活化能)是 与 生成 的部分反应过程中各物质的能量变化关系
图,下列说法正确的是( )
A.题述反应为吸热反应B.升高温度, 、 均减小,反应速率加快
C.第一步反应的方程式可表示为
D.第一步反应的速率大于第二步反应的速率
6.利用臭氧可以实现烟气脱硝,反应 在体积固定的密
闭容器中进行,反应过程中测得 的浓度随时间t的变化曲线如图所示。下列叙述错误的
是( )
A.反应速率:a-b段>c-d段
B.若向容器内充入一定体积的 ,化学反应速率加快
C.该脱硝技术还可以将NO转化为 ,并通过碱液吸收后得到盐,据此判断 是酸性氧
化物
D.2~8min的化学反应速率
7.1,3-丁二烯与 发生加成反应进程如图所示。已知在0℃和40℃时,1,2-加成产物与
1,4-加成产物的比例分别为 和 。下列说法正确的是( )
A.生成等物质的量1,4-加成产物比1,2-加成产物吸收的热量更多
B.升高温度,1,2-加成正反应速率增大,1,4-加成正反应速率减小
C.降低温度,可以降低产物中1,4-加成产物的比例
D.不同加成反应焓变不同,与反应的中间状态和产物稳定性有关
8.硫化氢与甲醇合成甲硫醇( )的催化过程如图。下列说法中错误的是( )A.过程①、②均需吸收能量
B.总反应可表示为
C.过程④中只形成了O-H键
D.反应前后催化剂的质量和化学性质没有改变
9.下列现象与化学反应速率有关且最快的是( )
A.加工馒头时添加膨松剂
B.进入公共场合需要佩戴口罩
C.黑火药爆炸
D.溶洞形成
10. 在强碱性溶液中主要以 形式存在。 燃料电池工作原理如图所示。正极
反应式为 。(提示:电池效率等于电路上通过的电子数与负极失
去电子数之比)下列说法正确的是( )
A.Al电极反应:
B.该电池不适合在较高温度下使用
C.电子由Al极经溶液流向Pt极
D.若正极生成 ,电路经过2.4mol电子,电池效率为60%
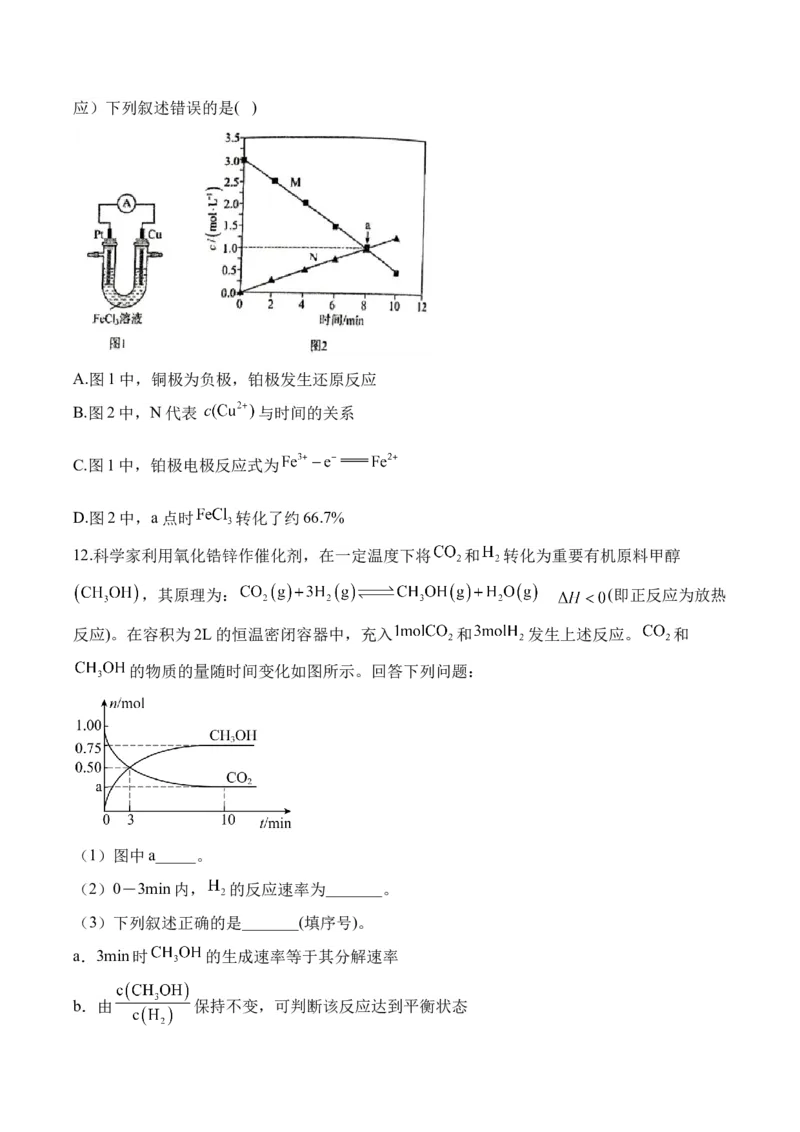
11.为了探究原电池工作原理,设计如图1装置,某离子浓度变化如图2所示(不考虑副反应)下列叙述错误的是( )
A.图1中,铜极为负极,铂极发生还原反应
B.图2中,N代表 与时间的关系
C.图1中,铂极电极反应式为
D.图2中,a点时 转化了约66.7%
12.科学家利用氧化锆锌作催化剂,在一定温度下将 和 转化为重要有机原料甲醇
,其原理为: (即正反应为放热
反应)。在容积为2L的恒温密闭容器中,充入 和 发生上述反应。 和
的物质的量随时间变化如图所示。回答下列问题:
(1)图中a_____。
(2)0-3min内, 的反应速率为_______。
(3)下列叙述正确的是_______(填序号)。
a.3min时 的生成速率等于其分解速率
b.由 保持不变,可判断该反应达到平衡状态c.当 时,该反应一定达到平衡状态
d.当 的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡时,混合气体中 的体积分数为________,此时体系压强与开始
时的压强之比为_____。
(5)其他条件不变时,下列措施不能使生成 的反应速率增大的是_______(填序号)。
a.增大 的浓度 b.将容器的容积变为
c.恒容条件下充入一定量 d.将恒温恒容容器改为绝热恒容容器
(6)已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气
体的平均摩尔质量____(填“增大”“减小”或“不变”)。
(7) 燃料电池的工作原理如图所示,a、b均为铂电极,A、B为燃料或氧气入口。
请写出A入口处电极反应方程式____。
答案以及解析
1.答案:C
解析:A.活化能:反应Ⅰ>反应Ⅱ,故A错误;
B.能量越低越稳定,产物的稳定性:1-丁烯<2-丁烯,故B错误;
C.1-丁烯的能量大于2-丁烯,所以相同条件下完全燃烧放出的热量:1-丁烯>2-丁烯,故C正
确;
D.活化能:反应Ⅰ>反应Ⅱ,反应Ⅱ速率快,选择相对较短的反应时间,及时分离可获得高产
率的2-丁烯,故D错误;
选C。
2.答案:A解析:A.由题给图象可知, 的断键吸收总能量-成键放出总能量=
>0,则该反应是吸热反应,故A
错误;
B.原子结合形成分子的过程是化学键形成过程,是放热过程,2molO原子结合生成 时
放出 能量,故B正确;
C.由图知形成2molNO(g)放热 能量,所以2molNO(g)中的化学键断裂时需要吸
收 能量,故C正确;
D.由图给出图像可知,1mol 断键生成2molN(g)及1mol 的2molO(g)吸收的总能量为
,故D正确;
故答案选A。
3.答案:B
4.答案:A
解析:A项中的图像表示生成物的能量比反应物的能量高,故为吸热反应;
B项中的图像表示反应物的能量比生成物的能量高,故为放热反应;
C项中浓硫酸溶于水放热,不是化学变化;
D项中锌与盐酸反应是放热反应。
5.答案:C
6.答案:C
7.答案:C
8.答案:C
解析:过程①、②均为断键过程,需要吸收能量,A项正确;
总反应方程式可以表示为 ,B项正确;
过程④中,形成了C-S键,C项错误;
反应前后催化剂的质量和化学性质没有改变,D项正确。
9.答案:C
解析:A.加工馒头时添加膨松剂,是为了让馒头更加松软可口,与调控化学反应速率无关,
故A错误;B.进入公共场合需要佩戴口罩可防止病菌的传播,与调控化学反应速率无关,故
B错误;C.黑火药爆炸能在瞬间完成,反应速率很快,故C符合;D.溶洞形成需要几十万年,反应速率很慢,故D不符合;故选C。
10.答案:B
11.答案:C
解析:该原电池的原理是Cu和 反应生成 和 ,Cu做负极,Pt做正极;该原
电池的原理是Cu和 反应生成 和 ,铜元素化合价升高,铜极为负极,铂极做
正极,铁离子得电子生成亚铁离子,化合价降低,发生还原反应,A正确;
由离子方程式 ,随着反应进行, 逐渐减小, 逐渐增
大,因此图2中,N代表 与时间的关系,B正确;
图1中,铂极做正极,铁离子得电子生成亚铁离子,电极反应式为 ,C错
误;
由离子方程式 ,当 时, ,因此a
点时 转化了约 ,D正确。
12.答案:(1)0.25
(2)0.25mol·L-1·min-1
(3)bd
(4)30%;5:8
(5)bc
(6)增大
(7)
解析:根据电子转移的方向,a为负极,b为正极,所以A通入 ,B为氧气或者空气,
A入口处电极反应方程式: 。
(1)根据题意,可列“三段式”如下:a为 的平衡物质的量,根据分析得a=0.25;
(2)3min时,参加反应的 为0.5mol,则 的反应速率为
;
(3)a. 3min时,平衡向正方向进行, 的生成速率大于其分解速率,a错误;
b.随反应进行, 增大,当保持不变时,反应到达平衡,b正确;
c.任意情况下,均存在v ,因此不能判断平衡,c错误;
d. 的体积分数不再变化说明反应已达平衡,d正确;答案选bd。
(4)①平衡时,水的体积分数
②反应前后的压强之比-气体物质的量之比=气体物质的量之比
=;
(5)a.增大反应物浓度,反应速率增大,a正确;
b.增大容器体积,相当于减小压强,反应速率减小,b错误;
c.恒容充入Ne,各物质浓度不变,反应速率不变,c错误;
d.该反应为放热反应,绝热容器中,随反应进行,温度升高,反应速率增大,d正确;故答案
选bc。
(6)该反应放热,降低温度,平衡正移,气体的物质的量减小,平均摩尔质量增大;
(7)根据分析可知,A入口处电极反应方程式:
。