文档内容
2022 届高三化学二轮复习分子结构与性质专题练习
一、选择题(共17题)
1.中国古代四大发明之一的黑火药,爆炸时发生反应:2KNO+S+3C=KS+N↑+3CO ↑。下列表示反应中
3 2 2 2
相关微粒的化学用语正确的是
A.CO 分子为非极性分子
2
B.N 分子中含有1个σ键、1个π键
2
C.KS的电子式:K
2
D.基态硫原子价电子的轨道表示式为
2. 分子的空间构型是三角锥形,而甲烷分子的空间构型是正四面体形,这是因为
A.两种分子的中心原子杂化轨道类型不同, 中N原子为 杂化,而 中C原子为 杂化
B. 分子中N原子形成三个杂化轨道, 分子中C原子形成4个杂化轨道
C. 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强, 分子中无孤电子对
D. 是极性分子而 是非极性分子
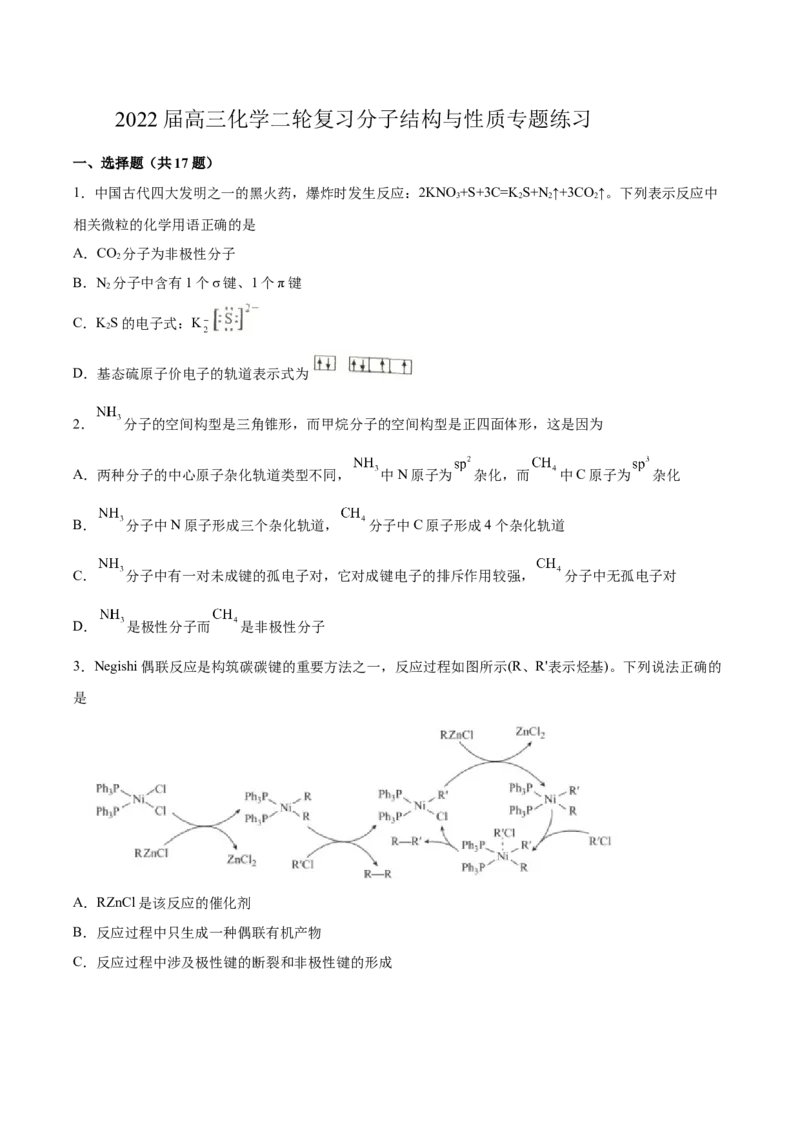
3.Negishi偶联反应是构筑碳碳键的重要方法之一,反应过程如图所示(R、R'表示烃基)。下列说法正确的
是
A.RZnCl是该反应的催化剂
B.反应过程中只生成一种偶联有机产物
C.反应过程中涉及极性键的断裂和非极性键的形成D.存在反应 +RZnCl= +ZnCl
2
4.下列说法正确的是
A.水蒸气转化为液态水的过程中,水分子变小,水的体积减小
B.二氧化碳气体在一定条件下转化为干冰,吸收热量
C.等离子体和离子液体都由阴、阳离子构成,故都能导电
D.固态时的粒子不能自由移动
5.下列各组中的两种固态物质熔化(或升华)时,克服的微粒间相互作用力属于同种类型的是
A.碘和碘化钠 B.金刚石和重晶石(BaSO)
4
C.干冰和二氧化硅 D.冰醋酸和硬脂酸甘油酯
6.干冰气化时,下列各项中发生变化的是
A.分子间化学键 B.分子间距离 C.分子构型 D.分子大小
7.下列变化过程中,没有破坏化学键的是
A.氯化镁熔化 B.冰融化成水 C.氯化氢溶于水 D.电解水
8.氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的
构型和阳离子中氮的杂化方式为( )
A.平面三角形 sp2杂化 B.V形 sp2杂化
C.三角锥形 sp3杂化 D.直线形 sp杂化
9.下列分子:①BF,②CCl ,③NH ,④HO,⑤CHCl,⑥CS。其中只含极性键的非极性分子有(
3 4 3 2 3 2
)
A.①②⑥ B.①②⑤
C.②⑤③ D.①②③
10.a、b两元素形成的一种常见致冷剂可用作人工降雨,c、d形成的一种常见化合物因易液化而用作致冷
剂,a、c两元素形成的一种常见化合物被称为生命之源.关于上述元素的下列说法正确的是
A.含a、b、c、d四种元素的化合物一定是无机物
B.c、d两元素形成的致冷剂还可用做极性溶剂
C.四种元素位于元素周期表的同一分区
D.基态原子含未成对电子数最多的是b元素原子
11.“类推”是常用的学习方法,下列类推的结论中,正确的是
A.存在离子键的化合物是离子化合物,则存在共价键的化合物是共价化合物
B.Cl+H O=HCl+HClO,所以F+H O=HF+HFO
2 2 2 2C.ⅣA族元素氢化物沸点顺序是GeH >SiH>CH,则VA族元素氢化物沸点顺序是AsH >PH >NH
4 4 4 3 3 3
D.第二周期元素氢化物的稳定性顺序是HF>HO>NH ,则第三周期元素氢化物的稳定性顺序是HCl>
2 3
HS>PH
2 3
12.二茂铁[(C H)Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可
5 5 2
作为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是
A.二茂铁分子中存在π键
B.lmol环戊二烯( )中含有σ键的数目为11N
A
C.Fe2+的电子排布式为ls 22s 22p63s23p63d54s1
D.二茂铁中Fe2+与环戊二烯离子(C H-)之间为配位键
5 5
13.下列说法中,不正确的是
A.X射线衍射实验是区别晶体与非晶体的最科学的方法
B.金属键无方向性,金属晶体中原子尽可能采取紧密堆积
C.凡AB 型的共价化合物,其中心原子A均采用sp2杂化轨道成键
3
D.乙醇与水互溶可以用“相似相溶”原理和氢键来解释
14.下列分子或离子的VSEPR模型与空间立体构型一致的是
A.NH B.CCl C.HO D.ClO
3 4 2
15.N 表示阿伏加德罗常数的值,下列叙述正确的是
A
A.HO 的稳定性大于 HS,是因为 HO分子间存在氢键
2 2 2
B.1~36 号元素中,基态原子未成对电子数最多的元素是 Cr
C.主族元素的电负性越大,元素原子的第一电离能一定越大
D.1 mol丙酮( )分子中含有σ键的数目为 8N
A
16.下列说法不正确的是
A.某金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、
21703…,当它与氯气反应时生成的阳离子是X2+
B.氨气极易溶于水的重要原因之一:氨分子与水分子之间能形成氢键C.标况下,22.4LCH 中所含的π键数和18g冰中所含的氢键数均为2N
2 2 A
D.由于氢键的作用,使NH 、HO、HF的沸点反常,且沸点高低顺序为HF>HO>NH
3 2 2 3
17.根据价层电子对互斥理论及原子轨道的杂化理论推测,SO 分子的空间构型和中心原子的杂化方式是
3
A.平面三角形,sp2杂化 B.三角形,sp3杂化
C.正四面体形,sp2杂化 D.正方形,sp3杂化
二、综合题(共6题)
18.Fe O 一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe O。某化学实验小组通过实验来探究
3 4 2 3
一黑色粉末是否由Fe O、CuO组成(不含有其它黑色物质)。探究过程如下:
3 4
提出假设:假设1. 黑色粉末是CuO;假设2. 黑色粉末是Fe O;
3 4
假设3. ______________________________。
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
⑴若假设1成立,则实验现象是________________。
⑵若所得溶液显血红色,则假设_________成立。
⑶为进一步探究,继续向所得溶液加入足量铁粉,若产生_______的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH ·H O=Cu(NH )2++4HO。
3 2 3 4 2
⑷为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生
__________现象,则假设2成立;若产生______________现象,则假设3成立。
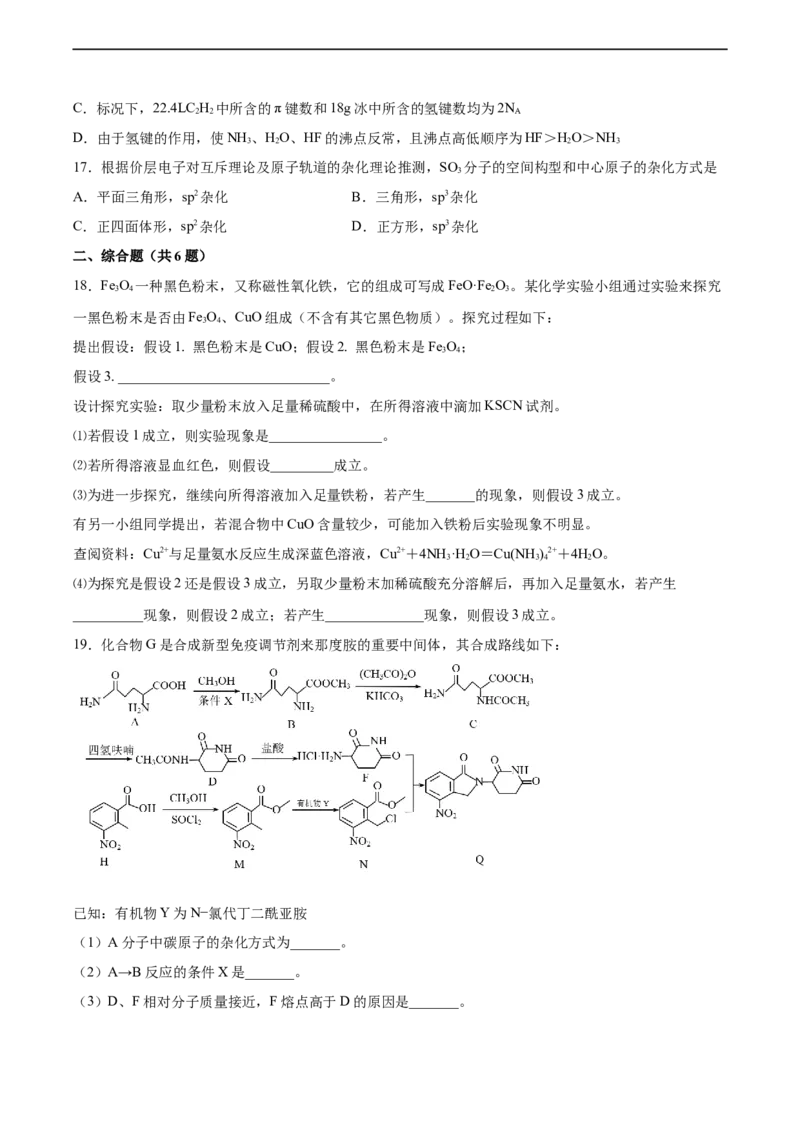
19.化合物G是合成新型免疫调节剂来那度胺的重要中间体,其合成路线如下:
已知:有机物Y为N−氯代丁二酰亚胺
(1)A分子中碳原子的杂化方式为_______。
(2)A→B反应的条件X是_______。
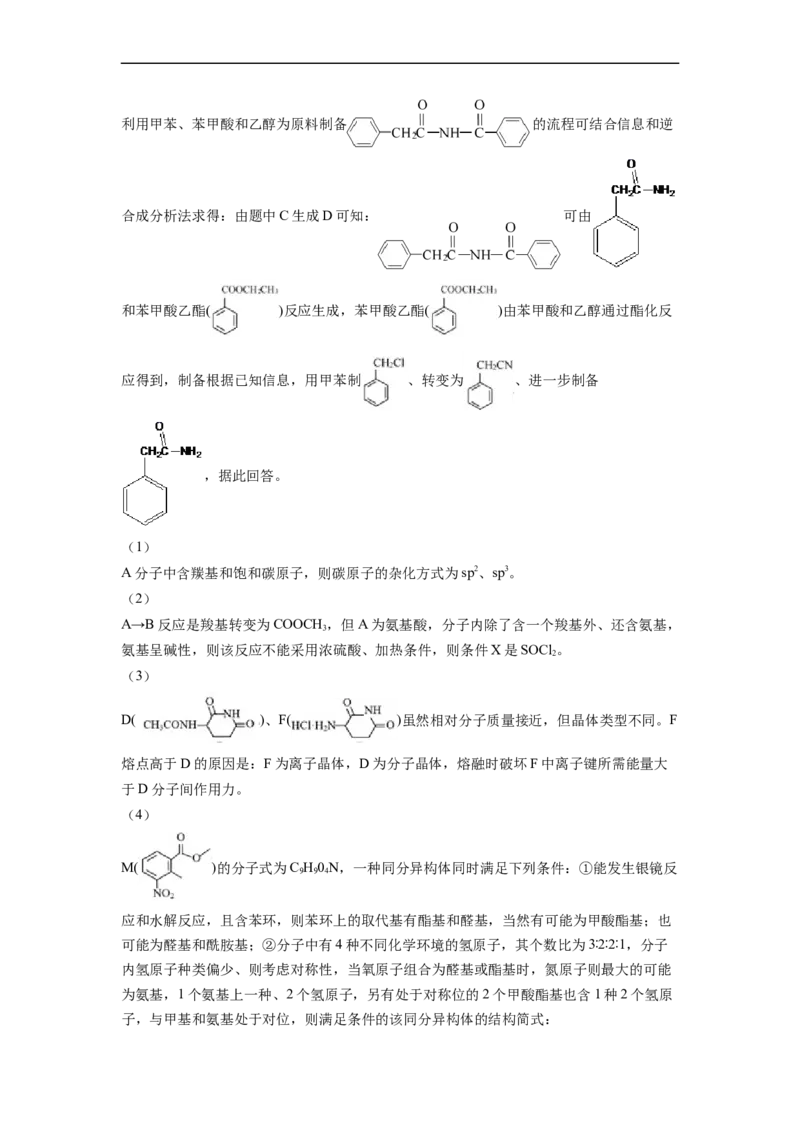
(3)D、F相对分子质量接近,F熔点高于D的原因是_______。(4)M的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式_______。
①能发生银镜反应和水解反应,且含苯环。
②分子中有4种不同化学环境的氢原子,其个数比为3∶2∶2∶1。
(5)已知:RCHBr RCHCN ,写出以甲苯、苯甲酸和CHCHOH为原料
2 2 3 2
制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例
见本题题干)_______。
20.已知X、Y、Z、W四种元素是元素周期表中三个不同短周期的元素,且原子序数依次增大。X、W同
主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中
有3个共价键。试推断:
(1)X、Y、Z、W四种元素的符号:X 、Y 、Z 、W 。元素Z在周期
表中的位置是______________________。
(2)由以上元素中的两种元素组成的化合物,溶于水后水溶液显碱性,该化合物的电子式分别为
、 (任写2种)。
(3)由X、Y、Z所形成的共价化合物(Y呈最高价)是 ,离子化合物是
。(均写化学式)
(4)由X和Y两种元素组成的18电子的分子为__________(写分子式),该分子中所有原子都已达到类
似于稀有气体原子的稳定结构,则其结构式为__________。
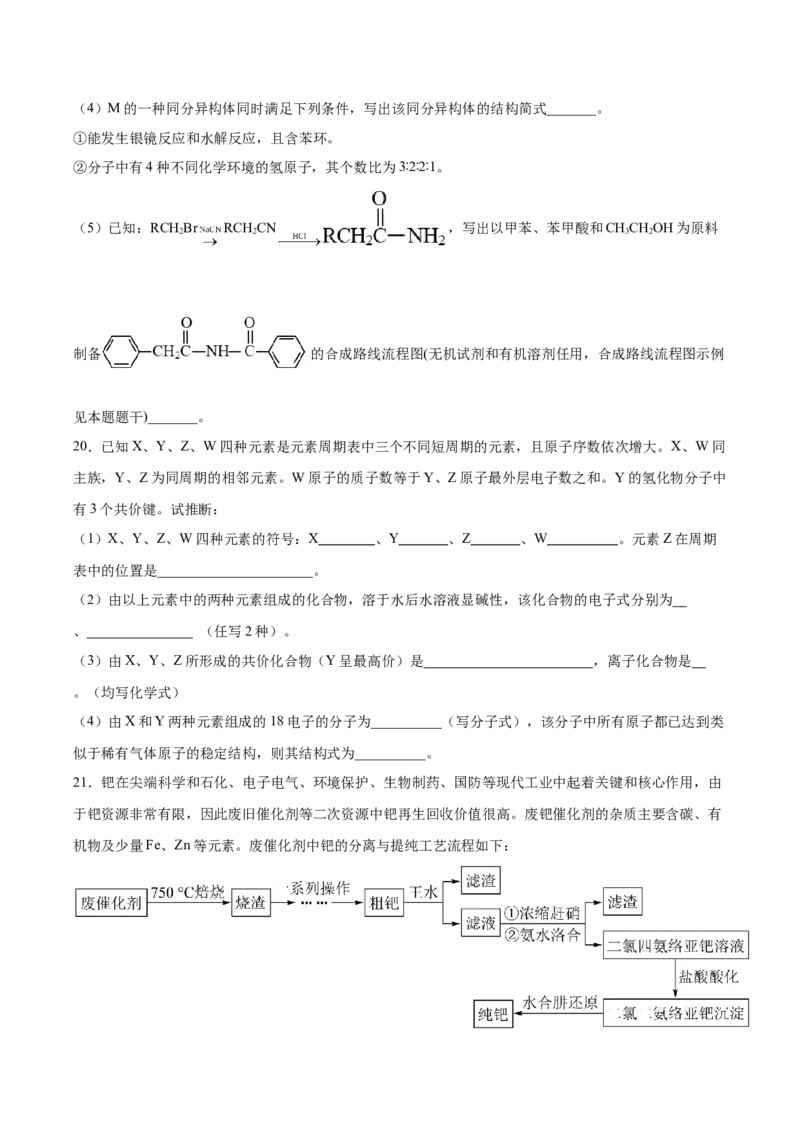
21.钯在尖端科学和石化、电子电气、环境保护、生物制药、国防等现代工业中起着关键和核心作用,由
于钯资源非常有限,因此废旧催化剂等二次资源中钯再生回收价值很高。废钯催化剂的杂质主要含碳、有
机物及少量Fe、Zn等元素。废催化剂中钯的分离与提纯工艺流程如下:已知:
①钯常见的化合价有+2价和+4价。钯容易形成配位化合物,如[Pd(NH)]Cl 、[Pb(NH)]Cl 、
3 4 2 3 2 2
[H Pd(NO )]。
2 3 4
②当有硝酸存在时,钯易与硝酸形成稳定的配位体。
回答下列问题:
(1)“焙烧”的目的是___________。
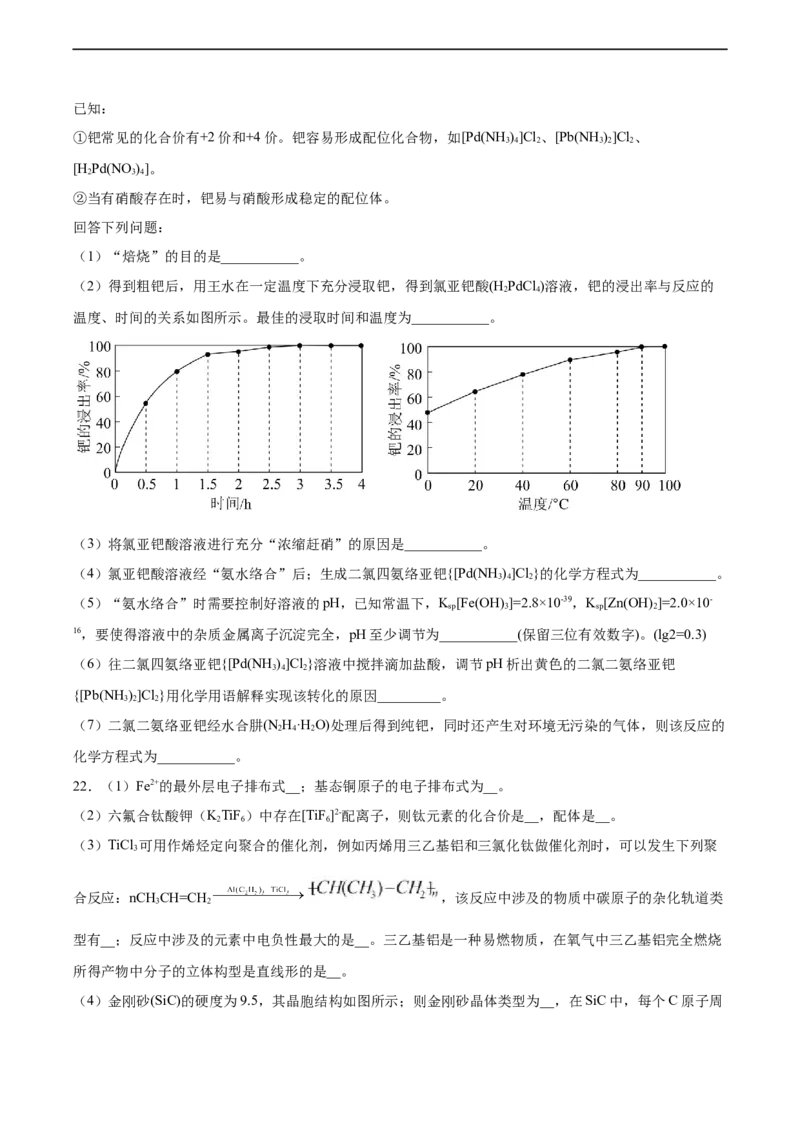
(2)得到粗钯后,用王水在一定温度下充分浸取钯,得到氯亚钯酸(H PdCl )溶液,钯的浸出率与反应的
2 4
温度、时间的关系如图所示。最佳的浸取时间和温度为___________。
(3)将氯亚钯酸溶液进行充分“浓缩赶硝”的原因是___________。
(4)氯亚钯酸溶液经“氨水络合”后;生成二氯四氨络亚钯{[Pd(NH)]Cl }的化学方程式为___________。
3 4 2
(5)“氨水络合”时需要控制好溶液的pH,已知常温下,K [Fe(OH) ]=2.8×10-39,K [Zn(OH) ]=2.0×10-
sp 3 sp 2
16,要使得溶液中的杂质金属离子沉淀完全,pH至少调节为___________(保留三位有效数字)。(lg2=0.3)
(6)往二氯四氨络亚钯{[Pd(NH)]Cl }溶液中搅拌滴加盐酸,调节pH析出黄色的二氯二氨络亚钯
3 4 2
{[Pb(NH)]Cl }用化学用语解释实现该转化的原因_________。
3 2 2
(7)二氯二氨络亚钯经水合肼(N H·H O)处理后得到纯钯,同时还产生对环境无污染的气体,则该反应的
2 4 2
化学方程式为___________。
22.(1)Fe2+的最外层电子排布式__;基态铜原子的电子排布式为__。
(2)六氟合钛酸钾(KTiF )中存在[TiF]2-配离子,则钛元素的化合价是__,配体是__。
2 6 6
(3)TiCl 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚
3
合反应:nCHCH=CH ,该反应中涉及的物质中碳原子的杂化轨道类
3 2
型有__;反应中涉及的元素中电负性最大的是__。三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧
所得产物中分子的立体构型是直线形的是__。
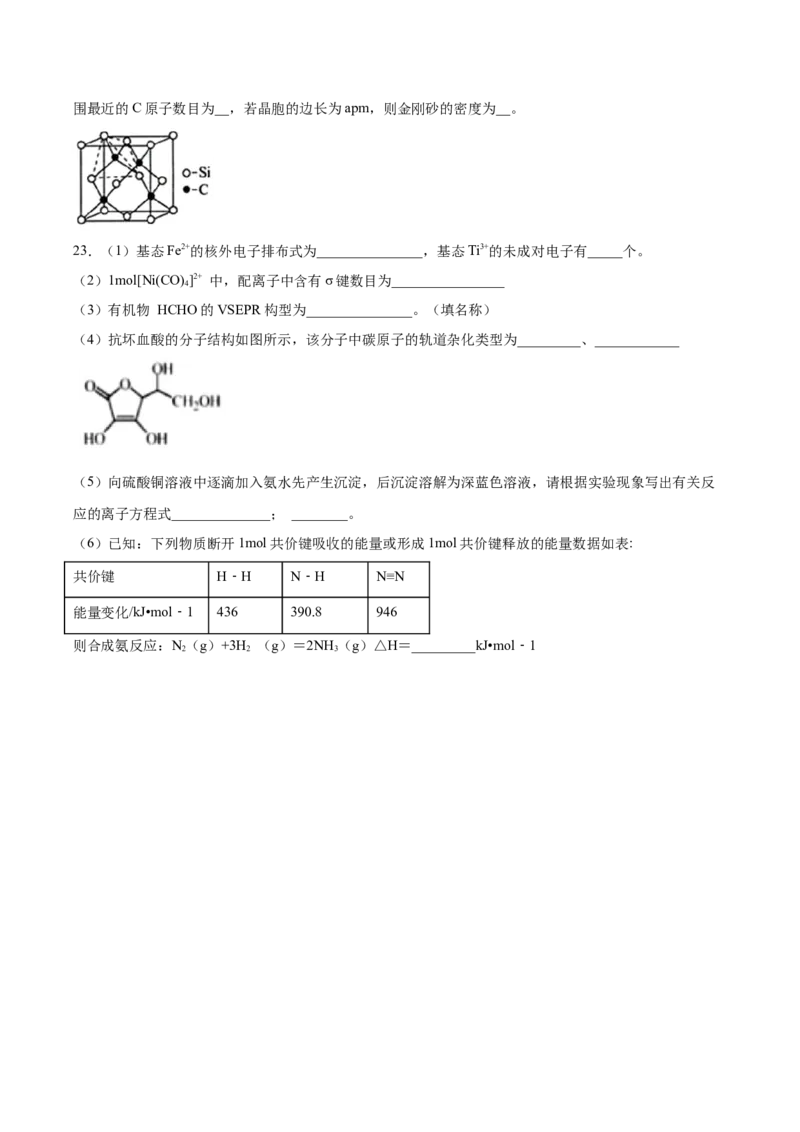
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为__,在SiC中,每个C原子周围最近的C原子数目为__,若晶胞的边长为apm,则金刚砂的密度为__。
23.(1)基态Fe2+的核外电子排布式为_______________,基态Ti3+的未成对电子有_____个。
(2)1mol[Ni(CO) ]2+ 中,配离子中含有σ键数目为________________
4
(3)有机物 HCHO的VSEPR构型为_______________。(填名称)
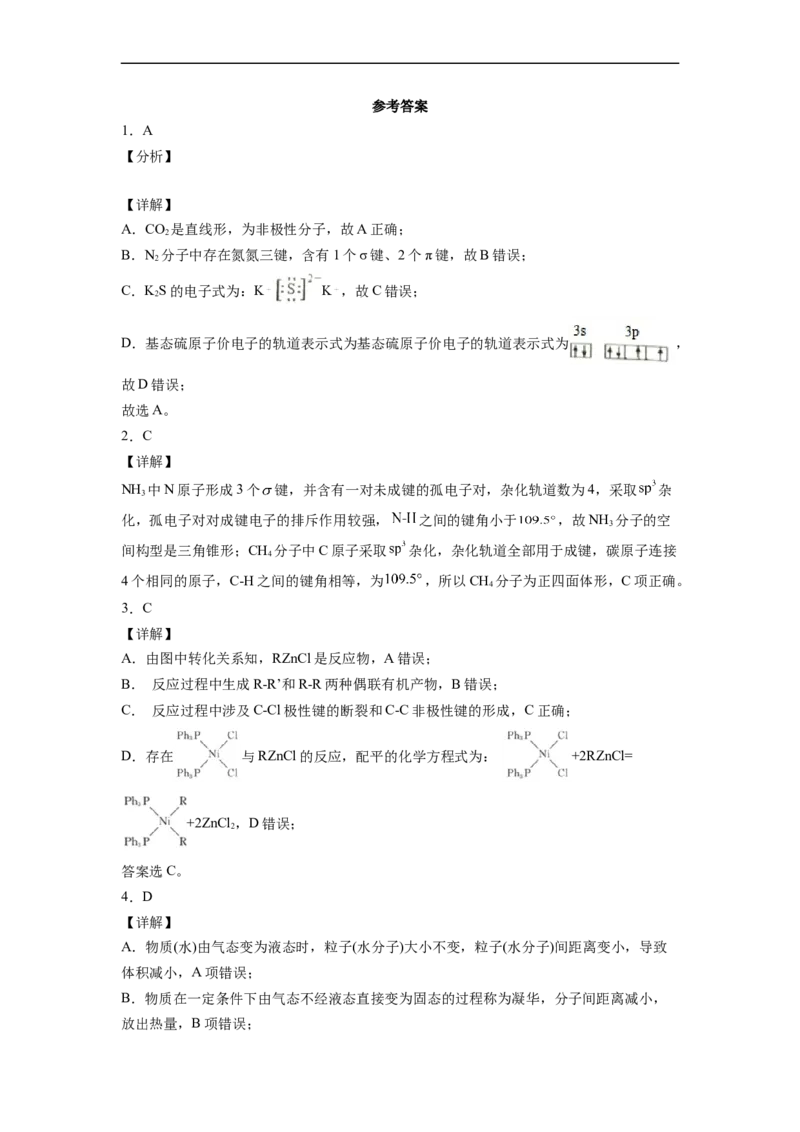
(4)抗坏血酸的分子结构如图所示,该分子中碳原子的轨道杂化类型为_________、____________
(5)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反
应的离子方程式______________; ________。
(6)已知:下列物质断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表:
共价键 H﹣H N﹣H N≡N
能量变化/kJ•mol﹣1 436 390.8 946
则合成氨反应:N(g)+3H (g)=2NH (g)△H=_________kJ•mol﹣1
2 2 3参考答案
1.A
【分析】
【详解】
A.CO 是直线形,为非极性分子,故A正确;
2
B.N 分子中存在氮氮三键,含有1个σ键、2个π键,故B错误;
2
C.KS的电子式为:K K ,故C错误;
2
D.基态硫原子价电子的轨道表示式为基态硫原子价电子的轨道表示式为 ,
故D错误;
故选A。
2.C
【详解】
NH 中N原子形成3个 键,并含有一对未成键的孤电子对,杂化轨道数为4,采取 杂
3
化,孤电子对对成键电子的排斥作用较强, 之间的键角小于 ,故NH 分子的空
3
间构型是三角锥形;CH 分子中C原子采取 杂化,杂化轨道全部用于成键,碳原子连接
4
4个相同的原子,C-H之间的键角相等,为 ,所以CH 分子为正四面体形,C项正确。
4
3.C
【详解】
A.由图中转化关系知,RZnCl是反应物,A错误;
B. 反应过程中生成R-R’和R-R两种偶联有机产物,B错误;
C. 反应过程中涉及C-Cl极性键的断裂和C-C非极性键的形成,C正确;
D.存在 与RZnCl的反应,配平的化学方程式为: +2RZnCl=
+2ZnCl ,D错误;
2
答案选C。
4.D
【详解】
A.物质(水)由气态变为液态时,粒子(水分子)大小不变,粒子(水分子)间距离变小,导致
体积减小,A项错误;
B.物质在一定条件下由气态不经液态直接变为固态的过程称为凝华,分子间距离减小,
放出热量,B项错误;C.等离子体是由电子、阳离子和电中性粒子(分子或原子)组成的整体上呈电中性的气态物
质,不存在阴离子;离子液体是熔点不高的仅由阴、阳离子组成的液体物质,二者均可以
导电,C项错误;
D.同种物质的粒子,在气态时能自由移动,在固态时只能在固定的位置上振动,在液态
时介于二者之间,D项正确;
答案选D。
5.D
【详解】
A.碘升华破坏分子间作用力,碘化钠熔化破坏离子键,两者克服的微粒间相互作用力不同,
不符合题意;
B.金刚石熔化破坏共价键,重晶石(BaSO)熔化破坏离子键,两者克服的微粒间相互作
4
用力不同,不符合题意;
C.干冰升华破坏分子间作用力,二氧化硅熔化破坏共价键,两者克服的微粒间相互作用力
不同,不符合题意;
D.冰醋酸和硬脂酸甘油酯熔化均破坏分子间作用力,两者克服的微粒间相互作用力相同,
符合题意;
答案选D。
6.B
【详解】
干冰气化时,由固态变为气态,分子间作用力被破坏,而分子间作用力属于范德华力,不
是化学键;气化过程中,分子间的距离发生改变,但分子的大小和分子的构型并未改变,
故选B。
7.B
【分析】
化学变化中化学键一定被破坏,共价化合物或离子化合物电离时化学键被破坏。
【详解】
A. 氯化镁熔化,离子键破坏,故A不选;
B. 冰融化成水共价键不变,只破坏分子间作用力,故B选;
C. 氯化氢溶于水,H-Cl共价键破坏,故C不选;
D. 电解水发生化学变化,化学键一定破坏,故D不选;
故选B。
8.D
【分析】
氮的最高价氧化物为NO,由两种离子构成,其中阴离子构型为平面正三角形,化学式应
2 5
为NO -,则其阳离子的化学式为:NO +,根据其价层电子对数判断。
3 2
【详解】
氮的最高价氧化物为NO,由两种离子构成,其中阴离子构型为平面正三角形,化学式应
2 5为NO -,则其阳离子的化学式为:NO +,其中心N原子价电子对数为2+ (5-1-2×2)=2,所
3 2
以其中的氮原子按sp方式杂化,阳离子的构型为直线型,故合理选项是D。
9.A
【分析】
由同种原子形成的共价键是非极性键,其共用电子对不偏向任何一个原子。共用电子对偏
移的共价键叫做极性键,上述分子都只含极性键。非极性分子指的是从整个分子看,分子
里电荷分布是对称的(正负电荷中心能重合)的分子。
【详解】
①BF 中含有极性键,为平面三角形分子,正负电荷重心重叠,为非极性分子,
3
②CCl 中含有极性键,空间结构为正四面体,正负电荷的中心重合,为非极性分子,
4
③NH 中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,为极性分子,
3
④H O中含有极性键,空间结构为V型,为极性分子;
2
⑤CHCl中含有极性键,空间结构为四面体,正负电荷的中心不重合,为极性分子,
3
⑥CS 中含有极性键,空间结构为直线型,正负电荷的中心重合,为非极性分子;
2
答案选A。
10.B
【分析】
a、b两元素形成的一种常见致冷剂可用作人工降雨,a、b两元素形成的化合物是CO;
2
c、d形成的一种常见化合物因易液化而用作致冷剂,c、d形成的一种常见化合物是NH ;
3
a、c两元素形成的一种常见化合物被称为生命之源,a、c两元素形成的一种常见化合物是
HO;a是O元素、b是C元素;c是H元素、d是N元素。
2
【详解】
A.含C、H、O、N四种元素的化合物可能是有机物,如氨基酸,故A错误;
B.NH 是极性分子,还可用做极性溶剂,故B正确;
3
C.H位于元素周期表的S区,C、O、N四种元素都位于元素周期表的P区,故C错误;
D.C原子的基态原子含2个未成对电子,N原子的基态原子含3个未成对电子,故D错误;
选B。
11.D
【详解】
A.存在离子键的化合物是一定是离子化合物,但存在共价键的化合物不一定是共价化合
物,如氢氧化钠含有共价键,属于离子化合物,故A错误;
B.氯气与水反应生成氯化氢和盐酸Cl+H O=HCl+HClO,但氟气与水反应生成氟化氢和
2 2
氧气2F+2H O=4HF+O ,故B错误;
2 2 2
C.氢化物的相对分子质量越大,沸点越高,分子间含有氢键的沸点较高,ⅣA族元素氢
化物沸点顺序是GeH >SiH>CH;而NH 分子间存在氢键,其沸点较高,所以ⅤA族元
4 4 4 3素氢化物沸点顺序是NH >AsH >PH ,故C错误;
3 3 3
D.元素的非金属性越强,其氢化物越稳定,非金属性F>O>N,Cl>S>P,所以第二周
期元素氢化物稳定性顺序是HF>HO>NH ,第三周期元素氢化物稳定性顺序是HCl>HS
2 3 2
>PH ,故D正确;
3
答案选D。
12.C
【详解】
A项、二茂铁中环戊二烯离子含有碳碳双键,碳碳双键之间存在π键,则二茂铁分子中存
在π键,故A正确;
B项、环戊二烯分子中含有σ键的数目为11,π键数目为2,则lmol环戊二烯中含有σ键的
数目为11N ,故B错误;
A
C项、铁原子核外有26个电子,铁原子失去最外层两个电子变为亚铁离子,根据构造原理
知,亚铁离子核外电子排布式为1s22s22p63s23p63d6,故C错误;
D项、二茂铁是Fe2+与环戊二烯离子(C H-)通过配位键形成的分子,故D正确;
5 5
故选C。
13.C
【详解】
A项,区别晶体与非晶体最科学的方法是X-射线衍射实验,A项正确;
B项,金属键无方向性,金属原子总是尽可能多的吸引其它原子,金属晶体中原子尽可能
采取紧密堆积,从而使空间被充分利用,B项正确;
C项,AB 型共价化合物中,若A上没有孤电子对则A采用sp2杂化轨道成键如BF 等,若
3 3
A上有1对孤电子对则A采用sp3杂化轨道成键如NH 等,C项错误;
3
D项,乙醇与水互溶的原因是:(1)乙醇和水都是极性分子,(2)乙醇和水分子中都含
O—H键,乙醇和水分子间形成氢键,乙醇与水互溶可以用“相似相溶”原理和氢键解释,
D项正确;
答案选C。
14.B
【分析】
如果该微粒中不存在孤电子对,则该微粒的VSEPR模型和其空间立体构型就一致,否则不
一致,据此分析解答。
【详解】
A.该分子中N原子价层电子对个数=3+ =4,含有一个孤电子对,VSEPR模型为四
面体形,立体构型为三角锥形,A不符合题意;
B.CCl 该分子中C原子价层电子对个数=4+ =4,且不含孤电子对,其VSEPR模型
4
和立体构型相同,均为四面体形,B符合题意;C.该分子中O原子价层电子对个数=2+ =4,且含有两个孤电子对,VSEPR模型为
四面体形,立体构型为V形,C不符合题意;
D.该离子中Cl原子价层电子对个数=3+ =4,且含有一个孤电子对,VSEPR模型
为四面体形,立体构型为三角锥形,D不符合题意;
故合理选项是B。
15.B
【详解】
A.物质的稳定性与化学键是强弱有关,与氢键无关,则HO的稳定性大于HS,与O-H
2 2
键比S-H键的键能大小有关,故A错误;
B.1~36 号元素中未成对电子数最多,则外围电子排布为3d54s1,核外电子数为24,为
Cr元素,是在第四周期第ⅥB族,故B正确;
C.元素的电负性大,第一电离能不一定大,如N元素的电负性小于氧元素的电负性,但
N元素原子2p能级为半满稳定状态,第一电离能大于O元素,故C错误;
D.丙酮分子含有6个C-H键、2个C-C键、1个C=O键,分子中含有9个σ键,因此1
mol丙酮分子中含有9 mol σ键,含有σ键的数目为9 N ,故D错误;
A
故选B。
16.D
【详解】
A.该元素第三电离能剧增,最外层应有2个电子,表现+2价,当它与氯气反应时最可能
生成的阳离子是X2+,故A正确;B.N、O的电负性强,分子之间形成氢键,氨溶于水后
氨分子与水分子之间形成氢键,故B正确;C.乙炔的结构式为H-C≡C-H,则1mol乙炔中
含2molπ键,冰中水分子的O原子以类似于金刚石中C原子的四面体空间网状结构排列,
每2个O原子间都有一个H原子,更靠近H原子的O原子与它形成共价键,另一个与它形
成氢键,即每个H原子都形成一个氢键,所以1mol冰中存在2mol氢键,标况下22.4LCH
2 2
的物质的量为1mol,18g冰的物质的量也为1mol,则标况下22.4LCH 中所含的π键数和
2 2
18g冰中所含的氢键数均为2mol,故C正确;D.由于氢键的作用,使NH 、HO、HF在
3 2
同主族氢化物中的沸点反常,但常温下水为液体,则沸点高低顺序为HO>HF>NH ,故
2 3
D错误;故选D。
17.A
【详解】
根据价层电子对互斥理论可知,SO 分子中硫原子含有的孤对电子对数= (6-2×3)=0,所以
3
SO 是平面三角形结构,硫原子是sp2杂化,答案选A。
3
18.黑色粉末是CuO和Fe O 的混合物 溶液显蓝色 2或3 有红色固体析出
3 4
红褐色沉淀 红褐色沉淀,同时溶液呈深蓝色【分析】
依据物质的颜色结合假设1和假设2解答;
(1)硫酸与氧化铜反应生成硫酸铜,硫酸铜溶液呈蓝色;
(2)三价铁离子遇到KSCN显血红色,据此解答;
(3)铁粉与铜离子反应置换出铜;
(4)如果假设2成立,则加入硫酸后得到的溶液中含有三价铁离子,加入氨水后生成氢氧化
铁红褐色沉淀;如果假设3成立则加入硫酸后溶液中既含有三价铁离子还含有铜离子,加
入足量氨水反应生成氢氧化铁红褐色沉淀;铜离子与氨水发生反应Cu2+
+4NH•H O═Cu(NH)2++4H O,盐酸变为深蓝色。
3 2 3 4 2
【详解】
该物质是黑色固体,也可能既含有CuO又含有Fe O 黑色粉末,是CuO和Fe O 的混合物;
3 4 3 4
(1)硫酸与氧化铜发生反应:CuO+HSO4=CuSO +H O,硫酸铜溶液显蓝色,若假设1成立,
2 4 2
实验现象为:溶液显蓝色;
(2)三价铁离子与KSCN试剂络合成红色络合物,所以如果所得溶液显血红色,证明加入硫
酸后生成了三价铁离子,说明黑色物质中含有Fe O,所以假设2或3都有可能;
3 4
(3)铁粉与铜离子发生反应:2Cu2++Fe=3Fe2++Cu,所以如果产生红色物质,证明溶液中存在
铜离子,则黑色固体中含有CuO,故假设3正确;
(4)如果假设2成立,则加入硫酸后得到的溶液中含有三价铁离子,加入氨水后生成氢氧化
铁红褐色沉淀;如果假设3成立则加入硫酸后溶液中既含有三价铁离子还含有铜离子,加
入足量氨水反应生成氢氧化铁红褐色沉淀;铜离子与氨水发生反应Cu2+
+4NH•H O═Cu(NH)2++4H O,盐酸变为深蓝色。
3 2 3 4 2
19.
(1)sp2、sp3
(2)SOCl
2
(3)F为离子晶体,D为分子晶体,熔融时破坏F中离子键所需能量大于D分子间作用力
(4) 或
(5)
【分析】利用甲苯、苯甲酸和乙醇为原料制备 的流程可结合信息和逆
合成分析法求得:由题中C生成D可知: 可由
和苯甲酸乙酯( )反应生成,苯甲酸乙酯( )由苯甲酸和乙醇通过酯化反
应得到,制备根据已知信息,用甲苯制 、转变为 、进一步制备
,据此回答。
(1)
A分子中含羰基和饱和碳原子,则碳原子的杂化方式为sp2、sp3。
(2)
A→B反应是羧基转变为COOCH ,但A为氨基酸,分子内除了含一个羧基外、还含氨基,
3
氨基呈碱性,则该反应不能采用浓硫酸、加热条件,则条件X是SOCl 。
2
(3)
D( )、F( )虽然相对分子质量接近,但晶体类型不同。F
熔点高于D的原因是:F为离子晶体,D为分子晶体,熔融时破坏F中离子键所需能量大
于D分子间作用力。
(4)
M( )的分子式为C H0N,一种同分异构体同时满足下列条件:①能发生银镜反
9 9 4
应和水解反应,且含苯环,则苯环上的取代基有酯基和醛基,当然有可能为甲酸酯基;也
可能为醛基和酰胺基;②分子中有4种不同化学环境的氢原子,其个数比为3∶2∶2∶1,分子
内氢原子种类偏少、则考虑对称性,当氧原子组合为醛基或酯基时,氮原子则最大的可能
为氨基,1个氨基上一种、2个氢原子,另有处于对称位的2个甲酸酯基也含1种2个氢原
子,与甲基和氨基处于对位,则满足条件的该同分异构体的结构简式:或 。酰胺基的不满足。
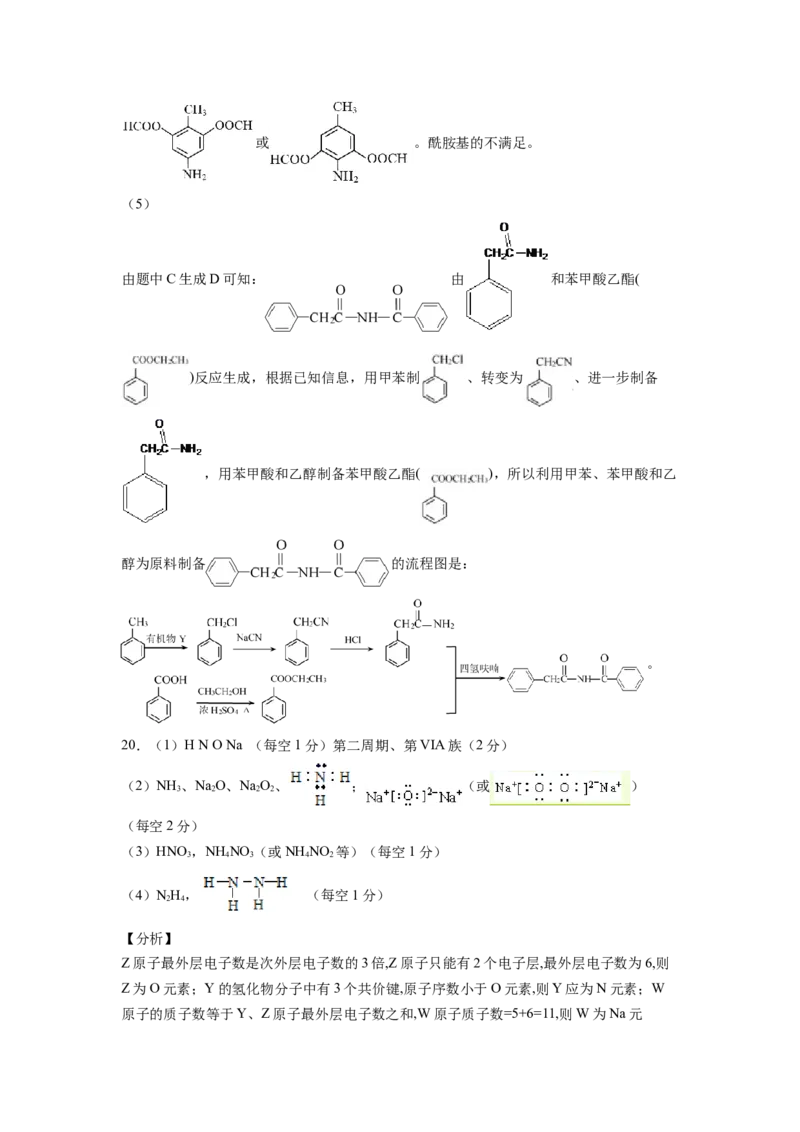
(5)
由题中C生成D可知: 由 和苯甲酸乙酯(
)反应生成,根据已知信息,用甲苯制 、转变为 、进一步制备
,用苯甲酸和乙醇制备苯甲酸乙酯( ),所以利用甲苯、苯甲酸和乙
醇为原料制备 的流程图是:
。
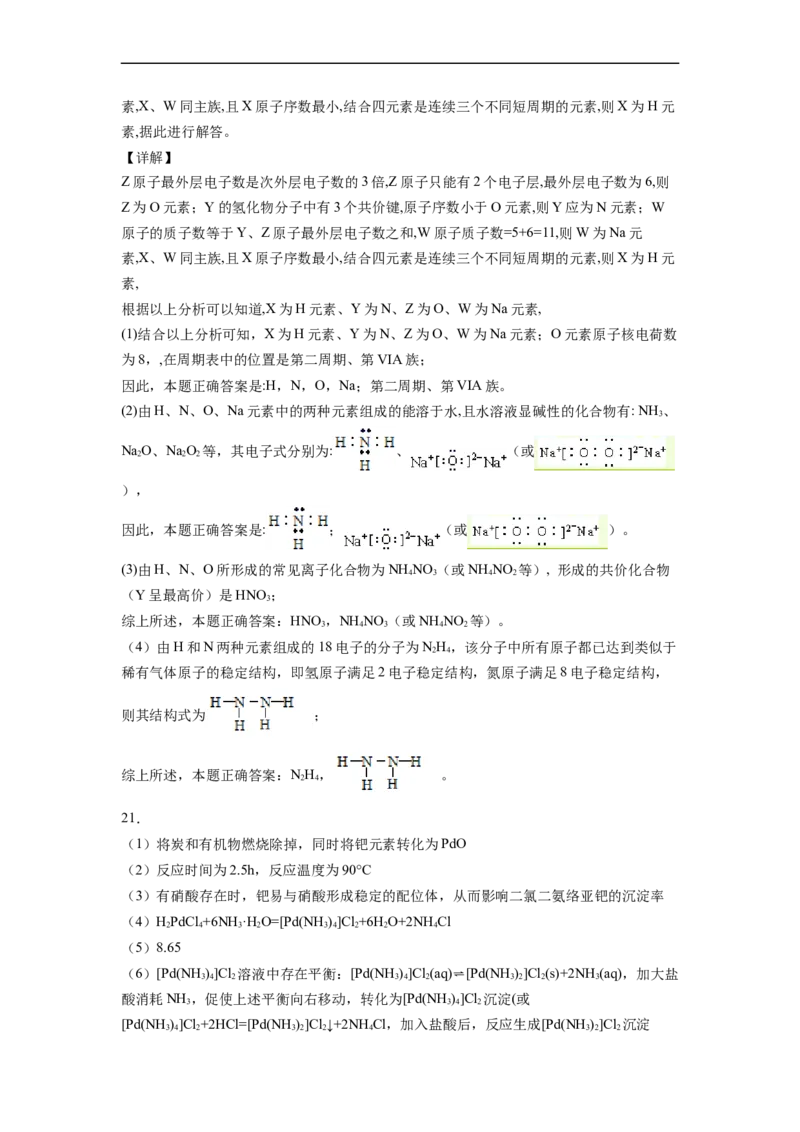
20.(1)H N O Na (每空1分)第二周期、第VIA族(2分)
(2)NH 、NaO、NaO、 ; (或 )
3 2 2 2
(每空2分)
(3)HNO,NH NO (或NH NO 等)(每空1分)
3 4 3 4 2
(4)NH, (每空1分)
2 4
【分析】
Z原子最外层电子数是次外层电子数的3倍,Z原子只能有2个电子层,最外层电子数为6,则
Z为O元素;Y的氢化物分子中有3个共价键,原子序数小于O元素,则Y应为N元素;W
原子的质子数等于Y、Z原子最外层电子数之和,W原子质子数=5+6=11,则W为Na元素,X、W同主族,且X原子序数最小,结合四元素是连续三个不同短周期的元素,则X为H元
素,据此进行解答。
【详解】
Z原子最外层电子数是次外层电子数的3倍,Z原子只能有2个电子层,最外层电子数为6,则
Z为O元素;Y的氢化物分子中有3个共价键,原子序数小于O元素,则Y应为N元素;W
原子的质子数等于Y、Z原子最外层电子数之和,W原子质子数=5+6=11,则W为Na元
素,X、W同主族,且X原子序数最小,结合四元素是连续三个不同短周期的元素,则X为H元
素,
根据以上分析可以知道,X为H元素、Y为N、Z为O、W为Na元素,
(1)结合以上分析可知,X为H元素、Y为N、Z为O、W为Na元素;O元素原子核电荷数
为8,,在周期表中的位置是第二周期、第VIA族;
因此,本题正确答案是:H,N,O,Na;第二周期、第VIA族。
(2)由H、N、O、Na元素中的两种元素组成的能溶于水,且水溶液显碱性的化合物有: NH 、
3
NaO、NaO 等,其电子式分别为: 、 (或
2 2 2
),
因此,本题正确答案是: ; (或 )。
(3)由H、N、O所形成的常见离子化合物为NH NO (或NH NO 等), 形成的共价化合物
4 3 4 2
(Y呈最高价)是HNO;
3
综上所述,本题正确答案:HNO,NH NO (或NH NO 等)。
3 4 3 4 2
(4)由H和N两种元素组成的18电子的分子为NH,该分子中所有原子都已达到类似于
2 4
稀有气体原子的稳定结构,即氢原子满足2电子稳定结构,氮原子满足8电子稳定结构,
则其结构式为 ;
综上所述,本题正确答案:NH, 。
2 4
21.
(1)将炭和有机物燃烧除掉,同时将钯元素转化为PdO
(2)反应时间为2.5h,反应温度为90°C
(3)有硝酸存在时,钯易与硝酸形成稳定的配位体,从而影响二氯二氨络亚钯的沉淀率
(4)HPdCl +6NH·H O=[Pd(NH )]Cl +6H O+2NH Cl
2 4 3 2 3 4 2 2 4
(5)8.65
(6)[Pd(NH
3
)
4
]Cl
2
溶液中存在平衡:[Pd(NH
3
)
4
]Cl
2
(aq)⇌[Pd(NH
3
)
2
]Cl
2
(s)+2NH
3
(aq),加大盐
酸消耗NH ,促使上述平衡向右移动,转化为[Pd(NH)]Cl 沉淀(或
3 3 4 2
[Pd(NH)]Cl +2HCl=[Pd(NH )]Cl ↓+2NHCl,加入盐酸后,反应生成[Pd(NH)]Cl 沉淀
3 4 2 3 2 2 4 3 2 2(7)2[Pd(NH)]Cl +N H∙H O=2Pd+4NH C1+H O+N↑
3 2 2 2 4 2 4 2 2
【分析】
废钯催化剂在750℃的高温下焙烧,碳、有机物及少量Fe、Zn被氧气氧化生成氧化物,经
系列操作得粗钯,滤渣中含有Pd、SiO,二氧化硅不溶于王水,但Pd能溶于王水生成溶液,
2
同时生成气体,加入浓氨水调节溶液pH沉淀铁离子,得到溶液中加入盐酸酸析得到沉淀
Pd(NH )Cl,通过水和肼还原得纯钯;
3 2 2
(1)
高温焙烧时,一方面可燃物(C、有机物)可燃烧变成CO、HO除去,另一方面钯元素以及
2 2
一些杂质元素在焙烧中转化,根据后续信息知钯变成PdO;
(2)
根据题中信息可得,在反应时间为2.5h和90℃时钯的浸出率最高;
(3)
将氯亚钯酸溶液进行充分“浓缩赶硝”的原因是有硝酸存在时,钯易与硝酸形成稳定的配
位体,从而影响二氯二氨络亚钯的沉淀率;
(4)
根据信息,反应方程式为HPdCl + 6NH ·H O= [Pd( NH )]Cl + 6H O + 2NH Cl;
2 4 3 2 3 4 2 2 4
(5)
Kp (Zn(OH) ] = [Zn2+]·[0H-]2= 2.0×10-16,沉淀完全时[Zn2+]可以计算得出[0H-] = ×10-5.5,则
2
[H+]= ×10-8.5,pH=-lg[H+] = -lg( ×10-8.5)=8.65;
(6)
[Pd( NH )]Cl 溶液中存在平衡;[Pd( NH ) ]Cl (aq) [Pd (NH )]Cl (s) + 2NH (aq),加入
3 4 2 3 4 2 3 4 2 3
盐酸消耗NH ,促使上述平衡向右移动,转化为[Pd( NH )]Cl 沉淀;
3 3 4 2
(7)
结合题意,该反应的化学方程式为:2[Pd( NH )]Cl + N H·H O=2Pd+4NH Cl+H O+N↑;
3 4 2 2 4 2 4 2 2
22.3s23p63d6 [Ar]3d104s1或1s22s22p63s23p63d104s1 +4 F- sp3、sp2 Cl
CO 原子晶体 12
2
【分析】
(1)Fe原子失去最外层2个电子生成Fe2+,其M电子层变为最外层,M电子层上3s、3p、3d
能级上分别含有2、8、6个电子;Cu原子核外有29个电子,根据构造原理书写基态Cu原
子电子排布式;
(2)F元素的化合价为-1价,该离子的化合价为-2价,据此计算Ti元素化合价;配体是氟离
子;
(3)甲基上的C原子价层电子对个数是4、其它两个碳原子价层电子对个数都是3,根据价层电子对互斥理论判断C原子杂化类型;元素的非金属性越强,其电负性越大;该物质燃
烧生成氧化铝和二氧化碳、水,立体构型是直线形的是CO;
2
(4)原子晶体硬度较大;在SiC中,每个C原子周围最近的C原子个数=3×8÷2;晶胞中C原
子个数是4、Si原子个数=8× +6× =4,晶胞体积=(a×10-10 cm)3,晶体密度= 。
【详解】
(1)Fe原子失去最外层2个电子生成Fe2+,其M电子层变为最外层,M电子层上3s、3p、3d
能级上分别含有2、8、6个电子,其最外层电子排布式为3s23p63d6;Cu原子核外有29个
电子,根据构造原理书写基态Cu原子电子排布式为[Ar]3d104s1或1s22s22p63s23p63d104s1;
(2)F元素的化合价为−1价,该离子的化合价为−2价,据此计算Ti元素化合价=−2−
(−1)×6=+4;配体是F−;
(3)甲基上的C原子价层电子对个数是4、其它两个碳原子价层电子对个数都是3,根据价
层电子对互斥理论判断C原子杂化类型分别为sp3、sp2;元素的非金属性越强,其电负性
越大,非金属性最强的是Cl元素,则电负性最大的是Cl;该物质燃烧生成氧化铝和二氧化
碳、水,立体构型是直线形的是CO;
2
(4)原子晶体硬度较大,SiC硬度很大,所以为原子晶体;在SiC中,每个C原子周围最近
的C原子个数=3×8÷2=12;晶胞中C原子个数是4、Si原子个数8× +6× =4,晶胞体积
=(a×10−10cm)3,晶体密度= = g/cm3= g⋅cm−3。
23.[Ar]3d6 或 1s22s22p63s23p63d6 1 8N 平面三角形 sp2 sp3 Cu2+
A
+2NH•H O=Cu(OH) ↓+2NH+; Cu(OH) +4NH=[Cu(NH )]2++2OH﹣ -90.8
3 2 2 4 2 3 3 4
【详解】
(1)Fe为26号元素,核外电子排布式为1s22s22p63s23p63d64s2,基态Fe2+的核外电子排布
式为1s22s22p63s23p63d6或[Ar]3d6,Ti元素为22号元素,核外电子排布式为
1s22s22p63s23p63d24s2,基态Ti3+的核外电子排布式为1s22s22p63s23p63d1未成对电子有1个。
答案为:[Ar]3d6 或 1s22s22p63s23p63d6 ;1 ;
(2)1个(CO)中含有1个σ键,4个(CO)中含有4个σ键,4个(CO)与Ni 结合形
成4个σ键,故一个[Ni(CO) ]2+中含有8个σ键;1mol[Ni(CO) ]2+ 中,配离子中含有σ键数
4 4
目为8N ;
A
答案为:8N
A;
(3)有机物 HCHO的中心原子是碳原子,其价电子对数为3,采用sp2杂化,共4个原子,
VSEPR构型为平面三角形;
答案为:平面三角形;(4) 中1、2、3号C原子价层电子对个数是4,4、5、6号碳原子
价层电子对个数是3,根据价层电子对互斥理论判断该分子中C原子轨道杂化类型,1、
2、3号C原子采用sp3杂化,4、5、6号C原子采用sp2杂化;
故答案为sp3、sp2;
(5)向硫酸铜中逐滴加入氨水先产生氢氧化铜沉淀,后沉淀溶解生成[Cu(NH )]2+,溶液
3 4
呈深蓝色溶液,反应离子方程式为:Cu2++2NH•H O=Cu(OH) ↓+2NH+、
3 2 2 4
Cu(OH) +4NH=[Cu(NH)]2++2OH-;
2 3 3 4
故答案为Cu2++2NH•H O=Cu(OH) ↓+2NH+;Cu(OH) +4NH=[Cu(NH)]2++2OH-;
3 2 2 4 2 3 3 4
(6)由表中数据可知,N(g)+3H(g)=2NH (g)△H=946kJ/mol+436kJ/mol×3−2×3×390.8kJ/
2 2 3
mol=−90.8kJ/mol,
故答案为−90.8。