文档内容
2022 届高三化学二轮复习物质的分离提纯专项练习
一、选择题(共16题)
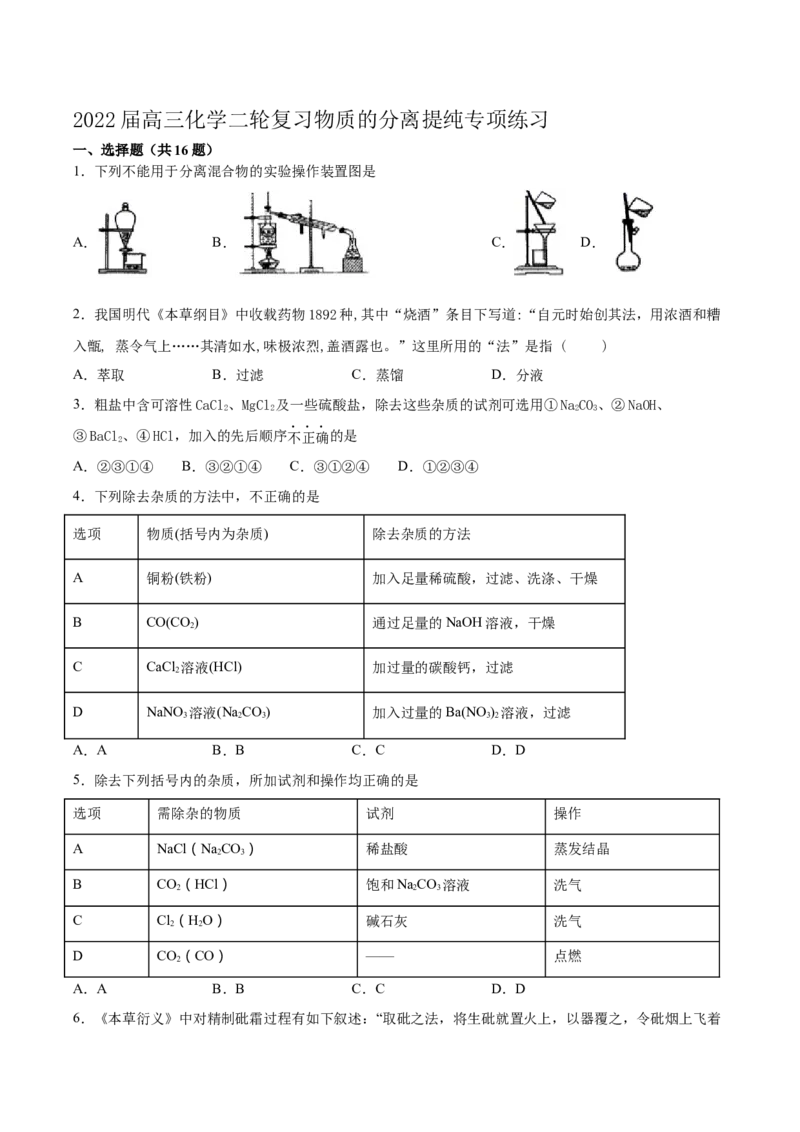
1.下列不能用于分离混合物的实验操作装置图是
A. B. C. D.
2.我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟
入甑, 蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指 ( )
A.萃取 B.过滤 C.蒸馏 D.分液
3.粗盐中含可溶性CaCl、MgCl 及一些硫酸盐,除去这些杂质的试剂可选用①NaCO、②NaOH、
2 2 2 3
③BaCl、④HCl,加入的先后顺序不正确的是
2
A.②③①④ B.③②①④ C.③①②④ D.①②③④
4.下列除去杂质的方法中,不正确的是
选项 物质(括号内为杂质) 除去杂质的方法
A 铜粉(铁粉) 加入足量稀硫酸,过滤、洗涤、干燥
B CO(CO ) 通过足量的NaOH溶液,干燥
2
C CaCl 溶液(HCl) 加过量的碳酸钙,过滤
2
D NaNO 溶液(Na CO) 加入过量的Ba(NO ) 溶液,过滤
3 2 3 3 2
A.A B.B C.C D.D
5.除去下列括号内的杂质,所加试剂和操作均正确的是
选项 需除杂的物质 试剂 操作
A NaCl(NaCO) 稀盐酸 蒸发结晶
2 3
B CO(HCl) 饱和NaCO 溶液 洗气
2 2 3
C Cl(HO) 碱石灰 洗气
2 2
D CO(CO) —— 点燃
2
A.A B.B C.C D.D
6.《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )
A.蒸馏 B.升华 C.干馏 D.萃取
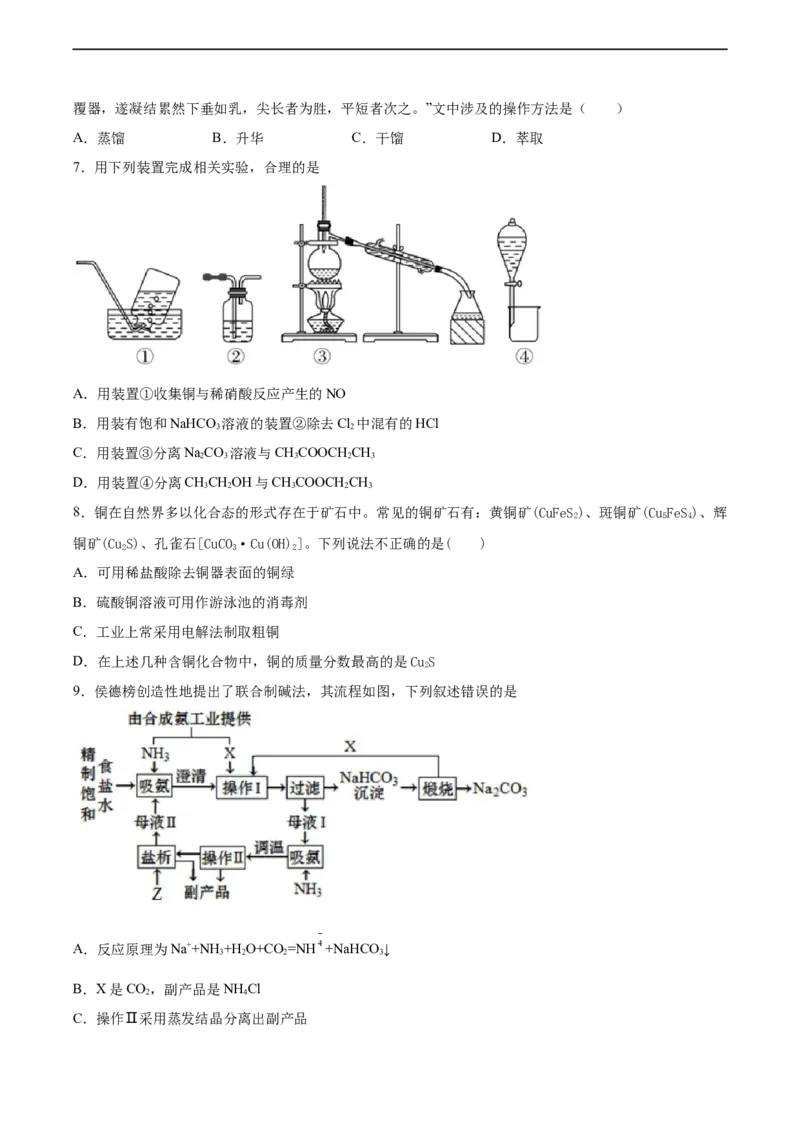
7.用下列装置完成相关实验,合理的是
A.用装置①收集铜与稀硝酸反应产生的NO
B.用装有饱和NaHCO 溶液的装置②除去Cl 中混有的HCl
3 2
C.用装置③分离NaCO 溶液与CHCOOCH CH
2 3 3 2 3
D.用装置④分离CHCHOH与CHCOOCH CH
3 2 3 2 3
8.铜在自然界多以化合态的形式存在于矿石中。常见的铜矿石有:黄铜矿(CuFeS)、斑铜矿(CuFeS)、辉
2 5 4
铜矿(CuS)、孔雀石[CuCO·Cu(OH)]。下列说法不正确的是( )
2 3 2
A.可用稀盐酸除去铜器表面的铜绿
B.硫酸铜溶液可用作游泳池的消毒剂
C.工业上常采用电解法制取粗铜
D.在上述几种含铜化合物中,铜的质量分数最高的是CuS
2
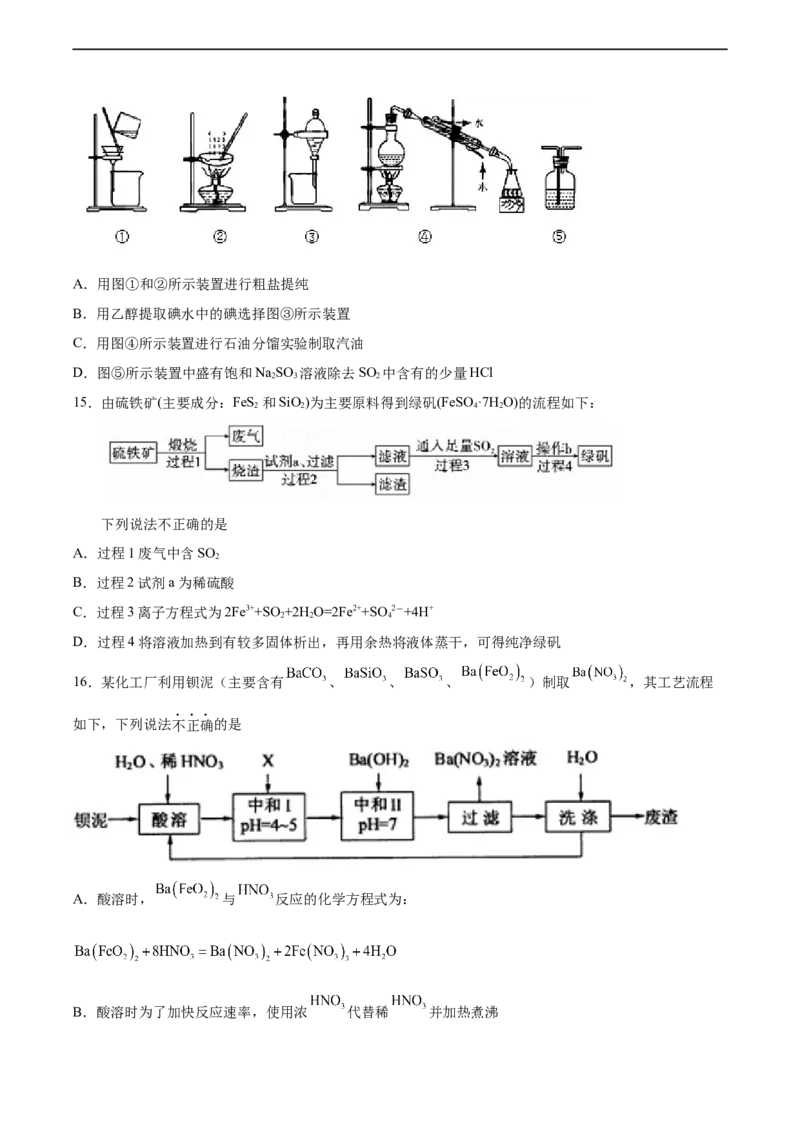
9.侯德榜创造性地提出了联合制碱法,其流程如图,下列叙述错误的是
A.反应原理为Na++NH+H O+CO=NH +NaHCO↓
3 2 2 3
B.X是CO,副产品是NH Cl
2 4
C.操作Ⅱ采用蒸发结晶分离出副产品D.“盐析”中加入的Z是NaCl
10.下列除去杂质的方法错误的是( )
物质 杂质 试剂 主要操作
FeCl 溶
A 2 CuCl Fe(足量) 过滤
液 2
饱和食盐水+浓硫
B Cl HCl 洗气
2 酸
C Fe FeO 稀盐酸(足量) 过滤
2 3
NaCO 固
D 2 3 NaHCO 无 加热
体 3
A.A B.B C.C D.D
11.除去下列括号内的杂质,所加试剂和操作均正确的是
选项 需除杂的物质 试剂 操作
A Fe O(Al O) NaOH溶液 过滤
2 3 2 3
B CO(HCl) NaOH溶液 将气体通过洗气瓶
2
C NaCl(NaCO) 稀硫酸 蒸发结晶
2 3
D Mg(Al) 氨水 过滤
A.A B.B C.C D.D
12.下列操作中正确的是( )
A.过滤时,玻璃棒与单层滤纸的一边接触
B.过滤时,漏斗下端紧贴烧杯内壁
C.加热试管内物质时,试管底部与酒精灯灯芯接触
D.向试管中滴加液体时,胶头滴管紧贴试管内壁
13.下列说法正确的是 ( )。
A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B.纤维分为天然纤维和化学纤维,化学纤维包括人造纤维和合成纤维
C.石油干馏可得到汽油、煤油等
D.油脂是高分子化合物,可发生水解反应
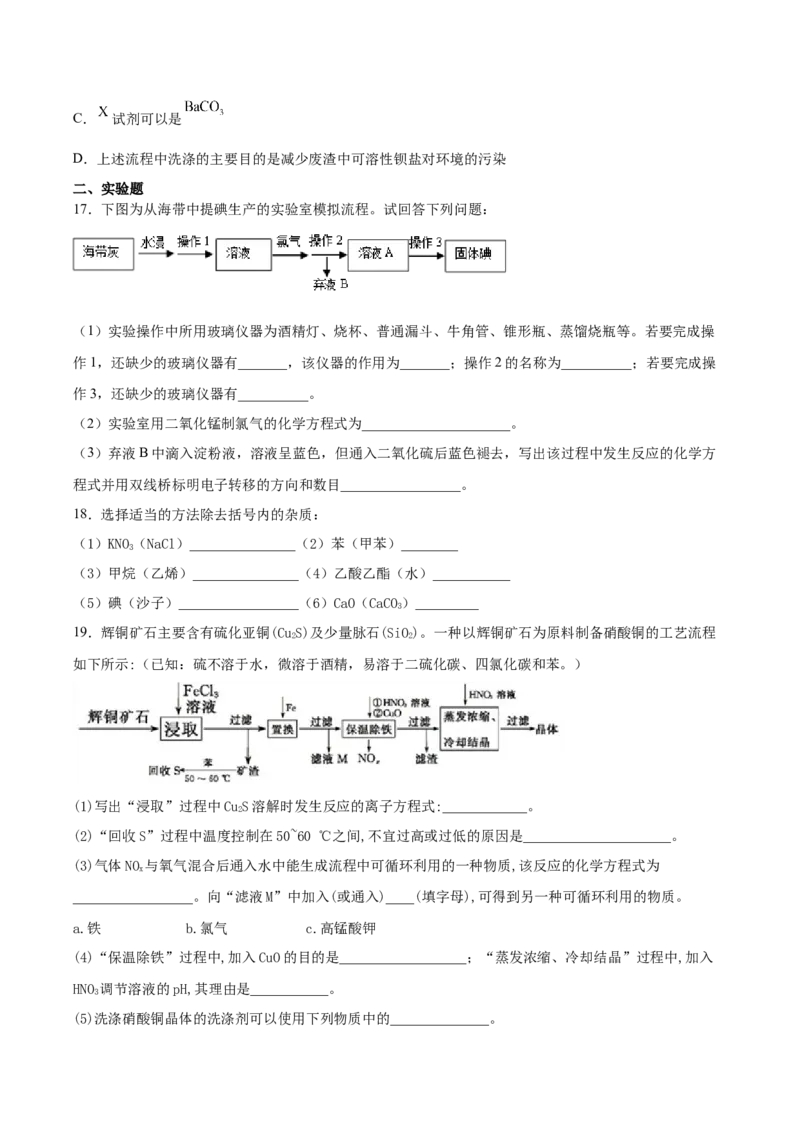
14.下列实验中,所选装置或实验设计合理的是( )A.用图①和②所示装置进行粗盐提纯
B.用乙醇提取碘水中的碘选择图③所示装置
C.用图④所示装置进行石油分馏实验制取汽油
D.图⑤所示装置中盛有饱和NaSO 溶液除去SO 中含有的少量HCl
2 3 2
15.由硫铁矿(主要成分:FeS 和SiO)为主要原料得到绿矾(FeSO ·7H O)的流程如下:
2 2 4 2
下列说法不正确的是
A.过程1废气中含SO
2
B.过程2试剂a 为稀硫酸
C.过程3离子方程式为2Fe3++SO+2H O=2Fe2++SO2-+4H+
2 2 4
D.过程4将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
16.某化工厂利用钡泥(主要含有 、 、 、 )制取 ,其工艺流程
如下,下列说法不正确的是
A.酸溶时, 与 反应的化学方程式为:
B.酸溶时为了加快反应速率,使用浓 代替稀 并加热煮沸C. 试剂可以是
D.上述流程中洗涤的主要目的是减少废渣中可溶性钡盐对环境的污染
二、实验题
17.下图为从海带中提碘生产的实验室模拟流程。试回答下列问题:
(1)实验操作中所用玻璃仪器为酒精灯、烧杯、普通漏斗、牛角管、锥形瓶、蒸馏烧瓶等。若要完成操
作1,还缺少的玻璃仪器有_______,该仪器的作用为_______;操作2的名称为__________;若要完成操
作3,还缺少的玻璃仪器有__________。
(2)实验室用二氧化锰制氯气的化学方程式为_____________________。
(3)弃液B中滴入淀粉液,溶液呈蓝色,但通入二氧化硫后蓝色褪去,写出该过程中发生反应的化学方
程式并用双线桥标明电子转移的方向和数目_________________。
18.选择适当的方法除去括号内的杂质:
(1)KNO(NaCl)_______________(2)苯(甲苯)________
3
(3)甲烷(乙烯)_______________(4)乙酸乙酯(水)___________
(5)碘(沙子)_________________(6)CaO(CaCO)_________
3
19.辉铜矿石主要含有硫化亚铜(CuS)及少量脉石(SiO)。一种以辉铜矿石为原料制备硝酸铜的工艺流程
2 2
如下所示:(已知:硫不溶于水,微溶于酒精,易溶于二硫化碳、四氯化碳和苯。)
(1)写出“浸取”过程中CuS溶解时发生反应的离子方程式:____________。
2
(2)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_____________________。
(3)气体NO 与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为
x
_________________。向“滤液M”中加入(或通入)____(填字母),可得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
(4)“保温除铁”过程中,加入CuO的目的是__________________;“蒸发浓缩、冷却结晶”过程中,加入
HNO 调节溶液的pH,其理由是___________。
3
(5)洗涤硝酸铜晶体的洗涤剂可以使用下列物质中的______________。a.酒精 b.热水 c.饱和硝酸铜溶液
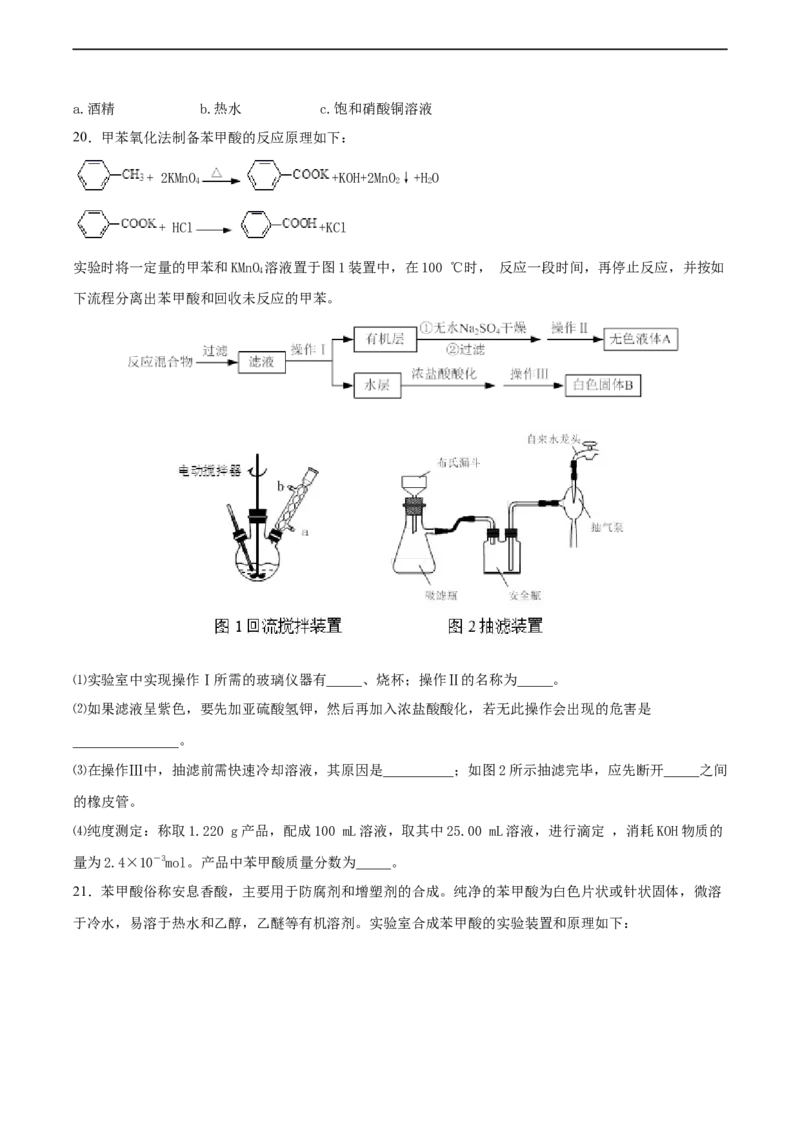
20.甲苯氧化法制备苯甲酸的反应原理如下:
+ 2KMnO +KOH+2MnO↓+HO
4 2 2
+ HCl +KCl
实验时将一定量的甲苯和KMnO 溶液置于图1装置中,在100 ℃时, 反应一段时间,再停止反应,并按如
4
下流程分离出苯甲酸和回收未反应的甲苯。
⑴实验室中实现操作Ⅰ所需的玻璃仪器有_____、烧杯;操作Ⅱ的名称为_____。
⑵如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是
_______________。
⑶在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是__________;如图2所示抽滤完毕,应先断开_____之间
的橡皮管。
⑷纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的
量为2.4×10-3mol。产品中苯甲酸质量分数为_____。
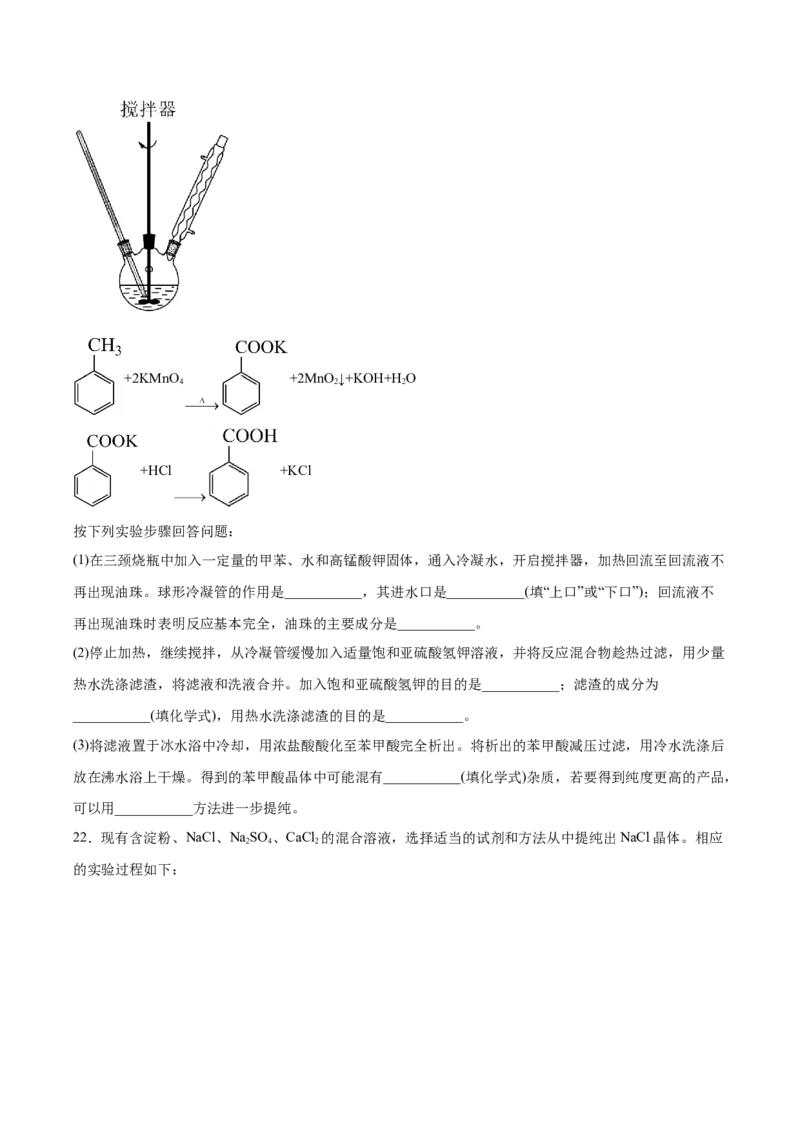
21.苯甲酸俗称安息香酸,主要用于防腐剂和增塑剂的合成。纯净的苯甲酸为白色片状或针状固体,微溶
于冷水,易溶于热水和乙醇,乙醚等有机溶剂。实验室合成苯甲酸的实验装置和原理如下:+2KMnO +2MnO↓+KOH+H O
4 2 2
+HCl +KCl
按下列实验步骤回答问题:
(1)在三颈烧瓶中加入一定量的甲苯、水和高锰酸钾固体,通入冷凝水,开启搅拌器,加热回流至回流液不
再出现油珠。球形冷凝管的作用是___________,其进水口是___________(填“上口”或“下口”);回流液不
再出现油珠时表明反应基本完全,油珠的主要成分是___________。
(2)停止加热,继续搅拌,从冷凝管缓慢加入适量饱和亚硫酸氢钾溶液,并将反应混合物趁热过滤,用少量
热水洗涤滤渣,将滤液和洗液合并。加入饱和亚硫酸氢钾的目的是___________;滤渣的成分为
___________(填化学式),用热水洗涤滤渣的目的是___________。
(3)将滤液置于冰水浴中冷却,用浓盐酸酸化至苯甲酸完全析出。将析出的苯甲酸减压过滤,用冷水洗涤后
放在沸水浴上干燥。得到的苯甲酸晶体中可能混有___________(填化学式)杂质,若要得到纯度更高的产品,
可以用___________方法进一步提纯。
22.现有含淀粉、NaCl、NaSO 、CaCl 的混合溶液,选择适当的试剂和方法从中提纯出NaCl晶体。相应
2 4 2
的实验过程如下:(1)操作①是利用胶体不能通过_____________而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:
试剂①___________________;试剂③_____________________。
(3)判断试剂①已过量的操作是:__________________。
(4)控制试剂③适量的方法是:__________________。
(5)试剂②的作用(用化学方程式表示):__________________。参考答案
1.D
【详解】
A选项,为分液操作,用于分离互不相溶的液体,故A不选;
B选项,为蒸馏操作,用于分离沸点不同的互溶的液体混合物,故B不选;
C选项,为过滤操作,用于分离固体与液体的混合物,故C不选;
D选项,为配制一定物质的量浓度的溶液的操作,不用于分离混合物,故D选。
故选D。
2.C
【分析】
由信息可知,蒸令气上,则利用互溶混合物的沸点差异分离,以此来解答。
【详解】
萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,分液适用于互不相溶的液
体之间的一种分离方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除
去易挥发、难挥发或不挥发杂质,过滤适用于不溶性固体和液体之间的一种分离方法。由
信息可知,蒸令气上,则利用互溶混合物的沸点差异分离,则该法为蒸馏,答案选C。
3.D
【解析】
【详解】
Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO 2-用氯化钡除去,过滤后向滤液中加入盐
4
酸酸化。但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必须放在氯化钡的后面,而氢
氧化钠可以随意调整,所以先后顺序可以是②③①④或③②①④或③①②④。答案选D。
4.D
【分析】
根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,
同时被提纯物质不得改变,除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,
不能与原物质反应;②反应后不能引入新的杂质,由此分析。
【详解】
A.铁粉能与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,再过滤、洗
涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故A不符合题意;
B.CO 能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再干燥,能
2
除去杂质且没有引入新的杂质,符合除杂原则,故B不符合题意;
C.HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能
除去杂质且没有引入新的杂质,符合除杂原则,故C不符合题意;
D.过量的Ba(NO ) 能与NaCO 溶液反应生成碳酸钡沉淀和硝酸钠,能除去杂质但引入了
3 2 2 3
新的杂质硝酸钡(过量的),不符合除杂原则,故D符合题意;
答案选D。5.A
【详解】
物质分离提纯时,选择试剂和实验操作方法应遵循三个原则:1.不能引入新的杂质(水除外),
即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提
纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物
理后化学,先简单后复杂的原则。
A.NaCO 可与盐酸反应生成NaCl,然后蒸发、结晶可到达纯净的NaCl,故A正确;
2 3
B.CO 和HCl都与饱和NaCO 溶液反应,应用饱和碳酸氢钠溶液除杂,故B错误;
2 2 3
C.氯气与碱石灰反应,应用浓硫酸除杂,故C错误;
D.二氧化碳中含有少量的CO,不易燃烧,应通过灼热的CuO,故D错误;
故选A。
6.B
【详解】
“将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳”,属于固态物质
受热直接转化为气态物质,类似于碘的升华,因此文中涉及的操作方法是升华。
答案选B。
7.A
【详解】
A.铜与稀硝酸反应产生的NO不溶于水,可用排水法收集,A项正确;
B.NaHCO 与HCl反应产生CO,会引入新杂质,B项错误;
3 2
C.NaCO 溶液与CHCOOCH CH 不互溶,应用分液法分离,C项错误;
2 3 3 2 3
D.CHCHOH与CHCOOCH CH 互溶,不可用分液法分离,D项错误;
3 2 3 2 3
故选A。
8.C
【详解】
A.稀盐酸和碱式碳酸铜发生复分解反应生成CuCl、HO和CO,Cu和稀盐酸不反应,所以
2 2 2
可以用稀盐酸除铜器表面的铜绿,选项A正确;B、CuSO 是重金属盐,能使蛋白质变性,
4
可用作游泳池的消毒剂,选项B正确;C、工业上常用热还原法制得粗铜,而用电解法精炼
铜,选项C不正确;D、黄铜矿(CuFeS)、斑铜矿(CuFeS)、辉铜矿(CuS)、孔雀石
2 5 4 2
[CuCO·Cu(OH)]中铜的质量分数分别为34.8%、63.5%、80%、57.7%,其中最高的是
3 2
CuS,选项D正确。答案选C。
2
9.C
【分析】
侯德榜联合制碱法的基本原理为:饱和氯化钠溶液先吸收氨气形成碱性溶液,再吸收过量
的二氧化碳,此时碳酸氢钠的溶解度再体系中最小,使其析出,分离,再经煅烧得到碳酸
钠,剩余母液再吸收过量氨气,得到副产品氯化铵,氯化钠循环使用,据此分析答题。
【详解】A.由上述分析可知联合制碱法的原理为:Na++NH+H O+CO=NH +NaHCO↓,故A正确;
3 2 2 3
B.根据反应原理可知先吸收氨气,再吸收二氧化碳,煅烧碳酸氢钠可得二氧化碳,均可
确定X是CO,向饱和氯化铵溶液中加入氯化钠发生盐析,得到副产品NH Cl,故B正确;
2 4
C.副产品为NH Cl,若采用蒸发结晶,会使NH Cl分解,故C错误;
4 4
D.“盐析”中加入的Z是NaCl,可使副产品NH Cl充分盐析,剩余氯化钠溶液循环使用,
4
故D正确;
答案为C。
10.C
【详解】
A. 与Fe反应,生成 和Cu,过滤可以除去Cu和多余的Fe,A正确;
B. 难溶于饱和食盐水,HCl极易溶于水,然后用浓硫酸干燥除去水蒸气,可以通过洗
气法除去氯气中的HCl,B正确;
C.Fe和 都能溶于盐酸,不能用盐酸除去Fe中的 ,C错误;
D. 受热分解生成碳酸钠和水和二氧化碳,除去碳酸钠中的碳酸氢钠可以用加热的
方法,D正确;
答案选C。
11.A
【详解】
A. Fe O 与NaOH不反应,Al O 与氢氧化钠反应生成偏铝酸钠和水,经过滤可得到纯净的
2 3 2 3
Fe O,故A正确;
2 3
B. CO 和HCl均能够与氢氧化钠反应,故B错误;
2
C. Na CO 与稀硫酸反应生成硫酸钠,引入了新杂质硫酸根离子,故C错误;
2 3
D.一水合氨是弱碱,与金属铝不反应,所以达不到除杂的目的,故D错误,
故选A。
12.B
【详解】
A.过滤时应防止滤纸捣破,则玻璃棒与三层滤纸的一边接触,故A错误;B.过滤时应防
止液滴飞溅,沿烧杯内壁流下,则漏斗下方紧贴烧杯内壁,故B正确;C.用酒精灯外焰
加热试管,试管底部不能与酒精灯灯芯接触,故C错误;D.向试管中滴加液体时,胶头
滴管应悬空正放,不能紧贴试管内壁,否则会时试剂污染或减少试剂的量,故D错误;故
答案为B。
13.B
【解析】
【详解】
A.乙烯分子中含有碳碳双键能使溴的四氯化碳溶液褪色,而和聚乙烯分子中无不饱和的碳
碳双键,因此不能使溴的四氯化碳溶液褪色,A错误;B.纤维分天然纤维和化学纤维,天然纤维是自然界原有的或经人工培植的植物上、人工饲
养的动物上直接取得的纺织纤维;化学纤维又可分为合成纤维和人造纤维,合成纤维是由
人工合成方法制得的,生产不受自然条件的限制,人造纤维是用木材、草类的纤维经化学
加工制成的粘胶纤维;B正确;
C.石油蒸馏可得到汽油、煤油等,C错误;
D.油脂是不属于高分子化合物,但油脂属于酯,可发生水解反应,D错误;
故合理选项是B。
14.A
【分析】
A. 粗盐提纯,需要溶解后,过滤、蒸发;
B.乙醇与水互溶;
C.石油的各组分沸点不同且互溶;
D.二者均与碳酸钠反应。
【详解】
A. 粗盐提纯,需要溶解后,过滤、蒸发,则图①和②所示装置可提纯,A正确;
B.乙醇与水互溶,不能作萃取剂,B错误;
C.石油是多种互溶的液态混合物,由于它们的沸点不同,所以可采用④装置,用蒸馏的方
法分离出汽油,C错误;
D.二者均与碳酸钠溶液反应,应选图⑤装置中盛有饱和亚硫酸氢钠溶液、洗气分离,D错
误
15.D
【分析】
由制备绿矾流程可知,硫铁矿(主要成分:FeS 和SiO)高温煅烧后的烧渣(主要成分:Fe O
2 2 2 3
和SiO)溶于硫酸,溶液中含Fe3+,过程2过滤除去二氧化硅,滤液中通入二氧化硫,将铁
2
离子还原生成亚铁离子,过程4为蒸发浓缩、冷却结晶析出绿矾。
【详解】
A.根据上述分析,过程1,废气中含SO ,故A正确;
2
B.因绿矾的酸根离子为硫酸根离子,则过程2最好用硫酸来溶解烧渣,故B正确;
C. 过程3中二氧化硫将铁离子还原生成硫酸亚铁,离子方程式为2Fe3++SO+2H O=2Fe2+
2 2
+SO2-+4H+,故C正确;
4
D. 过程4,将溶液加热到有较多固体析出,再用余热将液体蒸干,蒸干时绿矾受热失去结
晶水,得不到纯净绿矾,故D错误;
答案故选D。
16.B
【分析】
钡泥主要含BaCO 、BaSiO 、BaSO、Ba(FeO) 等,加入硝酸,在容器中充分溶解,可生
3 3 3 2 2
成硫酸钡、硅酸,溶液中含有铁离子、钡离子、硝酸根离子等,且溶液呈酸性,可加入碳酸钡,调节溶液pH=4~5,使铁离子水解生成Fe(OH) 沉淀,加入氢氧化钡中和至中性,
3
得到硝酸钡溶液,过滤得到的固体洗涤后除去废渣,滤液重新加入酸溶步骤充分利用。
【详解】
A.酸溶时, 与 反应,没有发生化合价变化,为非氧化还原反应,生成硝
酸钡、硝酸铁和水,故A正确;
B.不能用浓 代替稀硝酸,因为浓硝酸挥发,加热还会分解,故B错误;
C.加入X调节溶液的pH,X要能消耗氢离子,结合生产要求,不能引入新的杂质, 试
剂可以是 ,故C正确;
D.废渣中的可溶性钡盐可能造成重金属污染,需要洗涤减少废渣中可溶性钡盐对环境的
污染,故D正确;
答案选A。
17.玻璃棒 引流 萃取(分液) 温度计、冷凝管 MnO +4HCl(浓)
2
MnCl +Cl↑+2H O
2 2 2
【详解】
(1)由流程可知,将海带烧成灰,向灰中加水搅拌,操作1为分离固体和液体,即为过滤
操作,过滤操作用到的玻璃仪器有:烧杯、玻璃棒、漏斗,完成操作1,还缺少的玻璃仪
器有玻璃棒,其作用为引流;溶液A中含碘离子,加氯水发生氧化还原反应生成碘,操作
2为萃取,溶液B为含碘的有机溶液,则操作3为蒸馏得到碘单质,蒸馏操作用到的仪器
有,酒精灯、蒸馏烧瓶、冷凝管、牛角管、锥形瓶、温度计, 完成操作3,还缺少的玻璃
仪器有温度计、冷凝管。
(2)实验室用二氧化锰和浓盐酸反应制氯气,反应的化学方程式为MnO +4HCl(浓)
2
MnCl +Cl↑+2H O。
2 2 2
(3)在弃液中滴入淀粉溶液,溶液呈蓝色,说明在弃液中含有碘,该溶液中通入二氧化硫,
发现蓝色褪去,发生的反应为 。
18.重结晶 蒸馏 洗气 分液 升华 加热
【详解】
(1)硝酸钾和氯化钠的溶解度受温度影响变化程度本题,通过重结晶除去KNO 中
3
NaCl;(2)苯和甲苯互溶,但沸点不同,通过蒸馏分离;(3)乙烯能和溴水发生加成反
应,则通过洗去除去甲烷中的乙烯;(4)乙酸乙酯不溶于水,通过分液分离;(5)碘易
升华,通过升华法除去碘中的沙子;(6)碳酸钙高温分解生成氧化钙和CO,通过加热除
2去CaO中的CaCO 。
3
19. CuS+4Fe3+ 2Cu2++4Fe2++S 温度过低,矿渣的溶解速率小;温度过高,苯易挥发
2
4NO+(5-2x)O+2HO 4HNO b 加大Fe3+转化为Fe(OH) 的程度 抑制Cu2+的水解 ac
x 2 2 3 3
【解析】辉铜矿加入氯化铁溶液溶解浸取过滤,得到矿渣加入苯水浴加热回收硫单质;加
入在滤液中加入铁还原铁离子和铜离子过滤,滤液M中加入氯气氧化反应生成氯化铁循环
使用,保温除铁加入稀硝酸溶液和氧化铜反应,调节溶液PH除去杂质离子,过滤得到滤
液为硫酸亚铁溶液,在稀硝酸溶液中蒸发浓缩,冷却结晶过滤洗涤得到晶体。
(1)铁离子做氧化剂,Cu S被氧化,离子方程式为:Cu S+4Fe3+=2Cu2++4Fe2++S,故答案为:
2 2
Cu S+4Fe3+=2Cu2++4Fe2++S;
2
(2)苯沸点比较低,温度过高苯容易挥发,从反应动力学看温度过低溶解速率小,故答案为:
温度过低,矿渣的溶解速率小;温度过高,苯易挥发;
(3)NO 做还原剂,依据质量守恒和电子守恒写出方程式:4NOx+(5-2x)O +2H O=4HNO ,
x 2 2 3
向滤液M中通入Cl 将FeCl 氧化为FeCl ,可以循环使用,故选b,故答案为:4NO +(5-
2 2 3 x
2x)O +2H O=4HNO ,b;
2 2 3
(4)Fe3++3H O Fe(OH) +3H+,加入CuO使水解平衡正向进行,调节溶液的pH使铁元素完
2 3
全转化为氢氧化铁沉淀,加热过程中Cu2+会水解,加入硝酸抑制Cu2+的水解,不引入新的
⇌
杂质,故答案为:调节溶液pH使使铁元素完全转化为氢氧化铁沉淀,抑制铜离子水解;
(5) a. 硝酸铜在酒精中的溶解度较小,可以用酒精洗涤,正确;b. 硝酸铜在热水中的溶解
度增大,不能用热水洗涤,错误;c.饱和硝酸铜溶液中硝酸铜的溶解度很小,可以用饱和
硝酸铜溶液洗涤,正确;故选ac。
20.分液漏斗 蒸馏 过量的高锰酸钾氧化盐酸,产生氯气 得到较大的苯甲酸晶
粒,便于抽滤 抽气泵和安全瓶 96%
【解析】
试题分析:⑴操作I为分液操作,其所需的玻璃仪器有分液漏斗、烧杯;操作II为蒸馏操
作得无色液体A。
⑵为了避免过量的高锰酸钾氧化盐酸,产生有毒的氯气,应该先加亚硫酸氢钾除去过量的
高锰酸钾,然后再加入浓盐酸酸化。
⑶为了得到较大的苯甲酸晶粒,便于抽滤,应该在抽滤前需快速冷却溶液;为了避免管道
里的水在负压下回流,故在抽滤完毕,应先断开抽气泵和安全瓶。
⑷根据“1 ~1KOH”,则产品中苯甲酸质量分数为
。
考点:本题考查化学综合实验(分液、蒸馏、实验环保、安全、操作、计算等)。21.冷凝回流 下口 甲苯或 除去过量的高锰酸钾,防止其氧化后续加入
的HCl MnO 增大苯甲酸钾的溶解度,防止其降温结晶析出造成损失 KCl
2
重结晶
【详解】
(1)该制备原理的反应物为甲苯,加热过程中甲苯会挥发降低其利用率,因此利用冷凝管可
以使挥发出的甲苯冷凝回流到烧瓶中继续发生反应,可以提高甲苯的利用率,冷凝管的进
水是下进上出,可使冷凝管中充满水提高冷凝效果,在反应物和生成物中甲苯是油状液体
难溶于水,呈油状,故答案为:冷凝回流;下口;甲苯或 ;
(2)为使甲苯充分反应,过程中加入的高锰酸钾需过量,但过量的高锰酸钾会氧化酸化时用
到的浓盐酸,因此在加浓盐酸前先加亚硫酸氢钾溶液,利用其还原性将过量的高锰酸钾除
去,反应过程中生成的二氧化锰难溶于水通过过滤除去,过滤时为了防止生成的苯甲酸钾
降温结晶析出导致其损失,因此采用趁热过滤的方式,故答案为:除去过量的高锰酸钾,
防止其氧化后续加入的HCl;MnO;增大苯甲酸钾的溶解度,防止其降温结晶析出造成损
失;
(3)在酸化过程中除生成苯甲酸外还生成KCl,在结晶过程得到的苯甲酸中可能含有KCl,
在提纯粗品苯甲酸时可利用苯甲酸与KCl溶解度受温度影响的差异,采用重结晶法分离得
到纯净的苯甲酸,故答案为:KCl;重结晶;
22.)半透膜 BaCl HCl 静置,向上层清液中滴加少量氯化钡溶液,没有白色
2
沉淀产生,说明氯化钡溶液已过量 滴加稀盐酸至溶液呈中性(或滴加稀盐酸至溶液pH
值等7或滴加稀盐酸至溶液不再产生气泡) BaCl +Na CO=2NaCl+BaCO ↓;
2 2 3 3
CaCl +Na CO=2NaCl+CaCO ↓
2 2 3 3
【分析】
胶体不能透过半透膜,操作①为渗析,使淀粉和 NaSO 、CaCl 分开,要除去NaSO 、
2 4 2 2 4
CaCl ,可向混合液中分别加入BaCl 、NaCO,除去粗盐中含有的Ca2+、SO -可溶性杂质
2 2 2 3
的方法:加入过量BaCl ,去除硫酸根离子;再加入过量NaCO(去除钙离子),则试剂
2 2 3
①为BaCl ,操作②为过滤,沉淀A为硫酸钡,试剂②为NaCO,操作③为过滤,沉淀B
2 2 3
为碳酸钙和碳酸钡,试剂③为盐酸,加入盐酸可除去过量的NaCO,最后蒸发结晶可得到
2 3
NaCl晶体。
【详解】
(1)操作①是利用胶体不能通过半透膜而把淀粉胶体和溶液进行分离;
(2)由以上分析可知试剂①为BaCl ,试剂③为HCl;
2
(3)判断试剂①已过量的方法是静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量;
(4)盐酸的作用是除去碳酸钠,所以控制试剂③适量的方法是滴加稀盐酸至溶液呈中性(或
滴加稀盐酸至溶液pH值等7或滴加稀盐酸至溶液不再产生气泡);
(5)试剂②为NaCO,加入试剂②的作用是除去溶液中钙离子和过量的钡离子,反应的化
2 3
学方程式为BaCl +Na CO =2NaCl+BaCO ↓;CaCl +Na CO =2NaCl+CaCO ↓
2 2 3 3 2 2 3 3
【点晴】
解答时本题注意Ca2+、SO 的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握
实验的先后顺序。分离和提纯一般应遵循“四原则”和“三必须”:(1)“四原则”:一、不增(提
纯过程中不增加新的杂质);二、不减(不减少被提纯的物质);三、易分离(被提纯物质与杂
质容易分离);四、易复原(被提纯物质转化后要易复原)。(2)“三必须”:一、除杂试剂必须
过量;二、过量试剂必须除尽(因为过量试剂带入新的杂质);三、选最佳除杂途径;四、
除去多种杂质时必须考虑加入试剂的顺序。