文档内容
第3讲 氧化还原反应
[考纲要求]
1.了解氧化还原反应的本质是电子的转移。
2.了解常见的氧化还原反应。
3.掌握常见氧化还原反应的配平和相关计算。
4.能利用得失电子守恒原理进行相关计算。
考点一 氧化还原反应基本概念
1知识梳理
1.氧化还原反应
(1)本质和特征
(2)相关概念及其关系
(3)氧化还原反应中电子转移的表示方法
①双线桥法请标出Cu与稀硝酸反应中电子转移的方向和数目:
________________________________________________________________________。
②单线桥法
请标出Cu与稀硝酸反应中电子转移的方向和数目:
________________________________________________________________________。
[思考]
反应Cu+2HSO (浓)=====CuSO +SO↑+2HO中,氧化剂是 ,还原剂是
2 4 4 2 2
,氧化产物是 。生成1 mol SO 时转移电子数目为2N,被还原的HSO 的物质的量是
2 A 2 4
,浓硫酸表现的性质是 和 。
2.常见的氧化剂和还原剂
(1)常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非
金属单质及其氢化物等。如:
(3)元素化合价处于中间价态的物质既有氧化性,又有还原性其中:Fe2+、SO2−
主要表现 性,HO 主要表现 性。
3 2 2
[判断] (正确的打“√”,错误的打“×”)
(1)有单质参加或有单质生成的化学反应一定是氧化还原反应( )
(2)某元素从游离态变为化合态,该元素一定被氧化( )
(3)非金属阴离子只具有还原性,金属阳离子只具有氧化性( )
(4)HO作为还原剂时,产物中一般有O 生成( )
2 2
(5)氧化还原反应中的反应物,不是氧化剂就是还原剂( )
(6)强氧化剂与强还原剂混合不一定能发生氧化还原反应( )
(7)阳离子只有氧化性,阴离子只有还原性( )
(8)元素的非金属性越强,其氧化性越强,相应单质越活泼( )
(9)难失电子的物质一定易得电子( )
[提醒]
氧化还原反应与四种基本类型的关系
2对点速练
练点一 氧化还原反应基础判断
1.下列应用不涉及氧化还原反应的是( )
A.酸雨的形成 B.根瘤菌固氮
C.氨碱法制纯碱 D.电池放电
2.下列物质在生活中应用时,起还原作用的是( )
A.明矾作净水剂B.甘油作护肤保湿剂
C.漂粉精作消毒剂
D.铁粉作食品袋内的脱氧剂
3.氢化钙(CaH )可作为生氢剂,反应的化学方程式为 CaH +2HO===Ca(OH) +
2 2 2 2
2H↑,下列说法不正确的是( )
2
A.CaH 既是还原剂,又是氧化剂
2
B.H 既是氧化产物,又是还原产物
2
C.CaH 是还原剂,HO是氧化剂
2 2
D.氧化产物与还原产物的质量比为1∶1
4.赤铜矿的主要成分是CuO,辉铜矿的主要成分是CuS,将赤铜矿与辉铜矿混合加热
2 2
有以下反应:CuS+2CuO=====6Cu+SO↑,下列关于该反应的说法中,正确的是( )
2 2 2
A.该反应的氧化剂只有CuO
2
B.CuS在反应中既是氧化剂,又是还原剂
2
C.Cu既是氧化产物又是还原产物
D.每生成19.2 g Cu,反应中转移0.6 mol电子
练点二 电子转移方向和数目的分析
5.判断下列化学方程式中电子转移方向、数目表示的正误。6.HO 在Fe (SO ) 催化下发生分解反应,写出HO 分解反应方程式并用双线桥标出
2 2 2 4 3 2 2
电子转移的方向和数目:
。
练后归纳
1.正确分析氧化还原反应中电子转移的数目,其前提是确定物质中各元素(特别是变
价元素)的化合价。基本方法是先标出熟悉元素的化合价,再根据化合物中正负化合价的代
数和为零的原则求解其他元素的化合价。
2.根据化合价判断反应体系中的氧化剂、还原剂及氧化产物、还原产物。如对于反应
6HCl(浓)+NaClO===NaCl+3Cl↑+3HO中,氧化剂为NaClO,还原剂为HCl,氧化产物
3 2 2 3
和还原产物都为Cl。
2
3.近几年高考中一些特殊物质中元素化合价判断:
CuFeS、KFeO、LiNH、LiNH、AlN、NaSO、CO、HCN、CuH。
2 2 4 2 2 2 2 3 2
考点二 氧化还原反应规律
1知识梳理
1.守恒规律
化合价有升必有降,电子有得必有失。对于一个完整的氧化还原反应,化合价升降总
数相等,电子得失总数相等。
2.强弱规律
自发进行的氧化还原反应,一般遵循强氧化剂制弱氧化剂,强还原剂制弱还原剂,即
“强制弱”。
氧化剂+还原剂―→还原产物+氧化产物
氧化性:氧化剂 氧化产物;
还原性:还原剂 还原产物。3.先后规律
在浓度相差不大的溶液中:
(1)同时含有几种还原剂时――→将按照还原性由强到弱的顺序依次反应。如在
FeBr 溶液中通入少量Cl 时,因为还原性:Fe2+>Br-,所以Fe2+先与Cl 反应。
2 2 2
(2)同时含有几种氧化剂时――→将按照氧化性由强到弱的顺序依次反应。
如在含有Fe3+、Cu2+、H+的溶液中加入铁粉,因为氧化性Fe3+>Cu2+>H+,所以铁粉先
与Fe3+反应,然后再与Cu2+反应,最后与H+反应。
4.价态规律
(1)元素处于最高价,只有 ,如Fe3+、Ag+等;元素处于最低价,只有
,如S2-、I-等;元素处于中间价态,既有氧化性又有还原性,如Fe2+、Cl 等。
2
(2)归中反应规律
不同价态的同种元素间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低
价―→中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。
如在反应KClO +6HCl(浓)===KCl+3Cl↑+3HO中,氧化产物是 ,还原产
3 2 2
物是 ,1 mol KClO 反应时转移电子数是 。
3
(3)歧化反应规律
“中间价―→高价+低价”。具有多种价态的元素(如氯、硫、氮和磷元素等)均可
发生歧化反应,如:Cl +2NaOH===NaCl+NaClO+HO。1 mol Cl 反应时转移电子数为
2 2 2
。
[思考]
高铁酸钠(NaFeO )是一种新型、高效、多功能水处理剂,是比Cl 、O 、ClO 、KMnO
2 4 2 3 2 4
氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为
2Fe(OH)+3ClO-+4OH-===2Fe +3Cl-+5HO
3 O2− 2
4
干法制备的主要反应为
2FeSO+6NaO===2NaFeO+2NaO+2NaSO+O↑
4 2 2 2 4 2 2 4 2
(1)高铁酸钠中铁显 价。
(2)湿法中Fe 是 产物。
O2−
4
(3)干法中每生成1 mol NaFeO 转移 mol电子。
2 4
(4)NaFeO 可氧化水中的HS、NH,生成的 还能吸附悬浮杂质。
2 4 2 3[判断] (正确的打“√”,错误的打“×”)
(1)反应2Mn +5HO+6H+===2Mn2++5O↑+8HO,说明氧化性Mn >HO( )
O− 2 2 2 2 O− 2 2
4 4
(2)反应2Fe3++Fe===3Fe2+,说明金属阳离子还原产物不一定是金属单质( )
(3)反应2Fe3++Cu===2Fe2++Cu2+,说明还原性Cu>Fe2+( )
(4)反应Cu+HSO=====CuSO+H↑,说明还原性:Cu>H( )
2 4 4 2 2
(5)反应2Mn +10Cl-+16H+===2Mn2++5Cl↑+8HO,说明盐酸不能作高锰酸钾的
O− 2 2
4
酸化剂( )
(6)浓硫酸能干燥SO,说明强氧化剂与强还原剂不一定发生氧化还原反应( )
2
[提醒]
影响物质氧化性、还原性的因素
(1)浓度:同一种物质浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO>稀
2 4
HSO,浓HNO>稀HNO,还原性:浓HCl>稀HCl。
2 4 3 3
(2)温度:同一种物质,温度越高其氧化性越强。如:热的浓硫酸的氧化性比冷的浓
硫酸的氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化性(还原性)越强。
如:鉴别CH 和CH 用酸性KMnO ,N 在大量H+存在时,能将Fe2+、I-、S 等离子
4 2 4 4 O− O2−
3 3
氧化。
2对点速练
练点一 氧化还原反应规律性判断
1.已知有如下三个氧化还原反应:
2FeCl+2KI===2FeCl+2KCl+I
3 2 2
2FeCl+Cl===2FeCl
2 2 3
2KMnO+16HCl===2KCl+2MnCl+5Cl↑+8HO
4 2 2 2
若某溶液中 Fe2+和 I-共存,要除去 I-而不氧化 Fe2+和 Cl-,可以加入的试剂是
( )
A.Cl B.KMnO
2 4
C.FeCl D.HCl
3
2.铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①Tl3++2Ag===Tl++2Ag+,②Ag++Fe2+===Ag+Fe3+,③Fe+2Fe3+===3Fe2+,下列
离子氧化性比较顺序正确的是( )
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe3+
3.已知CoO 在酸性溶液中易被还原成Co2+,CoO、Cl、FeCl、I 的氧化性依次减弱。
2 3 2 3 2 3 2
下列反应在水溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl+4FeI
2 2 3 3
B.Cl+FeI===FeCl+I
2 2 2 2
C.CoO+6HCl===2CoCl+Cl↑+3HO
2 3 2 2 2
D.2Fe3++2I-===2Fe2++I
2
练后归纳
假设法判断氧化还原反应能否进行
已知物质的氧化性或者还原性的强弱关系,判断某一氧化还原反应能否发生时可
采用假设法。
先假设反应成立
然后根据氧化剂的氧化性>氧化产物的氧化性,还原剂的还原性>还原产物的还原
性的规律,列出假设反应中的上述关系
结合题干条件判断该结论是否符合事实,符合事实,则反应成立;反之,则不成
立
练点二 氧化还原反应规律性计算
4.氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应 AlO +C+
2 3
N=====2AlON+CO合成,下列有关说法正确的是( )
2
A.氮氧化铝中氮的化合价是-3价B.反应中每生成5.7 g AlON的同时生成1.12 L CO
C.反应中氮气作氧化剂
D.反应中氧化产物和还原产物的物质的量之比是2∶1
5.过氧化氢在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO+HO+2H+===Mn2++O↑+2HO;
2 2 2 2 2
②Mn2++HO===MnO+2H+。
2 2 2
下列说法正确的是( )
A.HO 在①中是氧化剂,在②中是还原剂
2 2
B.Mn2+在①中是还原产物,在②中是氧化产物
C.在①中每生成1 mol O,转移的电子数为2.408×1024
2
D.在MnO 催化作用下1 mol HO 分解生成0.5 mol O
2 2 2 2
6.已知:还原性HS >I-,氧化性I >I ,在含3 mol NaHSO 的溶液中逐滴加入
O− O− 2 3
3 3
KIO 溶液,加入 KIO 和析出 I 的物质的量的关系曲线如图所示。下列说法不正确的是
3 3 2
( )
A.0~a间发生反应:3HS +I ===3S +I-+3H+
O− O− O2−
3 3 4
B.a~b间共消耗NaHSO 的物质的量为1.8 mol
3
C.b~c间发生的反应中I 仅是氧化产物
2
D.当溶液中I-与I 的物质的量之比为5∶2时,加入的KIO 为1.08 mol
2 3
练后归纳
守恒法解题的“3步流程”练点三 氧化还原反应方程式的配平
7.正向配平类型训练
(1) HCl(浓)+ MnO===== Cl↑+ MnCl+ HO
2 2 2 2
(2) Cu+ HNO(稀)=== Cu(NO)+ NO↑+ HO
3 3 2 2
(3) KI+ KIO+ HSO=== I+ KSO+ HO
3 2 4 2 2 4 2
(4) Mn + H++ Cl-=== Mn2++ Cl↑+ HO
O− 2 2
4
8.逆向配平类型训练
(1) S+ KOH=== KS+ KSO+ HO
2 2 3 2
(2) P+ KOH+ HO=== KPO+ PH↑
4 2 3 4 3
9.缺项配平类型训练
(1) ClO-+ Fe(OH)+ === Cl-+ Fe + HO
3 O2− 2
4
(2) Mn + HO+ === Mn2++ O↑+ HO
O− 2 2 2 2
4
(3) P+ HClO+ === HCl↑+ HPO
4 3 3 4
方法总结
氧化还原方程式配平的一般步骤
练点四 信息型氧化还原反应方程式的配平
10.按要求书写方程式:(1)HPO 的工业制法是:将白磷(P )与 Ba(OH) 溶液反应生成 PH 气体和Ba
3 2 4 2 3
(HPO ) ,后者再与 HSO 反应。写出白磷与 Ba(OH) 溶液反应的化学方程式:
2 2 2 2 4 2
________________________________________________________________________。
( 2 ) ① PbO 与 浓 盐 酸 共 热 生 成 黄 绿 色 气 体 , 反 应 的 化 学 方 程 式 为
2
________________________________________________________________________。
②PbO 可 由 PbO 与 次 氯 酸 钠 溶 液 反 应 制 得 , 反 应 的 离 子 方 程 式 为
2
________________________________________________________________________。
(3)已知在酸性介质中FeSO 能将+6价铬还原成+3价铬。写出Cr 与FeSO 溶液
4 2O2− 4
7
在 酸 性 条 件 下 反 应 的 离 子 方 程 式 :
________________________________________________________________________。
(4)用NaClO—NaOH溶液氧化AgNO ,制得高纯度的纳米级AgO 。写出该反应的离子
3 2 2
方程式:________________________________________________________________________
________________________________________________________________________。
(5)生产硫化钠大多采用无水芒硝(NaSO )—碳粉还原法,若煅烧所得气体为等物
2 4
质 的 量 的 CO 和 CO , 写 出 煅 烧 时 发 生 反 应 的 化 学 方 程 式 :
2
________________________________________________________________________
________________________________________________________________________。
(6)KMnO 的氧化性随pH的减小而增大,在酸性介质中还原产物是Mn2+;在中性或碱
4
性介质中还原产物主要是MnO 。三氯乙烯(CHCl )是地下水有机污染物的主要成分,研究
2 2 3
显示在地下水中加入KMnO 溶液可将其中的三氯乙烯除去,氧化产物只有CO ,写出反应的化
4 2
学方程式________________________________________________________________________。
11.以粉煤灰(主要成分为AlO 和SiO,还含有少量的FeO、FeO 等)为原料制备AlO
2 3 2 2 3 2 3
的流程如下:
(1)“ 酸 浸 ” 时 需 加 入 过 量 的 稀 硫 酸 , 写 出 AlO 溶 解 的 离 子 方 程 式
2 3______________________________。
(2)证明酸浸后溶液中存在Fe3+的方法是:取酸浸后的溶液少许置于试管中,向其中滴
加硫氰化钾溶液,溶液变为红色;再慢慢滴入过量的HO 溶液,溶液的红色先变深,之后红
2 2
色逐渐褪去,继续滴加会有气泡逸出,该气体会使带火星的木条复燃。
① 红 色 变 深 的 原 因 是 ( 用 离 子 方 程 式 表 示 ) :
________________________________________________________________________
________________________________________________________________________;
②溶液红色褪去是由于过氧化氢氧化了硫氰根离子,已知双氧水氧化SCN-生成N、CO
2 2
和 SO , 写 出 该 反 应 的 离 子 方 程 式 :
________________________________________________________________________
________________________________________________________________________;
③有气体逸出,说明Fe3+对HO 的分解有催化作用,写出催化过程第一步反应的离子
2 2
方程式________________________________________________________________________
________________________________________________________________________。
练后归纳
信息型氧化还原反应方程式的配平书写步骤
本讲真题研练
1.[2019·北京卷,10]下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是(
)物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl) Fe粉
2 3
B NaCl溶液(MgCl) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO) HO、无水CaCl
2 2 2
2.[2019·浙江4月选考,6]反应8NH +3Cl===N +6NHCl,被氧化的NH 与被还原的
3 2 2 4 3
Cl 的物质的量之比为( )
2
A.2∶3 B.8∶3
C.6∶3 D.3∶2
3.[2018·北京卷,9]下列实验中的颜色变化,与氧化还原反应无关的是( )
A B C D
NaOH溶液滴入 石蕊溶液滴入氯水 NaS溶液滴入AgCl 热铜丝插入稀硝酸
实验 2
FeSO 溶液中 中 浊液中 中
4
产生白色沉淀,随 溶液变红,随后迅 沉淀由白色逐渐变 产生无色气体,随
现象
后变为红褐色 速褪色 为黑色 后变为红棕色
4.[2017·北京卷,8]下列变化中,气体被还原的是( )
A.二氧化碳使NaO 固体变白
2 2
B.氯气使KBr溶液变黄
C.乙烯使Br 的四氯化碳溶液褪色
2
D.氨气使AlCl 溶液产生白色沉淀
3
5.[2017·天津卷,3]下列能量转化过程与氧化还原反应无关的是( )
A.硅太阳能电池工作时,光能转化成电能
B.锂离子电池放电时,化学能转化成电能
C.电解质溶液导电时,电能转化成化学能
D.葡萄糖为人类生命活动提供能量时,化学能转化成热能
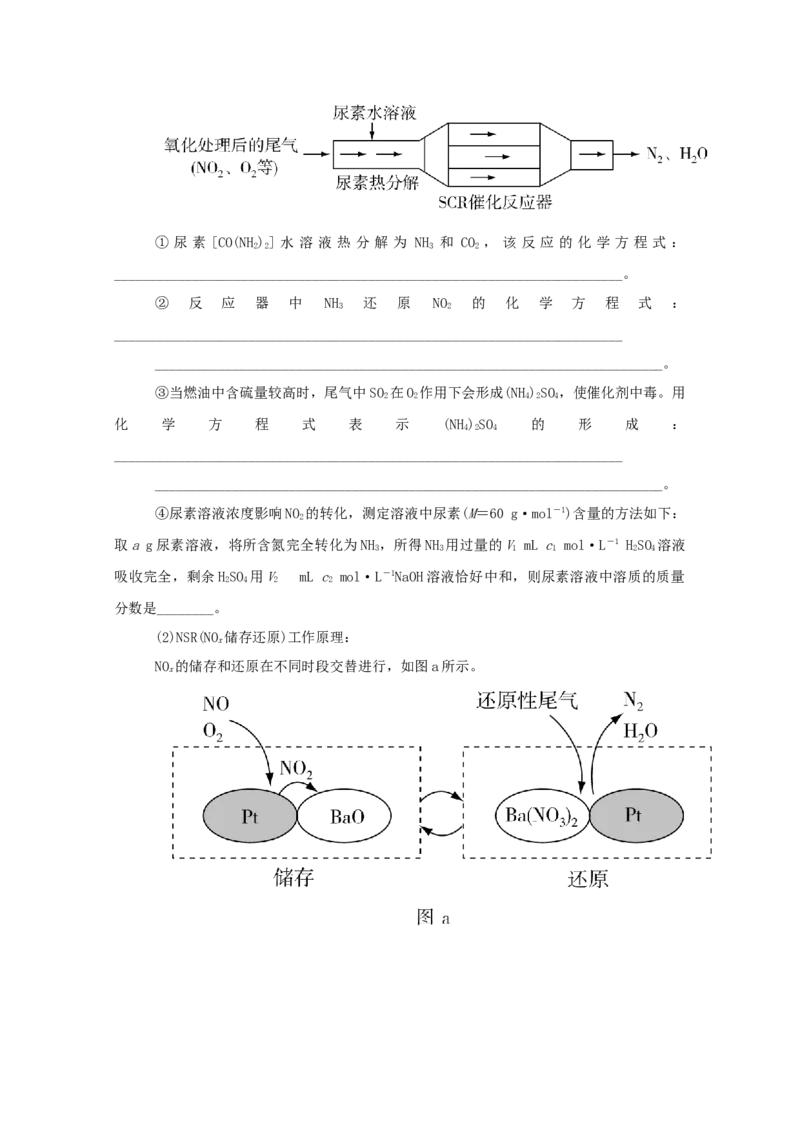
6.[2017·北京卷,27]SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NO
x
排放。
(1)SCR(选择性催化还原)工作原理:① 尿 素 [CO(NH)] 水 溶 液 热 分 解 为 NH 和 CO , 该 反 应 的 化 学 方 程 式 :
2 2 3 2
________________________________________________________________________。
② 反 应 器 中 NH 还 原 NO 的 化 学 方 程 式 :
3 2
________________________________________________________________________
________________________________________________________________________。
③当燃油中含硫量较高时,尾气中SO 在O 作用下会形成(NH)SO,使催化剂中毒。用
2 2 4 2 4
化 学 方 程 式 表 示 (NH)SO 的 形 成 :
4 2 4
________________________________________________________________________
________________________________________________________________________。
④尿素溶液浓度影响NO 的转化,测定溶液中尿素(M=60 g·mol-1)含量的方法如下:
2
取a g尿素溶液,将所含氮完全转化为NH ,所得NH 用过量的V mL c mol·L-1 H SO 溶液
3 3 1 1 2 4
吸收完全,剩余HSO 用V mL c mol·L-1NaOH溶液恰好中和,则尿素溶液中溶质的质量
2 4 2 2
分数是________。
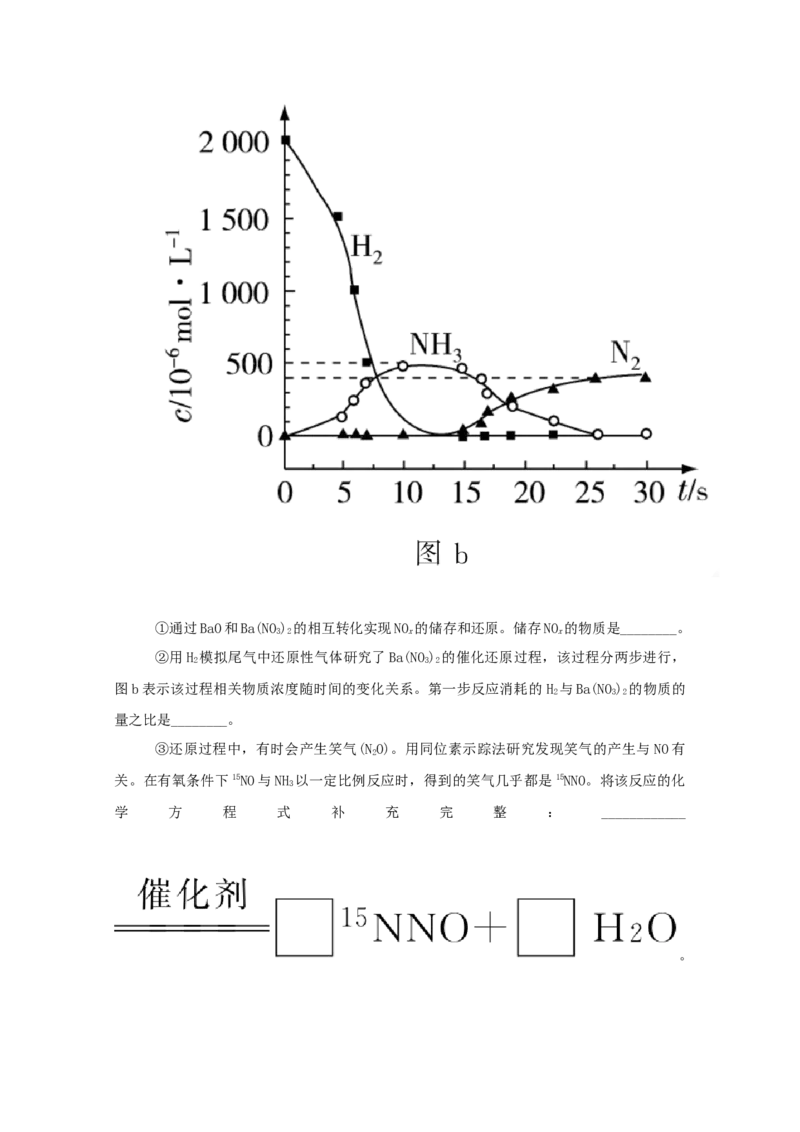
(2)NSR(NO 储存还原)工作原理:
x
NO 的储存和还原在不同时段交替进行,如图a所示。
x①通过BaO和Ba(NO) 的相互转化实现NO 的储存和还原。储存NO 的物质是________。
3 2 x x
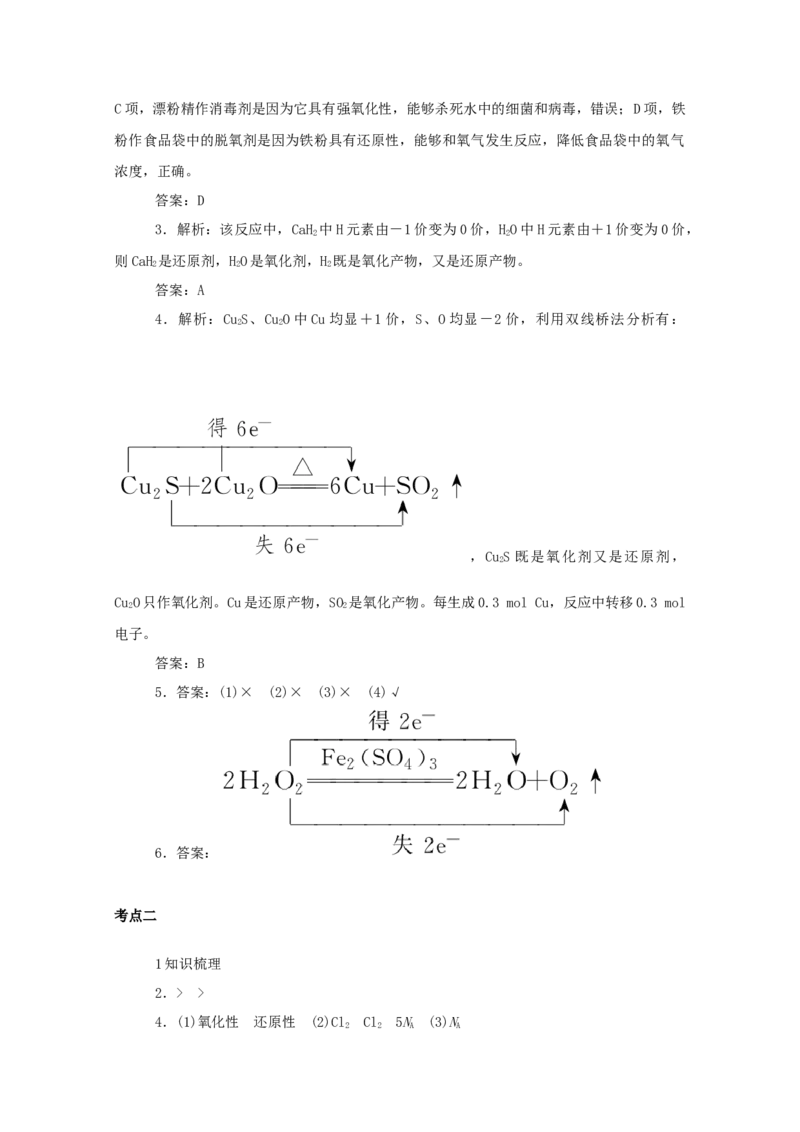
②用H 模拟尾气中还原性气体研究了Ba(NO) 的催化还原过程,该过程分两步进行,
2 3 2
图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 H 与Ba(NO) 的物质的
2 3 2
量之比是________。
③还原过程中,有时会产生笑气(NO)。用同位素示踪法研究发现笑气的产生与 NO有
2
关。在有氧条件下15NO与NH 以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化
3
学 方 程 式 补 充 完 整 : ____________
。第3讲 氧化还原反应
考点一
1知识梳理
1.(1)电子转移(得失或偏移) 元素的化合价发生变化 (2)失去 还原 氧化 氧化
氧化 还原 还原 得到
(3)
思考 答案:浓HSO Cu CuSO 1 mol 酸性 强氧化性
2 4 4
2.(1)Cl- SO NO 或 NO Mn2+ Fe2+或 Fe (2)Zn2+ H+ CO Fe3+ S I
2 2 2 2
(3)Fe S HO Fe3+ S O 还原 氧化
2 O2− 2
4
判断 答案:(1)× (2)× (3)× (4)√ (5)× (6)√ (7)× (8)× (9)×
2对点速练
1.解析:有电子转移的反应是氧化还原反应,酸雨的形成是燃烧含硫、氮化合物引起
的,是氧化还原反应;根瘤菌固氮是将氮气转化为化合态的氮;电池放电是氧化还原反应;
氨碱法制纯碱的反应是NaCl+NH +CO +HO===NaHCO↓+NHCl,2NaHCO=====NaCO +CO↑
3 2 2 3 4 3 2 3 2
+HO,选C。
2
答案:C
2.解析:A项,明矾作净水剂是因为它溶于水生成的Al(OH) 胶体具有较大的表面积,
3
能够吸附水中的悬浮物而沉降,错误;B项,甘油作护肤保湿剂是因为它具有吸湿性,错误;C项,漂粉精作消毒剂是因为它具有强氧化性,能够杀死水中的细菌和病毒,错误;D项,铁
粉作食品袋中的脱氧剂是因为铁粉具有还原性,能够和氧气发生反应,降低食品袋中的氧气
浓度,正确。
答案:D
3.解析:该反应中,CaH 中H元素由-1价变为0价,HO中H元素由+1价变为0价,
2 2
则CaH 是还原剂,HO是氧化剂,H 既是氧化产物,又是还原产物。
2 2 2
答案:A
4.解析:CuS、CuO中Cu均显+1价,S、O均显-2价,利用双线桥法分析有:
2 2
,CuS 既是氧化剂又是还原剂,
2
CuO只作氧化剂。Cu是还原产物,SO 是氧化产物。每生成0.3 mol Cu,反应中转移0.3 mol
2 2
电子。
答案:B
5.答案:(1)× (2)× (3)× (4)√
6.答案:
考点二
1知识梳理
2.> >
4.(1)氧化性 还原性 (2)Cl Cl 5N (3)N
2 2 A A思考 答案:(1)+6 (2)氧化 (3)5 (4)Fe(OH) 胶体
3
判断 答案:(1)√ (2)√ (3)√ (4)× (5)√ (6)√
2对点速练
1.解析:由题目中的三个反应可知氧化性强弱顺序为:Mn >Cl>Fe3+>I ,因Cl 、
O− 2 2 2
4
KMnO 均能氧化Fe2+,故选项A、B不合题意,HCl不能氧化I-,D项错误。
4
答案:C
2.解析:在氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性。
答案:D
3.解析:氧化还原反应发生的条件是强氧化剂+强还原剂=弱还原剂+弱氧化剂。由
于Fe3+氧化性强于I ,所以FeI 不存在,A中反应不可能发生;B、C、D中反应符合氧化还
2 3
原反应规律,所以可以发生。例如n(Cl)∶n(FeI)=1∶1时即发生B项的反应。
2 2
答案:A
4.解析:A项,AlON中铝显+3价,氧显-2价,则氮显-1价,错误;B项,没有指
明温度和压强,不能计算出生成物CO的体积,错误;C项,反应后氮元素的化合价降低,N
2
作氧化剂,正确;D项,AlON为还原产物,CO为氧化产物,两者物质的量之比为1∶2,错误。
答案:C
5.解析:HO 在①中是还原剂,在②中是氧化剂,A项错误。Mn2+在①中是还原产物,
2 2
在②中是还原剂,B项错误。①中氧元素由-1价变为0价,生成1 mol O 时转移2 mol电子,
2
即1.204×1024个电子,C项错误。由①、②可得总反应为 2HO=====2HO+O↑,故1 mol
2 2 2 2
HO 分解生成0.5 mol O,D项正确。
2 2 2
答案:D
6.解析:还原性HS >I-,所以首先发生的反应为:I +3HS ===I-+3S +3H
O− O− O− O2−
3 3 3 4
+,继续加入KIO ,氧化性I >I ,所以I 可以结合H+氧化I-生成I ,反应为I +6H+
3 O− 2 O− 2 O−
3 3 3
+5I-===3HO+3I,根据发生的反应来判断各个点的产物。
2 2
答案:C
7.答案:(1)4 1 1 1 2
(2)3 8 3 2 4
(3)5 1 3 3 3 3
(4)2 16 10 2 5 88.答案:(1)3 6 2 1 3
(2)2 9 3 3 5
9.答案:(1)3 2 4OH- 3 2 5
(2)2 5 6H+ 2 5 8
(3)3 10 18HO 10 12
2
10.答案:(1)6HO+2P+3Ba(OH)===2PH↑+3Ba(HPO)
2 4 2 3 2 2 2
(2)①PbO+4HCl(浓)=====PbCl+Cl↑+2HO
2 2 2 2
②PbO+ClO-===PbO+Cl-
2
(3)CrO+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(4)2Ag++ClO-+2OH-===AgO↓+Cl-+HO
2 2 2
(5)3NaSO+8C=====3NaS+4CO↑+4CO↑
2 4 2 2
(6)2KMnO+CHCl===2KCl+2CO↑+2MnO+HCl
4 2 3 2 2
11.解析:(2)①溶液呈红色,是因为发生了Fe3++3SCN- Fe(SCN) ,红色变深,说
⇌ 3
明c(Fe3+)增大,发生了Fe2+→Fe3+,故反应的离子方程式为2Fe2++HO +2H+===2Fe3++
2 2
2HO。
2
② 得 2e-, 失
11e-,由电子守恒、电荷守恒即可配平。
③催化作用中Fe3+一定要参与反应,故Fe3+在第一步反应中应作氧化剂,发生2Fe3+
+HO===2Fe2++O↑+2H+;第二步重新生成Fe3+,发生2Fe2++2H++HO===2Fe3++2HO。
2 2 2 2 2 2
答案:(1)AlO+6H+===2Al3++3HO
2 3 2
(2)①2Fe2++HO+2H+===2Fe3++2HO、Fe3++3SCN- Fe(SCN)
2 2 2 ⇌ 3
②2SCN-+11HO===2CO↑+N↑+2H++10HO+2S
2 2 2 2 2 O2−
4
③2Fe3++HO===2Fe2++O↑+2H+
2 2 2
本讲真题研练
1.解析:A项,用Fe粉除去FeCl 溶液中的Fe3+时,发生了氧化还原反应;C项,除
2
去Cl 中的HCl杂质一般用饱和食盐水,用水除会损失部分Cl ,同时Cl 与HO的反应是氧化
2 2 2 2
还原反应;D项,NO 和HO的反应属于氧化还原反应。
2 2答案:B
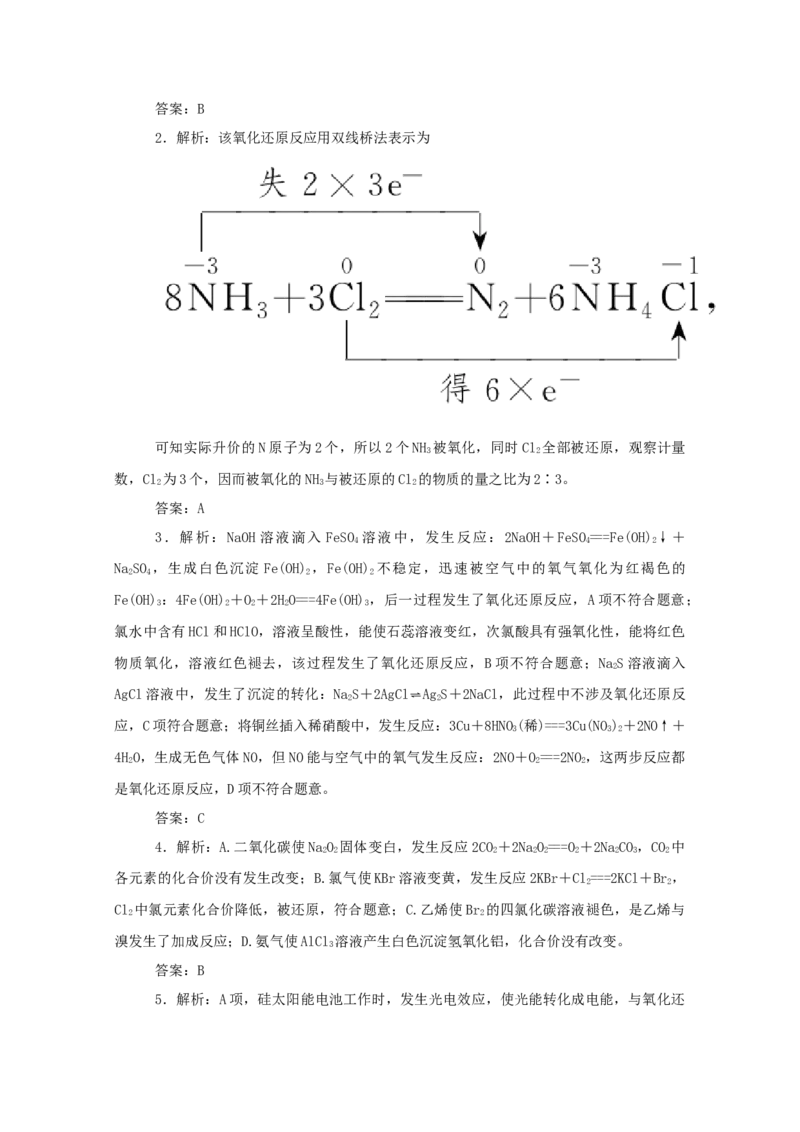
2.解析:该氧化还原反应用双线桥法表示为
可知实际升价的N原子为2个,所以2个NH 被氧化,同时Cl 全部被还原,观察计量
3 2
数,Cl 为3个,因而被氧化的NH 与被还原的Cl 的物质的量之比为2∶3。
2 3 2
答案:A
3.解析:NaOH 溶液滴入 FeSO 溶液中,发生反应:2NaOH+FeSO===Fe(OH)↓+
4 4 2
NaSO ,生成白色沉淀 Fe(OH) ,Fe(OH) 不稳定,迅速被空气中的氧气氧化为红褐色的
2 4 2 2
Fe(OH) :4Fe(OH) +O +2HO===4Fe(OH) ,后一过程发生了氧化还原反应,A项不符合题意;
3 2 2 2 3
氯水中含有HCl和HClO,溶液呈酸性,能使石蕊溶液变红,次氯酸具有强氧化性,能将红色
物质氧化,溶液红色褪去,该过程发生了氧化还原反应,B项不符合题意;NaS溶液滴入
2
AgCl溶液中,发生了沉淀的转化:NaS+2AgCl AgS+2NaCl,此过程中不涉及氧化还原反
2 ⇌ 2
应,C项符合题意;将铜丝插入稀硝酸中,发生反应:3Cu+8HNO(稀)===3Cu(NO)+2NO↑+
3 3 2
4HO,生成无色气体NO,但NO能与空气中的氧气发生反应:2NO+O===2NO ,这两步反应都
2 2 2
是氧化还原反应,D项不符合题意。
答案:C
4.解析:A.二氧化碳使NaO 固体变白,发生反应2CO +2NaO===O +2NaCO ,CO 中
2 2 2 2 2 2 2 3 2
各元素的化合价没有发生改变;B.氯气使KBr溶液变黄,发生反应2KBr+Cl===2KCl+Br ,
2 2
Cl 中氯元素化合价降低,被还原,符合题意;C.乙烯使Br 的四氯化碳溶液褪色,是乙烯与
2 2
溴发生了加成反应;D.氨气使AlCl 溶液产生白色沉淀氢氧化铝,化合价没有改变。
3
答案:B
5.解析:A项,硅太阳能电池工作时,发生光电效应,使光能转化成电能,与氧化还原反应无关;B项,锂离子电池放电时,正极和负极分别发生还原反应和氧化反应,使化学
能转化成电能;C项,电解质溶液导电时,阴极和阳极分别发生还原反应和氧化反应,使电
能转化成化学能;D项,葡萄糖在酶的作用下发生氧化还原反应等一系列反应的同时为人类
生命活动提供能量,使化学能转化成热能。
答案:A
6.解析:(1)①尿素[CO(NH)]水溶液热分解为NH 和CO ,结合原子守恒写出化学方
2 2 3 2
程式:
CO(NH)+HO――→2NH↑+CO↑。
2 2 2 3 2
②由SCR工作原理图可知,反应器中NH 还原NO 生成N 和HO,结合得失电子守恒及
3 2 2 2
原子守恒写出化学方程式:8NH+6NO=====7N+12HO。
3 2 2 2
③燃油中含硫量较高时,尾气中SO 在O 作用下会形成(NH)SO,结合得失电子守恒及
2 2 4 2 4
原子守恒写出化学方程式:2SO+O+2HO+4NH===2(NH)SO。
2 2 2 3 4 2 4
④分析尿素含量测定操作,结合N原子守恒可得关系式:CO(NH) ~2NH ~ HSO ~
2 2 3 2 4
(NH)SO ,则有 n[CO(NH)]=n(HSO)=c mol·L-1×V×10-3 L-1/2×c mol·L-
4 2 4 2 2 2 4 1 1 2
1×V×10-3 L=(cV-1/2cV)×10-3 mol,m[CO(NH)]=(cV-1/2cV)×10-3mol×60
2 1 1 2 2 2 2 1 1 2 2
g·mol-1=0.06(cV-1/2cV) g,故尿素溶液中溶质的质量分数为[0.06(cV-1/2cV)
1 1 2 2 1 1 2 2
3(2c V -c V ),100a
g]/a g×100%= 1 1 2 2 。
100a
(2)①由图a可知,NO 储存过程中,NO和O 在Pt催化下生成NO ,并被BaO吸收生成
x 2 2
Ba(NO) 而被储存,Ba(NO) 再被还原为N,故储存NO 的物质是BaO。
3 2 3 2 2 x
②第一步反应为H 与Ba(NO) 反应生成NH ,1 mol Ba(NO ) 被还原生成2 mol NH ,
2 3 2 3 3 2 3
转移电子的物质的量为2×[5― (―3)] mol=16 mol。根据氧化还原反应中得失电子守恒可
知,参加反应的H 的物质的量为16 mol×1/2=8 mol,故消耗H 和Ba(NO) 的物质的量之比
2 2 3 2
为8 mol∶1 mol=8∶1。
③已知反应物中有15NO、NH 和O ,产物中有15NNO和HO,结合得失电子守恒和原子守
3 2 2
恒可得此反应的化学方程式:3O+415NO+4NH=====415NNO+6HO。
2 3 2
答案:(1)①CO(NH)+HO――→CO↑+2NH↑
2 2 2 2 3
②8NH+6NO=====7N+12HO
3 2 2 2
③2SO+O+4NH+2HO===2(NH)SO
2 2 3 2 4 2 4
④
(2)①BaO ②8∶1③415NO+4NH+3O 4 6
3 2