文档内容
第 10 讲 氧化还原反应的基本概念
复习目标 1.了解氧化还原反应的概念。2.掌握氧化还原反应与四种基本反应类型的关系。
3.会用“单、双线桥”分析电子转移的方向和数目。4.掌握氧化性、还原性强弱的比较及应
用。
考点一 氧化还原反应与四种基本反应类型
1.氧化还原反应的本质和特征
2.氧化还原反应与四种基本反应类型间的关系图示
(1)有单质参加或单质生成的化学反应一定是氧化还原反应(×)
错因:如同素异形体之间的转化属于非氧化还原反应。
(2)无单质参加的化合反应一定不是氧化还原反应(×)
错因:如HO+SO ===HSO 属于氧化还原反应。
2 2 2 2 4
(3)Na O 和SO 的反应是氧化还原反应(√)
2 2 2
下列反应属于氧化还原反应的是__________,属于化合反应的是__________,属于分解反应
的 是 ____________ , 属 于 置 换 反 应 的 是 ____________ , 属 于 复 分 解 反 应 的 是
____________(填序号)。
①Cu S+O=====2Cu+SO
2 2 2
②3O=====2O
2 3
③Fe O+3CO=====2Fe+3CO
2 3 2
④2Na+2HO===2NaOH+H↑
2 2
⑤CaCO =====CaO+CO↑
3 2⑥2HO=====2HO+O↑
2 2 2 2
⑦SO +HO===HSO
3 2 2 4
⑧2Fe+3Cl=====2FeCl
2 3
⑨HSO +2NaOH===NaSO +2HO
2 4 2 4 2
⑩NaH+HO===NaOH+H↑
2 2
⑪IBr+HO===HIO+HBr
2
答案 ①③④⑥⑧⑩ ⑦⑧ ⑤⑥ ①④ ⑨⑪
1.(2020·北京密云区一模)下列颜色变化与氧化还原反应有关的是( )
A.氨气遇到HCl气体后产生白烟
B.品红溶液通入SO 气体后褪色
2
C.湿润的淀粉碘化钾试纸遇Cl 变蓝
2
D.在无色火焰上灼烧NaCl火焰呈黄色
答案 C
2.(2020·天津市静海区大邱庄中学模拟)下列化学反应属于区域3的是( )
A.4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
B.2NaHCO =====NaCO+HO+CO↑
3 2 3 2 2
C.4NH +5O=====4NO+6HO
3 2 2
D.Zn+HSO ===ZnSO+H↑
2 4 4 2
答案 C
解析 A项,该反应中有元素化合价的变化,因此属于氧化还原反应;反应物是三种,生成
物只有一种,反应类型属于化合反应,但不属于区域3,不符合题意;B项,该反应中没有
元素化合价的变化,因此不属于氧化还原反应;反应物是一种,生成物是多种,属于分解反
应,但不属于区域3,不符合题意;C项,该反应中有元素化合价的变化,因此属于氧化还
原反应;该反应不属于任意一种基本反应类型,但属于区域3,符合题意;D项,该反应中
有元素化合价的变化,因此属于氧化还原反应;反应物是一种单质和一种化合物,生成物是
另一种单质和另一种化合物,属于置换反应,但不属于区域3,不符合题意。
3.单晶硅是制作电子集成电路的基础材料,对硅的纯度要求很高。制得高纯度硅的化学方
程式为①SiO +2C=====Si+2CO↑;②Si+3HCl=====SiHCl +H ;③SiHCl +H=====Si
2 3 2 3 2
+3HCl,则有关反应分类说法正确的是( )A.①②③均属于氧化还原反应
B.只有①属于置换反应
C.只有①属于氧化还原反应
D.③属于复分解反应
答案 A
解析 ① SiO +2C=====Si+2CO↑,属于氧化还原反应、置换反应; ② Si+
2
3HCl=====SiHCl +H,属于氧化还原反应、置换反应;③SiHCl +H=====Si+3HCl,属于
3 2 3 2
氧化还原反应、置换反应。故①②③均属于氧化还原反应、置换反应,A正确;B、C错误;
③不属于复分解反应,D错误。
考点二 氧化还原反应的概念
1.基于双线桥理解氧化还原反应概念之间的关系
概括为“升失氧、降得还,剂性一致、其他相反”。
2.常见的氧化剂和还原剂
(1)常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见还原剂
常见还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离子、
某些非金属单质及其氢化物等。如:(3)元素化合价处于中间价态的物质既有氧化性,又有还原性
其中:Fe2+、SO主要表现还原性,HO 主要表现氧化性。
2 2
(1)金属阳离子一定只具有氧化性(×)
错因: Fe 2 + 既有氧化性,又有还原性 。
(2)氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原(×)
错因:Cl 和 NaOH 反应,氯元素既被氧化,又被还原 。
2
(3)氧化还原反应中的反应物,不是氧化剂就是还原剂(×)
错因:Cl 和 NaOH 的反应, NaOH 是反应物,既不是氧化剂,又不是还原剂 。
2
(4)某元素从游离态变为化合态,该元素可能被氧化也可能被还原(√)
(5)CaO 与水发生氧化还原反应时,CaO 只作氧化剂(×)
2 2
错因:CaO 和 H O 反应, CaO 既是氧化剂又是还原剂。
2 2 2
1.用双线桥法标出MnO +4HCl(浓)=====MnCl +Cl↑+2HO反应电子转移的方向和数目:
2 2 2 2
________________________________________________________________________。
此反应中氧化剂是__________,还原剂是____________,氧化产物是________,还原产物是
________,MnO 发生
2
________反应,HCl发生________反应;生成1 mol Cl 时转移电子数目为________,被氧化
2
的HCl的物质的量是______ mol,盐酸表现的性质是________性和______性。
答案
MnO HCl Cl MnCl 还原 氧化 2N 2
2 2 2 A
还原 酸
2.下列标明电子转移的方向和数目的化学方程式中,正确的是________(填序号)。①
②
③
④
其中①中MnO 的作用:__________。
2
②中Cl 表现的性质:______________________。
2
③中氧化产物和还原产物的质量比为________。
④中氧化剂与还原剂物质的量之比为________。
答案 ④ 催化剂 氧化性和还原性 5∶1 2∶1
题组一 氧化还原反应概念的判断
1.下列所加物质的作用与其还原性有关的是( )
A B C D
腌咸菜加氯化钠 食用盐中加碘酸钾 红酒中添加SO 生活用水消毒加入次氯酸钙
2
答案 C
解析 腌咸菜加氯化钠,不存在元素化合价的变化,不是氧化还原反应,A不合题意;食用
盐中加碘酸钾,没有发生化学变化,不表现还原性,B不合题意;红酒中添加SO ,SO 具
2 2
有还原性,可以防止红酒被氧化变质,所以与SO 的还原性有关,C符合题意;生活用水消
2
毒加入次氯酸钙是由于次氯酸钙能与空气中的 CO 和HO生成具有强氧化性的HClO,利用
2 2
其氧化性,D不合题意。
2.(2020·青岛通济实验学校月考)海水提溴过程中,将溴吹入吸收塔,使溴蒸气和吸收剂二
氧化硫发生作用以达到富集的目的,化学反应为Br +SO +2HO===2HBr+HSO ,下列说
2 2 2 2 4
法正确的是( )
A.溴发生了还原反应B.二氧化硫在反应中被还原
C.溴在反应中失去电子
D.该反应既是化合反应又是氧化还原反应
答案 A
解析 因Br元素的化合价由0降低为-1价,Br 在反应中作氧化剂,表现氧化性,发生了
2
还原反应,选项A正确;S元素的化合价由+4价升高到+6价,SO 作还原剂,被氧化,选
2
项B错误;Br元素的化合价由0降低为-1价,则Br 在反应中得到电子,选项C错误;该
2
反应的生成物为两种,不属于化合反应;反应中溴元素、硫元素化合价发生变化,属于氧化
还原反应,选项D错误。
题组二 基于双线桥分析复杂氧化还原反应
3.(2020·江西赣州模拟)制取新型水处理剂 ClO 的化学方程式为 2KClO +HC O +
2 3 2 2 4
HSO ===2ClO ↑+KSO +2CO↑+2HO。下列说法错误的是( )
2 4 2 2 4 2 2
A.KClO 在反应中得到电子
3
B.ClO 是还原产物
2
C.HC O 在反应中被氧化
2 2 4
D.1 mol KClO 参加反应有2 mol电子转移
3
答案 D
解析 反应中氯元素的化合价由+5降低为+4,则KClO 为氧化剂,在反应中得到电子,A
3
项正确;因KClO 为氧化剂,在反应中被还原,则ClO 是还原产物,B项正确;反应中碳
3 2
元素的化合价由+3升高到+4,则HC O 为还原剂,在反应中被氧化,C项正确;反应中
2 2 4
氯
元素的化合价由+5降低为+4,1 mol KClO 参加反应有1 mol×(5-4)=1 mol电子转移,D
3
项错误。
4.(2020·日照一模)Cu HgI 是一种红色固体,常用作示温涂料。制备反应为 2CuSO +
2 4 4
KHgI +SO +2HO===Cu HgI ↓+KSO +2HSO 。下列说法正确的是( )
2 4 2 2 2 4 2 4 2 4
A.上述反应的产物Cu HgI 中,Hg的化合价为+1
2 4
B.上述反应中Hg元素与Cu元素均被还原
C.上述反应中生成1 mol Cu HgI 时,转移的电子数为4N
2 4 A
D.由以上信息可推知:可发生反应2CuSO +2NaCl+SO +2HO===2CuCl↓+NaSO +
4 2 2 2 4
2HSO
2 4
答案 D
解析 根据反应方程式可知,Cu HgI 中Cu的化合价为+1价,则Hg的化合价为+2价,A
2 4
选项错误;上述反应中,只有Cu元素被还原,B选项错误;上述反应中,CuSO 中Cu的化
4
合价由+2价降至+1价,生成1 mol Cu HgI 时,转移2 mol电子,转移的电子数为2N ,C
2 4 A
选项错误;根据题干信息,CuSO 可与SO 在盐溶液中发生氧化还原反应,Cu2+被还原为Cu
4 2+,SO 被氧化为SO,则反应2CuSO +2NaCl+SO +2HO===2CuCl↓+NaSO +2HSO 可
2 4 2 2 2 4 2 4
以发生,D选项正确。
走好关键第一步——正确标出元素化合价
正确分析氧化还原反应中电子转移的数目,其前提是确定物质中各元素(特别是变价元素)的
化合价。基本方法是先标出熟悉元素的化合价,再根据化合物中正、负化合价的代数和为零
的原则求解其他元素的化合价。常见元素的化合价可以借助化合价口诀来记忆:一价氢、钾、
钠、氟、氯、溴、碘、银;二价氧、钙、钡、镁、锌;三铝、四硅、五价磷;说变价也不难,
二三铁、二四碳、二四六硫都齐全;铜汞二价最常见。
近几年高考中一些特殊物质中元素化合价判断
CuFeS Cu + 2 Fe + 2 S - 2 KFeO Fe + 6
2 2 4
LiNH N - 3 LiNH N - 3 AlN N - 3
2 2
NaSO S + 2 MO M + 5 C O C + 3
2 2 3 2
HCN C + 2 N - 3 CuH Cu + 1 H - 1
FeO Fe + (8 - n ) Si N Si + 4 N - 3
3 4
BH B + 3 H - 1
MnO(OH) Mn + 3 FePO Fe + 3
4
LiFePO Fe + 2 NH N - 2
4 2 4
HC O C + 3
2 2 4
CrO Cr + 6
SO S + 6 O - 1 、- 2
2
考点三 氧化性、还原性强弱的比较
1.氧化性、还原性的判断
(1)氧化性是指得电子的性质(或能力);还原性是指失电子的性质(或能力)。
(2)氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
如:Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na比Al活泼,更易失
去电子,所以Na比Al的还原性强。
从元素的价态考虑:
最高价态——只有氧化性,如:浓HSO 、KMnO 等;
2 4 4
最低价态——只有还原性,如:金属单质、Cl-、S2-等;
中间价态——既有氧化性又有还原性,如:Fe2+、S、Cl 等。
22.氧化性、还原性强弱的比较方法
(1)根据化学方程式判断
氧化剂(氧化性)+还原剂(还原性)===还原产物+氧化产物
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
(2)根据反应条件和产物价态高低进行判断
①与同一物质反应,一般越易进行,则其氧化性或还原性就越强。如Na与冷水剧烈反应,
Mg与热水反应,Al与水加热反应也不明显,所以还原性:Na>Mg>Al;非金属单质F 、
2
Cl、Br 、I 与H 反应,F 与H 暗处剧烈反应并爆炸,Cl 与H 光照剧烈反应并爆炸,Br 与
2 2 2 2 2 2 2 2 2
H 加热到500 ℃才能发生反应,I 与H 在不断加热的条件下才缓慢发生反应,且为可逆反
2 2 2
应,故氧化性:F>Cl>Br >I。
2 2 2 2
②当不同的氧化剂作用于同一还原剂时,如果氧化产物价态相同,可根据反应条件的高低进
行判断:一般条件越低,氧化剂的氧化性越强,如:MnO +4HCl(浓)=====MnCl +Cl↑+
2 2 2
2HO,2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO,由上述反应条件的不同,可
2 4 2 2 2
判断氧化性:KMnO >MnO 。
4 2
③当不同氧化剂作用于同一还原剂时,如果氧化产物价态不相同,可根据氧化产物的价态高
低进行判断:氧化产物的价态越高,则氧化剂的氧化性越强,如:2Fe+3Cl=====2FeCl ,
2 3
Fe+S=====FeS,则氧化性:Cl>S。
2
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应(√)
(2)阳离子只有氧化性,阴离子只有还原性(×)
错因: Fe 2 + 除了具有氧化性,还具有还原性 。
(3)元素的非金属性越强,其氧化性越强,相应单质越活泼(×)
错因: 氮的非金属性很强,但 N 不活泼。
2
(4)金属原子失电子数越多,金属的还原性越强(×)
错因: Na 、 Mg 在氧化还原反应中,分别失去 1 个、 2 个电子,但 Na 的金属性强 。
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。
下列各组物质:①Cu与HNO 溶液 ②Cu与FeCl 溶液 ③Zn与HSO 溶液 ④Fe与
3 3 2 4
FeCl 溶液 ⑤Cl 与NaOH溶液 ⑥Fe与HNO 溶液 ⑦Fe与HSO 溶液 ⑧Na与O
3 2 3 2 4 2
(1)由于浓度不同而发生不同氧化还原反应的是____________________(填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是______________________________________。
(3)氧化还原反应不受浓度、温度影响的是__________。
答案 (1)①③⑥⑦ (2)⑤⑥⑦⑧ (3)②④
解析 ⑥Fe和浓HNO 常温下钝化,加热继续反应,Fe和稀HNO 反应,HNO 被还原成
3 3 3
NO。⑦Fe和浓HSO 常温下钝化,加热继续反应,Fe和稀HSO 反应生成FeSO 和H。
2 4 2 4 4 2根据影响因素判断氧化性、还原性强弱的方法
(1)浓度:同一种物质浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀HSO ,浓
2 4 2 4
HNO>稀HNO;还原性:浓盐酸>稀盐酸。
3 3
(2)温度:同一种物质,温度越高其氧化性越强。如:热的浓硫酸的氧化性比冷的浓硫酸的
氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化性(还原性)越强。
如:酸性条件:2MnO+6H++5SO===2Mn2++5SO+3HO
2
中性条件:2MnO+HO+3SO===2MnO ↓+3SO+2OH-
2 2
碱性条件:2MnO+2OH-+SO===2MnO+SO+HO
2
其氧化性为KMnO (酸性)>KMnO (中性)>KMnO (碱性)。
4 4 4
题组一 氧化性、还原性强弱的判断
1.铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①Tl3
++2Ag===Tl++2Ag+,②Ag++Fe2+===Ag+Fe3+,③Fe+2Fe3+===3Fe2+,下列离子氧化
性比较顺序正确的是( )
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe3+
答案 D
2.铋(Bi)位于元素周期表中第ⅤA族,其价态为+3时较稳定,铋酸钠(NaBiO)溶液呈无色。
3
现取一定量的硫酸锰(MnSO )溶液,向其中依次滴加下列溶液,对应的现象如表所示:
4
加入溶液 ①适量铋酸钠溶液 ②过量的双氧水 ③适量KI-淀粉溶液
实验现象 溶液呈紫红色 紫红色消失,产生气泡 溶液变成蓝色
则NaBiO、KMnO 、I、HO 的氧化性由强到弱的顺序为( )
3 4 2 2 2
A.I、HO、KMnO 、NaBiO
2 2 2 4 3
B.HO、I、NaBiO、KMnO
2 2 2 3 4
C.NaBiO、KMnO 、HO、I
3 4 2 2 2
D.KMnO 、NaBiO、I、HO
4 3 2 2 2
答案 C
解析 由①中现象可知,NaBiO 把Mn2+氧化生成MnO,则NaBiO(氧化剂)的氧化性强于
3 3
KMnO (氧化产物)的氧化性;由②中现象可知,KMnO 氧化HO 产生O ,自身被还原为
4 4 2 2 2
Mn2+,则KMnO (氧化剂)的氧化性强于HO 的氧化性;从价态上看,高锰酸钾的氧化性一
4 2 2
定是强于二氧化锰;由③中现象可知:碘离子被双氧水氧化成单质碘,则双氧水(氧化剂)的氧化性强于碘单质(氧化产物)的氧化性,综上所述,NaBiO 、KMnO 、I 、HO 的氧化性由
3 4 2 2 2
强到弱的顺序是NaBiO>KMnO >HO>I。
3 4 2 2 2
题组二 氧化性、还原性强弱的应用
3.已知I-、Fe2+、SO 和HO 均有还原性,它们在酸性溶液中还原性的强弱顺序为Fe2+<
2 2 2
HO<I-<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
B.I+SO +2HO===HSO +2HI
2 2 2 2 4
C.HO+HSO ===SO ↑+O↑+2HO
2 2 2 4 2 2 2
D.2Fe3++HO===2Fe2++O↑+2H+
2 2 2
答案 C
解析 A项,还原性:SO >Fe2+,符合题意;B项,还原性:SO >I-,符合题意;C项,
2 2
还原性:HO>SO ,与题意矛盾;D项,还原性:HO>Fe2+,符合题意。
2 2 2 2 2
4.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 的氧化性依次减弱。
2 3 2 3 2 3 2
下列反应在水溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl +4FeI
2 2 3 3
B.Cl+FeI===FeCl +I
2 2 2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO
2 3 2 2 2
D.2Fe3++2I-===2Fe2++I
2
答案 A
解析 根据氧化还原反应中,氧化性:氧化剂>氧化产物,可判断B中氧化性Cl>I ;C中
2 2
氧化性Co O>Cl ;D中氧化性Fe3+>I ,这些结论与题给信息一致。对于A,由于I-的还原
2 3 2 2
性强于Fe2+,所以Cl 应先氧化I-,而不是先氧化Fe2+。
2
假设法突破氧化还原反应能否进行
先假设选项中的化学反应能够发生,依据此反应判断出还原性(或氧化性)的强弱,然后与题
目提供的还原性(或氧化性)强弱顺序对照,若二者表示的还原性(或氧化性)强弱顺序一致,
则此反应能够发生;若不一致,则此反应不能进行。
题组三 氧化性、还原性强弱的实验探究
5.为验证氧化性Cl >Fe3+>SO ,某小组用下图所示装置进行实验(夹持仪器和A中加热装
2 2
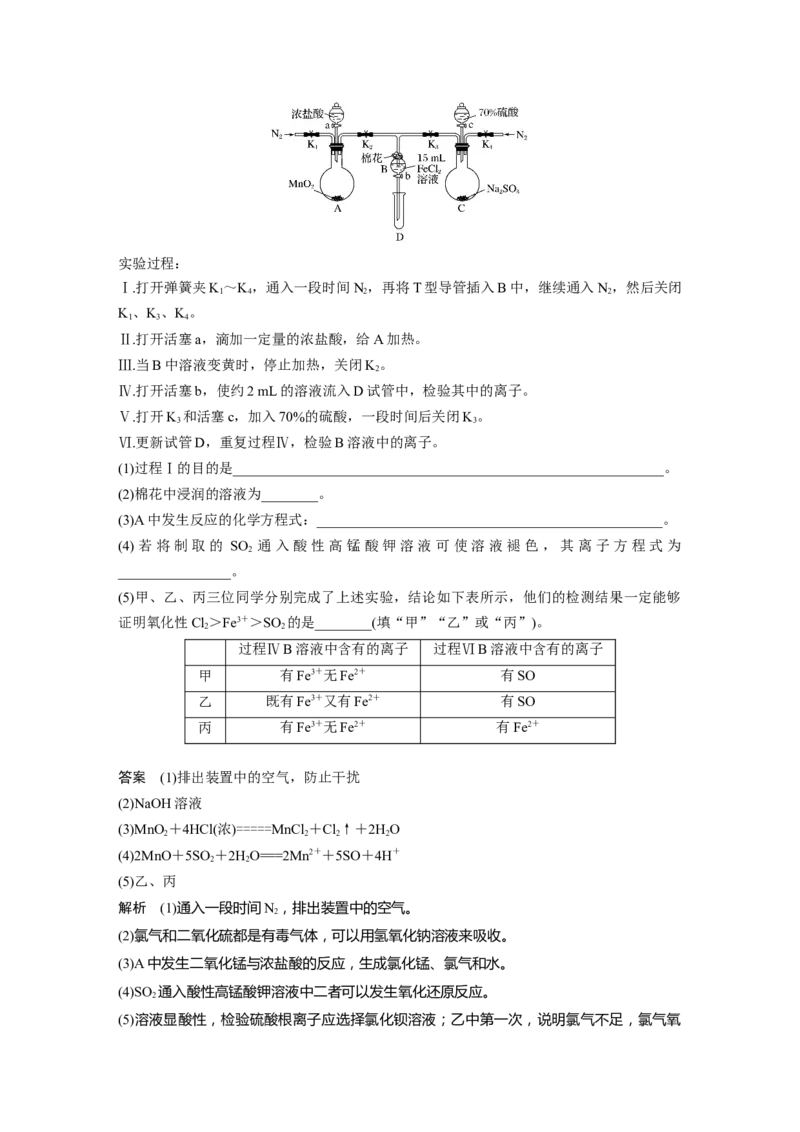
置已略,气密性已检验)。实验过程:
Ⅰ.打开弹簧夹K~K,通入一段时间N,再将T型导管插入B中,继续通入N,然后关闭
1 4 2 2
K、K、K。
1 3 4
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K。
2
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K 和活塞c,加入70%的硫酸,一段时间后关闭K。
3 3
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_____________________________________________________________。
(2)棉花中浸润的溶液为________。
(3)A中发生反应的化学方程式:_________________________________________________。
(4)若将制取的 SO 通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为
2
________________。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够
证明氧化性Cl>Fe3+>SO 的是________(填“甲”“乙”或“丙”)。
2 2
过程ⅣB溶液中含有的离子 过程ⅥB溶液中含有的离子
甲 有Fe3+无Fe2+ 有SO
乙 既有Fe3+又有Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+
答案 (1)排出装置中的空气,防止干扰
(2)NaOH溶液
(3)MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
(4)2MnO+5SO +2HO===2Mn2++5SO+4H+
2 2
(5)乙、丙
解析 (1)通入一段时间N,排出装置中的空气。
2
(2)氯气和二氧化硫都是有毒气体,可以用氢氧化钠溶液来吸收。
(3)A中发生二氧化锰与浓盐酸的反应,生成氯化锰、氯气和水。
(4)SO 通入酸性高锰酸钾溶液中二者可以发生氧化还原反应。
2
(5)溶液显酸性,检验硫酸根离子应选择氯化钡溶液;乙中第一次,说明氯气不足,氯气氧化性大于铁离子,第二次有硫酸根离子,说明发生二氧化硫与铁离子的反应,则铁离子的氧
化性大于二氧化硫;丙中第一次有Fe3+,无Fe2+,则氯气的氧化性大于铁离子,第二次有
亚铁离子,说明发生二氧化硫与铁离子的反应,则铁离子的氧化性大于二氧化硫。
1.正误判断
(1)向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色,所以 Br-还原性强
于Cl-(√)(2015·山东理综,11C)
(2)向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,加入淀粉后溶液变成蓝色,
则氧化性:Cl>I (√)(2015·广东理综,22C)
2 2
(3)向FeSO 溶液中先滴入KSCN溶液,再滴加HO 溶液,加入HO 后溶液变成红色,则
4 2 2 2 2
Fe2+既有氧化性又有还原性(×)(2015·广东理综,22D)
(4)在氧化还原反应中,还原剂失去电子的总数等于氧化剂得到电子的总数(√)
(2015·江苏,3C)
(5)在CO 中,Mg燃烧生成MgO和C,在该反应条件下,Mg的还原性强于C的还原性(√)
2
(2015·江苏,4C)
2.[2020·新高考全国卷Ⅰ(山东),2]下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
答案 B
解析 谷物发酵的过程中包含淀粉水解、葡萄糖转化为乙醇、乙醇氧化为乙酸的过程;小苏
打分解的化学方程式为2NaHCO =====NaCO +CO↑+HO,不是氧化还原反应;含氯消
3 2 3 2 2
毒剂有强氧化性,可用于环境消毒;NO 与水发生反应3NO +HO===NO+2HNO,是氧化
2 2 2 3
还原反应。
3.(2020·北京,2)下列物质的应用中,利用了氧化还原反应的是( )
A.用石灰乳脱除烟气中的SO
2
B.用明矾[KAl(SO)·12H O]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O·xHO)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
答案 D
解析 用石灰乳脱除烟气中的SO 时,SO 与氢氧化钙反应生成亚硫酸钙或亚硫酸氢钙,反
2 2
应过程中无元素化合价的变化,没有利用氧化还原反应,故 A 不符合题意;明矾
[KAl(SO)·12H O]溶于水,电离出的铝离子发生水解生成氢氧化铝胶体,利用胶体的吸附性
4 2 2可吸附污水中的固体颗粒物,该过程利用胶体的吸附性,发生的反应中元素化合价没有变化,
没有利用氧化还原反应,故B不符合题意;用盐酸去除铁锈(主要成分Fe O·xHO),发生的
2 3 2
主要反应为6HCl+Fe O===2FeCl +3HO,反应中没有元素化合价的变化,没有利用氧化
2 3 3 2
还原反应,故C不符合题意;84消毒液有效成分为NaClO,具有强氧化性,能使蛋白质发
生变性从而杀死细菌病毒,杀菌消毒的过程利用了氧化还原反应,故D符合题意。
4.(2020·北京,3)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.NaO
2 2 2
答案 A
解析 2Na+2HO===2NaOH+H↑,HO中H元素化合价由+1降为0,得电子被还原,
2 2 2
作氧化剂,在反应中表现出氧化性,故 A符合题意;Cl +HOHCl+HClO、3NO +
2 2 2
HO===2HNO +NO,HO中的元素没有发生化合价的变化,水在反应中既不是氧化剂也不
2 3 2
是还原剂,既不表现氧化性也不表现还原性,故C不符合题意;NaO+HO===2NaOH,该
2 2
反应没有元素化合价的变化,不是氧化还原反应,水在反应中既不表现氧化性也不表现还原
性,故D不符合题意。
5.(2020·浙江7月选考,10)反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化产物
2 2 2 2
与还原产物的物质的量之比是( )
A.1∶2 B.1∶1 C.2∶1 D.4∶1
答案 B
6.(2018·浙江11月选考,6)下列化学反应中溴元素仅被氧化的是( )
A.2NaBr+Cl===2NaCl+Br
2 2
B.Br +2NaI===2NaBr+I
2 2
C.3Br +6NaOH=====5NaBr+NaBrO +3HO
2 3 2
D.HBr+NaOH===NaBr+HO
2
答案 A
解析 溴化钠中溴元素化合价升高被氧化作还原剂,选项 A符合;溴单质中溴元素化合价
降低被还原作氧化剂,选项B不符合;溴单质既是氧化剂又是还原剂,被氧化生成溴酸钠,
被还原生成溴化钠,选项C不符合;反应属于中和反应,各元素化合价不变,不属于氧化
还原反应,选项D不符合。
7.(2019·北京,10)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
选项 物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2答案 B
解析 A项,Fe粉将溶液中的Fe3+转化为Fe2+,涉及氧化还原反应;B项,Mg2+与NaOH
溶液反应生成Mg(OH) 沉淀,过滤后多余的NaOH用稀盐酸中和,两个反应均不涉及氧化
2
还原反应;C项,Cl 能溶于水并与水发生氧化还原反应,不能用水除去Cl 中的HCl;D项,
2 2
NO 与水反应生成HNO 和NO,涉及氧化还原反应。
2 3
1.(2020·太原质检)下列应用不涉及物质氧化性或还原性的是( )
A.用葡萄糖制镜或保温瓶胆
B.用漂白液杀菌、消毒
C.用NaSiO 溶液制备木材防火剂
2 3
D.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
答案 C
解析 葡萄糖与银氨溶液发生氧化还原反应,生成银单质,葡萄糖作还原剂被氧化,故A
不选;用漂白液杀菌、消毒利用了NaClO的强氧化性,故B不选;用NaSiO 溶液制备木材
2 3
防火剂不发生氧化还原反应,与氧化性或还原性无关,故C选;高锰酸钾可氧化具有催熟
作用的乙烯,从而达到保鲜水果的目的,故D不选。
2.(2020·湖南省岳阳一中模拟)下列实验中,颜色的变化与氧化还原反应有关的是( )
A.向紫色石蕊溶液中加入盐酸,溶液变红
B.饱和FeCl 溶液在沸水中变成红褐色胶体
3
C.向FeSO 溶液中滴加NaOH溶液,生成的沉淀由白色迅速变成灰绿色,最后变成红褐色
4
D.SO 使滴有酚酞的NaOH溶液褪色
2
答案 C
解析 向FeSO 溶液中滴加NaOH溶液,得到白色沉淀Fe(OH) ,Fe(OH) 迅速与空气中的
4 2 2
O 发生氧化还原反应得到红褐色的Fe(OH) 。
2 3
3.对于反应:2HS+SO ===3S↓+2HO,氧化剂与还原剂的物质的量之比为( )
2 2 2
A.1∶1 B.2∶1 C.3∶1 D.1∶2
答案 D
解析 反应2HS+SO ===3S↓+2HO中,HS中S元素化合价由-2升高为0,HS是还原
2 2 2 2 2
剂;SO 中S元素化合价由+4降低为0,SO 是氧化剂,所以氧化剂与还原剂的物质的量之
2 2
比等于1∶2,D满足题意。
4.下列属于氧化还原反应,且氧化剂和还原剂为同一种物质的是( )
A.MgO+2HCl===MgCl +HO
2 2
B.C+HO(g)=====CO+H
2 2
C.8NH +6NO =====7N+12HO
3 2 2 2D.2NaO+2HO===4NaOH+O↑
2 2 2 2
答案 D
解析 MgO+2HCl===MgCl +HO中元素化合价没有发生变化,反应不是氧化还原反应,
2 2
A不符合题意;C+HO(g)=====CO+H 中C、H两种元素的化合价都发生了变化,反应属
2 2
于氧化还原反应,其中C是还原剂,HO是氧化剂,氧化剂和还原剂不是同一种物质,B不
2
符合题意;8NH +6NO =====7N +12HO中只有N元素的化合价发生了变化,反应属于氧
3 2 2 2
化还原反应,其中NH 是还原剂,NO 是氧化剂,氧化剂和还原剂不是同一种物质,C不符
3 2
合题意;反应2NaO +2HO===4NaOH+O↑中有O元素化合价的变化,反应属于氧化还
2 2 2 2
原反应,其中NaO 既是还原剂也是氧化剂,氧化剂和还原剂是同一种物质,D符合题意。
2 2
5.(2020·四川省泸县第二中学高三模拟)氯气是一种重要的工业原料。工业上利用下列反应
来检查氯气管道是否漏气:3Cl+8NH ===N+6NH Cl。下列说法错误的是( )
2 3 2 4
A.若有白烟产生则管道漏气
B.该反应中NH Cl是还原产物
4
C.反应中NH 只显还原性
3
D.生成1.4 g N 时转移0.3 mol电子
2
答案 C
解析 反应生成HCl,NH 可与HCl反应生成氯化铵,有白烟生成,故A正确;Cl元素化
3
合价降低,被还原,Cl 为氧化剂,所以NH Cl是还原产物,故B正确;反应中NH 中氮元
2 4 3
素是-3价,处于最低价态,部分显还原性,同时与氯化氢反应生成氯化铵,故 C错误;N
元素化合价由-3升高到0,则生成1 mol N 时有6 mol电子转移,生成1.4 g N 物质的量为0.05
2 2
mol,转移×6 mol=0.3 mol电子,故D正确。
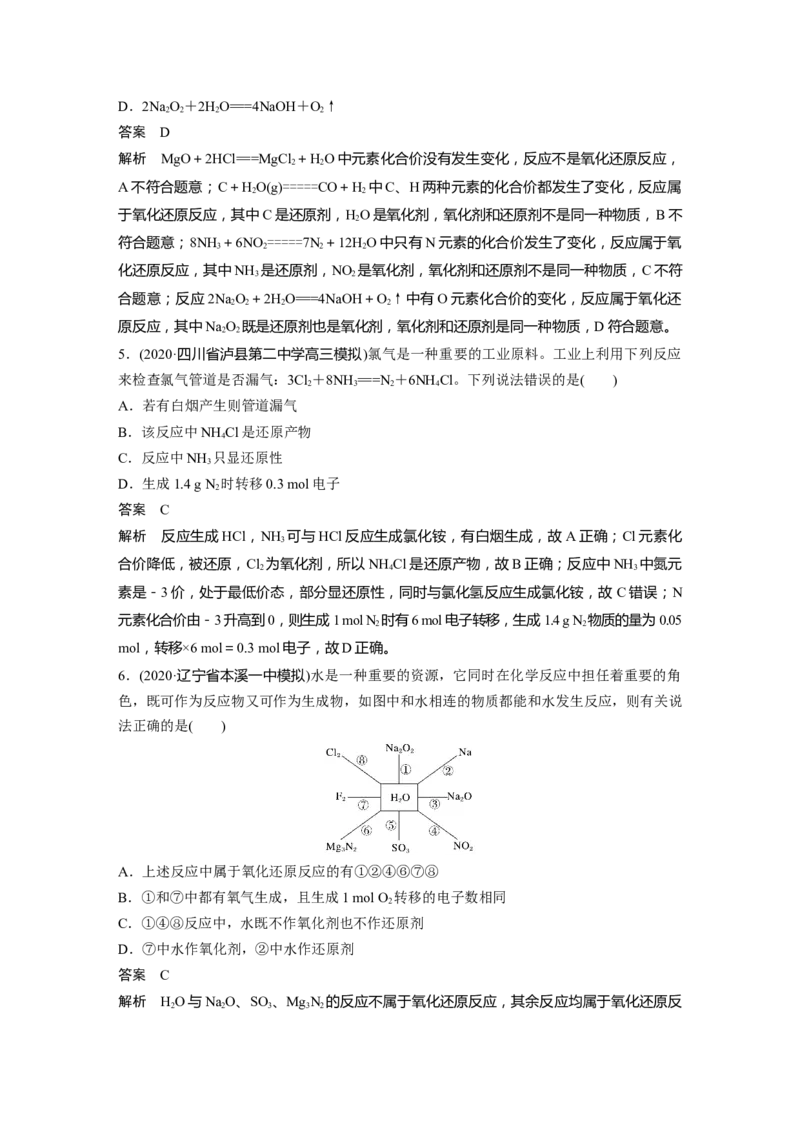
6.(2020·辽宁省本溪一中模拟)水是一种重要的资源,它同时在化学反应中担任着重要的角
色,既可作为反应物又可作为生成物,如图中和水相连的物质都能和水发生反应,则有关说
法正确的是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①和⑦中都有氧气生成,且生成1 mol O 转移的电子数相同
2
C.①④⑧反应中,水既不作氧化剂也不作还原剂
D.⑦中水作氧化剂,②中水作还原剂
答案 C
解析 HO与NaO、SO 、MgN 的反应不属于氧化还原反应,其余反应均属于氧化还原反
2 2 3 3 2应,A错误;①中2NaO +2HO===4NaOH+O↑,生成1 mol O 转移2 mol e-,⑦中2F
2 2 2 2 2 2
+2HO===4HF+O ,生成1 mol O 转移4 mol e-,B错误;①④⑧反应中,水既不作氧化
2 2 2
剂也不作还原剂,C正确;⑦中水作还原剂,②中水作氧化剂,D错误。
7.已知N元素的最低化合价是-3,最高化合价是+5,那么下列物质中的N元素只具有氧
化性的是( )
A.NH B.N C.NO D.HNO
3 2 2 3
答案 D
解析 N元素只具有氧化性,则化合价只能降低,化合价为+5。NH 中N的化合价为-3,
3
是最低价,只有还原性,与题意不符,A错误;N 中N的化合价为0,既可以升高,又可以
2
降低,与题意不符,B错误;NO 中N的化合价为+4,既可以升高,又可以降低,与题意
2
不符,C错误;HNO 中N的化合价为+5,符合题意,D正确。
3
8.在溶液中可以发生反应:X+2Y3+===2Y2++X2+,现有下列叙述①X被氧化;②X是氧
化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的
氧化性强。其中正确的是( )
A.②④⑥ B.①③④ C.①③⑤⑥ D.②⑤
答案 C
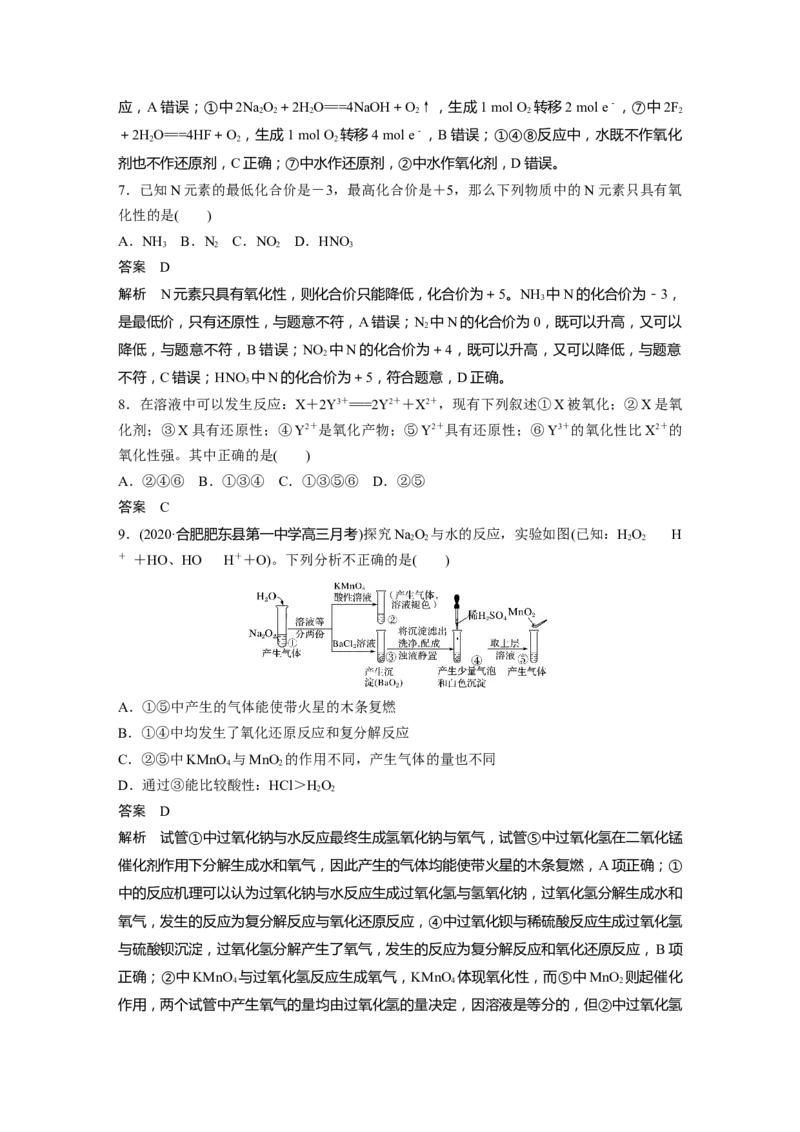
9.(2020·合肥肥东县第一中学高三月考)探究NaO 与水的反应,实验如图(已知:HO H
2 2 2 2
+ +HO、HOH++O)。下列分析不正确的是( )
A.①⑤中产生的气体能使带火星的木条复燃
B.①④中均发生了氧化还原反应和复分解反应
C.②⑤中KMnO 与MnO 的作用不同,产生气体的量也不同
4 2
D.通过③能比较酸性:HCl>HO
2 2
答案 D
解析 试管①中过氧化钠与水反应最终生成氢氧化钠与氧气,试管⑤中过氧化氢在二氧化锰
催化剂作用下分解生成水和氧气,因此产生的气体均能使带火星的木条复燃,A项正确;①
中的反应机理可以认为过氧化钠与水反应生成过氧化氢与氢氧化钠,过氧化氢分解生成水和
氧气,发生的反应为复分解反应与氧化还原反应,④中过氧化钡与稀硫酸反应生成过氧化氢
与硫酸钡沉淀,过氧化氢分解产生了氧气,发生的反应为复分解反应和氧化还原反应,B项
正确;②中KMnO 与过氧化氢反应生成氧气,KMnO 体现氧化性,而⑤中MnO 则起催化
4 4 2
作用,两个试管中产生氧气的量均由过氧化氢的量决定,因溶液是等分的,但②中过氧化氢全部被氧化,⑤中的过氧化氢发生歧化反应,所以产生气体的量不相同,C项正确;根据已
知条件可以看出过氧化氢属于二元弱酸,而HCl属于一元强酸,试管③因为生成了过氧化
钡沉淀,不是可溶性的盐溶液,则不能证明HCl与过氧化氢的酸性强弱,D项错误。
10.(2020·浙江省绍兴一中模拟)已知二氯化二硫(S Cl)的结构式为Cl—S—S—Cl,它易与水
2 2
反应:2SCl+2HO===4HCl+SO ↑+3S↓。对该反应的说法不正确的是( )
2 2 2 2
A.SCl 既作氧化剂又作还原剂
2 2
B.HO作氧化剂
2
C.每生成1 mol SO 转移3 mol电子
2
D.氧化产物与还原产物的物质的量之比为1∶3
答案 B
解析 因Cl的非金属性比S强,故SCl 中S、Cl的化合价分别为+1、-1;则在反应中只
2 2
有硫的化合价发生变化,氧化产物与还原产物的物质的量之比为 1∶3,A、D项正确,B项
错误;SO 中硫的化合价为+4,故每生成1 mol SO 转移3 mol电子,C项正确。
2 2
11.(2020·延安模拟)氯元素的化合价与其形成的常见物质种类的关系如图所示。
下列说法不正确的是( )
A.b只有还原性
B.c没有漂白性,d具有漂白性
C.一定条件下e和f均属于较强氧化剂
D.g的化学式为HClO
4
答案 A
解析 b为HCl,其中+1价的H化合价能降低,具有氧化性,A项错误;c为Cl ,没有漂
2
白性,d为HClO,具有漂白性,B项正确;e为ClO ,f含ClO,一定条件下二者均属于较
2
强氧化剂,C项正确;g的化学式为HClO,D项正确。
4
12.(2020·滨州模拟)工业上制备有机氟化剂 SF 的反应 3SCl +4NaF===SF +SCl +
4 2 4 2 2
4NaCl。下列说法正确的是( )
A.NaF既不作氧化剂也不作还原剂,SF 为氧化产物
4
B.SCl 与SCl 两种物质中的氯元素化合价不同
2 2 2
C.还原剂与氧化剂物质的量之比为2∶1
D.SF 属于有机物
4
答案 A
解析 NaF中钠元素和氟元素化合价均未变化,既不作氧化剂也不作还原剂,SCl 中硫元素
2化合价为+2价,SF 中硫元素化合价为+4,SF 为氧化产物,A正确;SCl 中氯元素化合
4 4 2
价为-1价,SCl 中氯元素化合价为-1价,Cl的化合价相同,B错误;SCl 中硫元素化合
2 2 2
价为+2价,氯元素化合价为-1价,SCl 中硫元素化合价为+1,氯元素化合价为-1价,
2 2
SCl 为还原产物,SF 中硫元素化合价为+4,SF 为氧化产物,SCl 既作氧化剂又作还原剂,
2 2 4 4 2
氧化剂与还原剂物质的量之比为2∶1,C错误;有机物含有C元素,SF 中没有C元素,不
4
是有机物,D错误。
13.已知氧化性:Fe3+>I >SO,下列说法或离子方程式正确的是( )
2
A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
B.Fe O 可写成FeO·Fe O,Fe I 可写成FeI·2FeI
3 4 2 3 3 8 2 3
C.还原性:Fe2+>SO>I-
2
D.反应HSO (浓)+2HI===I+SO ↑+2HO不能进行
2 4 2 2 2
答案 A
解析 反应2Fe3++SO +2HO===2Fe2++SO+4H+中,Fe3+是氧化剂,SO是氧化产物,该
2 2
反应的发生符合氧化性:Fe3+>SO,A正确;铁元素的化合价有+2和+3,碘元素的化合
价是-1价,由于氧化性:Fe3+>I,故I 不能将Fe2+氧化成Fe3+,只能将铁氧化到+2价,
2 2
Fe I 可表示为3FeI·I,B错误;根据离子的氧化性顺序:Fe3+>I>SO,得到还原性顺序是
3 8 2 2 2
SO >I->Fe2+,C错误;浓硫酸具有强氧化性,碘离子具有强还原性,反应 HSO (浓)+
2 2 4
2HI===I+SO ↑+2HO能进行,D错误。
2 2 2
14.已知反应:①2BrO+Cl===Br +2ClO
2 2
②5Cl+I+6HO===2HIO +10HCl
2 2 2 3
③ClO+5Cl-+6H+===3Cl↑+3HO,
2 2
下列物质(或微粒)氧化能力强弱顺序正确的是( )
A.ClO>BrO>HIO >Cl
3 2
B.BrO>Cl >ClO>HIO
2 3
C.BrO>ClO>Cl >HIO
2 3
D.Cl>BrO>ClO>HIO
2 3
答案 C
解析 已知反应:①2BrO+Cl===Br +2ClO,氧化剂为BrO,氧化产物为ClO,故氧化性
2 2
BrO>ClO;②5Cl +I +6HO===2HIO +10HCl,氧化剂为Cl ,氧化产物HIO ,故氧化性
2 2 2 3 2 3
Cl>HIO ;③ClO+5Cl-+6H+===3Cl↑+3HO,氧化剂为ClO,氧化产物为Cl ,氧化性
2 3 2 2 2
ClO>Cl ,因此氧化性强弱顺序为BrO>ClO>Cl >HIO,故C正确。
2 2 3
15.(2020·福建省莆田一中模拟)HNO 是一种弱酸,且不稳定,易分解生成NO和NO ;它
2 2
能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把 Fe2+氧化成Fe3+。
AgNO 是一种难溶于水、易溶于酸的化合物,试回答下列问题:
2
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO ),则导致血红蛋白中的Fe2+
2转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填字母)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO 溶液中,观察到氯水褪色,同时生成NaNO 和HCl,请
2 3
写出反应的离子方程式:_________________________________________________________。
(3)Fe与过量稀硫酸反应可以制取FeSO ,若用反应所得的酸性溶液将Fe2+转化为Fe3+,要
4
求产物纯净,可选用的最佳试剂是________(填字母)。
a.Cl b.Fe c.HO d.HNO
2 2 2 3
(4)FeSO 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na FeO),氧化性比
4 2 4
Cl 、O 、ClO 、KMnO 更强,主要反应:2FeSO +6NaO===2NaFeO +2NaO+2NaSO
2 2 2 4 4 2 2 2 4 2 2 4
+O↑。
2
①该反应中的氧化剂是________,还原剂是________。
②简要说明NaFeO 作为水处理剂时所起的作用____________________________________。
2 4
答案 (1)D (2)NO+Cl +HO===NO+2H++2Cl- (3)c (4)①NaO NaO 、FeSO ②
2 2 2 2 2 2 4
高铁酸钠具有强氧化性,能杀菌消毒,消毒过程中自身被还原为 Fe3+,Fe3+水解生成
Fe(OH) 胶体能吸附水中悬浮杂质而沉降
3
解析 (1)服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+,铁元素化合
价降低,被还原,则维生素C具有还原性,而亚硝酸盐会导致Fe2+转化为Fe3+,说明亚硝
酸盐具有氧化性,在反应中亚硝酸盐为氧化剂,所以维生素 C是还原剂。(3)由于Cl 、
2
HNO 都能氧化亚铁离子,但能引入新的杂质,铁不能氧化亚铁离子,双氧水作为氧化剂的
3
还原产物是水,不引入杂质,所以最佳试剂是双氧水。(4)该反应中铁元素化合价由+2变为
+6、氧元素化合价由-1变为0、-2。①得电子化合价降低的反应物是氧化剂、失电子化
合价升高的反应物是还原剂,所以NaO 是氧化剂,NaO 、FeSO 是还原剂;②NaFeO 中
2 2 2 2 4 2 4
铁元素的化合价为+6,具有强氧化性,能杀菌消毒且还原产物铁离子能水解生成氢氧化铁
胶体,胶体具有吸附性能吸附除去水中的悬浮杂质。