文档内容
专项特训 1 循环转化关系图中的氧化还原反应
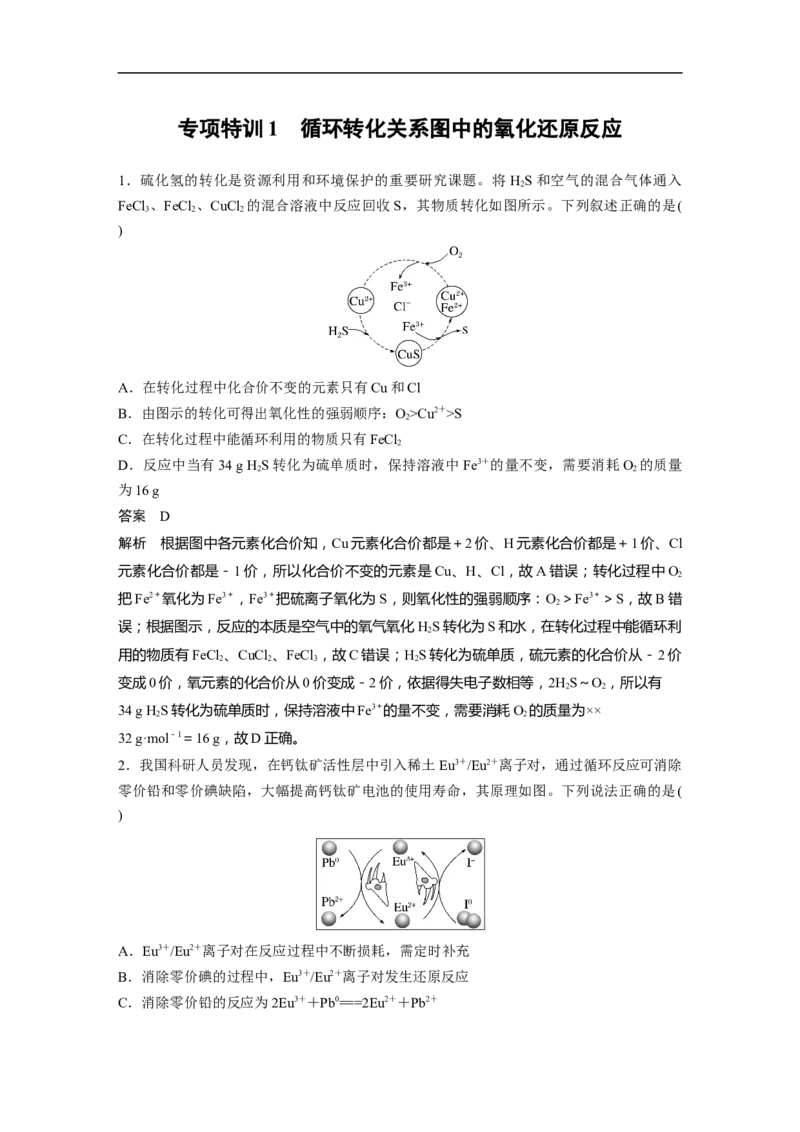
1.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
2
FeCl 、FeCl 、CuCl 的混合溶液中反应回收S,其物质转化如图所示。下列叙述正确的是(
3 2 2
)
A.在转化过程中化合价不变的元素只有Cu和Cl
B.由图示的转化可得出氧化性的强弱顺序:O>Cu2+>S
2
C.在转化过程中能循环利用的物质只有FeCl
2
D.反应中当有34 g H S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O 的质量
2 2
为16 g
答案 D
解析 根据图中各元素化合价知,Cu元素化合价都是+2价、H元素化合价都是+1价、Cl
元素化合价都是-1价,所以化合价不变的元素是Cu、H、Cl,故A错误;转化过程中O
2
把Fe2+氧化为Fe3+,Fe3+把硫离子氧化为S,则氧化性的强弱顺序:O >Fe3+>S,故B错
2
误;根据图示,反应的本质是空气中的氧气氧化HS转化为S和水,在转化过程中能循环利
2
用的物质有FeCl 、CuCl 、FeCl ,故C错误;HS转化为硫单质,硫元素的化合价从-2价
2 2 3 2
变成0价,氧元素的化合价从0价变成-2价,依据得失电子数相等,2HS~O,所以有
2 2
34 g HS转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O 的质量为××
2 2
32 g·mol-1=16 g,故D正确。
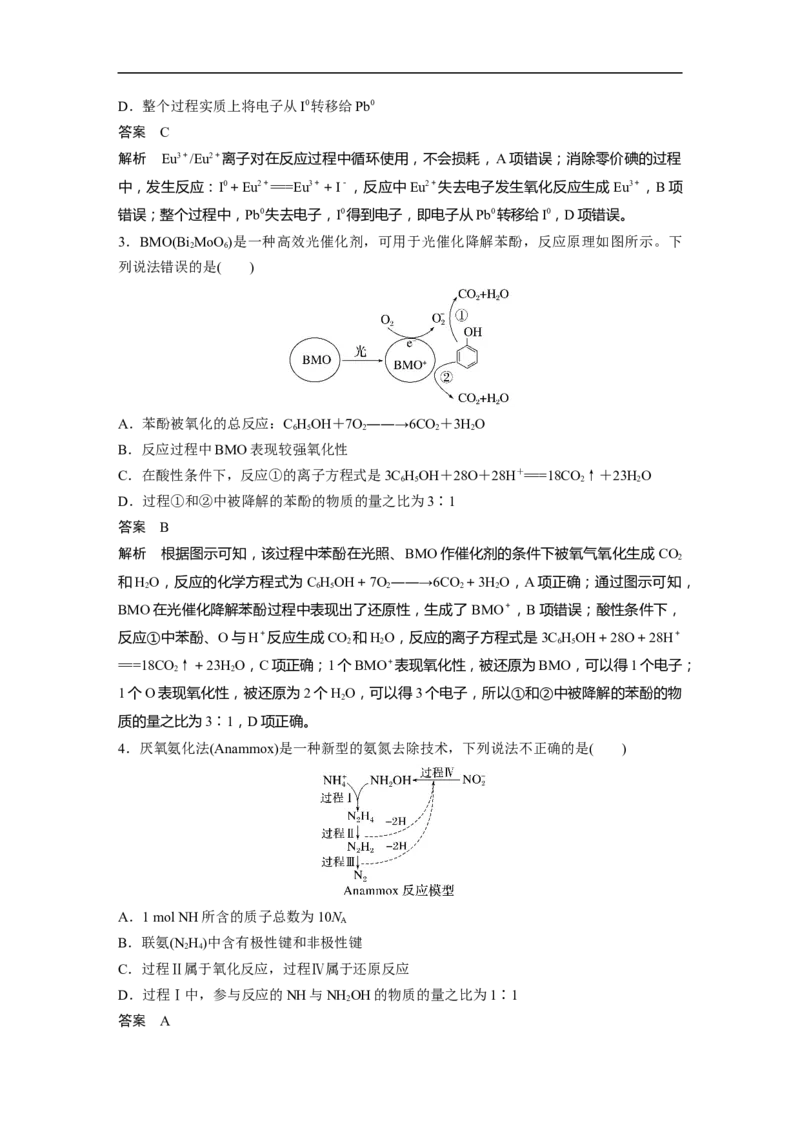
2.我国科研人员发现,在钙钛矿活性层中引入稀土Eu3+/Eu2+离子对,通过循环反应可消除
零价铅和零价碘缺陷,大幅提高钙钛矿电池的使用寿命,其原理如图。下列说法正确的是(
)
A.Eu3+/Eu2+离子对在反应过程中不断损耗,需定时补充
B.消除零价碘的过程中,Eu3+/Eu2+离子对发生还原反应
C.消除零价铅的反应为2Eu3++Pb0===2Eu2++Pb2+D.整个过程实质上将电子从I0转移给Pb0
答案 C
解析 Eu3+/Eu2+离子对在反应过程中循环使用,不会损耗,A项错误;消除零价碘的过程
中,发生反应:I0+Eu2+===Eu3++I-,反应中Eu2+失去电子发生氧化反应生成Eu3+,B项
错误;整个过程中,Pb0失去电子,I0得到电子,即电子从Pb0转移给I0,D项错误。
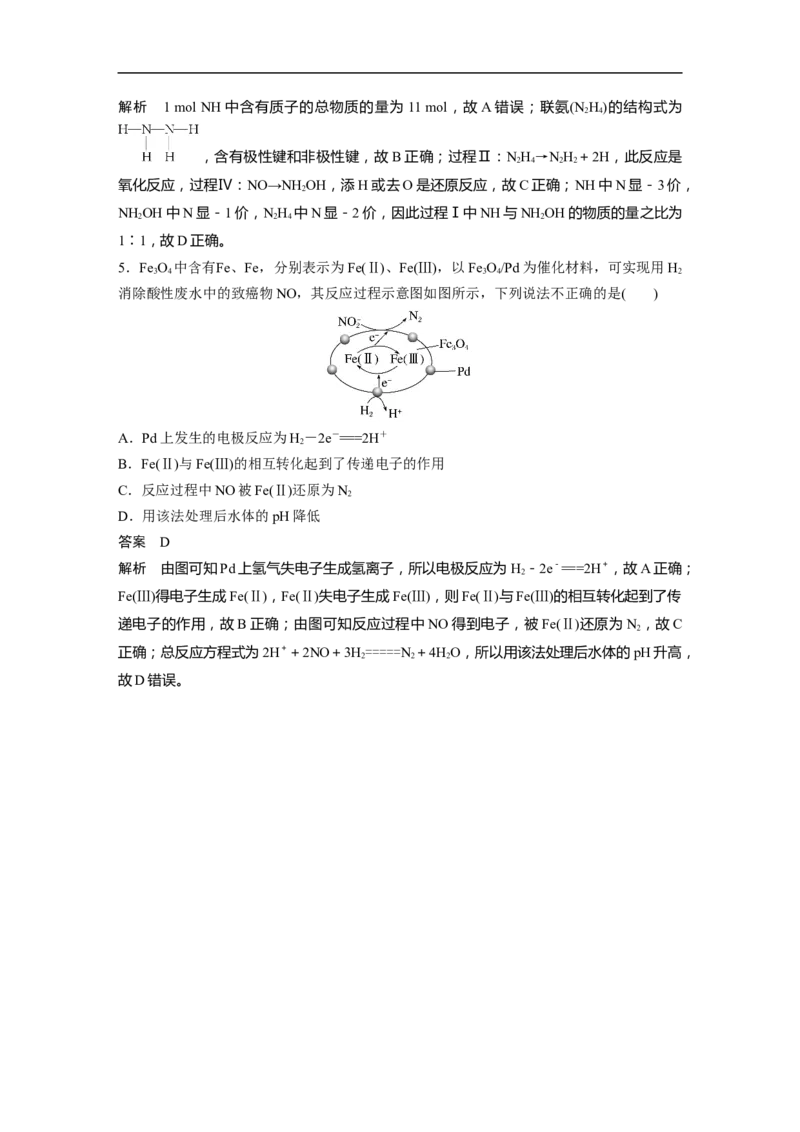
3.BMO(Bi MoO )是一种高效光催化剂,可用于光催化降解苯酚,反应原理如图所示。下
2 6
列说法错误的是( )
A.苯酚被氧化的总反应:C HOH+7O――→6CO+3HO
6 5 2 2 2
B.反应过程中BMO表现较强氧化性
C.在酸性条件下,反应①的离子方程式是3C HOH+28O+28H+===18CO↑+23HO
6 5 2 2
D.过程①和②中被降解的苯酚的物质的量之比为3∶1
答案 B
解析 根据图示可知,该过程中苯酚在光照、BMO作催化剂的条件下被氧气氧化生成 CO
2
和HO,反应的化学方程式为C HOH+7O――→6CO +3HO,A项正确;通过图示可知,
2 6 5 2 2 2
BMO在光催化降解苯酚过程中表现出了还原性,生成了 BMO+,B项错误;酸性条件下,
反应①中苯酚、O与H+反应生成CO 和HO,反应的离子方程式是3C HOH+28O+28H+
2 2 6 5
===18CO↑+23HO,C项正确;1个BMO+表现氧化性,被还原为BMO,可以得1个电子;
2 2
1个O表现氧化性,被还原为2个HO,可以得3个电子,所以①和②中被降解的苯酚的物
2
质的量之比为3∶1,D项正确。
4.厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法不正确的是( )
A.1 mol NH所含的质子总数为10N
A
B.联氨(N H)中含有极性键和非极性键
2 4
C.过程Ⅱ属于氧化反应,过程Ⅳ属于还原反应
D.过程Ⅰ中,参与反应的NH与NH OH的物质的量之比为1∶1
2
答案 A解析 1 mol NH中含有质子的总物质的量为11 mol,故A错误;联氨(N H)的结构式为
2 4
,含有极性键和非极性键,故B正确;过程Ⅱ:NH→NH +2H,此反应是
2 4 2 2
氧化反应,过程Ⅳ:NO→NH OH,添H或去O是还原反应,故C正确;NH中N显-3价,
2
NH OH中N显-1价,NH 中N显-2价,因此过程Ⅰ中NH与NH OH的物质的量之比为
2 2 4 2
1∶1,故D正确。
5.Fe O 中含有Fe、Fe,分别表示为Fe(Ⅱ)、Fe(Ⅲ),以Fe O/Pd为催化材料,可实现用H
3 4 3 4 2
消除酸性废水中的致癌物NO,其反应过程示意图如图所示,下列说法不正确的是( )
A.Pd上发生的电极反应为H-2e-===2H+
2
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO被Fe(Ⅱ)还原为N
2
D.用该法处理后水体的pH降低
答案 D
解析 由图可知Pd上氢气失电子生成氢离子,所以电极反应为H -2e-===2H+,故A正确;
2
Fe(Ⅲ)得电子生成Fe(Ⅱ),Fe(Ⅱ)失电子生成Fe(Ⅲ),则Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传
递电子的作用,故B正确;由图可知反应过程中NO得到电子,被Fe(Ⅱ)还原为N ,故C
2
正确;总反应方程式为2H++2NO+3H=====N +4HO,所以用该法处理后水体的pH升高,
2 2 2
故D错误。