文档内容
热点强化 6 工业流程中含铁化合物的制备
(一)含铁化合物制备的微型流程设计
例1 用废铁屑制备磁性氧化铁(Fe O),制取过程如图:
3 4
下列说法不正确的是( )
A.浸泡过程中适当加热并搅拌效果更好
B.检验A中的Fe3+可以用KSCN溶液
C.加HO 时发生反应的离子方程式为HO+2Fe2++2H+===2Fe3+ +2HO
2 2 2 2 2
D.制备Fe O 的反应Fe2++2Fe3++8OH-=====Fe O+4HO是氧化还原反应
3 4 3 4 2
答案 D
解析 浸泡过程中适当加热并搅拌可以提高反应速率,效果更好,A正确;检验铁离子可以
用硫氰化钾溶液,溶液显红色,B正确;过氧化氢能氧化亚铁离子,离子方程式为HO+
2 2
2Fe2++2H+===2Fe3+ +2HO,C 正确;制备 Fe O 的反应为 Fe2++2Fe3++8OH-
2 3 4
=====Fe O+4HO,没有元素化合价变化,不是氧化还原反应,D错误。
3 4 2
(二)含铁化合物制备的综合流程设计
例2 利用金属矿渣(含有FeS、SiO 及Cu O)制备(NH )Fe(SO ) 晶体的实验流程如下。
2 2 2 4 2 4 2
(1)煅烧过程中FeS 和Cu O转化为Fe O 和CuO。FeS 与O 反应生成Fe O 和SO 的化学方
2 2 2 3 2 2 2 3 2
程式为______________________________________________________________________。
(2)为提高酸浸过程中铁的浸出率,实验中可采取的措施有____________(填字母)。
A.增加矿渣的投料量 B.将矿渣粉碎并搅拌
C.缩短酸浸的时间 D.适当提高酸浸温度
(3)向酸浸后的溶液中加入过量铁屑,除能将Fe3+转化为Fe2+外,还能__________________;
检验Fe3+是否完全被还原的实验操作是____________________________________________。
(4)煅烧生成的SO 用石灰乳吸收得到CaSO 浆料,以CaSO 浆料制备NaHSO 溶液的实验方
2 3 3 3
案为_________________________________________________________________________。
(已知:2CaSO +NaSO +HSO +4HO===2CaSO·2H O+2NaHSO ;CaSO·2H O难溶于
3 2 4 2 4 2 4 2 3 4 2
水;pH=4~6的溶液中HSO能大量存在。实验中可选用的试剂:3 mol·L-1 Na SO ,3
2 4
mol·L-1HSO ,1 mol·L-1 NaOH)
2 4
答案 (1)4FeS +11O=====2Fe O+8SO
2 2 2 3 2
(2)BD
(3)将Cu2+转化为Cu 取少量还原后的上层清液于试管中,向其中滴加KSCN溶液,若溶液
不变红,则Fe3+已完全被还原
(4)向CaSO 浆料中加入一定量3 mol·L-1 Na SO ,边搅拌边缓慢滴加总量与NaSO 溶液相
3 2 4 2 4
同量的3 mol·L-1 HSO ,测定反应液的pH,再用3 mol·L-1 HSO 或1 mol·L-1 NaOH调节
2 4 2 4
pH在4~6之间,过滤(或向CaSO 浆料中边搅拌边缓慢滴加3 mol·L-1 HSO ,产生的气体
3 2 4
通入1 mol·L-1 NaOH溶液中,测定溶液pH,当测定pH在4~6之间,停止滴加HSO )
2 4
解析 (2)增大投料量并不能增大浸出率,故A不选;矿渣粉碎后,反应接触面积增大,反
应更快更充分,可提高浸出率,故 B选;缩短酸浸时间会降低浸出率,故 C不选;适当提
高温度可提高浸出率,故D选。
(3)加入过量铁屑除将Fe3+转化为Fe2+外,还能将铜离子转化为铜而过滤除去;检验铁离子
是否完全被还原的操作是:取少量还原后的上层清液于试管中,向其中滴加 KSCN溶液,
若溶液不变红,则Fe3+已完全被还原。(4)根据信息,pH=4~6时,HSO能大量共存,且
CaSO·2H O难溶于水,故该制备环境应在酸性条件下。
4 2
1.高磷鲕状赤铁矿(主要含有Fe O,含少量Al O、CaO、SiO 等)是我国一种重要的沉积型
2 3 2 3 2
铁矿资源,以高磷鲕状赤铁矿为原料制备纯度较高的铁红,其流程如图所示。下列说法错误
的是( )
A.铁红可用作油漆、油墨、建筑物的着色剂
B.酸浸液遇K[Fe(CN) ]溶液生成蓝色沉淀
3 6
C.洗涤滤渣时要用玻璃棒不断搅拌
D.氧化时选用的试剂可以是HO、NaClO溶液
2 2
答案 C
解析 铁红的主要成分是氧化铁,为红棕色,可用作油漆、油墨、建筑物的着色剂,A项正
确;酸浸液中含有 Fe2+,遇 K[Fe(CN) ]溶液生成蓝色沉淀,B 项正确;氧化时可选用
3 6
HO 、NaClO溶液作为氧化剂,将Fe2+氧化为Fe3+,反应原理分别为2Fe2++HO +2H+
2 2 2 2
===2Fe3++2HO、2Fe2++ClO-+2H+===2Fe3++Cl-+HO,D项正确。
2 2
2.从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯化铁晶体的流程如下,则下
2 3 2
列说法正确的是( )A.试剂a是铁、试剂b是稀硫酸
B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C.试剂c是氯气,相应的反应为2Fe2++Cl===2Cl-+2Fe3+
2
D.用酸性KMnO 溶液可检验溶液W中是否还有Fe2+
4
答案 C
解析 试剂a是铁,加入过量的铁,可把铜全部置换出来,并把FeCl 还原为FeCl ,则通过
3 2
过滤操作Ⅰ得到的滤液X为FeCl 溶液,滤渣Y为铜和过量的铁;由于最终得到的产品是
2
FeCl ,故试剂b是稀盐酸,铜不与盐酸反应,铁与盐酸反应生成FeCl ,故通过过滤操作Ⅱ
3 2
可得到铜单质,滤液Z为FeCl 溶液,在两次过滤得到的FeCl 溶液中通入氯气,发生反应:
2 2
2Fe2++Cl===2Cl-+2Fe3+,把FeCl 转化为FeCl ,然后通过操作Ⅲ(蒸发结晶并过滤)便可
2 2 3
得到氯化铁晶体,蒸发结晶与过滤所使用的仪器不相同,故A、B错误,C正确;溶液W中
有Cl-,酸性KMnO 溶液既可氧化Fe2+,又可氧化Cl-,故用酸性KMnO 溶液不可检验溶
4 4
液W中是否还有Fe2+,D错误。
3.高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,
2 4
微溶于浓KOH溶液,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高
3
铁酸钾有强氧化性,酸性条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的
2 4 2 4
流程如下:
下列关于KFeO 的说法正确的是( )
2 4
A.与水反应,每消耗1 mol K FeO 转移6 mol电子
2 4
B.将KFeO 与盐酸混合使用,可增强其杀菌消毒效果
2 4
C.可用丁达尔效应鉴别KFeO 和KMnO 两种紫红色溶液
2 4 4
D.KFeO 中,基态K+的核外三个电子能层均充满电子
2 4
答案 C
解析 KFeO 与水反应:4KFeO +10HO===3O↑+4Fe(OH) (胶体)+8KOH,由反应可知
2 4 2 4 2 2 3
每消耗4 mol K FeO 转移12 mol电子,则每消耗1 mol K FeO 转移3 mol电子,故A错误;
2 4 2 4
KFeO 有强氧化性,酸性条件下,其氧化性强于Cl,可知KFeO 与盐酸反应生成氯气,两
2 4 2 2 4者混合降低其杀菌消毒效果,故B错误;KFeO 能与水反应生成Fe(OH) 胶体,而高锰酸钾
2 4 3
溶于水形成的是溶液,可用丁达尔效应鉴别KFeO 和KMnO 两种紫红色溶液,故C正确;
2 4 4
K+的核外电子排布为2、8、8,第三层未充满电子,故D错误。
4.(2022·济宁一模)以黄铁矿的烧渣(主要成分为Fe O 、FeO、SiO 等)为原料制取新型高效
2 3 2
的无机高分子絮凝剂——聚合硫酸铁 (其中n<2)的工艺流程如图:
已知:为防止Fe3+水解,原料中的Fe3+必须先还原为Fe2+。
下列有关说法错误的是( )
A.“取样分析”目的是可以用来确定氧化Fe2+所需NaClO 的量
3
B.为促进水解反应,应在高温条件下进行
C.氧化反应的离子方程式为ClO+6H++6Fe2+===6Fe3++Cl-+3HO
2
D.水解时溶液的pH偏小或偏大都会影响聚合硫酸铁的产率
答案 B
解析 因为要控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的 Fe3+必须先还原
为Fe2+,所以需要确定下一步还原所需铁的量,然后Fe2+再被氧化为Fe3+,需要确定氧化
Fe2+所需NaClO 的量,A正确;该流程中要得到 ,若温度过高,则
3
将转化为Fe(OH) 沉淀,使得产物不纯,故应该控制反应温度,B错误;从流程中可知,进
3
入氧化反应的是Fe2+,即NaClO 将Fe2+氧化为Fe3+,故氧化反应的离子方程式为ClO+
3
6H++6Fe2+===6Fe3++Cl-+3HO,C正确;水解时溶液的pH偏小将使大部分Fe3+不能水
2
解仍然以Fe3+存在,而pH偏大将生成Fe(OH) 沉淀,故都会影响聚合硫酸铁的产率,D正
3
确。
5.(2022·北京一模)磷酸铁(FePO )常用作电极材料。以硫铁矿(主要成分是FeS ,含少量
4 2
Al O、SiO 和Fe O)为原料制备磷酸铁的流程如下:
2 3 2 3 4
已知几种金属离子沉淀的pH如下表所示:金属氢氧化物 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀的pH 2.3 7.5 4.0
完全沉淀的pH 4.1 9.7 5.2
请回答下列问题:
(1)滤渣3的主要成分是________(写出化学式)。
(2)用FeS还原Fe3+的目的是__________________________________________________,
加入FeO的作用是________________________________________(用离子方程式表示)。
(3)试剂R宜选择________(填字母)。
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)检验“氧化”之后溶液是否含Fe2+的操作是_________________________________。
答案 (1)Al(OH)
3
(2)避免在除去Al3+时Fe3+被一并沉淀 Al3++3HOAl(OH) +3H+、FeO+2H+===Fe2+
2 3
+HO(或2Al3++3FeO+3HO===2Al(OH) +3Fe2+)
2 2 3
(3) C
(4)取少量待测液于试管中,滴加几滴铁氰化钾溶液(或酸性高锰酸钾溶液),若产生蓝色沉淀
(或酸性高锰酸钾溶液褪色),则该溶液中含有Fe2+
解析 硫铁矿中含有的物质是FeS 、Al O 、SiO 、Fe O ,焙烧时FeS 转化成Fe O ,Fe O
2 2 3 2 3 4 2 2 3 2 3
为碱性氧化物,Al O 为两性氧化物,SiO 为酸性氧化物,能与稀硫酸反应的是 Fe O 、
2 3 2 2 3
Al O 、Fe O ,SiO 不与硫酸反应,滤渣1为SiO ,滤液中阳离子是Fe3+、Al3+、Fe2+、H+
2 3 3 4 2 2
等,加入FeS将Fe3+还原成Fe2+,加入FeO调节pH,使Al3+转化成Al(OH) 沉淀,除去Al3
3
+,然后加入氧化剂,将Fe2+氧化成Fe3+,据此分析。(3)KMnO 作氧化剂,引入新杂质Mn2
4
+、
K+,故A不适宜;稀硝酸作氧化剂,得到NO,NO有毒,污染环境,且容易引入硝酸根离
子成为新杂质,故B不适宜;双氧水作氧化剂,还原产物是HO,不引入杂质,对环境无影
2
响,故C适宜;次氯酸钠作氧化剂,引入新杂质Cl-、Na+,故D不适宜。
6.某化学小组用部分氧化的FeSO 为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧
4
化铁(Fe O),并进行铁含量的测定。主要操作步骤如下:
2 3
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合
物解离。②3DDTC-NH+Fe3+===(DDTC) -Fe↓+3NH。
4 3
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式:________________________________________。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏
斗的______________放气;为提高萃取率和产品产量,实验时应进行的操作是
______________。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)________。
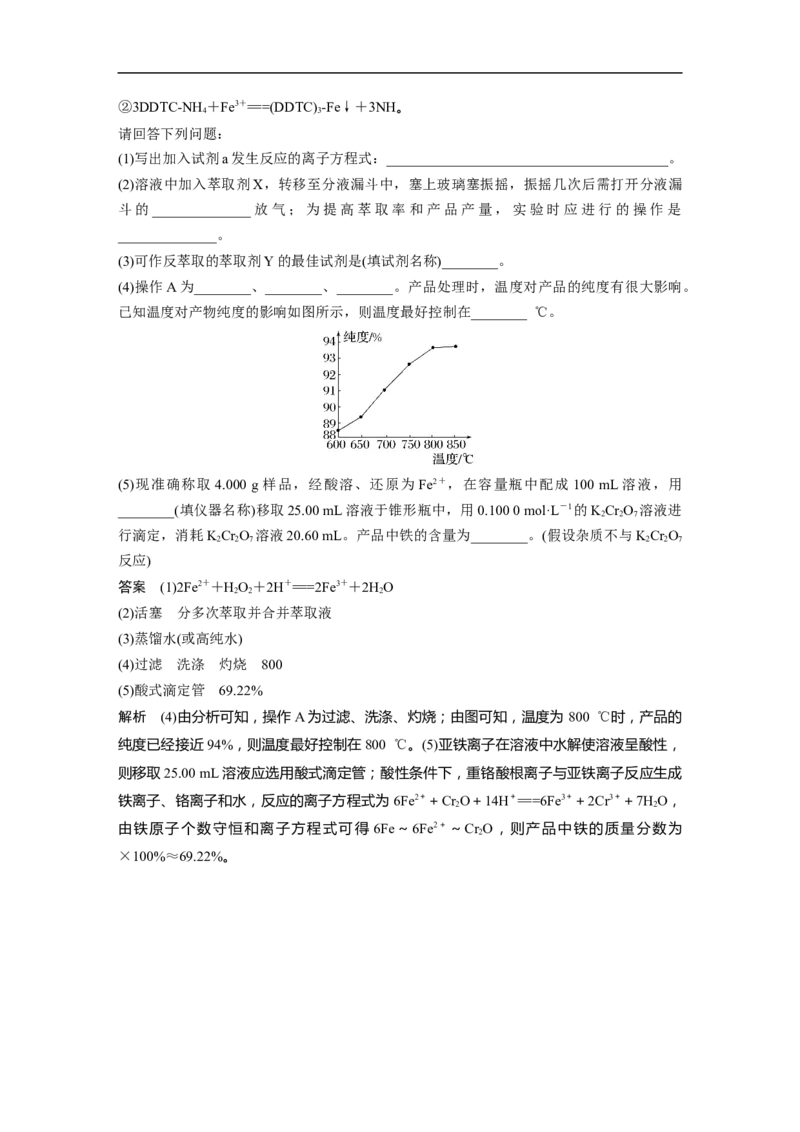
(4)操作A为________、________、________。产品处理时,温度对产品的纯度有很大影响。
已知温度对产物纯度的影响如图所示,则温度最好控制在________ ℃。
(5)现准确称取4.000 g 样品,经酸溶、还原为 Fe2+,在容量瓶中配成100 mL 溶液,用
________(填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.100 0 mol·L-1的KCr O 溶液进
2 2 7
行滴定,消耗KCr O 溶液20.60 mL。产品中铁的含量为________。(假设杂质不与KCr O
2 2 7 2 2 7
反应)
答案 (1)2Fe2++HO+2H+===2Fe3++2HO
2 2 2
(2)活塞 分多次萃取并合并萃取液
(3)蒸馏水(或高纯水)
(4)过滤 洗涤 灼烧 800
(5)酸式滴定管 69.22%
解析 (4)由分析可知,操作A为过滤、洗涤、灼烧;由图可知,温度为 800 ℃时,产品的
纯度已经接近94%,则温度最好控制在800 ℃。(5)亚铁离子在溶液中水解使溶液呈酸性,
则移取25.00 mL溶液应选用酸式滴定管;酸性条件下,重铬酸根离子与亚铁离子反应生成
铁离子、铬离子和水,反应的离子方程式为 6Fe2++Cr O+14H+===6Fe3++2Cr3++7HO,
2 2
由铁原子个数守恒和离子方程式可得 6Fe~6Fe2+~Cr O,则产品中铁的质量分数为
2
×100%≈69.22%。