文档内容
1.(2022·全国甲卷,35)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为
“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH==CH)与四氟
2 2
乙烯(CF==CF)的共聚物(ETFE)制成。回答下列问题:
2 2
(1)基态F原子的价电子排布图(轨道表示式)为__________。
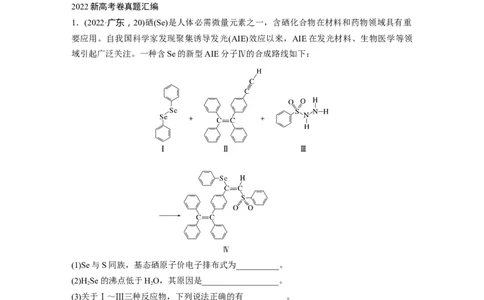
(2)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电
离能的变化图是__________(填标号),判断的根据是__________;第三电离能的变化图是
__________(填标号)。
(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构__________。
n 3
(4)CF ==CF 和ETFE分子中C的杂化轨道类型分别为__________和________;聚四氟乙烯
2 2
的化学稳定性高于聚乙烯,从化学键的角度解释原因__________________________________。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X 代表的离子是
2
__________;若该立方晶胞参数为a pm,正负离子的核间距最小为__________pm。
答案 (1) (2)图a 同一周期第一电离能从左向右有增大的趋势,但
由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高 图b
(3) (4)sp2 sp3 C—F的键能大于聚乙烯中C—H的键能,键能越大,化
学性质越稳定 (5)Ca2+ a解析 (1)F 为第 9 号元素,其电子排布式为 1s22s22p5,则其价电子排布图为
。(2)C、N、O、F四种元素在同一周期,同一周期第一电离能从左向右有增
大的趋势,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种
元素高,因此C、N、O、F四种元素的第一电离能从小到大的顺序为C一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,
形成的C—Cl越强 (3)CsCl CsCl为离子晶体,ICl为分子晶体 (4)电解质
解析 (1)F的原子序数为9,其基态原子电子排布式为1s22s22p5,1s22s22p43s1为基态氟原子2p
能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;1s22s22p43d2,核外共有
10个电子,不是氟原子,b错误;1s22s12p5,核外共有8个电子,不是氟原子,c错误;
1s22s22p33p2为基态氟原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d
正确;同一原子3p能级的能量比3s能级的能量高,因此能量较高的是 1s22s22p33p2。(2)①
一氯乙烯的结构式为 ,碳原子采取sp2杂化,因此C的一个sp2杂化轨道与Cl的
3p 轨道形成C—Cl σ键。②C的杂化轨道中s成分越多,形成的C—Cl越强,C—Cl的键长
x
越短,一氯乙烷中碳采取sp3杂化,一氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,
sp杂化时s成分多,sp3杂化时s成分少,同时Cl参与形成的大π键越多,形成的C—Cl的
键长越短,一氯乙烯中Cl的3p轨道与C的2p轨道形成3中心4电子的大π键(Π),一氯乙
炔中Cl的3p轨道与C的2p轨道形成2个3中心4电子的大π键(Π),因此三种物质中C—
Cl键长的顺序为一氯乙烷>一氯乙烯>一氯乙炔。(3)CsICl 发生非氧化还原反应,各元素化
2
合价不变,生成无色晶体和红棕色液体,则无色晶体为 CsCl,红棕色液体为ICl,而CsCl
为离子晶体,熔化时克服的是离子键,ICl为分子晶体,熔化时克服的是分子间作用力,因
此CsCl的熔点比ICl高。(4)由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发
生迁移,因此α-AgI晶体是优良的离子导体,在电池中可作为电解质;每个晶胞中含碘离子
的个数为8×+1=2个,依据化学式AgI可知,银离子个数也为2个,晶胞的物质的量n=
mol= mol,晶胞体积V=a3 pm3=(504×10-12)3 m3,则α-AgI晶体的摩尔体积V ===
m
m3·mol-1。
物质结构与性质综合题为“拼盘”命制的题型,各小题之间相对独立,重点考查考生对
基础知识的掌握情况,主要考查原子结构与性质、分子结构与性质、晶体结构与性质。①在
原子结构部分主要命题点有电子排布式或电子排布图的书写,电离能、电负性大小、微粒半
径的比较与判断。②在分子结构部分主要命题点有化学键类型的判断,空间结构的判断,中心原子杂化方式的判断,能从化学键角度认识分子的结构、性质,从宏观和微观相结合的视
角分析与解决实际问题。③在晶体结构部分主要命题点有晶体类型的判断,晶体结构的计算
等。
试题有“三种”呈现形式:①以一种已知的元素立题,选取与其相关的某些典型单质或
化合物展开设问,综合考查原子结构、分子结构和晶体结构。②以几种已知的元素立题,依
托不同元素的物质分别独立或侧重考查原子结构、分子结构和晶体结构。③以推断出的几种
元素立题,依托它们之间组成的物质综合考査原子结构、分子结构和晶体结构。
2022新高考卷真题汇编
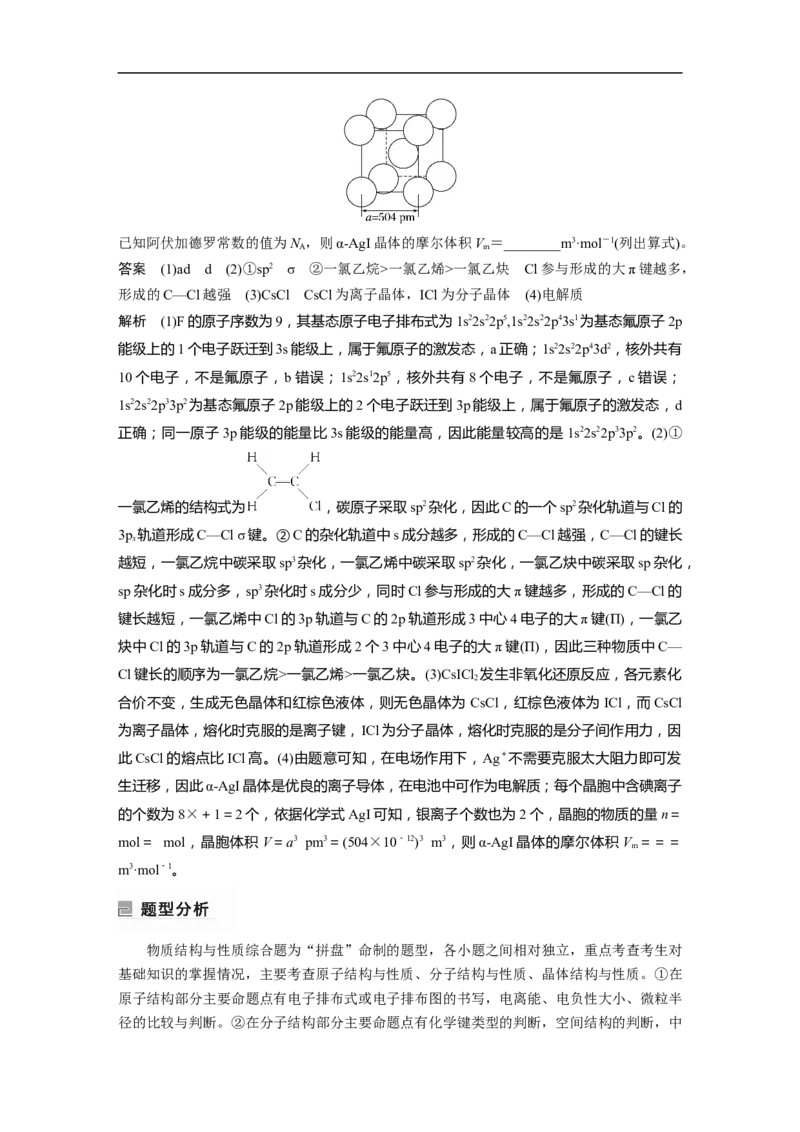
1.(2022·广东,20)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重
要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领
域引起广泛关注。一种含Se的新型AIE分子Ⅳ的合成路线如下:
(1)Se与S同族,基态硒原子价电子排布式为__________。
(2)H Se的沸点低于HO,其原因是__________________。
2 2
(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有__________。
A.Ⅰ中仅有σ键
B.Ⅰ中的Se—Se为非极性共价键
C.Ⅱ易溶于水
D.Ⅱ中原子的杂化轨道类型只有sp与sp2
E.Ⅰ~Ⅲ含有的元素中,O电负性最大
(4)Ⅳ中具有孤电子对的原子有__________。
(5)硒的两种含氧酸的酸性强弱为HSeO______(填“>”或“<”)H SeO 。研究发现,给小
2 4 2 3
鼠喂食适量硒酸钠(Na SeO)可减轻重金属铊引起的中毒。SeO的空间结构为________。
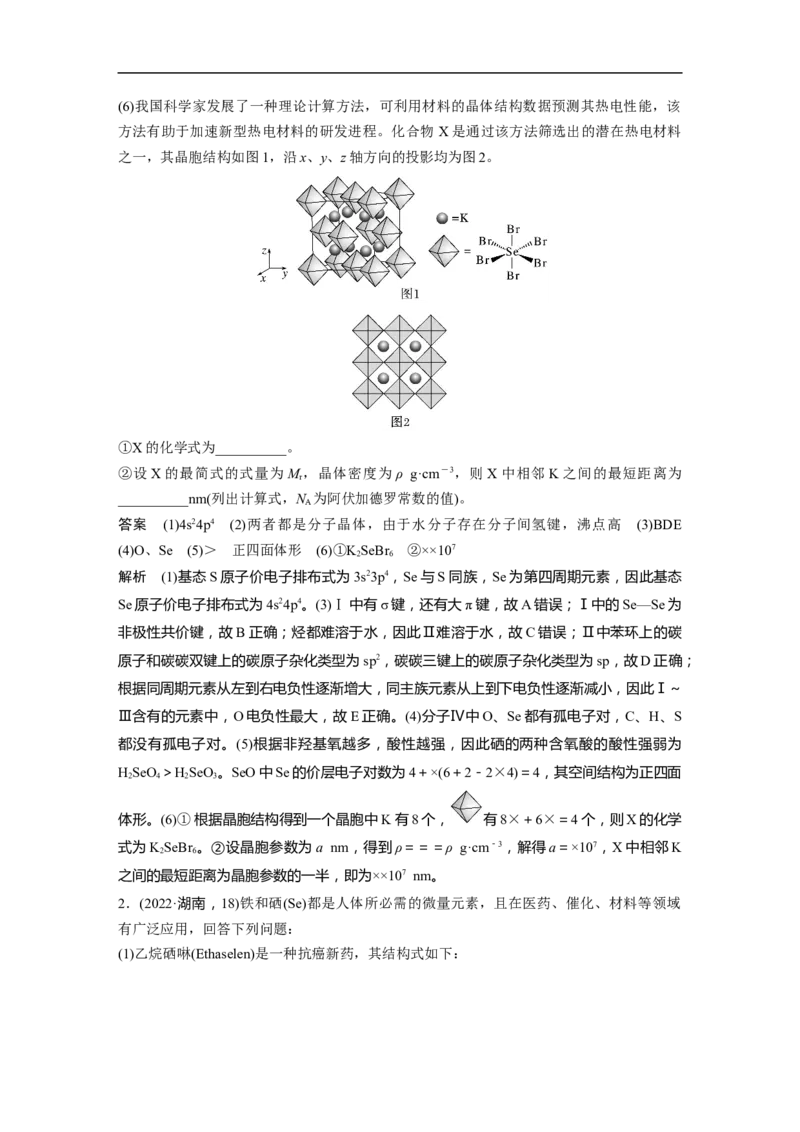
2 4(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该
方法有助于加速新型热电材料的研发进程。化合物 X是通过该方法筛选出的潜在热电材料
之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
①X的化学式为__________。
②设X的最简式的式量为 M,晶体密度为ρ g·cm-3,则X中相邻K之间的最短距离为
r
__________nm(列出计算式,N 为阿伏加德罗常数的值)。
A
答案 (1)4s24p4 (2)两者都是分子晶体,由于水分子存在分子间氢键,沸点高 (3)BDE
(4)O、Se (5)> 正四面体形 (6)①KSeBr ②××107
2 6
解析 (1)基态S原子价电子排布式为3s23p4,Se与S同族,Se为第四周期元素,因此基态
Se原子价电子排布式为4s24p4。(3)Ⅰ中有σ键,还有大π键,故A错误;Ⅰ中的Se—Se为
非极性共价键,故B正确;烃都难溶于水,因此Ⅱ难溶于水,故C错误;Ⅱ中苯环上的碳
原子和碳碳双键上的碳原子杂化类型为sp2,碳碳三键上的碳原子杂化类型为sp,故D正确;
根据同周期元素从左到右电负性逐渐增大,同主族元素从上到下电负性逐渐减小,因此Ⅰ~
Ⅲ含有的元素中,O电负性最大,故E正确。(4)分子Ⅳ中O、Se都有孤电子对,C、H、S
都没有孤电子对。(5)根据非羟基氧越多,酸性越强,因此硒的两种含氧酸的酸性强弱为
HSeO >HSeO 。SeO中Se的价层电子对数为4+×(6+2-2×4)=4,其空间结构为正四面
2 4 2 3
体形。(6)①根据晶胞结构得到一个晶胞中K有8个, 有8×+6×=4个,则X的化学
式为KSeBr 。②设晶胞参数为a nm,得到ρ===ρ g·cm-3,解得a=×107,X中相邻K
2 6
之间的最短距离为晶胞参数的一半,即为××107 nm。
2.(2022·湖南,18)铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域
有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:①基态Se原子的核外电子排布式为[Ar]__________。
②该新药分子中有__________种不同化学环境的C原子。
③比较键角大小:气态 SeO 分子________SeO 离子(填“>”“<”或“=”),原因是
3
_____________________________________________________________________________。
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中σ键与π键的数目比为________________________________。
②富马酸亚铁中各元素的电负性由大到小的顺序为__________。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H ,将N3-
2
转化为NH,反应过程如图所示:
①产物中N原子的杂化轨道类型为_________________。
②与NH互为等电子体的一种分子为__________(填化学式)。
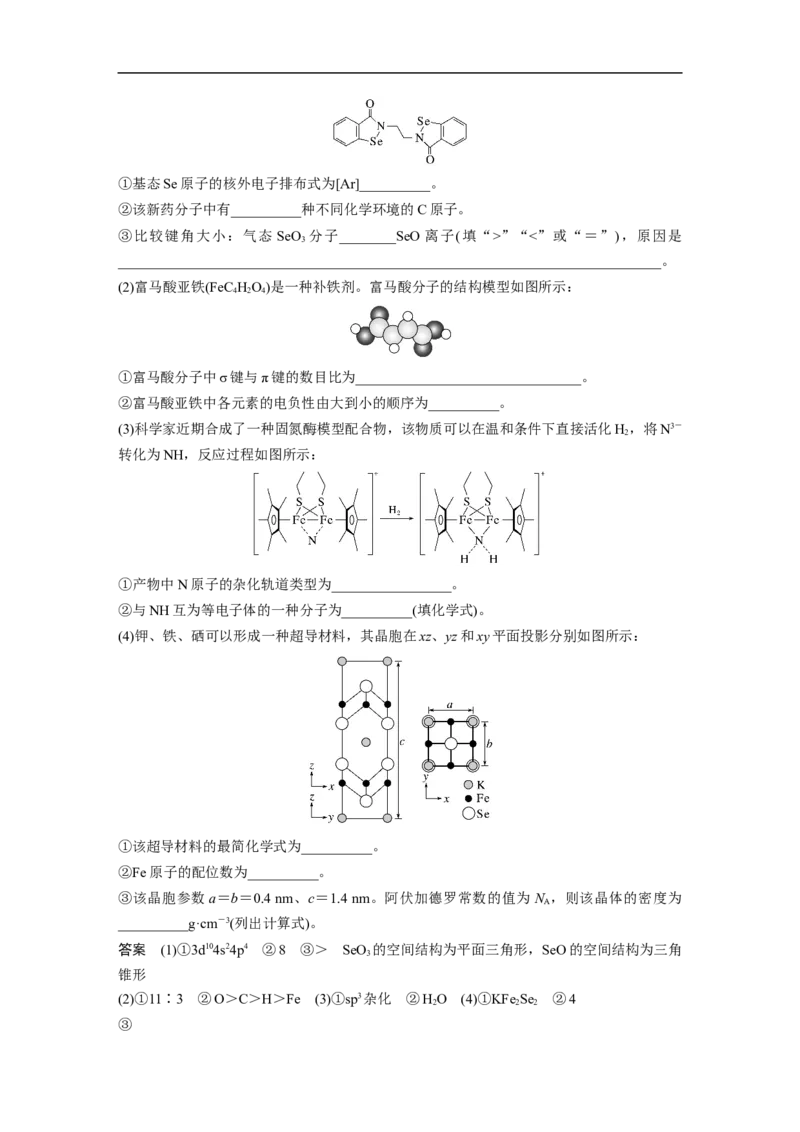
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为__________。
②Fe原子的配位数为__________。
③该晶胞参数a=b=0.4 nm、c=1.4 nm。阿伏加德罗常数的值为N ,则该晶体的密度为
A
__________g·cm-3(列出计算式)。
答案 (1)①3d104s24p4 ②8 ③> SeO 的空间结构为平面三角形,SeO的空间结构为三角
3
锥形
(2)①11∶3 ②O>C>H>Fe (3)①sp3杂化 ②HO (4)①KFe Se ②4
2 2 2
③解析 (1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar]3d104s24p4。
②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有8种不同化学环境的碳原子。
③三氧化硒分子中硒原子的价层电子对数为3,孤电子对数为0,分子的空间结构为平面三
角形,键角为120°,亚硒酸根离子中硒原子的价层电子对数为4,孤电子对数为1,离子的
空间结构为三角锥形,键角小于 120°。(2)① 由结构模型可知,富马酸的结构简式为
HOOCCH==CHCOOH,分子中的单键为σ键,双键中含有1个σ键和1个π键,则分子中σ
键和π键的数目比为11∶3。②金属元素的电负性小于非金属元素,则铁元素的电负性最小,
非金属元素的非金属性越强,电负性越大,氢、碳、氧的非金属性依次增强,则电负性依次
增大,所以富马酸亚铁中四种元素的电负性由大到小的顺序为 O>C>H>Fe。(3)①由结构
简式可知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化。②水分子和氨
基阴离子的原子个数都为3、价电子数都为8,互为等电子体。(4)①由平面投影图可知,晶
胞中位于顶点和体心的钾原子个数为8×+1=2,均位于棱上和体内的硒原子的个数为8×
+2=4,均位于面上的铁原子个数为8×=4,该物质的晶胞结构如图所示: ,
则超导材料的最简化学式为KFe Se 。②由平面投影图可知,铁原子的配位数为4。③设晶
2 2
体的密度为d g·cm-3,由晶胞的质量公式可得: g=abc×10-21×d g,解得d= g·cm-3。
3.(2022·北京,15)FeSO ·7H O失水后可转为FeSO ·H O,与FeS 可联合制备铁粉精(FeO)
4 2 4 2 2 x y
和HSO 。
2 4
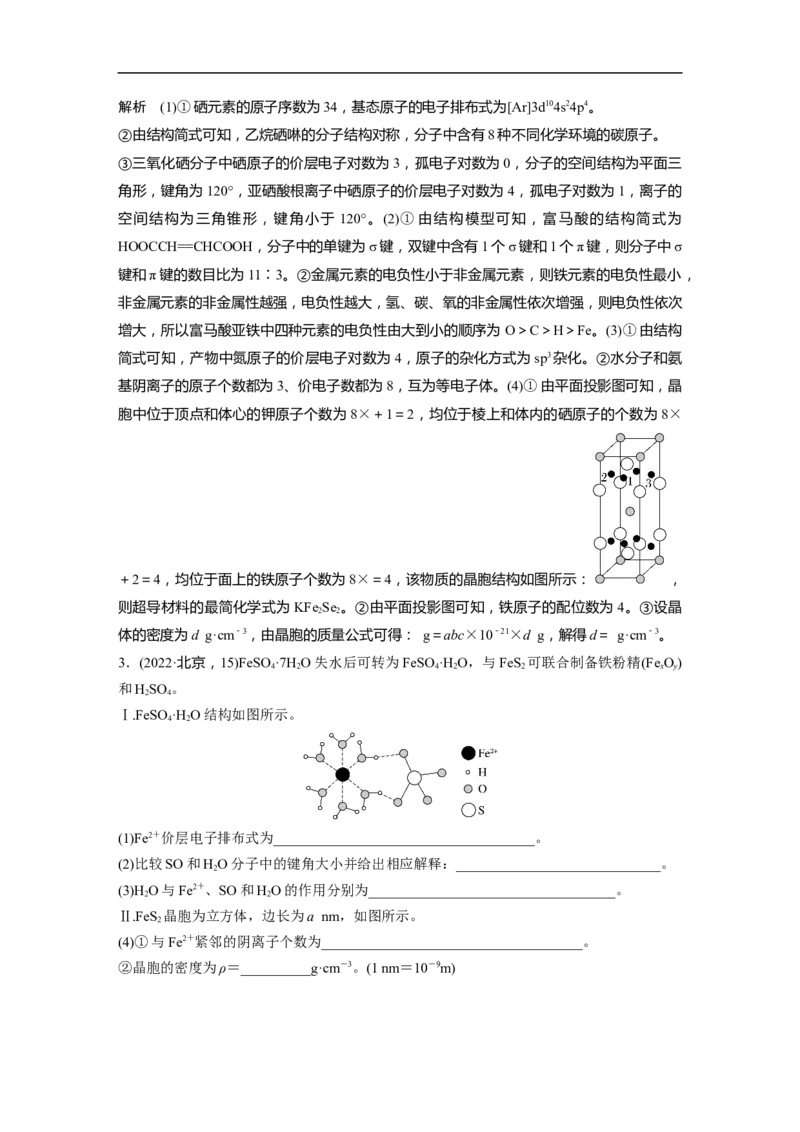
Ⅰ.FeSO·H O结构如图所示。
4 2
(1)Fe2+价层电子排布式为_____________________________________。
(2)比较SO和HO分子中的键角大小并给出相应解释:_____________________________。
2
(3)H O与Fe2+、SO和HO的作用分别为___________________________________。
2 2
Ⅱ.FeS 晶胞为立方体,边长为a nm,如图所示。
2
(4)①与Fe2+紧邻的阴离子个数为_____________________________________。
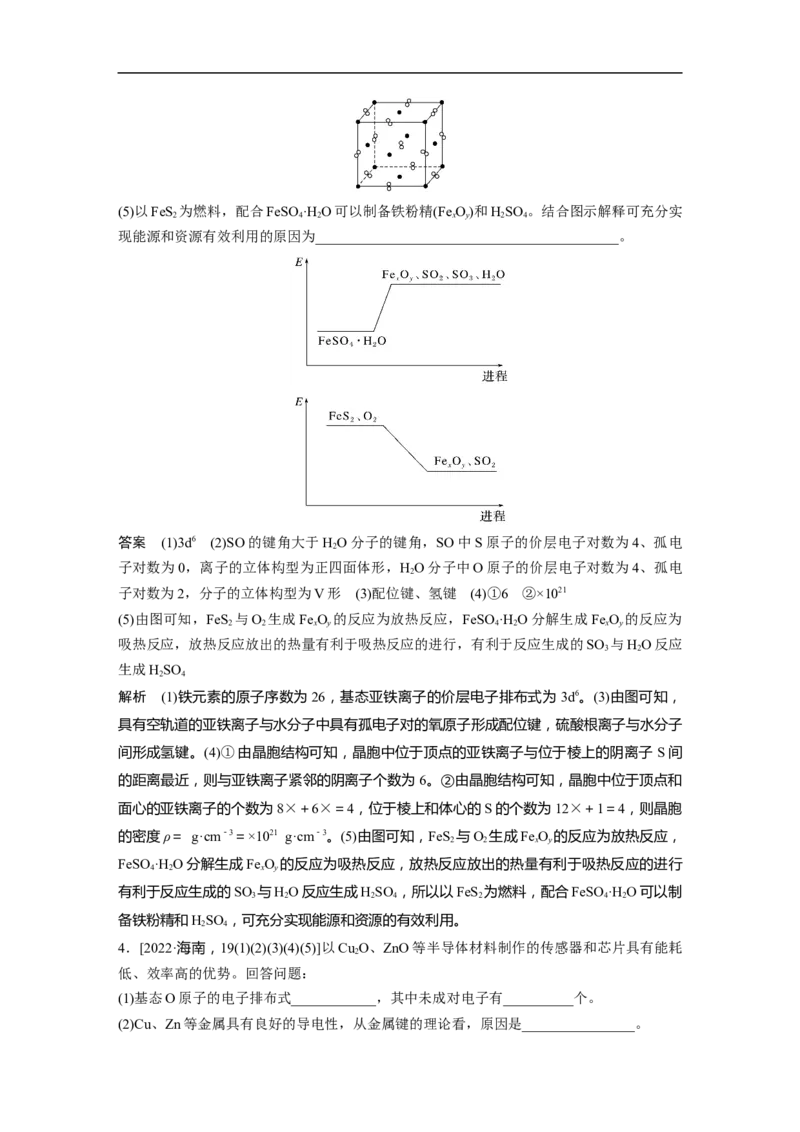
②晶胞的密度为ρ=__________g·cm-3。(1 nm=10-9m)(5)以FeS 为燃料,配合FeSO ·H O可以制备铁粉精(FeO)和HSO 。结合图示解释可充分实
2 4 2 x y 2 4
现能源和资源有效利用的原因为___________________________________________。
答案 (1)3d6 (2)SO的键角大于HO分子的键角,SO中S原子的价层电子对数为4、孤电
2
子对数为0,离子的立体构型为正四面体形,HO分子中O原子的价层电子对数为4、孤电
2
子对数为2,分子的立体构型为V形 (3)配位键、氢键 (4)①6 ②×1021
(5)由图可知,FeS 与O 生成FeO 的反应为放热反应,FeSO ·H O分解生成FeO 的反应为
2 2 x y 4 2 x y
吸热反应,放热反应放出的热量有利于吸热反应的进行,有利于反应生成的SO 与HO反应
3 2
生成HSO
2 4
解析 (1)铁元素的原子序数为26,基态亚铁离子的价层电子排布式为3d6。(3)由图可知,
具有空轨道的亚铁离子与水分子中具有孤电子对的氧原子形成配位键,硫酸根离子与水分子
间形成氢键。(4)①由晶胞结构可知,晶胞中位于顶点的亚铁离子与位于棱上的阴离子 S间
的距离最近,则与亚铁离子紧邻的阴离子个数为6。②由晶胞结构可知,晶胞中位于顶点和
面心的亚铁离子的个数为8×+6×=4,位于棱上和体心的S的个数为12×+1=4,则晶胞
的密度ρ= g·cm-3=×1021 g·cm-3。(5)由图可知,FeS 与O 生成FeO 的反应为放热反应,
2 2 x y
FeSO ·H O分解生成FeO 的反应为吸热反应,放热反应放出的热量有利于吸热反应的进行
4 2 x y
有利于反应生成的SO 与HO反应生成HSO ,所以以FeS 为燃料,配合FeSO ·H O可以制
3 2 2 4 2 4 2
备铁粉精和HSO ,可充分实现能源和资源的有效利用。
2 4
4.[2022·海南,19(1)(2)(3)(4)(5)]以Cu O、ZnO等半导体材料制作的传感器和芯片具有能耗
2
低、效率高的优势。回答问题:
(1)基态O原子的电子排布式____________,其中未成对电子有__________个。
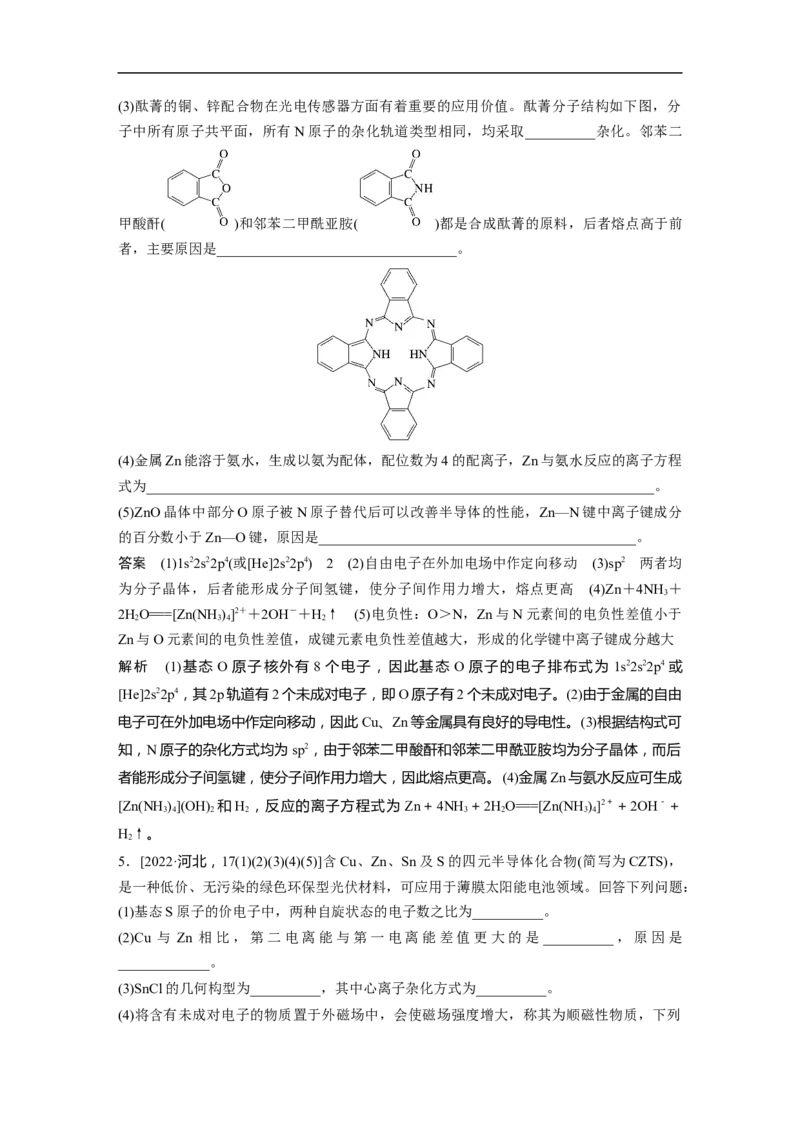
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是________________。(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分
子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取__________杂化。邻苯二
甲酸酐( )和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前
者,主要原因是__________________________________。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程
式为________________________________________________________________________。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn—N键中离子键成分
的百分数小于Zn—O键,原因是_____________________________________________。
答案 (1)1s22s22p4(或[He]2s22p4) 2 (2)自由电子在外加电场中作定向移动 (3)sp2 两者均
为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高 (4)Zn+4NH +
3
2HO===[Zn(NH )]2++2OH-+H↑ (5)电负性:O>N,Zn与N元素间的电负性差值小于
2 3 4 2
Zn与O元素间的电负性差值,成键元素电负性差值越大,形成的化学键中离子键成分越大
解析 (1)基态 O 原子核外有 8 个电子,因此基态 O 原子的电子排布式为 1s22s22p4或
[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子。(2)由于金属的自由
电子可在外加电场中作定向移动,因此Cu、Zn等金属具有良好的导电性。(3)根据结构式可
知,N原子的杂化方式均为sp2,由于邻苯二甲酸酐和邻苯二甲酰亚胺均为分子晶体,而后
者能形成分子间氢键,使分子间作用力增大,因此熔点更高。(4)金属Zn与氨水反应可生成
[Zn(NH )](OH) 和H ,反应的离子方程式为 Zn+4NH +2HO===[Zn(NH )]2++2OH-+
3 4 2 2 3 2 3 4
H↑。
2
5.[2022·河北,17(1)(2)(3)(4)(5)]含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),
是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为__________。
(2)Cu 与 Zn 相比,第二电离能与第一电离能差值更大的是__________,原因是
_____________。
(3)SnCl的几何构型为__________,其中心离子杂化方式为__________。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是____________(填字母)。
A.Cl B.SO
4
C.SO D.Na
4 2
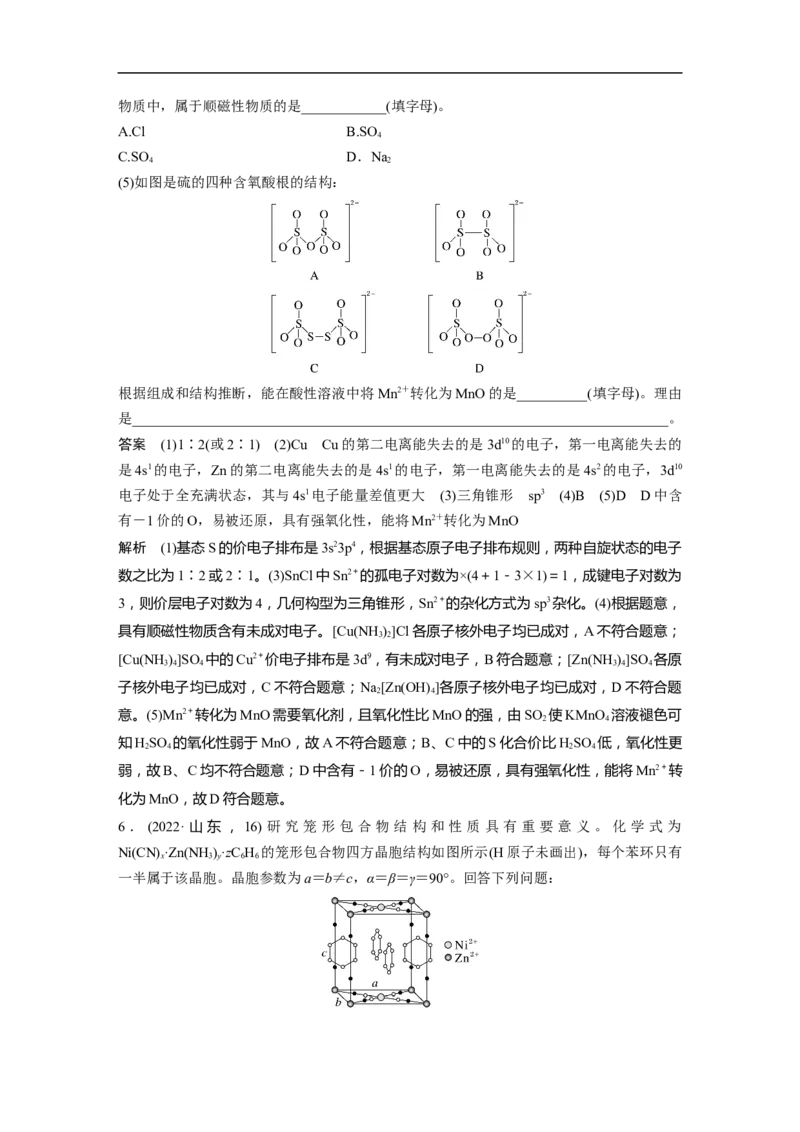
(5)如图是硫的四种含氧酸根的结构:
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO的是__________(填字母)。理由
是____________________________________________________________________________。
答案 (1)1∶2(或2∶1) (2)Cu Cu的第二电离能失去的是3d10的电子,第一电离能失去的
是4s1的电子,Zn的第二电离能失去的是4s1的电子,第一电离能失去的是4s2的电子,3d10
电子处于全充满状态,其与4s1电子能量差值更大 (3)三角锥形 sp3 (4)B (5)D D中含
有-1价的O,易被还原,具有强氧化性,能将Mn2+转化为MnO
解析 (1)基态S的价电子排布是3s23p4,根据基态原子电子排布规则,两种自旋状态的电子
数之比为1∶2或2∶1。(3)SnCl中Sn2+的孤电子对数为×(4+1-3×1)=1,成键电子对数为
3,则价层电子对数为4,几何构型为三角锥形,Sn2+的杂化方式为sp3杂化。(4)根据题意,
具有顺磁性物质含有未成对电子。[Cu(NH )]Cl各原子核外电子均已成对,A不符合题意;
3 2
[Cu(NH )]SO 中的Cu2+价电子排布是3d9,有未成对电子,B符合题意;[Zn(NH )]SO 各原
3 4 4 3 4 4
子核外电子均已成对,C不符合题意;Na[Zn(OH) ]各原子核外电子均已成对,D不符合题
2 4
意。(5)Mn2+转化为MnO需要氧化剂,且氧化性比MnO的强,由SO 使KMnO 溶液褪色可
2 4
知HSO 的氧化性弱于MnO,故A不符合题意;B、C中的S化合价比HSO 低,氧化性更
2 4 2 4
弱,故B、C均不符合题意;D中含有-1价的O,易被还原,具有强氧化性,能将Mn2+转
化为MnO,故D符合题意。
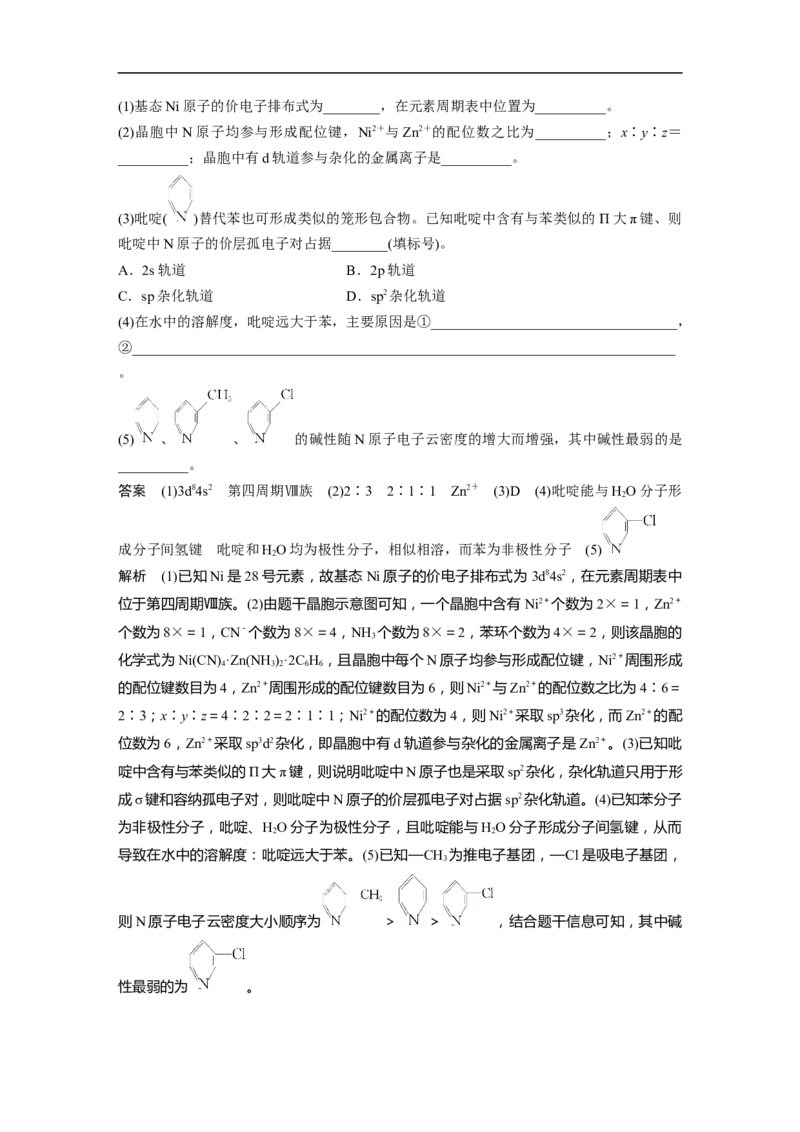
6 . (2022· 山 东 , 16) 研 究 笼 形 包 合 物 结 构 和 性 质 具 有 重 要 意 义 。 化 学 式 为
Ni(CN)·Zn(NH )·zC H 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有
x 3 y 6 6
一半属于该晶胞。晶胞参数为a=b≠c,α=β=γ=90°。回答下列问题:(1)基态Ni原子的价电子排布式为________,在元素周期表中位置为__________。
(2)晶胞中N原子均参与形成配位键,Ni2+与Zn2+的配位数之比为__________;x∶y∶z=
__________;晶胞中有d轨道参与杂化的金属离子是__________。
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 Π大π键、则
吡啶中N原子的价层孤电子对占据________(填标号)。
A.2s轨道 B.2p轨道
C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①___________________________________,
②_____________________________________________________________________________
。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
__________。
答案 (1)3d84s2 第四周期Ⅷ族 (2)2∶3 2∶1∶1 Zn2+ (3)D (4)吡啶能与HO分子形
2
成分子间氢键 吡啶和HO均为极性分子,相似相溶,而苯为非极性分子 (5)
2
解析 (1)已知Ni是28号元素,故基态Ni原子的价电子排布式为3d84s2,在元素周期表中
位于第四周期Ⅷ族。(2)由题干晶胞示意图可知,一个晶胞中含有Ni2+个数为2×=1,Zn2+
个数为8×=1,CN-个数为8×=4,NH 个数为8×=2,苯环个数为4×=2,则该晶胞的
3
化学式为Ni(CN) ·Zn(NH )·2C H ,且晶胞中每个N原子均参与形成配位键,Ni2+周围形成
4 3 2 6 6
的配位键数目为4,Zn2+周围形成的配位键数目为6,则Ni2+与Zn2+的配位数之比为4∶6=
2∶3;x∶y∶z=4∶2∶2=2∶1∶1;Ni2+的配位数为4,则Ni2+采取sp3杂化,而Zn2+的配
位数为6,Zn2+采取sp3d2杂化,即晶胞中有d轨道参与杂化的金属离子是Zn2+。(3)已知吡
啶中含有与苯类似的Π大π键,则说明吡啶中N原子也是采取sp2杂化,杂化轨道只用于形
成σ键和容纳孤电子对,则吡啶中N原子的价层孤电子对占据sp2杂化轨道。(4)已知苯分子
为非极性分子,吡啶、HO分子为极性分子,且吡啶能与HO分子形成分子间氢键,从而
2 2
导致在水中的溶解度:吡啶远大于苯。(5)已知—CH 为推电子基团,—Cl是吸电子基团,
3
则N原子电子云密度大小顺序为 > > ,结合题干信息可知,其中碱
性最弱的为 。专题强化练
1.(2022·吉林延边一模)铜是人类广泛使用的一种金属,含铜物质在生产、生活中有着广泛
应用。回答下列问题:
(1)铜锰氧化物(CuMn O)能在常温下催化氧化一氧化碳和甲醛(HCHO)。
2 4
①基态Cu原子的M层电子排布式为____________________________。
②CO和N 互为等电子体。标准状况下V L CO分子中π键数目为__________。
2
(2)钙铜合金可用作电解法制备金属钙的阴极电极材料。钙在元素周期表中位于
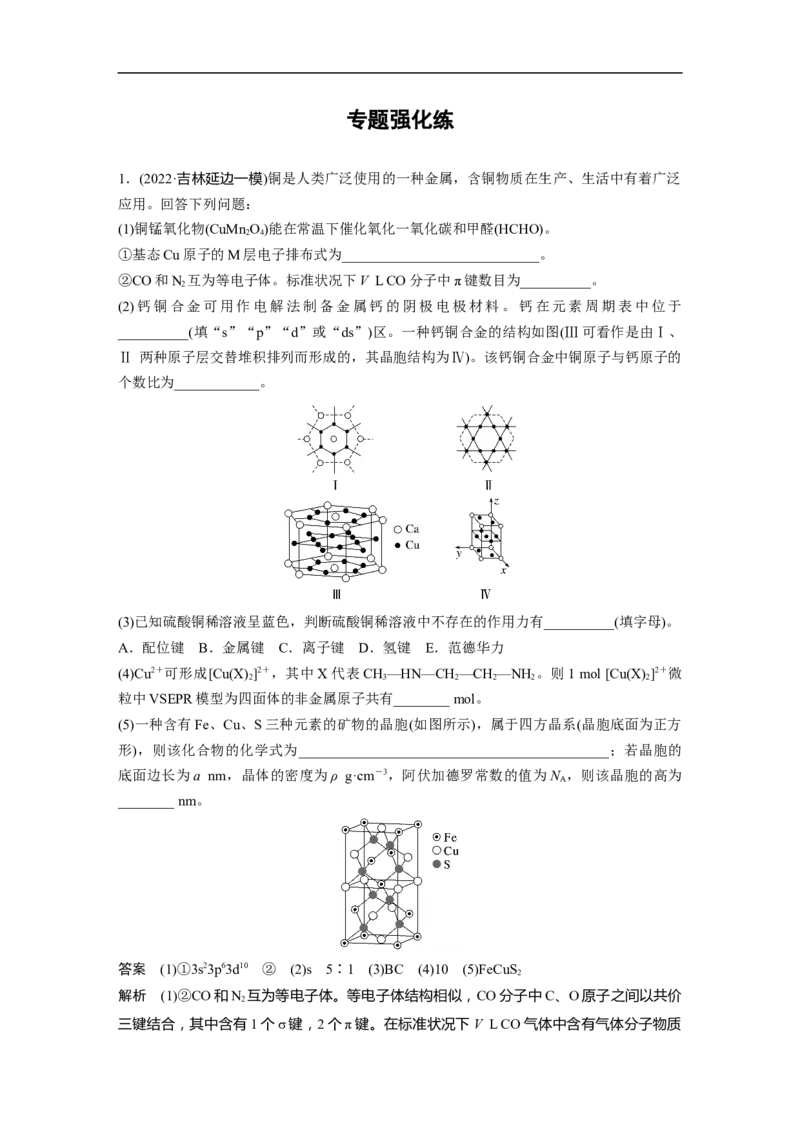
__________(填“s”“p”“d”或“ds”)区。一种钙铜合金的结构如图(Ⅲ可看作是由Ⅰ、
Ⅱ 两种原子层交替堆积排列而形成的,其晶胞结构为Ⅳ)。该钙铜合金中铜原子与钙原子的
个数比为____________。
(3)已知硫酸铜稀溶液呈蓝色,判断硫酸铜稀溶液中不存在的作用力有__________(填字母)。
A.配位键 B.金属键 C.离子键 D.氢键 E.范德华力
(4)Cu2+可形成[Cu(X) ]2+,其中X代表CH—HN—CH —CH—NH 。则1 mol [Cu(X) ]2+微
2 3 2 2 2 2
粒中VSEPR模型为四面体的非金属原子共有________ mol。
(5)一种含有Fe、Cu、S三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方
形),则该化合物的化学式为____________________________________________;若晶胞的
底面边长为a nm,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为N ,则该晶胞的高为
A
________ nm。
答案 (1)①3s23p63d10 ② (2)s 5∶1 (3)BC (4)10 (5)FeCuS
2
解析 (1)②CO和N 互为等电子体。等电子体结构相似,CO分子中C、O原子之间以共价
2
三键结合,其中含有1个σ键,2个π键。在标准状况下V L CO气体中含有气体分子物质的量n(CO)= mol,则该分子中含有的π键数目N(π)=2n(CO)N =。(2)Ca是20号元素,Ca
A
原子核外电子排布为2、8、8、2,所以Ca位于元素周期表第四周期ⅡA族,属于s区元素
由图Ⅳ可知:上下底面内角为120°、60°,上下面共用4个对称的Cu原子、前后面和左右面
共用1个Cu原子,体心有1个Cu原子;Ca原子为晶胞的顶点,则一个晶胞中含有Ca的数
目为4×+4×=1,含有Cu的数目为8×+1=5,所以钙铜合金中铜原子与钙原子的个数比
为5∶1。(3)硫酸铜在溶液中完全电离产生自由移动的离子,不存在离子键;水分子之间存
在范德华力、氢键,水分子、硫酸根离子中原子之间形成共价键,水合铜离子中存在配位键,
不存在金属键,故合理选项是BC。(4)Cu2+可形成[Cu(X) ]2+,其中X代表CH—HN—CH
2 3 2
—CH—NH ,其中的C、N原子价层电子对数都是4,VSEPR模型为四面体形,则1 mol
2 2
[Cu(X) ]2+微粒中VSEPR模型为四面体的非金属原子共有10 mol。(5)根据图示可知在一个
2
晶胞中含有的Fe原子数目为8×+4×+1=4;含有的Cu原子数目为4×+6×=4,含有的
S原子数目是8个,所以该物质的化学式为FeCuS;假设晶胞高度为c nm,该晶胞密度ρ=
2
= g·cm-3= g·cm-3,所以晶胞的高度c= nm。
2.(2022·江西上饶模拟预测)磷酸亚铁锂(LiFePO )电池是新能源汽车动力电池之一。
4
(1)写出基态Fe2+的核外电子排布式:________________________,请从原子结构角度解释
Fe能呈+2价的原因:____________。
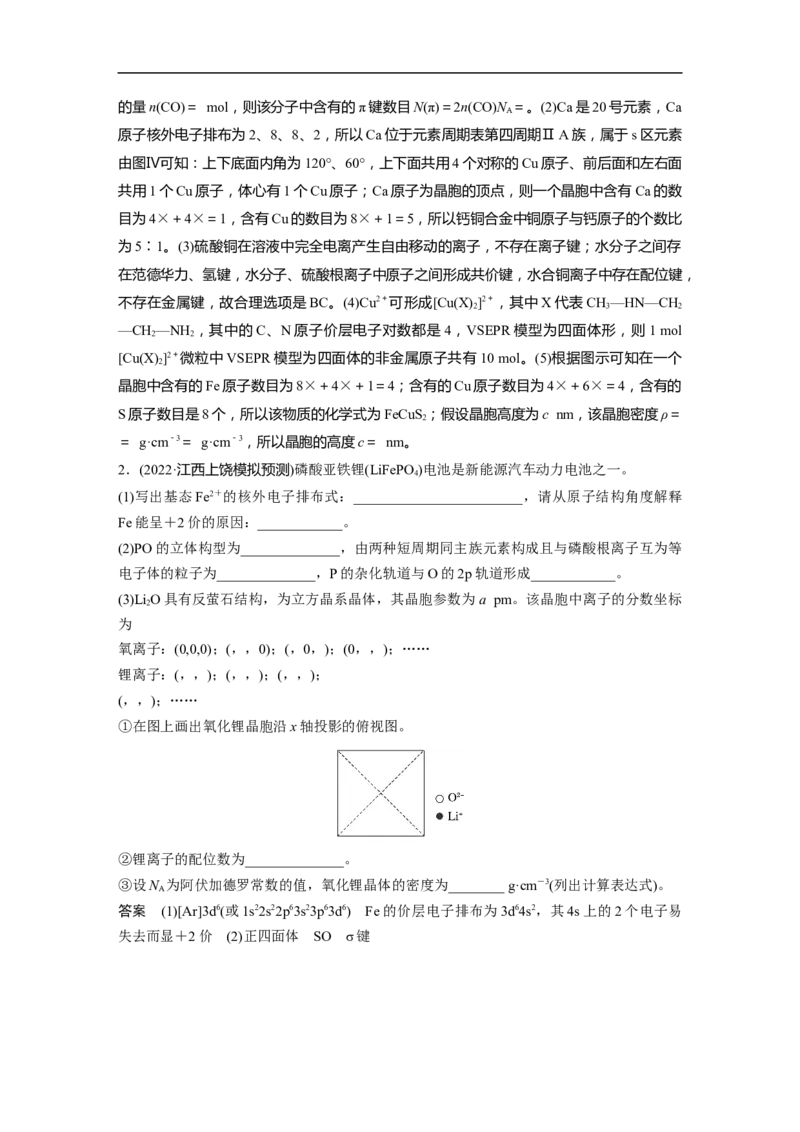
(2)PO的立体构型为______________,由两种短周期同主族元素构成且与磷酸根离子互为等
电子体的粒子为______________,P的杂化轨道与O的2p轨道形成____________。
(3)LiO具有反萤石结构,为立方晶系晶体,其晶胞参数为 a pm。该晶胞中离子的分数坐标
2
为
氧离子:(0,0,0);(,,0);(,0,);(0,,);……
锂离子:(,,);(,,);(,,);
(,,);……
①在图上画出氧化锂晶胞沿x轴投影的俯视图。
②锂离子的配位数为______________。
③设N 为阿伏加德罗常数的值,氧化锂晶体的密度为________ g·cm-3(列出计算表达式)。
A
答案 (1)[Ar]3d6(或1s22s22p63s23p63d6) Fe的价层电子排布为3d64s2,其4s上的2个电子易
失去而显+2价 (2)正四面体 SO σ键(3)① ②4 ③
解析 (2)PO的中心原子P上的孤电子对数为×(5+3-4×2)=0,σ键电子对数为4,价层电
子对数为4,P原子采取sp3杂化,VSEPR模型为四面体形,由于没有孤电子对,故立体构
型为正四面体;用“替代法”,由两种短周期同主族元素构成且与磷酸根离子互为等电子体
的粒子为SO;P的杂化轨道与O的2p轨道形成σ键。(3)①由题干得,LiO的晶胞中O2-位
2
于8个顶点和6个面心,1个晶胞中含8×+6×=4个O2-,Li+位于O2- 构成的八个四面体
空隙,1 个晶胞中含 8 个 Li+,则氧化锂晶胞沿 x 轴投影的俯视图为 。
②LiO的晶胞中O2-位于8个顶点和6个面心,Li+位于O2- 构成的八个四面体空隙,则锂
2
离子的配位数为4。③1个晶胞的质量为 g;晶胞参数为a pm,1个晶胞的体积为(a×
10-10cm)3=a3×10-30 cm3;则氧化锂晶体的密度为= g·cm-3。
3.(2022·云南二模)过渡金属及其化合物在生产、生活中有着广泛应用。回答下列问题:
(1)过渡元素Co基态原子的核外电子排布式为__________________;第四电离能I(Co)<
4
I(Fe),其原因是___________________________________________________________。
4
(2)Fe、Fe2+、Fe3+可以与CO、SCN-、CN-、HNCONH(尿素)等多种配体形成很多的配合
2 2
物。
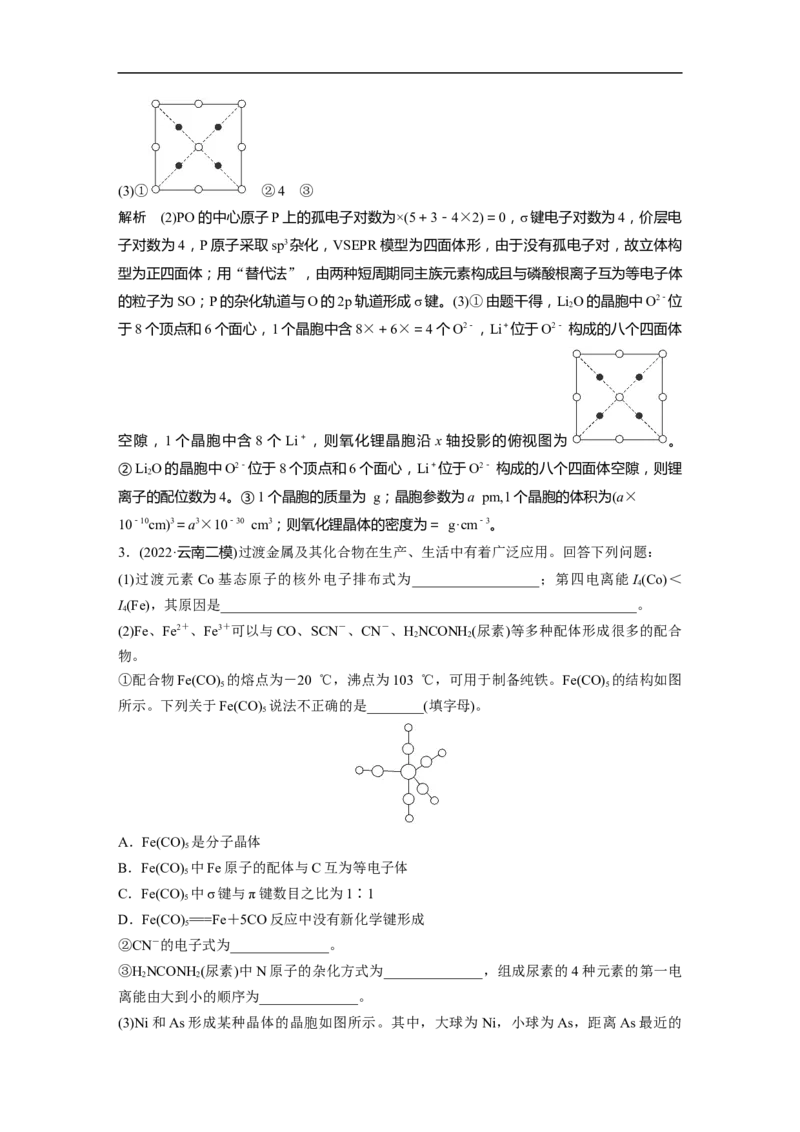
①配合物Fe(CO) 的熔点为-20 ℃,沸点为103 ℃,可用于制备纯铁。Fe(CO) 的结构如图
5 5
所示。下列关于Fe(CO) 说法不正确的是________(填字母)。
5
A.Fe(CO) 是分子晶体
5
B.Fe(CO) 中Fe原子的配体与C互为等电子体
5
C.Fe(CO) 中σ键与π键数目之比为1∶1
5
D.Fe(CO) ===Fe+5CO反应中没有新化学键形成
5
②CN-的电子式为______________。
③HNCONH(尿素)中N原子的杂化方式为______________,组成尿素的4种元素的第一电
2 2
离能由大到小的顺序为______________。
(3)Ni和As形成某种晶体的晶胞如图所示。其中,大球为 Ni,小球为As,距离As最近的Ni构成正三棱柱,其中晶胞下方As原子坐标为(,,)。
①Ni的配位数为______________。
②已知晶胞底面边长为 a pm,高为 c pm,N 为阿伏加德罗常数的值。则晶胞密度为
A
____________ g·cm-3。
答案 (1)1s22s22p63s23p63d74s2(或[Ar]3d74s2) Fe失去的是较稳定的3d5中的一个电子,Co失
去的是3d6中的一个电子 (2)①D
② ③sp3 N>O>H>C
(3)①6 ②
解析 (2)①配合物Fe(CO) 的熔点为-20 ℃,沸点为103 ℃,可知其属于分子晶体,故A
5
正确;Fe(CO) 中Fe原子的配体为CO,与C原子总数相等,价电子数也相同,所以CO、C
5
属于等电子体,故B正确;Fe与CO形成5个配位键即σ键,每个CO分子中含有1个σ键
和2个π键,σ键与π键数目之比为1∶1,故C正确;反应得到Fe单质,形成金属键,故
D 错误。② CN-与 N 互为等电子体,等电子体的结构相似,所以 CN-的电子式为
2
。③HNCONH(尿素)中N原子形成3个σ键,有1个孤电子对,价层电子对
2 2
个数是4,所以N原子的杂化方式为sp3;同一周期元素,其第一电离能随着原子序数增大
而呈增大趋势,但第ⅡA族、第ⅤA族第一电离能大于同周期相邻元素,所以第一电离能:
N>O>H>C。(3)①晶胞含Ni原子2个,As原子2个,化学式为NiAs,配位数之比应为
1∶1;与As配位的Ni形成正三棱柱,As的配位数是6,所以Ni的配位数为6。②由As配
位的Ni形成正三棱柱可判断,该三棱柱底面为正三角形,晶胞底面夹角为60°和120°,底
面积为a2×10-20 cm2,所以晶胞密度为 g·cm-3= g·cm-3。
4.(2022·安徽二模)镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币
等,镀在其他金属上可以防止生锈。回答下列问题:
(1)基态镍原子核外未成对的电子数为______个。
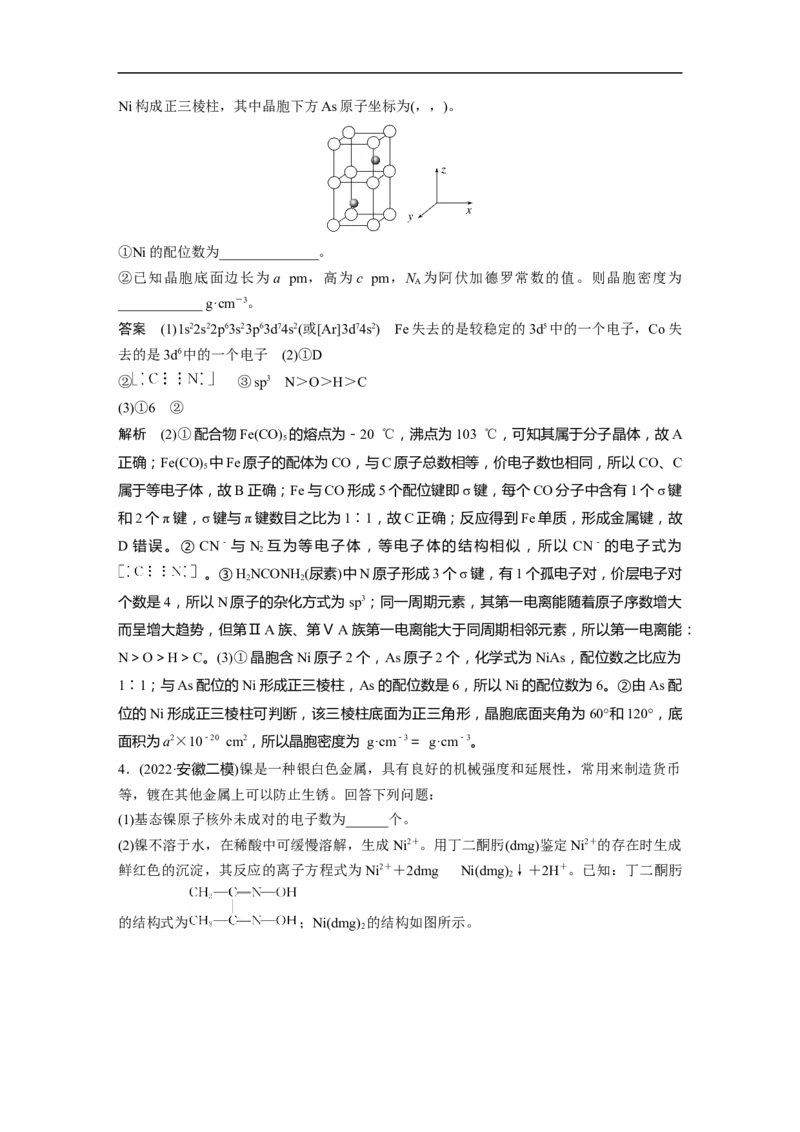
(2)镍不溶于水,在稀酸中可缓慢溶解,生成Ni2+。用丁二酮肟(dmg)鉴定Ni2+的存在时生成
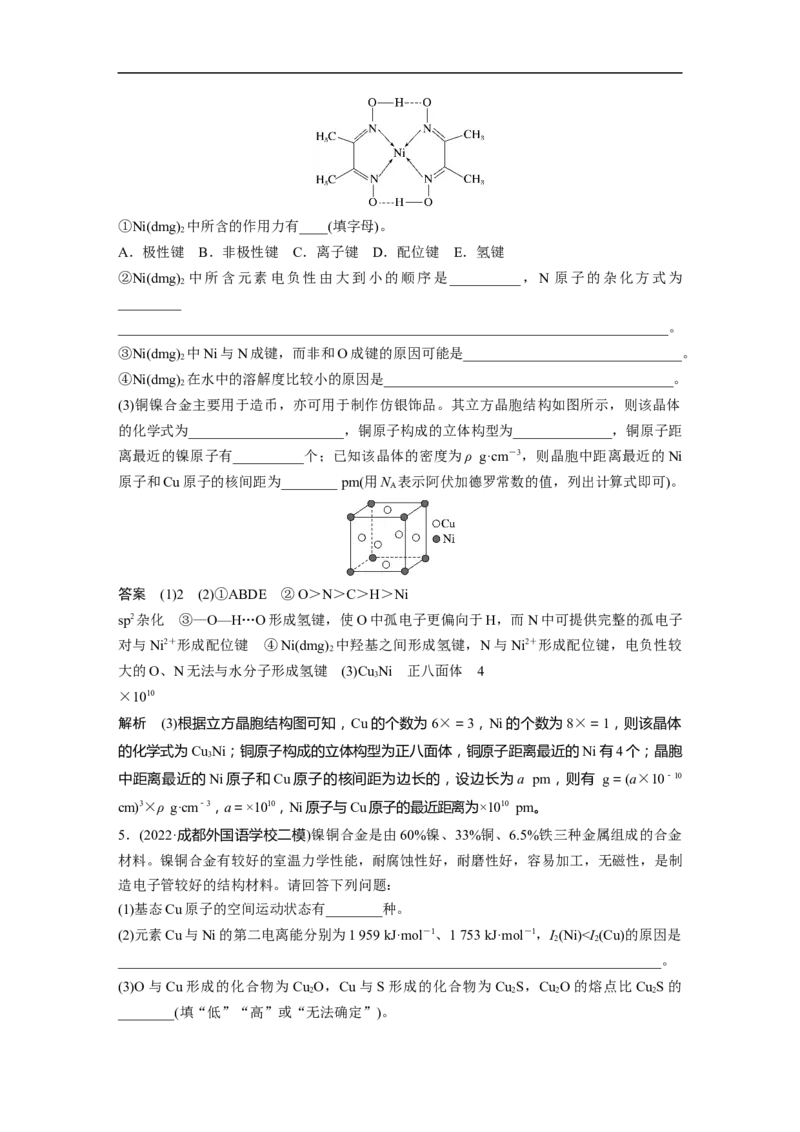
鲜红色的沉淀,其反应的离子方程式为Ni2++2dmgNi(dmg) ↓+2H+。已知:丁二酮肟
2
的结构式为 ;Ni(dmg) 的结构如图所示。
2①Ni(dmg) 中所含的作用力有____(填字母)。
2
A.极性键 B.非极性键 C.离子键 D.配位键 E.氢键
②Ni(dmg) 中所含元素电负性由大到小的顺序是__________,N 原子的杂化方式为
2
_________
______________________________________________________________________________。
③Ni(dmg) 中Ni与N成键,而非和O成键的原因可能是_______________________________。
2
④Ni(dmg) 在水中的溶解度比较小的原因是_________________________________________。
2
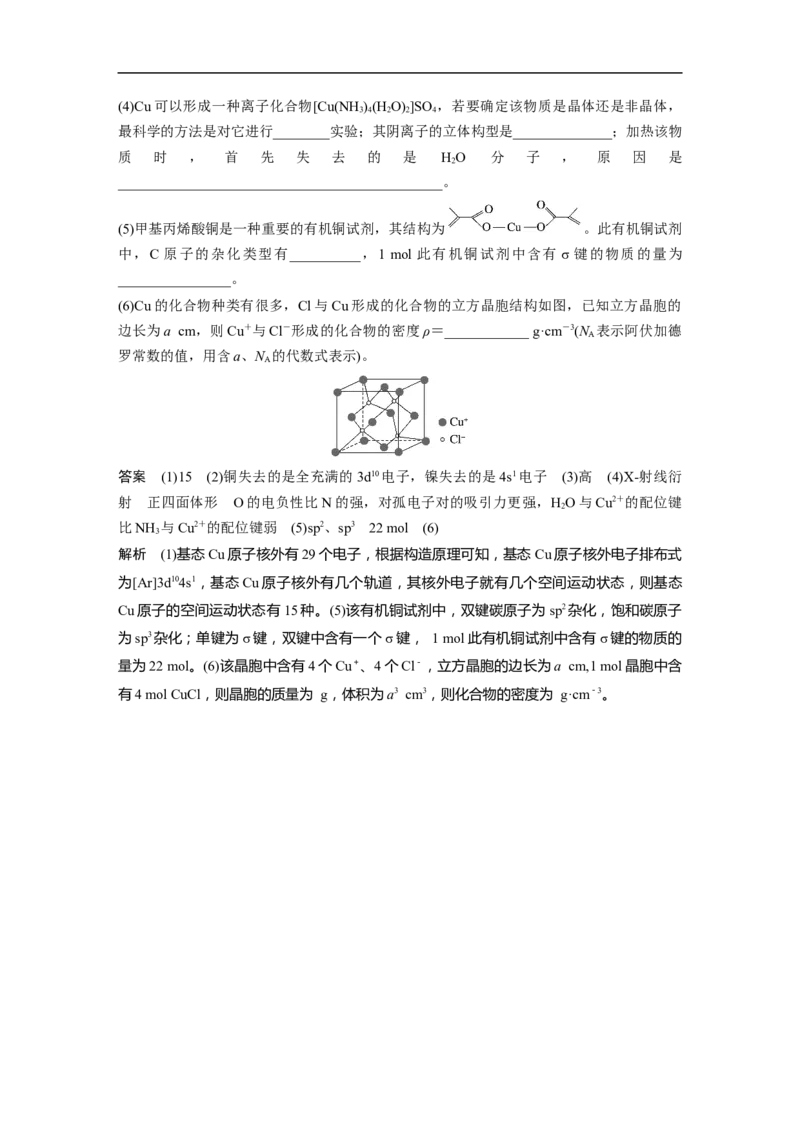
(3)铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体
的化学式为______________________,铜原子构成的立体构型为______________,铜原子距
离最近的镍原子有__________个;已知该晶体的密度为ρ g·cm-3,则晶胞中距离最近的Ni
原子和Cu原子的核间距为________ pm(用N 表示阿伏加德罗常数的值,列出计算式即可)。
A
答案 (1)2 (2)①ABDE ②O>N>C>H>Ni
sp2杂化 ③—O—H…O形成氢键,使O中孤电子更偏向于H,而N中可提供完整的孤电子
对与Ni2+形成配位键 ④Ni(dmg) 中羟基之间形成氢键,N与Ni2+形成配位键,电负性较
2
大的O、N无法与水分子形成氢键 (3)Cu Ni 正八面体 4
3
×1010
解析 (3)根据立方晶胞结构图可知,Cu的个数为6×=3,Ni的个数为8×=1,则该晶体
的化学式为Cu Ni;铜原子构成的立体构型为正八面体,铜原子距离最近的Ni有4个;晶胞
3
中距离最近的Ni原子和Cu原子的核间距为边长的,设边长为a pm,则有 g=(a×10-10
cm)3×ρ g·cm-3,a=×1010,Ni原子与Cu原子的最近距离为×1010 pm。
5.(2022·成都外国语学校二模)镍铜合金是由60%镍、33%铜、6.5%铁三种金属组成的合金
材料。镍铜合金有较好的室温力学性能,耐腐蚀性好,耐磨性好,容易加工,无磁性,是制
造电子管较好的结构材料。请回答下列问题:
(1)基态Cu原子的空间运动状态有________种。
(2)元素Cu与Ni的第二电离能分别为1 959 kJ·mol-1、1 753 kJ·mol-1,I(Ni)