文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题02
1.下列离子方程式与所给事实不相符的是
A.Cl 制备84消毒液(主要成分是NaClO):Cl+2OH-=Cl-+ClO-+HO
2 2 2
B.食醋去除水垢中的CaCO :CaCO +2H+=Ca2++HO+CO↑
3 3 2 2
C.利用覆铜板制作印刷电路板:2Fe3++Cu=2Fe2++Cu2+
D.NaS去除废水中的Hg2+:Hg2++S2-=HgS↓
2
答案:B
解析:A.Cl 和NaOH溶液反应产生NaCl、NaClO、HO,除了Cl 和HO不能拆写其余均可
2 2 2 2
拆写为离子,A项正确;
B.食醋中的醋酸CHCOOH为弱酸不能拆写为离子,反应为2CHCOOH+CaCO =Ca2++
3 3 3
2CHCOO-+CO+HO,B项错误;
3 2 2
C.FeCl 将Cu氧化为CuCl 而自身被还原为FeCl ,反应为2Fe3++Cu=2Fe2++Cu2+,C项正确;
3 2 2
D.NaS将Hg2+转化为沉淀除去,反应为Hg2++S2−=HgS↓,D项正确;
2
2.下列有关电极方程式或离子方程式错误的是
A. 碱性锌锰电池的正极反应:MnO +HO+e-=MnO(OH)+OH-
2 2
B. 铅酸蓄电池充电时的阳极反应:Pb2++2HO-2e-=PbO +4H+
2 2
C. K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN) ]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D. TiCl 加入水中:TiCl +(x+2)H O=TiO·xHO↓+4H++4Cl-
4 4 2 2 2
答案:B
解析:A.碱性锌锰电池放电时正极得到电子生成MnO(OH),电极方程式为MnO +HO+e-
2 2
=MnO(OH)+OH-,A正确;
B.铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-+2HO=PbO +4H++SO,B错
4 2 2
误;
C.K[Fe(CN) ]用来鉴别Fe2+生成滕氏蓝沉淀,反应的离子方程式为K++Fe2++[Fe(CN) ]3-=
3 6 6
KFe[Fe(CN) ]↓,C正确;
6
D.TiCl 容易与水反应发生水解,反应的离子方程式为TiCl +(x+2)H O=TiO·xHO↓+4H++
4 4 2 2 2
4Cl-,D正确;
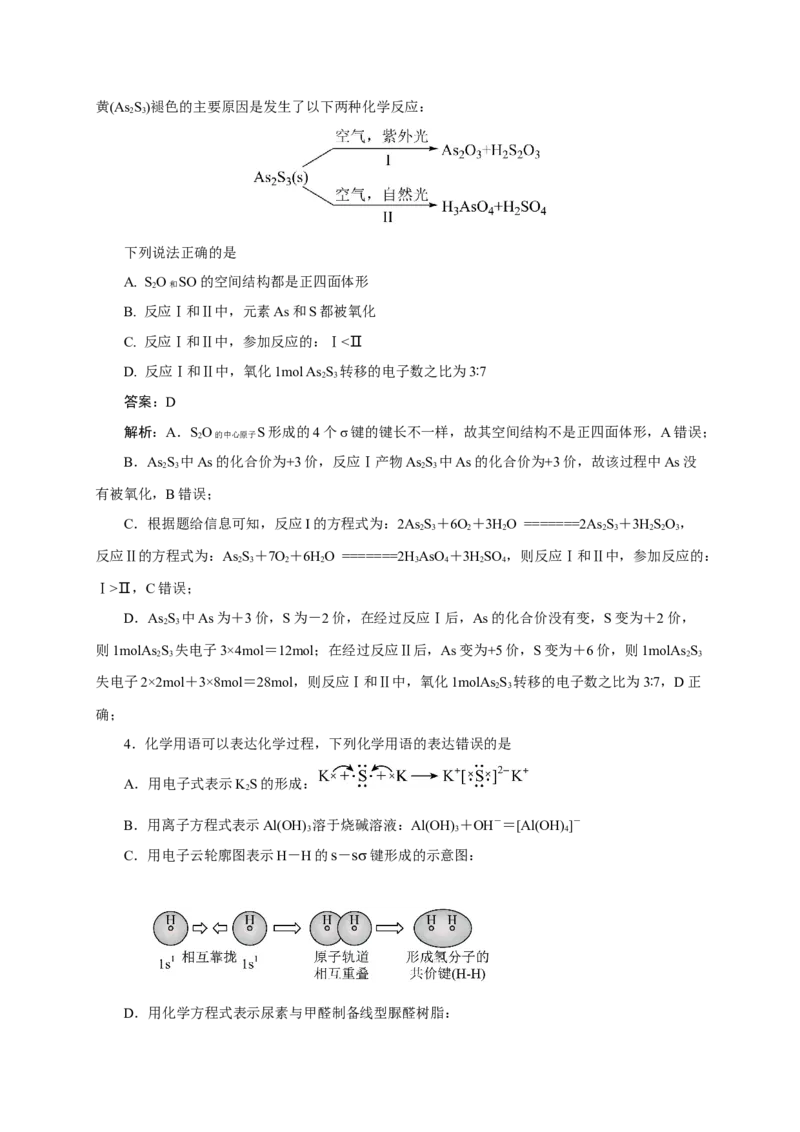
3.油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄(As S)褪色的主要原因是发生了以下两种化学反应:
2 3
下列说法正确的是
A. SO SO的空间结构都是正四面体形
2 和
B. 反应Ⅰ和Ⅱ中,元素As和S都被氧化
C. 反应Ⅰ和Ⅱ中,参加反应的:Ⅰ<Ⅱ
D. 反应Ⅰ和Ⅱ中,氧化1mol AsS 转移的电子数之比为3∶7
2 3
答案:D
解析:A.SO S形成的4个σ键的键长不一样,故其空间结构不是正四面体形,A错误;
2 的中心原子
B.As S 中As的化合价为+3价,反应Ⅰ产物As S 中As的化合价为+3价,故该过程中As没
2 3 2 3
有被氧化,B错误;
C.根据题给信息可知,反应I的方程式为:2As S+6O+3HO =======2As S+3HSO,
2 3 2 2 2 3 2 2 3
反应Ⅱ的方程式为:As S+7O+6HO =======2HAsO +3HSO ,则反应Ⅰ和Ⅱ中,参加反应的:
2 3 2 2 3 4 2 4
Ⅰ>Ⅱ,C错误;
D.As S 中As为+3价,S为-2价,在经过反应Ⅰ后,As的化合价没有变,S变为+2价,
2 3
则1molAs S 失电子3×4mol=12mol;在经过反应Ⅱ后,As变为+5价,S变为+6价,则1molAs S
2 3 2 3
失电子2×2mol+3×8mol=28mol,则反应Ⅰ和Ⅱ中,氧化1molAs S 转移的电子数之比为3∶7,D正
2 3
确;
4.化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示KS的形成:
2
B.用离子方程式表示Al(OH) 溶于烧碱溶液:Al(OH) +OH-=[Al(OH) ]-
3 3 4
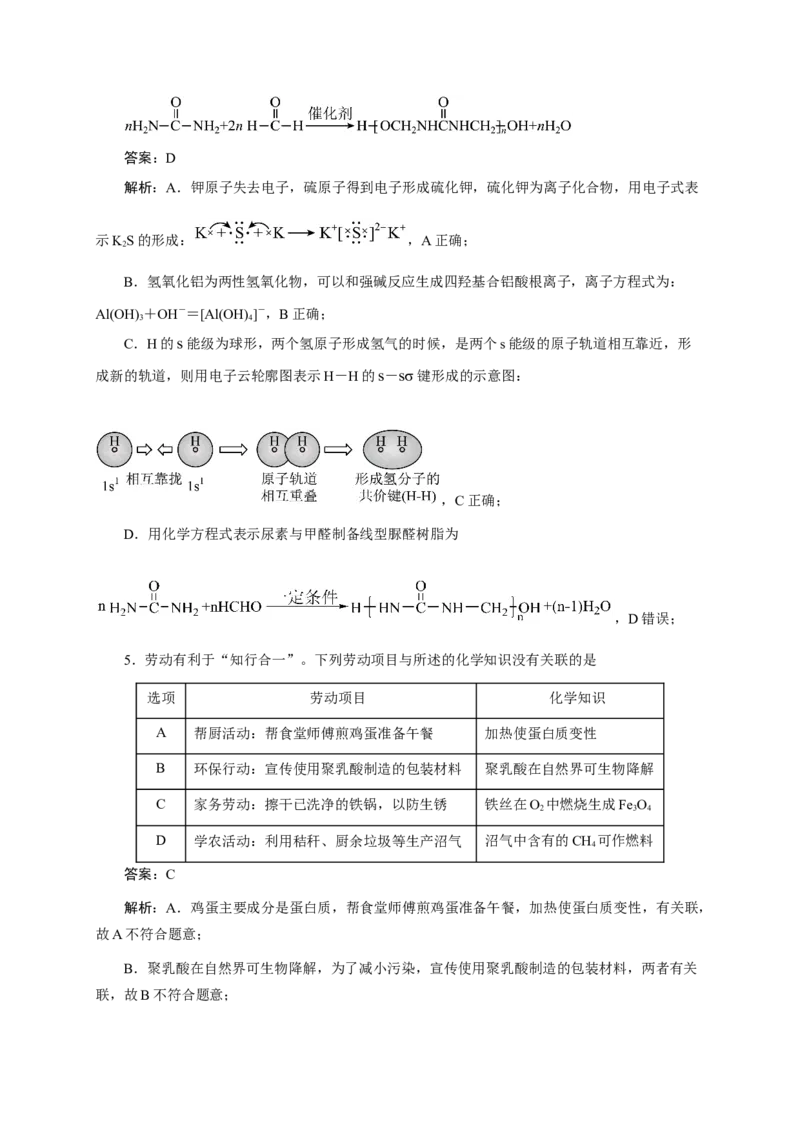
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:答案:D
解析:A.钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电子式表
示KS的形成: ,A正确;
2
B.氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:
Al(OH) +OH-=[Al(OH) ]-,B正确;
3 4
C.H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,形
成新的轨道,则用电子云轮廓图表示H-H的s-sσ键形成的示意图:
,C正确;
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂为
,D错误;
5.劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 帮厨活动:帮食堂师傅煎鸡蛋准备午餐 加热使蛋白质变性
B 环保行动:宣传使用聚乳酸制造的包装材料 聚乳酸在自然界可生物降解
C 家务劳动:擦干已洗净的铁锅,以防生锈 铁丝在O 中燃烧生成Fe O
2 3 4
D 学农活动:利用秸秆、厨余垃圾等生产沼气 沼气中含有的CH 可作燃料
4
答案:C
解析:A.鸡蛋主要成分是蛋白质,帮食堂师傅煎鸡蛋准备午餐,加热使蛋白质变性,有关联,
故A不符合题意;
B.聚乳酸在自然界可生物降解,为了减小污染,宣传使用聚乳酸制造的包装材料,两者有关
联,故B不符合题意;C.擦干已洗净的铁锅,以防生锈,防止生成氧化铁,铁丝在O 中燃烧生成Fe O,两者没有
2 3 4
关联,故C 符合题意;
D.利用秸秆、厨余垃圾等生产沼气,沼气主要成分是甲烷,甲烷用作燃料,两者有关系,故
D不符合题意。
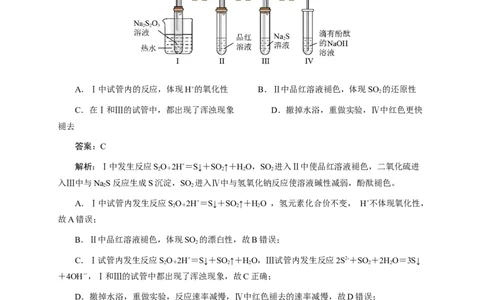
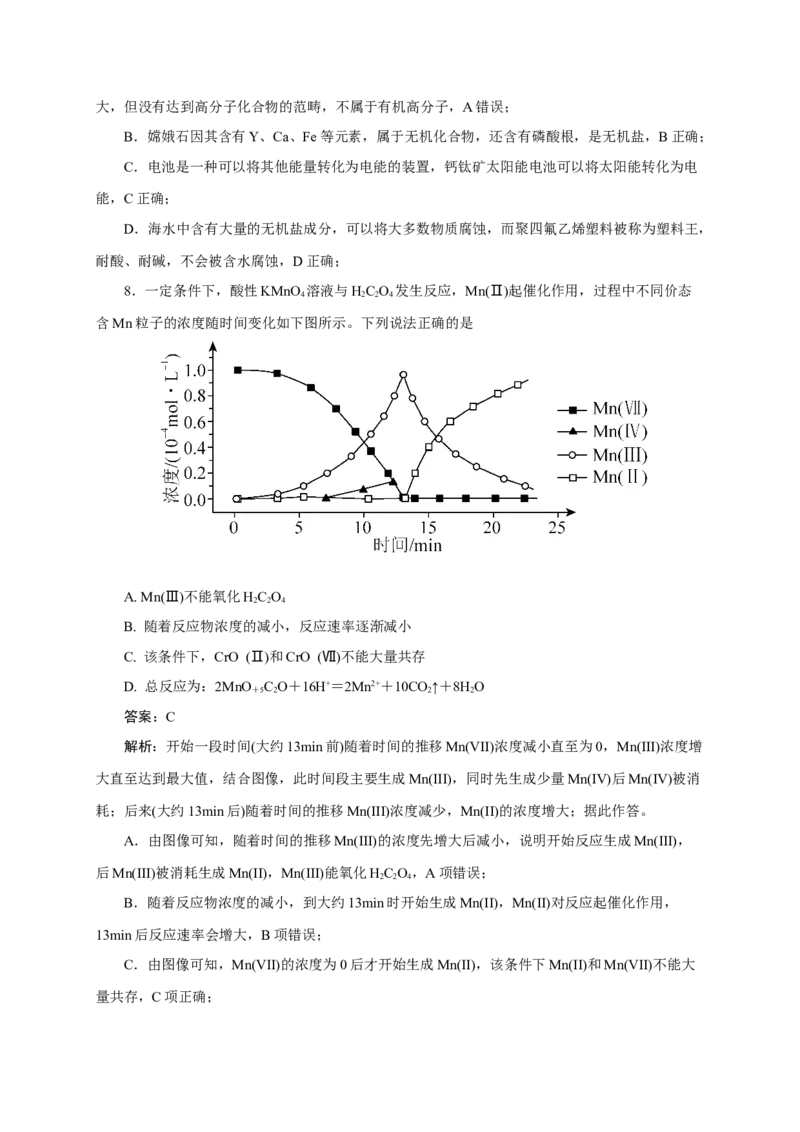
6.按图装置进行实验。将稀硫酸全部加入Ⅰ中的试管,关闭活塞。下列说法正确的是
A.Ⅰ中试管内的反应,体现H+的氧化性 B.Ⅱ中品红溶液褪色,体现SO 的还原性
2
C.在Ⅰ和Ⅲ的试管中,都出现了浑浊现象 D.撤掉水浴,重做实验,Ⅳ中红色更快
褪去
答案:C
解析:Ⅰ中发生反应SO 2H+=S↓+SO ↑+HO,SO 进入Ⅱ中使品红溶液褪色,二氧化硫进
2 + 2 2 2
入Ⅲ中与NaS反应生成S沉淀,SO 进入Ⅳ中与氢氧化钠反应使溶液碱性减弱,酚酞褪色。
2 2
A.Ⅰ中试管内发生反应SO 2H+=S↓+SO ↑+HO ,氢元素化合价不变, H+不体现氧化性,
2 + 2 2
故A错误;
B.Ⅱ中品红溶液褪色,体现SO 的漂白性,故B错误;
2
C.Ⅰ试管内发生反应SO 2H+=S↓+SO ↑+HO,Ⅲ试管内发生反应2S2-+SO +2HO=3S↓
2 + 2 2 2 2
+4OH-,Ⅰ和Ⅲ的试管中都出现了浑浊现象,故C正确;
D.撤掉水浴,重做实验,反应速率减慢,Ⅳ中红色褪去的速率减慢,故D错误;
7.科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是
A. 利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B. 发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7
C. 研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D. 革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
答案:A
解析:A.常见的脂肪酸有:硬脂酸(C H COOH)、油酸(C H COOH),二者相对分子质量虽
17 35 17 33大,但没有达到高分子化合物的范畴,不属于有机高分子,A错误;
B.嫦娥石因其含有Y、Ca、Fe等元素,属于无机化合物,还含有磷酸根,是无机盐,B正确;
C.电池是一种可以将其他能量转化为电能的装置,钙钛矿太阳能电池可以将太阳能转化为电
能,C正确;
D.海水中含有大量的无机盐成分,可以将大多数物质腐蚀,而聚四氟乙烯塑料被称为塑料王,
耐酸、耐碱,不会被含水腐蚀,D正确;
8.一定条件下,酸性KMnO 溶液与HC O 发生反应,Mn(Ⅱ)起催化作用,过程中不同价态
4 2 2 4
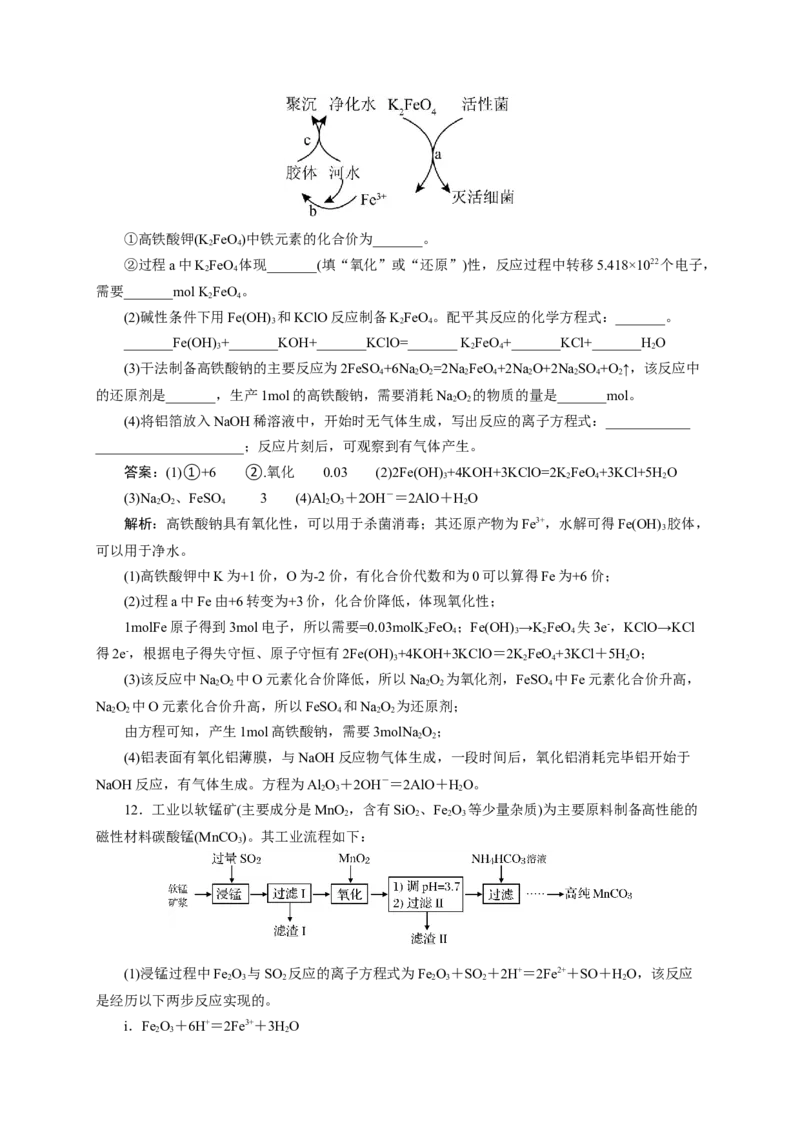
含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是
A. Mn(Ⅲ)不能氧化HC O
2 2 4
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下,CrO (Ⅱ)和CrO (Ⅶ)不能大量共存
D. 总反应为:2MnO C O+16H+=2Mn2++10CO↑+8HO
+5 2 2 2
答案:C
解析:开始一段时间(大约13min前)随着时间的推移Mn(VII)浓度减小直至为0,Mn(III)浓度增
大直至达到最大值,结合图像,此时间段主要生成Mn(III),同时先生成少量Mn(IV)后Mn(IV)被消
耗;后来(大约13min后)随着时间的推移Mn(III)浓度减少,Mn(II)的浓度增大;据此作答。
A.由图像可知,随着时间的推移Mn(III)的浓度先增大后减小,说明开始反应生成Mn(III),
后Mn(III)被消耗生成Mn(II),Mn(III)能氧化HC O,A项错误;
2 2 4
B.随着反应物浓度的减小,到大约13min时开始生成Mn(II),Mn(II)对反应起催化作用,
13min后反应速率会增大,B项错误;
C.由图像可知,Mn(VII)的浓度为0后才开始生成Mn(II),该条件下Mn(II)和Mn(VII)不能大
量共存,C项正确;D.HC O 为弱酸,在离子方程式中应以化学式保留,总反应为2MnO 5HC O+6H+=
2 2 4 + 2 2 4
2Mn2++10CO↑+8HO,D项错误;
2 2
9.化学与生产、生活密切相关。下列说法错误的是
A.PM2.5是指粒子直径不大于2.5μm的可吸入悬浮颗粒物
B.2022北京冬奥吉祥物“冰墩墩”总体的制作成分之一为聚碳酸酯,属于有机高分子材料
C.合金是生活中常用的材料,现代社会应用最广泛的合金是铁合金
D.煤经过液化、气化等清洁化处理后,可以减少二氧化碳的产生,避免“温室效应”
答案:D
解析:A.PM2.5是指粒子直径不大于2.5μm的可吸入悬浮颗粒物,A正确;
B.聚碳酸酯为有机合成材料,属于有机高分子材料,B正确;
C.合金性能优于成分金属,现代社会应用最广泛的合金是铁合金,故C正确;
D.根据碳元素守恒,煤经过液化、气化等清洁化处理后,不会减少二氧化碳的产生,故D错
误;
10.下列物质在指定条件下发生反应的化学方程式书写正确的是
A.NaHS溶于水HS-的电离:HS-+HO HS+OH-
2 2
B.石灰水表面漂着的“白膜”可用醋酸溶解:CaCO +2H+=Ca2++CO↑+HO
3 2 2
C.向NaClO溶液中通入少量SO :SO +ClO-+HO=SO+Cl-+2H+
2 2 2
D.向Mg(HCO ) 溶液中加入足量的澄清石灰水:Mg2++2HCO 2++4OH-=Mg(OH) ↓+
3 2 +2Ca 2
2CaCO ↓+2HO
3 2
答案:D
解析:A.HS-的电离生成硫离子和氢离子,HS- S2-+H+,A错误;
B.醋酸为弱酸不能拆,反应为CaCO +2CHCOOH=Ca2++2CHCOO-+HO+CO↑,B错误;
3 3 3 2 2
C.次氯酸钠具有氧化性,会和二氧化硫反应生成硫酸根离子,生成氢离子与次氯酸根离子生
成次氯酸,故向NaClO溶液中通入少量SO :3ClO-+SO +HO=SO+Cl-+2HClO,C错误;
2 2 2
D.向Mg(HCO ) 溶液中加入足量的澄清石灰水,镁离子、碳酸氢根离子完全反应生成氢氧化
3 2
镁沉淀、水、碳酸钙沉淀:Mg2++2HCO 2++4OH-=Mg(OH) ↓+2CaCO ↓+2HO,D正确;
+2Ca 2 3 2
11.根据所学知识,回答下列问题:
(1)K FeO 是常见的水处理剂,净水原理如图所示。请回答下列问题:
2 4①高铁酸钾(K FeO)中铁元素的化合价为_______。
2 4
②过程a中KFeO 体现_______(填“氧化”或“还原”)性,反应过程中转移5.418×1022个电子,
2 4
需要_______mol KFeO。
2 4
(2)碱性条件下用Fe(OH) 和KClO反应制备KFeO。配平其反应的化学方程式:_______。
3 2 4
_______Fe(OH) +_______KOH+_______KClO=_______ K FeO+_______KCl+_______H O
3 2 4 2
(3)干法制备高铁酸钠的主要反应为2FeSO +6Na O=2Na FeO+2Na O+2Na SO +O ↑,该反应中
4 2 2 2 4 2 2 4 2
的还原剂是_______,生产1mol的高铁酸钠,需要消耗NaO 的物质的量是_______mol。
2 2
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:____________
_____________________;反应片刻后,可观察到有气体产生。
答案:(1)①+6 ②.氧化 0.03 (2)2Fe(OH) +4KOH+3KClO=2K FeO+3KCl+5H O
3 2 4 2
(3)Na O、FeSO 3 (4)Al O+2OH-=2AlO+HO
2 2 4 2 3 2
解析:高铁酸钠具有氧化性,可以用于杀菌消毒;其还原产物为Fe3+,水解可得Fe(OH) 胶体,
3
可以用于净水。
(1)高铁酸钾中K为+1价,O为-2价,有化合价代数和为0可以算得Fe为+6价;
(2)过程a中Fe由+6转变为+3价,化合价降低,体现氧化性;
1molFe原子得到3mol电子,所以需要=0.03molK FeO;Fe(OH) →KFeO 失3e-,KClO→KCl
2 4 3 2 4
得2e-,根据电子得失守恒、原子守恒有2Fe(OH) +4KOH+3KClO=2KFeO+3KCl+5HO;
3 2 4 2
(3)该反应中NaO 中O元素化合价降低,所以NaO 为氧化剂,FeSO 中Fe元素化合价升高,
2 2 2 2 4
NaO 中O元素化合价升高,所以FeSO 和NaO 为还原剂;
2 2 4 2 2
由方程可知,产生1mol高铁酸钠,需要3molNa O;
2 2
(4)铝表面有氧化铝薄膜,与NaOH反应物气体生成,一段时间后,氧化铝消耗完毕铝开始于
NaOH反应,有气体生成。方程为Al O+2OH-=2AlO+HO。
2 3 2
12.工业以软锰矿(主要成分是MnO ,含有SiO、Fe O 等少量杂质)为主要原料制备高性能的
2 2 2 3
磁性材料碳酸锰(MnCO )。其工业流程如下:
3
(1)浸锰过程中Fe O 与SO 反应的离子方程式为Fe O+SO +2H+=2Fe2++SO+HO,该反应
2 3 2 2 3 2 2
是经历以下两步反应实现的。
i.Fe O+6H+=2Fe3++3HO
2 3 2ii..……
写出ii的离子方程式:_____________________________________________。
(2)氧化过程中被MnO 氧化的物质主要有(写化学式):_______________。
2
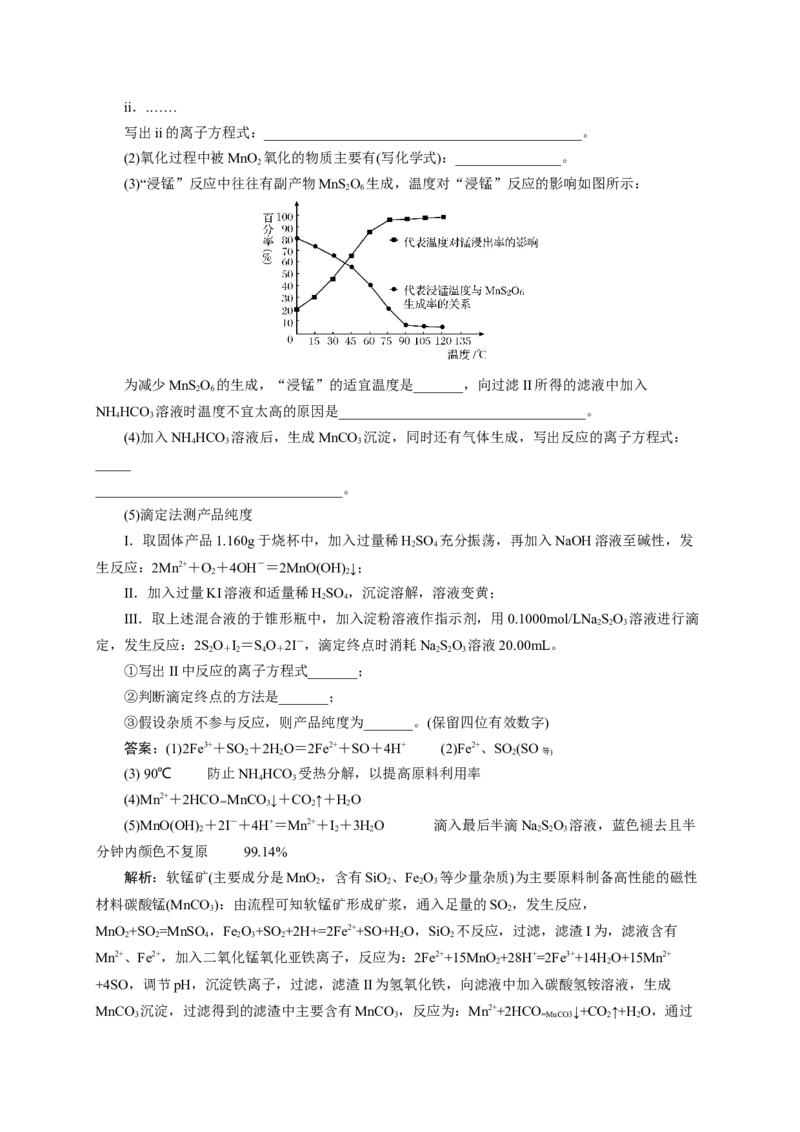
(3)“浸锰”反应中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图所示:
2 6
为减少MnS O 的生成,“浸锰”的适宜温度是_______,向过滤II所得的滤液中加入
2 6
NH HCO 溶液时温度不宜太高的原因是___________________________________。
4 3
(4)加入NH HCO 溶液后,生成MnCO 沉淀,同时还有气体生成,写出反应的离子方程式:
4 3 3
_____
___________________________________。
(5)滴定法测产品纯度
I.取固体产品1.160g于烧杯中,加入过量稀HSO 充分振荡,再加入NaOH溶液至碱性,发
2 4
生反应:2Mn2++O+4OH-=2MnO(OH) ↓;
2 2
II.加入过量KI溶液和适量稀HSO ,沉淀溶解,溶液变黄;
2 4
III.取上述混合液的于锥形瓶中,加入淀粉溶液作指示剂,用0.1000mol/LNa SO 溶液进行滴
2 2 3
定,发生反应:2SO I=SO 2I-,滴定终点时消耗NaSO 溶液20.00mL。
2 + 2 4 + 2 2 3
①写出II中反应的离子方程式_______;
②判断滴定终点的方法是_______;
③假设杂质不参与反应,则产品纯度为_______。(保留四位有效数字)
答案:(1)2Fe3++SO +2HO=2Fe2++SO+4H+ (2)Fe2+、SO (SO
2 2 2 等)
(3) 90℃ 防止NH HCO 受热分解,以提高原料利用率
4 3
(4)Mn2++2HCO MnCO ↓+CO↑+HO
= 3 2 2
(5)MnO(OH) +2I-+4H+=Mn2++I+3HO 滴入最后半滴NaSO 溶液,蓝色褪去且半
2 2 2 2 2 3
分钟内颜色不复原 99.14%
解析:软锰矿(主要成分是MnO ,含有SiO、Fe O 等少量杂质)为主要原料制备高性能的磁性
2 2 2 3
材料碳酸锰(MnCO ):由流程可知软锰矿形成矿浆,通入足量的SO ,发生反应,
3 2
MnO +SO=MnSO ,Fe O+SO+2H+=2Fe2++SO+H O,SiO 不反应,过滤,滤渣I为,滤液含有
2 2 4 2 3 2 2 2
Mn2+、Fe2+,加入二氧化锰氧化亚铁离子,反应为:2Fe2++15MnO+28H+=2Fe3++14H O+15Mn2+
2 2
+4SO,调节pH,沉淀铁离子,过滤,滤渣II为氢氧化铁,向滤液中加入碳酸氢铵溶液,生成
MnCO 沉淀,过滤得到的滤渣中主要含有MnCO ,反应为:Mn2++2HCO ↓+CO ↑+H O,通过
3 3 =MnCO3 2 2洗涤、烘干得到MnCO 晶体;
3
(1)浸锰过程中Fe O 与SO 反应的化学方程式为Fe O+SO+2H+=2Fe2++SO+H O,该反应是经过
2 3 2 2 3 2 2
氧化铁与酸反应生成铁离子,铁离子与二氧化硫反应实现的:Fe O+6H+=2Fe3++3H O、2Fe3++SO
2 3 2 2
+2HO=2Fe2++SO+4H+;故答案为:2Fe3++SO +2HO=2Fe2++SO+4H+;
2 2 2
(2)MnO 具有较强氧化性,氧化过程中被MnO 氧化的物质主要有Fe2+、SO (SO
2 2 2 等);
(3)由图可知,90℃时,MnS O 的生成率低,锰浸出率高,温度再高,变化不大,则“浸锰”
2 6
的适宜温度是90℃;NH HCO 受热易分解,温度不宜太高,防止NH HCO 受热分解,提高原料利
4 3 4 3
用率;故答案为:90℃;防止NH HCO 受热分解,以提高原料利用率;
4 3
(4)Mn2+的滤液中加入NH HCO 溶液后,发生彻底的双水解,生成MnCO 沉淀和二氧化碳,反应为:
4 3 3
Mn2++2HCO MnCO ↓+CO↑+HO;故答案为:Mn2++2HCO MnCO ↓+CO↑+HO;
= 3 2 2 = 3 2 2
(5)①II中加入过量KI溶液和适量稀HSO ,沉淀溶解,溶液变黄,则MnO(OH)2将碘离子氧
2 4
化生成碘单质,反应的离子方程式为MnO(OH) +2I-+4H+=Mn2++I+3HO;
2 2 2
②NaSO 将所有碘单质还原时溶液蓝色褪去,故判断滴定终点的方法是滴入最后半滴
2 2 3
NaSO 溶液,蓝色褪去且半分钟内颜色不复原;
2 2 3
③反应过程2Mn2++O+4OH-=MnO(OH) ↓,MnO(OH) +2I-+4H+=Mn2++I+3HO,2SO
2 2 2 2 2 2 +
I=SO -,,关系式为MnCO ~Mn2+~MnO(OH) ~I~2SO
2 4 +2I 3 2 2 2 ,故
)=×(0.1000mol·L-1×0.020L×10)=0.01mol,假设杂质不参与反应,则产品纯度为
n(MnCO3
×100%=99.14%,答案为99.14%。