文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题09
1.下列离子方程式正确的是
A. 向CuSO 溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
B. 向Fe(NO ) 溶液中加入过量的HI溶液:2NO ++6I-=3I+2NO↑+4HO
3 3 +8H 2 2
C. NaHSO 溶液与Ba(OH) 溶液混合后呈中性:2H++SO+Ba2++2OH-=BaSO↓+2H O
4 2 4 2
D.NaOH溶液与过量HC O 溶液反应:HC O+2OH-=C O+2HO
2 2 4 2 2 4 2 2
2.化学与生活、科技、社会发展息息相关。下列说法正确的是
A.“天宫”空间站使用聚乳酸材料餐具,聚乳酸是化合物
B.富勒烯与石墨烯用途广泛,它们都属于新型无机非金属材料
C. 冬奥场馆建筑使用碲化镉发电玻璃,碲和镉均属于主族元素
D. 中国承建的卡塔尔首座光伏电站中的光伏材料为高纯度二氧化硅
3.能正确表示下列反应的离子方程式的是
A. 用K[Fe(CN) ]溶液检验Fe2+:Fe2++K++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 6 6
B. 向二元弱酸亚磷酸(H PO )溶液中滴加足量的烧碱溶液:HPO +3OH-=PO O
3 3 3 3 +3H2
C. 用惰性电极电解氯化镁溶液:2Cl-+2H O=====Cl↑+H ↑+2OH-
2 2 2
D. 海水提溴工艺中用二氧化硫还原溴:SO +Br +2H O=2H++SO+2HBr
2 2 2
4.下列叙述不涉及氧化还原反应的是
A. 海水提溴 B. 苏打用作食用碱
C. 谷物发酵酿酒 D. 漂白粉久置空气中失效
5.下列消毒剂的有效成分属于盐的是
A. 高锰酸钾溶液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
6.下列物质属于纯净物的是
A. 漂白粉 B. 氯水 C. 柴油 D. 冰醋酸
7.下列物质属于电解质,且熔融状态下能导电的是
A. Cu B. HCl C. KNO D. 葡萄糖(C H O)
3 6 12 6
8.下列表示不正确的是
A. 氯化钠的电子式: B. 二氧化碳的结构式:O=C=O
C. 乙烷分子的空间填充模型: D. 1,3-丁二烯的键线式:
9.关于反应2NaNO +2KI+2H SO =2NO↑+I +Na SO +K SO +2HO,下列说法正确的是
2 2 4 2 2 4 2 4 2
A. KI发生还原反应
B. HSO 既不是氧化剂,也不是还原剂
2 4
C. 氧化产物与还原产物的物质的量之比为2:1
D. 消耗0.5molNaNO 时,转移1.0mol电子
210.下列反应对应的方程式不正确的是
A. 大理石与醋酸反应:CaCO +2CH COOH=Ca2++2CH COO−+H O+CO↑
3 3 3 2 2
B. 铜的电解精炼的总反应(粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解液):Cu(阳
极)=====Cu(阴极)
C. 钠与水反应生成气体:2Na+2HO=2NaOH+H ↑
2 2
D. 向Mg(HCO ) 溶液中加入过量NaOH溶液的反应:Mg2++2HCO−
3 2 3
+4OH−=Mg(OH) ↓+2CO 2−+2HO
2 3 2
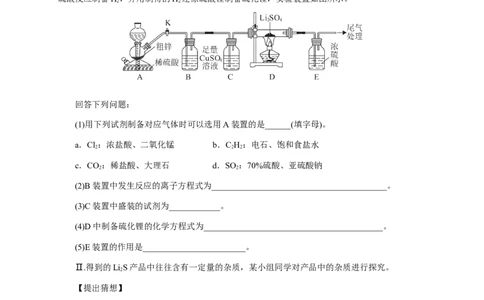
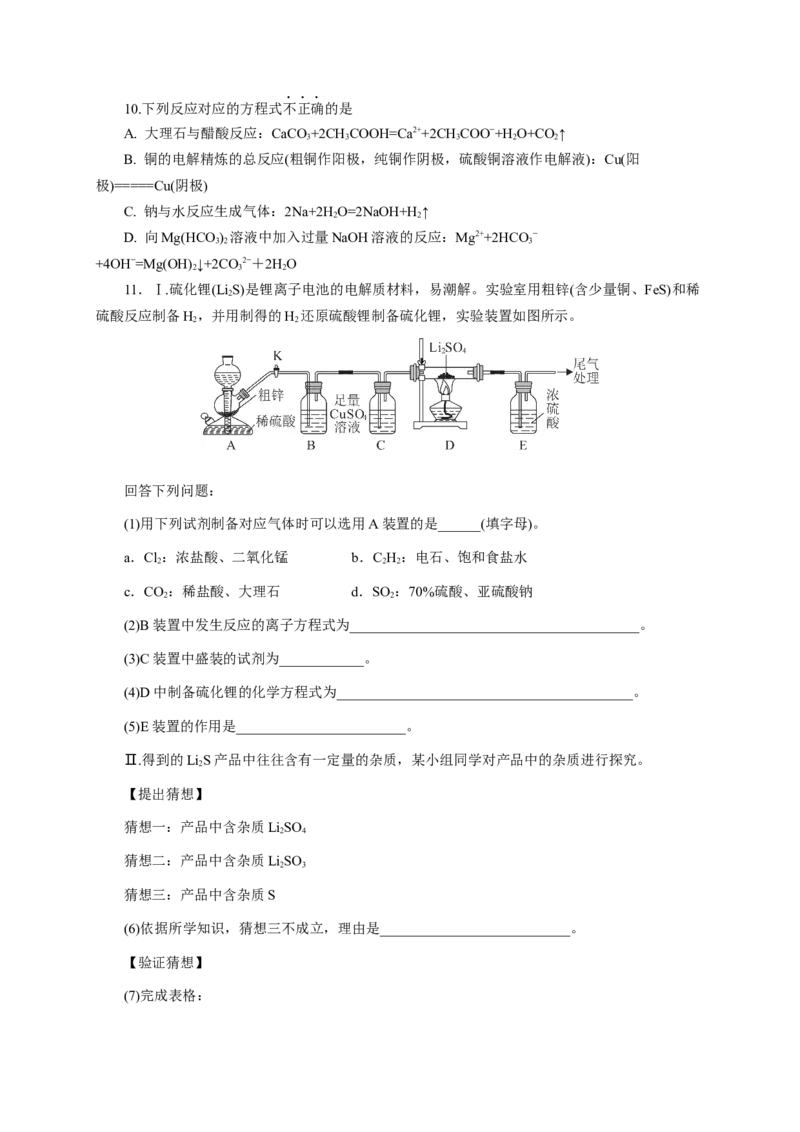
11.Ⅰ.硫化锂(Li S)是锂离子电池的电解质材料,易潮解。实验室用粗锌(含少量铜、FeS)和稀
2
硫酸反应制备H,并用制得的H 还原硫酸锂制备硫化锂,实验装置如图所示。
2 2
回答下列问题:
(1)用下列试剂制备对应气体时可以选用A装置的是______(填字母)。
a.Cl:浓盐酸、二氧化锰 b.C H:电石、饱和食盐水
2 2 2
c.CO:稀盐酸、大理石 d.SO :70%硫酸、亚硫酸钠
2 2
(2)B装置中发生反应的离子方程式为_________________________________________。
(3)C装置中盛装的试剂为____________。
(4)D中制备硫化锂的化学方程式为__________________________________________。
(5)E装置的作用是________________________。
Ⅱ.得到的LiS产品中往往含有一定量的杂质,某小组同学对产品中的杂质进行探究。
2
【提出猜想】
猜想一:产品中含杂质LiSO
2 4
猜想二:产品中含杂质LiSO
2 3
猜想三:产品中含杂质S
(6)依据所学知识,猜想三不成立,理由是___________________________。
【验证猜想】
(7)完成表格:限选试剂:稀盐酸、稀硫酸、蒸馏水、双氧水、氯化钡溶液、硝酸钡溶液
实验 操作与现象 结论
Ⅰ 取少量LiS样品溶于水,______ 样品中不含LiSO
2 2 3
Ⅱ 在实验Ⅰ反应后的溶液中,______ 样品中含LiSO
2 4
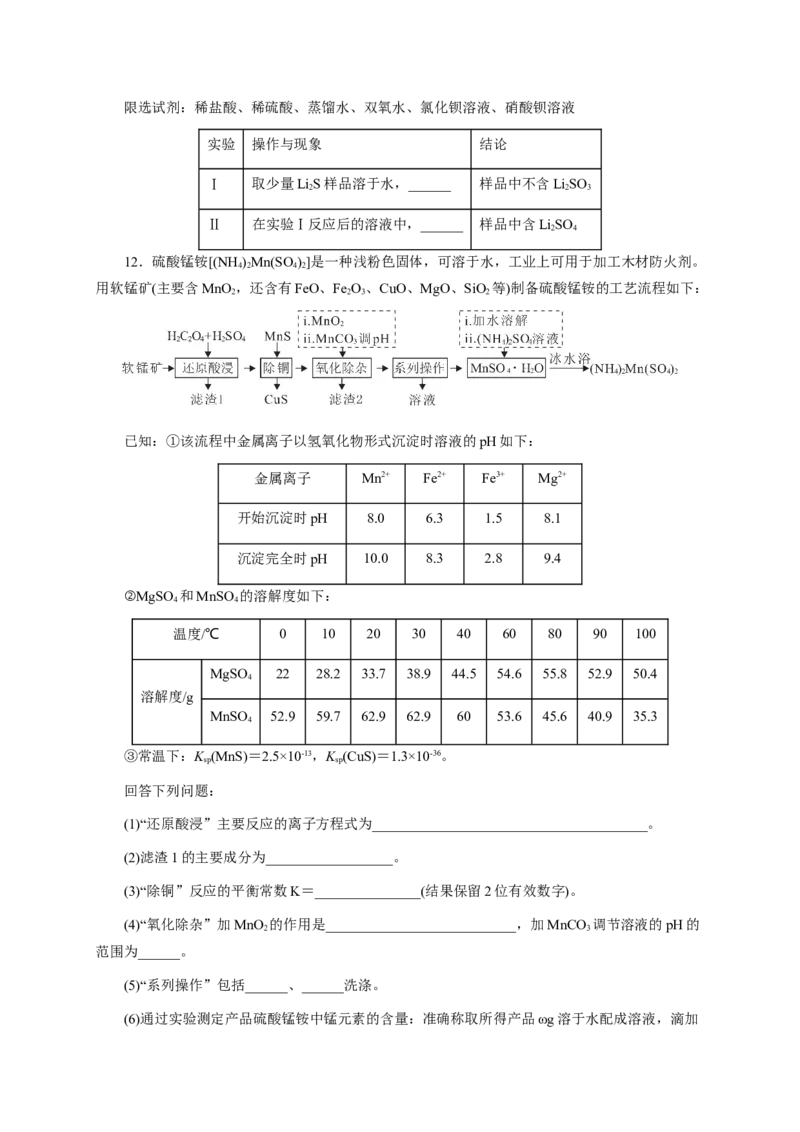
12.硫酸锰铵[(NH )Mn(SO )]是一种浅粉色固体,可溶于水,工业上可用于加工木材防火剂。
4 2 4 2
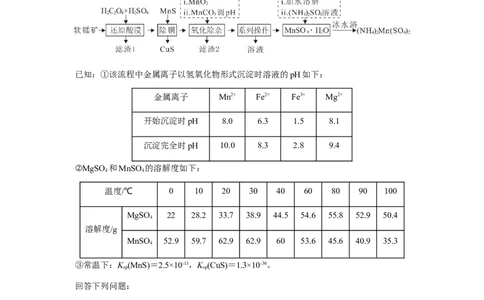
用软锰矿(主要含MnO ,还含有FeO、Fe O、CuO、MgO、SiO 等)制备硫酸锰铵的工艺流程如下:
2 2 3 2
已知:①该流程中金属离子以氢氧化物形式沉淀时溶液的pH如下:
金属离子 Mn2+ Fe2+ Fe3+ Mg2+
开始沉淀时pH 8.0 6.3 1.5 8.1
沉淀完全时pH 10.0 8.3 2.8 9.4
②MgSO 和MnSO 的溶解度如下:
4 4
温度/℃ 0 10 20 30 40 60 80 90 100
MgSO 22 28.2 33.7 38.9 44.5 54.6 55.8 52.9 50.4
4
溶解度/g
MnSO 52.9 59.7 62.9 62.9 60 53.6 45.6 40.9 35.3
4
③常温下:K (MnS)=2.5×10-13,K (CuS)=1.3×10-36。
sp sp
回答下列问题:
(1)“还原酸浸”主要反应的离子方程式为_______________________________________。
(2)滤渣1的主要成分为__________________。
(3)“除铜”反应的平衡常数K=_______________(结果保留2位有效数字)。
(4)“氧化除杂”加MnO 的作用是___________________________,加MnCO 调节溶液的pH的
2 3
范围为______。
(5)“系列操作”包括______、______洗涤。
(6)通过实验测定产品硫酸锰铵中锰元素的含量:准确称取所得产品ωg溶于水配成溶液,滴加氨水调pH至7~8,加入过量的cmol·L-1KMnO 溶液VmL,充分反应后过滤掉MnO ,将滤液与洗
1 4 1 2
涤液合并配制成100mL溶液,取20mL用cmol·L-1FeSO 酸性标准液滴定,重复实验3次,平均消
2 4
耗标准液VmL。滴定终点的判断依据是__________________________________,产品硫酸锰铵中
2
锰元素的质量分数为__________________(用相应字母表示)。