文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题14
1.下列离子方程式书写正确的是
A.向铜片中滴加浓硝酸有刺激性气味气体产生:Cu+4HNO=Cu2++2NO ↑+2HO+2NO
3 2 2
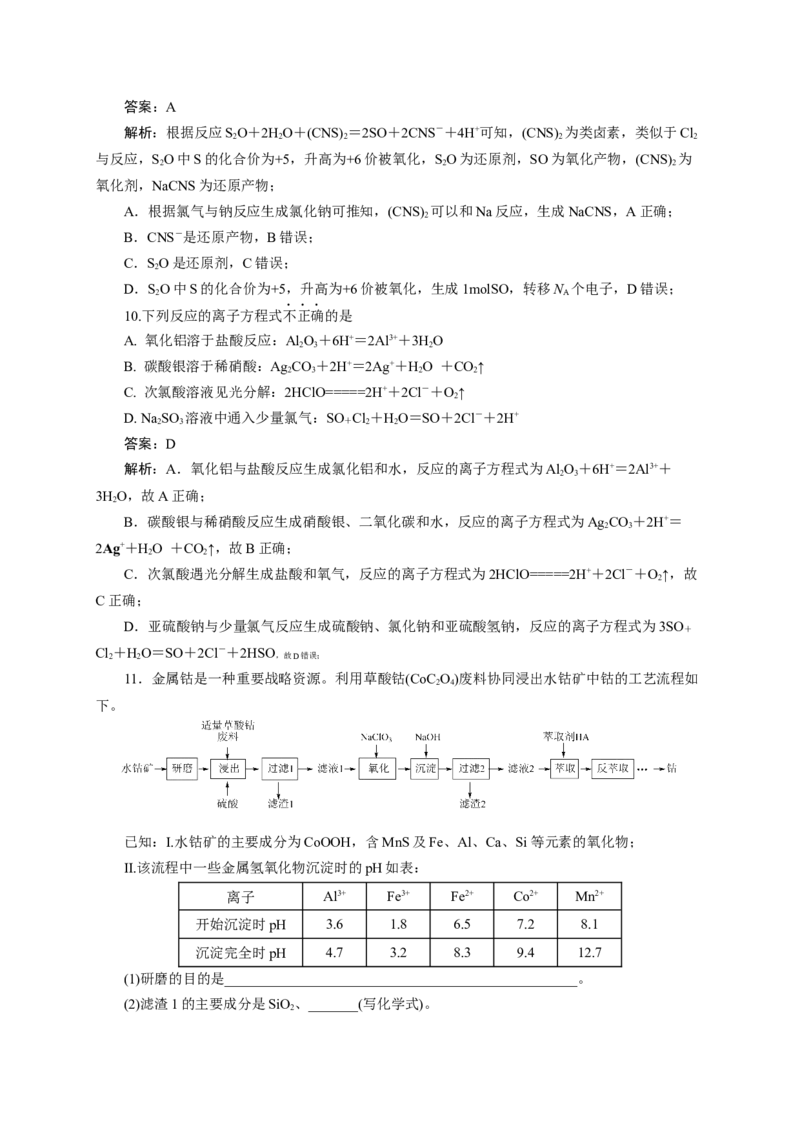
B.服用阿司匹林过量出现水杨酸( )中毒反应,可静脉注射NaHCO 溶液:
3
C.向NaClO和NaCl混合溶液中滴入少量FeSO 溶液:2Fe2++ClO-+2H+=Cl-+2Fe3++HO
3 2
D.向漂白粉溶液中通入少量的CO:2ClO-+Ca2++CO+HO=CaCO ↓+2HClO
2 2 2 3
答案:D
解析:A.浓硝酸可以拆开,故A错误;
B.由于酚羟基不与HCO
根反应,故B错误;
C.弱碱性条件下,Fe3+会转化为Fe(OH) 沉淀,则向NaClO和NaCl混合溶液中滴入少量
3
FeSO 溶液,反应的离子方程式为:2Fe2++ClO-+4OH-+H O=Cl-+2Fe(OH) ↓,故C错误;
4 2 3
D.向漂白粉溶液中通入少量的CO,CO 与漂白粉中Ca(ClO) 反应,反应的离子方程式为
2 2 2
2ClO-+Ca2++CO+HO=CaCO ↓+2HClO,故D错误;
2 2 3
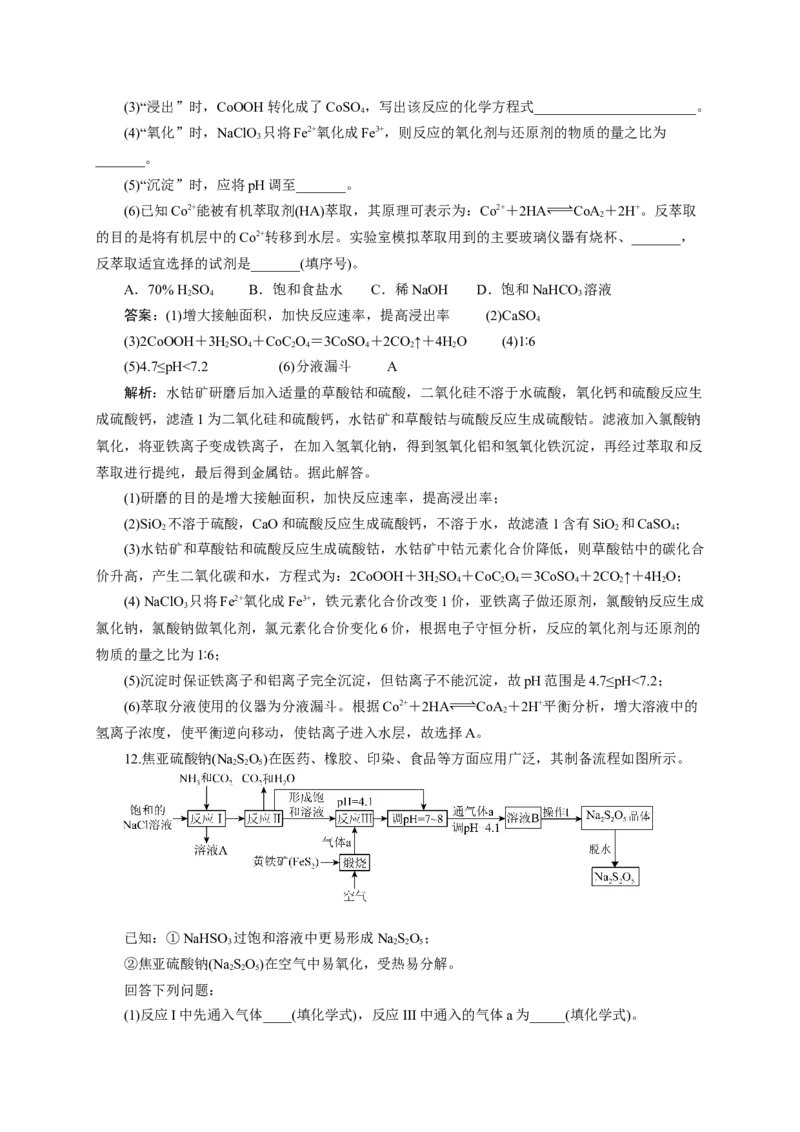
2.高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH
2 4
溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高铁酸钾有强
3
氧化性,酸性条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的流程如下:
2 4 2 4
下列关于KFeO 的说法错误的是
2 4
A.KFeO 是一种强氧化剂
2 4
B.与水反应,每消耗1个KFeO 转移3个电子
2 4
C.将KFeO 与盐酸混合使用,可增强其杀菌消毒效果
2 4
D.“反应Ⅱ”中,氧化剂和还原剂的个数之比为3∶2
答案:C
解析:A.常见的强氧化剂有Cl、KMnO (H+),高铁酸钾有强氧化性,酸性条件下,其氧化性
2 4
强于Cl、KMnO 等,所以KFeO 是一种强氧化剂,A正确;
2 4 2 4
B.能与水反应放出氧气,并生成Fe(OH) 胶体,根据氧化还原反应的规律可知,理论上每个
3
高铁酸钾中Fe化合价从+6价降低到+3价,电子转移数为3,与水反应,每消耗1个KFeO 转移3
2 4
个电子,B正确;C.KFeO 具有强氧化性,可氧化HCl中的Cl元素,使其转化为氯气,而高铁酸钾中铁元素
2 4
化合价降低,转化为铁离子,所以将KFeO 与盐酸混合使用,会降低杀菌消毒效果,C错误;
2 4
D.“反应Ⅱ”中,次氯酸钠做氧化剂,氧化铁离子生成高铁酸根离子,根据电子转移数守恒
可知,氧化剂和还原剂的个数之比为3∶2,D正确;
3.高铁酸钾是一种强氧化剂,也是一种绿色净水剂。已知:
(1)5FeO+3Mn2++16H+=5Fe3++3MnO 8HO
+ 2
(2)MnO 5Fe2++8H+=Mn2++5Fe3++4HO
+ 2
下列有关推断正确的是
A.明矾、高铁酸钾处理饮用水的原理完全相同
B.氧化性:FeO>MnO Fe3+
>
C.反应(1)中氧化剂、还原剂的物质的量之比为3∶5
D.若将反应(2)设计成原电池,Fe2+在正极放电
答案:B
解析:A.明矾的净水原理是Al3+水解生成Al(OH) 胶体,发生的是非氧化还原反应;而
3
KFeO 净水时发生了氧化还原反应,A项错误;
2 4
B.氧化剂的氧化性大于氧化产物,所以反应(1)中,氧化性:FeO>MnO (2)中氧化性:
,反应
MnO Fe3+,所以氧化性:FeO>MnO Fe3+,故B正确;
> >
C.反应(1)中FeO是氧化剂,Mn2+是还原剂,根据方程式可知,氧化剂、还原剂的物质的量之
比为5∶3,故C项错误;
D.将反应(2)设计成原电池,则负极上发生氧化反应,极反应式为Fe2+-e-=Fe3+ D项错误;
,
4.能正确表示下列反应的离子方程式是
A.电解MgCl 水溶液:2Cl-+2HO=====2OH-+Cl↑+H↑
2 2 2 2
B.少量SO 通入Ca(ClO) 液中:SO +HO+Ca2++2ClO-=CaSO↓+2HClO
2 2 2 2 3
C.KClO碱性溶液与Fe(OH) 反应:3ClO-+2 Fe(OH) =2FeO+3Cl-+4H++HO
3 3 2
D.用NaSO 溶液吸收少量Cl:3SO Cl+HO=2HSO 2Cl-+SO
2 3 2 + 2 2 +
答案:D
解析:A.电解MgCl 水溶液:2Cl-+Mg2++2HO=====Mg(OH)↓+Cl↑+H↑,A错误;
2 2 2 2 2
B.量SO 通入Ca(ClO) 液中:SO +HO+Ca2++ClO-=CaSO↓+Cl-+2H+,B错误;
2 2 2 2 3
C.KClO碱性溶液中氧化Fe(OH) ,反应后溶液不可能为酸性,C错误;
3
D.氯气能够把亚硫酸根离子氧化为硫酸根离子,D正确;
5.下列物质中不属于配合物的是
A.NaAl(OH) B.(NH )C O C.Ag(NH)NO D.CuSO ∙5HO
4 4 2 2 4 3 2 3 4 2
答案:B
解析:A.Al(OH)中四个羟基与Al3+间存在配位键,形成配合物。
B.不是配合物。
C.Ag(NH)2+中两个NH 分子与Ag+形成配位键,是配合物
3 3D.CuSO •5H O以Cu(HO) SO •H O形式存在,四个水分子与铜离子以配位键结合,形成配合
4 2 2 4 4 2
物。
6.在高温高压的水溶液中,AuS-与Fe2+发生反应2AuS-+3Fe2++4HO=Fe O+2Au+2HS↑
2 3 4 2
+4H+,下列说法正确的是
A.氧化剂与还原剂的物质的量之比为2:3
B.每生成4.48L H S,转移电子数为0.2N
2 A
C.反应中若有19.7g Au元素被还原,则生成0.05mol Fe O
3 4
D.若将此反应设计成原电池,则Fe2+在正极发生反应
答案:C
解析:A.该反应中,产物Fe O 中有一个铁为+2价,故氧化剂AuS-与还原剂Fe2+物质的量
3 4
之比为1:1,A错误;
B.无标准状况的条件,故无法计算。
C.被还原的19.7gAu为0.1mol,则对应产生的Fe O 为0.05mol,正确。
3 4
D.Fe2+在反应中失电子,发生氧化反应,原电池反应中正极为得电子发生还原反应的一极,
故D错误。
7.下列离子方程式书写正确的是
A.硝酸钡溶液中通入少量SO :Ba2++NO SO +HO=BaSO↓+NO+H+
2 + 2 2 4
B.用过量的碳酸钠溶液吸收氯气:CO Cl=CO+ClO-+Cl-
+ 2 2
C.氯乙酸乙酯在足量NaOH溶液中加热:ClCH COOC H+OH-—→ ClCH COO-+C HOH
2 2 5 2 2 5
D.铝片投入过量的NaOH溶液中发生反应:2Al+2OH-+6HO=2Al(OH) +3H↑
2 2
答案:D
解析:A.此反应中,氧化剂和还原剂得失电子不守恒,故错误,正确的写法为:3Ba2++
2NO -+3SO +2HO=3BaSO↓+2NO+4H+
3 2 2 4
B.碳酸钠过量时,产物为HCO -,正确写法为:2CO2-+Cl+HO=2HCO -+HClO-+Cl-
3 3 2 2 3
C.氯原子也会水解,应写为ClCH COOC H+2OH-—→ HOCH COO-+C HOH,故C错误。
2 2 5 2 2 5
D.铝能与氢氧化钠溶液反应,D正确。
8.下列物质中属于耐高温非金属材料的是
A. CO B. SiC C. Mg-Al D. P O
2 2 5
答案:B
解析:A.二氧化碳形成的晶体是熔沸点低的分子晶体,不属于耐高温非金属材料,故A错误;
B.碳化硅是熔沸点高的共价晶体,属于耐高温非金属材料,故B正确;
C.镁铝合金属于金属材料,不属于非金属材料,故C错误;
D.五氧化二磷形成的晶体是熔沸点低的分子晶体,不属于耐高温非金属材料,故D错误;
9.关于反应SO+2HO+(CNS) =2SO+2CNS-+4H+,下列说法正确的是
2 2 2
A. (CNS) 可以和Na反应,生成NaCNS B. CNS-是氧化产物
2
C. SO既是氧化剂又是还原剂 D. 生成1molSO,转移2N 个电子
2 A答案:A
解析:根据反应SO+2HO+(CNS) =2SO+2CNS-+4H+可知,(CNS) 为类卤素,类似于Cl
2 2 2 2 2
与反应,SO中S的化合价为+5,升高为+6价被氧化,SO为还原剂,SO为氧化产物,(CNS) 为
2 2 2
氧化剂,NaCNS为还原产物;
A.根据氯气与钠反应生成氯化钠可推知,(CNS) 可以和Na反应,生成NaCNS,A正确;
2
B.CNS-是还原产物,B错误;
C.SO是还原剂,C错误;
2
D.SO中S的化合价为+5,升高为+6价被氧化,生成1molSO,转移N 个电子,D错误;
2 A
10.下列反应的离子方程式不正确的是
A. 氧化铝溶于盐酸反应:Al O+6H+=2Al3++3HO
2 3 2
B. 碳酸银溶于稀硝酸:Ag CO+2H+=2Ag++HO +CO↑
2 3 2 2
C. 次氯酸溶液见光分解:2HClO=====2H++2Cl-+O↑
2
D. Na SO 溶液中通入少量氯气:SO Cl+HO=SO+2Cl-+2H+
2 3 + 2 2
答案:D
解析:A.氧化铝与盐酸反应生成氯化铝和水,反应的离子方程式为Al O+6H+=2Al3++
2 3
3HO,故A正确;
2
B.碳酸银与稀硝酸反应生成硝酸银、二氧化碳和水,反应的离子方程式为Ag CO+2H+=
2 3
2Ag++HO +CO↑,故B正确;
2 2
C.次氯酸遇光分解生成盐酸和氧气,反应的离子方程式为2HClO=====2H++2Cl-+O↑,故
2
C正确;
D.亚硫酸钠与少量氯气反应生成硫酸钠、氯化钠和亚硫酸氢钠,反应的离子方程式为3SO
+
Cl+HO=SO+2Cl-+2HSO
2 2 ,故D错误;
11.金属钴是一种重要战略资源。利用草酸钴(CoC O)废料协同浸出水钴矿中钴的工艺流程如
2 4
下。
已知:I.水钴矿的主要成分为CoOOH,含MnS及Fe、Al、Ca、Si等元素的氧化物;
II.该流程中一些金属氢氧化物沉淀时的pH如表:
离子 Al3+ Fe3+ Fe2+ Co2+ Mn2+
开始沉淀时pH 3.6 1.8 6.5 7.2 8.1
沉淀完全时pH 4.7 3.2 8.3 9.4 12.7
(1)研磨的目的是__________________________________________________。
(2)滤渣1的主要成分是SiO、_______(写化学式)。
2(3)“浸出”时,CoOOH转化成了CoSO ,写出该反应的化学方程式_______________________。
4
(4)“氧化”时,NaClO 只将Fe2+氧化成Fe3+,则反应的氧化剂与还原剂的物质的量之比为
3
_______。
(5)“沉淀”时,应将pH调至_______。
(6)已知Co2+能被有机萃取剂(HA)萃取,其原理可表示为:Co2++2HA CoA+2H+。反萃取
2
的目的是将有机层中的Co2+转移到水层。实验室模拟萃取用到的主要玻璃仪器有烧杯、_______,
反萃取适宜选择的试剂是_______(填序号)。
A.70% H SO B.饱和食盐水 C.稀NaOH D.饱和NaHCO 溶液
2 4 3
答案:(1)增大接触面积,加快反应速率,提高浸出率 (2)CaSO
4
(3)2CoOOH+3HSO +CoC O=3CoSO +2CO↑+4HO (4)1∶6
2 4 2 4 4 2 2
(5)4.7≤pH<7.2 (6)分液漏斗 A
解析:水钴矿研磨后加入适量的草酸钴和硫酸,二氧化硅不溶于水硫酸,氧化钙和硫酸反应生
成硫酸钙,滤渣1为二氧化硅和硫酸钙,水钴矿和草酸钴与硫酸反应生成硫酸钴。滤液加入氯酸钠
氧化,将亚铁离子变成铁离子,在加入氢氧化钠,得到氢氧化铝和氢氧化铁沉淀,再经过萃取和反
萃取进行提纯,最后得到金属钴。据此解答。
(1)研磨的目的是增大接触面积,加快反应速率,提高浸出率;
(2)SiO 不溶于硫酸,CaO和硫酸反应生成硫酸钙,不溶于水,故滤渣1含有SiO 和CaSO;
2 2 4
(3)水钴矿和草酸钴和硫酸反应生成硫酸钴,水钴矿中钴元素化合价降低,则草酸钴中的碳化合
价升高,产生二氧化碳和水,方程式为:2CoOOH+3HSO +CoC O=3CoSO +2CO↑+4HO;
2 4 2 4 4 2 2
(4) NaClO 只将Fe2+氧化成Fe3+,铁元素化合价改变1价,亚铁离子做还原剂,氯酸钠反应生成
3
氯化钠,氯酸钠做氧化剂,氯元素化合价变化6价,根据电子守恒分析,反应的氧化剂与还原剂的
物质的量之比为1∶6;
(5)沉淀时保证铁离子和铝离子完全沉淀,但钴离子不能沉淀,故pH范围是4.7≤pH<7.2;
(6)萃取分液使用的仪器为分液漏斗。根据Co2++2HA CoA+2H+平衡分析,增大溶液中的
2
氢离子浓度,使平衡逆向移动,使钴离子进入水层,故选择A。
12.焦亚硫酸钠(Na SO)在医药、橡胶、印染、食品等方面应用广泛,其制备流程如图所示。
2 2 5
已知:①NaHSO 过饱和溶液中更易形成NaSO;
3 2 2 5
②焦亚硫酸钠(Na SO)在空气中易氧化,受热易分解。
2 2 5
回答下列问题:
(1)反应I中先通入气体____(填化学式),反应III中通入的气体a为_____(填化学式)。(2)溶液A中含有三种阳离子,分别为Na+、H+和离子X。检验溶液A中离子X的方法是
_______。
(3)反应III调节pH为4.1,发生反应的离子方程式为_______。
(4)再次通入气体a得到溶液B的目的是_______。
(5)操作I为:在氮气氛围中,_______,_______,过滤,洗涤。其中洗涤NaSO 晶体时依次
2 2 5
用饱和SO 水溶液、无水乙醇。用饱和SO 水溶液洗涤的目的是__________________________。
2 2
(6)久置的NaSO 固体中若含有NaSO 杂质,其可能的原因是_______________________。(用
2 2 5 2 4
化学反应方程式表示)
答案:(1)NH SO (2)取少量溶液于试管,向试管中加入NaOH溶液,加热,用湿润红
3 2
色石蕊试纸靠近试管口,若试纸变蓝,则证明有NH
(3)CO +HO=2HSO CO (4)得到NaHSO 过饱和溶液
+2SO2 2 + 2 3
(5)低温蒸发(或减压蒸发,强调温度低即可) 冷却结晶 减少NaSO 在水中的溶解
2 2 5
(6) Na SO+HO+O=NaSO +HSO
2 2 5 2 2 2 4 2 4
解析:氨气和二氧化碳通入饱和氯化钠溶液生成NaHCO 析出晶体,溶液A为NH Cl,反应II
3 4
是NaHCO 受热分解生成二氧化碳和水和碳酸钠,FeS 和氧气煅烧生成氧化铁和SO ,反应III中
3 2 2
SO 和饱和碳酸钠溶液反应生成NaHSO,继续通入气体a为SO 形成NaHSO 过饱和溶液,由已知
2 3 2 3
信息①可知过滤得到NaSO 晶体,最后脱水得到NaSO;
2 2 5 2 2 5
(1)由于二氧化碳的溶解性不大,在碱性溶液中溶解更多,反应I中先通入气体NH 使溶液呈碱
3
性,能更好溶解二氧化碳,由已知信息①可知继续通入气体a为SO 形成NaHSO 过饱和溶液,反
2 3
应III中通入的气体a为SO ;
2
(2)溶液A为NH Cl,检验溶液A中离子X即铵根的方法是:取少量溶液于试管,向试管中加
4
入NaOH溶液,加热,用湿润红色石蕊试纸靠近试管口,若试纸变蓝,则证明有NH;
(3)反应III调节pH为4.1,SO 和饱和碳酸钠溶液反应生成NaHSO,发生反应的离子方程式为
2 3
CO +HO=2HSO CO;
+2SO2 2 + 2
(4)再次通入气体a得到溶液B的目的是得到NaHSO 过饱和溶液;
3
(5)已知焦亚硫酸钠(Na SO)在空气中易氧化,在氮气氛围中可防止被氧化,操作I为:低温蒸
2 2 5
发,冷却结晶,过滤,洗涤;用饱和SO (aq)洗涤NaSO 晶体的目的是减少NaSO 在水中的溶解;
2 2 2 5 2 2 5
(6) Na SO 在空气中易氧化,久置的NaSO 固体与氧气发生氧化还原反应生成NaSO ,反应
2 2 5 2 2 5 2 4
的化学反应方程式为NaSO+HO+O=NaSO +HSO 。
2 2 5 2 2 2 4 2 4