文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题15
1.常温下,下列各组离子在给定溶液中可能大量共存的是
A.麦芽糖溶液中:MnO K+、H+、NO
、
B.能使苯酚溶液显紫色的溶液中:SO、HCO Na+、Cl-
、
C.水电离出来的c(H+)=10-13mol·L-1的溶液中:K+、CO Br-、AlO
、
D.滴加甲基橙显红色的水溶液中:NH、K+、SO Cl-
2 、
2.下列离子方程式书写正确的是
A.NaHS水解:HS-+HO S2-+HO+
2 3
B.向FeI 溶液中通入少量Cl:2Fe2++Cl=2Fe3++2Cl-
2 2 2
C.向0.1mol·L-1NaHA溶液(pH=1)加入NaOH溶液:HA-+OH-=A2-+HO
2
D.用过量氨水吸收工业尾气中的SO :2NH ∙HO+SO =2NH+SO O
2 3 2 2 +H2
3.火箭推进发生反应的化学方程式为:C HN+2NO=2CO↑+4HO↑+3N↑(偏二甲肼中C、
2 8 2 2 4 2 2 2
N元素的化合价相等)。下列说法正确的是
A. C HN 是氧化剂 B. NO 被氧化
2 8 2 2 4
C. 氧化产物与还原产物之比为3∶2 D. N O 完全反应,有8N 个电子转移
2 4 A
4.下列反应的离子方程式正确的是
A. 明矾溶于水产生Al(OH) 胶体:Al3++3HO=Al(OH) ↓+3H+
3 2 3
B. 向二元弱酸HPO 溶液中滴入足量烧碱溶液:HPO +3OH-=PO 3HO
3 3 3 3 + 2
C.NaNH中加入硫酸中:HN2-+2H+=NH ↑
2 3
D. 实验室用过氧化钡与稀硫酸反应制备双氧水:BaO+2H++SO=BaSO↓+HO
2 4 2 2
5.下列反应的离子方程式不正确的是
A.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO OH-+Ca2+=MgCO ↓+CaCO ↓+2HO
+2 3 3 2
B.次氯酸钙溶液中通入过量的二氧化碳气体:CO+HO+ClO-=HCO
2 2 +HClO
C.次氯酸钠溶液吸收过量二氧化硫气体:SO +HO+ClO-=SO+Cl-+2H+
2 2
D.氯化铁溶液与过量硫化钠溶液反应:2Fe3++3S2-=2FeS↓+S↓
6.下列物质性质实验对应的离子方程式书写正确的是
A.钠与CuSO 溶液反应:2Na+Cu2+=Cu↓+2Na+
4
B.用碳酸钠溶液处理水垢中的硫酸钙:CO 2+=CaCO ↓
+Ca 3
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO+2HO
2
D.酸性KMnO 溶液中滴加HO 溶液:2MnO O+6H+=2Mn2++5O ↑+8H O
4 2 2 +5H2 2 2 2
7.列解释实验事实的化学方程式正确的是
A.形成NaCl的过程:
B.用FeCl 溶液“腐蚀”覆铜板:Fe3++Cu===Fe2++Cu2+
3
C.用石墨电极电解CuCl 溶液:2Cl-+2H+=====H↑+Cl↑
2 2 2
D.“84”消毒液中加少量醋增强漂白性:ClO-+H+===HClO
8.下列解释事实的方程式不正确的是A.用明矾净化水:Al3++3HO Al(OH) +3H+
2 3
B.氢氧化亚铁暴露于空气中变色:4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 3
C.常温下0.1 mol·L-1氨水的pH约为11:NH ·H O=NH+OH-
3 2
D.氢氧化钠溶液吸收氯气:Cl+2OH-=Cl-+ClO-+HO
2 2
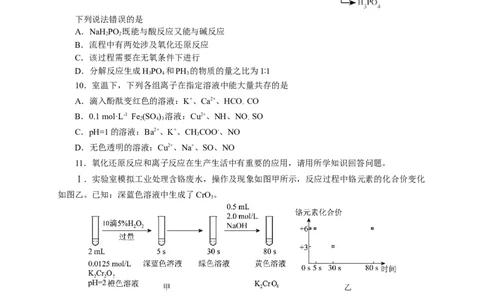
9.磷化氢(PH )是一种在空气中能自燃的剧毒气体,可通过以下流程制取:
3
下列说法错误的是
A.NaH PO 既能与酸反应又能与碱反应
2 2
B.流程中有两处涉及氧化还原反应
C.该过程需要在无氧条件下进行
D.分解反应生成HPO 和PH 的物质的量之比为1∶1
3 4 3
10.室温下,下列各组离子在指定溶液中能大量共存的是
A.滴入酚酞变红色的溶液:K+、Ca2+、HCO CO
、
B.0.1 mol·L-1 Fe (SO ) 溶液:Cu2+、NH、NO SO
2 4 3 、
C.pH=1的溶液:Ba2+、K+、CHCOO-、NO
3
D.无色透明的溶液:Cu2+、Na+、SO、NO
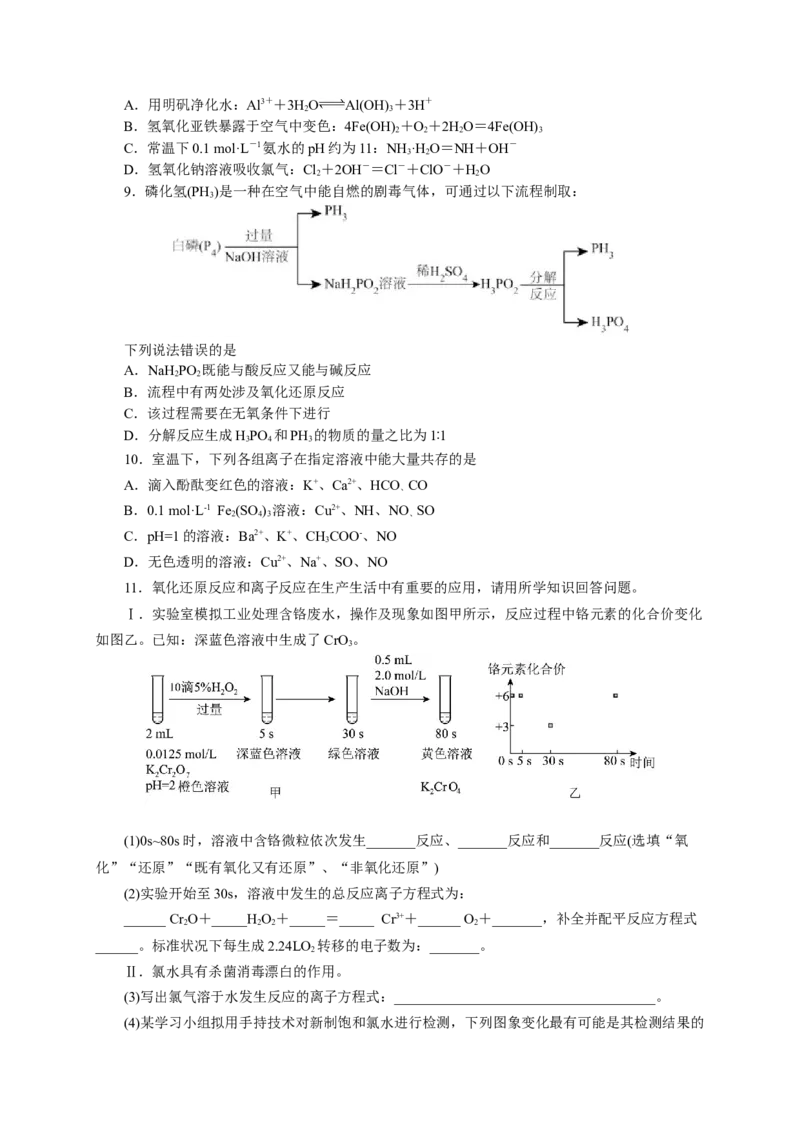
11.氧化还原反应和离子反应在生产生活中有重要的应用,请用所学知识回答问题。
Ⅰ.实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变化
如图乙。已知:深蓝色溶液中生成了CrO。
3
(1)0s~80s时,溶液中含铬微粒依次发生_______反应、_______反应和_______反应(选填“氧
化”“还原”“既有氧化又有还原”、“非氧化还原”)
(2)实验开始至30s,溶液中发生的总反应离子方程式为:
______ Cr O+_____HO+_____=_____ Cr3++______ O +_______,补全并配平反应方程式
2 2 2 2
______。标准状况下每生成2.24LO 转移的电子数为:_______。
2
Ⅱ.氯水具有杀菌消毒漂白的作用。
(3)写出氯气溶于水发生反应的离子方程式:_____________________________________。
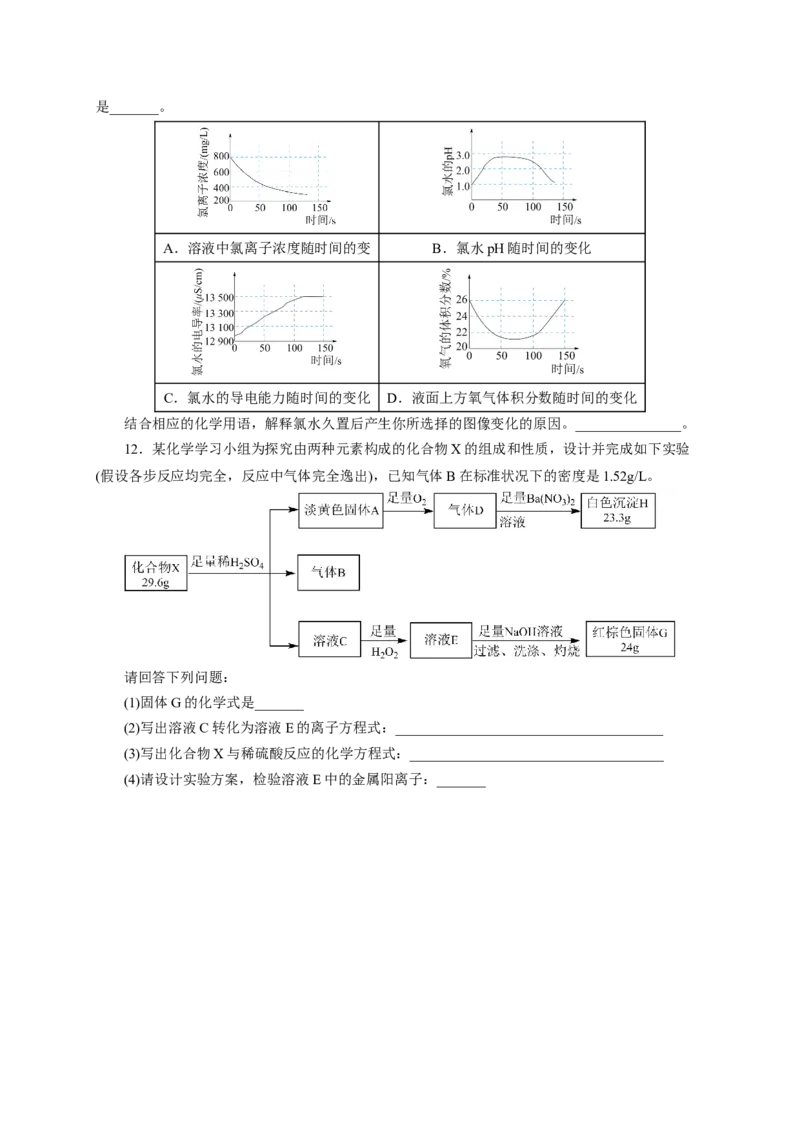
(4)某学习小组拟用手持技术对新制饱和氯水进行检测,下列图象变化最有可能是其检测结果的是_______。
A.溶液中氯离子浓度随时间的变 B.氯水pH随时间的变化
C.氯水的导电能力随时间的变化 D.液面上方氧气体积分数随时间的变化
结合相应的化学用语,解释氯水久置后产生你所选择的图像变化的原因。_______________。
12.某化学学习小组为探究由两种元素构成的化合物X的组成和性质,设计并完成如下实验
(假设各步反应均完全,反应中气体完全逸出),已知气体B在标准状况下的密度是1.52g/L。
请回答下列问题:
(1)固体G的化学式是_______
(2)写出溶液C转化为溶液E的离子方程式:______________________________________
(3)写出化合物X与稀硫酸反应的化学方程式:____________________________________
(4)请设计实验方案,检验溶液E中的金属阳离子:_______