文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题21
1. 下列离子共存的判断或离子方程式书写正确的是
A. 甲基橙显黄色的溶液中可存在大量以下离子:Cu2+、K+、CO Cl-
、
B. 强酸性溶液中可存在大量以下离子:SO ClO-、Na+
、
C. 将过氧化钠投入水中:2NaO+2HO=4Na++4OH-+O↑
2 2 2 2
D. 氨化的CaCl 溶液中通入过量CO:2NH +Ca2++CO+HO =CaCO ↓+2NH
2 2 3 2 2 3
2.下列各组离子在指定溶液中能大量共存的是
A. 中性溶液中:Fe3+、Na+、SO、NO
B. lg=10的溶液中:Na+、K+、CHCOO-、Cl-
3
C. 明矾溶液中:NH、K+、I-、Br-
D. 加入铝粉会产生H 的溶液中:Cu2+、Mg2+、NO ClO-
2 、
3.为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为0.1mol·L-1)。
3 3 2 3
实验 操作与现象
① 在5mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mLFeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶
② 3 2 3 3 6
液,产生蓝色沉淀。
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两
2 3 3
③ 份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色
3 6
沉淀。
依据上述实验现象,结论不合理的是
A. 实验①说明加热促进Fe3+水解反应
B. 实验②说明Fe3+既发生了水解反应,又发生了还原反应
C. 实验③说明Fe3+发生了水解反应,但没有发生还原反应
D. 整个实验说明SO Fe3+的水解反应无影响,但对还原反应有影响
对
4.某100mL溶液可能含有Na+、NH、Fe3+、CO SO、Cl-中的若干种,取该溶液进行连续实
、
验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法正确的是
A. 原溶液可能存在 Cl-和Na+
B. 原溶液一定存在CO SO和NH,一定不存在 Fe3+、Na+、Cl-
、
C. 原溶液中 c(CO是 0.01mol•L-1
)
D. 若原溶液中不存在 Na+,则c(Cl-)=0.1mol•L-15.利用NaClO氧化尿素制备NH·H O(水合肼),同时可制备NaSO ,制备流程如图所示:
2 4 2 2 3
已知:NH·H O有强还原性,NH·H O能与NaClO反应生成N;0.1mo1/L亚硫酸钠溶液的
2 4 2 2 4 2 2
pH约为9.5。
下列说法错误的是
A. 步骤I反应时,若产物中n(NaClO)∶n(NaClO)=5∶1,则n(NaCl)∶n(NaClO)=2∶1
3
B. 步骤II中须将尿素缓慢加入NaClO碱性溶液中
C. 步骤II反应的离子方程式为C1O-+CO(NH )+2OH-=C1-+N H·H O+CO
2 2 2 4 2
D. 步骤IV中反应过程中控制溶液为碱性,有利于吸收SO
2
6.向30mL1.0mol·L-1的HSO 和3 mL 30%的HO 的混合溶液中加入经处理过的铁丝,铁丝表
2 4 2 2
面产生气泡,随后消失,再产生气泡,再消失,周而往复,振荡周期(现象重复出现的时间间隔)为
20 s左右,可维持数小时。一种可能的反应机理为:
(a)Fe+2H+=Fe2++H↑ (b)2Fe2++HO+HO=Fe O+4H+
2 2 2 2 2 3
(c) Fe O+6H+=2Fe3++3HO (d)2Fe3++H=2Fe2++2H+
2 3 2 2
下列说法错误的是
A. 该振荡反应与H+浓度的变化有关 B. Fe O、Fe3+为中间产物
2 3
C. 冰水浴比室温条件下的振荡周期要短 D. 由该机理可知:产生的气体是H
2
7.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 小苏打溶液中:K+、Na+、Br-、AlO
B. =1012的溶液中:[Ag(NH)]+、K+、Cl-、NO
3 2
C. pH=7的溶液中:NH、Fe3+、Cl-、SO
D. 水电离的c(OH-)=1×10-13mol·L-1的溶液中:K+、Cl-、CHCOO-、Cu2+
3
8.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正
确的是
A. 在含Ba(OH) 、KOH的混合溶液中缓慢通入CO:KOH、Ba(OH) 、KCO、BaCO
2 2 2 2 3 3
B. 在含AlO、OH-、CO OH-、CO 、Al(OH)
的溶液中逐滴加入盐酸: 、AlO 3
C. 在含NH、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、NH、Al(OH)
3
D. 在含有Fe2+、Ag+、Cu2+、H+等离子且浓度相等的溶液中加入锌粉:H+、Ag+、Cu2+、Fe2+
9.关于反应2NaNH +N O=NaN +NaOH+NH ,下列说法正确的是
2 2 3 3
A. NaN 溶液通入CO 可以得到HN (酸性与醋酸相当)
3 2 3
B. 氧化剂和还原剂的物质的量之比为2∶1
C. NaN 既是还原产物又是氧化产物
3D. 生成1molNaN ,共转移4mol电子
3
10.下列离子方程式书写正确的是
A. 用FeS除去废水中的Hg2+:S2-+Hg2+=HgS↓
B. 向饱和食盐水中加浓盐酸析出固体:Na+(aq)+Cl-(aq) NaCl(s)
C. 在NaS溶液中滴加NaClO溶液:S2-+ClO-+2H+=S↓+Cl-+H O
2 2
D. 向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:2Fe3++Fe=3Fe2+
3
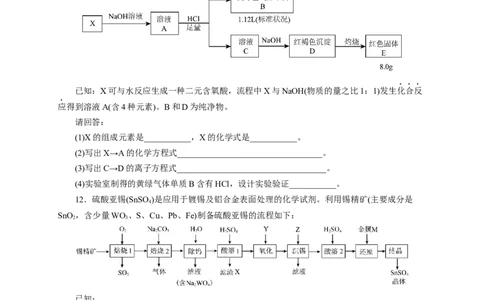
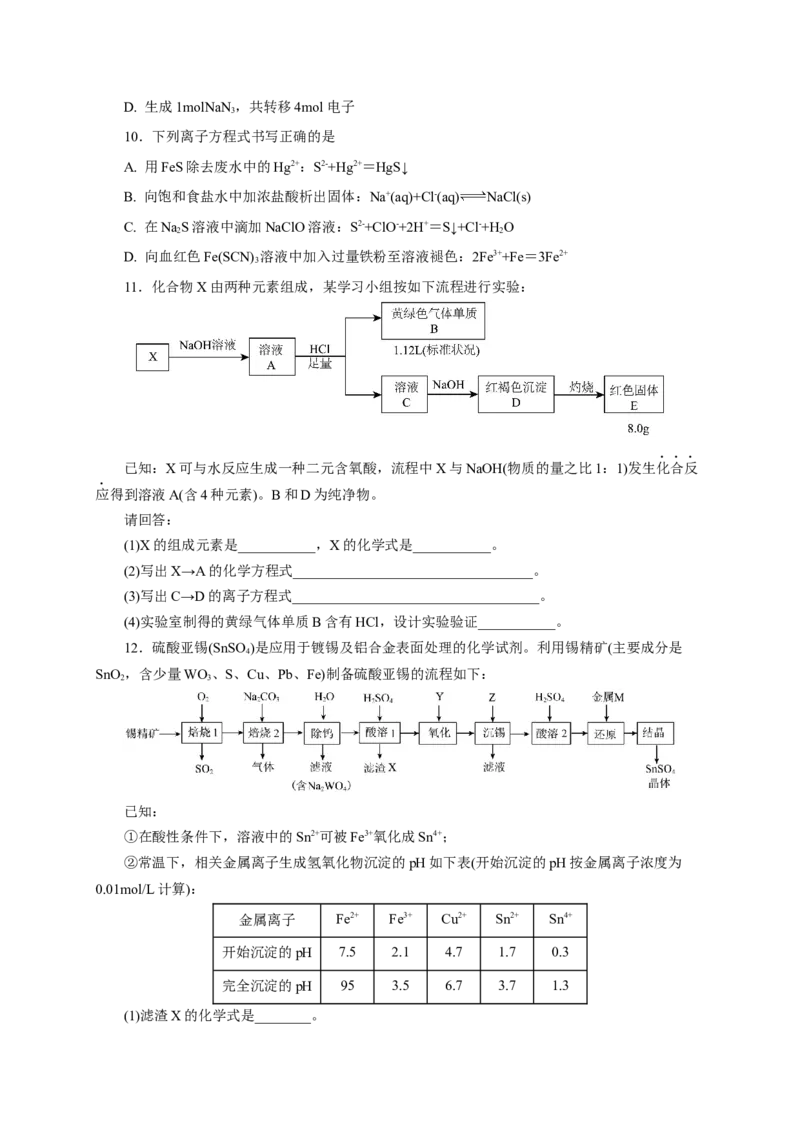
11.化合物X由两种元素组成,某学习小组按如下流程进行实验:
已知:X可与水反应生成一种二元含氧酸,流程中X与NaOH(物质的量之比1:1)发生化合反
应得到溶液A(含4种元素)。B和D为纯净物。
请回答:
(1)X的组成元素是___________,X的化学式是___________。
(2)写出X→A的化学方程式__________________________________。
(3)写出C→D的离子方程式___________________________________。
(4)实验室制得的黄绿气体单质B含有HCl,设计实验验证___________。
12.硫酸亚锡(SnSO )是应用于镀锡及铝合金表面处理的化学试剂。利用锡精矿(主要成分是
4
SnO ,含少量WO、S、Cu、Pb、Fe)制备硫酸亚锡的流程如下:
2 3
已知:
①在酸性条件下,溶液中的Sn2+可被Fe3+氧化成Sn4+;
②常温下,相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为
0.01mol/L计算):
金属离子 Fe2+ Fe3+ Cu2+ Sn2+ Sn4+
开始沉淀的pH 7.5 2.1 4.7 1.7 0.3
完全沉淀的pH 95 3.5 6.7 3.7 1.3
(1)滤渣X的化学式是________。(2)焙烧2中WO 发生反应的化学方程式是_______________________________。
3
(3)若氧化时不引入新的杂质,则足量的Y溶液与金属离子发生反应的离子方程式为________。
(4)利用表格数据,计算Sn(OH) 的K =________;沉锡控制溶液pH的范围是________;试剂
4 sp
Z可以是________(填字母)。
a.Ca(OH) b.Fe O c.NH HCO 溶液 d.氨水
2 2 3 4 3
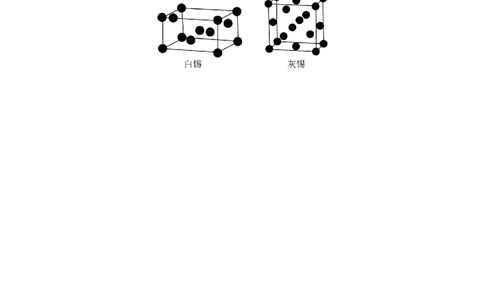
(5)锡有多种同素异形体,其中白锡为四方晶系,晶胞参数a=b=0.5832nm,c=0.3181nm,灰锡
为立方晶系,晶胞参数a=0.6489nm(如图)。在低温下,白锡转化为灰锡的现象常被称为锡疫。列式
比较并说明发生“锡疫”时体积如何变化_______________________________________。