文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题21
1. 下列离子共存的判断或离子方程式书写正确的是
A. 甲基橙显黄色的溶液中可存在大量以下离子:Cu2+、K+、CO Cl-
、
B. 强酸性溶液中可存在大量以下离子:SO ClO-、Na+
、
C. 将过氧化钠投入水中:2NaO+2HO=4Na++4OH-+O↑
2 2 2 2
D. 氨化的CaCl 溶液中通入过量CO:2NH +Ca2++CO+HO =CaCO ↓+2NH
2 2 3 2 2 3
答案:C
解析:A.甲基橙显黄色的溶液中含有大量的OH-,则Cu2++2OH-=Cu(OH) ↓,Cu2+
2
+CO ↓,A错误;
=CuCO3
B.强酸性溶液中含有大量的H+,则SO ClO-=SO+Cl-,B错误;
+
C.将过氧化钠投入水中的离子方程式为:2NaO+2HO=4Na++4OH-+O↑,C正确;
2 2 2 2
D.氨化的CaCl 溶液中通入过量CO 的离子方程式为:NH ∙HO+CO=HCO NH,D错误;
2 2 3 2 2 +
2.下列各组离子在指定溶液中能大量共存的是
A. 中性溶液中:Fe3+、Na+、SO、NO
B. lg=10的溶液中:Na+、K+、CHCOO-、Cl-
3
C. 明矾溶液中:NH、K+、I-、Br-
D. 加入铝粉会产生H 的溶液中:Cu2+、Mg2+、NO ClO-
2 、
答案:C
解析:A.中性溶液中Fe3+会发生水解,生成氢氧化铁沉淀,不能共存,A项错误;
B.lg=10的溶液中显酸性,酸性条件下,CHCOO-与氢离子会结合,不能共存,B项错误;
3
C.明矾溶液中存在Al3+,Al3+、NH、K+、I-、Br-互不反应,能大量共存,C项正确;
D.加入铝粉会产生H 的溶液中可能显酸性也可能显碱性,酸性条件下,ClO-不能大量共存,
2
碱性条件下,Cu2+、Mg2+不能大量共存,D项错误;
3.为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为0.1mol·L-1)。
3 3 2 3
实验 操作与现象
① 在5mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mLFeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶
② 3 2 3 3 6
液,产生蓝色沉淀。
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两
2 3 3
③ 份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色
3 6
沉淀。
依据上述实验现象,结论不合理的是
A. 实验①说明加热促进Fe3+水解反应
B. 实验②说明Fe3+既发生了水解反应,又发生了还原反应
C. 实验③说明Fe3+发生了水解反应,但没有发生还原反应D. 整个实验说明SO Fe3+的水解反应无影响,但对还原反应有影响
对
答案:D
解析:铁离子水解显酸性,亚硫酸根离子水解显碱性,两者之间存在相互促进的水解反应,同
时铁离子具有氧化性,亚硫酸根离子具有还原性,两者还会发生氧化还原反应,在同一反应体系中,
铁离子的水解反应与还原反应共存并相互竞争,结合实验分析如下:实验①为对照实验,说明铁离
子在水溶液中显棕黄色,存在水解反应Fe3++3H O Fe(OH) +3H+,煮沸,促进水解平衡正向移动,
2 3
得到红褐色的氢氧化铁胶体;实验②说明少量亚硫酸根离子加入铁离子后,两者发生水解反应得到
红褐色的氢氧化铁胶体;根据铁氰化钾检测结果可知,同时发生氧化还原反应,使铁离子被还原为
亚铁离子,而出现特征蓝色沉淀;实验③通过反滴操作,根据现象描述可知,溶液仍存在铁离子的
水解反应,但由于铁离子少量,没检测出亚铁离子的存在,说明铁离子的水解反应速率快,铁离子
的还原反应未来得及发生。
A.铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生
成较多的氢氧化铁,从而使溶液显红褐色,故A正确;
B.在5mLFeCl 溶液中滴加2滴同浓度的NaSO 溶液,根据现象和分析可知,Fe3+既发生了水
3 2 3
解反应,生成红褐色的氢氧化铁,又被亚硫酸根离子还原,得到亚铁离子,加入铁氰化钾溶液后,
出现特征蓝色沉淀,故B正确;
C.实验③中在5mL Na SO 溶液中滴加2滴同浓度少量FeCl 溶液,根据现象和分析可知,仍
2 3 3
发生铁离子的水解反应,但未来得及发生铁离子的还原反应,即水解反应比氧化还原反应速率快,
故C正确;
D.结合三组实验,说明铁离子与亚硫酸根离子混合时,铁离子的水解反应占主导作用,比氧
化还原反应的速率快,因证据不足,不能说明亚硫酸离子对铁离子的水解作用无影响,事实上,亚
硫酸根离子水解显碱性,可促进铁离子的水解反应,故D错误。
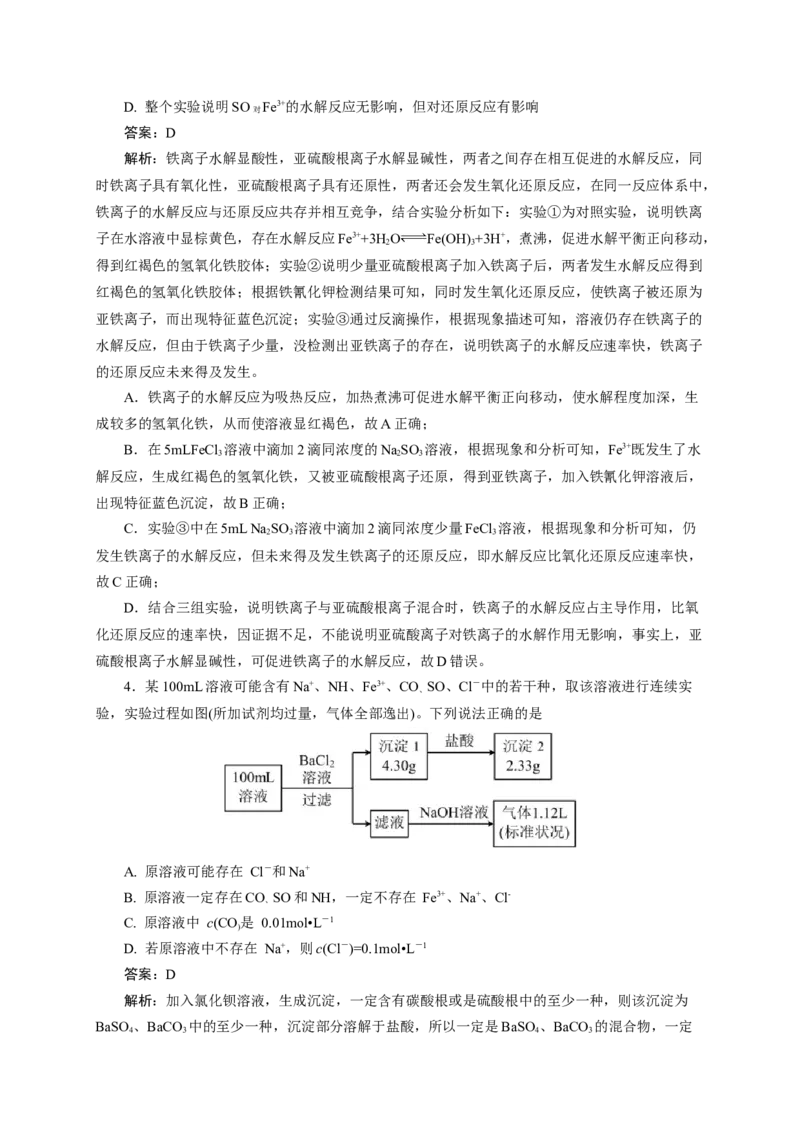
4.某100mL溶液可能含有Na+、NH、Fe3+、CO SO、Cl-中的若干种,取该溶液进行连续实
、
验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法正确的是
A. 原溶液可能存在 Cl-和Na+
B. 原溶液一定存在CO SO和NH,一定不存在 Fe3+、Na+、Cl-
、
C. 原溶液中 c(CO是 0.01mol•L-1
)
D. 若原溶液中不存在 Na+,则c(Cl-)=0.1mol•L-1
答案:D
解析:加入氯化钡溶液,生成沉淀,一定含有碳酸根或是硫酸根中的至少一种,则该沉淀为
BaSO、BaCO 中的至少一种,沉淀部分溶解于盐酸,所以一定是BaSO、BaCO 的混合物,一定
4 3 4 3存在CO SO,硫酸钡沉淀是2.33g,n(SO)=n(BaSO )===0.01mol,n(CO=n(BaCO)===
、 4 ) 3
0.01mol,碳酸根和铁离子不共存,一定不存在Fe3+,所得到的滤液中加入氢氧化钠,出现气体,为
氨气,一定含有NH,n(NH)=n(NH)===0.05mol,正电荷量为0.05mol,负电荷量为
3
0.01mol×2+0.01mol×2=0.04mol<0.05mol,根据电荷守恒可知,一定含有Cl-,可能含有Na+,则
n(Cl-)≥0.01mol,据此分析解答。
由上述分析可知,原溶液中一定含有0.01mol SO、0.01mol CO ≥0.01molCl-,可能含有
、0.05mol NH
Na+,一定不含有Fe3+;
A.由上述分析可知,原溶液中一定含有Cl-,可能含有Na+,故A错误;
B.由上述分析可知,原溶液中一定含有SO、CO +,一定不含有Fe3+,故B正确;
,可能含有Na
C.碳酸根离子的物质的量是n(CO===0.01mol,则c(CO===0.1mol·L-1 ,故C错误;
) )
D.若原溶液中不存在Na+,根据电荷守恒可知,n(Cl-)=0.01mol, c(Cl-)===0.1mol·L-1,
故D错误;
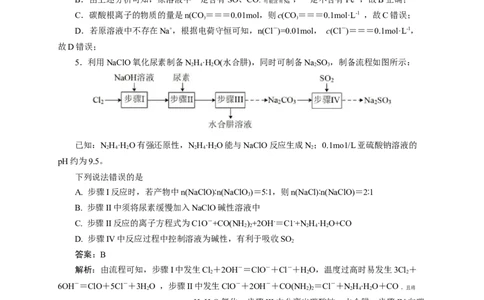
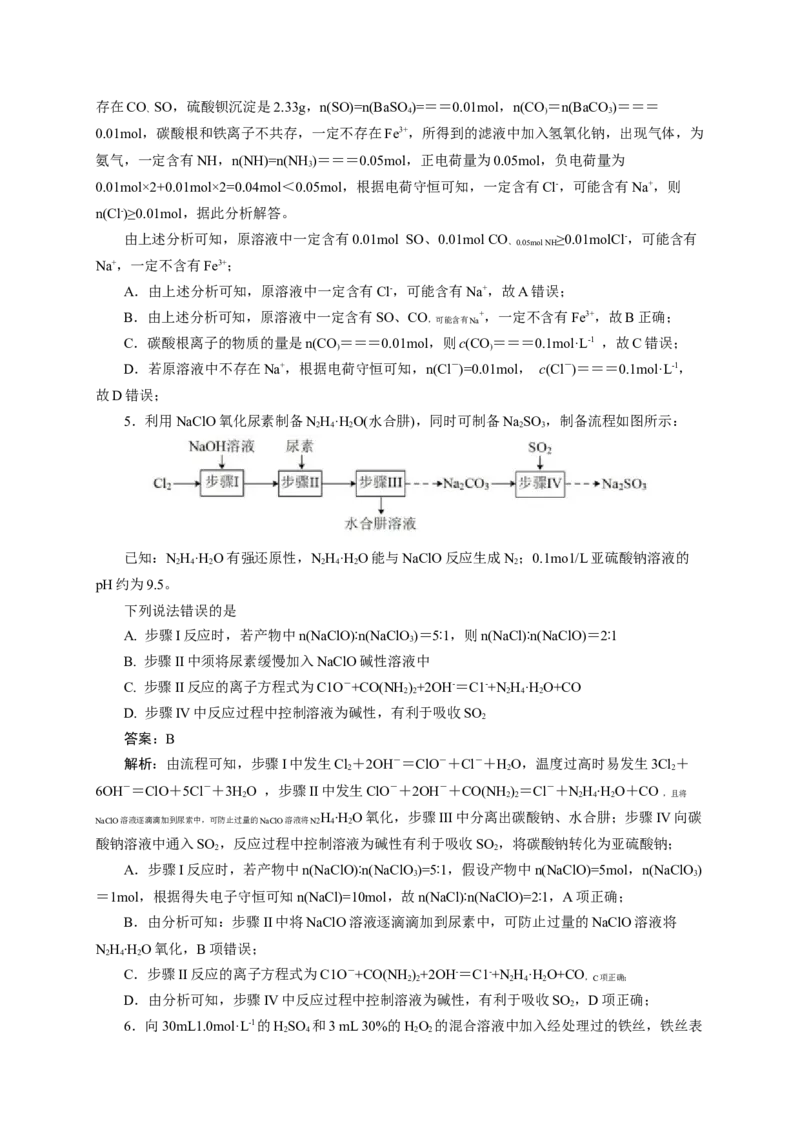
5.利用NaClO氧化尿素制备NH·H O(水合肼),同时可制备NaSO ,制备流程如图所示:
2 4 2 2 3
已知:NH·H O有强还原性,NH·H O能与NaClO反应生成N;0.1mo1/L亚硫酸钠溶液的
2 4 2 2 4 2 2
pH约为9.5。
下列说法错误的是
A. 步骤I反应时,若产物中n(NaClO)∶n(NaClO)=5∶1,则n(NaCl)∶n(NaClO)=2∶1
3
B. 步骤II中须将尿素缓慢加入NaClO碱性溶液中
C. 步骤II反应的离子方程式为C1O-+CO(NH )+2OH-=C1-+N H·H O+CO
2 2 2 4 2
D. 步骤IV中反应过程中控制溶液为碱性,有利于吸收SO
2
答案:B
解析:由流程可知,步骤I中发生Cl+2OH-=ClO-+Cl-+HO,温度过高时易发生3Cl+
2 2 2
6OH-=ClO+5Cl-+3HO ,步骤II中发生ClO-+2OH-+CO(NH)=Cl-+NH∙HO+CO
2 2 2 2 4 2 ,且将
H∙HO氧化,步骤III中分离出碳酸钠、水合肼;步骤IV向碳
NaClO溶液逐滴滴加到尿素中,可防止过量的NaClO溶液将N2 4 2
酸钠溶液中通入SO ,反应过程中控制溶液为碱性有利于吸收SO ,将碳酸钠转化为亚硫酸钠;
2 2
A.步骤I反应时,若产物中n(NaClO)∶n(NaClO)=5∶1,假设产物中n(NaClO)=5mol,n(NaClO)
3 3
=1mol,根据得失电子守恒可知n(NaCl)=10mol,故n(NaCl)∶n(NaClO)=2∶1,A项正确;
B.由分析可知:步骤II中将NaClO溶液逐滴滴加到尿素中,可防止过量的NaClO溶液将
NH∙HO氧化,B项错误;
2 4 2
C.步骤II反应的离子方程式为C1O-+CO(NH )+2OH-=C1-+N H·H O+CO
2 2 2 4 2 ,C项正确;
D.由分析可知,步骤IV中反应过程中控制溶液为碱性,有利于吸收SO ,D项正确;
2
6.向30mL1.0mol·L-1的HSO 和3 mL 30%的HO 的混合溶液中加入经处理过的铁丝,铁丝表
2 4 2 2面产生气泡,随后消失,再产生气泡,再消失,周而往复,振荡周期(现象重复出现的时间间隔)为
20 s左右,可维持数小时。一种可能的反应机理为:
(a)Fe+2H+=Fe2++H↑ (b)2Fe2++HO+HO=Fe O+4H+
2 2 2 2 2 3
(c) Fe O+6H+=2Fe3++3HO (d)2Fe3++H=2Fe2++2H+
2 3 2 2
下列说法错误的是
A. 该振荡反应与H+浓度的变化有关 B. Fe O、Fe3+为中间产物
2 3
C. 冰水浴比室温条件下的振荡周期要短 D. 由该机理可知:产生的气体是H
2
答案:C
解析:A.四步反应的总反应为Fe+HO+2H+=Fe2++2HO,反应物浓度影响反应速率,故
2 2 2
该振荡反应与H+浓度的变化有关,A正确;
B.Fe O、Fe3+在反应中生成又消耗,为中间产物,B正确;
2 3
C.温度越低,反应速率越慢,则冰水浴比室温条件下的振荡周期要长,C错误;
D.由该机理可知:产生的气体只能是H,D正确;
2
7.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 小苏打溶液中:K+、Na+、Br-、AlO
B. =1012的溶液中:[Ag(NH)]+、K+、Cl-、NO
3 2
C. pH=7的溶液中:NH、Fe3+、Cl-、SO
D. 水电离的c(OH-)=1×10-13mol·L-1的溶液中:K+、Cl-、CHCOO-、Cu2+
3
答案:B
解析:A.小苏打为NaHCO ,HCO 和HO反应生成CO
3 、AlO 2 和氢氧化铝沉淀,不能大量共存,A错误;
B.=1012>0,即c(OH-)>c(H+),溶液显碱性,[Ag(NH)]+、K+、Cl-和NO
3 2 在碱性环境下可大量共存,B正
确;
C.pH=7的溶液,可能为NH Cl和NH ∙HO的混合溶液,则Fe3+与NH ∙HO反应生成氢氧化
4 3 2 3 2
铁沉淀,不能大量共存,C错误;
D.水电离的c(OH-)=1×10-13mol·L-1,说明水的电离受到抑制,溶液可能为酸溶液,也可能为
碱溶液,若为酸溶液,CHCOO-与H+结合为醋酸而不能大量共存,若为碱溶液,Cu2+与OH-反应
3
生成氢氧化铜沉淀而不能大量共存,D错误;
8.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正
确的是
A. 在含Ba(OH) 、KOH的混合溶液中缓慢通入CO:KOH、Ba(OH) 、KCO、BaCO
2 2 2 2 3 3
B. 在含AlO、OH-、CO OH-、CO 、Al(OH)
的溶液中逐滴加入盐酸: 、AlO 3
C. 在含NH、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、NH、Al(OH)
3
D. 在含有Fe2+、Ag+、Cu2+、H+等离子且浓度相等的溶液中加入锌粉:H+、Ag+、Cu2+、Fe2+
答案:C
解析:A.在含Ba(OH) 、KOH的混合溶液中缓慢通入CO,首先会生成碳酸钡沉淀,故氢氧
2 2
化钡首先反应,A错误;B.在含AlO、OH-、CO
的溶液中逐滴加入盐酸,氢离子首先和氢氧根离子生成水、和偏铝酸根离子生成氢氧化铝沉淀、和碳酸根离子生成碳酸
氢根离子,B错误;
C.在含NH、Al3+、H+的溶液中逐滴加入KOH溶液,氢氧根离子首先和氢离子生成水、和铝
离子生成氢氧化铝沉淀、和铵根离子生成一水合氨,再和氢氧化铝生成偏铝酸根离子,C正确;
D.在含有Fe2+、Ag+、Cu2+、H+等离子且浓度相等的溶液中加入锌粉,锌首先会置换出银离子、
铜离子,再和氢离子、亚铁离子反应,D错误;
9.关于反应2NaNH +N O=NaN +NaOH+NH ,下列说法正确的是
2 2 3 3
A. NaN 溶液通入CO 可以得到HN (酸性与醋酸相当)
3 2 3
B. 氧化剂和还原剂的物质的量之比为2∶1
C. NaN 既是还原产物又是氧化产物
3
D. 生成1molNaN ,共转移4mol电子
3
答案:C
解析:A.由HN 的酸性与醋酸相当可知,NaN 溶液通入二氧化碳不可能生成HN ,否则违背
3 3 3
强酸制弱酸的原理,故A错误;
B.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则氧化剂一氧化二氮和还原剂氨基钠的物质的量之比为1∶2,故B错误;
C.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则NaN 既是还原产物又是氧化产物,故C正确;
3
D.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则反应生成1molNaN ,共转移电子的物质的量为1mol××2=mol,故D错误;
3
10.下列离子方程式书写正确的是
A. 用FeS除去废水中的Hg2+:S2-+Hg2+=HgS↓
B. 向饱和食盐水中加浓盐酸析出固体:Na+(aq)+Cl-(aq) NaCl(s)
C. 在NaS溶液中滴加NaClO溶液:S2-+ClO-+2H+=S↓+Cl-+H O
2 2
D. 向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:2Fe3++Fe=3Fe2+
3
答案:B
解析:A.FeS为沉淀不能拆,用FeS除去废水中的Hg2+:FeS+Hg2+ HgS↓+Fe2+,A错误;
B.向饱和食盐水中加浓盐酸,氯离子浓度增大,促使氯离子和钠离子析出氯化钠固体:Na+
(aq)+Cl-(aq) NaCl(s),B正确;
C.在NaS溶液中滴加NaClO溶液发生氧化还原反应生成硫单质和氯离子、同时生成氢氧根
2
离子:S2-+ClO-+H O=S↓+Cl-+2OH-,C错误;
2D.Fe(SCN) 为络合物不能拆,向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:
3 3
2Fe(SCN) +Fe=6SCN-+3Fe2+,D错误;
3
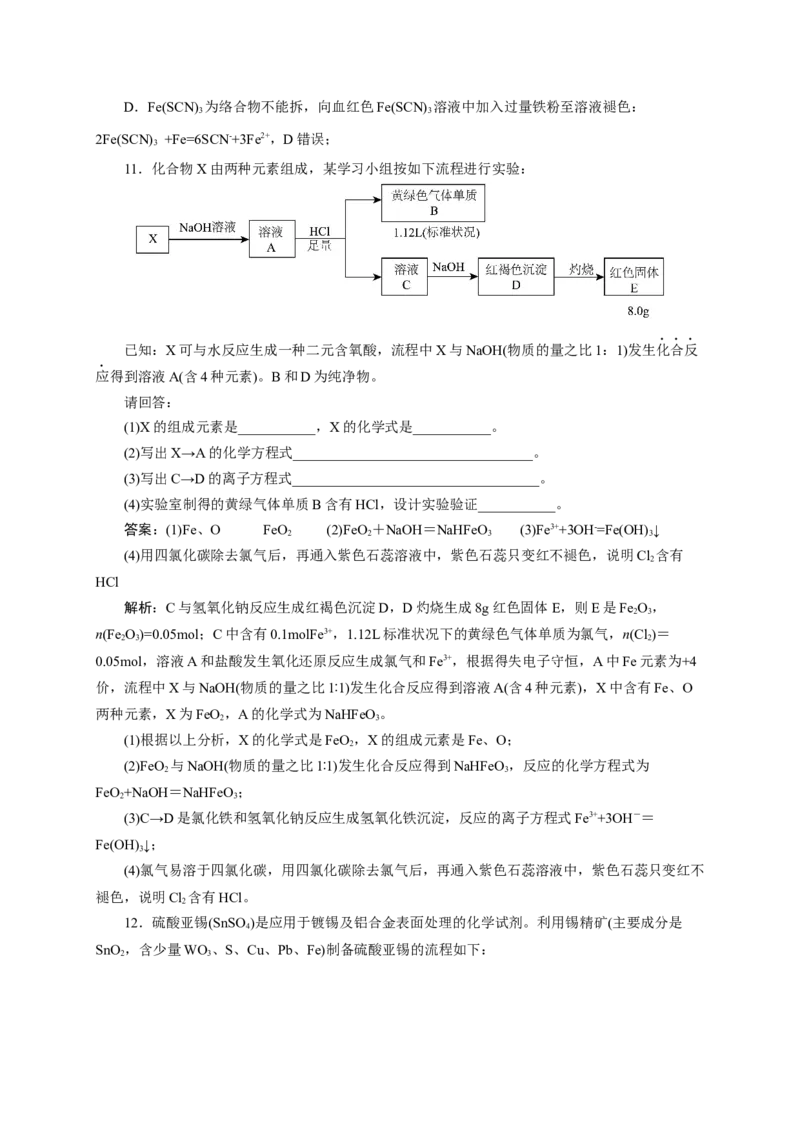
11.化合物X由两种元素组成,某学习小组按如下流程进行实验:
已知:X可与水反应生成一种二元含氧酸,流程中X与NaOH(物质的量之比1:1)发生化合反
应得到溶液A(含4种元素)。B和D为纯净物。
请回答:
(1)X的组成元素是___________,X的化学式是___________。
(2)写出X→A的化学方程式__________________________________。
(3)写出C→D的离子方程式___________________________________。
(4)实验室制得的黄绿气体单质B含有HCl,设计实验验证___________。
答案:(1)Fe、O FeO (2)FeO +NaOH=NaHFeO (3)Fe3++3OH-=Fe(OH) ↓
2 2 3 3
(4)用四氯化碳除去氯气后,再通入紫色石蕊溶液中,紫色石蕊只变红不褪色,说明Cl 含有
2
HCl
解析:C与氢氧化钠反应生成红褐色沉淀D,D灼烧生成8g红色固体E,则E是Fe O,
2 3
n(Fe O)=0.05mol;C中含有0.1molFe3+,1.12L标准状况下的黄绿色气体单质为氯气,n(Cl )=
2 3 2
0.05mol,溶液A和盐酸发生氧化还原反应生成氯气和Fe3+,根据得失电子守恒,A中Fe元素为+4
价,流程中X与NaOH(物质的量之比1∶1)发生化合反应得到溶液A(含4种元素),X中含有Fe、O
两种元素,X为FeO,A的化学式为NaHFeO 。
2 3
(1)根据以上分析,X的化学式是FeO,X的组成元素是Fe、O;
2
(2)FeO 与NaOH(物质的量之比1∶1)发生化合反应得到NaHFeO ,反应的化学方程式为
2 3
FeO+NaOH=NaHFeO ;
2 3
(3)C→D是氯化铁和氢氧化钠反应生成氢氧化铁沉淀,反应的离子方程式Fe3++3OH-=
Fe(OH) ↓;
3
(4)氯气易溶于四氯化碳,用四氯化碳除去氯气后,再通入紫色石蕊溶液中,紫色石蕊只变红不
褪色,说明Cl 含有HCl。
2
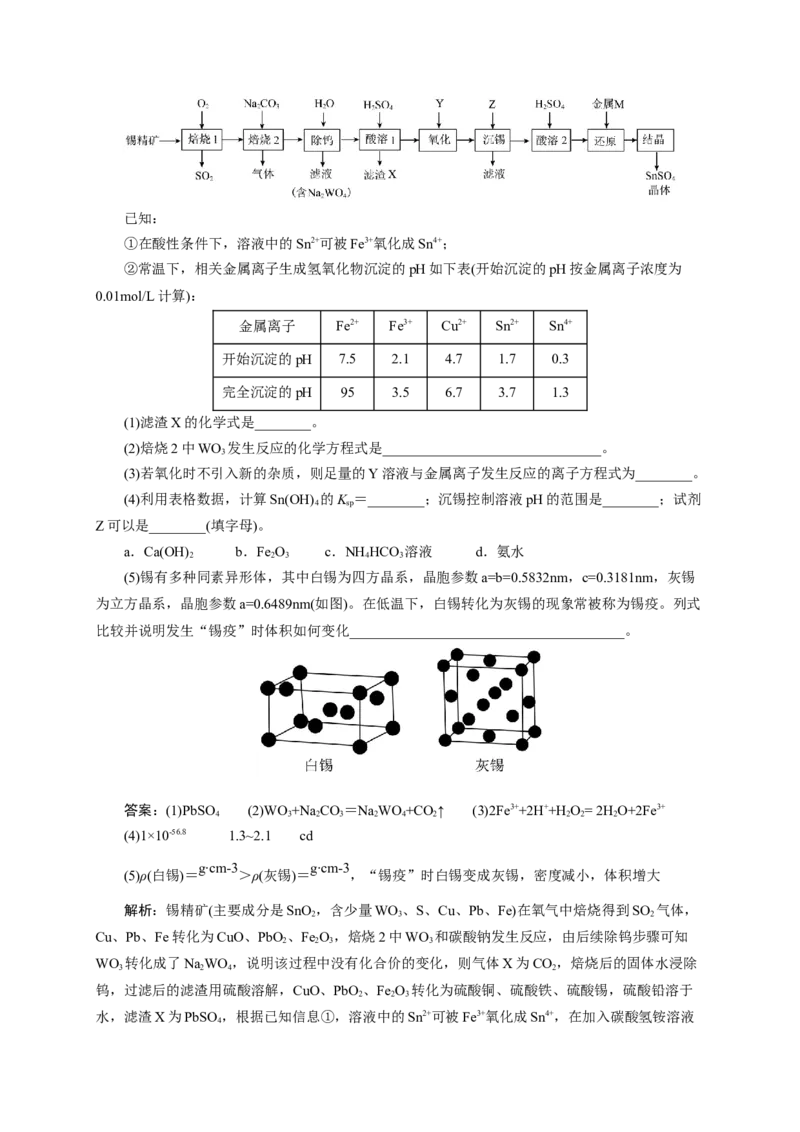
12.硫酸亚锡(SnSO )是应用于镀锡及铝合金表面处理的化学试剂。利用锡精矿(主要成分是
4
SnO ,含少量WO、S、Cu、Pb、Fe)制备硫酸亚锡的流程如下:
2 3已知:
①在酸性条件下,溶液中的Sn2+可被Fe3+氧化成Sn4+;
②常温下,相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为
0.01mol/L计算):
金属离子 Fe2+ Fe3+ Cu2+ Sn2+ Sn4+
开始沉淀的pH 7.5 2.1 4.7 1.7 0.3
完全沉淀的pH 95 3.5 6.7 3.7 1.3
(1)滤渣X的化学式是________。
(2)焙烧2中WO 发生反应的化学方程式是_______________________________。
3
(3)若氧化时不引入新的杂质,则足量的Y溶液与金属离子发生反应的离子方程式为________。
(4)利用表格数据,计算Sn(OH) 的K =________;沉锡控制溶液pH的范围是________;试剂
4 sp
Z可以是________(填字母)。
a.Ca(OH) b.Fe O c.NH HCO 溶液 d.氨水
2 2 3 4 3
(5)锡有多种同素异形体,其中白锡为四方晶系,晶胞参数a=b=0.5832nm,c=0.3181nm,灰锡
为立方晶系,晶胞参数a=0.6489nm(如图)。在低温下,白锡转化为灰锡的现象常被称为锡疫。列式
比较并说明发生“锡疫”时体积如何变化_______________________________________。
答案:(1)PbSO (2)WO +Na CO=NaWO+CO ↑ (3)2Fe3++2H++H O= 2H O+2Fe3+
4 3 2 3 2 4 2 2 2 2
(4)1×10-56.8 1.3~2.1 cd
g∙cm-3 g∙cm-3
(5)ρ(白锡)= >ρ(灰锡)= ,“锡疫”时白锡变成灰锡,密度减小,体积增大
解析:锡精矿(主要成分是SnO ,含少量WO、S、Cu、Pb、Fe)在氧气中焙烧得到SO 气体,
2 3 2
Cu、Pb、Fe转化为CuO、PbO 、Fe O,焙烧2中WO 和碳酸钠发生反应,由后续除钨步骤可知
2 2 3 3
WO 转化成了NaWO,说明该过程中没有化合价的变化,则气体X为CO,焙烧后的固体水浸除
3 2 4 2
钨,过滤后的滤渣用硫酸溶解,CuO、PbO 、Fe O 转化为硫酸铜、硫酸铁、硫酸锡,硫酸铅溶于
2 2 3
水,滤渣X为PbSO ,根据已知信息①,溶液中的Sn2+可被Fe3+氧化成Sn4+,在加入碳酸氢铵溶液
4调节pH沉锡,得到的固体在硫酸中溶解,再加入Sn单质将Sn4+还原为Sn2+得到SnSO ,以此解答。
4
(1)酸溶之前的步骤中,已经把S、W除去了,加入硫酸溶解时,硫酸铜、硫酸铁、硫酸锡都是
可溶于水的,但硫酸铅难溶于水,所以滤渣X就是硫酸铅PbSO 。
4
(2)焙烧2中WO 和碳酸钠发生反应,由后续除钨步骤可知WO 转化成了NaWO,说明该过程
3 3 2 4
中没有化合价的变化,则气体X为CO,化学方程式为:WO+Na CO=Na WO+CO ↑。
2 3 2 3 2 4 2
(3)氧化步骤是的目的是将Fe2+氧化为Fe3+,Y是能把Fe2+氧化成Fe3+的物质,且不引入新的杂
质,则Y为HO,该过程的离子方程式为:2Fe3++2H++H O= 2H O+2Fe3+。
2 2 2 2 2
(4)由表格数据可知,c(Sn4+)=0.01mol/L的溶液中,当pH=0.3时,Sn4+开始沉淀生成Sn(OH),
4
()4
则Sn(OH) 的K =c4(OH-)c(Sn4+)= ×0.01=1×10-56.8;要能使Sn4+全部沉淀,还不能沉淀其它离子,
4 sp
根据表格信息,沉淀pH应在1.3~2.1范围内;Z用碳酸氢铵溶液或氨水最合适,碳酸氢根或一水合
氨可以和氢离子反应,消耗溶液中的氢离子,达到调pH的目的;a的碱性太强,很容易使溶液pH
过高,b是固体,可能会和沉淀出来的氢氧化锡混在一起,引入杂质,故选cd。
g∙cm-3
(5)由白锡晶胞结构可知,其中Sn原子的个数为8×+4×+1=4,密度为ρ(白锡)= ,由灰
g∙cm-3
锡的晶胞结构可知,其中Sn原子的个数为8×+6×+4=8,密度为ρ(灰锡)= ,则ρ(白锡)=
g∙cm-3 g∙cm-3
>ρ(灰锡)= ,“锡疫”时白锡变成灰锡,密度减小,体积增大。