文档内容
2024 高考一轮复习收官卷
第 2 模拟
时间:100分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 N 14 O16 Cl 35.5 K 39 Fe 56 Cu 64 Zn 65
一、选择题(每小题只有一个正确选项,共16×3分)
1.(2023·山西晋城·晋城市第一中学校校考模拟预测)中华文化源远流长,化学与文化传承密不可分。下
列说法错误的是
A.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
B.长沙走马楼出土的竹木简牍主要成分是纤维素
C.青铜器“四羊方尊”的主要材质为合金
D.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
2.(2023·辽宁鞍山·统考一模)下列有关化学用语表示正确的是
A.HClO的电子式:
B.O 的分子结构空间模型:
3
C.基态As原子的电子排布式:[Ar]3d104s24p3
D.反式聚异戊二烯的结构简式:
3.(2023·河南焦作·博爱县第一中学校考三模)N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.11.2LCH 和44.8LCl (均为标准状况)在光照下充分反应后的分子数为2.5N
4 2 A
B.28g乙烯和丙烯的混合气体充分燃烧,消耗的O 分子数为4N
2 A
C.1mol14C16O(一氧化碳)中含有15N 个中子
A
D.1molNaHSO 固体中含离子总数为3N
4 A
4.(2023·福建福州·统考模拟预测)下列有关离子方程式书写正确的是
A.明矾净水的原理:
B.用小苏打治疗胃酸过多:
C.用醋酸和碘化钾淀粉溶液检验加碘盐中的 :
D.用纯碱溶液浸泡锅炉水垢( ):
5.(2022·浙江·校联考二模)关于反应 ,下列说法
不正确的是
A. 既是氧化剂又是还原剂B. 发生还原反应
C.若有 加反应,被 还原的 为
D.反应若生成 ,转移 电子
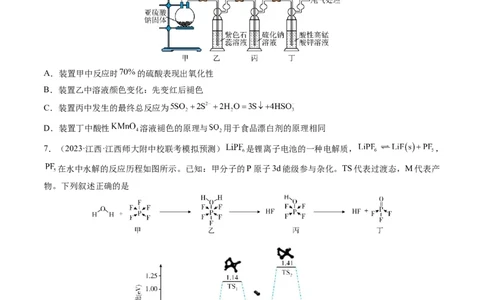
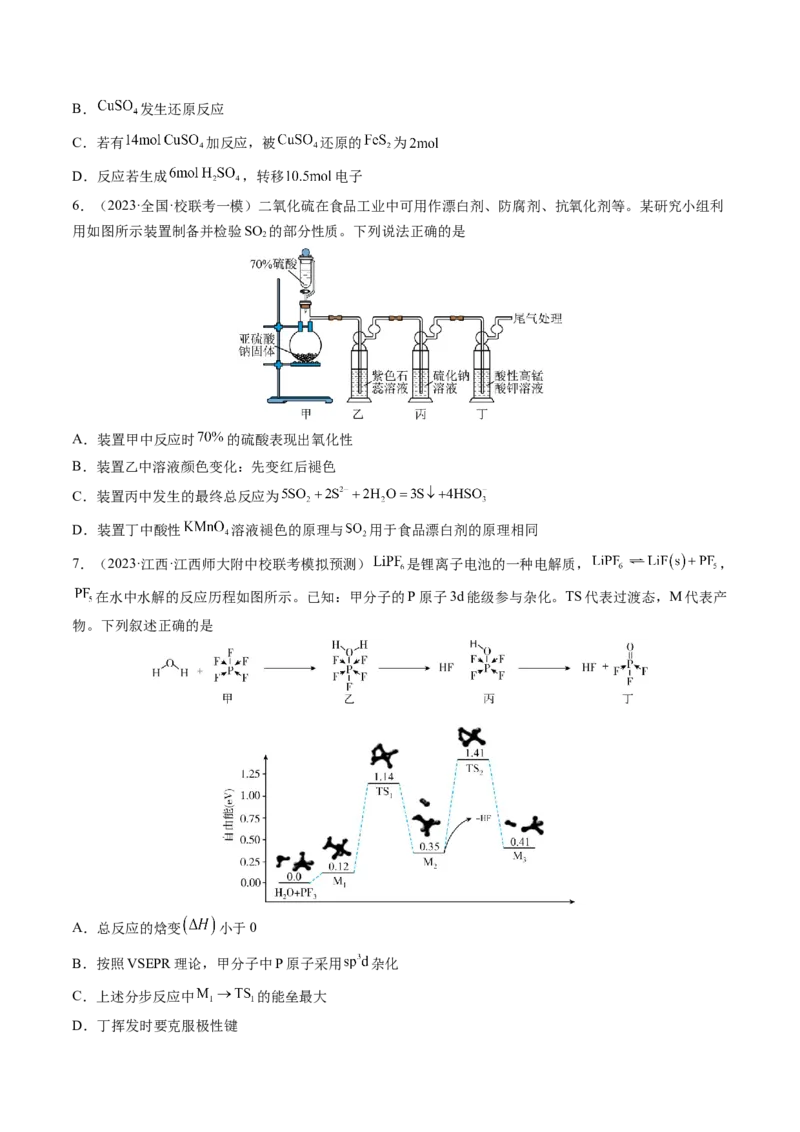
6.(2023·全国·校联考一模)二氧化硫在食品工业中可用作漂白剂、防腐剂、抗氧化剂等。某研究小组利
用如图所示装置制备并检验SO 的部分性质。下列说法正确的是
2
A.装置甲中反应时 的硫酸表现出氧化性
B.装置乙中溶液颜色变化:先变红后褪色
C.装置丙中发生的最终总反应为
D.装置丁中酸性 溶液褪色的原理与 用于食品漂白剂的原理相同
7.(2023·江西·江西师大附中校联考模拟预测) 是锂离子电池的一种电解质, ,
在水中水解的反应历程如图所示。已知:甲分子的P原子3d能级参与杂化。TS代表过渡态,M代表产
物。下列叙述正确的是
A.总反应的焓变 小于0
B.按照VSEPR理论,甲分子中P原子采用 杂化
C.上述分步反应中 的能垒最大
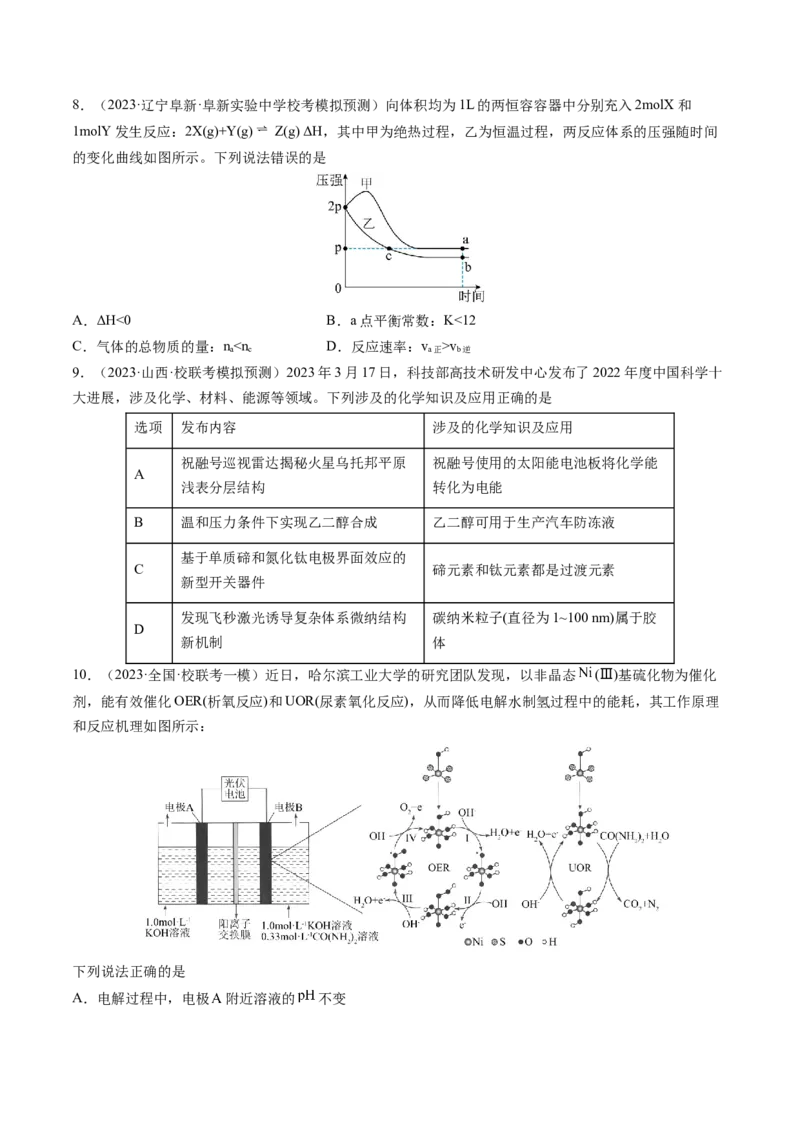
D.丁挥发时要克服极性键8.(2023·辽宁阜新·阜新实验中学校考模拟预测)向体积均为1L的两恒容容器中分别充入2molX和
1molY发生反应:2X(g)+Y(g) Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间
的变化曲线如图所示。下列说法错误的是
A.ΔH<0 B.a点平衡常数:K<12
C.气体的总物质的量:nv
a c a正 b逆
9.(2023·山西·校联考模拟预测)2023年3月17日,科技部高技术研发中心发布了2022年度中国科学十
大进展,涉及化学、材料、能源等领域。下列涉及的化学知识及应用正确的是
选项 发布内容 涉及的化学知识及应用
祝融号巡视雷达揭秘火星乌托邦平原 祝融号使用的太阳能电池板将化学能
A
浅表分层结构 转化为电能
B 温和压力条件下实现乙二醇合成 乙二醇可用于生产汽车防冻液
基于单质碲和氮化钛电极界面效应的
C 碲元素和钛元素都是过渡元素
新型开关器件
发现飞秒激光诱导复杂体系微纳结构 碳纳米粒子(直径为1~100 nm)属于胶
D
新机制 体
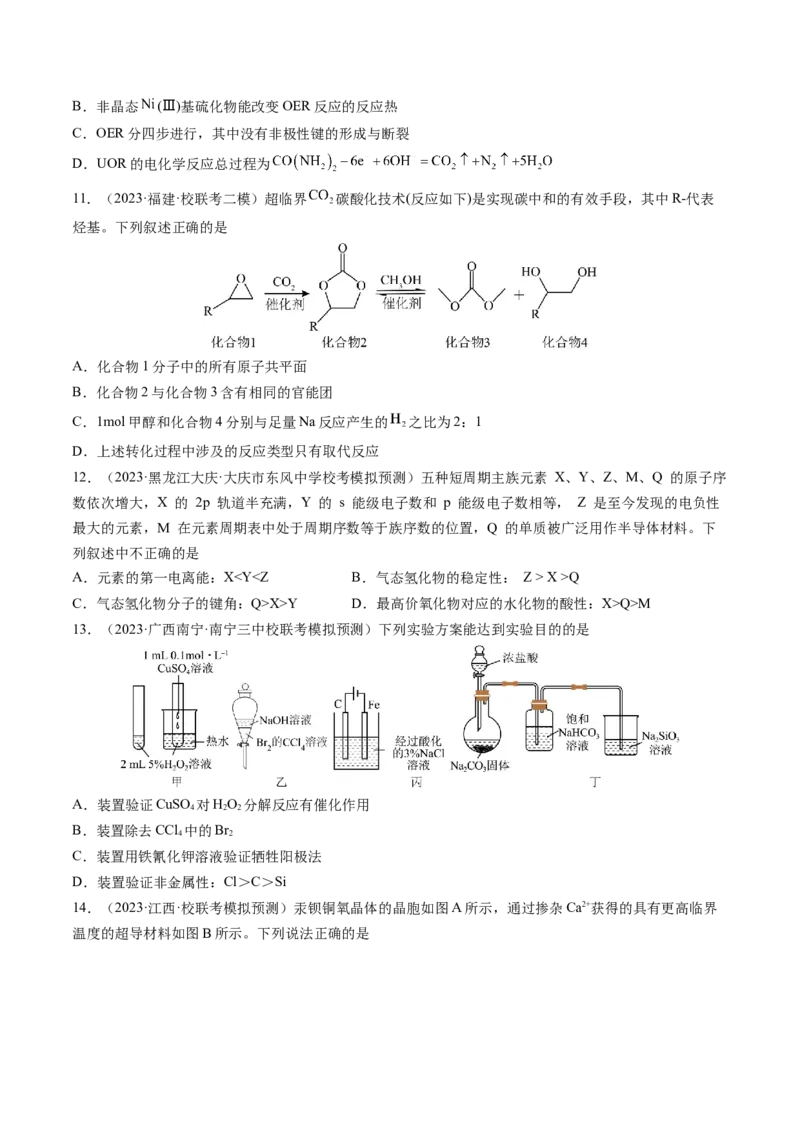
10.(2023·全国·校联考一模)近日,哈尔滨工业大学的研究团队发现,以非晶态 (Ⅲ)基硫化物为催化
剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理
和反应机理如图所示:
下列说法正确的是
A.电解过程中,电极 附近溶液的 不变B.非晶态 (Ⅲ)基硫化物能改变OER反应的反应热
C.OER分四步进行,其中没有非极性键的形成与断裂
D.UOR的电化学反应总过程为
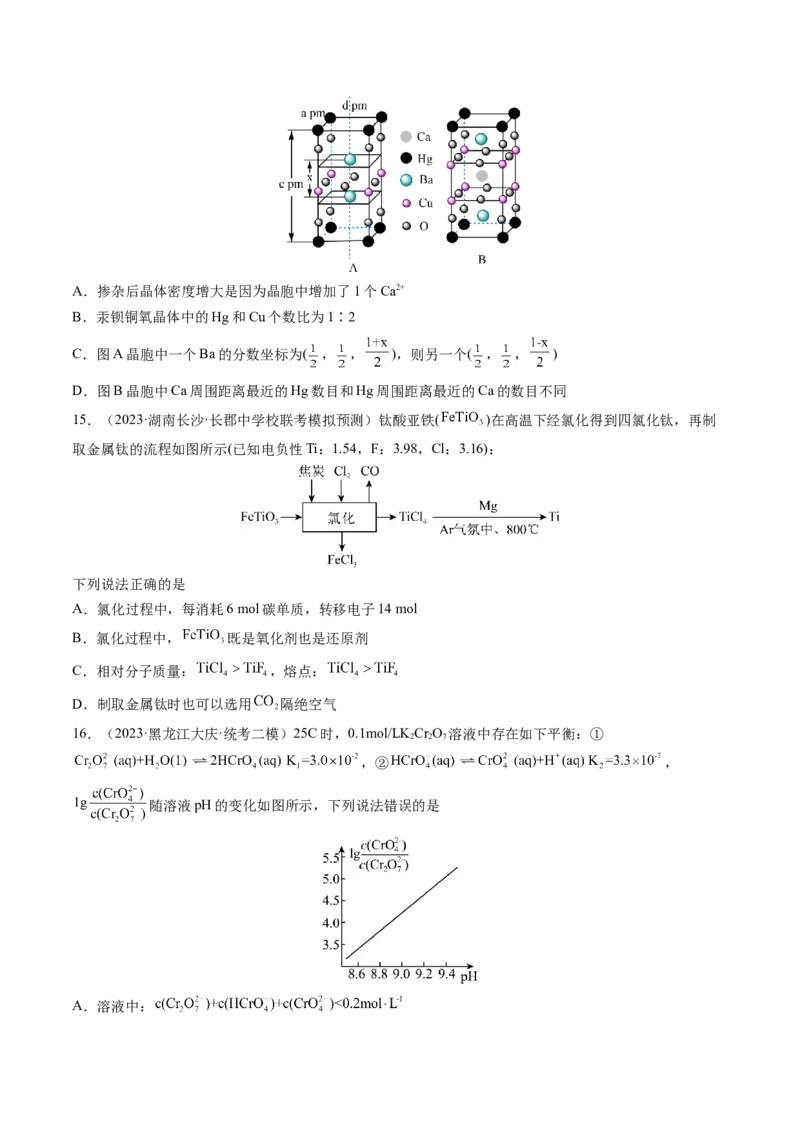
11.(2023·福建·校联考二模)超临界 碳酸化技术(反应如下)是实现碳中和的有效手段,其中R-代表
烃基。下列叙述正确的是
A.化合物1分子中的所有原子共平面
B.化合物2与化合物3含有相同的官能团
C.1mol甲醇和化合物4分别与足量Na反应产生的 之比为2:1
D.上述转化过程中涉及的反应类型只有取代反应
12.(2023·黑龙江大庆·大庆市东风中学校考模拟预测)五种短周期主族元素 X、Y、Z、M、Q 的原子序
数依次增大,X 的 2p 轨道半充满,Y 的 s 能级电子数和 p 能级电子数相等, Z 是至今发现的电负性
最大的元素,M 在元素周期表中处于周期序数等于族序数的位置,Q 的单质被广泛用作半导体材料。下
列叙述中不正确的是
A.元素的第一电离能:X X >Q
C.气态氢化物分子的键角:Q>X>Y D.最高价氧化物对应的水化物的酸性:X>Q>M
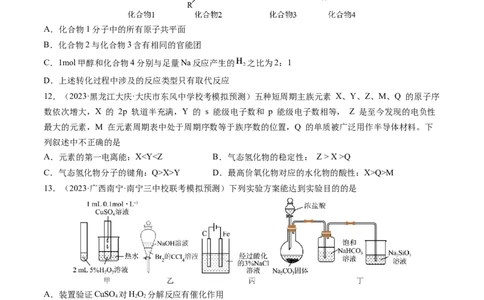
13.(2023·广西南宁·南宁三中校联考模拟预测)下列实验方案能达到实验目的的是
A.装置验证CuSO 对HO 分解反应有催化作用
4 2 2
B.装置除去CCl 中的Br
4 2
C.装置用铁氰化钾溶液验证牺牲阳极法
D.装置验证非金属性:Cl>C>Si
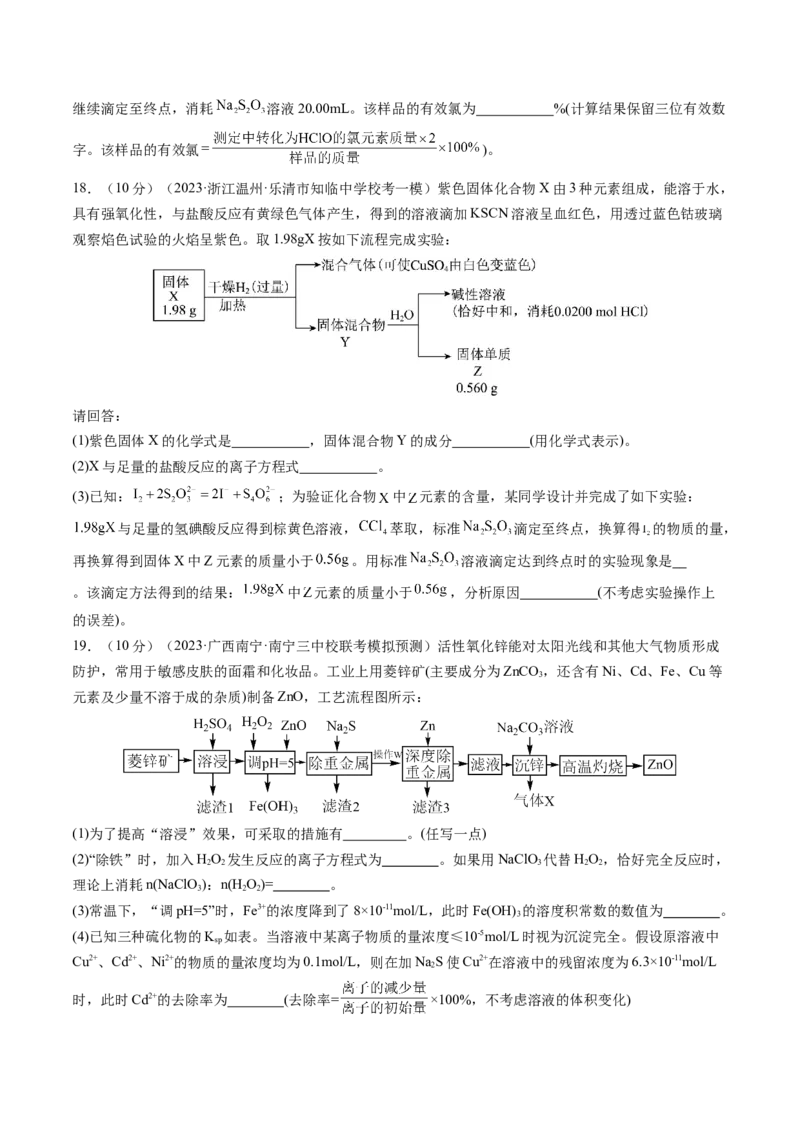
14.(2023·江西·校联考模拟预测)汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界
温度的超导材料如图B所示。下列说法正确的是A.掺杂后晶体密度增大是因为晶胞中增加了1个Ca2+
B.汞钡铜氧晶体中的Hg和Cu个数比为1∶2
C.图A晶胞中一个Ba的分数坐标为( , , ),则另一个( , , )
D.图B晶胞中Ca周围距离最近的Hg数目和Hg周围距离最近的Ca的数目不同
15.(2023·湖南长沙·长郡中学校联考模拟预测)钛酸亚铁( )在高温下经氯化得到四氯化钛,再制
取金属钛的流程如图所示(已知电负性Ti:1.54,F:3.98,Cl:3.16):
下列说法正确的是
A.氯化过程中,每消耗6 mol碳单质,转移电子14 mol
B.氯化过程中, 既是氧化剂也是还原剂
C.相对分子质量: ,熔点:
D.制取金属钛时也可以选用 隔绝空气
16.(2023·黑龙江大庆·统考二模)25C时,0.1mol/LK Cr O 溶液中存在如下平衡:①
2 2 7
,② ,
随溶液pH的变化如图所示,下列说法错误的是
A.溶液中:B.向KCr O 溶液中加入少量NaSO 固体,溶液的pH不变
2 2 7 2 4
C.溶液中
D.当溶液pH=9.0时,HCrO 的平衡浓度:
二、主观题(共5小题,共52分)
17.(10分)(2023·湖南长沙·长郡中学校联考模拟预测)DCCNa( )是一种高效、安全的消毒
杀菌剂。它常温下为白色固体,难溶于冷水,受热易分解。实验室利用NaClO溶液和氰尿酸( )溶
液反应制备DCCNa,实验装置如图所示:
已知:
回答下列问题:
(1)仪器a的名称为 。
(2)装置A中发生的离子反应方程式为 。
(3)当装置B的三颈烧瓶内液面上方有黄绿色气体时,再加入氰尿酸溶液。并在整个过程中不断通入一定量
的氯气,其原因是 。
(4)实验过程中B的温度必须保持为7~12℃,pH控制在6.5~8.5的范围。若温度过高,pH过低,会发生副
反应生成 和 等,写出该副反应的化学方程式: 。
(5)装置C的试剂可选用 (填标号)。
a. b.NaCl c. d.
(6)反应结束后,装置B中的浊液经过滤、 、干燥得DCCNa粗产品。
(7)有效氯含量是判断产品质量的标准。通过下列方法测定有效氯含量的原理为:
准确称取1.2000g样品,配成250 mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI
溶液,密封在暗处静置5min;用0.1000 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗 溶液20.00mL。该样品的有效氯为 %(计算结果保留三位有效数
字。该样品的有效氯 )。
18.(10分)(2023·浙江温州·乐清市知临中学校考一模)紫色固体化合物X由3种元素组成,能溶于水,
具有强氧化性,与盐酸反应有黄绿色气体产生,得到的溶液滴加KSCN溶液呈血红色,用透过蓝色钴玻璃
观察焰色试验的火焰呈紫色。取1.98gX按如下流程完成实验:
请回答:
(1)紫色固体X的化学式是 ,固体混合物Y的成分 (用化学式表示)。
(2)X与足量的盐酸反应的离子方程式 。
(3)已知: ;为验证化合物 中 元素的含量,某同学设计并完成了如下实验:
与足量的氢碘酸反应得到棕黄色溶液, 萃取,标准 滴定至终点,换算得 的物质的量,
再换算得到固体X中Z元素的质量小于 。用标准 溶液滴定达到终点时的实验现象是
。该滴定方法得到的结果: 中 元素的质量小于 ,分析原因 (不考虑实验操作上
的误差)。
19.(10分)(2023·广西南宁·南宁三中校联考模拟预测)活性氧化锌能对太阳光线和其他大气物质形成
防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO ,还含有Ni、Cd、Fe、Cu等
3
元素及少量不溶于成的杂质)制备ZnO,工艺流程图所示:
(1)为了提高“溶浸”效果,可采取的措施有 。(任写一点)
(2)“除铁”时,加入HO 发生反应的离子方程式为 。如果用NaClO 代替HO,恰好完全反应时,
2 2 3 2 2
理论上消耗n(NaClO):n(H O)= 。
3 2 2
(3)常温下,“调pH=5”时,Fe3+的浓度降到了8×10-11mol/L,此时Fe(OH) 的溶度积常数的数值为 。
3
(4)已知三种硫化物的K 如表。当溶液中某离子物质的量浓度≤10-5mol/L时视为沉淀完全。假设原溶液中
sp
Cu2+、Cd2+、Ni2+的物质的量浓度均为0.1mol/L,则在加NaS使Cu2+在溶液中的残留浓度为6.3×10-11mol/L
2
时,此时Cd2+的去除率为 (去除率= ×100%,不考虑溶液的体积变化)物质 CdS CuS NiS
K 8.0×10-27 6.3×10-36 1.0×10-26
sp
(5)“沉锌”时,在近中性条件下加入NaCO 可得碱式碳酸锌[ZnCO•2Zn(OH)•H O]固体,同时产生大量的
2 3 3 2 2
气体。该反应的离子方程式为 。
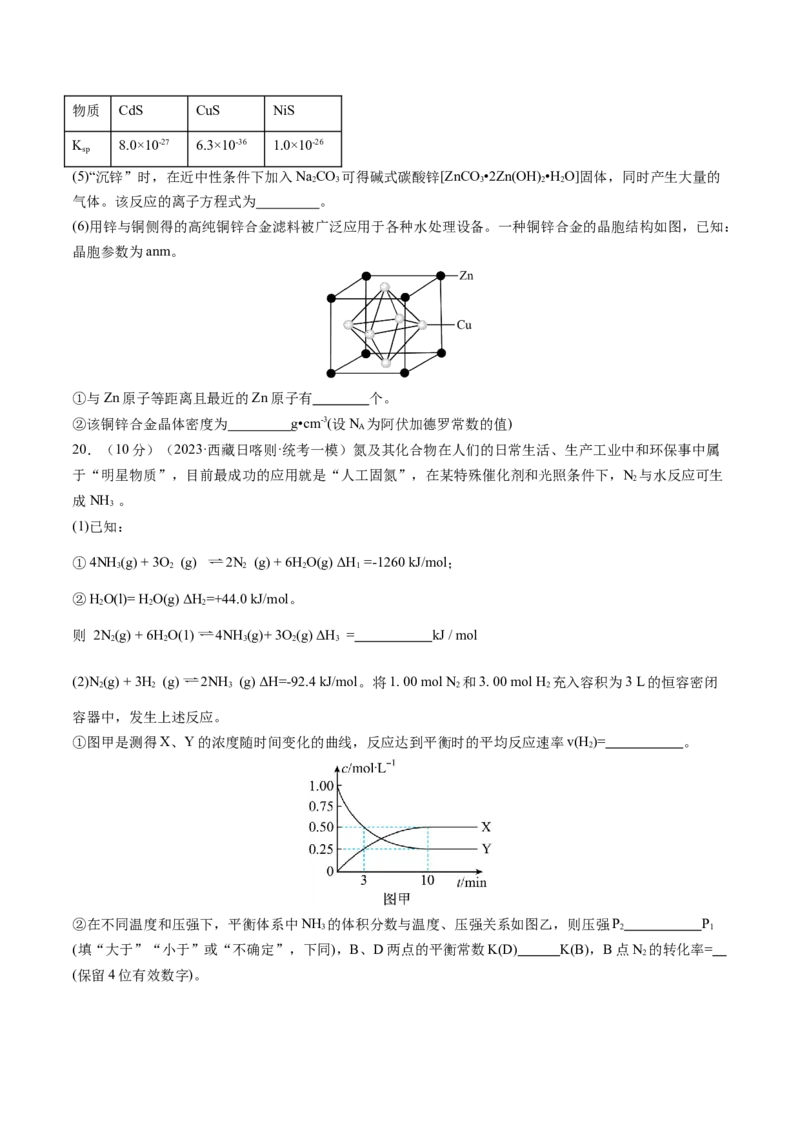
(6)用锌与铜侧得的高纯铜锌合金滤料被广泛应用于各种水处理设备。一种铜锌合金的晶胞结构如图,已知:
晶胞参数为anm。
①与Zn原子等距离且最近的Zn原子有 个。
②该铜锌合金晶体密度为 g•cm-3(设N 为阿伏加德罗常数的值)
A
20.(10分)(2023·西藏日喀则·统考一模)氮及其化合物在人们的日常生活、生产工业中和环保事中属
于“明星物质”,目前最成功的应用就是“人工固氮”,在某特殊催化剂和光照条件下,N 与水反应可生
2
成NH 。
3
(1)已知:
①4NH (g) + 3O (g) 2N (g) + 6H O(g) ΔH =-1260 kJ/mol;
3 2 2 2 1
②HO(l)= H O(g) ΔH=+44.0 kJ/mol。
2 2 2
则 2N(g) + 6HO(1) 4NH (g)+ 3O (g) ΔH = kJ / mol
2 2 3 2 3
(2)N (g) + 3H (g) 2NH (g) ΔH=-92.4 kJ/mol。将1. 00 mol N 和3. 00 mol H 充入容积为3 L的恒容密闭
2 2 3 2 2
容器中,发生上述反应。
①图甲是测得X、Y的浓度随时间变化的曲线,反应达到平衡时的平均反应速率v(H )= 。
2
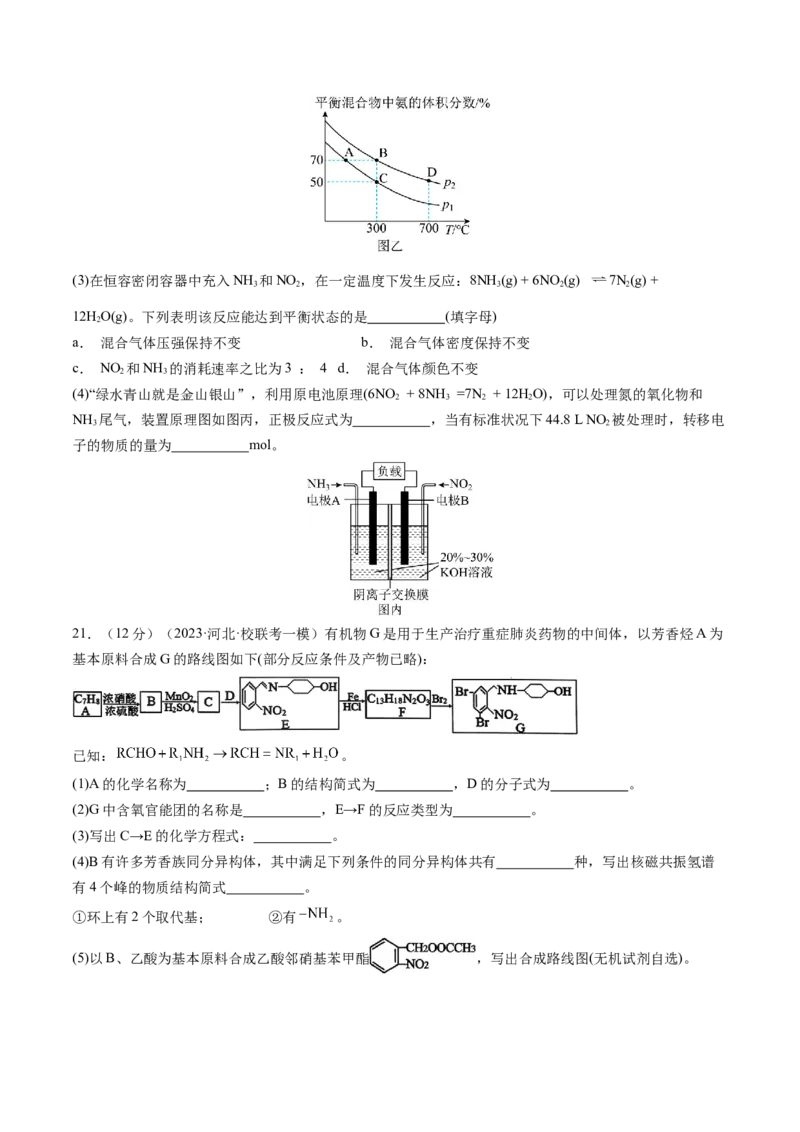
②在不同温度和压强下,平衡体系中NH 的体积分数与温度、压强关系如图乙,则压强P P
3 2 1
(填“大于”“小于”或“不确定”,下同),B、D两点的平衡常数K(D) K(B),B点N 的转化率=
2
(保留4位有效数字)。(3)在恒容密闭容器中充入NH 和NO ,在一定温度下发生反应:8NH (g) + 6NO (g) 7N(g) +
3 2 3 2 2
12HO(g)。下列表明该反应能达到平衡状态的是 (填字母)
2
a. 混合气体压强保持不变 b. 混合气体密度保持不变
c. NO 和NH 的消耗速率之比为3 : 4 d. 混合气体颜色不变
2 3
(4)“绿水青山就是金山银山”,利用原电池原理(6NO + 8NH =7N + 12H O),可以处理氮的氧化物和
2 3 2 2
NH 尾气,装置原理图如图丙,正极反应式为 ,当有标准状况下44.8 L NO 被处理时,转移电
3 2
子的物质的量为 mol。
21.(12分)(2023·河北·校联考一模)有机物G是用于生产治疗重症肺炎药物的中间体,以芳香烃A为
基本原料合成G的路线图如下(部分反应条件及产物已略):
已知: 。
(1)A的化学名称为 ;B的结构简式为 ,D的分子式为 。
(2)G中含氧官能团的名称是 ,E→F的反应类型为 。
(3)写出C→E的化学方程式: 。
(4)B有许多芳香族同分异构体,其中满足下列条件的同分异构体共有 种,写出核磁共振氢谱
有4个峰的物质结构简式 。
①环上有2个取代基; ②有 。
(5)以B、乙酸为基本原料合成乙酸邻硝基苯甲酯 ,写出合成路线图(无机试剂自选)。