文档内容
2025届高三化学一轮专题复习讲义(25)
专题六 化学实验和化学计算
6-2 化学实验的设计与评价(1课时)
【复习目标】
1.能依据实验目的和假设,设计解决简单问题的实验方案,能对实验方案进行评价。
2.能运用实验基本操作实施实验方案,具有安全意识和环保意识。
3.能根据不同类型实验的特点,设计并实施实验。
【重点突破】能对实验方案进行评价,并设计解决简单问题的实验方案
【真题再现】
例1.(2023·辽宁选择考)2-噻吩乙醇(M=128)是抗血栓药物氯吡格雷的重要中间体,
r
其制备方法如下:
Ⅰ.制钠砂。向烧瓶中加入300 mL液体A和4.60g金属钠,加热至钠熔化后,盖紧塞
子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10 ℃,加入25 mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10 ℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30
min。
Ⅳ.水解。恢复室温,加入70 mL水,搅拌30 min;加盐酸调pH至4~6,继续反应2
h,分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋
4
喃、噻吩和液体A后,得到产品17.92 g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择________。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是_________________________________。
(3)步骤Ⅱ的化学方程式为___________________________________________。
(4)步骤Ⅲ中反应放热,为防止温度过高引发其它副反应,加入环氧乙烷溶液的方法
是 。
(5)步骤Ⅳ中用盐酸调节pH的目的是 。
(6)下列仪器在步骤Ⅴ中无需使用的是 (填名称);加入无水MgSO 的
4
作用为________________________。
(7)产品的产率为____________(用Na计算,精确至0.1%)。
解析:(1)步骤I制钠砂过程中,液体A不能和Na反应,而乙醇、水和液氨都能和金属
Na反应,故选c。(2)噻吩沸点低于吡咯( )的原因是 中含有N原子,
可以形成分子间氢键,氢键可以使沸点升高。(3)步骤Ⅱ中 和Na反应生成2-
噻吩钠和H,化学方程式为2 +2Na 2 +H ↑。(4)步骤Ⅲ中反应放
2 2
热,为防止温度过高引发副反应,将烧瓶置于冰水浴中,少量多次地滴加环氧乙烷溶液,边加边搅拌,可控制温度。(5)2-噻吩乙醇钠水解生成2-噻吩乙醇的过程中有
NaOH生成,用盐酸调节pH的目的是将NaOH中和,使平衡正向移动,增大反应物的
转化率。(6)步骤Ⅴ中的操作有过滤、蒸馏,蒸馏的过程中需要直形冷凝管,无需液
体回流,不能用球形冷凝管,无需使用的是球形冷凝管、分液漏斗;向有机相中加入
无水MgSO 的作用是除去水。(7)步骤Ⅰ中向烧瓶中加入300 mL液体A和4.60 g金
4
4.60g
属钠,Na的物质的量为 =0.2 mol,步骤Ⅱ中Na完全反应,根据反应方
23g·mol-1
程式可知,理论上可以生成0.2 mol 2-噻吩乙醇,产品的产率为
17.92g
×100%=70.0%。
0.2mol×128g·mol-1
答案:(1)c
(2) 中含有N原子,可以形成分子间氢键,氢键可以使沸点升高
(3)2 +2Na 2 +H ↑
2
(4)将烧瓶置于冰水浴中,少量多次地滴加环氧乙烷溶液,边加边搅拌,可控制温度
(5)将NaOH中和,使平衡正向移动,增大反应物的转化率
(6)球形冷凝管、分液漏斗 除去水
(7)70.0%
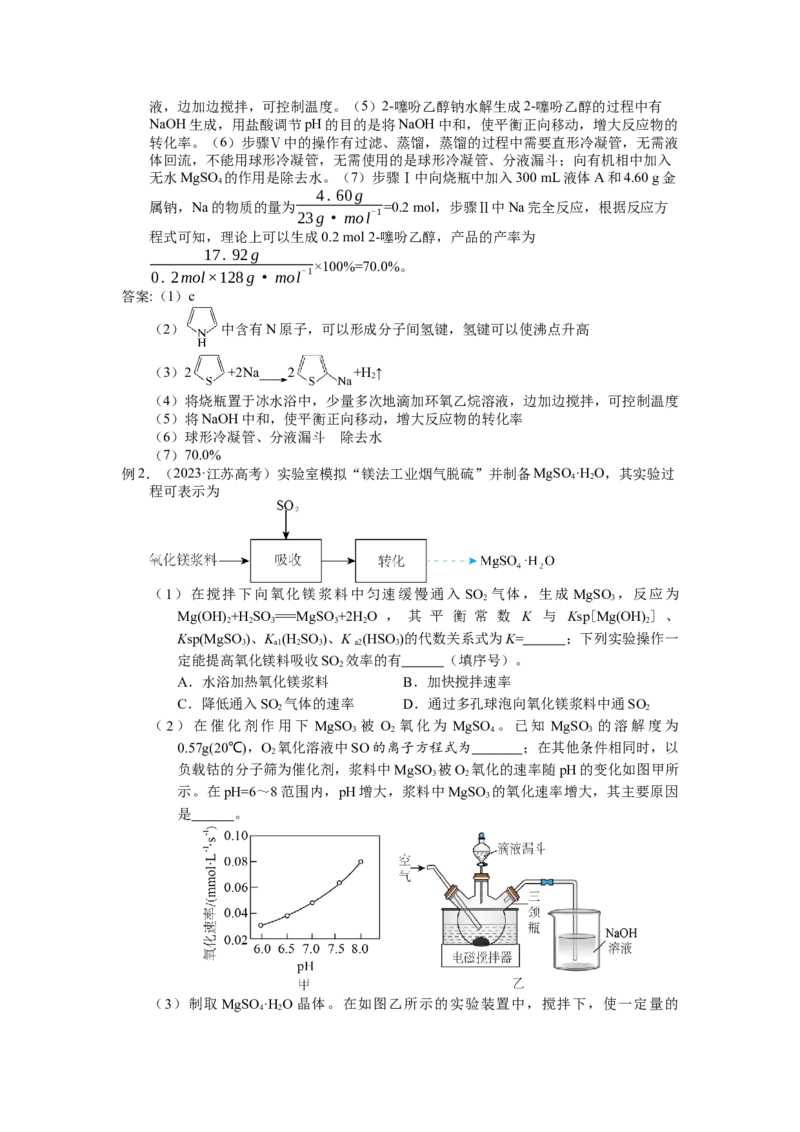
例2.(2023·江苏高考)实验室模拟“镁法工业烟气脱硫”并制备MgSO ·H O,其实验过
4 2
程可表示为
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 SO 气体,生成 MgSO ,反应为
2 3
Mg(OH) +H SO ===MgSO +2H O , 其 平 衡 常 数 K 与 Ksp[Mg(OH) ] 、
2 2 3 3 2 2
Ksp(MgSO )、K (H SO)、K (HSO )的代数关系式为K= ;下列实验操作一
3 a1 2 3 a2 3
定能提高氧化镁料吸收SO 效率的有 (填序号)。
2
A.水浴加热氧化镁浆料 B.加快搅拌速率
C.降低通入SO 气体的速率 D.通过多孔球泡向氧化镁浆料中通SO
2 2
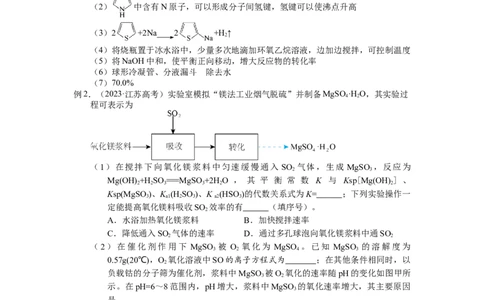
(2)在催化剂作用下 MgSO 被 O 氧化为 MgSO 。已知 MgSO 的溶解度为
3 2 4 3
0.57g(20℃),O 氧化溶液中SO的离子方程式为 ;在其他条件相同时,以
2
负载钴的分子筛为催化剂,浆料中MgSO 被O 氧化的速率随pH的变化如图甲所
3 2
示。在pH=6~8范围内,pH增大,浆料中MgSO 的氧化速率增大,其主要原因
3
是 。
(3)制取 MgSO ·H O晶体。在如图乙所示的实验装置中,搅拌下,使一定量的
4 2MgSO 浆料与HSO 溶液充分反应。MgSO 浆料与HSO 溶液的加料方式是
3 2 4 3 2 4
;补充完整制取MgSO ·H O晶体的实验方案:含有少量Fe3+、Al3+的MgSO 溶液
4 2 4
中, 。[已知:Fe3+、Al3+在pH≥5 时完全转化为氢氧化物沉淀;室温下
从MgSO 饱和溶液中结晶出MgSO ·H O,MgSO ·H O在150℃~170℃下干燥得
4 4 2 4 2
到MgSO ·H O,实验中需要使用MgO粉末。]
4 2
答案:(1) BD
(2)2SO+O=====2SO
2
pH增大,抑制SO的水解,反应物SO的浓度增大,故可加快氧化速率
(3)用滴液漏斗向盛有MgSO 浆料的三颈烧瓶中缓慢滴加硫酸溶液
3
分批加入少量氧化镁粉末,搅拌,直至用pH试纸测得pH≥5,过滤;将滤液蒸
发浓缩、降温至室温结晶,过滤,所得晶体在150~170℃干燥。
解析:本实验的目的是为了制取MgSO ·H O,首先在搅拌下向氧化镁浆料中匀速缓慢通入
4 2
SO 气体,生成MgSO ,然后使一定量的MgSO 浆料与HSO 溶液充分反应生成硫酸
2 3 3 2 4
镁,在硫酸镁的溶液中加入氧化镁调节溶液的pH除去三价铁和三价铝,将滤液蒸发
浓缩、降温至室温结晶,过滤,所得晶体在150~170℃干燥即可得到MgSO ·H O。
4 2
(1)已知下列反应:①Mg(OH) +H SO ===MgSO +2HO 其平衡常数K
2 2 3 3 2
②Mg(OH) (s) Mg2+(aq) +2OH-(aq) Ksp[Mg(OH) ]
2 2
③MgSO (s) Mg2+(aq) + SO(aq) Ksp(MgSO)
3 3
④HSO H++ HSO K (H SO )
2 3 a1 2 3
⑤HSO H++SO K (H SO )
a2 2 3
⑥HO H++OH K
2 w
根据盖斯定律,①=②-③+④+⑤-⑥×2,故K=;
A项,加热可加快反应速率,但温度升高,SO 在水中溶解度降低,且会导致HSO 受
2 2 3
热分解,不一定能提高吸收SO 效率,错误;B项,加快搅拌速率,可以使反应物充
2
分接触,提高吸收SO 效率,正确;C项,降低通入SO 气体的速率,SO 可与MgO
2 2 2
浆料充分接触,但会降低反应速率,不一定能提高吸收SO 效率,错误;D项,多孔
2
球泡可以让SO 与MgO浆料充分接触,能提高吸收SO 效率,正确;
2 2
(2)根据题意,O 氧化溶液中的SO,SO被氧化为SO,1molO 氧化2mol SO,故O
2 2 2
氧化溶液中SO的离子方程式为:2SO+O=====2SO;pH增大,抑制SO的水解,
2
反应物SO的浓度增大,故可加快氧化速率;
(3)在进行含固体物质的反应物与液体反应的实验时,应将含固体物质的反应物放在
三颈瓶中,通过滴液漏斗滴加液体,HSO 溶液的滴加速率要慢,以免HSO 过量;
2 4 2 4
根据题意,首先需要调节pH≥5以除去Fe3+、Al3+杂质,需要用到的试剂为MgO粉末,
操作细节为分批加入少量MgO粉末,以免pH过高,不断搅拌进行反应直至检测到
pH≥5,然后过滤除去氢氧化铁、氢氧化铝沉淀;接着需要从溶液中得到MgSO ·H O,
4 2
根据题目信息,室温下结晶只能得到MgSO ·H O,因此需要在150~170℃下干燥得到
4 2
MgSO ·H O,操作细节为将滤液蒸发浓缩、降温至室温结晶,过滤,所得晶体在
4 2
150~170℃干燥。
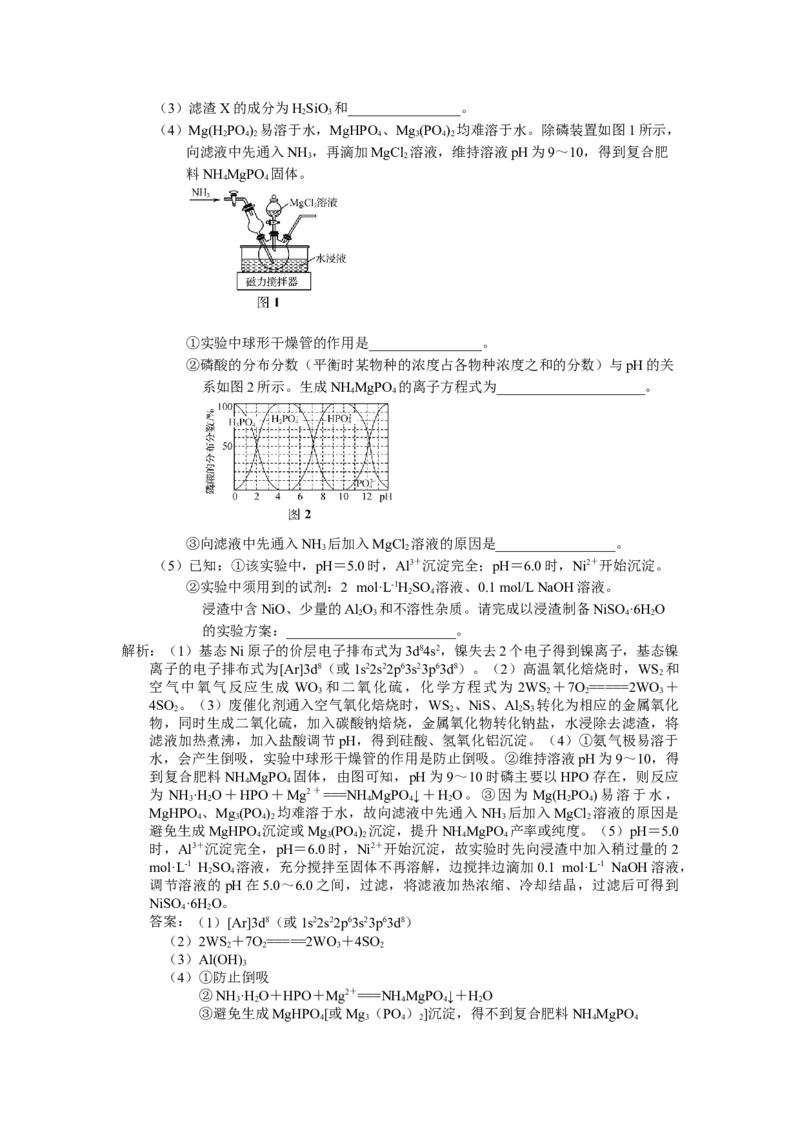
例3.(2023·苏锡常镇一调)对SiO 为载体的加氢废催化剂(主要含有WS 、NiS、
2 2
Al S,少量碳、磷)处理的实验流程如下。
2 3
(1)NiS中,基态镍离子的电子排布式为__________________。
(2)高温氧化焙烧时,WS 发生反应的化学方程式为 。
2(3)滤渣X的成分为HSiO 和________________。
2 3
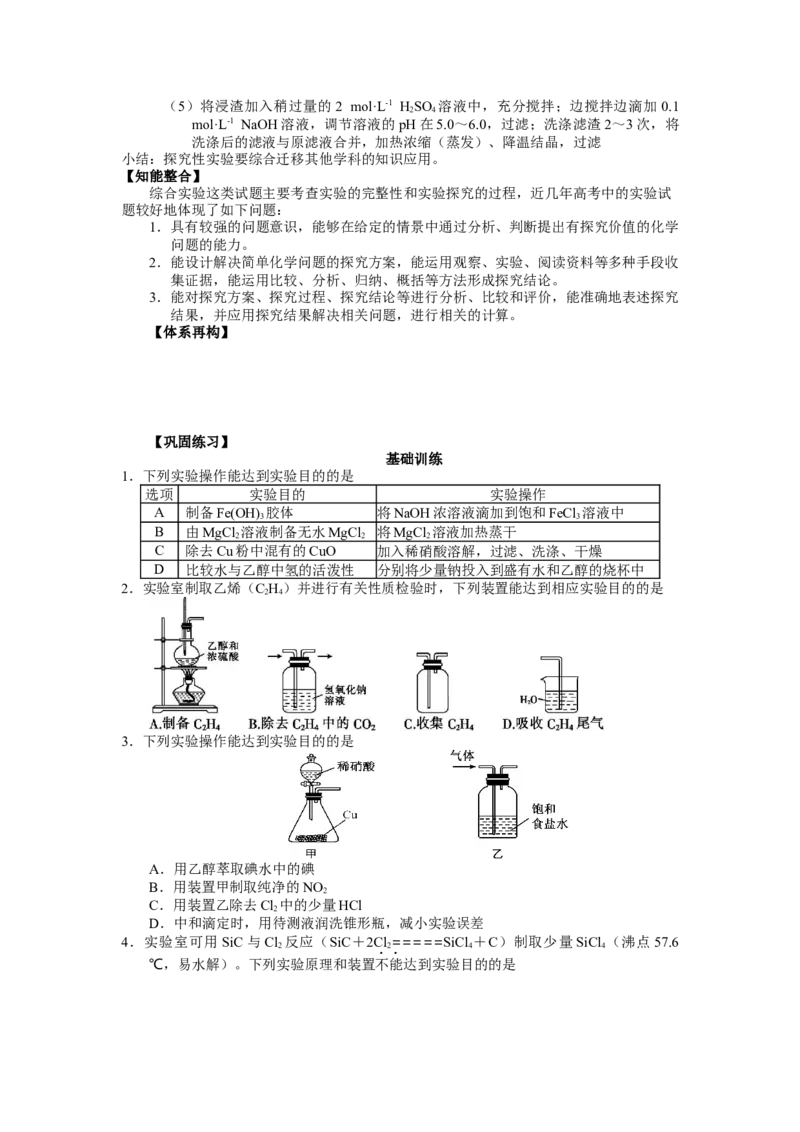
(4)Mg(HPO ) 易溶于水,MgHPO、Mg(PO ) 均难溶于水。除磷装置如图1所示,
2 4 2 4 3 4 2
向滤液中先通入NH ,再滴加MgCl 溶液,维持溶液pH为9~10,得到复合肥
3 2
料NH MgPO 固体。
4 4
①实验中球形干燥管的作用是________________。
②磷酸的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关
系如图2所示。生成NH MgPO 的离子方程式为_____________________。
4 4
③向滤液中先通入NH 后加入MgCl 溶液的原因是_________________。
3 2
(5)已知:①该实验中,pH=5.0时,Al3+沉淀完全;pH=6.0时,Ni2+开始沉淀。
②实验中须用到的试剂:2 mol·L-1HSO 溶液、0.1 mol/L NaOH溶液。
2 4
浸渣中含NiO、少量的Al O 和不溶性杂质。请完成以浸渣制备NiSO ·6H O
2 3 4 2
的实验方案:________________________。
解析:(1)基态Ni原子的价层电子排布式为3d84s2,镍失去2个电子得到镍离子,基态镍
离子的电子排布式为[Ar]3d8(或1s22s22p63s23p63d8)。(2)高温氧化焙烧时,WS 和
2
空气中氧气反应生成 WO 和二氧化硫,化学方程式为 2WS +7O=====2WO +
3 2 2 3
4SO 。(3)废催化剂通入空气氧化焙烧时,WS 、NiS、Al S 转化为相应的金属氧化
2 2 2 3
物,同时生成二氧化硫,加入碳酸钠焙烧,金属氧化物转化钠盐,水浸除去滤渣,将
滤液加热煮沸,加入盐酸调节pH,得到硅酸、氢氧化铝沉淀。(4)①氨气极易溶于
水,会产生倒吸,实验中球形干燥管的作用是防止倒吸。②维持溶液pH为9~10,得
到复合肥料NH MgPO 固体,由图可知,pH为9~10时磷主要以HPO存在,则反应
4 4
为 NH ·H O+HPO+Mg2+===NH MgPO ↓+HO。③因为 Mg(HPO )易溶于水,
3 2 4 4 2 2 4
MgHPO 、Mg(PO ) 均难溶于水,故向滤液中先通入NH 后加入MgCl 溶液的原因是
4 3 4 2 3 2
避免生成MgHPO 沉淀或Mg(PO ) 沉淀,提升NH MgPO 产率或纯度。(5)pH=5.0
4 3 4 2 4 4
时,Al3+沉淀完全,pH=6.0时,Ni2+开始沉淀,故实验时先向浸渣中加入稍过量的2
mol·L-1 HSO 溶液,充分搅拌至固体不再溶解,边搅拌边滴加0.1 mol·L-1 NaOH溶液,
2 4
调节溶液的pH在5.0~6.0之间,过滤,将滤液加热浓缩、冷却结晶,过滤后可得到
NiSO ·6H O。
4 2
答案:(1)[Ar]3d8(或1s22s22p63s23p63d8)
(2)2WS +7O=====2WO+4SO
2 2 3 2
(3)Al(OH)
3
(4)①防止倒吸
②NH ·H O+HPO+Mg2+===NH MgPO ↓+HO
3 2 4 4 2
③避免生成MgHPO[或Mg(PO )]沉淀,得不到复合肥料NH MgPO
4 3 4 2 4 4(5)将浸渣加入稍过量的2 mol·L-1 HSO 溶液中,充分搅拌;边搅拌边滴加 0.1
2 4
mol·L-1 NaOH溶液,调节溶液的pH在5.0~6.0,过滤;洗涤滤渣2~3次,将
洗涤后的滤液与原滤液合并,加热浓缩(蒸发)、降温结晶,过滤
小结:探究性实验要综合迁移其他学科的知识应用。
【知能整合】
综合实验这类试题主要考查实验的完整性和实验探究的过程,近几年高考中的实验试
题较好地体现了如下问题:
1.具有较强的问题意识,能够在给定的情景中通过分析、判断提出有探究价值的化学
问题的能力。
2.能设计解决简单化学问题的探究方案,能运用观察、实验、阅读资料等多种手段收
集证据,能运用比较、分析、归纳、概括等方法形成探究结论。
3.能对探究方案、探究过程、探究结论等进行分析、比较和评价,能准确地表述探究
结果,并应用探究结果解决相关问题,进行相关的计算。
【体系再构】
【巩固练习】
基础训练
1.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 制备Fe(OH) 胶体 将NaOH浓溶液滴加到饱和FeCl 溶液中
3 3
B 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
C 除去Cu粉中混有的CuO 加入稀硝酸溶解,过滤、洗涤、干燥
D 比较水与乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
2.实验室制取乙烯(C H)并进行有关性质检验时,下列装置能达到相应实验目的的是
2 4
3.下列实验操作能达到实验目的的是
A.用乙醇萃取碘水中的碘
B.用装置甲制取纯净的NO
2
C.用装置乙除去Cl 中的少量HCl
2
D.中和滴定时,用待测液润洗锥形瓶,减小实验误差
4.实验室可用SiC与Cl 反应(SiC+2Cl=====SiCl +C)制取少量SiCl (沸点57.6
2 2 4 4
℃,易水解)。下列实验原理和装置不能达到实验目的的是甲乙丙丁
A.用装置甲制取氯气
B.用装置乙净化氯气,气体从接口①进入
C.用装置丙制取四氯化硅
D.用装置丁收集四氯化硅粗产品
5. 下列制取、净化Cl,验证其氧化性并进行尾气吸收的装置和原理能达到实验目的的是
2
A. 制取Cl B. 除去HCl C. 验证Cl 的氧化性 D. 吸收尾气
2 2
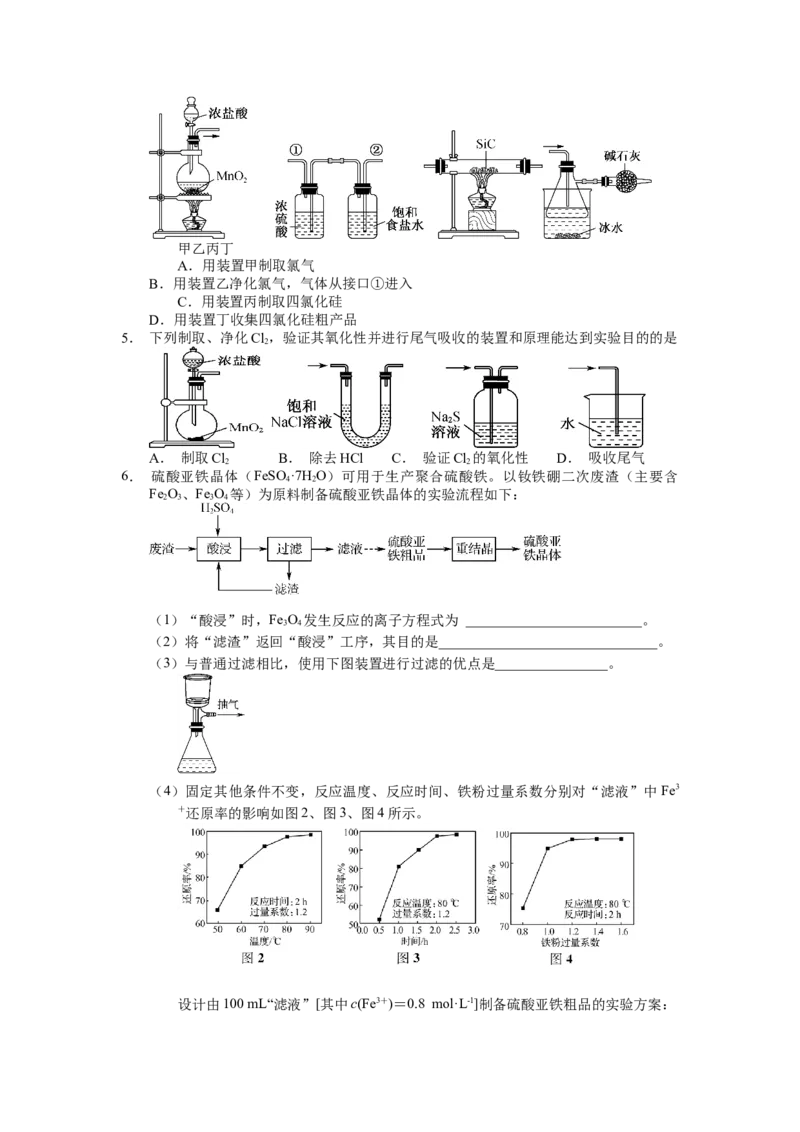
6. 硫酸亚铁晶体(FeSO ·7H O)可用于生产聚合硫酸铁。以钕铁硼二次废渣(主要含
4 2
Fe O、Fe O 等)为原料制备硫酸亚铁晶体的实验流程如下:
2 3 3 4
(1)“酸浸”时,Fe O 发生反应的离子方程式为 _________________________。
3 4
(2)将“滤渣”返回“酸浸”工序,其目的是_______________________________。
(3)与普通过滤相比,使用下图装置进行过滤的优点是________________。
(4)固定其他条件不变,反应温度、反应时间、铁粉过量系数分别对“滤液”中Fe3
+还原率的影响如图2、图3、图4所示。
设计由100 mL“滤液”[其中c(Fe3+)=0.8 mol·L-1]制备硫酸亚铁粗品的实验方案:(须使用的试
剂和仪器:铁粉、冰水、真空蒸发仪)。
(5)通过下列实验测定硫酸亚铁晶体样品的纯度。准确称取 1.2000 g样品置于锥形瓶
中,用 50 mL 蒸馏水完全溶解,加一定量硫酸和磷酸溶液;用 0.02000
mol·L-1KMnO 标准溶液滴定至终点(MnO转化为Mn2+),平行滴定3次,平均
4
消耗KMnO 标准溶液42.90mL。计算硫酸亚铁晶体样品中FeSO ·7H O的质量分
4 4 2
数(写出计算过程)。
【巩固练习】答案
1.D 2.B 3.C 4.B 5.C
6.(1)Fe O+8H+===2Fe3++Fe2++4HO
3 4 2
(2)提高铁元素的浸出率
(3)过滤速率更快
(4)在80 ℃水浴加热条件下,向“滤液”中加入2.688 g铁粉,搅拌下反应2 h后,过
滤;滤液在真空蒸发仪中蒸发、在冰水浴中冷却结晶、过滤
(5)MnO~5Fe2+
n(FeSO ·7H O)=n(Fe2+)=5n(MnO)=5×0.02000 mol·L-1×42.90×10-3 L
4 2
=4.29×10-3 mol
w(FeSO ·7H O)=×100%≈99.39%
4 2
【课后作业】
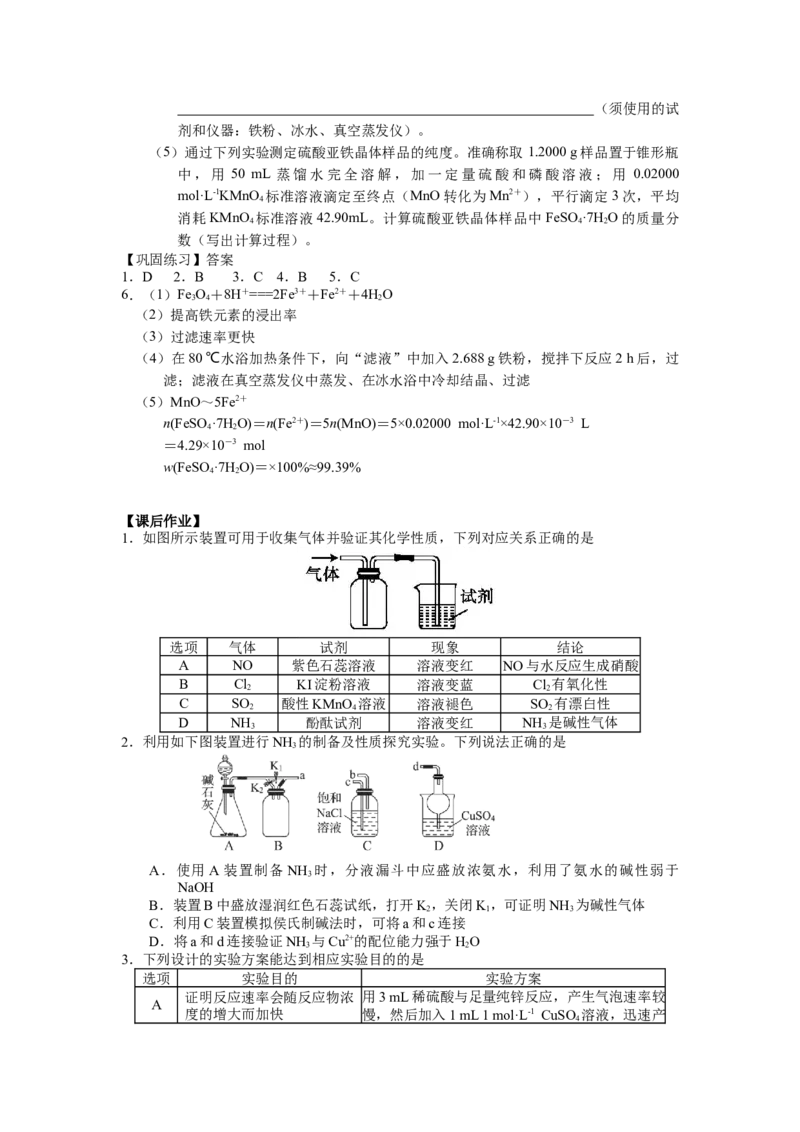
1.如图所示装置可用于收集气体并验证其化学性质,下列对应关系正确的是
选项 气体 试剂 现象 结论
A NO 紫色石蕊溶液 溶液变红 NO与水反应生成硝酸
B Cl KI淀粉溶液 溶液变蓝 Cl 有氧化性
2 2
C SO 酸性KMnO 溶液 溶液褪色 SO 有漂白性
2 4 2
D NH 酚酞试剂 溶液变红 NH 是碱性气体
3 3
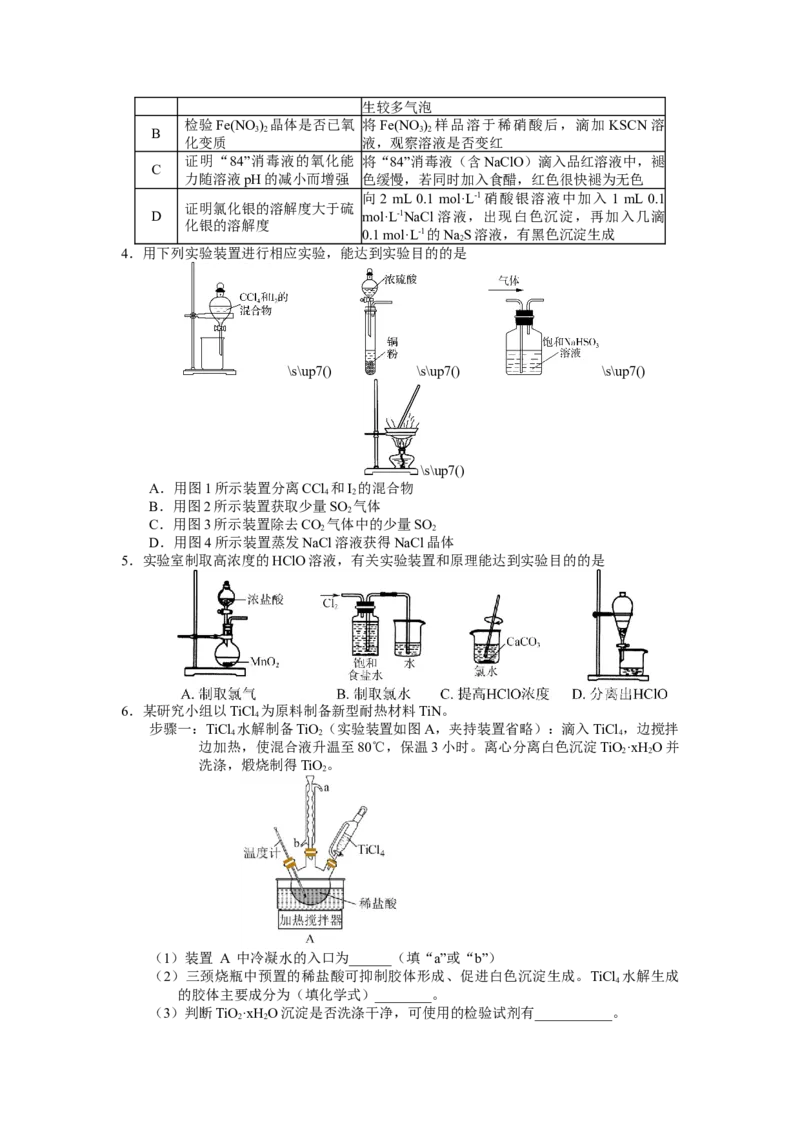
2.利用如下图装置进行NH 的制备及性质探究实验。下列说法正确的是
3
A.使用A装置制备NH 时,分液漏斗中应盛放浓氨水,利用了氨水的碱性弱于
3
NaOH
B.装置B中盛放湿润红色石蕊试纸,打开K,关闭K,可证明NH 为碱性气体
2 1 3
C.利用C装置模拟侯氏制碱法时,可将a和c连接
D.将a和d连接验证NH 与Cu2+的配位能力强于HO
3 2
3.下列设计的实验方案能达到相应实验目的的是
选项 实验目的 实验方案
证明反应速率会随反应物浓 用3 mL稀硫酸与足量纯锌反应,产生气泡速率较
A
度的增大而加快 慢,然后加入1 mL 1 mol·L-1 CuSO 溶液,迅速产
4生较多气泡
检验Fe(NO ) 晶体是否已氧 将 Fe(NO ) 样品溶于稀硝酸后,滴加 KSCN 溶
B 3 2 3 2
化变质 液,观察溶液是否变红
证明“84”消毒液的氧化能 将“84”消毒液(含NaClO)滴入品红溶液中,褪
C
力随溶液pH的减小而增强 色缓慢,若同时加入食醋,红色很快褪为无色
向 2 mL 0.1 mol·L-1硝酸银溶液中加入 1 mL 0.1
证明氯化银的溶解度大于硫
D mol·L-1NaCl溶液,出现白色沉淀,再加入几滴
化银的溶解度
0.1 mol·L-1的NaS溶液,有黑色沉淀生成
2
4.用下列实验装置进行相应实验,能达到实验目的的是
\s\up7() \s\up7() \s\up7()
\s\up7()
A.用图1所示装置分离CCl 和I 的混合物
4 2
B.用图2所示装置获取少量SO 气体
2
C.用图3所示装置除去CO 气体中的少量SO
2 2
D.用图4所示装置蒸发NaCl溶液获得NaCl晶体
5.实验室制取高浓度的HClO溶液,有关实验装置和原理能达到实验目的的是
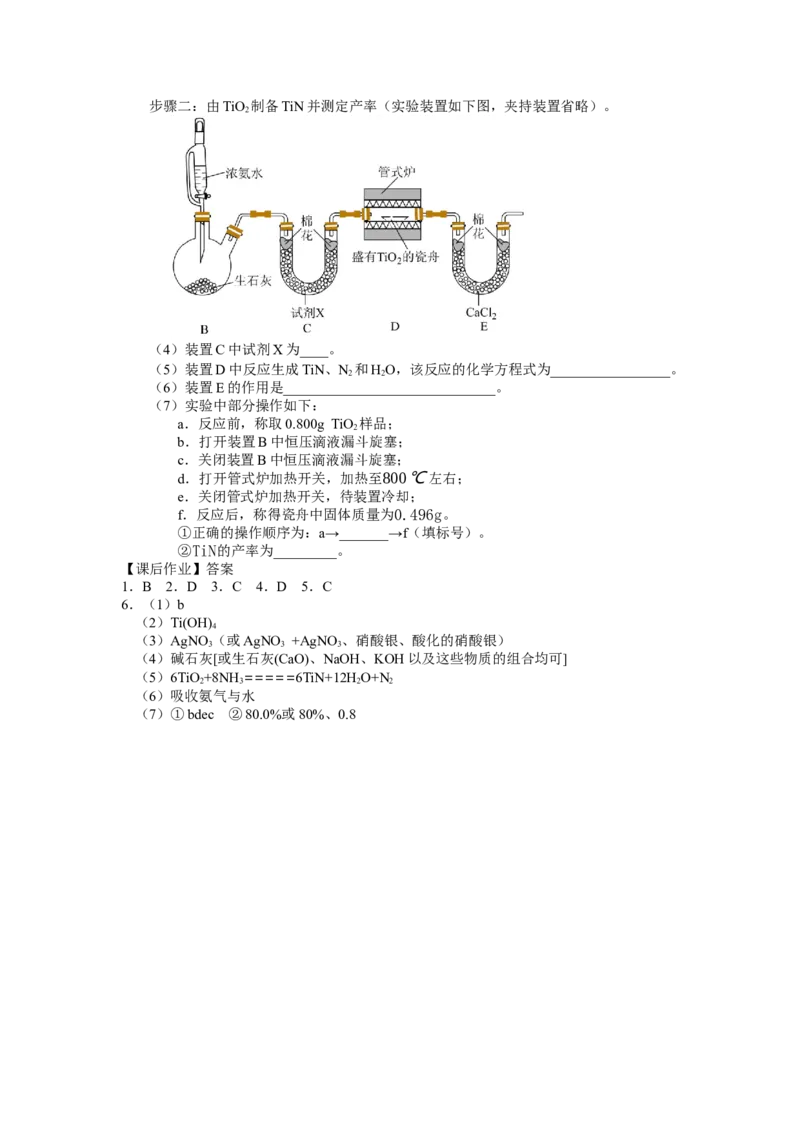
6.某研究小组以TiCl 为原料制备新型耐热材料TiN。
4
步骤一:TiCl 水解制备TiO(实验装置如图A,夹持装置省略):滴入TiCl ,边搅拌
4 2 4
边加热,使混合液升温至80℃,保温3小时。离心分离白色沉淀TiO·xHO并
2 2
洗涤,煅烧制得TiO。
2
(1)装置 A 中冷凝水的入口为______(填“a”或“b”)
(2)三颈烧瓶中预置的稀盐酸可抑制胶体形成、促进白色沉淀生成。TiCl 水解生成
4
的胶体主要成分为(填化学式)________。
(3)判断TiO·xHO沉淀是否洗涤干净,可使用的检验试剂有___________。
2 2步骤二:由TiO 制备TiN并测定产率(实验装置如下图,夹持装置省略)。
2
(4)装置C中试剂X为____。
(5)装置D中反应生成TiN、N 和HO,该反应的化学方程式为_________________。
2 2
(6)装置E的作用是______________________________。
(7)实验中部分操作如下:
a.反应前,称取0.800g TiO 样品;
2
b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至800℃左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为0.496g。
①正确的操作顺序为:a→_______→f(填标号)。
②TiN的产率为_________。
【课后作业】答案
1.B 2.D 3.C 4.D 5.C
6.(1)b
(2)Ti(OH)
4
(3)AgNO (或AgNO +AgNO 、硝酸银、酸化的硝酸银)
3 3 3
(4)碱石灰[或生石灰(CaO)、NaOH、KOH以及这些物质的组合均可]
(5)6TiO+8NH=====6TiN+12HO+N
2 3 2 2
(6)吸收氨气与水
(7)①bdec ②80.0%或80%、0.8