文档内容
课时检测(五十七) pH计算与酸碱中和滴定的拓展应用
1.在室温下,等体积的酸和碱的溶液混合后,pH一定小于7的是( )
A.pH=3的HNO 和pH=11的KOH溶液
3
B.pH=3的盐酸和pH=11的氨水
C.pH=3的醋酸和pH=11的Ba(OH) 溶液
2
D.pH=3的硫酸和pH=11的NaOH溶液
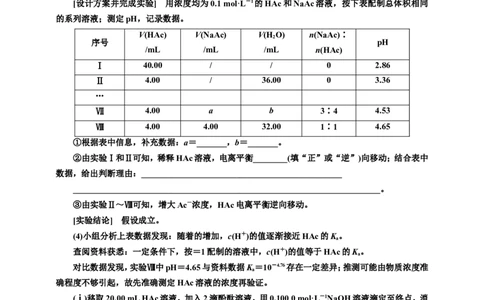
2.(2023·重庆等级考)(NH)SO 溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列
4 2 4
说法正确的是( )
A.M点K 等于N点K
w w
B.M点pH大于N点pH
C.N点降温过程中有2个平衡发生移动
D.P点c(H+)+c(NH)+c(NH·HO)=c(OH-)+2c(SO)
3 2
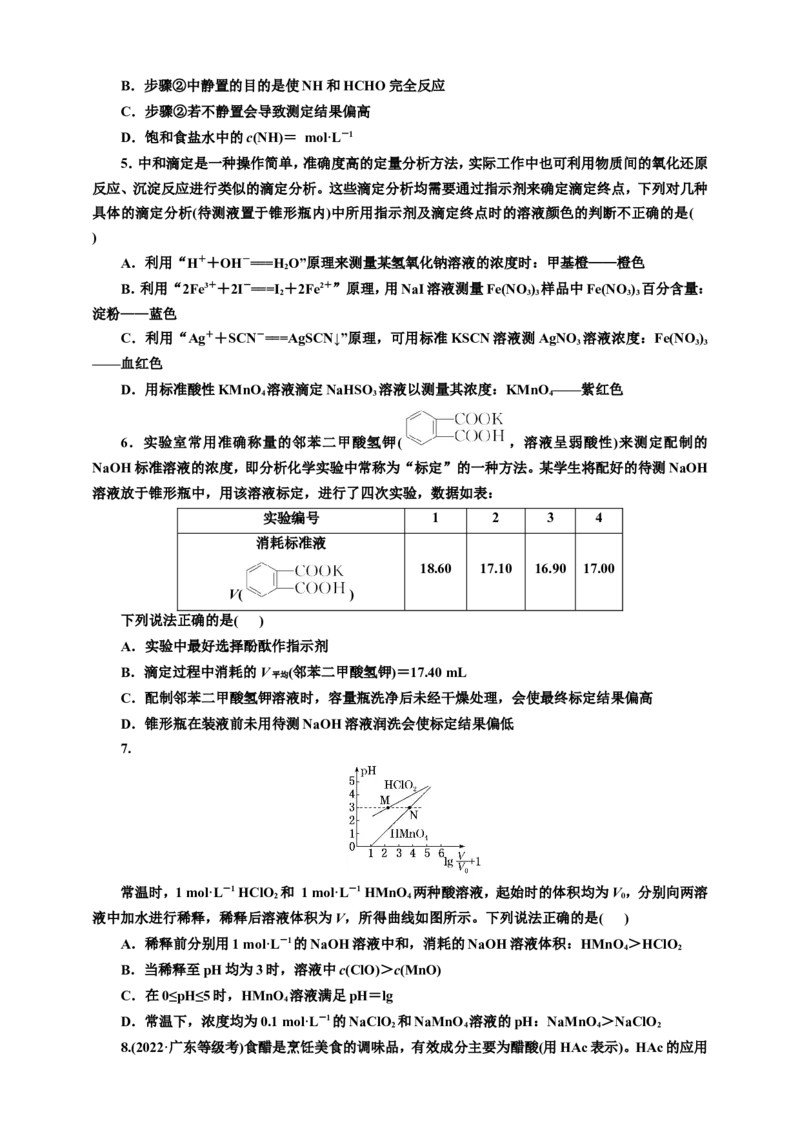
3.(2024·福建福州模拟)下列滴定中,指示剂的选择或滴定终点颜色变化有错误的是( )
提示:2KMnO +5KSO +3HSO ===6K SO +2MnSO +3HO、I+Na S===2NaI+S↓
4 2 3 2 4 2 4 4 2 2 2
滴定管中 锥形瓶中 滴定终点
选项 指示剂
的溶液 的溶液 颜色变化
CH COOH 无色→
3
A NaOH溶液 酚酞
溶液 浅红色
浅红色→
B HCl溶液 氨水 酚酞
无色
酸性KMnO KSO 无色→
4 2 3
C 无
溶液 溶液 浅紫红色
D 碘水 Na S溶液 淀粉 无色→蓝色
2
4.生产和实验中广泛采用甲醛法测定饱和食盐水样品中的NH含量,利用的反应原理为4NH+
6HCHO===(CH)NH+(一元酸)+3H++6HO。实验步骤如下:
2 6 4 2
①甲醛中常含有微量甲酸,应先除去。取甲醛a mL于锥形瓶,加入1~2滴指示剂,用浓度为b
mol·L-1的NaOH溶液滴定,滴定管的初始读数为V mL,当锥形瓶内溶液呈微红色时,滴定管的读数
1
为V mL。
2
②向锥形瓶中加入饱和食盐水试样c mL,静置1分钟。
③用上述滴定管中剩余的NaOH溶液继续滴定锥形瓶内溶液,至溶液呈微红色时,滴定管的读数
为V mL。
3
下列说法不正确的是( )
A.步骤①中的指示剂可以选用酚酞溶液B.步骤②中静置的目的是使NH和HCHO完全反应
C.步骤②若不静置会导致测定结果偏高
D.饱和食盐水中的c(NH)= mol·L-1
5.中和滴定是一种操作简单,准确度高的定量分析方法,实际工作中也可利用物质间的氧化还原
反应、沉淀反应进行类似的滴定分析。这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种
具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是(
)
A.利用“H++OH-===H O”原理来测量某氢氧化钠溶液的浓度时:甲基橙——橙色
2
B.利用“2Fe3++2I-===I +2Fe2+”原理,用NaI溶液测量Fe(NO) 样品中Fe(NO) 百分含量:
2 3 3 3 3
淀粉——蓝色
C.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测AgNO 溶液浓度:Fe(NO)
3 3 3
——血红色
D.用标准酸性KMnO 溶液滴定NaHSO 溶液以测量其浓度:KMnO ——紫红色
4 3 4
6.实验室常用准确称量的邻苯二甲酸氢钾( ,溶液呈弱酸性)来测定配制的
NaOH标准溶液的浓度,即分析化学实验中常称为“标定”的一种方法。某学生将配好的待测NaOH
溶液放于锥形瓶中,用该溶液标定,进行了四次实验,数据如表:
实验编号 1 2 3 4
消耗标准液
18.60 17.10 16.90 17.00
V( )
下列说法正确的是( )
A.实验中最好选择酚酞作指示剂
B.滴定过程中消耗的V (邻苯二甲酸氢钾)=17.40 mL
平均
C.配制邻苯二甲酸氢钾溶液时,容量瓶洗净后未经干燥处理,会使最终标定结果偏高
D.锥形瓶在装液前未用待测NaOH溶液润洗会使标定结果偏低
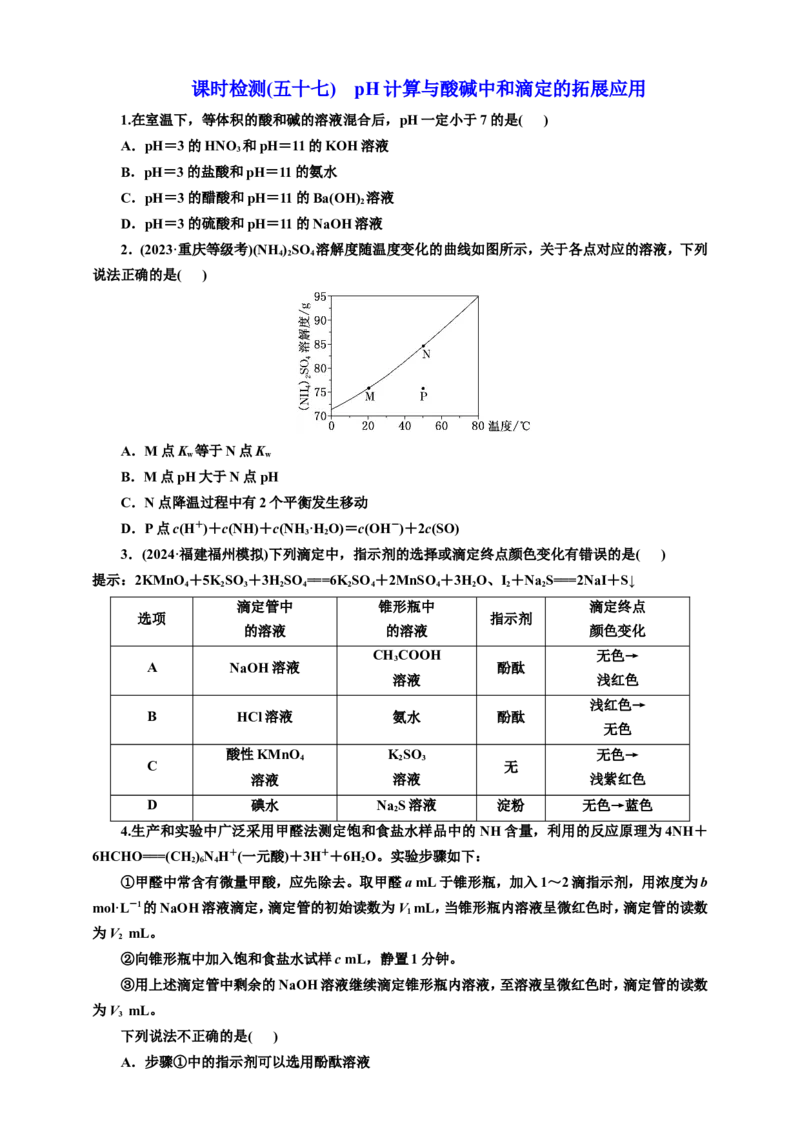
7.
常温时,1 mol·L-1 HClO 和 1 mol·L-1 HMnO 两种酸溶液,起始时的体积均为V ,分别向两溶
2 4 0
液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是( )
A.稀释前分别用1 mol·L-1的NaOH溶液中和,消耗的NaOH溶液体积:HMnO >HClO
4 2
B.当稀释至pH均为3时,溶液中c(ClO)>c(MnO)
C.在0≤pH≤5时,HMnO 溶液满足pH=lg
4
D.常温下,浓度均为0.1 mol·L-1的NaClO 和NaMnO 溶液的pH:NaMnO >NaClO
2 4 4 2
8.(2022·广东等级考)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。25 ℃时,HAc的K =1.75×10-5=10-4.76。
a
(1)配制250 mL 0.1 mol·L-1的HAc溶液,需5 mol·L-1HAc 溶液的体积为________ mL。
(2)下列关于250 mL容量瓶的操作,正确的是________。
(3)某小组研究25 ℃下HAc电离平衡的影响因素。
[提出假设] 稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
[设计方案并完成实验] 用浓度均为0.1 mol·L-1的HAc和NaAc溶液,按下表配制总体积相同
的系列溶液;测定pH,记录数据。
V(HAc) V(NaAc) V(H O) n(NaAc)∶
2
序号 pH
/mL /mL /mL n(HAc)
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3∶4 4.53
Ⅷ 4.00 4.00 32.00 1∶1 4.65
①根据表中信息,补充数据:a=_______,b=_______。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡________(填“正”或“逆”)向移动;结合表中
数据,给出判断理由:_______________________________________________
________________________________________________________________________。
③由实验Ⅱ~Ⅷ可知,增大Ac-浓度,HAc电离平衡逆向移动。
[实验结论] 假设成立。
(4)小组分析上表数据发现:随着的增加,c(H+)的值逐渐接近HAc的K 。
a
查阅资料获悉:一定条件下,按=1配制的溶液中,c(H+)的值等于HAc的K 。
a
对比数据发现,实验Ⅷ中pH=4.65与资料数据K =10-4.76存在一定差异;推测可能由物质浓度准
a
确程度不够引起,故先准确测定HAc溶液的浓度再验证。
(ⅰ)移取20.00 mL HAc溶液,加入2滴酚酞溶液,用0.100 0 mol·L-1NaOH溶液滴定至终点,消
耗体积为22.08 mL,则该HAc溶液的浓度为________ mol·L-1。画出上述过程的滴定曲线示意图并标
注滴定终点。
(ⅱ)用上述HAc溶液和0.100 0 mol·L-1NaOH溶液,配制等物质的量的HAc与NaAc混合溶液,
测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1 mol·L-1的HAc和NaOH溶液,如何准确测定HAc
的K ?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
a
Ⅰ 移取20.00 mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V mL
1
________________________________________________________________________,
Ⅱ
测得溶液的pH为4.76[实验总结] 得到的结果与资料数据相符,方案可行。
(6)根据K 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途____________。
a
9.向含有NaOH的NaClO溶液中逐滴滴入FeSO 溶液,滴加过程中溶液的pH随FeSO 溶液的
4 4
体积的变化曲线及实验现象见表:
变化曲线 实验现象
ⅰ.A→B产生红褐色沉淀
ⅱ.B→C红褐色沉淀的量增多
ⅲ.C→D红褐色沉淀的量增多
ⅳ.D点附近产生有刺激性气味的气体
ⅴ.D→E红褐色沉淀的量略有增多
资料:①饱和NaClO溶液的pH约为11;
②K [Fe(OH)]=2.8×10-39。
sp 3
(1)Cl 和NaOH溶液制取NaClO的离子方程式是
2
________________________________________________________________________。
(2)A点溶液的pH约为13,主要原因是_____________________________________
________________________________________________________________________。
(3)结合离子方程式解释A→B溶液的pH显著下降的主要原因:___________________
________________________________________________________________________。
(4)NaClO溶液中含氯各微粒的物质的量分数与pH的关系如图:
①M点溶液含氯的微粒有___________________________________________。
②C点附近生成红褐色沉淀的主要反应的离子方程式是________________________。
(5)检验ⅳ中气体的方法是______________________________________________
________________________________________________________________________。
(6)A→D的过程中,溶液的pH一直下降,原因是_____________________________
________________________________________________________________________。
(7)整个滴加过程中发生的反应与_______________________________________
________________________________________________________、微粒的浓度等有关。
10.(1)(2024·湖北调研)实验室常用甲醛法测定含(NH)CrO 的样品中氮的质量分数,其反应原
4 2 2 7
理为2Ba2++CrO+HO===2BaCrO ↓+2H+、4NH+6HCHO===3H++6HO+(CH)NH+[滴定时,
2 2 4 2 2 6 4
1 mol(CH )NH+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。
2 6 4
实验步骤:称取样品2.800 g,配成250 mL溶液,移取25.00 mL样品溶液于250 mL锥形瓶中,用
氯化钡溶液使CrO完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2 滴
2
酚酞溶液,用0.200 mol·L-1 NaOH标准溶液滴定至终点。重复上述操作3次。①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则滴定时用去NaOH标准溶
液的体积________(填“偏大”“偏小”或“无影响”);滴定时边滴边摇动锥形瓶,眼睛应观察
______________________________。
②滴定结果如表所示:
标准溶液的体积
滴定 待测溶液的
滴定前刻 滴定后刻度/
次数 体积/mL
度/mL mL
1 25.00 1.07 21.06
2 25.00 0.88 20.89
3 25.00 0.20 21.20
4 25.00 0.66 20.66
该样品中氮元素的质量分数为________。
(2)测定POCl 含量。用PCl 氧化法制备的POCl 中常含有PCl 杂质。
3 3 3 3
已知:PCl 遇水生成HPO 和HCl,POCl 遇水生成HPO 和HCl。
3 3 3 3 3 4
Ⅰ.准确称取1.455 g制得的POCl 产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解;
3
Ⅱ.将水解液配成100.00 mL溶液,取10.00 mL溶液于锥形瓶中;
Ⅲ.加入10.00 mL 0.320 0 mol·L-1AgNO 溶液,使氯离子完全沉淀;向其中加入少许硝基苯用力
3
摇动;
Ⅳ.以Fe3+为指示剂,用0.020 0 mol·L-1KSCN标准溶液滴定过量的AgNO 溶液,达到滴定终点
3
时共用去10.00 mL KSCN溶液。已知:Ag++SCN-===AgSCN↓;K (AgCl)>K (AgSCN)。
sp sp
①滴定终点的现象为_________________________________________________
________________________________________________________________________。
②实验过程中加入硝基苯的目的是______________________________________
________________________________________________________________________;
若无此操作,则所测POCl 含量将会__________(填“偏大”“偏小”或“不变”)。
3
③产品中POCl 的百分含量为______________(保留三位有效数字)。
3
(3)CuSO ·5HO的含量通常利用“间接碘量法”测定,步骤如下:
4 2
①称取1.250 g产品配成100 mL溶液。
②取其中25.00 mL溶液,加入足量的NaF溶液后,滴加KI溶液至不再产生沉淀。
③用0.100 0 mol·L-1Na SO 标准溶液滴定,平行滴定3次。已知Cu2+与F-不反应,Fe3+与F-反
2 2 3
应生成FeF,氧化性:I>FeF;I+2Na SO===2NaI+Na SO。步骤②中,若不加足量的NaF溶液,最
2 2 2 2 3 2 4 6
终的测量值将__________(填“偏大”“偏小”或“无影响”)。滴加KI溶液,有白色碘化物沉淀生成,
反应的离子方程式为_____________________________;若Na SO 标准溶液的平均用量为10.00 mL,
2 2 3
则胆矾产品纯度为________%。
课时检测(五十七)
1.C A项,pH=3的HNO 和pH=11的KOH溶液,c(H+)=c(OH-)=10-3 mol·L-1,等体积混
3
合恰好反应生成硝酸钾,溶液为中性,错误;B项,pH=3的盐酸c(H+)=
10-3 mol·L-1,氨水浓度大于10-3 mol·L-1,等体积混合时碱过量,溶液pH大于7,错误;C项,pH=3的醋酸的浓度大于10-3mol·L-1,pH=11的Ba(OH) 溶液中c(OH-)=
2
10-3 mol·L-1,等体积混合时酸过量,pH一定小于7,正确;D项,pH=3的硫酸和pH=11的
NaOH溶液,c(H+)=c(OH-)=10-3 mol·L-1,等体积混合恰好反应生成硫酸钠,溶液为中性,错误。
2.B M点和N点温度不同,故K 不相等,A错误;升高温度促进铵根离子的水解,且N点铵根
w
离子的浓度更大,水解生成的氢离子浓度更大,故M点pH大于N点pH,B正确;N点降温过程中有
水的电离平衡、铵根离子的水解平衡、硫酸铵的溶解平衡3个平衡发生移动,C错误;P点为硫酸铵的
不饱和溶液,溶液中存在电荷守恒:c(H+)+c(NH)=c(OH-)+2c(SO),故D错误。
3.B A项,锥形瓶中为酸,加入酚酞无色,达到滴定终点,溶液显碱性,溶液变为浅红色,故现象
为无色→浅红色,正确;B项,锥形瓶中为碱,达到滴定终点,溶液显酸性,应选择指示剂甲基橙,现象
是溶液由黄色变为橙色,错误。
4.C 甲酸和氢氧化钠反应生成甲酸钠,溶液呈碱性,步骤①中的指示剂可以选用酚酞溶液,A正
确;通过延长反应时间,使反应进行得更充分,步骤②中静置的目的是使NH和HCHO完全反应,B正
确;步骤②若不静置,反应4NH+6HCHO===(CH)NH+(一元酸)+3H++6HO进行不完全,生成的
2 6 4 2
酸少,最终会导致测定结果偏低,C错误;4NH~[(CH)NH+(一元酸)+3H+]~4OH-,氢氧化钠的物
2 6 4
质的量和氮元素的物质的量相同,所以饱和食盐水中c(NH)== mol·L-1,D正确。
5.B A项,用标准的盐酸溶液滴定氢氧化钠溶液,甲基橙为指示剂,溶液滴定终点的现象为由黄
色变为橙色,正确;B项,利用2Fe3++2I-===I +2Fe2+原理,由于一开始就生成了单质碘,溶液呈蓝色,
2
无法判断终点,错误;C项,利用Ag++SCN-===AgSCN↓原理,用标准KSCN溶液测量AgNO 溶液
3
浓度,Fe(NO) 为指示剂,溶液滴定终点的现象为由无色变为血红色,正确;D项,用标准酸性KMnO
3 3 4
溶液滴定Na SO 溶液,KMnO 本身就是指示剂,溶液滴定终点的现象为由无色变为紫红色,正确。
2 3 4
6.A A项,邻苯二甲酸氢钾呈弱酸性,滴定终点时生成强碱弱酸盐,溶液呈碱性,所以选用酚酞
作指示剂,正确;B项,第1组数据为18.60 mL,与其他三组相差较大,应该舍弃,则滴定过程中消耗的
V(邻苯二甲酸氢钾)==17.00 mL,错误;C项,配制邻苯二甲酸氢钾溶液时,容量瓶洗净后未经干燥处
理,该操作方法不影响配制结果,错误;D项,中和滴定过程中,盛放待测液的锥形瓶不能润洗,否则影
响滴定结果,错误。
7.C HClO 与HMnO 两种酸都为一元酸且物质的量相等,消耗的NaOH溶液体积相同,故A
2 4
错误;当稀释至pH均为3时,两溶液中均存在电荷守恒,分别为c(H+)=c(OH-)+c(ClO),c(H+)=
c(OH-)+c(MnO),则溶液中c(ClO)=c(MnO),故B错误;由题图可知lg +1=1时,1 mol·L-1
HMnO 溶液中c(H+)=1 mol·L-1,说明HMnO 为强酸,在0≤pH≤5时,HMnO 溶液满足pH=lg ,故
4 4 4
C正确;由题图可知 HClO 为弱酸,则浓度均为 0.1 mol·L-1的NaClO 和NaMnO 溶液的pH:
2 2 4
NaMnO <NaClO ,故D错误。
4 2
8.解析:(1)溶液稀释过程中,溶质的物质的量不变,因此250 mL×0.1 mol·L-1=V×5 mol·L-1,解
得V=5.0 mL。(2)容量瓶使用过程中,不能用手等触碰瓶口,以免污染试剂,故A错误;定容时,视线
应平视刻度线且与溶液凹液面相切,不能仰视或俯视,故B错误;向容量瓶中转移液体,需用玻璃棒引
流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶口,故C正确;定容完成后,盖上瓶塞,将
容量瓶来回颠倒,将溶液摇匀,颠倒过程中,左手食指抵住瓶塞,防止瓶塞脱落,右手扶住容量瓶底部,
防止容量瓶从左手掉落,故D错误。(3)①实验Ⅶ的溶液中n(NaAc)∶n(HAc)=3∶4,V(HAc)=4.00
mL,因此V(NaAc)=3.00 mL,即a=3.00,由实验Ⅰ可知,溶液最终的体积为40.00 mL,因此V(H O)
2
=40.00 mL-4.00 mL-3.00 mL=33.00 mL,即b=33.00。②实验Ⅰ所得溶液的pH=2.86,实验Ⅱ的溶液中c(HAc)为实验Ⅰ的,稀释过程中,若不考虑电离平衡移动,则实验Ⅱ所得溶液的pH=2.86+1
=3.86,但实际溶液的pH=3.36<3.86,说明稀释过程中,溶液中n(H+)增大,即电离平衡正向移动。
(4)ⅰ.滴定过程中发生反应:HAc+NaOH===NaAc+HO,由反应方程式可知,滴定至终点时,n(HAc)
2
=n(NaOH),因此22.08 mL×0.1 mol·L-1=20.00 mL×c(HAc),解得c(HAc)=0.110 4 mol·L-1。ⅱ.滴定
过程中,当V(NaOH)=0时,c(H+)=≈ mol·L-1=10-2.86mol·L-1,溶液的pH=2.86,当V(NaOH)=
11.04 mL时,n(NaAc)=n(HAc),溶液的pH=4.76,当V(NaOH)=22.08 mL时,达到滴定终点,溶液中
溶质为NaAc溶液,Ac-发生水解,溶液呈弱碱性,当NaOH溶液过量较多时,c(NaOH)无限接近0.1
mol·L-1,溶液pH接近13。(5)向20.00 mL的HAc溶液中加入V mL NaOH溶液达到滴定终点,滴定
1
终点的溶液中溶质为NaAc,当=1时,溶液中c(H+)的值等于HAc的K ,因此可再向溶液中加入
a
20.00 mL HAc溶液,使溶液中n(NaAc)=n(HAc)。(6)不同的无机弱酸在生活中应用广泛,如HClO具
有强氧化性,在生活中可用于漂白和消毒,HSO 具有还原性,可用作还原剂,在葡萄酒中添加适量
2 3
HSO 可用作防腐剂,HPO 可用作食品添加剂,同时在制药、生产肥料等行业有广泛用途。
2 3 3 4
答案:(1)5.0 (2)C (3)①3.00 33.00
②正 实验Ⅱ相较于实验Ⅰ,醋酸溶液稀释了10倍,而实验Ⅱ的pH增大值小于1 (4)0.110 4
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\5\\22HXGKGD-16.TIF" \*
MERGEFORMATINET
(5)向滴定后的混合液中加入20 mL HAc溶液
(6)HClO:漂白剂和消毒液(或HSO :还原剂、防腐剂或HPO:食品添加剂、制药、生产肥料)
2 3 3 4
9.解析:向含有NaOH的NaClO溶液中逐滴滴入FeSO 溶液,结合变化曲线图和实验现象,发现
4
A→B过程,溶液的碱性较强,此时发生ClO-+2Fe2++4OH-+HO===Cl-+2Fe(OH) ↓,从B→C的
2 3
过程ClO-的含量减少,HClO含量增多,到C点主要发生HClO+2Fe2++5HO===2Fe(OH) +Cl-+
2 3
5H+,D→E过程溶液中NaOH和NaClO已完全反应,此时红褐色沉淀略有增多,主要是Fe2+被空气
中的O 氧化为Fe3+,Fe3+发生水解生成Fe(OH) 沉淀。(2)A点溶液的pH约为13,主要原因是溶液中
2 3
含有NaOH,NaOH电离出OH-使溶液的pH约为13。(3)A→B产生红褐色沉淀,说明有Fe(OH) 生成,
3
所以A→B溶液的pH显著下降是ClO-将Fe2+氧化为+3价,消耗溶液中的OH-,使c(OH-) 减小。
(4)M点pH略小于8,产生红褐色沉淀,所以溶液含氯的微粒有ClO-、HClO、Cl-;C点pH约为6.5,
溶液中HClO含量较多,所以C点附近生成红褐色沉淀的主要反应的离子方程式是HClO+2Fe2++
5HO===2Fe(OH) +Cl-+5H+。(5)根据现象ⅳ:D点附近产生有刺激性气味的气体,该气体为氯气,
2 3
利用反应Cl +2KI===2KCl +I 和碘单质遇淀粉溶液变蓝进行检验。(6)A→D的过程中,产生的红褐
2 2
色沉淀在不断增多,即Fe2+不断地转化为Fe(OH) 沉淀,此过程需不断地消耗溶液中的OH-,所以溶
3
液的pH一直下降。(7)不同阶段有不同的氧化剂将Fe2+氧化为Fe(OH) ,因此整个滴加过程中发生的
3
反应与反应物的相对用量或氧化剂的种类、微粒的浓度等有关。
答案:(1)Cl+2OH-===Cl-+ClO-+HO
2 2
(2)溶液中含有NaOH,NaOH电离出OH-使溶液的pH约为13(3)A→B发生反应ClO-+2Fe2++4OH-+HO===Cl-+2Fe(OH) ↓,消耗OH-,使溶液的pH显
2 3
著下降
(4)①ClO-、HClO、Cl-
②HClO+2Fe2++5HO===2Fe(OH) +Cl-+5H+
2 3
(5)用湿润的淀粉碘化钾试纸检验气体,试纸变蓝
(6)Fe2+向Fe(OH) 转化时消耗了NaOH和HO电离的OH-,c(OH-)减小、c(H+)增大,pH一直
3 2
下降
(7)反应物的相对用量或氧化剂的种类
10.解析:(1)4次滴定消耗氢氧化钠溶液体积依次为19.99 mL、20.01 mL、21.00 mL、20.00 mL,第
3次测定误差较大,舍去,取剩下3次滴定的平均值得消耗氢氧化钠溶液体积为20.00 mL。由题给关系
可知(NH)CrO~4OH-,则w(N)=×100%=10.00%。
4 2 2 7
(2)①滴加KSCN标准溶液,先生成AgSCN沉淀,达到滴定终点时,溶液变为红色,且半分钟不褪
色。②根据题给信息,加入硝基苯可覆盖AgCl沉淀,避免AgCl与KSCN标准溶液反应,若无此操作,
则KSCN标准溶液用量偏多,测得的Ag+浓度偏大,从而使所测POCl 含量偏小。③Ⅰ~Ⅲ涉及的反
3
应有 PCl +3HO===H PO +3HCl,POCl +3HO===H PO +3HCl,HCl+AgNO ===AgCl↓+
3 2 3 3 3 2 3 4 3
HNO ,此过程消耗AgNO 的物质的量为0.01 L×0.320 0 mol·L-1-0.01 L×0.020 0 mol·L-1=0.003
3 3
mol,由关系式PCl ~3HCl~3AgNO 及POCl ~3HCl~3AgNO 可知,10.00 mL 溶液中n(PCl )+
3 3 3 3 3
n(POCl )=0.001 mol,则产品中n(PCl )+n(POCl )=0.001× mol=0.01 mol,设POCl 的物质的量为x
3 3 3 3
mol,(153.5×x)g+[137.5×(0.01-x)]g=1.455 g,则x=0.005 mol,故产品的纯度为×100%≈52.7%。(3)
结合题中信息可知Cu2+与I-发生氧化还原反应的离子方程式为2Cu2++4I-===2CuI↓+I,若步骤②
2
中不加入足量的NaF溶液,Fe3+也消耗I-,导致最终测量值将偏大。根据关系式:2Cu2+~I ~
2
2Na S O ,可得c(Cu2+)=0.040 0 mol·L-1,则胆矾产品纯度=80.00%。
2 2 3
答案:(1)①偏大 锥形瓶内溶液颜色的变化 ②10.00%
(2)①当滴入最后半滴KSCN标准溶液时,溶液变为红色,且半分钟内不褪色 ②使生成的AgCl
沉淀与溶液隔离,避免滴定过程中 SCN-与AgCl反应 偏小 ③52.7% (3)偏大 2Cu2++4I-
===2CuI↓+I 80.00
2