文档内容
课时检测(五十九) 溶液中粒子浓度大小比较
1.常温下,某NH Cl溶液的pH=4,下列说法正确的是( )
4
①溶液中c(H+)>c(OH-)
②由水电离产生的c(H+)约为10-10 mol·L-1
③溶液中离子浓度关系为
c(Cl-)>c(NH)>c(H+)>c(OH-)
④在纯水中加入该NH Cl溶液,水的电离被抑制
4
A.①② B.①③
C.①④ D.①②③④
2.(2024·广西柳州模拟)次磷酸(H PO)是一种一元弱酸,与等浓度等体积的NaOH完全反应后生
3 2
成NaH PO,下列叙述错误的是( )
2 2
A.NaH PO 的水溶液加水稀释,增大
2 2
B.HPO 溶液中存在电离平衡:HPO HPO+H+
3 2 3 2 2
C.NaH 2 PO 2 溶液中: ⥫⥬
c(Na+)>c(H PO)>c(OH-)>c(H+)
2
D.NaH PO 溶液中存在:
2 2
c(H PO)+c(OH-)=c(H+)+c(Na+)
2
3.(2024·天津模拟)常温下,下列有关电解质溶液的叙述正确的是( )
A.0.1 mol·L-1HPO 溶液中:c(H PO)>c(H PO)>c(HPO)>c(PO)
3 4 3 4 2
B.0.1 mol·L-1Na CO 溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO)+c(C O)
2 2 4 2 2
C.0.1 mol·L-1NaHCO 溶液中:
3
c(H CO )+c(HCO)=0.1 mol·L-1
2 3
D.氨水和NH Cl溶液混合形成的pH=9的溶液中:c(Cl-)>c(NH)>c(OH-)>c(H+)
4
4.(2024·北京海淀模拟)向1 L 0.3 mol·L-1的氢氧化钠溶液中通入二氧化碳,假设完全反应,下列
说法错误的是( )
A.通入二氧化碳为0.15 mol时,2c(Na+)=c(H CO )+c(HCO)+c(CO)
2 3
B.通入二氧化碳为0.15 mol时,c(Na+)>c(CO)>c(OH-)>c(HCO)
C.通入二氧化碳为0.2 mol时,c(H+)+c(Na+)=c(OH-)+c(HCO)+2c(CO)
D.向A选项反应后的溶液中通入0.3 mol HCl,加热,c(Na+)=c(Cl-)=0.3 mol·L-1
5.常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的HCl和CH COOH的混合液,
3
下列说法不正确的是( )
A.在氨水滴定前,HCl和CH COOH的混合液中c(Cl-)>c(CHCOO-)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH·HO)=c(CHCOO-)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH·HO)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)c(NH)
3
D.当c(HR)=c(R-)时,溶液呈中性
11.25 ℃时,向10 mL 0.01 mol·L-1NaCN溶液中逐滴加入0.01 mol·L-1盐酸,溶液中CN-、HCN
的分布分数δ(X)δ(X)=,X=CN-或HCN随溶液pH的变化关系如图1所示,溶液pH随加入盐酸体
积的变化曲线如图2所示。下列说法正确的是( )
A.在pH=6的溶液中c(Cl-)c(Cl-)>c(HCN)>c(OH-)>c(H+)
D.c点对应溶液中:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
12.(2024·安徽蚌埠模拟)一种吸收SO 再经氧化得到硫酸盐的过程如图所示。室温下,用0.1
2
mol·L-1 的NaOH溶液吸收SO ,若通入SO 所引起的溶液体积变化和HO挥发可忽略,溶液中含硫
2 2 2
物种的浓度c =c(H SO )+c(HSO)+c(SO)。HSO 的电离常数分别为K =1.29×10-2,K =6.24×10-
总 2 3 2 3 a1 a2
8。下列说法错误的是( )A.“吸收”所得溶液中:c(Na+)+c(H+)=2c(SO)+c(HSO)+c(OH-)
B.“吸收”所得溶液中不可能存在:c(Na+)>c(H+)>c(SO)>c(HSO)>c(OH-)
C.“吸收”所得c =0.1 mol·L-1的溶液中:c(H SO )>c(SO)
总 2 3
D.调节“吸收”所得溶液的pH约为5,“氧化”时主要发生的反应为2HSO+O===2SO+2H+
2
课时检测(五十九)
1.B ②中c(H+)=10-4 mol·L-1,④中NH水解,水的电离被促进。
2.A NaH PO 的水溶液加水稀释,HPO水解程度增大:HPO+HO HPO+OH-,K =·,
2 2 2 2 2 3 2 h
则=·c(H PO),c(H PO) 不断变小,所以减小,A错误;次磷酸是一元弱酸,不完全电离,B正确;HPO
2 2 ⥫⥬ 2
水解,离子数量少于Na+,阴离子水解溶液显碱性,c(OH-) > c(H+),HPO水解数量极少,C正确;根
2
据溶液中电荷守恒,阳离子所带正电荷总量等于阴离子所带负电荷总量,D正确。
3.A 磷酸为多元酸,第一步电离程度>第二步电离程度>第三步电离程度,所以在0.1 mol·L-
1HPO 溶液中:c(H PO)>c(H PO)>c(HPO)>c(PO),故A正确;0.1 mol·L-1Na CO 溶液中,根据电
3 4 3 4 2 2 2 4
荷守恒得到c(Na+)+c(H+)=c(OH-)+c(HCO)+2c(C O),故B错误;0.1 mol·L-1NaHCO 溶液中,根
2 2 3
据物料守恒得到c(H CO )+c(HCO)+c(CO)=0.1 mol·L-1,故C错误;氨水和NH Cl溶液混合形成的
2 3 4
pH=9的溶液中:c(OH-)>c(H+),根据电荷守恒c(Cl-)+c(OH-)=c(NH)+c(H+),则c(Cl-)c(CHCOO-),A项正确;当滴入氨水10 mL 时,溶质为等物质的量的NH Cl和CH COOH溶液,
3 4 3
B项正确;当滴入氨水 20 mL时,溶液中溶质为CH COONH 和NH Cl,C项正确;恰好反应时,生成
3 4 4
等物质的量的氯化铵和醋酸铵,此时溶液呈酸性,若溶液呈中性,则氨水滴入量大于 20 mL,
c(NH)>c(Cl-),D项错误。
6.B 实验①反应后溶液的pH=9,即溶液显碱性,说明HA为弱酸,二者等浓度等体积混合恰好
反应生成KA,A-水解,A项正确;实验①反应后的溶液中,由电荷守恒式c(H+)+c(K+)=c(A-)+
c(OH-)知,c(K+)-c(A-)=c(OH-)-c(H+),B项错误;因为HA为弱酸,如果与等体积等浓度的KOH
溶液混合,溶液显碱性,若溶液显中性,则在两溶液体积相等的条件下,HA溶液的浓度应大于0.2
mol·L-1,所以实验②反应后的溶液中,c(A-)+c(HA)>0.1 mol·L-1,C项正确;实验②反应后溶液显中性,根据电荷守恒式c(H+)+c(K+)=c(A-)+c(OH-),且c(H+)=c(OH-),则c(K+)=c(A-),即c(K
+)=c(A-)>c(H+)=c(OH-),D项正确。
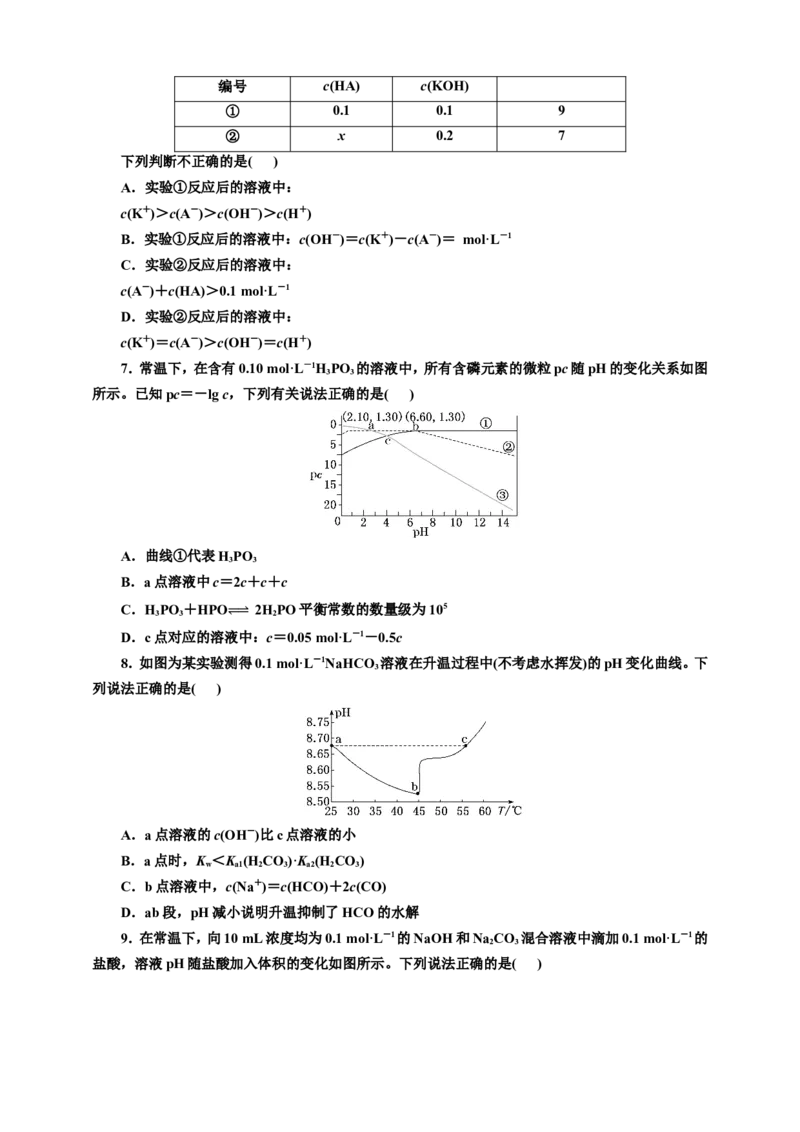
7.D HPO 的浓度随pH增大而减小,因此曲线③代表HPO,HPO的浓度随pH先增大后减
3 3 3 3 2
小,因此曲线②代表HPO,HPO的浓度随pH增大而增大,因此曲线①代表HPO;根据a、b两个交点
2
分别可以算出HPO 的K =10-2.1、K =10-6.6。根据分析,曲线③代表HPO,A错误;由电荷守恒关
3 3 a1 a2 3 3
系可知a点c<2c+c+c,B错误;该反应平衡常数K===104.5,因此平衡常数的数量级为104,C错误;
根据物料守恒:c+c+c(H PO)=0.1,而c点:c=c,代入物料守恒式即可推出c=0.05 mol·L-1-0.5c,
3 3
D正确。
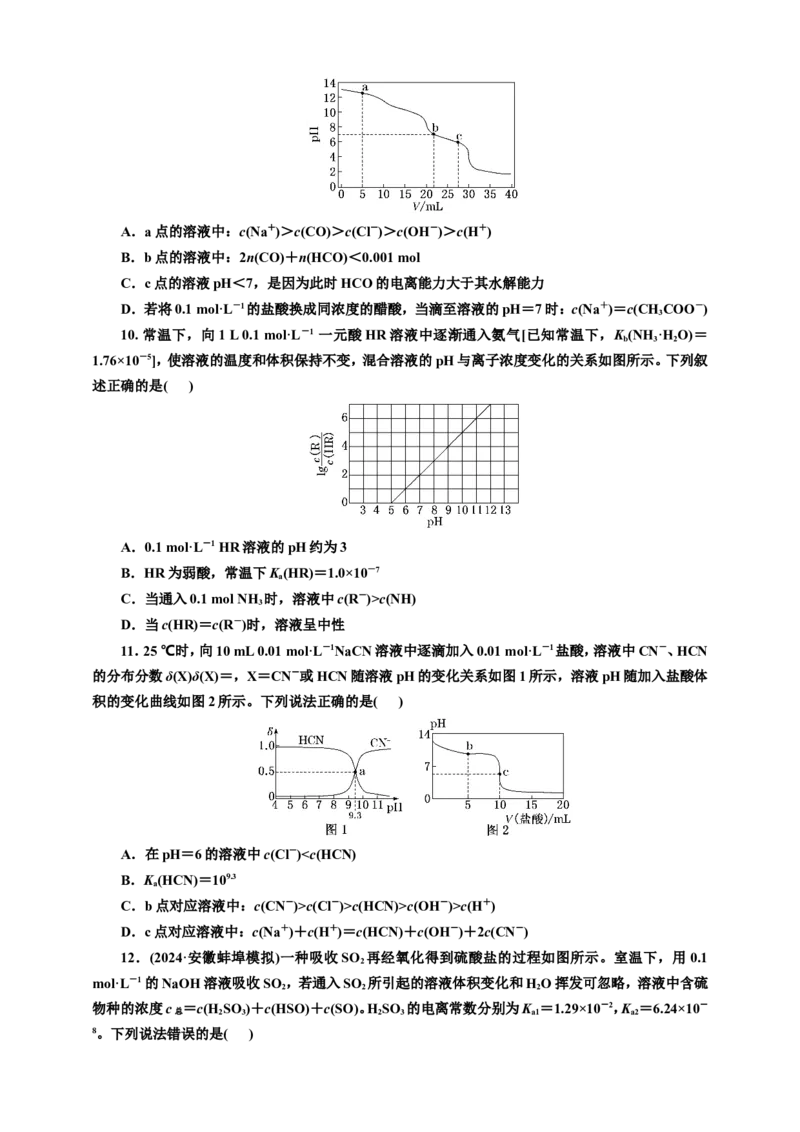
8.A K =c(H+)c(OH-),随着温度的升高,K 增大;a点、c点的pH相同,即氢离子浓度相同,但
w w
是c(OH-)不同,c点的K 大,所以a点溶液的c(OH-)比c点溶液的小,故A正确;碳酸氢钠溶液中存
w
在电离平衡和水解平衡,根据图示可知,碳酸氢钠溶液显碱性,碳酸氢根离子的水解程度大于电离程
度,K = >K ,所以K >K (H CO )·K (H CO ),故B错误;b点溶液显碱性,溶液中存在电荷守恒:
h a2 w a1 2 3 a2 2 3
c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-),由于c(H+)c(CO)>c(OH-)>c(Cl-)>c(H+ ),A错误;b点溶液pH=7,溶液为氯化钠、
碳酸氢钠和碳酸溶液,n(CO)c(CHCOO-),D错误。
3
10.A 由题图可知,pH=5时,lg=0,则有=1,说明HR在溶液中不能完全电离,则HR是弱酸,
存在电离平衡:HR H++R-,HR的电离平衡常数为K (HR)== c(H+)=1×10-5 mol·L-1,由于温
a
度不变,则K (HR)始终不变。设HR溶液中c(H+)=x mol·L-1,则有K (HR)==1×10-5,解得x=1×10
a ⥫⥬ a
-3,则pH=3,A正确,B错误。1 L 0.1 mol·L-1 一元酸HR溶液中通入0.1 mol NH ,二者恰好完全反
3
应生成NH R,由于K (HR)<K (NH·HO)=1.76×10-5,则R-的水解程度大于NH的水解程度,故溶
4 a b 3 2
液中c(R-)<c(NH),C错误。由题图可知,当c(HR)=c(R-)时,lg=0,pH=5,溶液呈酸性,D错误。
11.D 溶液中存在物料守恒:c(Na+)=c(HCN)+c(CN-)①、电荷守恒:c(Na+)+c(H+)=c(OH
-)+c(CN-)+c(Cl-)②,将①代入②得c(HCN)+c(H+)=c(OH-)+c(Cl-),又常温下pH=6时c(H
+)>c(OH-),则c(Cl-)>c(HCN),A项错误;题图1中a点对应溶液中c(CN-)=c(HCN),且此时溶液
pH=9.3,故K (HCN)==c(H+)=10-9.3,B项错误;b点对应溶液中的溶质是等物质的量的HCN、
a
NaCl与NaCN,且溶液呈碱性,则CN-的水解程度大于HCN的电离程度,故c(HCN)>c(Cl-)>c(CN
-),C项错误;c点对应溶液中的溶质是等物质的量的HCN和NaCl,电荷守恒关系式为c(Na+)+c(H
+)=c(OH-)+c(CN-)+c(Cl-)③,物料守恒关系式为c(Na+)=c(HCN)+c(CN-)=c(Cl-)④,联立
③④得c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-),D项正确。
12.C 二氧化硫被氢氧化钠吸收后可生成亚硫酸钠或亚硫酸氢钠,溶液中根据电荷守恒:c(Na+)+
c(H+)=2c(SO)+c(HSO)+c(OH-),A正确;HSO H++SO,无论是Na SO 或NaHSO ,不可能存
2 3 3
⥫⥬在c(Na+)>c(H+)>c(SO)>c(HSO)>c(OH-),B正确;c =0.1 mol·L-1时,相当于NaHSO 溶液,根
总 3
据电离常数计算,电离程度大于水解程度,c(SO)>c(H SO ),C错误;根据平衡常数数据可知,亚硫酸
2 3
氢钠的电离大于水解,溶液显酸性,所以若“吸收”所得溶液的pH约为5时,溶液中主要的阴离子为
HSO,“氧化”时主要发生的反应为2HSO+O===2SO+2H+,D正确。
2