文档内容
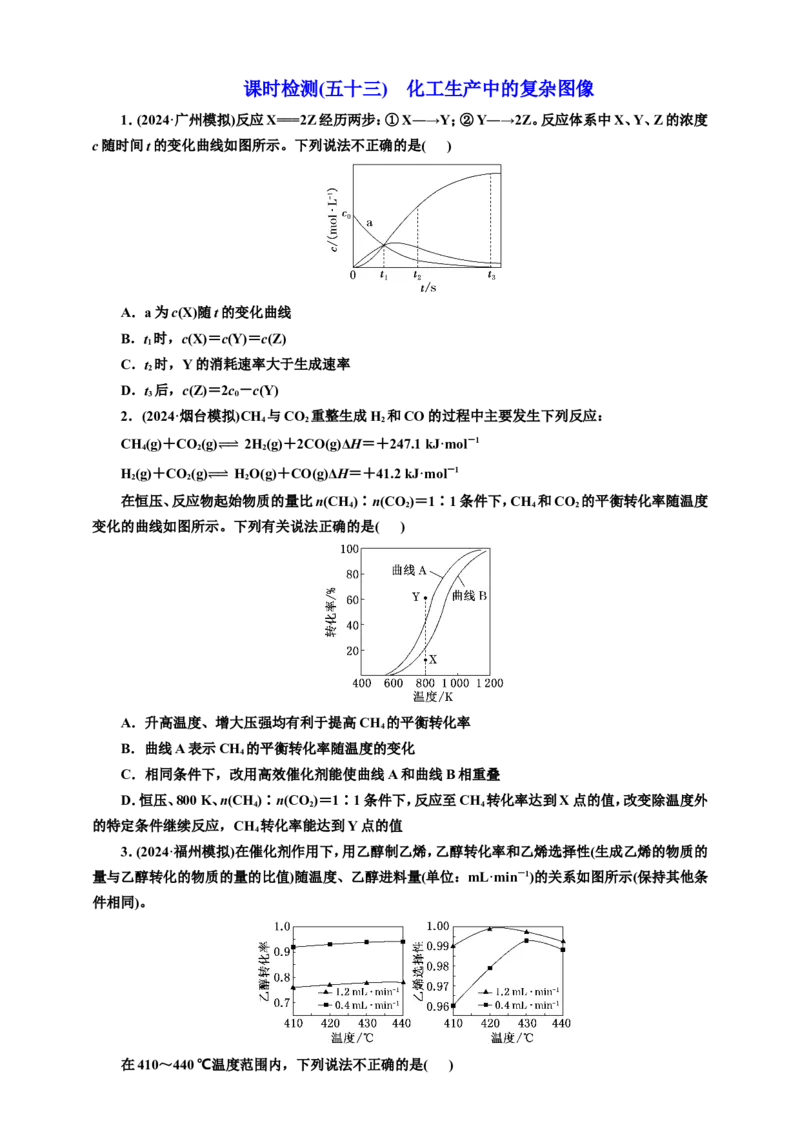
课时检测(五十三) 化工生产中的复杂图像
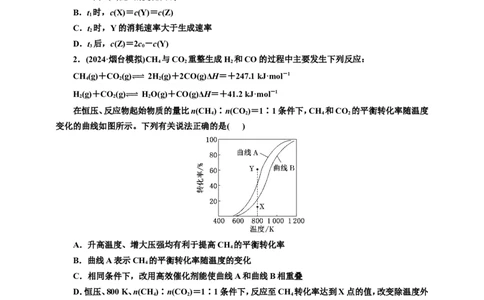
1.(2024·广州模拟)反应X===2Z经历两步:①X―→Y;②Y―→2Z。反应体系中X、Y、Z的浓度
c随时间t的变化曲线如图所示。下列说法不正确的是( )
A.a为c(X)随t的变化曲线
B.t 时,c(X)=c(Y)=c(Z)
1
C.t 时,Y的消耗速率大于生成速率
2
D.t 后,c(Z)=2c-c(Y)
3 0
2.(2024·烟台模拟)CH 与CO 重整生成H 和CO的过程中主要发生下列反应:
4 2 2
CH (g)+CO (g) 2H(g)+2CO(g)ΔH=+247.1 kJ·mol-1
4 2 2
H 2 (g)+CO 2 (g) ⥫⥬ H 2 O(g)+CO(g)ΔH=+41.2 kJ·mol-1
在恒压、反应物
⥫
起
⥬
始物质的量比n(CH
4
)∶n(CO
2
)=1∶1条件下,CH
4
和CO
2
的平衡转化率随温度
变化的曲线如图所示。下列有关说法正确的是( )
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线A表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH)∶n(CO)=1∶1条件下,反应至CH 转化率达到X点的值,改变除温度外
4 2 4
的特定条件继续反应,CH 转化率能达到Y点的值
4
3.(2024·福州模拟)在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的
量与乙醇转化的物质的量的比值)随温度、乙醇进料量(单位:mL·min-1)的关系如图所示(保持其他条
件相同)。
在410~440 ℃温度范围内,下列说法不正确的是( )A.当乙醇进料量一定,随乙醇转化率增大,乙烯选择性升高
B.当乙醇进料量一定,随温度的升高,乙烯选择性不一定增大
C.当温度一定,随乙醇进料量增大,乙醇转化率减小
D.当温度一定,随乙醇进料量增大,乙烯选择性增大
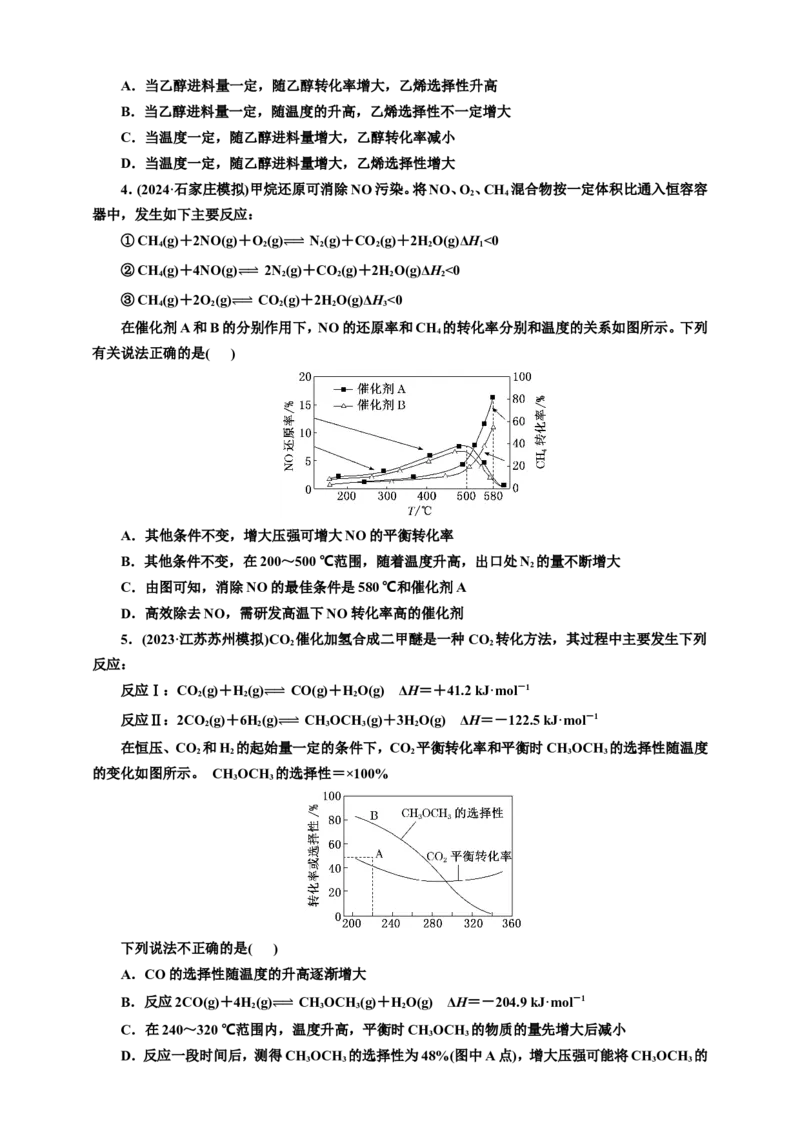
4.(2024·石家庄模拟)甲烷还原可消除NO污染。将NO、O、CH 混合物按一定体积比通入恒容容
2 4
器中,发生如下主要反应:
①CH (g)+2NO(g)+O(g) N(g)+CO (g)+2HO(g)ΔH<0
4 2 2 2 2 1
②CH
4
(g)+4NO(g) 2N 2⥫(g⥬)+CO
2
(g)+2H
2
O(g)ΔH
2
<0
③CH 4 (g)+2O 2 (g) ⥫⥬ CO 2 (g)+2H 2 O(g)ΔH 3 <0
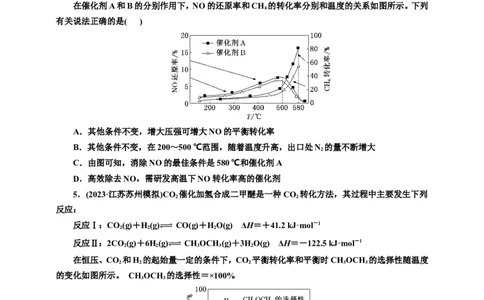
在催化剂A和B的
⥫
分
⥬
别作用下,NO的还原率和CH
4
的转化率分别和温度的关系如图所示。下列
有关说法正确的是( )
A.其他条件不变,增大压强可增大NO的平衡转化率
B.其他条件不变,在200~500 ℃范围,随着温度升高,出口处N 的量不断增大
2
C.由图可知,消除NO的最佳条件是580 ℃和催化剂A
D.高效除去NO,需研发高温下NO转化率高的催化剂
5.(2023·江苏苏州模拟)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下列
2 2
反应:
反应Ⅰ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
反应Ⅱ:2CO
2
(g)+6H
2
(⥫g⥬) CH
3
OCH
3
(g)+3H
2
O(g) ΔH=-122.5 kJ·mol-1
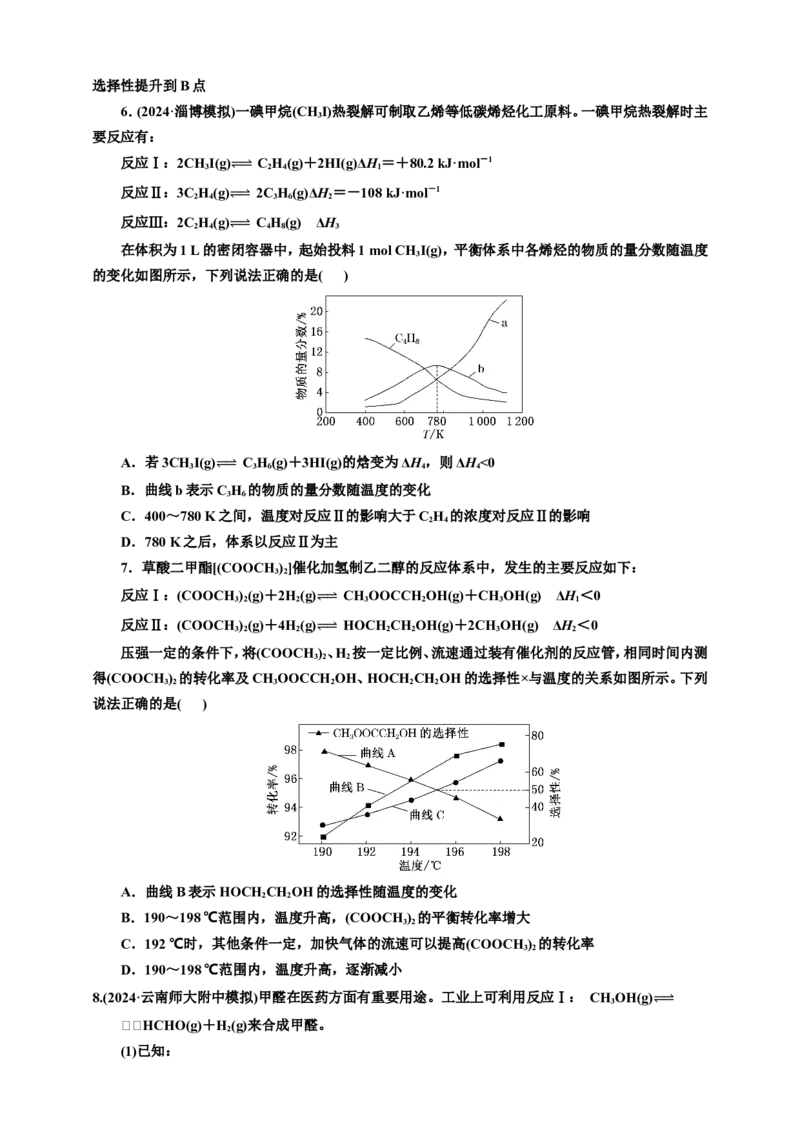
在恒压、CO 2 和H 2 的起始 ⥫ 量 ⥬ 一定的条件下,CO 2 平衡转化率和平衡时CH 3 OCH 3 的选择性随温度
的变化如图所示。 CH OCH 的选择性=×100%
3 3
下列说法不正确的是( )
A.CO的选择性随温度的升高逐渐增大
B.反应2CO(g)+4H(g) CH OCH (g)+HO(g) ΔH=-204.9 kJ·mol-1
2 3 3 2
C.在240~320 ℃范围内 ⥫ , ⥬ 温度升高,平衡时CH 3 OCH 3 的物质的量先增大后减小
D.反应一段时间后,测得CH OCH 的选择性为48%(图中A点),增大压强可能将CH OCH 的
3 3 3 3选择性提升到B点
6.(2024·淄博模拟)一碘甲烷(CHI)热裂解可制取乙烯等低碳烯烃化工原料。一碘甲烷热裂解时主
3
要反应有:
反应Ⅰ:2CH I(g) CH(g)+2HI(g)ΔH=+80.2 kJ·mol-1
3 2 4 1
反应Ⅱ:3C
2
H
4
(g)⥫⥬ 2C
3
H
6
(g)ΔH
2
=-108 kJ·mol-1
反应Ⅲ:2C
2
H
4
(g)⥫⥬ C
4
H
8
(g) ΔH
3
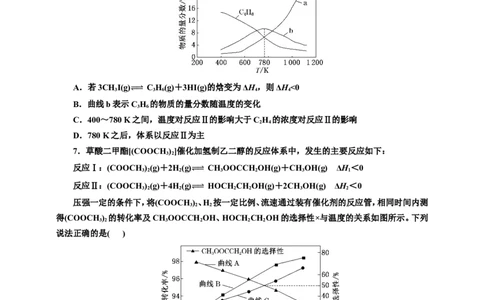
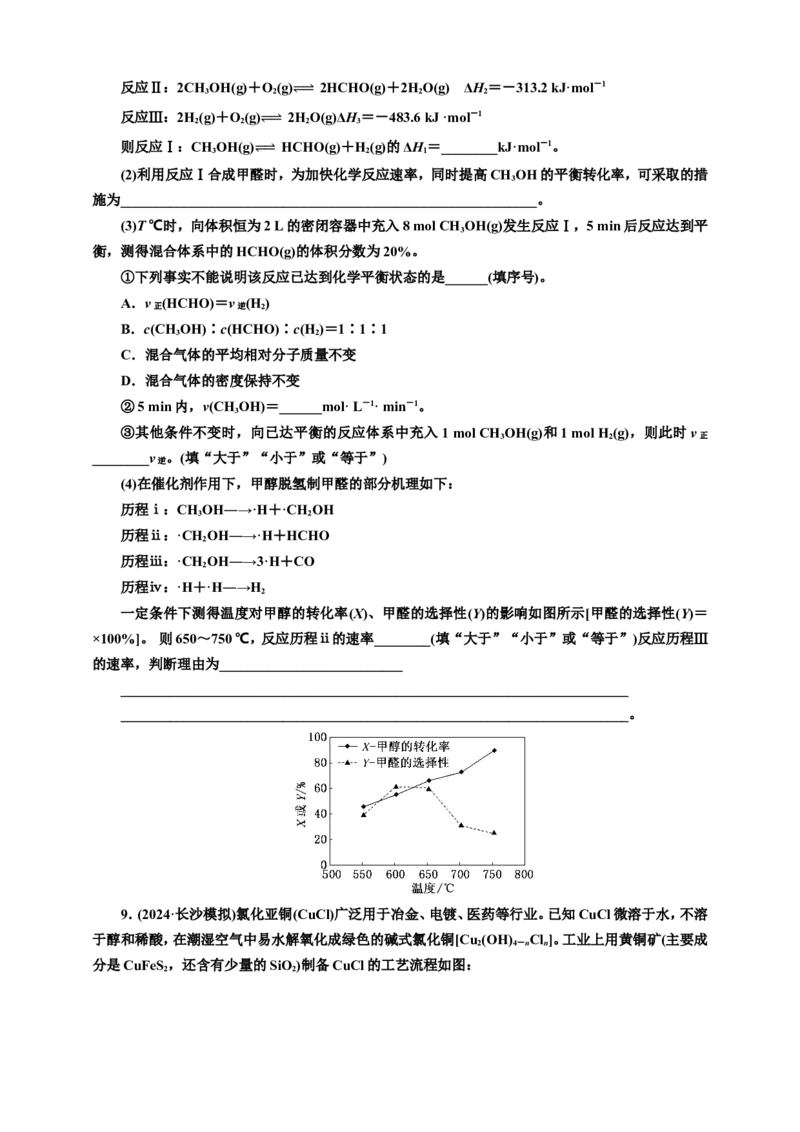
在体积为1 L的密 ⥫ 闭 ⥬ 容器中,起始投料1 mol CH 3 I(g),平衡体系中各烯烃的物质的量分数随温度
的变化如图所示,下列说法正确的是( )
A.若3CH I(g) CH(g)+3HI(g)的焓变为ΔH,则ΔH<0
3 3 6 4 4
B.曲线b表示 ⥫C⥬3 H
6
的物质的量分数随温度的变化
C.400~780 K之间,温度对反应Ⅱ的影响大于CH 的浓度对反应Ⅱ的影响
2 4
D.780 K之后,体系以反应Ⅱ为主
7.草酸二甲酯[(COOCH )]催化加氢制乙二醇的反应体系中,发生的主要反应如下:
3 2
反应Ⅰ:(COOCH )(g)+2H(g) CH OOCCH OH(g)+CH OH(g) ΔH<0
3 2 2 3 2 3 1
反应Ⅱ:(COOCH
3
)
2
(g)+4H
2
(g)⥫⥬ HOCH
2
CH
2
OH(g)+2CH
3
OH(g) ΔH
2
<0
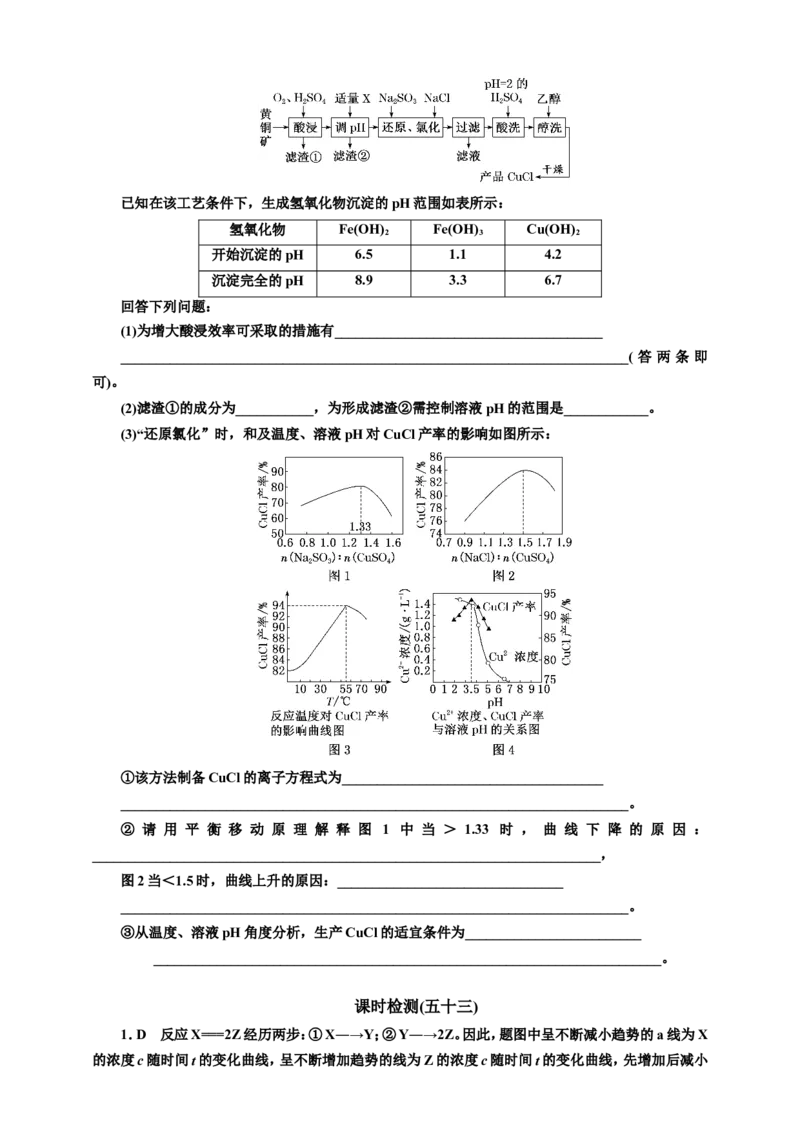
压强一定的条件下,将(COOCH 3⥫) 2⥬ 、H 2 按一定比例、流速通过装有催化剂的反应管,相同时间内测
得(COOCH ) 的转化率及CH OOCCH OH、HOCH CH OH的选择性×与温度的关系如图所示。下列
3 2 3 2 2 2
说法正确的是( )
A.曲线B表示HOCH CH OH的选择性随温度的变化
2 2
B.190~198 ℃范围内,温度升高,(COOCH ) 的平衡转化率增大
3 2
C.192 ℃时,其他条件一定,加快气体的流速可以提高(COOCH ) 的转化率
3 2
D.190~198 ℃范围内,温度升高,逐渐减小
8.(2024·云南师大附中模拟)甲醛在医药方面有重要用途。工业上可利用反应Ⅰ: CH OH(g)
3
HCHO(g)+H
2
(g)来合成甲醛。
⥫⥬
(1)已知:反应Ⅱ:2CH OH(g)+O(g) 2HCHO(g)+2HO(g) ΔH=-313.2 kJ·mol-1
3 2 2 2
反应Ⅲ:2H
2
(g)+O
2
(g) 2⥫H⥬2 O(g)ΔH
3
=-483.6 kJ ·mol-1
则反应Ⅰ:CH 3 OH(g) ⥫⥬ HCHO(g)+H 2 (g)的ΔH 1 =________kJ·mol-1。
(2)利用反应Ⅰ合成甲醛
⥫
时
⥬
,为加快化学反应速率,同时提高CH
3
OH的平衡转化率,可采取的措
施为___________________________________________________________。
(3)T ℃时,向体积恒为2 L的密闭容器中充入8 mol CH OH(g)发生反应Ⅰ,5 min后反应达到平
3
衡,测得混合体系中的HCHO(g)的体积分数为20%。
①下列事实不能说明该反应已达到化学平衡状态的是______(填序号)。
A.v (HCHO)=v (H )
正 逆 2
B.c(CHOH)∶c(HCHO)∶c(H )=1∶1∶1
3 2
C.混合气体的平均相对分子质量不变
D.混合气体的密度保持不变
②5 min内,v(CHOH)=______mol· L-1· min-1。
3
③其他条件不变时,向已达平衡的反应体系中充入1 mol CH OH(g)和1 mol H (g),则此时v
3 2 正
________v 。(填“大于”“小于”或“等于”)
逆
(4)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
历程ⅰ:CH OH―→·H+·CH OH
3 2
历程ⅱ:·CH OH―→·H+HCHO
2
历程ⅲ:·CH OH―→3·H+CO
2
历程ⅳ:·H+·H―→H
2
一定条件下测得温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如图所示[甲醛的选择性(Y)=
×100%]。 则650~750 ℃,反应历程ⅱ的速率________(填“大于”“小于”或“等于”)反应历程Ⅲ
的速率,判断理由为__________________________
________________________________________________________________________
________________________________________________________________________。
9.(2024·长沙模拟)氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl微溶于水,不溶
于醇和稀酸,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu (OH) Cl ]。工业上用黄铜矿(主要成
2 4-n n
分是CuFeS ,还含有少量的SiO )制备CuCl的工艺流程如图:
2 2已知在该工艺条件下,生成氢氧化物沉淀的pH范围如表所示:
氢氧化物 Fe(OH) Fe(OH) Cu(OH)
2 3 2
开始沉淀的pH 6.5 1.1 4.2
沉淀完全的pH 8.9 3.3 6.7
回答下列问题:
(1)为增大酸浸效率可采取的措施有______________________________________
________________________________________________________________________( 答 两 条 即
可)。
(2)滤渣①的成分为___________,为形成滤渣②需控制溶液pH的范围是____________。
(3)“还原氯化”时,和及温度、溶液pH对CuCl产率的影响如图所示:
①该方法制备CuCl的离子方程式为_____________________________________
________________________________________________________________________。
② 请 用 平 衡 移 动 原 理 解 释 图 1 中 当 > 1.33 时 , 曲 线 下 降 的 原 因 :
________________________________________________________________________,
图2当<1.5时,曲线上升的原因:________________________________
________________________________________________________________________。
③从温度、溶液pH角度分析,生产CuCl的适宜条件为_________________________
________________________________________________________________________。
课时检测(五十三)
1.D 反应X===2Z经历两步:①X―→Y;②Y―→2Z。因此,题图中呈不断减小趋势的a线为X
的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加后减小的线为Y的浓度c随时间t的变化曲线,A正确;由题图可知,分别代表3种不同物质的曲线相交于t
1
时刻,c(X)=c(Y)=c(Z),B正确;t 时刻以后,Y的浓度仍在不断减小,说明反应①生成Y的速率小于
2
反应②消耗Y的速率,C正确;t 时刻反应①完成,X完全转化为Y,若无反应②发生,则c(Y)=c,t 时
3 0 3
刻Y浓度的变化量为c-c(Y),所以Z的浓度的变化量为2[c-c(Y)],这种关系在t 后仍成立,因此,
0 0 3
D不正确。
2.D 甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应方向即正向移动,甲烷转化率
增大;甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,A错误。加
入的CH 与CO 物质的量相等,CO 消耗量大于CH ,因此CO 的转化率大于CH ,因此曲线B表示
4 2 2 4 2 4
CH 的平衡转化率随温度变化,B错误;使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,
4
C错误;800 K时甲烷的转化率为X点,可以通过改变二氧化碳的量来提高甲烷的转化率达到Y点的
值,D正确。
3.A 根据图像,当乙醇进料量一定,随乙醇转化率增大,乙烯选择性逐渐升高,但温度高于430
℃后,乙烯选择性逐渐降低,A错误;根据图像,当乙醇进料量一定,随温度升高,乙烯选择性先逐渐升
高,后逐渐降低,B正确;根据左图,当温度一定,随乙醇进料量增大,乙醇转化率减小,C正确;根据右
图,当温度一定,随乙醇进料量增大,乙烯选择性增大,D正确。
4.B 反应①和②均是反应前后气体体积不变的反应,增大压强平衡不发生移动,NO的平衡转化
率不变,故A错误;在200~500 ℃范围,随着温度升高,NO的还原率增大,NO还原为氮气的浓度增
大,则出口处N 的量不断增大,故B正确;500 ℃时催化剂A作用下NO还原率最高,是消除NO的最
2
佳条件,故C错误;使用催化剂,能加快反应速率,但平衡不移动,NO转化率不变,故D错误。
5.C 由题图可知,升高温度,二甲醚的选择性减小,由碳原子守恒可知,一氧化碳的选择性增大,
故A正确;由盖斯定律可知,反应Ⅱ-2×反应Ⅰ得2CO(g)+4H(g)CHOCH (g)+HO(g) ΔH=
2 3 3 2
(-122.5 kJ·mol-1)-2×(+41.2 kJ·mol-1)=-204.9 kJ·mol-1,故B正确;反应Ⅱ是放热反应,升高温
度,平衡向逆反应方向移动,二甲醚的物质的量减小,故C错误;反应Ⅱ是气体体积减小的反应,在温
度不变的条件下,增大压强,平衡向正反应方向移动,二甲醚的物质的量增大,二甲醚的选择性增大,
则增大压强可能将二甲醚的选择性由A点提升到B点,故D正确。
6.B 根据盖斯定律,反应Ⅰ×+反应Ⅱ×得到反应3CH I(g)CH(g)+3HI(g),则ΔH =(+
3 3 6 4
80.2 kJ·mol-1) ×+(-108 kJ·mol-1)×=+66.3 kJ·mol-1>0,故A错误;由热化学方程式可知,反应Ⅰ
为吸热反应,升高温度,平衡向正反应方向移动,CH 的物质的量分数增大,反应Ⅱ为放热反应,升高
2 4
温度,平衡向逆反应方向移动,CH 的物质的量分数增大、CH 的物质的量分数减小,则曲线b表示
2 4 3 6
CH 的物质的量分数随温度的变化,故B正确;由题图可知,780 K时CH 的物质的量分数最大,说
3 6 3 6
明反应达到平衡,则温度400~780 K时,反应未达到平衡,说明温度对反应Ⅱ的影响小于CH 的浓度
2 4
对反应Ⅱ的影响,故C错误;反应Ⅱ、Ⅲ为放热反应,升高温度,平衡向逆反应方向移动,反应Ⅰ为吸热
反应,升高温度,平衡向正反应方向移动,所以不能确定780 K之后体系以反应Ⅱ为主,故D错误。
7.D 由题给选择性的公式可知,相同条件下CH OOCCH OH和HOCH CH OH的选择性之和
3 2 2 2
为100%,曲线A表示CH OOCCH OH的选择性随温度的变化,则曲线C表示HOCH CH OH的选
3 2 2 2
择性随温度的变化,A项错误;两个反应均为放热反应,升高温度,平衡均逆向移动,故190~198 ℃范
围内,温度升高,(COOCH ) 的平衡转化率减小,B项错误;192 ℃时,其他条件一定,加快气体的流速,
3 2
反应物(COOCH ) 的转化率降低,C项错误;根据题图知,190~198 ℃范围内,升高温度,生成的
3 2
HOCH CH OH的量逐渐增大,利用极值法进行判断,设190 ℃时只发生反应Ⅰ,则的值无穷大,升高
2 2温度,198 ℃时只发生反应Ⅱ,则的值为2,逐渐减小,故D项正确。
8.解析:(1)由盖斯定律可得,ΔH=(ΔH-ΔH)=×(-313.2+483.6)kJ·mol-1=+85.2 kJ·mol-1。
1 2 3
(2)反应Ⅰ为吸热反应,因此可采取升高温度的措施来加快化学反应速率,同时提高CH OH的平衡转
3
化率。(3)①当 v (HCHO)=v (H )时,说明反应已经达到平衡状态, A 项正确;
正 逆 2
c(CHOH)∶c(HCHO)∶c(H )=1∶1∶1时不能说明反应已经达到平衡状态,B项错误;该反应前后气
3 2
体分子数不等,当混合气体的平均相对分子质量不变时,混合体系中气体总物质的量不变,说明反应
已经达到平衡状态,C项正确;该反应在体积不变的容器中进行,反应过程中混合气体的密度始终保
持不变,故混合气体的密度不变时不能说明反应已经达到平衡状态,D项错误。②平衡时混合体系中
HCHO(g)的体积分数为20%,若甲醇消耗的物质的量为x mol,则×100%=20%,x=2,则5 min内,
v(CHOH)==0.2 mol·L-1·min-1。③反应达平衡时,CH OH(g)、HCHO(g)、H(g)的物质的量浓度分别
3 3 2
为3 mol·L-1、1 mol·L-1、1 mol·L-1,该条件下反应的平衡常数K==,向已达平衡的反应体系中充入
1 mol CH OH(g)和1 mol H (g)时,CH OH(g)、HCHO(g)、H(g)的物质的量浓度分别为3.5 mol·L-1、1
3 2 3 2
mol·L-1、1.5 mol·L-1,则浓度商Q==>,反应向逆反应方向进行,故v 小于v 。(4)由题图可知650~
正 逆
750 ℃,甲醇的转化率增大,甲醛的选择性减小,即生成的甲醛减少,CO增多,所以反应历程ⅱ的速率
小于反应历程ⅲ的速率。
答案:(1)+85.2 (2)升高温度 (3)①BD ②0.2 ③小于
(4)小于 由图可知650~750 ℃,甲醇的转化率增大,甲醛的选择性减小,即生成的甲醛减少,CO
增多,所以反应历程ⅱ的速率小于反应历程ⅲ的速率
9.解析:(1)为增大酸浸效率,即加快反应速率,可采用适当增大硫酸的浓度、升高温度等措施来加
快反应的速率。(2)加入硫酸和O 酸浸后,生成硫酸铜和硫酸铁,SiO 不与硫酸反应,则滤渣①为二氧
2 2
化硅。加入适量X调节pH的目的是让溶液中的铁离子生成氢氧化铁沉淀,同时铜离子不能沉淀,故控
制pH为3.3~4.2。(3)①CuSO 与Na SO 、NaCl溶液反应生成CuCl的离子方程式为2Cu2++SO+
4 2 3
2Cl-+HO===2CuCl↓+SO+2H+。②亚硫酸钠水解显碱性,随着不断增大,溶液的碱性不断增强,
2
Cu2+及CuCl的水解程度增大,导致CuCl产率减小;CuCl微溶于水,Cu+(aq)+Cl-(aq)CuCl(s),
适当增大氯离子浓度,有利于平衡正向移动,生成更多的CuCl。③根据图3和图4可知,当反应温度为
55 ℃,溶液pH为3.5时,CuCl的产率最高。
答案:(1)适当增大硫酸的浓度、升高温度 (2)SiO 3.3~4.2
2
(3)①2Cu2++SO+2Cl-+HO===2CuCl↓+SO+2H+ ②随着不断增大,溶液的碱性不断增强,
2
Cu2+及CuCl的水解程度增大,导致CuCl产率减小 适当增大氯离子浓度,有利于平衡Cu+(aq)+Cl
-(aq)CuCl(s)正向移动,生成更多的CuCl ③反应温度为55 ℃,溶液pH为3.5