文档内容
课时检测(十九) 变价金属与两性金属
1.2023年9月12日,天舟五号货运飞船再入大气层。天舟五号飞船的天线用钛镍记忆合金制造,
工业上用钛酸亚铁(FeTiO )冶炼钛的原理如下。
3
①高温下:
2FeTiO+6C+7Cl ===2TiCl +2FeCl+6CO
3 2 4 3
②在氩气氛围高温中:
2Mg+TiCl===Ti+2MgCl
4 2
下列有关说法正确的是( )
A.①中化合价变化的元素只有C、Cl
B.①中TiCl 是氧化产物
4
C.②中氩气的作用是防止Mg、Ti被氧化
D.②中可以得出Mg得电子的能力强于Ti
2.含铬废水会严重污染环境,一种烟气协同处理含铬废水(含CrO、CrO、泥沙等)的流程如图:
2
下列说法不正确的是( )
A.“沉降”的主要目的是除去泥沙等不溶物
B.溶液A通常选用硫酸“调pH”,目的是将CrO转化为CrO
2
C.“还原”过程涉及的氧化还原反应中,氧化剂与还原剂的物质的量之比为2∶3
D.母液经处理可获得(NH)SO
4 2 4
3.(2023·山东烟台模拟)“太空金属”钛广泛应用于新型功能材料等方面,工业上用钛铁矿(主要成
分是TiO,含少量FeO和FeO)冶炼金属钛的工艺流程如图所示,下列说法正确的是( )
2 2 3
A.基态钛原子核外最外层有2个未成对电子
B.金属Mg与TiCl 可在氮气气氛条件下进行反应
4
C.步骤Ⅱ加热可促进TiO2+的水解
D.步骤Ⅲ中可能发生的反应为TiO+2Cl +C=====TiCl+CO
2 2 4
4.工业上以碳酸锰矿(主要成分为MnCO ,另含FeO、FeO、CaO等杂质)为主要原料生产锰酸锂
3 2 3
(LiMn O),工艺流程如下:
2 4下列说法错误的是( )
A.可采用搅拌的方法提高“酸浸”时碳酸锰矿的浸出速率
B.加入CaO的目的是调节pH,使Fe3+转化为Fe(OH) 除去
3
C.“合成MnO ”的化学方程式为MnSO +KSO+2HO===MnO ↓+KSO +2HSO
2 4 2 2 8 2 2 2 4 2 4
D.“气体1”中含两种气体,一种是CO ,另一种可能是CO
2
5.草酸钴主要用作制氧化钴的原料,也可用于制取其他钴化合物。利用废料铝钴膜(含有LiCoO 、
2
Al、Fe)制备草酸钴的工艺如下:
下列有关说法错误的是( )
A.碱浸的目的是溶解除铝
B.氢碘酸在流程中既表现酸性,又表现还原性
C.滤渣的主要成分是氢氧化铁
D.沉钴时检验沉淀是否洗涤干净可用的试剂为盐酸
6.(2023·广东等级考·节选)Ni、Co均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+、
Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品。工艺流程如图:
已知:氨性溶液由NH ·HO、(NH)SO 和(NH)CO 配制。常温下,Ni2+、Co2+、Co3+与NH 形成
3 2 4 2 3 4 2 3 3
可溶于水的配离子;lg K (NH·HO)=-4.7;Co(OH) 易被空气氧化为Co(OH) ;部分氢氧化物的K
b 3 2 2 3 sp
如下表。
氢氧化物 Co(OH) Co(OH) Ni(OH)
2 3 2
K 5.9×10-15 1.6×10-44 5.5×10-16
sp
氢氧化物 Al(OH) Mg(OH)
3 2
K 1.3×10-33 5.6×10-12
sp
回答下列问题:(1)活性MgO可与水反应,化学方程式为______________________________________
________________________________________________________________________。
(2)常温下,pH=9.9的氨性溶液中,c(NH·HO)________c(NH)(填“>”“<”或“=”)。
3 2
(3)“氨浸”时,由Co(OH) 转化为[Co(NH )]2+的离子方程式为_________________
3 3 6
________________________________________________________________________。
(4)“析晶”过程中通入的酸性气体A为__________________________________。
(5)①“结晶纯化”过程中,没有引入新物质。晶体 A含6个结晶水,则所得HNO 溶液中
3
n(HNO )与n(H O)的比值,理论上最高为_________________________________。
3 2
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO 和________(填化学式)。
3
7.以电解金属锰的阳极渣(主要成分为MnO ,杂质为PbCO 、FeO、CuO)和黄铁矿(FeS )为原料
2 3 2 3 2
可制备Mn O,其流程如图所示:
3 4
已知部分阳离子以氢氧化物的形式完全沉淀时的pH:Fe3+为3.7,Fe2+为9.7,Cu2+为7.4,Mn2+为
9.8。
回答下列问题:
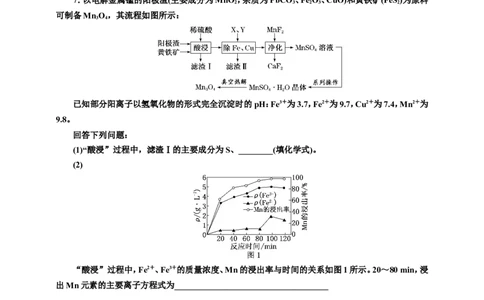
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、________(填化学式)。
(2)
“酸浸”过程中,Fe2+、Fe3+的质量浓度、Mn的浸出率与时间的关系如图1所示。20~80 min,浸
出Mn元素的主要离子方程式为____________________________________
________________________________________________________________________。
80~100 min时,Fe2+的质量浓度上升的原因可能是___________________________
________________________________________________________________________。
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为________(填字母)。
A.NH ·HO、HO
3 2 2 2
B.HO、CaCO
2 2 3
C.SO 、MnCO
2 3
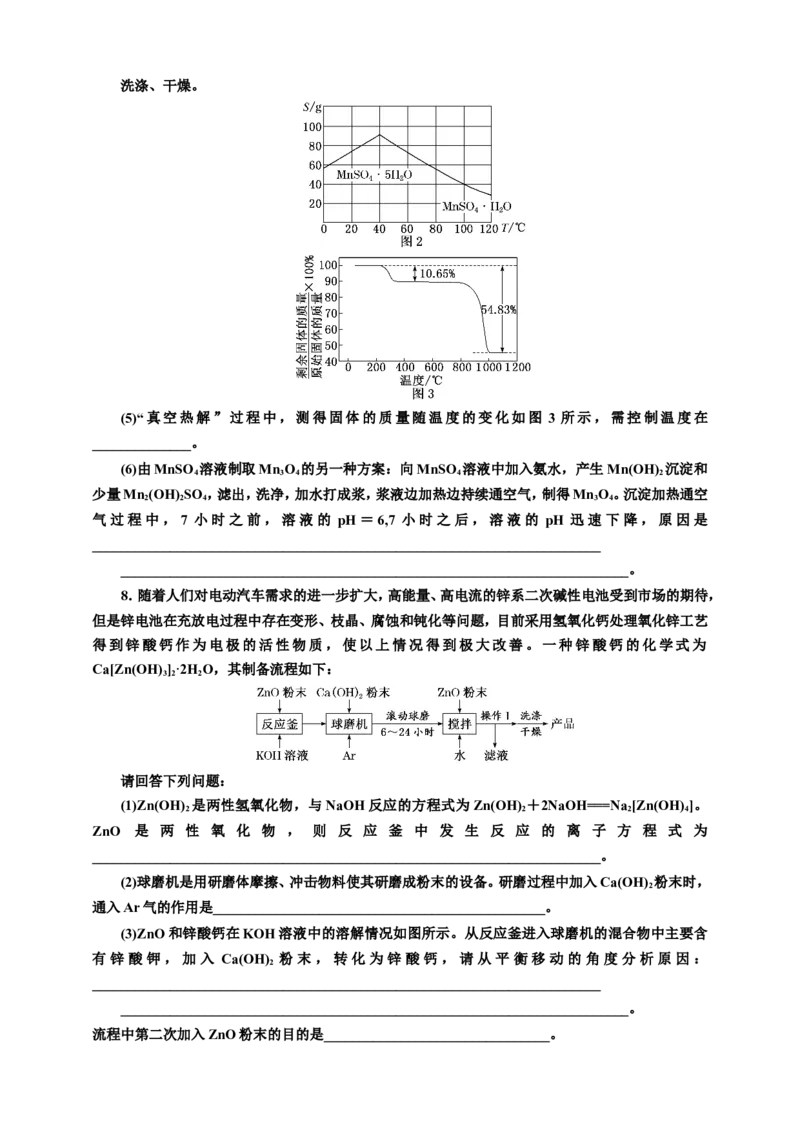
(4)硫酸锰晶体的溶解度曲线如图 2,由 MnSO 溶液获得 MnSO ·HO 晶体的系列操作为
4 4 2
________________________________________________________________________
________________________________________________________________________、洗涤、干燥。
(5)“真空热解”过程中,测得固体的质量随温度的变化如图 3 所示,需控制温度在
______________。
(6)由MnSO 溶液制取Mn O 的另一种方案:向MnSO 溶液中加入氨水,产生Mn(OH) 沉淀和
4 3 4 4 2
少量Mn (OH) SO ,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn O。沉淀加热通空
2 2 4 3 4
气过程中,7 小时之前,溶液的 pH=6,7 小时之后,溶液的 pH 迅速下降,原因是
________________________________________________________________________
________________________________________________________________________。
8.随着人们对电动汽车需求的进一步扩大,高能量、高电流的锌系二次碱性电池受到市场的期待,
但是锌电池在充放电过程中存在变形、枝晶、腐蚀和钝化等问题,目前采用氢氧化钙处理氧化锌工艺
得到锌酸钙作为电极的活性物质,使以上情况得到极大改善。一种锌酸钙的化学式为
Ca[Zn(OH) ]·2HO,其制备流程如下:
3 2 2
请回答下列问题:
(1)Zn(OH) 是两性氢氧化物,与NaOH反应的方程式为Zn(OH) +2NaOH===Na [Zn(OH) ]。
2 2 2 4
ZnO 是 两 性 氧 化 物 , 则 反 应 釜 中 发 生 反 应 的 离 子 方 程 式 为
________________________________________________________________________。
(2)球磨机是用研磨体摩擦、冲击物料使其研磨成粉末的设备。研磨过程中加入Ca(OH) 粉末时,
2
通入Ar气的作用是_______________________________________________。
(3)ZnO和锌酸钙在KOH溶液中的溶解情况如图所示。从反应釜进入球磨机的混合物中主要含
有锌酸钾,加入 Ca(OH) 粉末,转化为锌酸钙,请从平衡移动的角度分析原因:
2
________________________________________________________________________
________________________________________________________________________。
流程中第二次加入ZnO粉末的目的是________________________________。(4)滚动球磨6~24小时的目的是__________________________________________
________________。
(5) 操 作 Ⅰ 为 __________ 。 干 燥 产 品 时 必 须 在 低 温 减 压 条 件 下 进 行 , 理 由 是
________________________________________________________________________。
9.以某废钒渣(主要成分为VO,含有少量Al O、CaO)为原料生产VO 的工艺流程如下:
2 3 2 3 2 5
已知:钒酸(H VO)是强酸,NH VO 难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关
3 4 4 3
系如表:
pH 4~6 6~8 8~10 10~12
主要离子 VO VO VO VO
2
(1)“酸浸”前需将块状固体粉碎,其目的是________________________________
________________________________________________________________________。
(2)已知Ca(VO) 难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO) 溶于盐酸的离
3 2 3 2
子方程式为__________________________________________________
________________________________________________________________________。
(3)“沉钒 2”的沉钒率随温度的变化如图所示,温度高于 80 ℃沉钒率下降的原因是
________________________________________________________________________
________________________________________________________________________。
(4)NHVO 灼烧脱氨可得VO。在硫酸酸化条件下,VO 可与草酸(H CO)溶液反应得到含VO2
4 3 2 5 2 5 2 2 4
+的溶液,反应的离子方程式为_____________________________________
________________________________________________________________________。
(5) 测定产品中VO 的纯度:取a g产品用硫酸溶解得(VO)SO 溶液,加入b mL c mol·L-
2 5 2 2 4 1 1
1(NH)Fe(SO ) 溶液(VO+2H++Fe2+===VO2++Fe3++HO),再用c mol·L-1KMnO 溶液滴定过量
4 2 4 2 2 2 4
的(NH)Fe(SO ) 至终点,消耗KMnO 溶液的体积为b mL。已知MnO被还原为Mn2+,假设杂质不
4 2 4 2 4 2
参与反应,则产品中VO 的质量分数是____________________(V O 的摩尔质量为M g·mol-1)。
2 5 2 5课时检测(十九)
1.C ①中化合价变化的元素有 C、Cl、Fe,A 错误;①中TiCl 是还原产物,B 错误;②中氩气的
4
作用是隔绝空气,防止 Mg、Ti高温时被氧化,C正确;②中可以得出镁的还原性强于 Ti,还原性是一
种失电子的能力,D错误。
2.C “沉降”的主要目的是除去泥沙等不溶物,A正确;CrO+HO 2CrO+2H+,加入稀
2 2
硫酸,氢离子浓度变大,平衡逆向移动,CrO转化为CrO,B正确;“还原⥫”⥬过程发生反应CrO+
2 2
3SO +2H+===2Cr3++3SO+HO,CrO为氧化剂,SO 为还原剂,则氧化剂与还原剂的物质的量之
2 2 2 2
比为1∶3,C错误;调节pH时加硫酸,沉铬时加氨水,则母液经处理可获得(NH)SO ,D正确。
4 2 4
3.C 钛铁矿(主要成分是TiO,含少量FeO和FeO)加硫酸酸浸,浸出液中含铁离子、亚铁离子
2 2 3
和TiO2+,加适量铁将铁离子还原为亚铁离子,蒸发浓缩,冷却结晶得绿矾晶体,滤液经加热使TiO2+
水解得TiO·nHO,分解得到粗TiO 后,加焦炭、氯气反应得到TiCl,用Mg还原得到Ti。基态钛原子
2 2 2 4
核外电子排布式为[Ar]3d24s2,次外层3d轨道有2个未成对电子,A错误;Mg为活泼金属,能与CO 、
2
O、N、HO等物质发生反应,故金属Mg与TiCl 必须在稀有气体氛围条件下进行反应,B错误;TiO2
2 2 2 4
+会水解,步骤Ⅱ加热可促进TiO2+的水解,C正确;方程式未配平,步骤Ⅲ中可能发生的反应为TiO
2
+2Cl +2C=====TiCl+2CO ,D错误。
2 4
4.D 搅拌可使反应物之间接触更充分,从而提高“酸浸”时碳酸锰矿的浸出速率,故A正确;
加入CaO生成氢氧化钙,能使铁离子转化成氢氧化铁沉淀除去,故B正确;“合成MnO ”过程中,硫
2
酸锰作还原剂,KSO 作氧化剂(-1价的氧得电子),根据得失电子守恒可得反应:MnSO +KSO+
2 2 8 4 2 2 8
2HO===MnO ↓+KSO +2HSO ,故C正确;二氧化锰与碳酸锂混合反应生成LiMn O,LiMn O
2 2 2 4 2 4 2 4 2 4
中Mn的化合价有+3价、+4价两种,可知发生了氧化还原反应,二氧化锰作氧化剂,则化合价升高
的只能是-2价氧元素,故产物中还有氧气,“气体1”中所含的两种气体应为二氧化碳和氧气,故D
错误。
5.D 碱浸时Al溶于氢氧化钠溶液生成四羟基合铝酸钠和氢气,碱浸的目的是溶解除铝,故A正
确;氢碘酸溶解LiCoO 和Fe,发生反应的离子方程式为2LiCoO +2I-+8H+===2Li++2Co2++I+
2 2 2
4HO、Fe+2H+===Fe2++H↑,在流程中氢碘酸体现酸性和还原性,故B正确;净化过程中,氧气把
2 2
Fe2+氧化为Fe3+,用氢氧化钠溶液调节pH生成氢氧化铁沉淀,除去铁元素,滤渣的主要成分是氢氧化
铁,故C正确;沉淀表面有碘化铵,可向最后一次洗涤液中加硝酸和硝酸银溶液,若没有淡黄色沉淀生
成,说明不含碘离子,沉淀已经洗涤干净,故D错误。
6.解析:矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中加入活性氧化镁调节溶液pH,过滤,得到
的滤液1中的溶质主要是硝酸镁,结晶纯化得到硝酸镁晶体,再热解得到氧化镁和硝酸;滤泥中加入
氨性溶液氨浸,过滤,将得到的滤液2进行镍钴分离,经过一系列操作得到氯化铬和饱和氯化镍溶液,
向饱和氯化镍溶液中加入氯化氢气体得到氯化镍晶体。(1)活性MgO可与水反应,化学方程式为MgO
+HO===Mg(OH) 。(2)常温下,pH=9.9的氨性溶液中,lg K (NH·HO)=-4.7,K (NH·HO)=10-4.7
2 2 b 3 2 b 3 2
=,===10-0.6<1,则c(NH·HO)>c(NH)。(3)“氨浸”时,Co(OH) 与亚硫酸根离子发生氧化还原反
3 2 3
应,再与氨水反应生成[Co(NH )]2+,则由Co(OH) 转化为[Co(NH )]2+的离子方程式为2Co(OH) +
3 6 3 3 6 3
12NH ·HO+SO===2[Co(NH )]2++SO+13HO+4OH-或 2Co(OH) +8NH ·HO+4NH+
3 2 3 6 2 3 3 2SO===2[Co(NH )]2++SO+13HO。(4)“析晶”过程中为了防止Ni2+水解,因此通入的酸性气体A为
3 6 2
HCl。(5)①“结晶纯化”过程中,没有引入新物质。晶体 A 含 6 个结晶水,则晶体 A 为
Mg(NO )·6HO,根据Mg(NO )+2HO===Mg(OH) ↓+2HNO ,Mg(OH) =====MgO+HO,还剩余
3 2 2 3 2 2 2 3 2 2
5个水分子,因此所得HNO 溶液中n(HNO )与n(H O)的比值理论上最高为2∶5。②“热解”得到
3 3 2
HNO 和MgO,结合工艺流程可知,其意义在于可重复利用HNO 和MgO。
3 3
答案:(1)MgO+HO===Mg(OH) (2)>
2 2
(3)2Co(OH) +12NH ·HO+SO===2[Co(NH )]2++SO+13HO+4OH-(或 2Co(OH) +
3 3 2 3 6 2 3
8NH ·HO+4NH+SO===2[Co(NH )]2++SO+13HO) (4)HCl
3 2 3 6 2
(5)①0.4(或2∶5) ②MgO
7.解析:向电解金属锰的阳极渣(主要成分为MnO ,杂质为PbCO 、FeO、CuO)和黄铁矿(FeS )
2 3 2 3 2
中加入硫酸,MnO 将FeS 氧化生成S,PbCO 转化成PbSO 沉淀,氧化铁、氧化铜转化成硫酸铁、硫
2 2 3 4
酸铜,滤液中含有Fe3+、Fe2+、Mn2+、Cu2+等,加入HO 溶液将Fe2+氧化为Fe3+,再加入CaO或
2 2
CaCO 调节pH除去Fe3+、Cu2+,之后滤液中主要含有Ca2+、Mn2+,加入MnF 除去Ca2+,最终得到
3 2
MnSO 溶液,经过一系列操作得到Mn O。(1)由分析可知,“酸浸”过程中,滤渣Ⅰ的主要成分为S、
4 3 4
PbSO 。(2)由题图1可知,80 min时,Mn的浸出率高,Fe3+的质量浓度大,说明20~80 min MnO 与
4 2
FeS 反应生成Mn2+、Fe3+、S等,对应的离子方程式为3MnO +2FeS +12H+===3Mn2++4S+2Fe3+
2 2 2
+6HO;80~100 min时,剩余MnO 较少,FeS 浸出的Fe2+与MnO 接触机会减少,所以Fe2+的质量
2 2 2 2
浓度上升。(3)由分析可知,滤液中含有Fe3+、Fe2+、Mn2+、Cu2+等,加入HO 溶液将Fe2+氧化为Fe3+,
2 2
再加入CaO或CaCO 调节pH除去Fe3+、Cu2+,故选B。(4)由题图2可知,温度高于40 ℃时
3
MnSO ·HO的溶解度减小,故由MnSO 溶液获得MnSO ·HO晶体的系列操作为蒸发浓缩、结晶、趁
4 2 4 4 2
热过滤、洗涤、干燥。(5)根据Mn守恒可知,3MnSO ·HO~Mn O,此时Mn O 的质量占原固体质量
4 2 3 4 3 4
的×100%≈45.17%,失重1-45.17%=54.83%,结合题图2可知,需控制温度在1 000~1 200 ℃。
答案:(1)PbSO (2)3MnO +2FeS +12H+===3Mn2++4S+2Fe3++6HO 剩余MnO 较少,
4 2 2 2 2
FeS 浸出的Fe2+与MnO 接触机会减少 (3)B (4)蒸发浓缩、结晶、趁热过滤 (5)1 000~1
2 2
200 ℃ (6)7小时之前Mn(OH) 被O 氧化生成水,溶液pH无明显变化;7小时之后Mn (OH) SO 被
2 2 2 2 4
O 氧化生成HSO ,溶液pH减小(或7小时之前发生反应6Mn(OH) +O=====2Mn O+6HO,溶液
2 2 4 2 2 3 4 2
pH无明显变化;7小时之后发生反应3Mn (OH) SO +O=====2Mn O+6H++3SO,溶液pH减小)
2 2 4 2 3 4
8.解析:(2)由于空气中含有二氧化碳,能被氢氧化钙溶液吸收,所以通入Ar气的作用是防止
Ca(OH) 遇到空气中的CO 转化为CaCO 。(3)在碱性溶液中,锌酸钾的溶解度大于锌酸钙的溶解度,
2 2 3
加入Ca(OH) 粉末,增大了Ca2+浓度,使锌酸钙溶解平衡向沉淀生成的方向移动;根据产品的化学式
2
Ca[Zn(OH) ]·2HO可判断流程中第二次加入ZnO粉末的目的是调整ZnO与Ca(OH) 的物质的量之
3 2 2 2
比为2∶1。(5)由于操作Ⅰ得到滤液,则其操作为过滤;由于产品含有结晶水,则干燥产品时必须在低
温减压条件下进行,防止高温下产物分解失去结晶水。
答案:(1)ZnO+2OH-+HO===[Zn(OH) ]2-
2 4
(2)防止Ca(OH) 遇到空气中的CO 转化为CaCO
2 2 3
(3)在碱性溶液中,锌酸钾的溶解度大于锌酸钙的溶解度,加入Ca(OH) 粉末,增大了Ca2+浓度,
2
使锌酸钙溶解平衡向沉淀生成的方向移动 调整ZnO与Ca(OH) 的物质的量之比为2∶1
2
(4)使ZnO固体与KOH溶液充分混合,反应完全,提高产率
(5)过滤 防止高温下产物分解失去结晶水9.解析:(5)由滴定原理,根据得失电子守恒,(VO)SO 和KMnO 得电子总数等于(NH)Fe(SO )
2 2 4 4 4 2 4 2
失电子总数,结合VO→VO2+得1e-,MnO→Mn2+得5e-,Fe2+→Fe3+失1e-,可得n[(NH)Fe(SO )]
4 2 4 2
=2n[(VO)SO ]+5n(KMnO )。n[(VO)SO ]=(c mol·L-1×b×10-3 L-c mol ·L-1×b×10-3 L×5)=
2 2 4 4 2 2 4 1 1 2 2
mol,根据V元素守恒可得VO~(VO)SO ,则样品中五氧化二钒的纯度为×100%=×100%。
2 5 2 2 4
答案:(1)增大反应物接触面积,加快酸浸速率,使酸浸更加充分 (2)Ca(VO )+4H+===Ca2++
3 2
2VO+2HO (3)NH水解程度增大,NH浓度减小导致沉钒率下降 (4)V O+HCO+4H+===2VO2
2 2 5 2 2 4
++2CO ↑+3HO (5)×100%
2 2