文档内容
课时检测(十二) 化学计算的重要方法及类型
1.28 g铁粉溶于稀盐酸中,然后加入足量的Na O 固体,充分反应后过滤,将滤渣加强热,最终
2 2
得到的固体质量为( )
A.36 g B.40 g C.80 g D.160 g
2.向一定量的Fe、FeO、FeO、FeO 的混合物中加入150 mL 4 mol·L-1的稀硝酸,恰好使混合物
2 3 3 4
完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的H 在
2
加热条件下还原相同质量的混合物,所得铁的物质的量为( )
A.0.25 mol B.0.2 mol
C.0.3 mol D.0.35 mol
3.为了避免 NO、NO 、NO 对大气的污染,常采用 NaOH 溶液进行吸收处理:2NO +
2 2 4 2
2NaOH===NaNO +NaNO +HO;NO +NO+2NaOH===2NaNO +HO。现有由a mol NO、b mol
3 2 2 2 2 2
NO 、c mol NO 组成的混合气体恰好被V L NaOH溶液吸收(无气体剩余),则此NaOH溶液的物质的
2 2 4
量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
4.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生
素”。经热重分析测得NH VO 在焙烧过程中,固体残留率随温度变化的曲线如图所示。则NH VO 在
4 3 4 3
分解过程中( )
INCLUDEPICTURE "25YLCXHXⅡ2-37.TIF" \* MERGEFORMAT
A.先分解失去HO,再分解失去NH
2 3
B.先分解失去NH ,再分解失去HO
3 2
C.同时分解失去HO和NH
2 3
D.同时分解失去H、N 和HO
2 2 2
5.用足量的CO还原13.7 g某铅氧化物,把生成的CO 全部通入过量的澄清石灰水中,得到的沉
2
淀干燥后质量为8.0 g,则此铅氧化物的化学式为( )
A.PbO B.Pb O C.Pb O D.PbO
2 3 3 4 2
6.在氧气中燃烧0.22 g硫和铁组成的混合物,使其中的硫全部转化为二氧化硫,把这些二氧化硫
全部氧化成三氧化硫并转变为硫酸,这些硫酸可用10 mL 0.5 mol·L-1的氢氧化钠溶液完全中和,则原
混合物中硫的质量分数为( )
A.72% B.40% C.36% D.18%
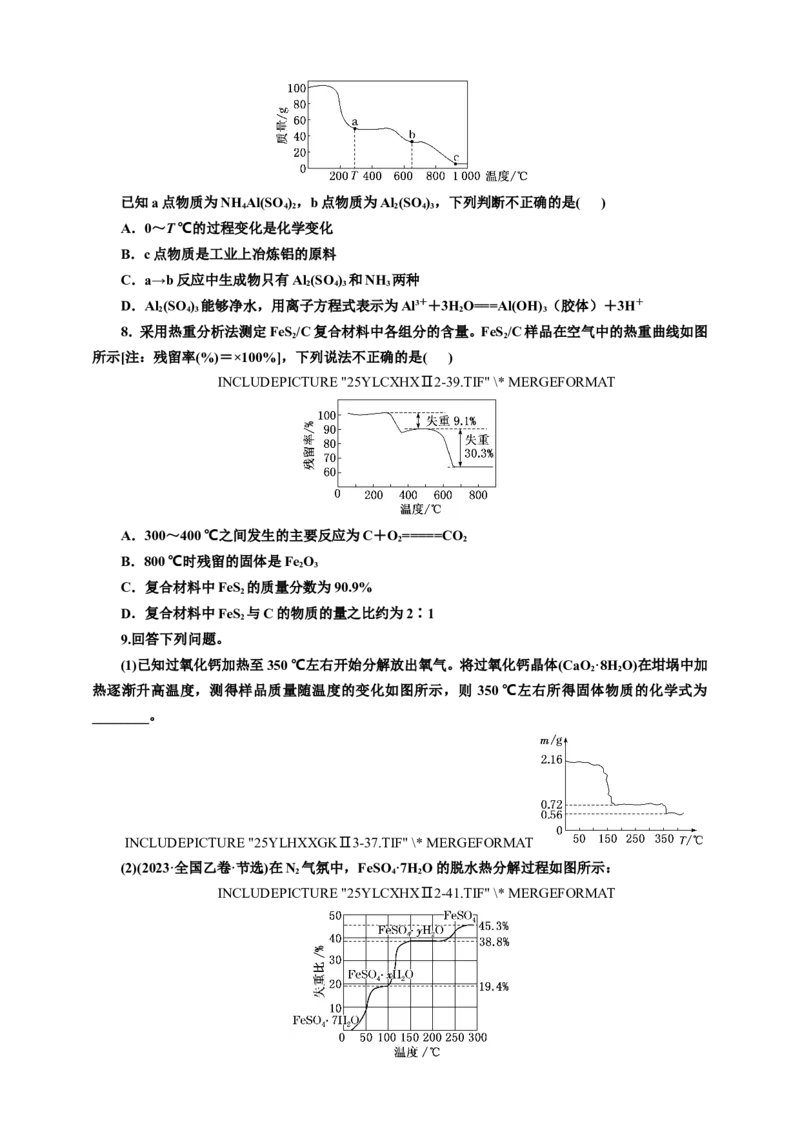
7.在加热固体NH Al(SO )·12HO时,固体质量随温度的变化曲线如图所示:
4 4 2 2
INCLUDEPICTURE "25YLCXHXⅡ2-38.TIF" \* MERGEFORMAT已知a点物质为NH Al(SO ),b点物质为Al (SO ),下列判断不正确的是( )
4 4 2 2 4 3
A.0~T ℃的过程变化是化学变化
B.c点物质是工业上冶炼铝的原料
C.a→b反应中生成物只有Al (SO ) 和NH 两种
2 4 3 3
D.Al (SO ) 能够净水,用离子方程式表示为Al3++3HO===Al(OH) (胶体)+3H+
2 4 3 2 3
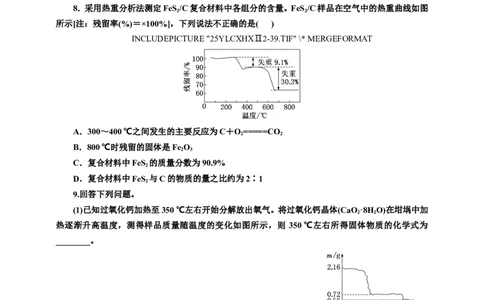
8.采用热重分析法测定FeS /C复合材料中各组分的含量。FeS /C样品在空气中的热重曲线如图
2 2
所示[注:残留率(%)=×100%],下列说法不正确的是( )
INCLUDEPICTURE "25YLCXHXⅡ2-39.TIF" \* MERGEFORMAT
A.300~400 ℃之间发生的主要反应为C+O=====CO
2 2
B.800 ℃时残留的固体是FeO
2 3
C.复合材料中FeS 的质量分数为90.9%
2
D.复合材料中FeS 与C的物质的量之比约为2∶1
2
9.回答下列问题。
(1)已知过氧化钙加热至350 ℃左右开始分解放出氧气。将过氧化钙晶体(CaO·8HO)在坩埚中加
2 2
热逐渐升高温度,测得样品质量随温度的变化如图所示,则 350 ℃左右所得固体物质的化学式为
________。
INCLUDEPICTURE "25YLHXXGKⅡ3-37.TIF" \* MERGEFORMAT
(2)(2023·全国乙卷·节选)在N 气氛中,FeSO·7HO的脱水热分解过程如图所示:
2 4 2
INCLUDEPICTURE "25YLCXHXⅡ2-41.TIF" \* MERGEFORMAT根据上述实验结果,可知x=______,y=_______。
(3)如图是1.00 g MgC O·nHO晶体在坩埚中从25 ℃缓缓加热至700 ℃分解时,所得固体产物的
2 4 2
质量(m)随温度(t)变化的关系曲线(已知100 ℃以上才会逐渐失去结晶水,并约在230 ℃时完全失去结
晶水):
INCLUDEPICTURE "25YLCXHXⅡ2-42.TIF" \* MERGEFORMAT
试回答下列问题:
①MgCO·nHO中n≈__________。
2 4 2
②C点固体物质的化学式为
________________________________________________________________________。
③E点到F点过程中发生反应的化学方程式为
________________________________________________________________________。
10.(2024·河南周口郸城一中期检)工业上利用锌焙砂(主要成分为ZnO,含有少量CuO、As O、
2 3
NiO等)生产高纯ZnO的流程示意图如下:
INCLUDEPICTURE "24HXSDKQMNJ-84.TIF" \* MERGEFORMAT
(1)用足量 SO 溶液和氨水“浸出”锌焙砂。
2 4
①“浸出”前,锌焙砂预先粉碎的目的是
________________________________________________________________________
________________________________________________________________________。
②通过“浸出”步骤,锌焙砂中的ZnO转化为2+,该反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(2)“除重金属”时,加入BaS溶液。滤渣Ⅱ中含有的主要物质是____________和BaSO 。
4
(3)“蒸氨”时会出现白色固体ZnSO ·Zn,运用平衡移动原理解释原因:
4 2
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)“沉锌”步骤①中加入足量NH HCO 溶液将白色固体转化为ZnCO 的离子方程式
4 3 3为______________________________________________________________________
________________________________________________________________________。
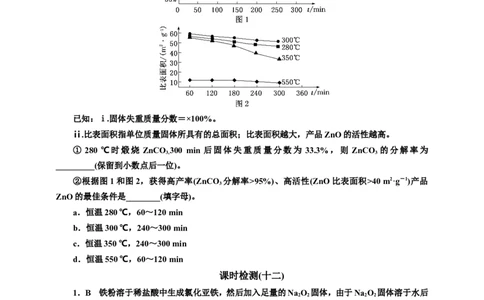
(5)“煅烧”步骤中,不同温度下,ZnCO 分解的失重曲线和产品ZnO的比表面积变化情况如图
3
1、图2所示:
INCLUDEPICTURE "24HXSDKQMNJ-85.TIF" \* MERGEFORMAT
已知:ⅰ.固体失重质量分数=×100%。
ⅱ.比表面积指单位质量固体所具有的总面积;比表面积越大,产品ZnO的活性越高。
① 280 ℃时煅烧 ZnCO 300 min 后固体失重质量分数为 33.3%,则 ZnCO 的分解率为
3, 3
_________(保留到小数点后一位)。
②根据图1和图2,获得高产率(ZnCO 分解率>95%)、高活性(ZnO比表面积>40 m2·g-1)产品
3
ZnO的最佳条件是________(填字母)。
a.恒温280 ℃,60~120 min
b.恒温300 ℃,240~300 min
c.恒温350 ℃,240~300 min
d.恒温550 ℃,60~120 min
课时检测(十二)
1.B 铁粉溶于稀盐酸中生成氯化亚铁,然后加入足量的Na O 固体,由于Na O 固体溶于水后
2 2 2 2
生成氢氧化钠和氧气,充分反应后生成氢氧化铁沉淀,过滤,将滤渣加强热,最终得到的固体为FeO,
2 3
根据铁原子守恒,n(Fe O)=n(Fe)=×=0.25 mol,则m(Fe O)=0.25 mol×160 g·mol-1=40 g。
2 3 2 3
2.A 由题意可知,混合物中的Fe元素全部转化为Fe(NO),根据N元素守恒,n[Fe(NO )]=
3 2 3 2
[n(HNO )-n(NO)]=×(0.15 L×4 mol·L-1-)=0.25 mol,则n(Fe)=0.25 mol,所以用足量的H 在加热
3 2
条件下还原相同质量的混合物,所得铁的物质的量为0.25 mol。
3.B 根据N元素守恒,可知反应后得到的NaNO 和NaNO 的物质的量之和为(a+b+2c)mol;
2 3
再根据Na元素守恒,可知参加反应的NaOH为(a+b+2c)mol,故c(NaOH)= mol·L-1。
4.B NH VO 的摩尔质量为117 g·mol-1,设NH VO 的物质的量为1 mol,则210 ℃时失重的质
4 3 4 3
量为1 mol×117 g·mol-1×(1-85.47%)≈17 g,NH 的摩尔质量为17 g·mol-1,所以先分解失去NH ,化
3 3
学方程式为NH VO=====HVO +NH ↑;380 ℃时失重的质量为1 mol×117 g·mol-1×(1-77.78%)≈26
4 3 3 3g,在第一次失重的基础上,第二次又失去的质量为26 g-17 g=9 g,HO的摩尔质量为18 g·mol-1,所
2
以再分解失去0.5 mol H O,化学方程式为2HVO =====VO+HO↑;故选B。
2 3 2 5 2
5.C 得到的沉淀为CaCO ,根据碳原子守恒,n(CO)=n(CO)=n(CaCO )==0.08 mol;CO与
3 2 3
铅的氧化物反应生成Pb和CO 1个CO变为1个CO 增加了1个氧原子,该氧原子来自铅的氧化物,
2, 2
故该铅氧化物中n(O)=n(CO)=0.08 mol,m(O)=1.28 g,m(Pb)=13.7 g-1.28 g=12.42 g,n(Pb)==
0.06 mol,n(Pb)∶n(O)=0.06∶0.08=3∶4,则此铅氧化物的化学式为Pb O。
3 4
6.C 根据S元素守恒和有关反应,有
S~HSO ~2NaOH
2 4
1 2
n(S) (0.5×10×10-3)mol
n(S)=n(NaOH)=×(0.5×10×10-3)mol=2.5×10-3 mol,m(S)=32 g·mol-1×2.5×10-3 mol=0.08 g,原混
合物中ω(S)=×100%≈36%。
7.C a 点物质为 NH Al(SO ) ,则 0~T ℃的过程为 NH Al(SO )·12H O 失去结晶水生成
4 4 2 4 4 2
NH Al(SO ),是化学变化,A项正确;b点物质为Al (SO ),加热会继续分解生成Al O,Al O 是工业
4 4 2 2 4 3 2 3 2 3
上冶炼铝的原料,B项正确;a→b发生的反应为硫酸铝铵分解生成硫酸铝、氨气和硫酸,C项错误;硫
酸铝能够净水,其原理是铝离子水解生成氢氧化铝胶体,离子方程式为Al3++3HO===Al(OH) (胶体)
2 3
+3H+,D项正确。
8.D 300~400 ℃之间发生的主要反应为C+O=====CO ,A正确;550~700 ℃之间发生反应
2 2
的化学方程式为4FeS +11O=====2FeO+8SO ,故800 ℃时残留的固体是FeO,B正确;由题图可
2 2 2 3 2 2 3
知,复合材料中碳完全反应时失重9.1%,则碳的质量分数为9.1%,FeS 的质量分数为90.9%,C正确;
2
FeS 与C的物质的量之比为∶≈1∶1,D错误。
2
9.解析:(1)由题图可知,起始时CaO ·8HO的质量为2.16 g,为0.01 mol,350 ℃左右所得固体质
2 2
量为0.56 g,根据钙原子守恒,可知该固体物质的化学式为CaO。(2)由题图可知,FeSO·7HO→FeSO
4 2 4
即7个结晶水完全失去时失重比为45.3%,则失重比为19.4%时,失去的结晶水数目为≈3,故x=7-
3=4,同理可推出y=7-≈1。(3)①B→D为MgCO·nHO晶体受热分解失去全部结晶水,
2 4 2
MgCO·nHO=====MgCO+nHO↑
2 4 2 2 4 2
112+18n 18n
1.00 g (1.00-0.76)g
=,解得n≈2。②B→C为MgCO·2HO晶体受热分解失去部分结晶水,设C点固体物质化学式
2 4 2
中结晶水的系数为x,
MgCO·2HO=====MgCO·xHO+(2-x)H O↑
2 4 2 2 4 2 2
148 18(2-x)
1.00 g (1.00-0.88)g
=,解得x≈1,故C点固体物质的化学式为 MgCO·HO。③E点固体物质与D点相同,为
2 4 2
MgCO,MgCO 受热分解,设最终残留固体为X,根据Mg元素守恒,n(MgCO)∶n(X)=∶=1∶1,
2 4 2 4 2 4
解得M(X)≈40 g·mol-1,则X为MgO,根据原子守恒和得失电子守恒,草酸镁中C元素化合价为+3
价,逸散气体不只有 CO ,应该还有 CO,所以 E 点到 F 点过程中发生反应的化学方程式为
2
MgCO=====MgO+CO↑+CO ↑。
2 4 2
答案:(1)CaO (2)4 1 (3)①2②MgCO·HO
2 4 2
③MgCO=====MgO+CO↑+CO ↑
2 4 2
10.解析:用足量硫酸铵溶液和氨水“浸出”锌焙砂(主要成分为ZnO,含有少量CuO、As O、
2 3
NiO等),加入(NH)SO 溶液、氧化钙、硫酸亚铁“除砷”得到滤渣Ⅰ(FeAsO 、氢氧化亚铁、氢氧化铁
4 2 2 8 4
等),过滤,向滤液中加入BaS溶液除铜离子,过滤,加入锌粉“深度除重金属”,过滤,“蒸氨”得到
白色固体ZnSO ·Zn ,加入碳酸氢铵溶液、通二氧化碳得到碳酸锌,“烘干煅烧”得到氧化锌。
4 2
(1)①“浸出”前,锌焙砂预先粉碎的目的是增大接触面积,提高反应速率,提高浸出率。②通过“浸
出”步骤,锌焙砂中的ZnO在氨水和铵根离子作用下生成2+和水,该反应的离子方程式为ZnO+
2NH ·HO+2NH===2++3HO。(2)根据前后除杂分析“除重金属”时,加入BaS溶液是除掉铜离子,
3 2 2
故滤渣Ⅱ中含有的主要物质是CuS和BaSO 。(5)①“烘干燃烧”时发生反应:ZnCO =====ZnO+
4 3
CO ↑,设起始ZnCO 为1 mol,分解率为x,则剩余固体为(1-x)mol ZnCO 和x mol ZnO,由固体失
2 3 3
重质量分数可得=33.3%,解得x≈94.6%。②ZnCO 分解率>95%,则固体失重质量分数=×100%=
3
33.44%,由题图1和2可知,获得高产率、高活性产品ZnO的最佳条件是恒温300 ℃,240~300 min。
答案:(1)①提高浸出效率 ②ZnO+2NH ·HO+2NH===2++3HO (2)CuS
3 2 2
(3)“蒸氨”过程中将NH 蒸出后,溶液中NH 的浓度降低,平衡2+⥫⥬ Zn2++4NH ↑正向移动,2+转化
3 3 3
为Zn2+,溶液中Zn2+浓度增大,发生反应:2Zn2++2OH-+SO===ZnSO ·Zn(OH) ↓,得到白色固体
4 2
(4)ZnSO ·Zn(OH) +2HCO===2ZnCO +SO+2HO (5)①94.6% ②b
4 2 3 2