文档内容
物质的量&物质的分类作业题
作业题目难度分为3档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目1-12,16-19题为三星,13—15,20-31为四星。
1.下列数量的各物质所含原子个数由大到小顺序排列的是( ) ☆☆☆
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠
A.④③②① B.①④③② C.②③④① D.①④②③
【解答】
①氨气分子含有 4 个原子,原子的物质的量为氨气的 4 倍,0.5mol 氨气含有原
子的物质的量为0.5mol×4=2mol;
②氦气的物质的量为 =1mol,氦气是单原子分子,故氦原子的物质的量为
1mol;
③水的质量为 9mL×1g/mL=9g,故水的物质的量为 =0.5mol,原子物质
的量为水的3倍,故含有原子的物质的量为0.5mol×3=1.5mol;
④磷酸分子含有 8 个原子,原子的物质的量为磷酸的 8 倍,0.2mol 磷酸含有原
子的物质的量为0.2mol×8=1.6mol;
故含有原子数目由大到小顺序排列为:①④③②
故选B.
2.等物质的量的 SO 和 SO 相比较,下列结论错误的是( ) ☆☆☆
2 3
A.它们的分子数目之比是 1:1 B.它们的氧原子数目之比为 2:3
C.它们的质量之比为 1:1 D.它们所含原子数目之比为 3:4
第1页(共18页)【解答】
A、等物质的量的SO 和SO 分子数目之比等于物质的量之比=1:1,故A正确;
2 3
B、等物质的量的 SO 和SO 分子数目之比等于物质的量之比=1:1,1个SO 分子
2 3 2
中含有2个氧原子,1个SO 分子中含有3个氧原子,则所含O原子数之比为(1
3
×2):(1×3)=2:3,故B正确;
C、等物质的量的 SO 和SO 质量之比等于物质的摩尔质量之比=64:80=4:5,故
2 3
C错误;
D、等物质的量的 SO 和SO 分子数目之比等于物质的量之比=1:1,1个SO 分子
2 3 2
中含有3个原子,1个SO 分子中含有4个原子,则原子总数之比为(1×3):(1
3
×4)=3:4,故D正确。
故选:C.
3.现有 HO、NH 、CH 三种物质,它们分别都含有 1mol 氢原子,则三种物质的
2 3 4
物质的量之比为( ) ☆☆☆
A.1:1:1 B.6:4:3 C.4:3:2 D.6:3:2
【解答】
根据1mol HO、NH、CH 三种分子中分别含有2mol、3mol、4mol氢原子来计算.
2 3 4
设三种物质的物质的量分别是 x、y、z,
分别都含有1mol氢原子,
则2x=3y=4z=1mol,所以x:y:z=6:4:3
故选B.
4.有 15g A 物质和 10.5g B 物质完全反应后,生成 7.2g C 物质,1.8g D 物质
和0.3mol E物质.则E的摩尔质量是( ) ☆☆☆
A.100g/mol B.111g/mol C.55g/mol D.27.5g/mol
【解答】
根 据 反 应 前 后 质 量 守 恒 得 , E 的 质 量 =15g+10.5g-7.2g-1.8g=16.5g ,
第2页(共18页)M= = =55g/mol
故选C.
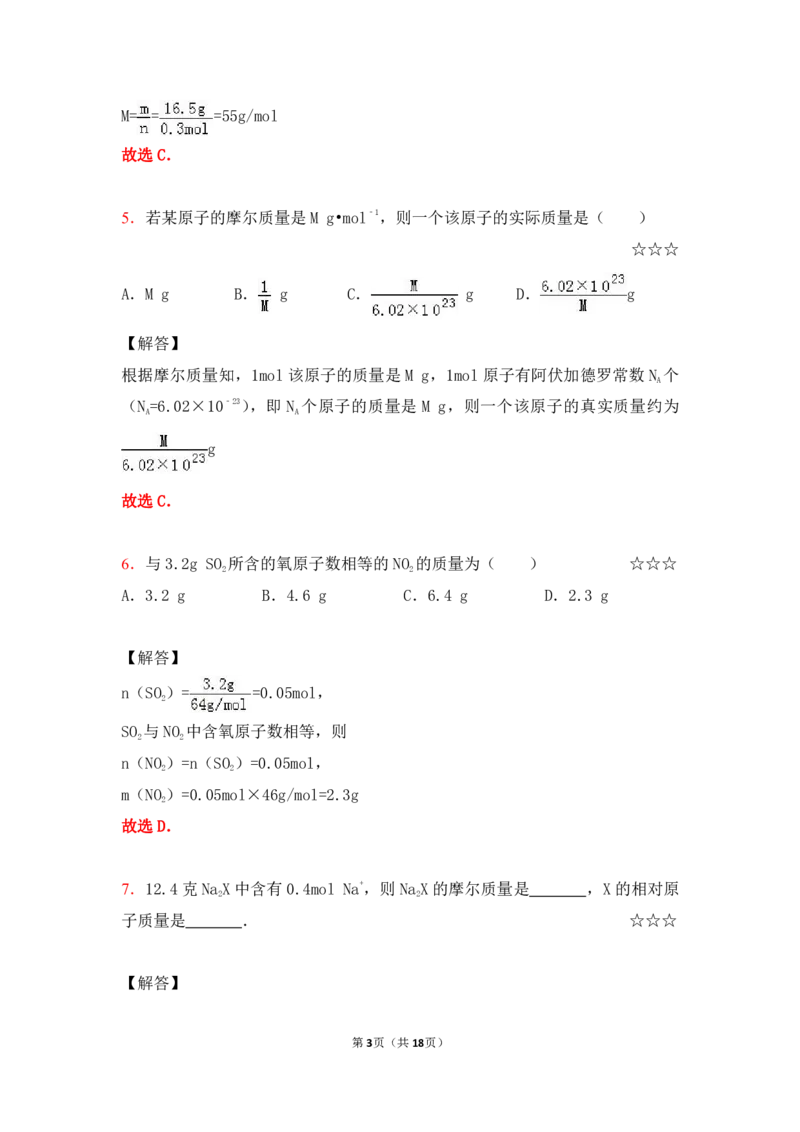
5.若某原子的摩尔质量是M g•mol﹣1,则一个该原子的实际质量是( )
☆☆☆
A.M g B. g C. g D. g
【解答】
根据摩尔质量知,1mol 该原子的质量是 M g,1mol 原子有阿伏加德罗常数 N 个
A
(N=6.02×10﹣23),即 N 个原子的质量是 M g,则一个该原子的真实质量约为
A A
g
故选C.
6.与3.2g SO 所含的氧原子数相等的 NO 的质量为( ) ☆☆☆
2 2
A.3.2 g B.4.6 g C.6.4 g D.2.3 g
【解答】
n(SO)= =0.05mol,
2
SO 与NO 中含氧原子数相等,则
2 2
n(NO)=n(SO)=0.05mol,
2 2
m(NO)=0.05mol×46g/mol=2.3g
2
故选D.
7.12.4 克NaX 中含有0.4mol Na+,则 NaX 的摩尔质量是 ,X 的相对原
2 2
子质量是 . ☆☆☆
【解答】
第3页(共18页)12.4克NaX中含有0.4molNa+,NaX的物质的量为:n(NaX)= n(Na+)=0.4mol
2 2 2
× =0.2mol,
NaX的摩尔质量为:M(NaX)= =62g/mol,即NaX的相对原子量为62,
2 2 2
X的相对原子质量为:62﹣23×2=16。
故答案为:62g/mol;16.
8.下列说法正确的是( ) ☆☆☆
A.标准状况下,1mol任何物质的体积约是22.4L
B.1mol任何气体的体积都约是22.4L
C.1mol He和1mol O 的体积相同
2
D.标准状况下,1mol O 和N 的混合气体的体积约是22.4L
2 2
【解答】
A、标准状况下,1mol 气体的体积约是 22.4L,选项中物质不一定是气体,故 A
错误;
B、标准状况下,1mol 任何气体的体积约是 22.4L,气体所处的状态不一定是标
准状况,其体积与温度、压强有关,故B错误;
C、1molHe和1molO 所处的状态不一定相同,体积不一定相等,其体积与温度、
2
压强有关,故C错误;
D、标准状况下,气体摩尔体积为 22.4L/mol,所以标准状况下,1mol O 和N 的
2 2
混合气体的体积约是22.4L,故D正确。
故选D.
9.下列关于气体摩尔体积的几种说法正确的是( ) ☆☆☆
A.22.4L任何气体的物质的量均为1mol
B.非标准状况下,1mol任何气体不可能占有22.4L体积
C.0.4mol H 、0.2mol O 、和 0.4mol CO 组成的混合气体,在标准状况下约为
2 2 2
22.4L
第4页(共18页)D.同温、同压下,相同质量的 CO和CO 具有相同的体积
2
【解答】
A、气体的物质的量 n= ,故 22.4L 气体的物质的量与气体所处的状态的气体
摩尔体积的数值有关,故不一定为1mol,故A错误;
B、在标况下,气体摩尔体积为 22.4L/mol,而当气体摩尔体积为22.4L/mol时,
不一定为标况下,故在非标况下,1mol气体的体积也可能为22.4L,故B错误;
C、在标况下,1mol任何气体的体积均为22.4L,故0.4molH、0.2molO 和0.4mol
2 2
CO 组成的混合气体即1mol混合气体,在标况下体积约为 22.4L,故C正确;
2
D、CO 和二氧化碳的摩尔质量不同,故等质量的 CO 和二氧化碳的物质的量之比
为44:28=11:7,则在同温同压下的体积之比为11:7,故D错误。
故选C.
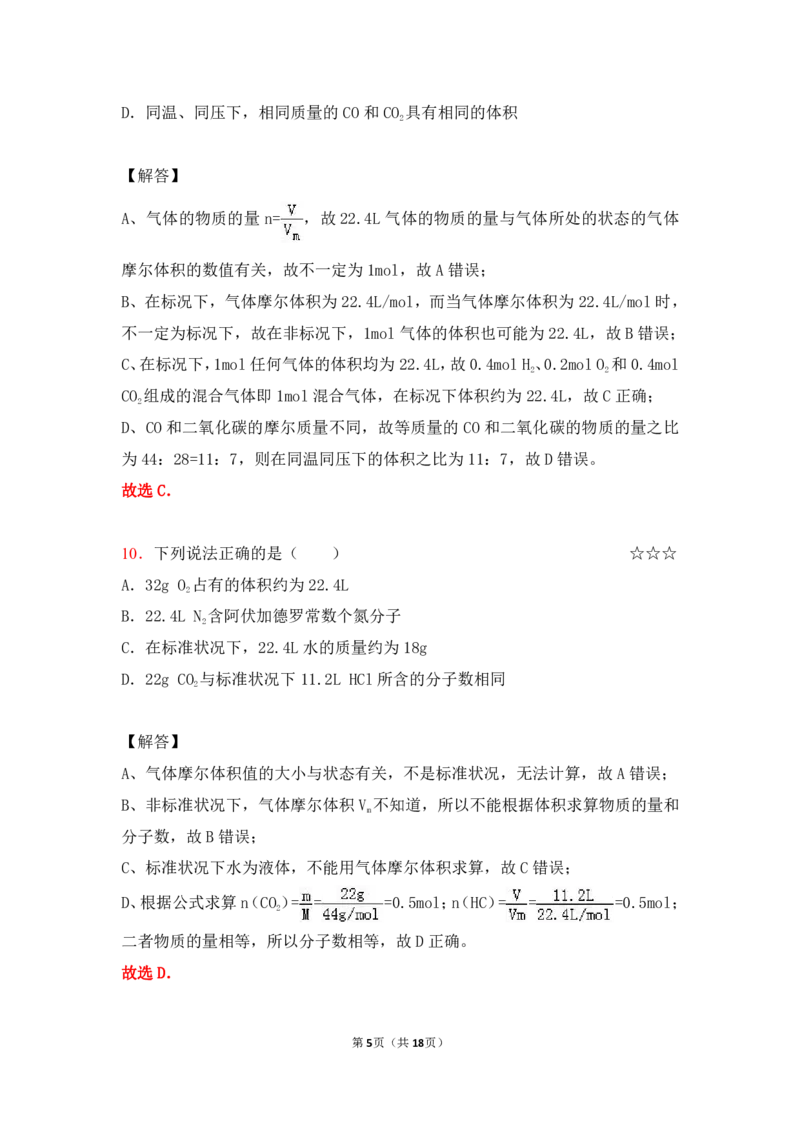
10.下列说法正确的是( ) ☆☆☆
A.32g O 占有的体积约为22.4L
2
B.22.4L N 含阿伏加德罗常数个氮分子
2
C.在标准状况下,22.4L水的质量约为18g
D.22g CO 与标准状况下11.2L HCl所含的分子数相同
2
【解答】
A、气体摩尔体积值的大小与状态有关,不是标准状况,无法计算,故 A错误;
B、非标准状况下,气体摩尔体积V 不知道,所以不能根据体积求算物质的量和
m
分子数,故B错误;
C、标准状况下水为液体,不能用气体摩尔体积求算,故 C错误;
D、根据公式求算 n(CO)= = =0.5mol;n(HC)= = =0.5mol;
2
二者物质的量相等,所以分子数相等,故D正确。
故选D.
第5页(共18页)11.已知 m mol 某气体的质量为 a g,则 b g 该气体在标准状况下的体积(L)
为( ) ☆☆☆
A. B. C. D.
【解答】
m mol某气体的质量为a g,
所以该气体的摩尔质量为M= = g/mol,
则b g该气体的物质的量为n= = mol,
所以标准状况下,b g该气体的体积为 mol×22.4L/mol= L
故选C.
12.1g N 所占有的体积为V L,则 N 的摩尔体积为( ) ☆☆☆
2 2
A.28V L/mol B.22.4 L/mol C.(28/V)L/mol D.(V/28)L/mol
【解答】
1g氮气的物质的量为 = mol,氮气的摩尔体积V= = =28VL/mol
m
故选A.
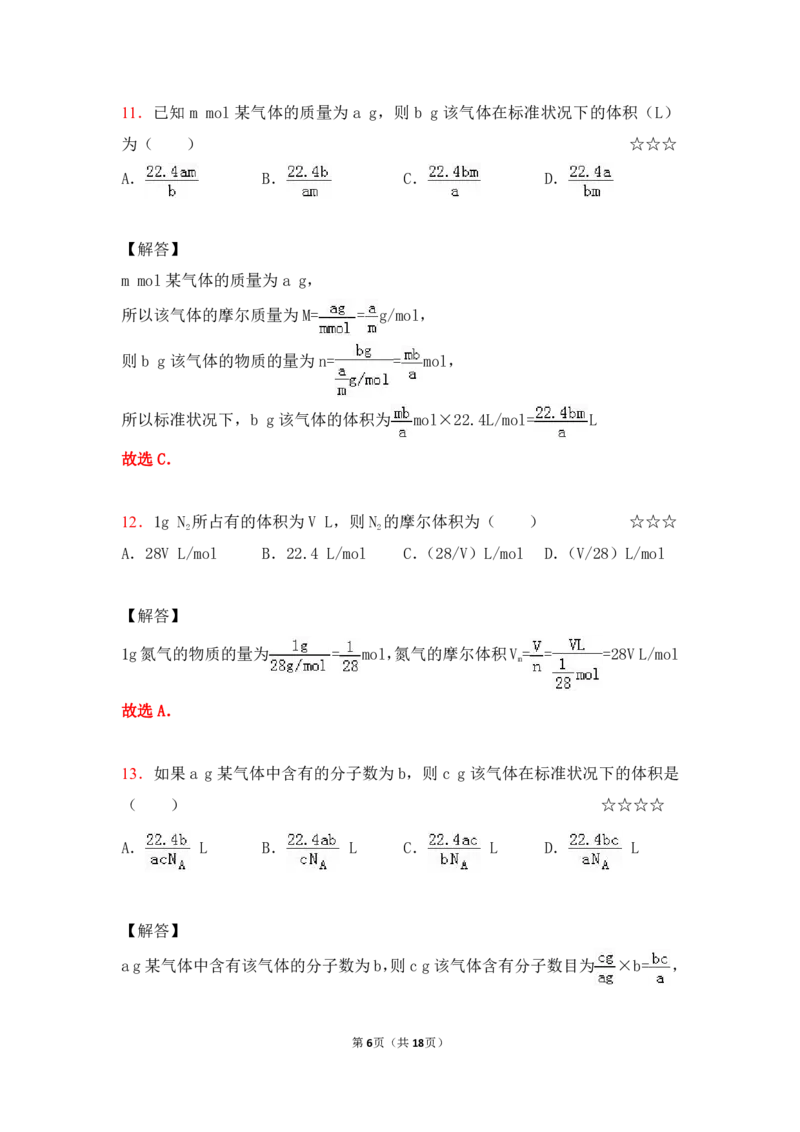
13.如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是
( ) ☆☆☆☆
A. L B. L C. L D. L
【解答】
ag某气体中含有该气体的分子数为b,则cg该气体含有分子数目为 ×b= ,
第6页(共18页)则 c g 该气体的物质的量为 = mol,标况下,c g 该气体的体积为
mol×22.4L/mol= L
故选D.
14.已知 a g 气体 X 中含有 b 个 X 原子,那么 c g 该气体在 0℃、1.01×105Pa
2
条件下的体积是(N 表示阿伏加德罗常数的值)( ) ☆☆☆☆
A
A. L B. L C. L D. L
【解答】
a g气体X 中含有b个X原子,气体摩尔质量设为 M,则 ×2= mol,
2
M= g/mol;
0 ℃ 、 1.01 × 105Pa 条 件 是 标 准 状 况 , c g 该 气 体 的 体 积
= = L= L
故选A.
15.标准状况下有①6.72L CH②3.01×1023个HCl③13.6g HS④0.2mol NH,下
4 2 3
列对四种气体的关系从小到大表示不正确的是( ) ☆☆☆☆
A.体积④<①<③<② B.密度①<④<③<②
C.质量④<①<③<② D.氢原子数④<②<③<①
【解答】
A、3.01×1023个 HCl 的体积 V= Vm=0.5mol×22.4L/mol=11.2L,13.6g HS 的
2
第7页(共18页)体积 V= Vm= ×22.4L/mol=8.96L,0.2mol NH 的体积 V=0.2mol×
3
22.4L/mol═4.48L,所以体积关系为:④<①<③<②,故A正确;
B、根据阿伏伽德罗定律的推论:同温同压下,密度之比等于相对分子质量之比,
所以密度关系为:①<④<③<②,故B正确;
C、6.72L CH 的质量是 m= M= ×16g/mol=4.8g,3.01×1023个 HCl
4
的 质 量 为 0.5mol × 36.5g/mol=18.25g , 0.2mol NH 的 质 量 是 0.2mol ×
3
17g/mol=3.4g,所以质量关系是④<①<③<②,故C正确;
D、6.72L CH 的物质的量为0.3mol,所以氢原子的物质的量为1.2mol,
4
3.01×1023个HCl的物质的量为 0.5mol,所以氢原子的物质的量为0.5mol,
13.6g H S的物质的量为0.4mol,所以氢原子的物质的量为0.8mol,0.2mol NH
2 3
氢原子的物质的量为 0.6mol,氢原子数目和氢原子的物质的量成正比,所以氢
原子数关系是②<④<③<①,故D错误。
故选D.
16.下列溶液中Cl﹣的物质的量浓度最大的是( ) ☆☆☆
A.200mL 2mol/L MgCl 溶液 B.1000mL 2.5mol/L NaCl溶液
2
C.250mL 1mol/L AlCl 溶液 D.300mL 5mol/L KClO 溶液
3 3
【解答】
A、200mL 2mol•L﹣1MgCl 溶液中 c(Cl﹣)=2c(MgCl)=2mol/L×2=4mol/L;
2 2
B、1000mL 2.5mol•L﹣1NaCl溶液中c(Cl﹣)=c(NaCl)=2.5mol/L;
C、250mL 1mol•L﹣1AlCl 溶液中 c(Cl﹣)=3c(AlCl)=1mol/L×3=3mol/L;
3 3
D、氯酸钾中不含氯离子,所以氯离子的物质的量浓度是 0;
所以氯离子浓度最大的是4mol/L。
故选:A.
17.在2L 0.1mol•L﹣1 NaSO 溶液中,下列说法正确的是( ) ☆☆☆
2 4
A.Na+物质的量为0.2mol B.Na+物质的量浓度为0.2 mol•L﹣1
第8页(共18页)C.SO2﹣物质的量为0.1mol D.SO2﹣物质的量浓度为0.2 mol•L﹣1
4 4
【解答】
在2L 0.1mol•L﹣1 NaSO 溶液中溶质物质的量=2L×0.1mol•L﹣1=0.2mol,
2 4
含Na+物质的量为0.4mol,SO2﹣物质的量为0.2mol,
4
Na+物质的量浓度=0.1mol/L×2=0.2 mol•L﹣1,
SO2﹣物质的量浓度为0.1mol•L﹣1
4
故选B.
18.下列溶液中物质的量浓度肯定为1mol/L的是( ) ☆☆☆
A.将40g NaOH固体溶解于1L水中
B.将22.4L氯化氢气体溶于水配成1L溶液
C.将1L 10 mol/L浓盐酸与10L水混合
D.10g NaOH固体溶解在水中配成250mL溶液
【解答】
A、40gNaOH的物质的量为1mol,溶液的体积不等于溶剂的体积,溶液的体积不
是1L,因此溶液中物质的量浓度不是1mol/L,故A错误;
B、22.4L 氯化氢气体的物质的量不一定等于 1mol,因此溶液中物质的量浓度不
是1mol/L,故B错误;
C、混合溶液的体积不等于 10L,根据稀释定律可知混合液的物质的量浓度不是
1mol/L,故C错误;
D、10g NaOH 的物质的量为 0.25mol,溶液的体积为 0.25L,因此溶液中物质的
量浓度是1mol/L,故D正确。
故选D.
19.某盐的混合物溶液中含有 Na+、Mg2+、Cl﹣、SO2﹣4 种离子,其 3 种浓度分别
4
为0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Cl﹣,则c(SO2﹣)为( )
4
☆☆☆
第9页(共18页)A.0.1 mol/L B.0.2 mol/L C.0.3 mol/L D.0.4 mol/L
【解答】
溶液呈电中性,根据电荷守恒可知:c(Na+)+2c(Mg2+)=c(Cl﹣)+2c(SO2﹣),
4
即:0.2mol/L+2×0.4mol/L=0.4mol/L+2c(SO2﹣),
4
解得:c(SO2﹣)=0.3mol/L。
4
故选C.
20.将标准状况下的a L氨气溶于1000g水中,得到氨水的密度为b g•cm﹣3,则
该氨水的物质的量浓度为( ) ☆☆☆☆
A. mol/L B. mol/L
C. mol/L D. mol/L
【解答】
标况下 aL 氨气的物质的量为: = mol,氨气的质量为:17g/mol
× mol= g,该氨水的质量为:1000g+ g,该溶液的体积为:
V= = mL
则该氨水的物质的量浓度为:c= = mol/L
故选C.
21.设N 为阿伏伽德罗常数的值,下列说法正确的是( ) ☆☆☆☆
A
A.标准状况下,0.1mol Cl 溶于水,转移的电子数目为 0.1N
2 A
B.标准状况下,22.4L HO含有的分子数为N
2 A
C.1.8g DO含有的电子数为0.1N
2 A
D.常温常压下,1.06g NaCO 含有的 Na+数为0.02N
2 3 A
第10页(共18页)【解答】
A、Cl 溶于水形成盐酸与次氯酸属于可逆反应,则 0.1 moL Cl 溶于水转移的电
2 2
子数目小于0.1N,故A错误;
A
B、因标准状况下,水不是气体,不能按气体摩尔体积计算 22.4 L HO的物质的
2
量,则其分子数无法计算,故 B错误;
C、1mol重水含有10mol的电子,1.8gDO含有的电子数为 10N=0.9N,
2 A A
�రꀰ
故C错误; �Ͳꀰ݃�Ȁ��
D、1.06 g NaCO 的物质的量 0.01 mol,因NaCO 为强电解质,所以
2 3 2 3
�ͲͲꀰ
0.01 mol的NaCO 中含Na+数�为�2Ͳ×Ͳꀰ݃0�.Ȁ0�1�=0.02 N,故D正确;
2 3 A
故选:D.
22.设N 为阿伏加德罗常数的数值,下列说法正确的是( ) ☆☆☆☆
A
A.常温常压下,11.2L Cl 含氯原子数为 N
2 A
B.3.1g白磷(P)分子中含质子数为1.5N
4 A
C.1 mol NaO 与足量水反应转移电子数为 2N
2 2 A
D.1mol N 和3mol H 充分反应生成NH 分子数为2N
2 2 3 A
【解答】
A、常温常压下,不能使用气体摩尔体积计算氯气的物质的量,故 A错误;
B、3.1g白磷(P)分子的物质的量为 0.025mol,含有质子的物质的量
4
��ꀰ
为0.025mol×60=1.5mol,其数目为�1�.�5ꀰN݃�;Ȁ�故� B正确;
A
C、,根据关系式:NaO ~e﹣,1 mol NaO 与足量水反应转移电子数为 N ,故 C
2 2 2 2 A
错误;
D、合成氨是可逆反应,1mol N 和3mol H 充分反应生成NH 分子数小于2N,故
2 2 3 A
D错误;
故选:B.
23.设N 为阿伏加德罗常数,下列说法正确的是( ) ☆☆☆☆
A
第11页(共18页)A.标准状况下的0.1mol SO 的体积为 2.24L
3
B.1.8g水中含有的氢原子数为0.2N
A
C.1mol铁与硫反应转移电子数一定为3N
A
D.在0.1mol•L﹣1的硝酸钠溶液中含有的钠离子数为 0.1N
A
【解答】
A、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故 A
错误;
B、1.8g水的物质的量为0.1mol,而水中含2个H原子,故0.1mol水中含 0.2N
A
个H原子,故B正确;
C、铁和硫反应后变为+2价,1mol铁反应后转移2N 个电子,故C错误;
A
D、溶液体积不明确,故溶液中钠离子的个数无法计算,故 D错误。
故选:B.
24.设N 为阿伏加德罗常数,下列说法正确的是( ) ☆☆☆☆
A
A.1L 2mol•L﹣1的MgCl 溶液中含Mg2+数为2N
2 A
B.23g Na在氧气中完全燃烧失电子数为0.5N
A
C.标准状况下,11.2L SO 所含分子数为 0.5N
3 A
D.室温下,8g甲烷含有共价键数为2N
A
【解答】
A、镁离子在溶液中会水解,故溶液中镁离子的个数小于 2N 个,故A错误;
A
B、23g 钠的物质的量为 1mol,而钠反应后变为+1 价,故 1mol 钠反应后失去 N
A
个电子,故B错误;
C、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故 C
错误;
D、8g 甲烷的物质的量为 0.5mol,而甲烷中含 4条共价键,故 0.5mol 甲烷中含
共价键为2N 条,故D正确。
A
故选:D.
第12页(共18页)25.设N 为阿伏加德罗常数的数值,下列说法正确的是( ) ☆☆☆☆
A
A.50mL 12moI/L盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
B.2.8g乙烯与丙烯的混合物中含碳原子的数目为0.2N
A
C.1L 0.1moI/L的醋酸溶液中含有CHCOO﹣的数目0.1N
3 A
D.制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为N
A
【解答】
A、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故转移的电子数小于 0.3N
A
个,故A错误;
B、乙烯和丙烯的最简式均为 CH ,故 2.8g 混合物中含有的 CH2 的物质的量为
2
0.2mol,故含碳原子为0.2N 个,故 B正确;
A
C、醋酸是弱酸,不能完全电离,故溶液中醋酸根的个数小于 0.1N 个,故 C 错
A
误;
D、氯气和氢氧化钠反应时,1mol氯气生成1molNaClO,转移1mol电子,故 0.5mol
氯气转移0.5N 个电子,故D错误。
A
故选:B.
26.N 代表阿伏加德罗常数的值,下列说法错误的是( ) ☆☆☆☆
A
A.a g CHOH中所含碳氢键数目为
2 5
����
B.92.0 g乙醇与足量金属钠完全反�应Ͳ生成氢气的分子数为N
A
C.标准状况下,11.2 L乙醇中含氢原子数目为3N
A
D.相同物质的量的﹣OH和﹣CH 含有相同数目的电子
3
【解答】
A、根据 CHOH结构,1mol 该物质含有5mol 的C﹣H键,所以 ag CHOH中所含
2 5 2 5
碳氢键数目为 ,故A正确;
����
B、钠足量,乙醇�Ͳ的物质的量是2mol,产生1mol氢气,生成氢气的分子数为N ,
A
第13页(共18页)故B正确;
C、乙醇在标况下是非气态,不能使用22.4L/mol来计算,故C错误;
D、一个﹣OH 和﹣CH 都含有 9 个电子,所以相同的物质的量的两物质含有相同
3
数目的电子,故D正确;
故选:C.
27.用N 表示阿伏加德罗常数的数值,下列说法不正确的是( ) ☆☆☆☆
A
A.1mol分子式为CHO的物质,含O﹣H数目一定是N
2 6 A
B.标准状况下,22.4L CH=CH 中含C﹣H数目为4N
2 2 A
C.1mol甲基(﹣CH)中含有的电子数目为9N
3 A
D.0.1mol由乙烯与乙醇组成的混合物完全燃烧所消耗的氧气分子数目为 0.3N
A
【解答】
A、CHO可以为乙醇,还可能为二甲醚,故此物质中不一定含﹣OH,故A错误;
2 6
B、标况下22.4L乙烯的物质的量为1mol,而乙烯中含4条C﹣H键,故1mol 乙
烯中含4N 条C﹣H键,故B正确;
A
C、甲基中含9个电子,1mol甲基中含9N 个电子,故C正确;
A
D、1mol 乙烯和 1mol 乙醇燃烧均消耗 3mol 氧气,故 0.1mol 混合物燃烧消耗氧
气为0.3N 个,故D正确。
A
故选:A.
28.N 表示阿伏加德罗常数的值。下列说法正确的是( ) ☆☆☆☆
A
A.常温下,15 g甲醛中含有的共用电子对总数为2N
A
B.0.5 mol•L﹣1 CHCOONa溶液中含有CHCOO﹣的数目少于0.5N
3 3 A
C.16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1N
3 3 A
D.足量的锌与一定量的浓硫酸充分反应,放出2.24 L SO 和H 混合气体时,转
2 2
移电子数为0.2N
A
【解答】
第14页(共18页)A、15g甲醛的物质的量为0.5mol,而甲醛中含4对共用电子对,故0.5mol甲醛
中含共用电子对为2N 对,故A正确;
A
B、溶液体积不明确,故溶液中醋酸根的个数无法计算,故 B错误;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故所形成的氢氧化铁胶粒的个
数小于0.1N 个,故C错误;
A
D、气体所处的状态不明确,故其物质的量无法计算,则转移的电子数无法计算,
故D错误。
故选:A.
29.N 表示阿伏伽德罗常数,下列叙述正确的是( ) ☆☆☆☆
A
A.1mol FeI 与足量氯气反应时转移的电子数为 2N
2 A
B.室温下,1L pH=13的NaOH溶液中,由水电离的OH﹣数目为0.1N
A
C.标准状况下,2.24L N 和O 的混合气体中分子数为0.2N
2 2 A
D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6N
A
【解答】
A.氯气与FeI 的反应:2FeI+3Cl =2FeCl+2I,故1 mol FeI 与足量氯气反应
2 2 2 3 2 2
时转移的电子数为3N,故A错误;
A
B.室温下,1L pH=13的NaOH溶液中的氢离子为水电离的,氢离子浓度为
1×10﹣13mol/L,1L该溶液中含有1×10﹣13mol氢离子,水电离的氢氧根离子和氢
离子都是1×10﹣13mol,则水电离的OH﹣离子数目为1×10﹣13N,故B错误;
A
C.标况下 2.24L 混合气体的物质的量为 0.1mol,而分子数 N=nN =0.1N 个,
A A
故C错误;
D.丙烯和环丙烷的最简式均为CH,故42g混合物中含有的CH 的物质的量为3mol,
2 2
则含H原子个数为6N 个,故D正确。
A
故选:D.
30.设N 为阿伏加德罗常数的值,下列说法一定正确的是( ) ☆☆☆☆
A
A.0.1mol FeCl 形成的胶体粒子数为 0.1N
3 A
第15页(共18页)B.常温下,1L氢氧根离子浓度为0.01moI/L氨水中含有OH﹣的数目为0.01N
A
C.0.1mol O 完全反应时,转移的电子数为 0.4N
2 A
D.12g碳单质中所含的共价键数为2N
A
【解答】
A.一个胶粒是多个氢氧化铁的聚集体,故将 0.1 mol FeCl 水解制成胶体,所
3
得胶体粒子数小于0.1N,故A错误;
A
B.常温下,1L 氢氧根离子浓度为 0.01moI/L 氨水中含有 OH﹣的数目=1L×
0.01mol/L×N=0.01N,故B正确;
A A
C.氧气反应后的价态可能为﹣2价或﹣1价,则 0.1mol氧气反应电子转移数可
能为0.4N 或0.2N,故C错误;
A A
D.12g 碳的物质的量为 1mol,碳单质可能是金刚石、石墨、C 等单质,结构不
60
同含有的共价键数不同,故 D错误。
故选:B.
31.实验室需要 0.2 mol/L NaOH 溶液 450 mL 和 1 mol/L 硫酸溶液 500 mL.根
据这两种溶液的配制情况回答下列问题: ☆☆☆☆
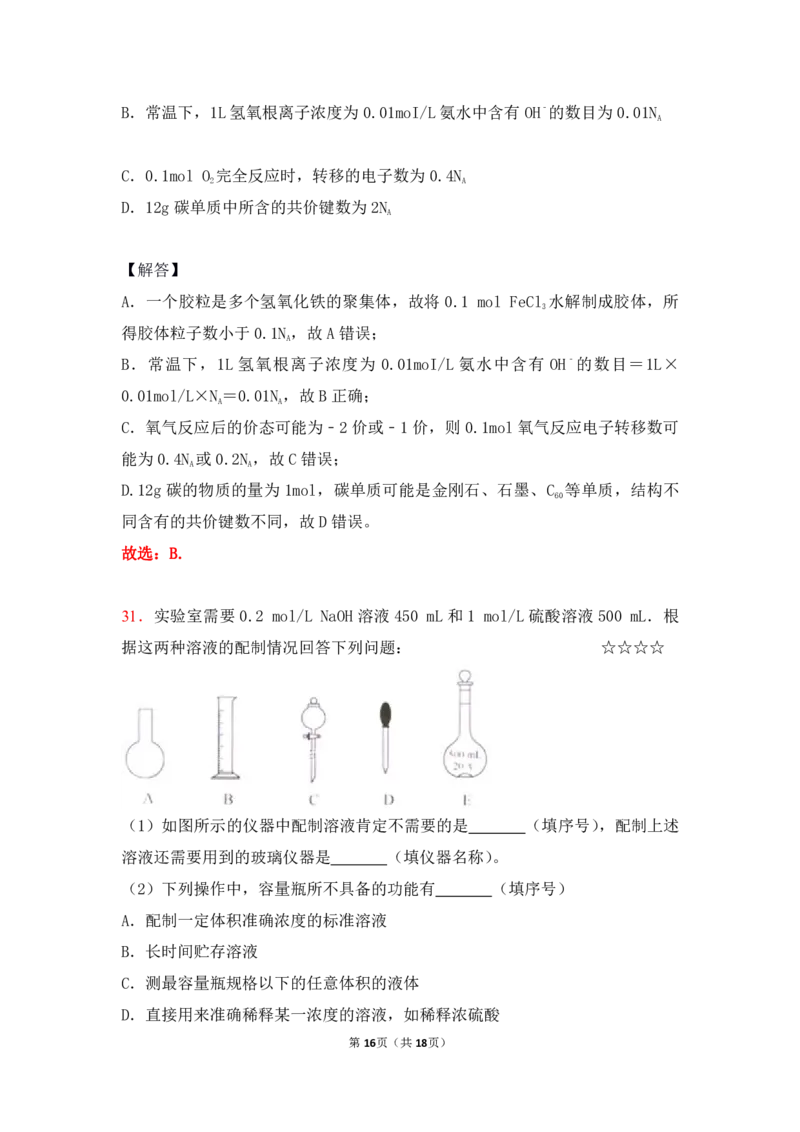
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述
溶液还需要用到的玻璃仪器是 (填仪器名称)。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)
A.配制一定体积准确浓度的标准溶液
B.长时间贮存溶液
C.测最容量瓶规格以下的任意体积的液体
D.直接用来准确稀释某一浓度的溶液,如稀释浓硫酸
第16页(共18页)F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取 NaOH的质量为 g.在实验中其他操作均正
确,若定容时仰视刻度线,则所得溶液浓度 0.2 mol/L(填“大于”“等
于”或“小于”,下同)。若 NaOH 溶液在转移至容量瓶时未经冷却,则所得溶液
浓度 0.2 mol/L。
(4)根据计算得知,所需质量分数为 98%、密度为 1.84 g/cm3的浓硫酸的体积
为 mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进
行稀释,稀释时操作方法是 。
(5)若配制某NaOH溶液,需称量溶质10.2 g,某同学称量时将砝码放往左盘,
装 NaOH 的烧杯放在了右盘,且称量时使用了游码,这会使所配溶液浓度
(填“偏大”“偏小”或“无影响”)。
【解答】
(1)配制一定物质的量浓度溶液一般步骤:计算、称量、稀释、冷却、移液、
洗涤、定容、摇匀等,用到的仪器:托盘天平(量筒)、烧杯、玻璃棒、500mL
容量瓶、胶头滴管,所以用不到的仪器:圆底烧瓶,分液漏斗,还缺少的玻璃仪
器:烧杯、玻璃棒;
故答案为:AC;烧杯、玻璃棒;
(2)容量瓶只能用来配制一定体积准确浓度的溶液,不能配制或测量容量瓶规
格以下的任意体积的液体,不能稀释或溶解药品,不能用来加热溶解固体溶质,
故选BCDF;
故答案为:BCDF;
(3)需要0.2 mol/LNaOH溶液450 mL,应选择500mL容量瓶,需要氢氧化钠质
量为:0.5L×0.2mol/L×40g/mol=4.0g,在实验中其他操作均正确,若定容时
仰视刻度线,导致溶液体积偏大,则所得溶液浓度小于 0.2 mol/L,若 NaOH溶
液在转移至容量瓶时未经冷却,冷却后溶液体积偏小,则所得溶液浓度大于0.2
mol/L;
故答案为:4.0;小于;大于;
(4)量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为c(浓硫酸)
第17页(共18页)18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的
�ͲͲͲ��ర���రல
�体积为 �Vర,所以�18.4mol/L×V=1mol/L×500mL,得 V=27.2mL;浓硫酸稀释的
正确操作;将浓硫酸沿着烧杯壁缓缓注入水中,同时用玻璃棒不断搅拌;
故答案为:27.2;将浓硫酸沿着烧杯壁缓缓注入水中,同时用玻璃棒不断搅拌;
(5)需称量溶质10.2g,某同学称量时将砝码放在左盘,装NaOH的烧杯放在了
右盘,且称量时使用了游码,则称取质量为10g﹣0.2g=9.8g,导致溶质的物质
的量偏小,依据c 可知溶液浓度偏小。
�
故答案为:偏小。� �
第18页(共18页)