文档内容
一、选择题
1.下列说法不正确的是( )
A.明矾水解生成Al(OH) 胶体,可用作净水剂
3
B.水解反应NH+HONH ·H O+H+达到平衡后,升高温度平衡逆向移动
2 3 2
C.制备AlCl 、FeCl 、CuCl 均不能采用将溶液直接蒸干的方法
3 3 2
D.盐类水解反应的逆反应是中和反应
解析:选B。水解吸热,升高温度促进水解,平衡正向移动,B错误。
2.下列有关电解质溶液的说法正确的是( )
A.将Ca(ClO) 、NaSO 溶液蒸干均得不到原溶质
2 2 3
B.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解
C.室温下,向 0.1 mol·L-1的 CHCOOH 溶液中加入少量水溶液显碱性的物质,
3
CHCOOH的电离程度一定增大
3
D.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同
3 4
解析:选A。Ca(ClO) 在水中发生水解:Ca(ClO) +2HOCa(OH) +2HClO,HClO不
2 2 2 2
稳定,受热会分解:2HClO=====2HCl+O↑,生成的HCl会和Ca(OH) 反应生成CaCl 和
2 2 2
HO,故加热蒸干Ca(ClO) 溶液得到的固体是CaCl ;加热NaSO 溶液的过程中,发生反应:
2 2 2 2 3
2NaSO +O===2Na SO ,蒸干会得到NaSO 固体,A项正确。保存氯化亚铁溶液时,在溶液
2 3 2 2 4 2 4
中放少量铁粉,可防止Fe2+被氧化为Fe3+,B项错误。水溶液显碱性的物质不一定是碱,如强
碱弱酸盐 CHCOONa,其水溶液显碱性,向 CHCOOH 溶液中加入少量 CHCOONa,
3 3 3
CHCOO-浓度增大,会抑制CHCOOH的电离,CHCOOH的电离程度减小,C项错误。
3 3 3
CHCOONH 是能发生水解相互促进反应的盐,CHCOO-、NH的水解均会促进水的电离,溶
3 4 3
液中水的电离程度较大,但溶液中的H+浓度与OH-浓度相等,故溶液呈中性,D项错误。
3.(2019·抚顺六校联考)常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法
正确的是( )
A.当溶液中c(CHCOO-)=c(Na+)时,醋酸与氢氧化钠恰好完全反应
3
B.当溶液中c(CHCOO-)=c(Na+)时,一定是氢氧化钠过量
3
C.当溶液中c(CHCOO-)=c(Na+)>c(H+)=c(OH-)时,一定是醋酸过量
3
D.当溶液中c(Na+)>c(CHCOO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量
3
解析:选C。当溶液中c(CHCOO-)=c(Na+)时,根据电荷守恒 c(Na+)+c(H+)=
3
c(CHCOO-)+c(OH-)可得,c(H+)=c(OH-),即醋酸稍过量,A、B项错误,C项正确;当氢氧
3
化钠与醋酸恰好完全反应时,D项中关系式也符合,D项错误。
4.在一定条件下,NaS溶液中存在水解平衡:S2-+HOHS-+OH-。下列说法正确
2 2
的是( )
A.稀释溶液,水解常数增大
B.通入HS,HS-浓度减小
2C.升高温度,增大
D.加入NaOH固体,溶液pH减小
解析:选C。水解常数只与温度有关,因此稀释溶液,水解常数不变,A项错误;通入
HS,HS-浓度增大,B项错误;升高温度,水解平衡向右移动,溶液中c(HS-)增大、c(S2-)减小,
2
故增大,C项正确;加入NaOH固体,溶液碱性增强,pH增大,D项错误。
5.(2019·江南十校检测)常温下,下列有关叙述不正确的是( )
A.若NH Cl溶液的pH=6,则c(Cl-)-c(NH)=9.9×10-7 mol/L
4
B.CHCOONa和CaCl 混合溶液中:c(Na+)+c(Ca2+)=c(CHCOO-)+c(CHCOOH)+
3 2 3 3
2c(Cl-)
C.等物质的量浓度的NaCO 与NaHCO 混合溶液中:
2 3 3
2c(Na+)=3c(CO)+3c(HCO)+3c(H CO)
2 3
D.已知HA的K =4.17×10-7,K =4.9×10-11,则NaHA溶液呈碱性
2 a1 a2
解析:选B。A.根据电荷守恒,c(NH)+c(H+)=c(Cl-)+c(OH-),溶液的pH=6,即c(H+)
=10-6 mol/L,c(OH-)=10-8 mol/L,因此有c(Cl-)-c(NH)=c(H+)-c(OH-)=(10-6-10-8)
mol/L=9.9×10-7 mol/L,故A说法正确;B.根据物料守恒,c(CHCOO-)+c(CHCOOH)=
3 3
c(Na+),c(Cl-)=2c(Ca2+),因此有c(Na+)+2c(Ca2+)=c(CHCOO-)+c(CHCOOH)+c(Cl-),
3 3
故B说法错误;C.根据物料守恒,2c(Na+)=3c(CO)+3c(HCO)+3c(H CO),故C说法正确;
2 3
D.根据K 、K 、K 关系,K =K /K =10-14/(4.17×10-7)=2.4×10-8>4.9×10-11,推出NaHA
w h a h w a1
溶液显碱性,故D说法正确。
6.有关①100 mL 0.1 mol·L-1NaHCO 、②100 mL 0.1 mol·L-1NaCO 两种溶液的叙述不
3 2 3
正确的是( )
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO)>c(H CO)
2 3
D.②溶液中:c(HCO)>c(H CO)
2 3
解析:选C。CO的水解能力比HCO的强,故NaCO 溶液的pH较大,水电离出的H+总
2 3
数与OH-总数相同,A项正确;NaCO 溶液中Na+的浓度是NaHCO 溶液中的两倍,根据电
2 3 3
荷守恒可知B项正确;①溶液中HCO的水解能力大于其电离能力,C项不正确;②溶液中
HCO、HCO 分别是CO的第一步水解产物和第二步水解产物,D项正确。
2 3
7.(2019·昆明质检)有机酸种类繁多,甲酸(HCOOH)是常见的一元酸,常温下其K=
a
1.8×10-4,草酸(H C O)是常见的二元酸,常温下,K =5.4×10-2,K =5.4×10-5。下列说法
2 2 4 a1 a2
正确的是( )
A.甲酸钠溶液中:c(Na+)>c(HCOO-)>c(H+)>c(OH-)
B.草酸氢钠溶液中加入甲酸钠溶液至中性:c(Na+)=c(HC O)+2c(C O)+c(HCOO-)
2 2
C.NaC O 溶液中:c(HC O)+c(H C O)+c(H+)=c(OH-)
2 2 4 2 2 2 4
D.足量甲酸与草酸钠溶液反应:2HCOOH+NaC O===H C O+2HCOONa
2 2 4 2 2 4解析:选B。A.甲酸为弱酸,甲酸钠为强碱弱酸盐,离子浓度大小顺序是c(Na+)>
c(HCOO-)>c(OH-)>c(H+),故A错误;B.根据电荷守恒,c(Na+)+c(H+)=c(OH-)+
c(HC O)+2c(C O)+c(HCOO-),溶液显中性,即c(Na+)=c(HC O)+2c(C O)+c(HCOO-),故
2 2 2 2
B正确;C.根据质子守恒,有c(OH-)=c(H+)+c(HC O)+2c(H C O),故C错误;D.根据电离
2 2 2 4
平衡常数K >K >K ,因此足量甲酸与草酸钠反应:HCOOH+NaC O===HCOONa+
a1 a a2 2 2 4
NaHC O,故D错误。
2 4
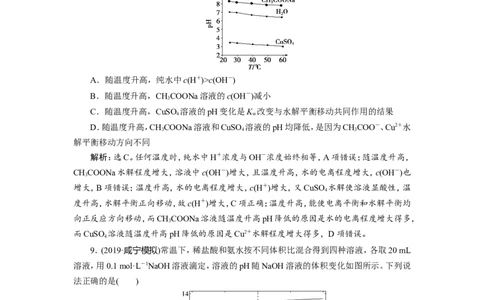
8.(2019·高考北京卷)实验测得0.5 mol·L-1 CHCOONa溶液、0.5 mol·L-1 CuSO 溶液
3 4
以及HO的pH随温度变化的曲线如图所示。下列说法正确的是( )
2
A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水
3 4 3
解平衡移动方向不同
解析:选C。任何温度时,纯水中H+浓度与OH-浓度始终相等,A项错误;随温度升高,
CHCOONa水解程度增大,溶液中c(OH-)增大,且温度升高,水的电离程度增大,c(OH-)也
3
增大,B项错误;温度升高,水的电离程度增大,c(H+)增大,又CuSO 水解使溶液显酸性,温
4
度升高,水解平衡正向移动,故c(H+)增大,C项正确;温度升高,能使电离平衡和水解平衡均
向正反应方向移动,而CHCOONa溶液随温度升高pH降低的原因是水的电离程度增大得多,
3
而CuSO 溶液随温度升高pH降低的原因是Cu2+水解程度增大得多,D项错误。
4
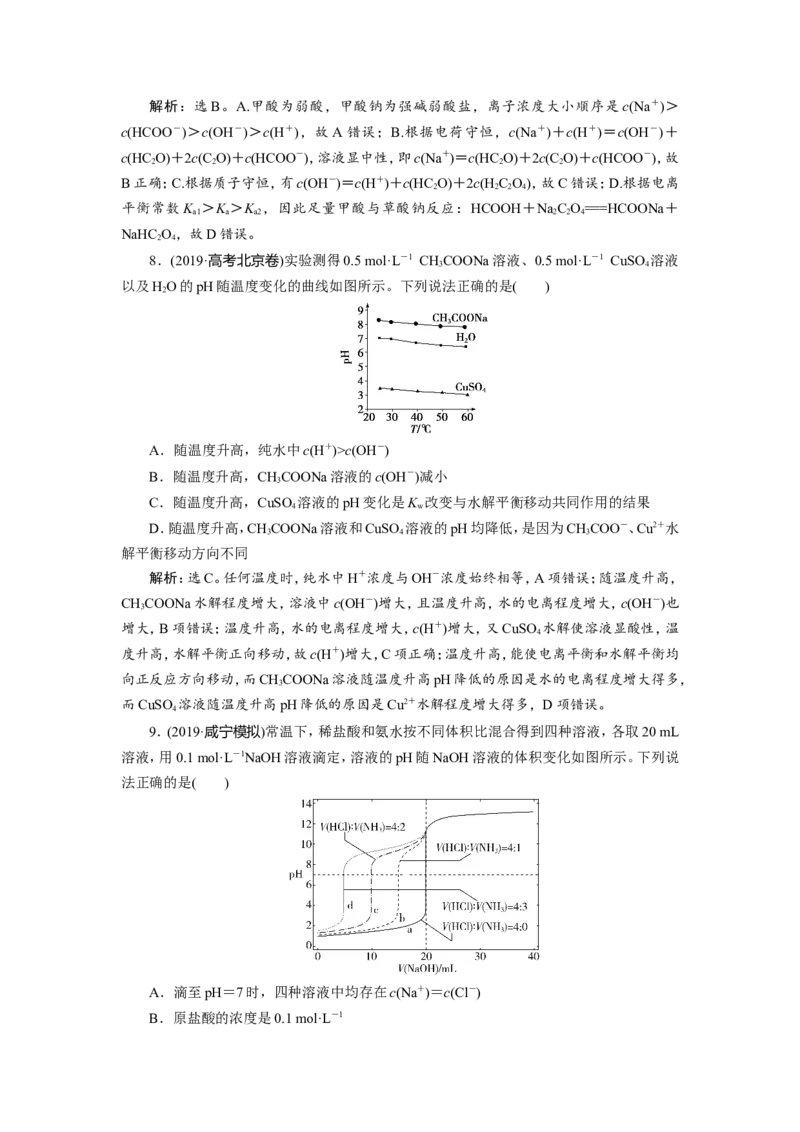
9.(2019·咸宁模拟)常温下,稀盐酸和氨水按不同体积比混合得到四种溶液,各取20 mL
溶液,用0.1 mol·L-1NaOH溶液滴定,溶液的pH随NaOH溶液的体积变化如图所示。下列说
法正确的是( )
A.滴至pH=7时,四种溶液中均存在c(Na+)=c(Cl-)
B.原盐酸的浓度是0.1 mol·L-1C.V(NaOH)=10 mL,溶液中Na+浓度a>b
D.当V(NaOH)>20 mL时,四种溶液的pH相同,溶液中的NH浓度近似相等
解析:选B。根据电荷守恒,滴至pH=7时,c(H+)=c(OH-),则a溶液中c(Na+)=c(Cl-),
b、c、d三种溶液中c(Na+)+c(NH)=c(Cl-),A错误;a溶液中稀盐酸和氨水按4∶0的比例混
合,溶液中只含盐酸,当滴入0.1 mol·L-1NaOH溶液20 mL时溶液呈中性,则盐酸的浓度为
0.1 mol·L-1,B正确;V(NaOH)=10 mL,由于向a和b中加入的氢氧化钠的量相同,则溶液
中Na+浓度a=b,C错误;当V(NaOH)>20 mL时,根据电荷守恒,溶液中均存在c(Na+)+
c(NH)+c(H+)=c(OH-)+c(Cl-)。四种溶液中加入的氢氧化钠的量均相同,则溶液中的c(Na
+)均相同,因为四种溶液的pH相同,则四种溶液中的c(H+)和c(OH-)均相同,又因为四种溶
液中稀盐酸和氨水混合比例不同,则溶液中c(Cl-)大的,c(NH)也大,则溶液中的NH浓度不
相等,D错误。
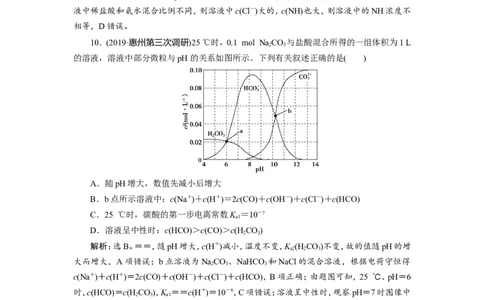
10.(2019·惠州第三次调研)25 ℃时,0.1 mol NaCO 与盐酸混合所得的一组体积为1 L
2 3
的溶液,溶液中部分微粒与pH 的关系如图所示。下列有关叙述正确的是( )
A.随pH增大,数值先减小后增大
B.b点所示溶液中:c(Na+)+c(H+)=2c(CO)+c(OH-)+c(Cl-)+c(HCO)
C.25 ℃时,碳酸的第一步电离常数K =10-7
a1
D.溶液呈中性时:c(HCO)>c(CO)>c(H CO)
2 3
解析:选B。==,随pH增大,c(H+)减小,温度不变,K (H CO)不变,故的值随pH的增
a2 2 3
大而增大,A项错误;b点溶液为NaCO 、NaHCO 和NaCl的混合溶液,根据电荷守恒得
2 3 3
c(Na+)+c(H+)=2c(CO)+c(OH-)+c(Cl-)+c(HCO),B项正确;由题图可知,25 ℃、pH=6
时,c(HCO)=c(H CO),K ==c(H+)=10-6,C项错误;溶液呈中性时,观察pH=7时图像中
2 3 a1
的三条曲线可知,c(HCO)>c(H CO)>c(CO),D项错误。
2 3
二、非选择题
11.现有0.175 mol·L-1醋酸钠溶液500 mL(已知醋酸的电离平衡常数K=1.75×10-5)。
a
(1)写出醋酸钠发生水解反应的化学方程式:__________________________________
________________________________________________________________________。
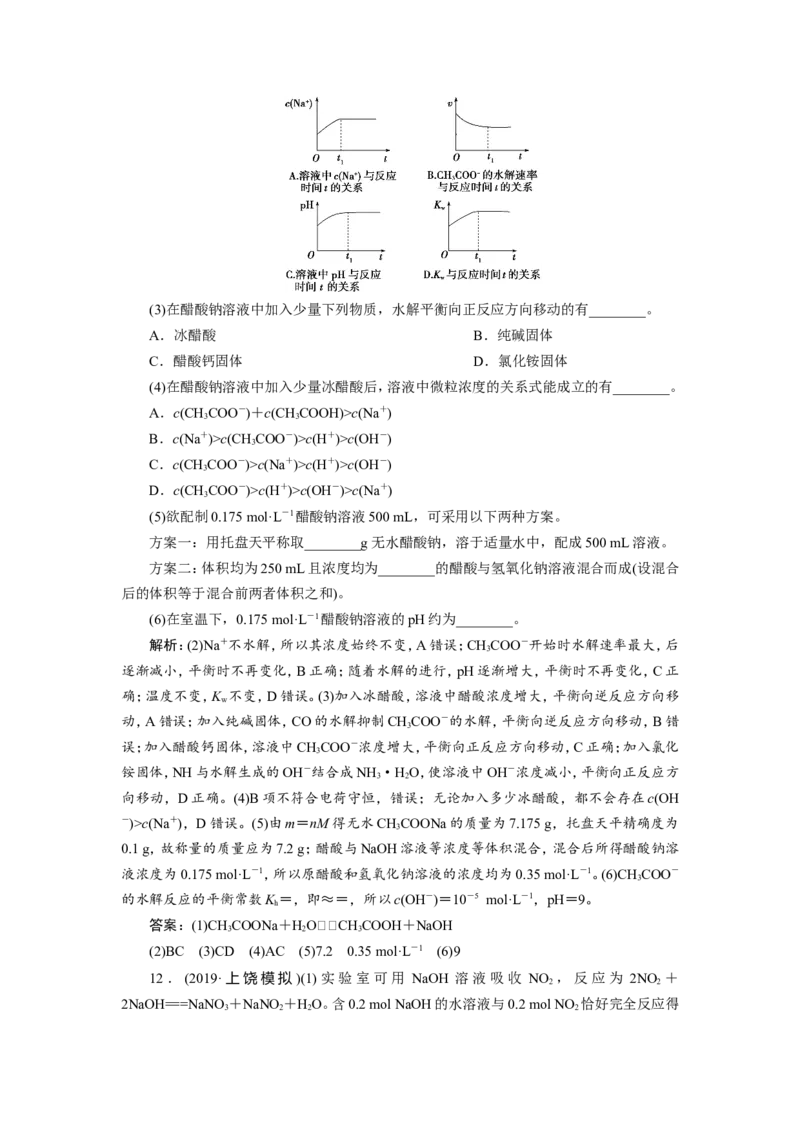
(2)下列图像能说明醋酸钠的水解反应达到平衡的是________。(3)在醋酸钠溶液中加入少量下列物质,水解平衡向正反应方向移动的有________。
A.冰醋酸 B.纯碱固体
C.醋酸钙固体 D.氯化铵固体
(4)在醋酸钠溶液中加入少量冰醋酸后,溶液中微粒浓度的关系式能成立的有________。
A.c(CHCOO-)+c(CHCOOH)>c(Na+)
3 3
B.c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
C.c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
D.c(CHCOO-)>c(H+)>c(OH-)>c(Na+)
3
(5)欲配制0.175 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案。
方案一:用托盘天平称取________g无水醋酸钠,溶于适量水中,配成500 mL溶液。
方案二:体积均为250 mL且浓度均为________的醋酸与氢氧化钠溶液混合而成(设混合
后的体积等于混合前两者体积之和)。
(6)在室温下,0.175 mol·L-1醋酸钠溶液的pH约为________。
解析:(2)Na+不水解,所以其浓度始终不变,A错误;CHCOO-开始时水解速率最大,后
3
逐渐减小,平衡时不再变化,B正确;随着水解的进行,pH逐渐增大,平衡时不再变化,C正
确;温度不变,K 不变,D错误。(3)加入冰醋酸,溶液中醋酸浓度增大,平衡向逆反应方向移
w
动,A错误;加入纯碱固体,CO的水解抑制CHCOO-的水解,平衡向逆反应方向移动,B错
3
误;加入醋酸钙固体,溶液中CHCOO-浓度增大,平衡向正反应方向移动,C正确;加入氯化
3
铵固体,NH与水解生成的OH-结合成NH ·HO,使溶液中OH-浓度减小,平衡向正反应方
3 2
向移动,D正确。(4)B项不符合电荷守恒,错误;无论加入多少冰醋酸,都不会存在c(OH
-)>c(Na+),D错误。(5)由m=nM得无水CHCOONa的质量为7.175 g,托盘天平精确度为
3
0.1 g,故称量的质量应为7.2 g;醋酸与NaOH溶液等浓度等体积混合,混合后所得醋酸钠溶
液浓度为0.175 mol·L-1,所以原醋酸和氢氧化钠溶液的浓度均为0.35 mol·L-1。(6)CH COO-
3
的水解反应的平衡常数K =,即≈=,所以c(OH-)=10-5 mol·L-1,pH=9。
h
答案:(1)CH COONa+HOCHCOOH+NaOH
3 2 3
(2)BC (3)CD (4)AC (5)7.2 0.35 mol·L-1 (6)9
12.(2019·上饶模拟)(1)实验室可用 NaOH 溶液吸收 NO ,反应为 2NO +
2 2
2NaOH===NaNO +NaNO +HO。含0.2 mol NaOH的水溶液与0.2 mol NO 恰好完全反应得
3 2 2 21 L溶液A,溶液B为0.1 mol·L-1的CHCOONa溶液,则两种溶液中 c(NO)、c(NO)和
3
c(CHCOO-)由大到小的顺序为________________________________________________
3
(已知HNO 的电离常数K=7.1×10-4,CHCOOH的电离常数K=1.7×10-5)。
2 a 3 a
可使溶液A和溶液B的pH相等的方法是________(填字母)。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
(2)Na SO 溶于水即生成NaHSO。证明NaHSO 中HSO的电离程度大于水解程度,可采
2 2 5 3 3
用的实验方法是________(填字母)。
a.测定溶液的pH b.加入Ba(OH) 溶液
2
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
答案:(1)c(NO)>c(NO)>c(CHCOO-) bc (2)ae
3
13.(创新题)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1 CHCOOH溶液中加入0.1 mol CH COONa固体,则
3 3
溶液中________(填“增大”“不变”或“减小”);写出表示该混合溶液中所有离子浓度之
间的一个等式:___________________________________________。
(2)土壤的pH一般在4~9。土壤中NaCO 含量较高时,pH可高达10.5,试用离子方程式
2 3
解释土壤呈碱性的原因:_________________________________________________。
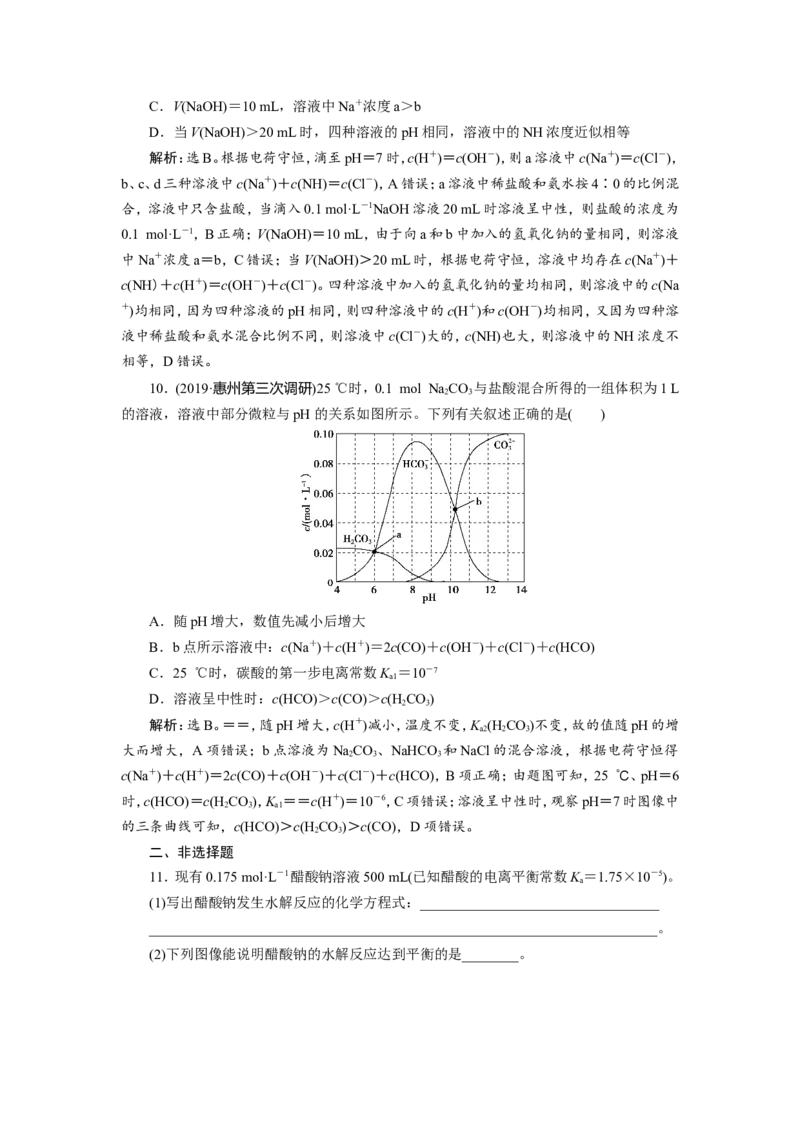
(3)常温下在20 mL 0.1 mol·L-1 NaCO 溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,
2 3
溶液中含碳元素的各种微粒(CO 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分
2
情况如图所示。
回答下列问题:
①在同一溶液中,HCO、HCO,CO__________(填“能”或“不能”)大量共存;
2 3
②当pH=7时,溶液中含碳元素的主要微粒为__________________,溶液中各种离子的
物质的量浓度的大小关系为_________________________________________________;
③已知在25 ℃时,CO水解反应的平衡常数即水解常数 K ==2.0×10-4,当溶液中
h
c(HCO)∶c(CO)=2∶1时,溶液的pH=________。
解析:(1)K =,K 仅受温度影响,温度不变,K 值不变。若写电荷守恒的等式则为
a a a
c(CHCOO-)+c(OH-)=c(H+)+c(Na+),若写物料守恒的等式则为 c(CHCOO-)+
3 3
c(CHCOOH)=0.2 mol·L-1。
3(2)土壤呈碱性,是CO水解所致,CO的水解以第一步为主。
(3)①通过观察图像可知HCO 和CO不可以共存,会发生反应生成HCO。②通过观察
2 3
图像可知当pH=7时,溶液中含碳元素的主要微粒为HCO、HCO。③当c(HCO)∶c(CO)=
2 3
2∶1时,K ==2c(OH-)=2.0×10-4,则c(OH-)=1.0×10-4 mol·L-1,故c(H+)==1.0×10-
h
10 mol·L-1,pH=10。
答案:(1)不变 c(CHCOO-)+c(OH-)=c(H+)+c(Na+)(答案合理即可)
3
(2)CO+HOHCO+OH-
2
(3)①不能
②HCO、HCO c(Na+)>c(Cl-)>c(HCO)>c(H+)=c(OH-)
2 3
③10