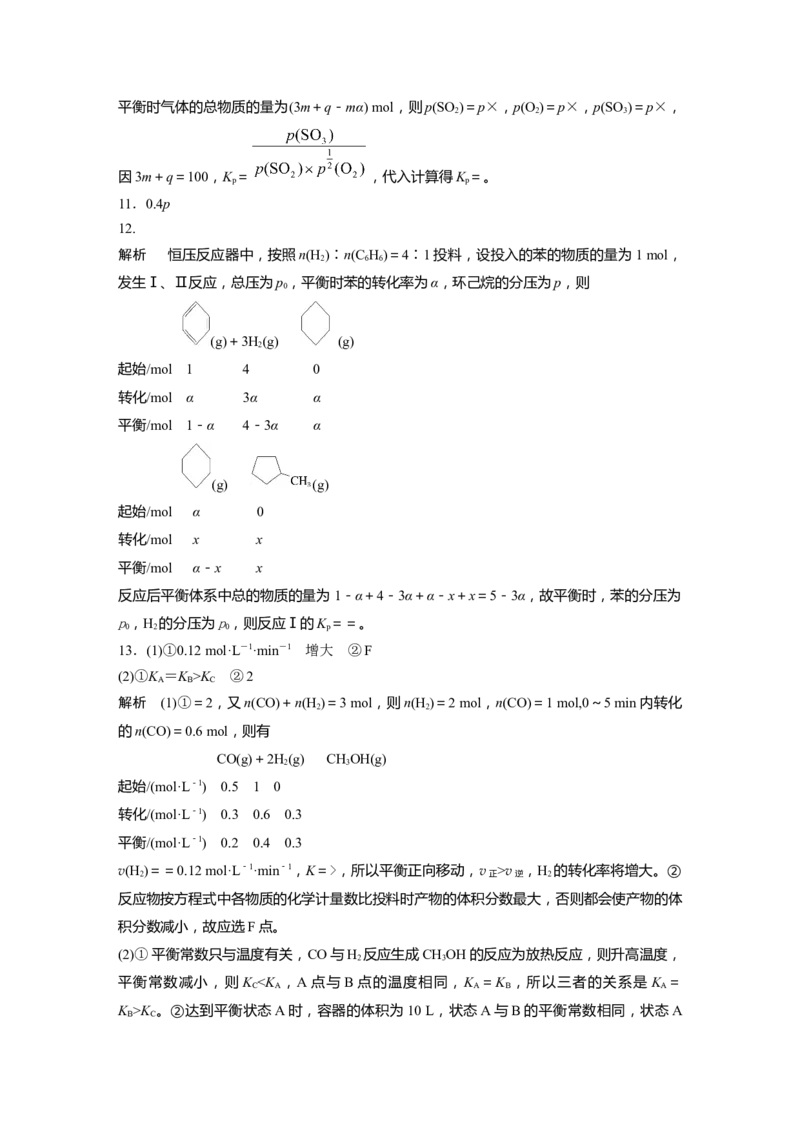文档内容
一轮复习 74 练答案精析
第一章 化学物质及其变化
第 1 练 物质的组成、性质和转化
1.A 2.D 3.D 4.D
5.D [茶多酚的性质不稳定,在高温下易被空气中的氧气氧化,故“翻炒”时,木炭火的
温度不是越高越好,A错误;100 ℃时水的离子积K =10-12,此时中性溶液的pH=6,且
w
酚羟基具有弱酸性,茶叶中含有茶多酚,故用开水刚泡制的茶水 pH应该小于6,B错误;
瓷器茶杯是陶瓷制品,是无机硅酸盐材料,属于传统的无机非金属材料,C错误。]
6.B 7.C
8.C [A项,氢、氧两种元素除组成HO外还可以组成HO ,错误;B项,导热性、折射
2 2 2
率、导电性属于水的物理性质,错误;C项,冰浮在水上,说明冰的密度小于液态水,正确;
D项,液态水两种形态间的转化属于物理变化,错误。]
9.B [在晶体硅中,每个Si与其周围的4个Si形成共价键并形成空间网状结构,因此,平
均每个Si形成2个共价键, 1 mol Si含Si—Si的数目约为2×6.02×1023,B说法错误;
SiHCl 易水解,氢气中混有氧气易爆炸,原料气HCl和H 应充分去除水和氧气 ,C说法正
3 2
确;Si+3HCl=====SiHCl +H ,该反应是气体分子数减少的反应,因此,生成SiHCl 的反
3 2 3
应为熵减过程,D说法正确。]
10.B
11.A [SO 可与NaOH溶液反应,①可以实现;HS+CuSO ===CuS↓+HSO ,②可以实
2 2 4 2 4
现;HSO +2CHCOONa===2CHCOOH+NaSO ,没有水、沉淀和气体生成,③可以实现;
2 4 3 3 2 4
HSO +2HS===3S↓+3HO,④可以实现;同素异形体之间的转化不属于氧化还原反应,
2 3 2 2
但有单质参加,⑤可以实现;2NaO+2HO===4NaOH+O↑,⑥可以实现。]
2 2 2 2
12.B [若A为Fe,D为Cl,Fe与Cl 反应生成FeCl 而不是FeCl ,B错误。]
2 2 3 2
13.(1)① ②④ ④ (2)胶体 金颗粒
14.(1)FeCl 、Fe(OH) (2)②③⑤ 4Fe(OH) +O +2HO===4Fe(OH) (3)1~100 nm 丁
2 2 2 2 2 3
达尔效应
(4)Fe O 或Fe O FeSO 分解生成SO 和SO ,部分S元素被还原,则Fe元素应被氧化,所
2 3 3 4 4 2 3
以X为Fe O 或Fe O (5)bc
2 3 3 4第 2 练 离子反应 离子方程式
1.C 2.D
3.B [二氧化氮和水生成硝酸和NO,反应为3NO +HO===2H++2NO+NO,A正确;石
2 2
灰乳不能拆,反应为Cl +Ca(OH) ===Ca2++ClO-+Cl-+HO,B错误;Al放入NaOH溶
2 2 2
液中生成偏铝酸钠和氢气:2Al+2OH-+2HO===2AlO+3H↑,C正确;Pb放入Fe (SO )
2 2 2 4 3
溶液中发生氧化还原反应生成二价铅和二价铁离子,反应为 Pb+SO+2Fe3+===2Fe2++
PbSO ,D正确。]
4
4.C
5.D [向溶液中加入硫酸锌,硫酸根离子会与溶液中的钡离子反应生成BaSO 沉淀,故A
4
不符合题意;向溶液中加入铁粉,铁离子会与铁反应生成亚铁离子,故B不符合题意;向
溶液中通入氨气,铝离子、铁离子会与氨水反应生成氢氧化铝、氢氧化铁沉淀,故C不符
合题意;向溶液中通入二氧化碳,二氧化碳与溶液中离子均不发生反应,故D符合题意。]
6.A 7.D
8.D [硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或
NO ,反应的离子方程式为 4H++2NO+S2-===S↓+2NO ↑+2HO或8H++2NO+3S2-
2 2 2
===3S↓+2NO↑+4HO,A错误;明矾在水中可以电离出Al3+,可以与NH ·H O电离出的
2 3 2
OH-发生反应生成 Al(OH) ,但由于 NH ·H O的碱性较弱,生成的 Al(OH) 不能继续与
3 3 2 3
NH ·H O发生反应,故反应的离子方程式为 Al3++3NH ·H O===Al(OH) ↓+3NH,B错误;
3 2 3 2 3
硅酸的酸性弱于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其
通入的量的多少反应生成碳酸根或碳酸氢根,反应的离子方程式为 SiO+HO+CO(少
2 2
量)===HSiO↓+CO或SiO+2HO+2CO(过量)===HSiO↓+2HCO,C错误;将等物质
2 3 2 2 2 3
的量浓度的Ba(OH) 与NH HSO 溶液以体积比1∶2混合,由于H+与OH-结合能力强于
2 4 4
NH,H+恰好完全反应,反应的离子方程式为Ba2++2OH-+2H++SO===BaSO↓+2HO,
4 2
D正确。]
9.B [碘化亚铁溶液与等物质的量的氯气反应,碘离子与氯气恰好完全反应:2I-+
Cl===I+2Cl-,故A错误;向次氯酸钙溶液通入足量二氧化碳,反应生成碳酸氢钙和次氯酸:
2 2
ClO-+CO +HO===HClO+HCO,故B正确;铜与稀硝酸反应生成硝酸铜、一氧化氮和水:
2 2
3Cu+8H++2NO===3Cu2++2NO↑+4HO,故C错误;向硫化钠溶液通入足量二氧化硫,
2
发生反应:2S2-+5SO +2HO===3S↓+4HSO,故D错误。]
2 2
10.D 11.D
12.A [二氧化碳和水在叶绿素作用下光合作用是氧化还原反应,A错误;根据反应图像分
析,钙化过程中HCO转化为CO、HCO,HCO 分解产生CO、HO,CO与Ca2+结合形成
2 3 2 3 2 2CaCO 沉淀,所以钙化作用的离子方程式之一为Ca2+ +2HCO===CaCO ↓+CO↑+HO,
3 3 2 2
D正确。]
13.(1)Cl- Na+ Ca2+ (2)CO+Ca2+===CaCO ↓ (3)5
3
14.(1)Ba2++SO+H++HCO===BaSO↓+HO+CO↑
4 2 2
HCO+H+===CO↑+HO
2 2
(2)2Al3++3SO+3Ba2++6OH-===2Al(OH) ↓+3BaSO↓
3 4
(3)Cu2++2HS-===CuS↓+HS↑
2
(4)4CO +5OH-===CO+3HCO+HO
2 2
(5)CO+CHCOOH===HCO+ CHCOO-
3 3
第 3 练 氧化还原反应的概念和规律
1.B 2.C
3.A [用FeCl 溶液刻蚀铜质电路板过程中发生反应:2Fe3++Cu===Cu2++2Fe2+,氧化剂
3
的氧化性强于氧化产物,即氧化性:Fe3+>Cu2+,A项正确;用NaO 作呼吸面具的氧气来
2 2
源时,NaO 自身发生歧化反应,未氧化CO ,B项错误;用NaS除去废水中的Cu2+和Hg2
2 2 2 2
+是发生复分解反应的过程,与NaS的还原性无关,C项错误;用石灰乳脱除烟气中的SO
2 2
过程中,先生成CaSO,后被O 氧化为CaSO,与SO 的氧化性无关,D项错误。]
3 2 4 2
4.D 5.D
6.C [Te为第ⅥA族元素,与Cu形成化合物时显-2价,则Cu Te中Cu为+1价,A项
2
错误;反应①中,Cu和Te元素化合价均升高,则氧化产物为CuSO 和TeO ,B项错误;反
4 2
应②中每生成1 mol Te,转移4 mol电子,反应①中每生成1 mol TeO ,转移8 mol电子,则
2
每制备1 mol Te,理论上共转移12 mol电子,C项正确;根据反应①判断,氧化剂的氧化性
强于氧化产物,则O 氧化性强于TeO ,根据反应②判断,TeO 为氧化剂,SO 为还原剂,
2 2 2 2
则TeO 氧化性强于SO ,D项错误。]
2 2
7.A [该反应中只有碘元素的价态升高,由0价升高至KH(IO) 中的+5价,每个碘原子
3 2
升高5价,即6I ~60e-,又因化学方程式中6I ~3Cl ,故3Cl ~60e-,即Cl ~20e-,所以
2 2 2 2 2
产生22.4 L (标准状况) Cl 即1 mol Cl 时,反应中应转移20 mol e-,A错误;该反应中
2 2
KClO 中氯元素价态降低,KClO 作氧化剂,I 中碘元素价态升高,I 作还原剂,由该化学
3 3 2 2
方程式的计量数可知,11KClO ~6I ,故该反应的氧化剂和还原剂的物质的量之比为
3 2
11∶6,B正确;漂白粉的有效成分是次氯酸钙,工业制漂白粉可用石灰乳与氯气反应,C
正确;食盐中IO可先与酸化的淀粉碘化钾溶液中的H+、I-发生归中反应:IO+5I-+6H+
===3I+3HO,淀粉与生成的I 发生特征反应变为蓝色,故可用酸化的淀粉碘化钾溶液检验
2 2 2食盐中IO的存在,D正确。]
8.C 9.A 10.D
11.(1)Cu > (2)33.6 (3)D
(4) +8HO
2
解析 (3)根据氧原子守恒则n=2,根据氢原子守恒则y=4,根据R原子守恒则x=m,根据
电荷守恒则2x+y=3m,所以x=y=m=4;在反应中,R的化合价升高,R2+是还原剂,则
R3+是氧化产物,氧元素化合价降低,所以HO是还原产物。
2
12.(1)CuI I (2)2Cu+I===2CuI (3)> 高 (4)AC
2 2
13.(1)NaOH溶液 防止尾气污染环境
(2)MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
(3)2Fe3++SO +2HO===2Fe2++SO+4H+ 取少许溶液于试管中,先加入足量稀盐酸酸化,
2 2
再滴加少量BaCl 溶液,若有白色沉淀生成,证明有SO,反之无SO
2
(4)SO >Fe2+>Cl- (5)乙、丙
2
解析 (1)向B中的FeCl 溶液中通入氯气和二氧化硫,为防止多余的氯气和二氧化硫污染空
2
气,需要将其除去,所以棉花中浸润的溶液为 NaOH溶液。(2)实验室制备氯气用的是二氧
化锰和浓盐酸在加热的条件下反应,化学方程式为 MnO +4HCl(浓)=====MnCl +Cl↑+
2 2 2
2HO。(3)先向B中的FeCl 溶液中通入Cl ,B中的亚铁离子被氯气氧化为铁离子,再向B
2 2 2
中通入一定量的SO 气体,铁离子被二氧化硫还原为亚铁离子,离子方程式为2Fe3++SO +
2 2
2HO===2Fe2++SO+4H+。(5)过程Ⅱ是为了检验Fe2+被氯气氧化后的产物,过程Ⅳ是为了
2
检验二氧化硫被Fe3+氧化后的产物。甲:过程Ⅱ中检出离子有Fe3+无Fe2+,说明氯气过量,
过程Ⅳ中检出离子有SO,不能说明二氧化硫是被铁离子氧化的,也可能是被氯气氧化的,
甲错误;乙:过程Ⅱ中检出离子既有Fe3+又有Fe2+,说明亚铁离子未被氧化完全,氯气量
不足,过程Ⅳ中检出离子有SO,一定是二氧化硫被铁离子氧化得到的,乙正确;丙:过程
Ⅱ检出离子有Fe3+无Fe2+,而过程Ⅳ中检出离子有Fe2+,说明二氧化硫把铁离子还原为亚
铁离子,丙正确。
第 4 练 氧化还原反应方程式的配平及计算
1.A
2.B [由题干信息得到该离子方程式为5IO+2Mn2++3HO===2MnO+5IO+6H+,IO中
2
的碘元素在反应中化合价降低,得电子,作氧化剂,具有氧化性,故 A正确;根据反应方
程式可知,该反应的氧化剂是IO,氧化产物是MnO,则氧化性强弱顺序是IO>MnO,故B错误;根据方程式可知:氧化剂碘酸根离子和还原剂锰离子的物质的量之比为5∶2,故C
正确;根据离子方程式可知,有2个 Mn2+参加反应时,转移电子的个数是10个,故D正
确。]
3.B [根据原子守恒并结合离子方程式两边离子所带电荷总数相等可知,反应①为SO +
2
2Fe3++2HO===SO+2Fe2++4H+,W为4H+,A错误;由反应①可知,还原性:SO >Fe2
2 2
+,B正确;反应②中,根据得失电子守恒可得,Cr O和Cr3+对应的化学计量数分别为1、
2
2,Fe2+和Fe3+对应的化学计量数均为6,则a=6,再结合离子方程式两边离子所带电荷总
数相等可得,b=14,C错误;Cr O具有强氧化性,SO 具有还原性,且由①、②可知氧化
2 2
性:Cr O>SO,则Cr O能将SO 氧化为SO,即反应Cr O+3SO +2H+===2Cr3++3SO+
2 2 2 2 2
HO能发生,D错误。]
2
4.C 5.A
6.(1)1 1 2 1 1 1 (2)1 1 2 1 2 (3)1 1 2 1 1 1
7.(1)6 1 12 12 6 6 6 (2)1 12 4 2 13
(3)2x 2 2x 2x 1 (4)1 6 1 6 12
8.(1)Na SO ·10H O+4C=====NaS+4CO↑+10HO
2 4 2 2 2
(2)FeS+CrO+4HO===Fe(OH) +Cr(OH) +S+2OH-
2 3 3
9.2IO+5HSO===I+5SO+3H++HO
2 2
10 . (1)ZnO + 2NH ·H O + 2NH===[Zn(NH )]2 + + 3HO (2)2AsCl + 2HO +
3 2 3 4 2 2 2
6NH ·H O===As O(胶体)+10Cl-+6NH+5HO
3 2 2 5 2
11.(1)Pb+HO+2HAc===Pb(Ac) +2HO
2 2 2 2
(2)5TiO+6C+10Cl=====5TiCl +2CO+4CO
2 2 4 2
12.(1)H S+2Fe3+===2Fe2++S↓+2H+
2
(2)NO 3Fe 8 3 NH 2HO
2
13.(1)4Al+3MnO =====3Mn+2Al O
2 2 3
(2)①MnO +SO ======MnSO ②2Fe2++MnO +4H+===Mn2++2Fe3++2HO ③溶液中
2 2 4 2 2
存在平衡:MnCO (s)Mn2+(aq)+CO(aq),CO消耗溶液中的H+,促进SO 溶解:SO +
3 2 2
HOHSO H++HSO,Mn2+有催化作用,可促进反应2SO +O +2HO=====2HSO
2 2 3 2 2 2 2 4
发生 (3)55c(V-V)×10-3
1 0
解析 (2)②据图可知过程Ⅰ中MnO 被Fe2+还原生成Mn2+,Fe2+被氧化为Fe3+,根据电子
2
守恒和元素守恒可得离子方程式为2Fe2++MnO +4H+===Mn2++2Fe3++2HO。(3)滴定时
2 2
发生反应Fe2++Mn3+===Fe3++Mn2+,所以n(Mn)=n(Mn3+)=n(Fe2+)=c(V -V)×10-3
1 0
mol,所取废水为1 mL,所以废水中锰的含量为55c(V-V)×10-3 g·mL-1。
1 0
14.(1)②Fe3+、Mn2+ (2)①2 4 Cl- 2 Fe2+
(3)①2[AgCl ]-+Fe===Fe2++2Ag+4Cl-、2Fe3++Fe===3Fe2+
2第二章 物质的量
第 5 练 物质的量 气体摩尔体积
1.C 2.C 3.D
4.A [据n=可知,该气体的物质的量为1 mol。该温度和压强下,1 mol该气体的体积为
30 L,若是标准状况,其体积约是 22.4 L,故 A 不正确、B 正确;1 mol 该气体含有
1.204×1024个原子,则1个该气体分子中含有原子个数为=2,故C正确;因1 mol该气体
在该条件下为30 L,由此可知该条件下气体摩尔体积为30 L·mol-1,故若O 在该条件下为
2
气态,则1 mol O 在该条件下的体积也为30 L,故D正确。]
2
5.A 6.D
7.A [溶液体积未知,不能计算Co2+的数目,B错误;合成氨是可逆反应,0.1 mol N 不
2
能完全反应,故生成的NH 分子数小于0.2N ,C错误;水中也含有氧原子,则n(O)=×2
3 A
+≈5.6 mol,D错误。]
8.D [根据阿伏加德罗定律的推论:同温同压下,同质量气体的体积与其摩尔质量成反比。
四种气体的摩尔质量的大小关系为M(SO )>M(CO)>M(O )>M(CH),所以气球①②③④中的
2 2 2 4
气体分别为SO 、CO 、O 、CH ,A错误;同质量的气体,分子数之比等于其物质的量之
2 2 2 4
比,也等于其摩尔质量的反比,气球①和气球③中气体分子数不相等,气球①和气球④中气
体物质的量之比为1∶4,B、C错误;同温同压下,气体的密度与其摩尔质量成正比,气球
③和气球④中气体密度之比为2∶1,D正确。]
9.B 10.A
11.A [由题意知,n(CO)×28 g·mol-1+n(CO)×44 g·mol-1=14.4 g、n(CO)+n(CO)==
2 2
0.4 mol,联立两式解得:n(CO)=n(CO)=0.2 mol。A错,混合气体的总物质的量为 0.4
2
mol,则所含碳原子总数为0.4N ;B对,混合气体通过NaOH溶液时,CO 被吸收,气球中
A 2
收集到的气体是CO,其物质的量为 0.2 mol,故在标准状况下的体积为 4.48 L;C对,
NaOH溶液吸收CO 生成NaCO 和HO,则NaOH溶液增加的质量即为CO 的质量,应为
2 2 3 2 2
0.2 mol×44 g·mol-1=8.8 g;D对,相同温度和压强下,气体的体积之比等于其物质的量之
比,则CO和CO 的体积之比等于0.2 mol∶0.2 mol=1∶1。]
2
12.C [左右两室体积相同,气体密度相同,则气体质量相同,根据 N=n·N =N ,相同质
A A
量时,分子数与摩尔质量成反比,则开始时氢气室分子数多,故 A错误;两种气体质量相
同时,氢气的物质的量多,氢气和氯气以1∶1反应,则氢气过量,所以最终容器内有氢气
剩余,故B错误;反应中氢气有剩余,且气体总的物质的量不变,反应后两室气体物质的量相同,氢气室气体的物质的量减小,即压强减小,故C正确;反应前后气体总质量不变,
容器体积不变,根据ρ=知,最终容器内气体密度与原来相同,故D错误。]
13.(1)17∶16 (2)80% (3)5(a+b-d)g·mol-1
(4)a.①<②<③ b.②<③<① c.②<③<①
14.(1)1 (2)11 (3)11 (4)2
解析 (1)同温同压下,气体的物质的量之比等于其体积之比,由图可知甲室中气体的物质
的量为=1 mol。(2)乙室中HCl气体的质量为0.6 mol×36.5 g·mol-1=21.9 g,则甲室中气体
的质量为21.9 g-10.9 g=11 g。(3)甲室中气体的物质的量为1 mol,质量为11 g,平均摩尔
质量为11 g·mol-1,则甲室中NH 、H 的平均相对分子质量为11。(4)设甲室中氨气的物质的
3 2
量为x,氢气的物质的量为y,根据其物质的量、质量列方程组为x+y=1 mol,17 g·mol-1
×x+2 g·mol-1×y=11 g,可得x=0.6 mol、y=0.4 mol;如果将隔板a去掉,0.6 mol HCl与
0.6 mol NH 恰好完全反应生成氯化铵固体,剩余H 的物质的量为0.4 mol,同温同压下,气
3 2
体的体积之比等于其物质的量之比,所以隔板b将会左移至刻度“2”处。
第 6 练 物质的量浓度
1.C 2.C 3.B
4.A [98%的浓H SO 中溶质的物质的量浓度c==mol·L-1=18.4 mol·L-1,配制1 mol·L
2 4
-1的稀HSO 100 mL需要浓硫酸的体积V=≈0.005 4 L,即5.4 mL。]
2 4
5.D [配制500 mL 0.100 mol·L-1 NaCl溶液用到的仪器有托盘天平、药匙、烧杯、玻璃棒、
500 mL容量瓶、胶头滴管等,A错误;配制一定物质的量浓度的溶液的步骤有计算、称量、
溶解、转移、洗涤、定容、摇匀等,操作步骤正确的顺序为②①④③,B错误;容量瓶用蒸
馏水洗净后,不必干燥,C错误;定容时仰视容量瓶的刻度线,则所加蒸馏水偏多,溶液的
体积V偏大,溶液的浓度偏低,D正确。]
6.C 7.A 8.B 9.D
10.C [根据溶质的质量分数w=×100%,m =A g,V mL水的质量为V g,m =(A
溶质 溶液
+V) g,w=×100%,故A正确;根据溶质的物质的量浓度c=,n= mol,V′= L,代入
可得c= mol·L-1,故B正确;1 mL 该溶液中n(Cl-)= mol·L-1×1 mL×10-3 L·mL-1×n
= mol,故C错误;该温度下此盐的溶解度S= g,故D正确。 ]
11.C [根据题意可知,钠离子的质量是ρVa% g,物质的量是 mol,所以硫酸钠的物质的
量是 mol,质量是 mol×142 g·mol-1 g,溶质的质量分数是=%,A正确;溶液的物质的量
浓度c== mol·L-1,B正确;溶质和溶剂的物质的量之比是 mol∶=9a∶(2 300-71a),C
错误;硫酸根离子的质量分数是=%,D正确。]
12.C [根据c=,可知该硝酸的物质的量浓度c= mol·L-1=14.0 mol·L-1,A项正确;某同学用该浓硝酸配制稀硝酸,定容时俯视读数,溶液体积偏小,会造成最终配制的稀硝酸
浓度偏高,B项正确;Cu与浓HNO 发生反应:Cu+4HNO(浓)===Cu(NO ) +2NO ↑+
3 3 3 2 2
2HO,硝酸浓度降低到某一浓度后,开始生成NO,不再生成NO 50 mL该浓硝酸中,硝酸
2 2,
的物质的量n=0.05 L×14 mol·L-1=0.7 mol,由4HNO ~2NO 可知,生成NO 的物质的量
3 2 2
小于0.35 mol,C项错误;等体积的水与该硝酸混合所得溶液的体积小于原硝酸体积的 2倍,
因此所得溶液的物质的量浓度大于7.0 mol·L-1,D项正确。]
13.(1)7.14 mol·L-1 > (2)32 0.2 (3)65.57% (4)22.35 g
14.(1)⑤ (2)50 mL容量瓶 (3)偏小 (4)2 (5)当滴入最后半滴酸性KMnO 溶液,溶液由
4
无色变为浅紫色,且半分钟内不褪色 (6)1.2
解析 (3)用图示的操作配制溶液,定容时仰视刻度线,会使溶液体积偏大,配制的溶液浓
度将偏小。(6)20.00 mL血液样品经过处理后得到草酸,草酸消耗的高锰酸钾的物质的量
为0.020 mol·L-1×0.012 L=2.4×10-4 mol,根据反应的离子方程式5HC O +2MnO+6H+
2 2 4
===2Mn2++10CO↑+8HO 及草酸钙的化学式 CaC O 可知,n(Ca2+)=n(H C O)=
2 2 2 4 2 2 4
×2.4×10-4 mol=6×10-4 mol,Ca2+的质量为40 g·mol-1×6×10-4 mol=0.024 g,其浓度
为=1.2 mg·cm-3。
第 7 练 化学计算的常用方法
1.C 2.C
3.A [设该氮氧化合物的分子式为NO,化学方程式为NO+xH===N +xHO,相同条
2 x 2 x 2 2 2
件下参加反应的气体的体积之比等于其物质的量之比也等于其化学计量数之比,
NO+xH===N+xHO ΔV
2 x 2 2 2
1 x
15.6 L 46.8 L
则1∶x=15.6 L∶46.8 L,x=3,所以其化学式为NO。]
2 3
4.B [M的化合价为+n,NaCO 与MCl 反应对应的关系式为
2 3 n
2Mn+ ~ nCO
2 n
0.04 L×0.5 mol·L-1 0.015 L×2 mol·L-1
解得n=3。]
5.C 6.C
7.C [高锰酸根离子与亚铁离子反应的离子方程式为 MnO+5Fe2++8H+===Mn2++5Fe3+
+4HO,n(KMnO)=20.00×10-3 L×0.010 00 mol·L-1=2.0×10-4 mol,则n(FeSO ·7H O)
2 4 4 2
=5n(KMnO)=1.0×10-3 mol,w(FeSO ·7H O)=×100%≈96.7%。]
4 4 28.A [由题意可知,混合物中的Fe元素全部转化为Fe(NO ) ,根据N元素守恒可得,
3 2
n[Fe(NO )]=(0.15 L×4 mol·L-1-)×=0.25 mol,则n(Fe)=0.25 mol,所以用足量的H 在
3 2 2
加热条件下还原相同质量的混合物,所得到的铁的物质的量为0.25 mol。]
9.D [在溶液中微粒反应的顺序是Fe2+> Br-,n(Cl )==0.15 mol;n(Cl-)=0.3 mol;假
2
设FeBr 溶液的浓度是x mol·L-1,则在原溶液中 n(Fe2+)=0.1x mol,n(Br-)=0.2x mol;方
2
法一:得失电子守恒,由题意可得:0.1x+(0.2x-0.3)=0.15×2,解得x=2。方法二:电荷
守恒,反应后主要离子为Fe3+、Cl-和Br-可知:3×0.1x=0.3+0.3,解得x=2。也可依据
分步反应或总反应求解。]
10.
11.(1)溶液由蓝色变无色,且30 s内不恢复蓝色 ×100% (2)CaO
解析 (1)根据得失电子守恒,可得关系式 CaO ~I ~2SO,则样品中CaO 的质量分数为
2 2 2 2
×100%=×100%。(2)CaO·8H O的摩尔质量为216 g·mol-1,故2.16 g过氧化钙晶体为0.01
2 2
mol,350 ℃左右所得固体质量为0.56 g,根据钙原子守恒,可知为CaO。
12.(1)17% (2)
13.(1)2Fe2++HO+2H+===2Fe3++2HO 减小
2 2 2
(2)①偏大 ②12.32%
解析 (1)H O 氧化后的溶液为 Fe (SO ) 溶液,Fe (SO ) 发生水解反应:Fe (SO ) +(6-
2 2 2 4 3 2 4 3 2 4 3
2n)H OFe (OH) (SO ) +(3-n)H SO ,Fe (OH) (SO ) 聚合得到聚合硫酸铁,根据水
2 2 6-2n 4 n 2 4 2 6-2n 4 n
解方程式知水解聚合反应会导致溶液的酸性增强,pH减小。(2)①根据题意,Sn2+能将Fe3+
还原为Fe2+,发生的反应为Sn2++2Fe3+===Sn4++2Fe2+,则还原性:Sn2+>Fe2+,实验中若
不除去过量的Sn2+,则加入的KCr O 先氧化过量的Sn2+再氧化Fe2+,导致消耗的KCr O
2 2 7 2 2 7
溶液的体积偏大,则样品中铁的质量分数的测定结果将偏大。②实验过程中消耗的n(CrO)
2
=5.000×10-2 mol·L-1×22.00×10-3 L=1.100×10-3mol,根据得失电子守恒得滴定时反应
的离子方程式为Cr O+6Fe2++14H+===6Fe3++2Cr3++7HO,可得微粒的关系式:Cr O~
2 2 2
6Fe2+,则n(Fe2+)=6n(CrO)=6×1.100×10-3mol=6.6×10-3mol,根据Fe元素守恒,样品
2
中铁元素的质量m(Fe)=6.6×10-3mol×56 g·mol-1=0.369 6 g,样品中铁元素的质量分数
w(Fe)=×100%=12.32%。
第三章 化学实验基础知识
第 8 练 化学实验基础知识和技能
1.B 2.A 3.A4.A [检测气体的酸碱性时需要润湿pH试纸,而测定溶液的pH时不需要润湿,故A错误;
硫易溶于CS ,则可用CS 洗去试管内壁上残留的硫,故B正确;碘不易溶于水,易溶于苯
2 2
或四氯化碳,则可用苯代替四氯化碳萃取碘水中的碘,故C正确;丁达尔效应为胶体特有
的性质,则用聚光手电筒照射CuSO 溶液和Fe(OH) 胶体时,产生的现象不同,故D正
4 3
确。]
5.C [银单质与氨水不反应,可用稀硝酸清洗,A不符合题意;油脂在碱性环境下水解生
成高级脂肪酸盐和甘油,高级脂肪酸盐和甘油都能溶于水而洗去,反应中没有元素化合价变
化,不属于氧化还原反应,B不符合题意;二氧化锰与热的浓盐酸反应生成氯气、氯化锰和
水,不溶性的二氧化锰转化为可溶性的氯化锰而洗去,反应中氯元素、锰元素的化合价发生
变化,属于氧化还原反应,C符合题意;碘能溶于酒精形成溶液,因此附有碘的试管用酒精
清洗,但属于物理变化,D不符合题意。]
6.A 7.A 8.A 9.D
10.B [NaH、CaC 均易与水反应,所以应密封保存,A正确;液溴和少量白磷保存时均加
2
水液封,前者是为了防止液溴挥发,后者是为了防止白磷与空气中的氧气反应,B错误;
FeCl 中的Fe2+易被氧化、易水解,保存时,加入铁屑可防止 Fe2+被氧化,加入稀盐酸可抑
2
制Fe2+水解,C正确;NaF水解可产生HF,HF易与玻璃中的SiO 反应,所以HF溶液和
2
NaF溶液都应用塑料瓶盛装,D正确。]
11.D [将黑木耳灼烧灰化,应该在坩埚中灼烧,选用的仪器有①②⑥⑦⑨,故A正确;
用胶头滴管把浓硝酸滴入木耳灰中,使木耳灰溶解,用过滤的方法获得滤液,选用的仪器有
④⑤⑦⑩,故B正确;检验滤液中的Fe3+,取少量滤液于试管中,用胶头滴管滴加几滴
KSCN溶液,若溶液变红说明含有Fe3+,选用③⑧⑩,故C正确;进行硫酸铜结晶水含量的
测定需要称重,缺少天平,故D错误。]
12.D
13.B [从海带中提取I ,需要灼烧、溶解、氧化、过滤,使用的玻璃仪器有酒精灯、漏斗
2
玻璃棒、烧杯、分液漏斗,需要的试剂有蒸馏水、新制氯水、CCl ,仪器缺少漏斗,A不符
4
合题意;乙醛的银镜反应需热水浴加热,用胶头滴管向盛有银氨溶液的试管中滴加乙醛溶液,
然后将该试管放入热水浴中进行反应,故使用到的玻璃仪器有烧杯、酒精灯、试管、胶头滴
管,试剂有乙醛溶液、银氨溶液,B符合题意;用一个干燥的烧瓶收集氨气,并用带有玻璃
导管和胶头滴管(事先吸有水)的双孔塞塞紧,导管末端放入盛有水的烧杯中,当实验时,将
止水夹移到玻璃管处,挤压胶头滴管,使少量水进入烧瓶中,就会形成压强差而形成喷泉,
仪器缺少胶头滴管,C不符合题意;用95%的乙醇制取无水乙醇时,需将95%的乙醇、生石
灰混合加热,用温度计测量蒸气温度,用冷凝管冷却降温,冷凝管与接收器锥形瓶通过牛角
管连接,仪器缺少温度计,药品缺少生石灰,D不符合题意。]
14.(1)容量瓶 (直形)冷凝管 (2)②⑥ (3)试管(4)②④⑧⑨ (5)⑧⑨ (6)B (7)砝码放在左盘,烧杯放在右盘(或砝码和烧杯的位置放反了)
27.4 (8)胶头滴管伸入试管内 试管口向上倾斜 混合气体从短导管进入洗气瓶
第 9 练 物质的分离与提纯
1.A 2.C 3.A
4.C [①加入氯化铁,生成KCl,引入新杂质,应加入硝酸铁除杂,错误;②铁可置换出
铜,可除去杂质,正确;③二氧化碳与氢氧化钠溶液反应,可除去杂质,干燥后得到纯净的
氢气,正确;④碳酸钙不溶于水,可用过滤的方法除去,正确。]
5.A [乙酸乙酯与饱和碳酸钠溶液分层,可以采用分液法进行分离,A 项正确;
FeSO ·7H O易被氧化,且蒸干易分解,应该采用蒸发浓缩、冷却结晶的方法来制备,B项
4 2
错误;硫酸铜溶液经蒸发浓缩、冷却结晶可得到CuSO ·5H O,但仪器应选蒸发皿,C项错
4 2
误;应采用萃取、分液、蒸馏的方法得到I,D项错误。]
2
6.A 7.B 8.B
9.A [NaCO 溶液也能吸收CO ,应用饱和NaHCO 溶液除去CO 中的HCl,故A错误;
2 3 2 3 2
由于KNO 的溶解度受温度影响较大,故可采用蒸发结晶、趁热过滤的方法分离KNO 和
3 3
NaCl,故B正确;碱石灰可除去H 中的HCl和HO(g),故C正确;碱石灰能干燥NH ,故
2 2 3
D正确。]
10.C [浓硫酸与铜反应需要加热,装置甲中没有酒精灯,无法反应制取 SO ,故A错误;
2
胶头滴管使用时应悬于容量瓶上方,不能伸入容量瓶内,会污染试剂,故B错误;灼烧
CoCO 固体应用坩埚,故D错误。]
3
11.B 12.A
13.(1)防止CuO颗粒穿过滤纸或防止滤纸破损
(2)取少量最后一次洗涤液于试管中,滴加BaCl 溶液,若无白色沉淀产生,说明洗涤干净
2
14.(1)B (2)③④②(或④②③或④③②)
(3)KOH + HCl===KCl + HO、KCO +2HCl===2KCl+HO+CO ↑ (4)取少量液体Ⅱ
2 2 3 2 2
于试管中,滴加氯化钡溶液,若无沉淀生成,则SO已沉淀完全
第四章 金属及其化合物
第 10 练 碱金属 钠及其氧化物
1.C 2.D 3.C4.B [金属钠失电子均变为+1价的阳离子,等质量的两块钠,失电子数是一样的;根据
反应:4Na+O===2NaO,1 mol金属钠完全反应得氧化钠的质量是31 g,根据反应:2Na
2 2
+O=====NaO 1 mol金属钠完全反应得过氧化钠的质量是39 g,故等质量的两块钠,生成
2 2 2,
过氧化钠的质量大,即第一块钠的反应产物质量大。]
5.B [金属钠和二氧化碳反应生成金刚石,反应中碳元素化合价降低、钠元素化合价升高,
钠作还原剂,二氧化碳发生还原反应,故A、C正确;钠与二氧化碳反应生成金刚石和氧化
钠,氧化钠和二氧化碳反应生成碳酸钠,故B错误,D正确。]
6.D 7.A
8.D [Na O 与水反应生成氢氧化钠和氧气,溶液呈碱性,HCO与OH-反应生成CO,则
2 2
②HCO浓度减小,④CO浓度增大;NaO 具有强氧化性,将SO氧化为SO,则③SO浓度
2 2
减小,⑤SO浓度增大;①NO浓度基本不变,故选D。]
9.B
10 . C [H 、 CO 发 生 反 应 的 化 学 方 程 式 分 别 为 2H + O=====2HO,2Na O +
2 2 2 2 2 2
2HO===4NaOH+O↑;2CO+O=====2CO 2NaO +2CO===2NaCO +O ,则过氧化钠
2 2 2 2, 2 2 2 2 3 2
增加的质量即为H、CO的质量。因此只要是CO或H 或它们的混合气体或化学式组成符合
2 2
(CO) ·(H ),过氧化钠固体增重的质量就等于原物质的质量,则①②符合;而④HCHO可以
m 2 n
改写成CO·H ,⑤CHCOOH可以改写成(CO) ·(H ) ,⑥HCOOH可以改写成CO·H ,故
2 3 2 2 2 2 2
①②④⑤符合。]
11.D
12.D [KO 中K元素显+1价,则O元素显-价,A错误;KO 是由K+和O构成的,其
2 2
阴、阳离子个数之比为 1∶1,B 错误;KO 与 CO 反应的化学方程式为 4KO +
2 2 2
2CO===2KCO+3O Δm=8,即4 mol KO 完全反应,固体质量减少8 g,则1 mol KO 与
2 2 3 2 2 2
CO 反应后,固体质量减少2 g,C错误;KO 和NaO 分别与足量水反应的化学方程式为
2 2 2 2
4KO +2HO===4KOH+3O↑、2NaO +2HO===4NaOH+O↑,所以当=1时,生成O
2 2 2 2 2 2 2 2
的物质的量之比为3∶2,D正确。]
13.(1)饱和碳酸氢钠 (2)C (3)5 变浑浊
(4)①2Na+2CO=====NaCO+CO ②4Na+3CO=====2NaCO+C
2 2 3 2 2 3
14.(1)2Na O +2CO===2NaCO +O 、2NaO +2HO===4NaOH+O↑ (2)①长颈漏斗
2 2 2 2 3 2 2 2 2 2
吸收氢气中的杂质气体(或除去氢气中的水蒸气和氯化氢气体) ②检验氢气纯度 ③检验是
否有水生成 ④NaO+H=====2NaOH
2 2 2
第 11 练 碳酸钠和碳酸氢钠 钠及其化合物的相互转化
1.C 2.B 3.D4.B [CO、HCO发生水解,溶液显碱性,相同浓度下,CO的水解程度比HCO的大,所
以相同浓度和体积的NaCO 溶液和NaHCO 溶液,pH(Na CO)>pH(NaHCO ),故A正确;
2 3 3 2 3 3
实验后,碳酸钠溶液和氯化钙溶液恰好反应生成碳酸钙沉淀和氯化钠,溶液中的离子主要有
Na+、Cl-,而碳酸氢钠溶液和氯化钙溶液反应生成碳酸钙沉淀、氯化钠、水和二氧化碳,
氯化钙有剩余,溶液中的离子主要有Na+、Cl-、Ca2+,故两者的离子种类不完全相同,故
B错误;加入氯化钙后,左侧试管中只有白色沉淀生成,则反应的化学方程式为 NaCO +
2 3
CaCl ===CaCO ↓+2NaCl,右侧试管中有白色沉淀和无色气体产生,则反应的化学方程式
2 3
为2NaHCO +CaCl ===CaCO ↓+2NaCl+CO↑+HO,由化学方程式可知起始CO、HCO
3 2 3 2 2
的物质的量相同时,NaCO 溶液中生成的沉淀比NaHCO 溶液中生成的沉淀多,故C正确;
2 3 3
两试管中发生的反应均为复分解反应,故D正确。]
5.B 6.A
7.B [二氧化碳与氢氧化钠反应生成碳酸钠和水,则反应③表明CO 具有酸性氧化物的性
2
质,故A正确;碳酸氢钠受热分解生成碳酸钠,则反应④说明NaCO 的热稳定性强于
2 3
NaHCO ,故B错误;过氧化钠与水、二氧化碳反应生成氧气,可用于潜水艇中氧气的供给,
3
故C正确;④是分解反应,①是化合反应,②是置换反应,故D正确。]
8.D [为了防止空气中的二氧化碳对实验的影响,需先通过装置 A吸收空气中的二氧化碳,
则装置 A 中的试剂为 NaOH 溶液,C 中的试剂应能与二氧化碳反应生成沉淀,应为
Ba(OH) 溶液,故A错误;若B、C之间添加饱和NaHCO 溶液的洗气瓶,挥发出的HCl气
2 3
体会和NaHCO 反应生成CO 气体,对测定纯碱纯度会有影响,故B错误;盐酸易挥发,B
3 2
中可能有HCl、HO进入C中,不能通过测定C的质量差来确定CO 的质量,应通过测量C
2 2
中产生的沉淀质量来确定碳酸钠的质量分数,故C错误;沉淀表面可能附着少量水分和溶
于水的杂质,应经过过滤、洗涤、干燥、称量等操作测定装置C中沉淀质量,故D正确。]
9.B
10.D [由175 mL到275 mL是盐酸与碳酸氢钠反应,则n(Na CO)=n(NaHCO )=n(CO)
2 3 3 2
=0.02 mol,根据关系式NaHCO ~HCl可得,c(HCl)==0.2 mol·L-1,A正确;由图像可知,
3
因为175>275-175,所以固体混合物为NaOH、NaCO ,B正确;分析可知,反应后的固
2 3
体中n(Na CO)∶n(NaOH)=4∶3,再根据反应后固体溶于水无气体放出,则发生反应:
2 3
2NaHCO =====NaCO + CO↑ + HO 、 2NaO + 2CO===2NaCO + O 、 2NaO +
3 2 3 2 2 2 2 2 2 3 2 2 2
2HO===4NaOH+O↑,密闭容器中排出气体的成分为O 和HO,C正确;根据碳原子守
2 2 2 2
恒可知,n(NaHCO )=n(CO) =0.02 mol,盐酸体积为275 mL时溶质是单一的氯化钠,根
3 2
据钠原子守恒可知n(Na O)==0.017 5 mol,固体的质量为(0.02×84) g+(0.017 5×78) g=
2 2
3.045 g,故x=3.045,D错误。]
11.D [Ⅱ和Ⅰ的pH曲线基本重合,说明加入的碳酸根离子只与石灰水中的钙离子反应,
不与氢氧根离子反应,反应的离子方程式为CO+Ca2+===CaCO ↓,故B正确;Ⅲ的pH曲
3线逐渐降低,说明反应开始时,少量的碳酸氢钠与石灰水反应生成碳酸钙沉淀、氢氧化钠和
水,反应的离子方程式为HCO+OH-+Ca2+===CaCO ↓+HO,故C正确;石灰水恰好完
3 2
全反应时,碳酸氢钠与石灰水反应生成碳酸钙沉淀、碳酸钠和水,碳酸钠是强碱弱酸盐,在
溶液中水解使溶液呈碱性,故D错误。]
12.(1)淡黄 (2)2NaHCO =====NaCO+HO+CO↑ (3)点燃的蚊香燃烧更剧烈 制氧剂
3 2 3 2 2
13.(1)①CD ②防倒吸 ③NH 在水中溶解度大,而CO 在水中溶解度小,先通入NH ,
3 2 3
可提高CO 利用率 ④控制氨气(或CO)的通入量 (2)①碳酸氢钠溶液碱性相对较弱,可防
2 2
止生成碱式碳酸镧 ②2La3++3HCO===La(CO)↓+3H+
2 3 3
14.(1)Na CO 分液漏斗 除去CO 中的水蒸气 (2)①液面上升 ②体积 (3)①过滤 称
2 3 2
量 ②×100%
解析 (2)①将针筒活塞向内推压,增大了容器中的压强,若仪器b下端玻璃管中的液面上
升,则装置气密性良好。②CO 是气体,故能直接测得的数据是 CO 的体积。(3)根据
2 2
NaCO +Ba(OH) ===BaCO ↓+2NaOH,n(Na CO)=n(BaCO)= mol,所以NaCO 的质量
2 3 2 3 2 3 3 2 3
分数为×100%。
第 12 练 铁及其氧化物和氢氧化物
1.C 2.A
3.C [铁的三种氧化物中,氧元素的化合价都为-2价;铁元素的化合价不同,氧化铁中
铁为+3价,氧化亚铁中铁为+2价,四氧化三铁中铁为+2价和+3价;氧化铁俗称铁红,
是一种红棕色粉末;铁在氧气中燃烧生成四氧化三铁,是一种黑色固体。]
4.D [氢氧化铁和硫酸反应生成硫酸铁和水,A项错误;铁和盐酸反应生成氯化亚铁和氢
气,B项错误;氧化亚铁和盐酸反应生成氯化亚铁和水,C项错误;氧化铁和盐酸反应生成
氯化铁和水,可以制备氯化铁溶液,D项正确。]
5.C 6.D
7.D [准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得水,获得水的
2
准确质量,计算得到氧元素的质量和铁元素的质量,依据铁元素和氧元素物质的量之比确定
化学式,能计算得到物质组成,故 A不选;准确称量一定质量的黑色粉末,溶解于足量盐
酸,加热蒸干溶液并在空气中灼烧至质量不变,称量所得粉末质量,即氧化铁的质量,依据
铁元素和氧元素守恒计算铁元素和氧元素物质的量之比,判断氧化物的化学式,能计算得到
物质组成,故B不选;准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却
后准确称量剩余固体的质量,依据铁元素和氧元素质量守恒计算铁元素和氧元素物质的量之
比,分析判断氧化物的存在形式,能计算得到物质组成,故C不选;准确称量一定质量的
黑色粉末,与一定质量铝粉混合后点燃,充分反应后冷却,准确称量剩余固体质量,反应前后都是固体,反应前后固体质量不变,不能计算确定该黑色粉末的成分,故D选。]
8.C 9.B 10.C
11.C [“氧化Ⅰ”中主要发生的是铁和水蒸气在高温条件下生成四氧化三铁和 H 的反应,
2
则M为Fe O ,A正确;甲烷中碳元素是-4价,二氧化碳中碳元素是+4价,因此“干重
3 4
整”时有可能生成单质碳,装置中可能出现积碳,B正确;“氧化Ⅱ”中发生的主要反应是
O +4Fe O=====6Fe O ,C错误;根据题图和已知信息可判断该过程能有效实现温室气体
2 3 4 2 3
(CH、CO)的回收利用,D正确。]
4 2
12.C [根据两套装置中各仪器的功能,可以判断出A中放置普通铁粉,B中放一定体积的
水,持续加热提供水蒸气,C是安全瓶,用于防倒吸,D是利用排水集气法收集氢气。E中
反应物为A中生成的四氧化三铁,I中放置普通铁粉,通过分液漏斗加入一定体积的盐酸制
备H ,从I中逸出的气体中含有挥发出的氯化氢,经过G(内有碱石灰)除杂干燥后得到纯净
2
的氢气,氢气进入E中和Fe O 在一定温度下进行反应,得到“引火铁”,剩余的氢气在F
3 4
处进行收集或其他处理。]
13.(1)关闭a,从球形漏斗口加水,待水从漏斗管上升与容器的水面形成一段水柱差,停止
加水,静置片刻,如水柱不下降,证明其气密性良好 (2)在b出口处检验氢气的纯度
(3)除去H 中混有的HCl气体 浓硫酸 干燥氢气
2
(4)Fe O+3H=====2Fe+3HO、FeO+H=====Fe+HO
2 3 2 2 2 2
(5)16 g
14.(1)抑制Fe3+的水解 (2)铁粉逐渐溶解,有无色气体生成,溶液由棕黄色逐渐变为浅绿
色 (3)ACBD 将装置中的氨气全部排入装置D中被吸收,防止拆除装置时残留的氨气逸
出污染空气 (4)Fe2++2NH +2HO===Fe(OH) ↓+2NH 作安全瓶,防倒吸 (5)1∶2
3 2 2
FeO·Fe O·4H O (6)取少量灰绿色物质于试管中,加入稀盐酸(或稀硫酸)溶解,将溶液分成
2 3 2
两份,一份滴入几滴KSCN溶液,变为红色;另一份加入适量K[Fe(CN) ]溶液,生成蓝色
3 6
沉淀,则灰绿色物质中含Fe (OH)
3 8
解析 (3)制备氢氧化亚铁的装置中,A装置中将浓氨水滴到生石灰上,使生石灰和水反应
放出热量,使氨气逸出,一开始通入氮气的作用是将装置中的空气全部排出,B装置的作用
是使氨气和新制硫酸亚铁溶液反应产生氢氧化亚铁,C装置的作用是作为安全瓶,防止倒吸,
D装置的作用是吸收尾气,故装置连接顺序为A→C→B→D。(6)要设计实验证明灰绿色物
质中含Fe (OH) ,即要证明此物质中既有Fe2+又有Fe3+,Fe2+用K[Fe(CN) ]溶液检验,Fe3+
3 8 3 6
用KSCN溶液检验。第 13 练 铁盐、亚铁盐 铁及其化合物的转化
1.A
2.C [铁可用于湿法炼铜:Fe+Cu2+===Fe2++Cu,是因为铁的还原性大于铜,与Fe有导
电性无关,故不选A;FeCl 可用于净水,是因为Fe3+水解生成的氢氧化铁胶体能吸附水中
3
的悬浮杂质,与FeCl 的氧化性无关,故不选B;Fe O 呈红棕色,可用于制作红色颜料,故
3 2 3
选C;KFeO 可用于杀菌消毒,是因为KFeO 具有强氧化性,与KFeO 的溶解性无关,故
2 4 2 4 2 4
不选D。]
3.C 4.D
5.B [FeCl 溶液中Fe3+水解:Fe3++3HOFe(OH) +3H+,且将NaS溶液逐滴加入等
3 2 3 2
物质的量浓度的FeCl 溶液中,发生反应:2Fe3++S2-===2Fe2++S↓,由此看出Fe3+在酸性
3
环境中氧化性较强,故A正确;NaS溶液中S2-水解:S2-+HOHS-+OH-(主要)、HS
2 2
-+HOHS+OH-(少量),将FeCl 溶液逐滴加入等物质的量浓度的NaS溶液中,发生
2 2 3 2
反应:2Fe3++3S2-===Fe S↓,没有生成硫单质,S2-在碱性环境中还原性较弱,故B错误
2 3
由于将 FeCl 溶液逐滴加入等物质的量浓度的 NaS 溶液中,发生反应:2Fe3++3S2-
3 2
===Fe S↓,不生成Fe(OH) ,说明相同温度下Fe(OH) 的溶解度比Fe S 的大,故C正确;
2 3 3 3 2 3
向FeCl 溶液中通入HS,硫离子被铁离子氧化成硫单质,有硫析出,故D正确。]
3 2
6.C
7.B [铁和盐酸反应生成氯化亚铁和氢气,所以B中收集到的气体是氢气,A项正确;双
氧水具有氧化性,可将Fe2+氧化为Fe3+,B项错误;氧化铁为碱性氧化物,可与盐酸反应生
成氯化铁和水,C项正确;因铁离子易水解,故FeCl 溶液应在氯化氢气氛下,经蒸发浓缩、
3
冷却结晶、过滤后得到氯化铁晶体,D项正确。]
8.C [Mg与FeCl 反应生成FeCl ,过量Mg可与FeCl 反应置换出Fe,过滤可分离,A正
3 2 2
确;加入过量铁粉,FeCl 与Fe反应生成FeCl ,过滤可达到除杂的目的,B正确;加入
3 2
NaOH溶液,Cu2+、Fe3+均能转化成氢氧化物沉淀,不符合除杂要求,C错误;HO 可将
2 2
Fe2+氧化成Fe3+,加CuO可促进铁离子水解转化成Fe(OH) 沉淀,过滤可分离,D正确。]
3
9.C 10.C
11.A [由题意知铁离子、银离子均被还原,氧化性:Zn2+<Cu2+<Fe3+<Ag+,A错误、
B正确;Fe先还原Ag+,发生的反应为2Ag++Fe===Fe2++2Ag,然后发生反应:Fe+2Fe3
+===3Fe2+,所以n(Fe2+)∶n(Cu2+)=(0.05+0.15) mol∶0.1 mol=2∶1,C正确;由Fe+2Fe3
+===3Fe2+可知,1 mol Fe恰好还原2 mol Fe3+,D正确。]
12.C [操作①是过滤,过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗,故 A正确;该流程
中试剂B的作用是将Fe2+氧化成Fe3+,酸性高锰酸钾溶液和稀硝酸都可以将Fe2+氧化成Fe3+,但都会引入新杂质,故C错误;由D→E的化学方程式可知反应中生成的二氧化硫可将
氯化铁还原为氯化亚铁,若是SO 作还原剂,则氧化产物为硫酸盐,故取样溶解后,先加盐
2
酸酸化,再加BaCl 溶液,产生白色沉淀,则可证明二氧化硫将Fe3+还原,故D正确。]
2
13.(1)防止Fe2+被氧化 (2)2Fe2++Cl===2Fe3++2Cl- (3)隔绝空气(排除氧气对实验的影
2
响) (4)Fe2+ Fe3+ 可逆反应 (5)H O+2Fe2++2H+===2Fe3++2HO Fe3+催化HO 分解
2 2 2 2 2
产生O HO 分解反应放热,促进Fe3+的水解平衡正向移动
2 2 2
14.(1)Fe O 和SiO SiO (2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
2 3 2 2
(3)7Fe (SO )+FeS+8HO=====15FeSO +8HSO (4)蒸发浓缩、冷却结晶、过滤洗涤 (5)
2 4 3 2 2 4 2 4
+2 6Fe(NH )Fe(CN) +ClO+6H+=====6Fe(NH )Fe(CN) +Cl-+3HO+6NH (6)H O
4 2 6 4 6 2 2 2
NH ·H O
3 2
解析 已知黄铁矿高温煅烧生成Fe O ,反应为4FeS +11O=====2Fe O +8SO ,故产生的
2 3 2 2 2 3 2
红渣主要成分为Fe O 和SiO ;将红渣粉碎后加入足量的50%的HSO 溶液加热,反应为
2 3 2 2 4
Fe O +3HSO ===Fe (SO ) +3HO,过滤出滤渣①,主要成分为SiO ,向滤液中加入黄铁
2 3 2 4 2 4 3 2 2
矿进行还原,将Fe3+还原为Fe2+,由(3)小问可知不生成S单质,则硫元素被氧化为SO,反
应为14Fe3++FeS +8HO=====15Fe2++2SO+16H+,然后进行工序①为蒸发浓缩、冷却结
2 2
晶、过滤,得到FeSO 晶体和母液,母液中主要含有FeSO 溶液和HSO ,加水溶解FeSO
4 4 2 4 4
晶体,向所得溶液中加入(NH )SO 、K[Fe(CN) ]并用HSO 调节溶液的pH为3,进行沉铁,
4 2 4 4 6 2 4
反应原理为Fe2++2NH+[Fe(CN) ]4-===Fe(NH )Fe(CN) ↓,然后过滤出沉淀,洗涤后加入
6 4 2 6
HSO 和NaClO 进行氧化,反应为6Fe(NH )Fe(CN) +ClO+6H+=====6Fe(NH )Fe(CN) +Cl
2 4 3 4 2 6 4 6
-+3HO+6NH,过滤、洗涤、干燥即制得Fe(NH )Fe(CN) ,据此分析解题。
2 4 6
第 14 练 铝、镁及其化合物
1.C 2.D
3.C [可溶性的铝盐Al (SO ) 溶液与少量NaOH溶液反应生成氢氧化铝沉淀,继续加过量
2 4 3
的氢氧化钠溶液,氢氧化铝沉淀会溶解,氢氧化铝沉淀中加盐酸也会溶解。]
4.C [铝与NaOH溶液反应的离子方程式为2Al+2OH-+2HO===2AlO+3H↑,A错误;
2 2
Al O 与NaOH溶液反应的离子方程式为Al O +2OH-===2AlO+HO,B错误;明矾溶于水
2 3 2 3 2
后电离产生的铝离子发生水解,产生的氢氧化铝胶体能吸附悬浮物,起到净水作用,C正确;
一水合氨为弱碱,故氢氧化铝无法与一水合氨发生反应。 ]
5.B 6.D
7.A [MgCO 是微溶物,不可拆成离子,故A错误;SiO 不溶于盐酸,浸出渣为SiO ,故
3 2 2
B正确;加入氨水沉镁:MgCl +2NH ·H O ===Mg(OH) ↓+2NH Cl,母液的主要溶质是
2 3 2 2 4
NH Cl,故C、D正确。]
48.D [向NaAlO 溶液中通入CO 气体,发生反应生成Al(OH) ,Al(OH) 不稳定,受热分
2 2 3 3
解产生Al O ,在上述转化过程中无元素化合价的变化,因此涉及的反应均为非氧化还原反
2 3
应,A正确;Al O 是两性氧化物,与NaOH溶液反应产生NaAlO 和水,B正确;酸性:
2 3 2
HCO >Al(OH) ,向NaAlO 溶液中通入过量CO 气体,反应产生Al(OH) 、NaHCO ,该反
2 3 3 2 2 3 3
应的离子方程式为AlO+CO +2HO===Al(OH) ↓+HCO,C正确;电解熔融Al O 时,阳
2 2 3 2 3
极上O2-失去电子变为O,电极反应式为2O2--4e-===O↑,D错误。]
2 2
9.C
10.B [冷凝管起到冷凝回流的作用,冷凝管内冷却水的方向为下进上出,则 a为冷却水进
水口,故A正确;MgBr 具有较强的吸水性,制备无水MgBr ,需要防止空气中的水蒸气进
2 2
入三颈烧瓶,则装置A的作用是吸收水蒸气,但无水CaCl 不能吸收溴蒸气,故B错误;制
2
取MgBr 的反应剧烈且放出大量的热,实验时利用干燥的氮气将溴蒸气带入三颈烧瓶中,为
2
防止反应过于剧烈,实验时需缓慢通入N ,故C正确;不能用干燥空气代替N ,空气中含
2 2
有的氧气可将镁氧化为副产物MgO,会阻碍反应的进行,故D正确。]
11.D [镓(Ga)与铝同主族,均位于第ⅢA族,A项正确;GaO 与Al O 的性质相似,可
2 3 2 3
与盐酸反应生成GaCl ,B项正确;Ga(OH) 属于两性氢氧化物,与Al(OH) 的性质相似,能
3 3 3
与 NaOH 溶液反应生成 NaGaO ,C 项正确;在 NaAlO 和 NaGaO 的混合液中通入适量
2 2 2
CO,只有Al(OH) 沉淀,而没有Ga(OH) 沉淀,根据强酸制弱酸的原理,Ga(OH) 的酸性强
2 3 3 3
于碳酸,则酸性:Al(OH) ClO ;吸收塔内
3 2 2
ClO 与双氧水、氢氧化钠反应生成NaClO 和氧气,ClO 作氧化剂,HO 作还原剂,则氧化
2 2 2 2 2
性:ClO >H O,故氧化性:ClO>ClO >H O,故B正确。]
2 2 2 2 2 2
5.B [①为制取C NOClNa的装置,②为除去氯气中的HCl的装置,③为尾气处理装置,
3 3 3 2
④为制取氯气装置,按气流从左至右,导管连接顺序为f→c→d→a→b→e,A正确;升高温
度,氯气和NaOH溶液反应生成NaClO ,生成NaClO的浓度减小,不利于装置①中产品的
3
生成,B错误;由Cl+2NaOH===NaCl+NaClO+HO、2NaClO+C HNO===C NOClNa
2 2 3 3 3 3 3 3 3 2
+NaOH+H O,可得关系式:4NaOH~2NaClO~C H N O ,加入4 mol NaOH时,可消耗
2 3 3 3 3
1 mol C HNO,由于生成了NaOH,则消耗氰尿酸的量大于1 mol,C正确。]
3 3 3 3
6.D [氯气与热的石灰乳反应生成Ca(ClO ) 、CaCl ,制备漂白粉不能用热的石灰乳和氯
3 2 2
气反应,故A错误;若反应①中n(ClO-)∶n(ClO)=3∶1,根据得失电子守恒,反应的化学
方程式为6Cl +12KOH===8KCl+3KClO+KClO +6HO,则该反应还原产物与氧化产物的
2 3 2物质的量之比为2∶1,故B错误;若反应①中不生成KClO ,得到2 mol K FeO 转移6 mol
3 2 4
电子,根据得失电子守恒,消耗3 mol Cl ,由于反应①中生成KClO,所以消耗氯气的物质
2 3
的量最少为3 mol,故C错误;KFeO 具有强氧化性,能杀菌消毒,同时还原产物Fe3+发生
2 4
水解生成氢氧化铁胶体,能吸附悬浮杂质,所以处理饮用水时,加入高铁酸钾效果相当于加
入氯气和铝盐两种物质,故D正确。]
7.B 8.C 9.D 10.C
11.C [根据题意分析,气体A为H ,故A错误;在NCl 溶液中加入NaClO 溶液加热反
2 3 2
应生成ClO 、NH 和溶液B,由氢元素守恒可知,有水参加反应,结合得失电子守恒、原子
2 3
守恒和电荷守恒可知,反应还生成 NaCl 与 NaOH,化学方程式为 6NaClO +NCl +
2 3
3HO===3NaCl+6ClO ↑+NH ↑+3NaOH,参加反应的NaClO 和NCl 的物质的量之比为
2 2 3 2 3
6∶1,故B错误;根据上述分析可知,溶液B中含有NaCl与NaOH,则含有大量的Na+、
Cl-、OH-,故C正确;二氧化氯(ClO )是一种黄绿色、易溶于水的气体,不可用饱和食盐
2
水除去ClO 中的NH ,故D错误。]
2 3
12.D [尾气含有氯气,与氯化亚铁反应生成氯化铁,可再利用,故 B正确;反应中Cl元
素化合价由+1价降低为-1价,Fe元素化合价由+3价升高到+6价,则氧化剂与还原剂的
物质的量之比为3∶2,故C正确;结晶过程中加入饱和KOH溶液,增大了K+浓度,该温
度下,高铁酸钾的溶解度比高铁酸钠的溶解度小,有利于KFeO 晶体的析出,故D错误。]
2 4
13.(1)MnO +4H++2Cl-=====Mn2++Cl↑+2HO (2)防止空气中的水蒸气进入E装置
2 2 2
吸收未反应完的氯气,防止污染空气 在瓶E和F之间连接装有干燥剂的装置
14.(1)2KClO +HC O=====KCO +2ClO ↑+CO↑+HO 盛有冰水混合物的水槽
3 2 2 4 2 3 2 2 2
(2)C C处为密封装置,气体不能排出,可导致仪器炸裂 (3)2ClO +2OH-===ClO+ClO+
2
HO 80.0 g 500 mL容量瓶、烧杯
2
第 18 练 卤族元素 溴、碘单质的提取
1.B 2.C
3.C [NaCN溶液呈碱性说明HCN 为弱酸, A正确;类比卤素单质,(CN) 也可与烯烃发
2
生加成反应,B正确;由题干可知还原性:Br-<CN-<I-,C项反应不能发生;类比氯气
与氢氧化钠的反应推知D正确。]
4.C [易被氧化的物质应具有较强的还原性,卤素离子中,I-的还原性最强,故卤素的钾
盐中,最易被氧化的是KI,①错误;卤化银中除AgF外均有感光性,③错误;能与淀粉-KI
溶液反应出现蓝色现象的除氯水或溴水外,还可以是过氧化氢等,④错误。]
5.D
6.C [实验1中,浓硫酸与氯化钠反应生成氯化氢气体,氯化氢与氨气反应生成 NH Cl固
4体,故A合理;实验1溶液颜色无明显变化说明浓硫酸不能氧化氯离子,实验2溶液变黄说
明浓硫酸能氧化溴离子,所以判断还原性:Br->Cl-,故B合理;②中溶液含有浓硫酸和
溴单质,均能将碘化钠氧化成碘单质,不能判断还原性:I->Br-,故C不合理;实验1体
现浓硫酸的难挥发性,实验2体现浓硫酸的氧化性,故D合理。]
7.D
8.C [A项,向苦卤中通入Cl 时发生反应:Cl +2Br-===2Cl-+Br ,是为了提取溴,正
2 2 2
确;B项,将粗盐溶解、过滤除去难溶性杂质,然后向滤液中加入沉淀剂,过滤除去可溶性
杂质,最后重结晶可得精盐,正确;C项,工业生产常选用廉价的Ca(OH) 作为沉淀剂,错
2
误;D项,由于通入Cl 后所得溶液中Br 的浓度很小,因此利用Br 的挥发性,可先用热空
2 2 2
气和水蒸气吹出Br ,再用SO 将其还原为HBr进行富集,正确。]
2 2
9.B 10.C
11.D [流程中①和④所得溶液中的碘离子物质的量相同,为碘富集过程,c(I-)后者大于
前者,故A错误;流程中④为碘与亚硫酸钠发生氧化还原反应生成碘化氢和硫酸钠,离子
方程式为I +SO+HO===2I-+SO+2H+,故C错误;②中离子反应为Cl +2I-===I +2Cl
2 2 2 2
-,⑤中氯酸钾可氧化碘离子生成碘单质,离子反应为 6I-+ClO+6H+===3I +Cl-+
2
3HO,则得到等量的I 时消耗的n(Cl )∶n(KClO)=3∶1;制备10 mol I ,理论上需KClO
2 2 2 3 2 3
的物质的量为 mol,质量为122.5 g·mol-1× mol≈408 g,故B错误、D正确。]
12.(1)SO+I +HO===2I-+SO+2H+ 使CCl 中的碘进入水层 (2)分液 (3)使氯气在溶
2 2 4
液中有较大的溶解度(或防止I 升华或防止I 进一步被氧化) NaOH溶液 (4)从水层取少量
2 2
溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加FeCl 溶液,若溶液变蓝,说明废水中含
3
有I-,若溶液不变蓝,说明废水中不含有I-;另从水层取少量溶液,加入1~2 mL淀粉溶
液,加盐酸酸化,滴加NaSO 溶液,若溶液变蓝,说明废水中含有IO,若溶液不变蓝,说
2 3
明废水中不含有IO
13.(1) 除去Cl 中挥发出的HCl 3Br +3CO===5Br-+BrO+3CO↑ (2)5Br-+BrO+6H
2 2 2
+===3Br +3HO
2 2
(3)①使A中Br 进入B瓶中 ②NaOH溶液 ③导管中液面上升
2
第 19 练 硫及其氧化物
1.B 2.D 3.C
4.D [正交硫与单斜硫都是由硫元素组成的单质,所以两者互为同素异形体,A正确;由
结构示意图可知,S 分子中每个硫原子与2个硫原子形成共价键,则每个硫原子均满足8电
8
子稳定结构,B正确;同素异形体之间的转化属于化学变化,C正确。]
5.D [SO 分子中S原子为sp2杂化,孤电子对数为1,分子空间结构为V形,SO 为极性
2 2分子,SO 分子中S原子为sp2杂化,孤电子对数为0,分子空间结构为平面三角形,SO 为
3 3
非极性分子,A、C错误;SO 遇水迅速反应生成硫酸,SO 与HO不能形成分子间氢键,
3 3 2
但HSO 与HO能形成分子间氢键,B错误。]
2 4 2
6.C [A项,溶液中SO 被FeCl 氧化生成SO,再与BaCl 反应产生白色沉淀,体现了SO
2 3 2 2
的还原性;B项,SO 与HS溶液发生反应:SO +2HS===3S↓+2HO,体现了SO 的氧化
2 2 2 2 2 2
性;C项,SO 使酸性KMnO 溶液褪色,体现了SO 的还原性;D项,SO 与NaSiO 溶液
2 4 2 2 2 3
反应产生胶状沉淀,根据强酸制弱酸,则酸性:HSO >HSiO。]
2 3 2 3
7.B 8.A 9.B
10.B [由反应Ⅰ可知,SO 的氧化性强于I,由反应Ⅱ可知,I 的氧化性强于SO ,故可说
2 2 2 2
明SO 、I 的氧化性强弱与外界条件有关,A正确;由反应Ⅱ可知,每生成0.1 mol SO,转
2 2
移电子为0.2 mol,同时生成0.2 mol I-,反应0.1 mol I ,由反应Ⅰ可知生成0.1 mol I 消耗
2 2
0.2 mol I-,转移电子为0.2 mol,故整个过程中转移0.4 mol电子,不消耗KI,B错误;由
题干信息可知,反应Ⅰ+2反应Ⅱ可得该过程的总反应为3SO +2HO===2SO+S↓+4H+,
2 2
C正确;由C项分析可知,该反应过程中KI作催化剂,D正确。]
11.D
12.A [二氧化硫具有还原性,可以被氯水氧化为硫酸,但是氯水也可以和氢氧化钠反应,
所以试剂B不能选择NaOH标准液,A错误;若试剂A选择碱液,可以和二氧化硫反应得
到亚硫酸盐或亚硫酸氢盐,该盐可以被碘单质氧化为硫酸盐,试剂B可选择I 标准液,D正
2
确。]
13.(1)搅拌(或粉碎、加热)
(2)过滤
(3)NaHSO+NaOH===NaSO +HO
3 2 3 2
(4)Na SO 具有较强还原性,易被空气中的氧气氧化
2 3
(5)加入过量盐酸,再加入BaCl 溶液
2
14.(1)避免引入空气中的杂质,同时使煅烧更充分 SO (2)CD (3)①碱式滴定管 滴入
2
最后半滴NaOH溶液后,溶液由无色变为浅红色并保持30 s不褪色 ②0.032% (4)①还原
性 ②吸收CO 气体前后CO 吸收瓶的质量
2 2
解析 (2)为了防倒吸和安全起见,选择C或D装置。(3)①NaOH溶液应置于碱式滴定管中,
酚酞遇碱变红,当达到滴定终点时,硫酸被消耗完,故滴定终点的现象为滴入最后半滴
NaOH溶液后,溶液由无色变为浅红色并保持30 s不褪色。②由S~HSO ~2NaOH可知,
2 4
滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,即0.01 mol·L-1×2.0×10-3L=2.0×10-5 mol时,
钢样中硫的物质的量为1.0×10-5 mol,即质量为1.0×10-5 mol×32 g·mol-1=3.2×10-4g,
则该钢样中硫的质量分数为×100%=0.032%。(4)①MnO 和KCr O 都是强氧化剂,由此可
2 2 2 7
知该法利用了SO 的还原性。②对比CO 吸收瓶吸收二氧化碳前后的质量可以得出CO 的质
2 2 2量,从而知道钢样中碳的质量,进而求出钢样中碳的质量分数。
第 20 练 硫酸 硫酸盐
1.D 2.A
3.D [稀硫酸中硫酸完全电离,离子浓度较大,浓硫酸几乎没有电离,因此常温下测定两
溶液的导电能力,导电能力强的是稀硫酸,故 A错误;常温下,铜与稀硫酸和浓硫酸均不
反应,不能鉴别两种溶液,故B错误;常温下,铝片与稀硫酸反应能够产生气泡,铝遇浓
硫酸发生钝化,可以鉴别两种溶液,故C错误;浓硫酸具有吸水性,两溶液敞口在空气中
放置一段时间后质量明显增大的是浓硫酸,故D正确。]
4.D 5.C 6.C
7.D [98%的浓硫酸的主要成分是硫酸分子,溶液中氢离子浓度小,与亚硫酸钠固体的反
应速率慢,故B正确;二氧化硫与水反应生成亚硫酸,亚硫酸电离出的氢离子能与硫代硫
酸钠溶液反应,导致产率降低,所以制备硫代硫酸钠时,不能通入过量的二氧化硫,故D
错误。]
8.C [连二亚硫酸钠的还原性比NaSO 强,其水溶液能被空气中的氧气氧化,因此连二亚
2 3
硫酸钠可以用于除去废水中的重铬酸根离子,使Cr O转化为Cr3+,故A正确;连二亚硫酸
2
钠溶液能被空气中的氧气氧化,所以敞口放置可能会发生反应的化学方程式为2NaSO+O
2 2 4 2
+2HO===4NaHSO ,故B正确;连二亚硫酸钠用于纸浆漂白的原理与ClO 的漂白原理不
2 3 2
相同,因为前者具有还原性,后者具有强氧化性,故C错误;保险粉在碱性介质中相对稳
定,在包装保存保险粉时加入少量NaCO 固体,可以提高保险粉的稳定性,故D正确。]
2 3
9.A [①中有红棕色气体产生,此气体为Br ,浓硫酸作氧化剂把Br-氧化成Br ,②中有
2 2
白雾,此白雾是浓硫酸与NaCl反应生成的HCl的小液滴,Cl-没有被氧化,说明Br-的还原
性强于Cl-,故A正确、B错误;③中发生的反应为NaSO +HSO (浓)===NaSO +SO ↑
2 3 2 4 2 4 2
+HO,此反应不是氧化还原反应,故 C错误;Cu与浓硫酸反应生成CuSO 、SO 、HO,
2 4 2 2
利用浓硫酸的吸水性,溶液中应析出白色固体,故D错误。]
10.C 11.B
12.C [稀释至0.8 L时,c(H+)=0.2 mol·L-1,说明硫酸过量,反应的硫酸的物质的量为
(0.2×18.4-0.8×0.1) mol=3.6 mol,假设只生成SO ,发生的反应是Zn+2HSO (浓)=====
2 2 4
ZnSO +SO ↑+2HO,SO 的体积为(×22.4) L=40.32 L<44.8 L,说明除生成SO 外,还有
4 2 2 2 2
氢气生成,A正确;设生成SO 的物质的量为x mol,则氢气的物质的量为(2-x) mol,生成
2
SO 消耗的硫酸的物质的量为2x mol,生成氢气消耗的硫酸的物质的量为(2-x) mol,则根
2
据A选项的分析,有2x+2-x=3.6,解得x=1.6,氢气的物质的量为0.4 mol,转移电子的物质的量为(1.6×2+0.4×2) mol=4 mol,B正确;气体X中SO 与H 的体积比为4∶1,C
2 2
错误;根据得失电子守恒,消耗的锌的质量为2 mol×65 g·mol-1=130 g,D正确。]
13.(1)将三颈烧瓶中产生的NH 及时排出,减少副反应的发生
3
(2)①NaHSO HO ②2Cr3++3SO+7HO===6SO+Cr O+14H+
4 2 2 2 2 2
14.(1)把导管放入盛有水的水槽中,微热烧瓶,如果导管口有气泡产生,停止加热后导管
中产生一段水柱 (2)×100% (3)除去CO 中的SO 并检验SO 是否除尽
2 2 2
(4)在E的后边再连接一个与E相同的装置 (5)反应产生的CO 气体未能完全排到E中,导
2
致 b 偏低 (6)常温下,Fe 被浓 HSO 钝化,碳与浓 HSO 不反应 (7)2Fe +
2 4 2 4
6HSO (浓)=====Fe (SO ) + 3SO ↑ + 6HO
2 4 2 4 3 2 2
解析 (2)铁、碳在加热条件下与浓硫酸反应产生SO 和CO ,用品红溶液检验SO ,用足量
2 2 2
酸性高锰酸钾溶液除去SO ,酸性KMnO 溶液颜色变浅但未完全褪色说明SO 已除尽;浓
2 4 2
硫酸作干燥剂,碱石灰吸收产生的CO ,根据碳元素守恒,n(C)=n(CO)= mol,则铁的质
2 2
量为(a-b×) g= g,铁的质量分数为×100%。
第 21 练 硫及其化合物的相互转化
1.A 2.B
3.D [根据图中信息,b为HSO ,d为S,f为亚硫酸盐,其中S元素都处于中间价态,既
2 3
有氧化性,又有还原性,A正确;硫酸型酸雨的形成涉及HSO 被氧气氧化转化为HSO ,
2 3 2 4
B正确;a为HS,b为HSO ,a溶液与b溶液反应过程中有淡黄色沉淀生成,C正确;d为
2 2 3
S,e 为 S2-形成的盐,f 为 SO 形成的盐,由 3S+6OH-=====2S2-+SO+3HO 可得,
2
n(e)∶n(f)=2∶1,D错误。]
4.A 5.A
6.B [通入空气的目的是将CaSO 氧化为CaSO ,故A、C错误;“高温”时发生反应:
3 4
CaCO =====CaO+CO↑、CaO+SO =====CaSO、2CaSO+O=====2CaSO,故D错误。]
3 2 2 3 3 2 4
7.D [硫燃烧只能得到SO ,A项错误;盐酸的酸性大于亚硫酸的酸性,故SO 不与BaCl
2 2 2
溶液反应,B项错误;无水CuSO 为白色,C项错误;NaSO 与HSO 反应生成SO 、S、
4 2 2 3 2 4 2
HO、NaSO ,D项正确。]
2 2 4
8.C 9.B 10.B
11.C [根据转化关系图,过程Ⅱ中S2-与MnO生成SO和Mn(OH) ,根据氧化还原反应
2 2
得失电子守恒和元素守恒,反应的离子方程式为4MnO+2S2-+9HO===SO+4Mn(OH) ↓
2 2 2
+10OH-,故B正确;分析可知过程Ⅰ中发生反应:2Mn(OH) +O +4OH-===2MnO+
2 2
4HO,溶液的pH减小,溶液碱性减弱,故C错误;10 L上清液中的S2-的物质的量为=
2
0.15 mol,根据物质转化过程可知,S2-转化为SO过程中需要消耗氧气,SO转化为SO也
2 2需要消耗氧气,在转化过程中,硫元素的化合价由-2价变成+6价,S2-共失去 0.15
mol×8=1.2 mol电子,1 mol O 在反应中得到4 mol电子,所以将10 L上清液中的S2-转化
2
为SO,理论上共需要O 的物质的量为=0.3 mol,故D正确。]
2
12.C [导管a可以平衡分液漏斗和烧瓶内的气压,有利于硫酸顺利滴入,A正确;装置A
中发生反应的化学方程式为HSO +NaSO ===NaSO +HO+SO ↑,利用复分解反应制备
2 4 2 3 2 4 2 2
SO ,该反应体现了硫酸的酸性,B正确;实验过程中可以通过B中产生气泡的速率调节滴
2
加硫酸的速率,同时二氧化硫与C中物质反应易引起倒吸,B还可以起到平衡气压、防倒吸
的作用,D的作用仅仅是作安全瓶,起防倒吸的作用,C错误;C中出现淡黄色浑浊,说明
C中产生了硫单质,最终又变澄清,说明硫单质又反应了,D正确。]
13.(1) 2HS+O===2S↓+2HO 弱 (2)bd
2 2 2
(3)2CO+SO =====S+2CO
2 2
解析 (1)H S水溶液在空气中放置易变浑浊是因为HS被氧气氧化为S,反应的化学方程式
2 2
为2HS+O===2S↓+2HO,所以S的非金属性比O弱。(2)Na SO 中S为+2价,从氧化
2 2 2 2 2 3
还原的角度分析,反应物中S的化合价必须分别大于2和小于2,b、d符合题意。
14.(1)检查装置气密性 K、K K 冷却结晶
1 2 3
(2)2CO+4SO +2S2-+HO===3SO+2HCO
2 2 2
(3)除去SO ,使SO 与SO 分离
3 3 2
(4)pH小于7时,会造成生成的硫代硫酸根离子在酸性条件下分解;pH大于8时,原料反应
不充分,二者都会影响硫代硫酸钠的产率和纯度 (5)m处接一个尾气处理装置
第 22 练 氮及其氧化物 硝酸
1.B 2.C
3.D [D项中“滴有酚酞的氢氧化钠溶液红色褪去”,其褪色的原因可能是硝酸的强氧化
性把酚酞氧化而褪色,但也有可能是硝酸与氢氧化钠发生中和反应,究竟是哪个原因,还需
要实验验证,D项不准确。]
4.B [铜丝溶解于稀HNO ,生成硝酸铜、NO和水,无色气体为NO,不会生成氢气,故
3
A错误;NH 能使热的氧化铜产生红色物质,原理是3CuO+2NH =====N +3Cu +3HO,
3 3 2 2
说明氨气具有还原性,故B正确;N 与H 混合,在催化剂、高温、高压的条件下反应生成
2 2
氨气,没有催化剂时加热反应速率慢,生成物的含量少,但不能说明N的非金属性弱,故C
错误;NO 被NaOH溶液吸收,生成硝酸钠、亚硝酸钠和水,发生歧化反应,体现NO 的氧
2 2
化性和还原性,没有体现酸性,故D错误。]
5.A [溴蒸气和二氧化氮气体均呈红棕色,所以至少含有溴蒸气和二氧化氮气体中的一种;溴水为橙黄色,所以含有溴蒸气;再打开玻璃片后,瓶中气体又变为红棕色,说明有一氧化
氮存在,二氧化氮在水溶液中发生氧化还原反应生成硝酸和一氧化氮无色气体,再打开玻璃
片后,一氧化氮遇到氧气迅速变为二氧化氮,所以至少还存在二氧化氮或 NO气体中的一
种。]
6.D 7.D
8.B [浓硝酸和铜反应生成硝酸铜、水和NO ,A正确;NO 的密度比空气大,应用向上
2 2
排空气法收集,即导气管应长进短出,B错误;NO 可以和NaOH溶液反应得到可溶性盐,
2
所以可以用NaOH溶液处理尾气,C正确;试管中发生反应:4NO +O+2HO===4HNO,
2 2 2 3
可以使NO 充分转化为HNO,D正确。]
2 3
9.C 10.B
11.C [先检查装置气密性,加入药品后,为防止装置中的氧气影响实验结果,需关闭c,
打开a和b,通入一段时间氮气,将装置内的空气排尽,故 A正确;关闭a、c,打开b及分
液漏斗活塞,浓硝酸与Cu反应生成NO ,NO 通入水中与水反应生成NO,NO进入丙和丁
2 2
后,丙中含亚铁离子的溶液变为深棕色,而丁中无明显变化,说明NO与Fe2+反应,故B正
确;甲中反应一段时间后浓硝酸变稀,生成的气体中有 NO,所以该操作无法证明NO 是否
2
与Fe2+反应,故C错误;实验中未反应的NO 和NO会污染空气,需要尾气处理装置,故D
2
正确。]
12.A [铁粉既能与硝酸反应,也能与硫酸反应,从题图看出OA段产生的是NO,发生反
应为Fe+4H++NO===Fe3++NO↑+2HO,AB段的反应为Fe+2Fe3+===3Fe2+,BC段产
2
生的是氢气,反应为Fe+2H+===Fe2++H↑,可知OA段NO完全反应,第二份溶液中
2
n(NO)=n(Fe)==0.1 mol,溶液中最终溶质为FeSO ,此时反应的铁的质量是14.0 g(即0.25
4
mol),故原混合酸中HSO 浓度为=2.5 mol·L-1,NO物质的量为0.2 mol。]
2 4
13.(1) SO、SO 、NO (2) 2SO+O2SO
2 3 2 5 2 2 3
(3)N + 3H 2NH (4) 4HNO =====4NO ↑ + O↑ + 2HO (5) 6NO +
2 2 3 3 2 2 2
4NH ======5N+6HO
3 2 2
14.(1)3 mol·L-1稀硝酸、浓硝酸、氢氧化钠溶液 (2)打开弹簧夹,通入一段时间CO ,关
2
闭弹簧夹,将装置⑤中的导管末端伸入倒置的烧瓶内 (3)Cu+4HNO(浓)===Cu(NO ) +
3 3 2
2NO ↑+2HO (4)将NO 转化为NO 3NO +HO===2HNO +NO (5)装置③中液面上方
2 2 2 2 2 3
气体仍为无色,装置④中液面上方气体由无色变为红棕色 (6)acd
解析 (1)根据装置特点和实验目的,装置⑤收集NO,装置④盛放浓硝酸,装置⑥中盛放
NaOH溶液吸收NO ,因为要验证稀HNO 不能氧化NO,所以装置③中应该盛放3 mol·L-1
2 3
稀硝酸。(2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO 之前需
3
要通入一段时间的CO 赶走装置中的空气,同时也需将装置⑤中的导管末端伸入倒置的烧瓶
2
内防止反应产生的NO气体逸出。(5)NO通过稀HNO 后,若无红棕色NO 产生,说明稀
3 2HNO 不能氧化NO,所以盛放稀HNO 的装置③液面上方没有颜色变化即可说明。装置④中
3 3
盛放的是浓HNO ,若浓HNO 能氧化NO,则装置④的液面上方会产生红棕色气体。(6)要
3 3
证明是Cu(NO ) 浓度过高或是溶解了NO 导致装置①中溶液呈绿色,可设计将溶解的NO
3 2 2 2
赶走(a、c方案),再观察颜色变化,也可在饱和Cu(NO ) 溶液中通入NO ,观察比较反应后
3 2 2
的颜色变化(d方案),确定是不是因为溶有NO 引起的。
2
第 23 练 氨 铵盐
1.A 2.C
3.C [实验一是氨的喷泉实验,证明氨极易溶于水,形成的氨水为弱碱性溶液,酚酞溶液
变红色,证明氨是碱性气体。实验二中浓氨水挥发出的氨分子和浓盐酸挥发出的氯化氢分子
结合生成氯化铵固体小颗粒,证明浓氨水易挥发、氨是碱性气体。]
4.D [氨极易溶于水,将集有氨的试管倒扣于盛有水的水槽中,液体迅速充满试管,故 A
正确;氨水呈碱性:NH +HONH ·H ONH+OH-,故B正确;氨被氧气直接氧化为
3 2 3 2
NO,NO被O 氧化为红棕色的NO ,故D错误。]
2 2
5.A [NH ·H O是弱电解质,NaOH是强电解质,前者部分电离,后者完全电离,故通过
3 2
室温下测定等浓度的氨水和NaOH溶液的pH,可比较NH ·H O和NaOH的碱性强弱,A正
3 2
确;NH 极易溶于水,稀溶液中不加热,NH 不能逸出,无法确定是否含NH,B错误;NH
3 3 3
不易燃烧,产生的NO是大气污染物,不能作清洁能源,C错误;NH Cl受热也会分解,故
4
不可采用加热法除杂,D错误。]
6.A [因NaHCO 溶液抑制CO 的溶解,则挤压胶头滴管,气压变化不明显,则不会形成
3 2
喷泉,故A错误;因氨极易溶于水,则挤压胶头滴管,使烧瓶中的气压减小,且小于外界
大气压,又因氨水显碱性,酚酞遇碱变红,甲基橙遇碱变黄,故B中形成红色喷泉,C中形
成黄色喷泉,故B、C正确;因HCl与AgNO 溶液反应生成白色的AgCl沉淀,则挤压胶头
3
滴管,使烧瓶中的气压减小,且小于外界大气压,形成白色喷泉,故D正确。]
7.A 8.C 9.B
10.C [NH Cl是常见的化肥,NaHCO 不是,故B错误;NO 与NH 可以发生反应:6NO
4 3 2 3 2
+8NH ===7N +12HO,故C正确;NH Cl受热易分解生成HCl和NH ,HNO 受热时分解
3 2 2 4 3 3
生成二氧化氮、氧气和水,NaCO 性质稳定,难以分解,故D错误。]
2 3
11.B [由于CO 微溶于水,NH 极易溶于水,应先通入足量NH ,使溶液呈碱性,然后再
2 3 3
通入适量CO ,通入NH 和CO 的顺序不可以互换,故A错误;步骤②中反应的离子方程
2 3 2
式为CaSO +2NH +CO +HO===CaCO +2NH+SO,故C错误;反应过程中二氧化碳参
4 3 2 2 3
与反应生成硫酸铵和碳酸钙,碳酸钙分解生成二氧化碳,工艺流程中产生的CO 可循环利用,
2但应通适量二氧化碳,否则碳酸钙溶解,故D错误。]
12.D
13.(1)2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑
4 2 2 2 3
(3)平衡气压防倒吸 倒吸 (4)NH PO (5)酚酞 无色 浅红色
解 析 本 实 验 的 目 的 为 制 备 磷 酸 氢 二 铵 [(NH )HPO ] , 实 验 原 理 为 2NH +
4 2 4 3
HPO ===(NH )HPO ,结合相关实验基础知识分析解答问题。(3)由于NH 极易溶于水,因
3 4 4 2 4 3
此可选择打开活塞K 以平衡气压,防止发生倒吸,所以实验过程中,当出现倒吸现象时,
2
应及时关闭K ,打开K 。(4)继续通入NH ,(NH )HPO 继续反应生成(NH )PO ,当pH>
1 2 3 4 2 4 4 3 4
10.0时,溶液中OH-、NH、PO的浓度明显增加。(5)由(4)可知,当pH为8.0~9.0时,可制
得(NH )HPO ,说明(NH )HPO 溶液显碱性,因此若不选用pH传感器,还可以选用酚酞作
4 2 4 4 2 4
指示剂,当溶液颜色由无色变为浅红色时,停止通入NH ,即可制得(NH )HPO 溶液。
3 4 2 4
14.(1)分液漏斗 球形干燥管 (2)A (3)B
(4)4NH +5O=====4NO+6HO (5)①NH NO
3 2 2 4 3
②3Cu+8H++2NO===3Cu2++2NO↑+4HO (6)调节K 增加装置A中产生氧气的量或调
2 1
节K 减少装置B中产生氨气的量或在E、F间增加盛有浓硫酸的洗气装置
2
第 24 练 氮及其化合物的转化关系
1.B 2.B
3.B [N→NH 属于氮的固定,NH →NO不属于氮的固定,A错误;催化剂可以提高化学
2 3 3
反应速率,可以提高单位时间内生成物的产量,B正确;催化剂a作用下,N→NH ,断裂
2 3
N≡N非极性共价键;催化剂b作用下,NH →NO,断裂N—H极性共价键,C错误;催化
3
剂a作用下,N→NH ,氮原子化合价从0价降低至-3价,发生了还原反应,D错误。]
2 3
4.B [如果X是水,分解可生成O,O 与N 反应生成NO,X可能是一种氢化物,故A正
2 2 2
确;Z为NO,如果Y是O ,那么NH 与O 在催化剂的条件下可以生成NO,所以Y生成Z
2 3 2
不一定是化合反应,故B错误;Z是NO,NO与O 反应产生红棕色的NO 气体,所以E可
2 2
能是红棕色NO ,故C正确;F可以是HNO,M元素的化合价可能为+5,故D正确。]
2 3
5.C 6.C 7.C
8.C [反应①使用催化剂可以提高反应速率,但不能提高甲烷的平衡转化率,A错误;反
应②的化学方程式为 CO +2NH ======CO(NH) +HO,则该反应的原子利用率小于
2 3 2 2 2
100%,B 错误;由天然气经过各步转化,最终生成 NH NO 涉及的化学反应有 CH +
4 3 4
2HO=====CO +4H ,N +3H2NH 2NH +2O===NH NO +HO,则有NH NO
2 2 2 2 2 3, 3 2 4 3 2 4 3
~2NH ~3H ~CH ,故生成1.0 mol NH NO 至少需要0.75 mol CH ,C正确;反应③的化
3 2 4 4 3 4
学方程式为2NH +2O===NH NO +HO,则理论上当n(NH )∶n(O )=1∶1时,恰好完全
3 2 4 3 2 3 2反应,D错误。]
9.D [根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先利用铜与
2
稀硝酸反应生成NO,由于硝酸具有挥发性,所以制得的 NO中会混有硝酸蒸气和产生的
NO ,故先通过装置D除去挥发出的HNO 和产生的NO ,再通过装置F干燥,得到纯净干
2 3 2
燥的NO,然后进入装置E中与铁粉反应,最后处理多余的NO,由于NaOH溶液不与NO
反应,而浓硝酸可氧化NO生成NO ,所以先通过装置B氧化NO,再通过装置C吸收尾气,
2
故上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A正确。]
10.D 11.C
12.A [合成氨反应为放热反应,温度降低,平衡正向移动,原料的转化率升高,所以400
~500 ℃不利于提高原料的转化率,故A错误;气体2为NO 气体,NO 气体和溴蒸气都能
2 2
使淀粉-KI试纸变蓝,故B正确;气体1为NO,气体2为NO 1 L NO、NO 的混合气与1 L
2, 2
NH 在一定条件下转化为对环境无害的物质,反应的化学方程式为 2NH +NO+
3 3
NO =====2N+3HO,NO、NO 的体积比等于化学计量数之比,为1∶1,故D正确。]
2 2 2 2
13.(1)CD (2)(或0.045) (3)4NH +3O=====2N+6HO (4)氧化 (5)①NaNO ②1∶3
3 2 2 2 2
解析 (5)②7 mol氨失去21 mol电子,根据题意和得失电子守恒可得n(NO)+n(NO )=6
2
mol,2n(NO)+4n(NO )=21 mol,解得n(NO)=1.5 mol,n(NO )=4.5 mol,则混合气体中NO
2 2
和NO 的物质的量之比为1∶3,若用通式NO 表示氮氧化物,反应过程中NO 分子得到2x e
2 x x
-,则每摩尔氨可将 mol的NO 转化为N。
x 2
14.(1)CaO+NH ·H O===Ca(OH) +NH ↑ (2)球形干燥管 碱石灰 (3)吸收并检验氨气,
3 2 2 3
防止氨气直接排入空气中 关闭K 和K ,打开K (4)abcdgh 安全瓶、防倒吸 排尽装置
1 2 3
内的空气(合理即可) (5)Cu O 0.075 mol、Cu 0.075 mol
2
第 25 练 碳、硅 无机非金属材料
1.C 2.A 3.C
4.A [CO 中C采取sp杂化,空间结构为直线形,CO 是非极性分子,A项错误;CO 在
2 2 2
电催化下与氢气反应可以降低碳的化合价,生成一系列化合物,如 CH 、CH===CH 、
4 2 2
CHOH、HCOOH等,B项正确;干冰气化时吸收大量热量,使水蒸气液化而增雨,C项正
3
确 ; 侯 氏 制 碱 法 的 化 学 反 应 原 理 是 NaCl + NH + CO + HO===NaHCO ↓ +
3 2 2 3
NH Cl,2NaHCO =====NaCO+CO↑+HO,D项正确。]
4 3 2 3 2 2
5.C 6.C
7.C [金刚石属于共价晶体,石墨属于混合型晶体,C 属于分子晶体,因此金刚石和石墨
60
的熔点肯定比C 高,故A正确;分子晶体的相对分子质量越大,熔点越高,因此熔点:C
60 60
<C <C ,故B正确。]
70 908.B [通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,a、c判断错误;反应②是一个置
换反应,其中二氧化硅被还原,表现出氧化性,b判断正确;反应④用难挥发的二氧化硅制
取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价由0价变为-4价和+2价,硅的化
合价和氧的化合价都没有改变,因此二氧化硅没有参加氧化还原反应,e判断正确。]
9.D 10.D
11.B [A项,反应②中生成的HCl在反应①中循环利用,反应①中生成的H 在反应②中
2
循环利用,正确;B项,反应①与反应②的反应温度不同,不是可逆反应,错误;C项,高
温条件下,Si、SiHCl 、H 都与O 反应,故需隔绝空气,正确;D项,SiO 不与HCl(aq)反
3 2 2 2
应,不能通过上述途径制硅,正确。]
12.A [根据图示可知:在Ag薄膜附近发生反应:2H++2e-+HO===2HO,所以随着反
2 2 2
应的进行,c(H+)减小,故pH逐渐增大,A错误;根据图示可知:在Si电极上,Si失去电
子与 HF 结合形成 HSiF 和 H+,反应方程式为 Si+2HO-4e-===SiO +4H+,SiO +
2 6 2 2 2
6HF===HSiF +2HO,B正确;由Ag、Si极发生的电极反应及电子转移数目相等,可知总
2 6 2
反应方程式为Si+6HF+2HO===HSiF +4HO,C正确;根据上述分析可知:在Ag电极
2 2 2 6 2
上得到电子,在Si电极上失去电子,电解质溶液为HF和HO ,它们形成闭合回路,实现
2 2
了化学能向电能的转化,即构成了原电池,D正确。]
13.(1)14 蒸馏 (2)Si+4HNO(浓)+6HF===HSiF +4NO ↑+4HO (3)①分液漏斗 浓
3 2 6 2 2
硫酸 ②加热均匀,便于控制温度使SiHCl 汽化 ③检验氢气的纯度(或先滴加稀硫酸,产
3
生氢气,排尽装置中的空气) SiHCl +H==========Si+3HCl
3 2
第六章 元素及其化合物综合应用
第 26 练 化学与 STSE 化学与中华文明
1.C
2.B [芯片主要材料为硅,故A错误;母船海水浸泡区的铝与船体构成原电池,金属性强
于铁的铝基作原电池的负极被损耗,船体作正极被保护,该保护方法为牺牲阳极法,故B
正确;铷单质的金属性强,与水剧烈反应放出氢气,故C错误;复合纤维属于合成有机高
分子化合物,故D错误。]
3.B [柳絮的主要成分为纤维素,属于糖类,A项正确;海市蜃楼形成美景的本质原因是
空气中的小水滴颗粒直径大小约为1~100 nm,B项错误;青丝与白发均指头发,主要成分
均属于蛋白质,D项正确。]
4.B 5.D6.B [“薪柴之灰”中含有碳酸钾,与铵态氮肥混合施用时,铵根离子与碳酸根离子发生
相互促进的水解反应生成氨气、二氧化碳,易造成 N元素以氨气形式逸散,降低氮肥肥效,
B正确;火药是硝酸钾、硫粉、木炭粉按一定比例混合而成,此处的“硝”指的是硝酸钾,
KNO 水溶液呈中性,C错误;“酒曲”酿酒工艺利用了催化剂加快化学反应速率,但是不
3
能提高反应物的平衡转化率,D错误。]
7.D 8.D 9.A
10.A [碳纤维由碳元素组成,属于新型无机非金属材料,A正确;高聚物的聚合度不确定,
所以高聚物属于混合物,B错误;量子通信材料螺旋碳纳米管、石墨均为碳元素组成的单质,
互为同素异形体,C错误;碲属于第五周期第ⅥA族元素,镉属于第五周期第ⅡB族元素,
D错误。]
11.D [“投泥泼水愈光明,烁玉流金见精悍”涉及碳和HO反应生成CO和氢气,属于氧
2
化还原反应,属于化学变化,A正确;“凡火药,硫为纯阳,硝为纯阴”中“硫”指的是硫
黄,“硝”指的是硝酸钾,B正确;“盖此矾色绿味酸,烧之则赤”,“矾”指的是绿色的
FeSO ·7H O,属于强酸弱碱盐,水解显酸性,火烧之后会转化为红色的氧化铁,C正确;
4 2
《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应的条件不同,不属于可逆反应,
D错误。]
12.A 13.C 14.B
15.A [通过清洁煤技术减少煤燃烧污染,但不能减少CO 排放,不利于实现碳中和,故B
2
错误;纳米铁粉可以从溶液中将Cu2+、Ag+等重金属离子置换成单质,与吸附性无关,故D
错误。]
第 27 练 常见物质(离子)的检验与推断
1.A
2.C [当固体中含有SO时,在酸性条件下滴加Ba(NO ) 溶液会被氧化生成硫酸根离子,
3 2
有相同现象,故不一定存在SO,A错误;若固体为FeCl 和Fe的混合物时,也有相同的现
3
象,故固体试样中可能存在Fe3+,B错误;检验NH时应加NaOH溶液,加热,产生使湿润
红色石蕊试纸变蓝的气体,选项中没有加热,故不能确定有没有铵根离子,C正确;滴加盐
酸出现白色沉淀,再加NaOH溶液沉淀溶解,可能原固体中有AlO,不一定为SiO,D错
误。]
3.D 4.C
5.B [加入浓溴水后,Al (SO ) 溶液无明显现象,AgNO 溶液中有淡黄色沉淀生成,苯酚
2 4 3 3
溶液中有白色沉淀生成,A项可行;通入SO 后,Al (SO ) 溶液无明显现象,AgNO 溶液中
2 2 4 3 3
出现白色浑浊,苯酚溶液无明显现象,B项不可行;通入足量氨气后,Al (SO ) 溶液中有白
2 4 3色沉淀生成,AgNO 溶液中先有白色沉淀生成,后沉淀消失,苯酚溶液无明显变化,C项可
3
行。]
6.C [溴乙烷和NaOH乙醇溶液共热,所产生气体中含有乙醇蒸气,乙醇、乙烯都能使酸
性高锰酸钾溶液褪色,高锰酸钾溶液褪色不能证明有乙烯生成,故A错误;将SO 通入溴水
2
中生成硫酸和氢溴酸,该反应体现SO 的还原性,不能体现SO 的漂白性,故B错误;在待
2 2
测液中先用稀硝酸酸化,再滴加AgNO 溶液,生成白色沉淀,该沉淀是氯化银,证明原溶
3
液中含有Cl-,故C正确;碳碳双键、醛基都能与溴水反应,向丙烯醛溶液中滴加溴水,溶
液褪色,不能证明丙烯醛中含有碳碳双键,故D错误。]
7.D [A项,HCO会产生干扰,错误;B项,SO会产生干扰,错误;C项,使酸性高锰酸
钾溶液褪色的不一定是Fe2+,如SO等,错误;D项,新制氯水能把I-氧化成I ,淀粉遇碘
2
变蓝,因此可以检验I-的存在,正确。]
8.C 9.C 10.B
11.A [亚硫酸根离子的还原性强于碘离子,优先与少量氯水反应,由向溶液中滴加少量
新制氯水,所得溶液为无色可知,溶液中一定含有亚硫酸根离子,一定不含氢离子和钡离子;
溶液中各离子物质的量相等,由电荷守恒可知,溶液中一定含有钠离子和铵根离子,一定不
含有氯离子、碘离子和硫酸根离子,故选A。]
12.A [根据①可判断溶液中有Br-和CO,根据离子共存原则,不存在Al3+、Mg2+;根据
②可判断溶液中无SO;根据③不能确定是否含有I-,因为在①中氯水可能把I-氧化成了
IO,致使淀粉溶液不变蓝色。]
13.(1)SO 、CO HO (2)H O SO 、CO (3)SO 、CO HO
2 2 2 2 2 2 2 2 2
14.(1)Fe2+、Cu2+、Cl-、NO、SO 酸 Fe2++2HOFe(OH) +2H+、Cu2++
2 2
2HOCu(OH) +2H+(任写一个) (2)3Fe2++4H++NO===3Fe3++NO↑+2HO
2 2 2
(3)Fe(OH) Cu(OH) (4)ab (5)NO+NO +2OH-===2NO+HO
3 2 2 2
第 28 练 常见气体的实验室制备、净化和收集
1.B 2.A
3.C [二氧化锰和浓盐酸反应需要加热,故A错误;用饱和食盐水除去Cl 中的HCl,气
2
体应该“长进短出”,故B错误;氯气和氢氧化钠在较低温度下反应生成氯化钠、次氯酸
钠和水,故C正确;石灰水的浓度太小,应该用氢氧化钠溶液吸收氯气,故D错误。]
4.D [稀盐酸和二氧化锰不反应,装置Ⅱ中无明显现象,故A错误;浓氨水和氧化钙反应
生成氨气,氨气与硫酸亚铁溶液反应生成 Fe(OH) 白色沉淀,然后变为灰绿色,最终变为
2
Fe(OH) 红褐色沉淀,故B错误;酯化反应需要加热,但图中没有加热装置,不能生成乙酸
3
乙酯,故C错误;浓盐酸与碳酸钙反应生成CO 气体,且浓盐酸易挥发,CO 、HCl均与
2 2NaCO 反应使溶液碱性减弱,观察到装置Ⅱ中溶液由红色最终变为无色,故D正确。]
2 3
5.B 6.B
7.D [反应2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO可用于制备氨,A正确;NH 是
4 2 2 3 2 3
碱性气体,可用碱石灰进行干燥,B正确;装置丙发生反应3CuO+2NH =====3Cu+N +
3 2
3HO,可验证氨的还原性,C正确;氨的密度比空气小,收集时应从短管进长管出,D错
2
误。]
8.D [反应温度如果过高,HNO 分解生成NO ,NO 溶于HNO 使制得的HNO 呈现黄色,
3 2 2 3 3
B正确;实验室中浓硝酸应保存在棕色瓶内,防止其见光分解,D错误。]
9.B [A项,气体从溶液中逸出易带出水蒸气,所以浓硫酸应放在③中,错误;B项,先
通H 以排出空气,加热前应先检验H 的纯度,正确;C项,若先停止通H ,空气中的氧气
2 2 2
有可能重新将W氧化,应先停止加热,待装置冷却后再关闭活塞K,错误;D项,MnO 和
2
浓盐酸反应制氯气需要加热,不能用启普发生器制备,错误。]
10.D 11.D
12.(1)2KMnO=====KMnO +MnO +O↑(或 2KClO=====2KCl+3O↑) Ca(OH) +
4 2 4 2 2 3 2 2
2NH Cl=====CaCl +2NH ↑+2HO (2)2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+
4 2 3 2 4 2 2
8HO Cu+4HNO(浓)===Cu(NO ) +2NO ↑+2HO 把氨水滴加到NaOH固体上,NaOH
2 3 3 2 2 2
溶于水放出热量可促进 NH ·H O的分解;NaOH溶于水电离产生的OH-促使平衡NH +
3 2 3
HONH ·H ONH+OH-逆向移动,导致放出NH (3)c或e
2 3 2 3
13.(1)a→b→f→g→c 除去二氧化碳中的HCl杂质
(2)关闭K ,打开K (3)6VOCl +6HO+17NH HCO ===(NH )[(VO) (CO)(OH) ]·10H O↓
2 1 2 2 4 3 4 5 6 3 4 9 2
+13CO↑+12NH Cl
2 4
第 29 练 非金属及其化合物拓展创新
1.B 2.C
3.C [直形冷凝管一般用于冷凝收集;球形冷凝管一般用于冷凝回流,装置 m用于产物的
冷凝收集,不能用球形冷凝管代替,A正确;水浴加热可避免直接加热造成的局部过度剧烈,
并能最大限度保证温度低于100 ℃,避免磷酸分子间脱水生成焦磷酸等,B正确;过滤时
应控制温度为30~42 ℃,使磷酸以晶体形式存在,而杂质2HPO ·H O为液态,从而通过
3 4 2
过滤除去杂质,C错误;磷酸的结构简式为 ,其中的羟基可以与水分子形成氢键,
从而提高除水难度,D正确。]
4.D [置换出海绵铜的试剂X为Fe,故A错误;加入亚硫酸氢钠,反应的离子方程式为
AsO+HSO+2H+===SO+HAsO↓+HO,反应后溶液的酸性减弱,故B错误;加入HO
2 2 2 2将Fe2+氧化为Fe3+,通过调节溶液pH,使Fe3+完全转化为Fe(OH) 沉淀而除去,故C错误;
3
流程中钠离子和生成的硫酸根离子没从体系中分离出去,故达标废液中含有的溶质主要为
NaSO ,故D正确。]
2 4
5.(1)+4 第四周期第ⅥA族 (2)SeO +2OH-===SeO+HO (3)蒸发浓缩、冷却结晶
2 2
防止NaSeO 被空气中的氧气氧化 (4)C (5)
2 3
6.(1)球形冷凝管 a (2)平衡气压(或与大气相通,保持装置压强恒定或防止装置内压强过
大) (3)防止空气中的水蒸气进入装置C导致产物水解 (4)2PCl +O=======2POCl 温度
3 2 3
低,反应速率慢,温度高,原料易挥发,利用率低 (5)①b ②使生成的沉淀被硝基苯覆盖,
防止AgCl转化为AgSCN ③×100%
7.(1)F (2)增大固体和液体接触面积 (3)Na S+CuSO ===CuS↓+NaSO 6.0×10-30
2 4 2 4
(4)1∶1 过滤 温度过高,双氧水分解加快,反应物浓度降低 (5)陶瓷的主要成分是硅酸
盐,HF与硅酸盐反应
解析 锑矿(主要含Sb O 、Sb S ,还含有少量Sb O 、Fe O 、CuO等)加NaOH浓溶液、
2 3 2 3 2 5 2 3
NaSO 溶液进行碱浸、还原,过滤除去不溶的Fe O 、CuO,Sb O 、Sb S 与NaOH溶液反
2 2 3 2 3 2 3 2 3
应最终转化为 NaSbO 、NaS,Sb O 、NaOH 溶液与 NaSO 溶液反应生成 NaSbO 、
2 2 2 5 2 2 3 2
NaSO ;含NaSbO 、NaS的溶液加硫酸铜将硫离子转化为CuS,将过量的氢氧根离子转化
2 4 2 2
为氢氧化铜除去,得到主要溶质为NaSbO 的溶液,NaSbO 溶液加过氧化氢、浓NaOH转化
2 2
得到NaSbO ·3H O,再用HF进行氟化得到NaSbF 。(3)“除杂”时NaS和CuSO 反应生成
3 2 6 2 4
CuS沉淀,化学方程式为NaS+CuSO ===CuS↓+NaSO ,“除杂”结束后溶液中c(S2-)=
2 4 2 4
1×
10-6mol·L-1,此时溶液中c(Cu2+)=mol·L-1=6.0×10-30mol·L-1。
第 30 练 陌生过渡金属及其化合物的制备流程分析
1.C 2.D
3.C [由电极电位表可知金属活动性顺序为Fe>Cd>Ni>Pb>Cu。镍镉矿浆化后,在空气中
加入稀硫酸酸浸,硫化镍和金属氧化物溶于稀硫酸得到硫酸盐,二氧化硅不与稀硫酸反应,
过滤得到含有二氧化硅、硫酸铅的滤渣 Ⅰ 和滤液;向滤液中加入碳酸镍或氧化镍调节溶液
pH,将溶液中铁离子转化为氢氧化铁沉淀,过滤得到含有氢氧化铁的滤渣Ⅱ和滤液;由金
属活动性顺序可知,向滤液中只能加入镍,将溶液中铜离子转化为铜,过滤得到含有铜、镍
的金属A和硫酸镍、硫酸镉的滤液;滤液经电解、过滤得到含有镉和镍的固体和稀硫酸;
固体通入一氧化碳气化分离得到Ni(CO) 和镉;Ni(CO) 受热分解生成一氧化碳和镍,则该
4 4
工艺流程中可以循环利用的物质为一氧化碳、硫酸和镍等。]
4.D [0~5 s过程中,溶液中Cr元素的化合价都呈+6价,发生的离子反应为Cr O+
24HO+2H+===2CrO+5HO,A正确;30~80 s过程中,Cr元素由+3价升高到+6价,失
2 2 5 2
电子被氧化,由Cr3+转化为CrO,可能是溶解的氧气和剩余的HO 所致,C正确;0~80 s
2 2
时,溶液中含铬微粒转化过程中Cr元素化合价变化为+6→+6、+6→+3、+3→+6,依
次发生非氧化还原反应、还原反应和氧化反应,D不正确。]
5.(1) 2VO +NH +8HCl=====4VOCl +N↑+6HO (2)①分液漏斗
2 5 2 4 2 2 2
关闭旋塞a ②Ⅲ Ⅰ Ⅱ
(3)Cl- 除去晶体表面的乙醇 (4)×100%
6.(1)NiO NaVO 、NaHCO (2)2MoS+2NaCO +5O=====2NaMoO +2CO +2SO
3 3 2 3 2 2 4 2 2
Al O+NaCO=====2NaAlO +CO↑ (3)20 g·L-1 10 g·L-1 (4)2∶3
2 3 2 3 2 2
解析 (1)硫化物焙烧时生成氧化物和二氧化硫,由于NiO不能与碳酸钠反应,故“水浸”
时以“浸渣”的形式沉淀出来,而MoO 、VO 、Al O 与纯碱反应生成NaMoO 、NaVO
3 2 5 2 3 2 4 3
和 NaAlO ,通入过量 CO 生成沉淀 Al(OH) 和 NaHCO ,故“滤液 2”中的成分除了
2 2 3 3
NaMoO 外,还含有 NaVO 、NaHCO 。(4)由信息和流程及氧化还原反应原理可知,
2 4 3 3
NH VO 沉淀煅烧时分解产生VO、N 和NH ,故反应的化学方程式为6NH VO =====3VO
4 3 2 3 2 3 4 3 2 3
+2N↑+2NH ↑+9HO,氧化产物为N,还原产物为VO,故比值为2∶3。
2 3 2 2 2 3
7.(1)哑铃形 (2)SiO 、PbSO ZnS+MnO +2HSO ===ZnSO +MnSO +S↓+2HO
2 4 2 2 4 4 4 2
(3)4
(4)Cu2++S2- +Ba2++SO===CuS↓+BaSO↓
4
(5)333 趁热过滤 (6)CD
第七章 原子结构与性质
第 31 练 原子结构 核外电子排布规律
1.A 2.B 3.B
4.A [H X的摩尔质量为(A+m) g·mol-1,a g H X的物质的量为 mol;X原子的质量数为
m m
A,含N个中子,则质子数为A-N,所以a g H X中含质子的物质的量为 mol×(A-N+m)
m
= mol,A正确。]
5.C [绝大多数基态原子的核外电子排布都遵循构造原理,但也有少数例外,如Cu,故C
错误。]
6.A [N能层中有4s、4p、4d、4f四个能级,各具有1、3、5、7个轨道,每个轨道最多可
容纳2个电子,故可容纳32个电子,所以有32种运动状态,A正确;在K能层中,只有1个轨道,能容纳自旋相反的2个电子,B不正确;电子云通常是用小黑点来表示电子出现的
机会多少,但小黑点不表示电子,D不正确。]
7.B 8.D
9.B [最外层电子排布式为ns2的基态原子所对应元素不一定位于第ⅡA族,可能位于副
族或0族,如副族的Zn或0族的He,故A错误;d区元素的基态原子都含有d轨道电子,
故B正确;最外层电子排布式为ns1的基态原子所对应元素不一定是金属元素,如H,故C
错误;基态原子价层电子排布式为nsnnpn的元素,s能级上最多排列2个电子,则n=2,所
以该原子价层电子排布式为2s22p2,为C元素,是非金属元素,故D错误。]
10.C 11.B 12.D
13.B [X基态原子核外只有三个能级,且各能级电子数相等,为1s22s22p2,为C元素,Z
原子的核外电子有8种运动状态,Z为O元素,Y为N元素,Z与W元素位于同一族,W
为S元素,P原子核外有4个能层,最外层只有1个电子,其余各层均排满电子,为Cu元
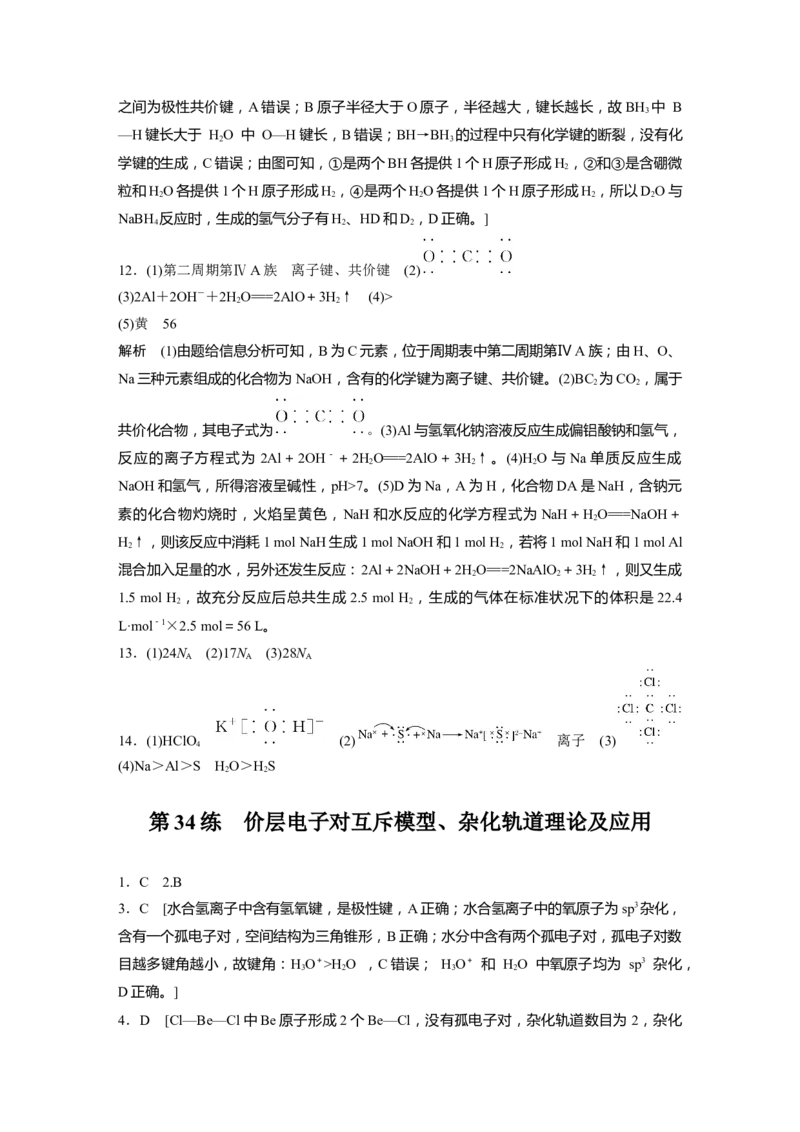
素。X为C元素,最外层有2个未成对电子,A错误;Y为N元素,基态原子的轨道表示式:
,B正确;P为Cu元素,价层电子排布为3d104s1,C错
误;Cu和O 反应生成CuO,Cu元素的化合价为+2价,Cu和S反应生成Cu S,Cu元素的
2 2
化合价为+1价,D错误。]
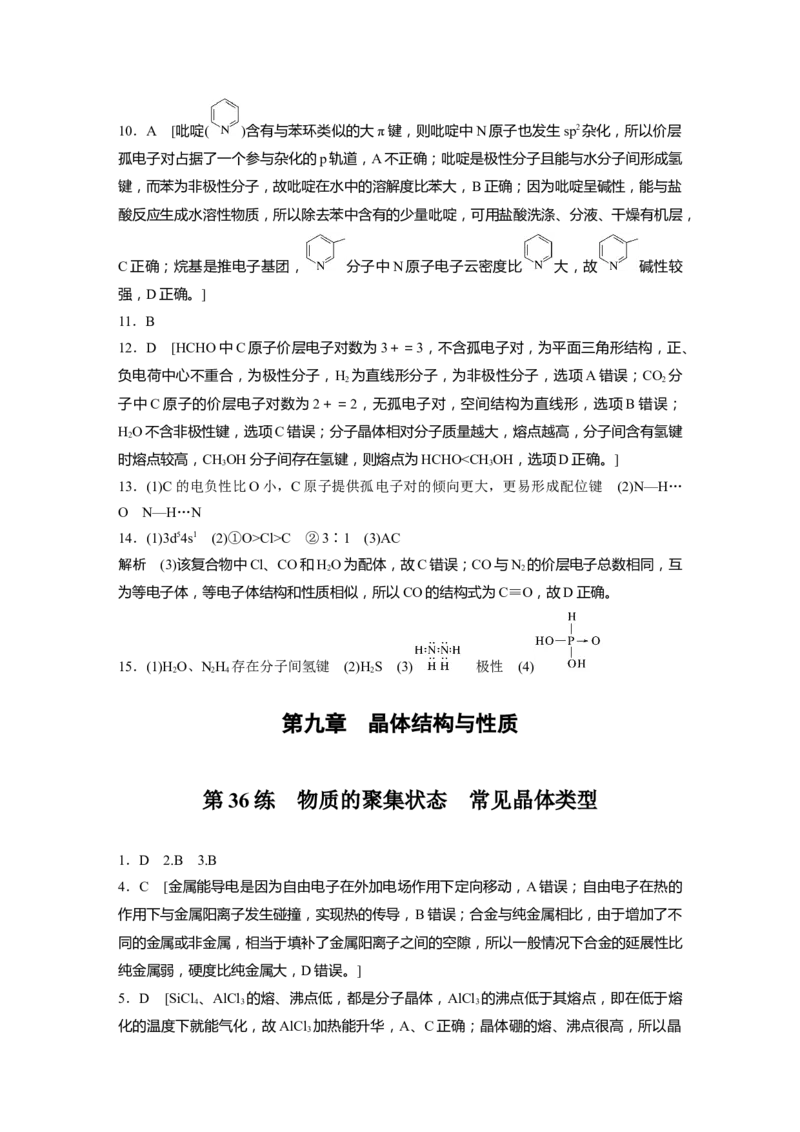
14.(1)①6 13 ②N 哑铃 (2)①1s22s1 ②< Fe3+的3d轨道处于半充满的稳定状态,其
稳定性强于Fe2+
15.(1)B、Cu (2)
(3)1s22s22p63s1 6 (4)三种元素的非金属性依次增强,其最高价氧化物对应水化物的酸性依
次增强 (5)C N
3 4
解析 由题意,A原子核外电子占据三个轨道,A为B元素;B原子核外有6种运动状态不
同的电子,B为C元素;C元素位于第二周期,又因为其核外p能级电子数比s能级电子数
少1个,因此C为N元素; D元素基态原子核外有6个原子轨道排有电子同时仅有1个未
成对电子,s能级含1个轨道,p能级含有3个轨道,则D所含有的未成对电子在3s能级,
因此D为Na元素;E+的各能级电子均充满,因此E为Cu元素。(5)该化合物具有三维骨架
结构,其中每个C原子与4个N原子形成共价键,所以C的化合价为+4价,每个N原子与
3个C原子形成共价键,所以N的化合价为-3价,则该化合物的化学式为C N。
3 4第 32 练 元素周期表 元素的性质
1.D 2.D 3.C 4.C
5.B [元素的非金属性越强,其简单氢化物越稳定,非金属性:F>Cl>S>P,所以HF、
HCl、HS、PH 的稳定性依次减弱,故A错误;①中由于P原子3p能级半充满,所以第一
2 3
电离能较大;②同主族元素自上而下第一电离能逐渐减小,所以Mg的第一电离能较大;③
同周期元素从左到右,第一电离能呈增大趋势,所以Si的第一电离能较大,P、Mg、Si的
原子序数之和为15+12+14=41,故B正确;根据表格数据可知该元素的第三电离能和第
四电离能相差较大,所以应为第ⅢA族元素,故C错误;一般电子层数越多,原子半径越
大,电子层数相同,核电荷数越小,原子半径越大,所以原子半径由大到小的顺序为Mg、
Si、N、F,故D错误。]
6.A 7.C
8.D [L为O,M为金属,二者电负性差值大于1.7,可形成离子化合物,故A正确;Z为
-1价、电负性小于L,可知Z为Cl,在周期表中的位置为第三周期第ⅦA族,故B正确;
由分析可知,L为O,Y为S,Z为Cl,YLZ 为SOCl ,加入水中生成SO 与HCl,故C正
2 2 2
确;X为C,电子排布式为1s22s22p2,核外电子共占据4个原子轨道,故D错误。]
9.B
10.D [当I ≫I 时,元素的最高化合价为+n,故R和U最高价为+1,S最高价为+
n+1 n
2,T最高价为+3,A、C项正确;由表中数据可知,Q元素各电离能都较大,而且各级电
离能之间无太大差距,故Q最可能为稀有气体元素,所以氦元素最有可能与Q元素位于同
一族,B项正确;R出现了I,而锂核外只有3个电子,D项错误。]
4
11.A [①为铝元素,②为硅元素,③为磷元素,④为硫元素,同周期元素从左到右,元
素的电负性逐渐增大,因此电负性最大的是④,A错误;第三电离能远大于第二电离能,所
以是第ⅡA族元素,形成的阳离子是X2+,B正确;同一主族从上到下,元素的第一电离能
逐渐减小,①Na、K、Rb,②N、P、As,③O、S、Se均符合此规律,同一周期从左到右,
元素的第一电离能呈逐渐增大的趋势,④Na、P、Cl符合此规律,C正确;①为硅元素,②
为氮元素,③为碳元素,④为硫元素,同周期元素从左到右,原子半径逐渐减小,同主族元
素从上到下,原子半径逐渐增大,因此原子半径最大的为①,D正确。]
12.(1)第二周期第ⅥA族 F (2)Na+ (3)NaOH
(4)Al(OH) +KOH===KAlO +2HO
3 2 2
13.(1)5 (2)O>N>C>H 吸收
14.(1)1s22s22p63s23p63d64s2(或[Ar]3d64s2)(2)电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量 (3)Mn2+的
3d轨道电子排布为半充满状态,比较稳定 (4)2 (5)Al
第八章 分子结构与性质
第 33 练 化学键
1.B 2.D
3.D [NH 通入水中生成NH ·H O,只破坏了共价键,A不符合题意;NaOH熔化后电离
3 3 2
生成Na+、OH-,只破坏了离子键,B不符合题意;HBr通入水中发生电离,只破坏了共价
键,C不符合题意;KHSO 溶于水电离出K+、H+和SO,既破坏了离子键又破坏了共价键,
4
D符合题意。]
4.A [HCl分子中的σ键由氢原子提供的未成对电子的1s原子轨道和氯原子提供的未成对
电子的3p原子轨道“头碰头”重叠形成,故A错误;N 分子中p轨道与p轨道通过“肩并
2
肩”重叠形成p-p π键,π键为镜面对称,不能绕键轴旋转,故B正确;CH 中的碳原子为
4
sp3杂化,碳原子的4个sp3杂化轨道分别与氢原子的1s轨道重叠,形成C—H σ键,故C正
确;CH==CH 中碳碳之间形成双键,双键中有1个σ键和1个π键,故D正确。]
2 2
5.D 6.C 7.D
8.B [三硫化磷分子中存在P—P共价键和S—P共价键,为共价化合物,故A正确;由图
可知,PS 分子中存在6个P—S极性键,故B错误;由图可知,P原子最外层有5个电子,
4 3
每个P原子形成3个共价键,S原子最外层有6个电子,每个S原子形成2个共价键,故分
子中每个原子最外层均达到 8电子稳定结构,故 C 正确;已知 PS 燃烧时 P被氧化为
4 3
PO ,充分燃烧时S会生成SO ,故D正确。]
4 10 2
9.C [含有孤电子对和空轨道的原子之间存在配位键,所以二茂铁中Fe2+与环戊二烯离子
(C H)之间为配位键,故A错误;一个环戊二烯( )分子中含有σ键的数目为11,则1 mol
5
环戊二烯中含有σ键的数目为11N ,故B错误;碳碳双键之间存在π键,所以该分子中存
A
在π键,故C正确;铁原子核外有26个电子,铁原子失去最外层两个电子变为亚铁离子,
根据构造原理可知,亚铁离子核外电子排布式为1s22s22p63s23p63d6,故D错误。]
10.C
11.D [硼氢化钠(NaBH )与水在催化剂作用下获得氢气的总反应方程式为 NaBH +
4 4
4HO=====NaB(OH) +4H↑。NaBH 为离子化合物,阳离子和阴离子之间为离子键,B—H
2 4 2 4之间为极性共价键,A错误;B原子半径大于O原子,半径越大,键长越长,故BH 中 B
3
—H键长大于 HO 中 O—H键长,B错误;BH→BH 的过程中只有化学键的断裂,没有化
2 3
学键的生成,C错误;由图可知,①是两个BH各提供1个H原子形成H,②和③是含硼微
2
粒和HO各提供1个H原子形成H ,④是两个HO各提供1个H原子形成H ,所以DO与
2 2 2 2 2
NaBH 反应时,生成的氢气分子有H、HD和D,D正确。]
4 2 2
12.(1)第二周期第ⅣA族 离子键、共价键 (2)
(3)2Al+2OH-+2HO===2AlO+3H↑ (4)>
2 2
(5)黄 56
解析 (1)由题给信息分析可知,B为C元素,位于周期表中第二周期第ⅣA族;由H、O、
Na三种元素组成的化合物为NaOH,含有的化学键为离子键、共价键。(2)BC 为CO,属于
2 2
共价化合物,其电子式为 。(3)Al与氢氧化钠溶液反应生成偏铝酸钠和氢气,
反应的离子方程式为 2Al+2OH-+2HO===2AlO+3H↑。(4)H O 与 Na 单质反应生成
2 2 2
NaOH和氢气,所得溶液呈碱性,pH>7。(5)D为Na,A为H,化合物DA是NaH,含钠元
素的化合物灼烧时,火焰呈黄色,NaH和水反应的化学方程式为NaH+HO===NaOH+
2
H↑,则该反应中消耗1 mol NaH生成1 mol NaOH和1 mol H ,若将1 mol NaH和1 mol Al
2 2
混合加入足量的水,另外还发生反应:2Al+2NaOH+2HO===2NaAlO +3H↑,则又生成
2 2 2
1.5 mol H ,故充分反应后总共生成2.5 mol H ,生成的气体在标准状况下的体积是22.4
2 2
L·mol-1×2.5 mol=56 L。
13.(1)24N (2)17N (3)28N
A A A
14.(1)HClO (2) 离子 (3)
4
(4)Na>Al>S HO>HS
2 2
第 34 练 价层电子对互斥模型、杂化轨道理论及应用
1.C 2.B
3.C [水合氢离子中含有氢氧键,是极性键,A正确;水合氢离子中的氧原子为sp3杂化,
含有一个孤电子对,空间结构为三角锥形,B正确;水分中含有两个孤电子对,孤电子对数
目越多键角越小,故键角:HO+>H O ,C错误; HO+ 和 HO 中氧原子均为 sp3 杂化,
3 2 3 2
D正确。]
4.D [Cl—Be—Cl中Be原子形成2个Be—Cl,没有孤电子对,杂化轨道数目为 2,杂化轨道类型为sp杂化; 中Be原子形成3个Be—Cl,没有孤电子对,杂
化轨道数目为3,杂化轨道类型为sp2杂化; 中Be原子形成4个Be
—Cl,没有孤电子对,杂化轨道数目为4,杂化轨道类型为sp3杂化,故选D。]
5.A 6.D
7.D [BF 中心原子的价层电子对数为 3+×(3-3×1)=3 ,中心原子采取sp2杂化,没有
3
孤电子对,BF 的VSEPR模型为平面三角形;SO 中心原子的价层电子对数为 3+×(6-
3 3
3×2)=3 ,中心原子采取sp2杂化,没有孤电子对,SO 的VSEPR模型为平面三角形,故A
3
正确;CH 含有C—H极性键,CCl 含有C—Cl极性键,二者结构对称、正负电荷中心重合,
4 4
都为非极性分子,故B正确;C与O互为等电子体,C中含有1个碳碳三键,则O中含有1
个氧氧三键,氧氧三键中含有2个π键,所以1 mol O中含有的π键数目为2N ,故C正确;
A
AB 的空间结构为V形,A原子价层电子对数可能是3或4,如SO 中S原子为sp2杂化,
2 2
HO中O为sp3杂化,故D错误。]
2
8.B [①BCl 中B的价层电子对数为 3+=3,中心B原子为sp2杂化,键角为 120°;
3
②NH 中N的价层电子对数为3+=4,中心N原子为sp3杂化,由于NH 分子中有孤电子
3 3
对存在,使键角小于109°28′;③HO中O的价层电子对数为2+=4,中心O原子为sp3
2
杂化,理论上正四面体结构键角为109°28′,由于HO分子中存在两个孤电子对,使得键
2
角比NH 分子的键角还小;④PCl中P的价层电子对数为4+=4,中心P原子为sp3杂化,
3
键角为109°28′;⑤HgCl 中Hg的价层电子对数为2+=2,中心Hg原子为sp杂化,键角
2
为180°;综上,键角由大到小的顺序为⑤①④②③。]
9.C 10.B 11.C
12.D [Z的一种超原子Z具有40个价电子,则Z原子的价电子数为=3,则Z为Al元素;
Y为N元素;X为C元素。金属元素的电负性和电离能均小于非金属元素,同周期元素,
从左到右第一电离能呈增大趋势,电负性依次增大,所以碳、氮、铝三种元素的电负性和电
离能的大小顺序均为Y>X>Z,故A正确;碳酸根离子中碳原子的价层电子对数为3,孤电
子对数为0,碳酸根离子的空间结构为平面三角形,故B正确;硝酸根离子中氮原子的价层
电子对数为3,杂化方式为sp2杂化,故C正确;电子层结构相同的离子,核电荷数越大,
离子半径越小,则氮离子的半径大于铝离子,故D错误。]
13.(1)NH 分子中N原子的孤电子对进入Zn2+的空轨道形成配位键后,原孤电子对与成键
3
电子对间的排斥作用变为成键电子对间的排斥作用,排斥作用减弱 (2)砷原子的电负性小
于氮原子,其共用电子对离砷核距离较远,斥力较小,键角较小 (3)C==O对C—C的斥力
大于C—O对C—C的斥力
14.(1)否 若是sp3杂化,[Cu(NH )]2+的空间结构为正四面体形,将配离子[Cu(NH )]2+中
3 4 3 4的2个NH 换为CN-,则只有1种结构 (2)< (3)四面体形 > (4)sp2、sp3
3
解析 (2)甲醛分子中,碳氧之间为双键,根据价层电子对互斥模型可知双键与单键之间的
斥力大于单键与单键之间的斥力,所以H—C—H的键角小于120°。(3)当中心原子的价层电
子对数为4时,VSEPR模型为四面体形,硫原子无孤电子对,所以空间结构为四面体形;
配位原子得电子能力越弱,其与中心原子形成的共用电子对之间的斥力越强,F原子的得电
子能力大于氯原子,所以SO Cl 分子中∠Cl—S—Cl>SO F 分子中∠F—S—F。
2 2 2 2
15.(1)H—Cl 2+×(6-1×1-1×1) V形 (2)3s23p4 平面三角形 (3)SiCl 109°28′
4
(4)c
第 35 练 分子的性质 配合物与超分子
1.C 2.C
3.B [甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,为四面体结构,是由极性键
组成的极性分子,A正确;NH 中N原子的杂化方式为sp3,不是平面形,B错误;NH 分
2 4 2 4
子中连接N原子的H原子数多,存在氢键的数目多,而偏二甲肼[(CH )NNH]只有一端可以
3 2 2
形成氢键,另一端的两个甲基基团比较大,影响了分子的排列,沸点比 NH 的低,C正确;
2 4
CHOH和(CH)NNH 中C、O、N杂化方式均为sp3,D正确。]
3 3 2 2
4.B
5.A [Cl、P的电负性差值大于Cl、N的电负性差值,三氯化氮、三氯化磷的空间结构都
是三角锥形,故三氯化氮分子的极性小于三氯化磷,A项错误;分子的稳定性与键能、键数
目有关,N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高,B项正确;
NH 、PH 分子空间结构都是三角锥形NH 、PH ,N、P原子孤电子对数都为1,杂化类型
3 3 3 3
都是sp3,但是N原子半径小于P,N的电负性大于P,NH 分子中成键电子对之间排斥力大
3
于PH ,故NH 键角大于PH ,C项正确;晶体熔点高低由构成晶体的微粒之间作用力大小
3 3 3
决定,它们都是分子晶体,HNO 分子间作用力小于HPO ,HPO 的熔点高于HNO ,D项
3 3 4 3 4 3
正确。]
6.B [向CuSO 溶液中滴加氨水至过量,先生成氢氧化铜蓝色沉淀,后溶解形成铜氨溶液,
4
为深蓝色溶液,故A错误;Cu2+提供空轨道,NH 中的氮原子提供孤电子对,形成配位键,
3
故C错误;NH 分子为三角锥形,∠HNH为107°,故D错误。]
3
7.D 8.D
9.C [同周期元素,从左到右原子半径依次减小,则原子半径:C>N>O,故A错误;碳元
素的氢化物不能形成分子间氢键,故B错误;由图可知,螯合物中Mn+与氮原子和氧原子
形成配位键,配位数为6,故C正确;由图可知,螯合物中氮原子的杂化方式都为sp3杂化,
孤电子对用于形成配位键,则氮碳键的夹角均大于107°,故D错误。]10.A [吡啶( )含有与苯环类似的大π键,则吡啶中N原子也发生sp2杂化,所以价层
孤电子对占据了一个参与杂化的p轨道,A不正确;吡啶是极性分子且能与水分子间形成氢
键,而苯为非极性分子,故吡啶在水中的溶解度比苯大,B正确;因为吡啶呈碱性,能与盐
酸反应生成水溶性物质,所以除去苯中含有的少量吡啶,可用盐酸洗涤、分液、干燥有机层,
C正确;烷基是推电子基团, 分子中N原子电子云密度比 大,故 碱性较
强,D正确。]
11.B
12.D [HCHO中C原子价层电子对数为3+=3,不含孤电子对,为平面三角形结构,正、
负电荷中心不重合,为极性分子,H 为直线形分子,为非极性分子,选项A错误;CO 分
2 2
子中C原子的价层电子对数为2+=2,无孤电子对,空间结构为直线形,选项B错误;
HO不含非极性键,选项C错误;分子晶体相对分子质量越大,熔点越高,分子间含有氢键
2
时熔点较高,CHOH分子间存在氢键,则熔点为HCHOCl>C ②3∶1 (3)AC
解析 (3)该复合物中Cl、CO和HO为配体,故C错误;CO与N 的价层电子总数相同,互
2 2
为等电子体,等电子体结构和性质相似,所以CO的结构式为C≡O,故D正确。
15.(1)H O、NH 存在分子间氢键 (2)H S (3) 极性 (4)
2 2 4 2
第九章 晶体结构与性质
第 36 练 物质的聚集状态 常见晶体类型
1.D 2.B 3.B
4.C [金属能导电是因为自由电子在外加电场作用下定向移动,A错误;自由电子在热的
作用下与金属阳离子发生碰撞,实现热的传导,B错误;合金与纯金属相比,由于增加了不
同的金属或非金属,相当于填补了金属阳离子之间的空隙,所以一般情况下合金的延展性比
纯金属弱,硬度比纯金属大,D错误。]
5.D [SiCl 、AlCl 的熔、沸点低,都是分子晶体,AlCl 的沸点低于其熔点,即在低于熔
4 3 3
化的温度下就能气化,故AlCl 加热能升华,A、C正确;晶体硼的熔、沸点很高,所以晶
3体硼是共价晶体,B正确;由金刚石与晶体硅的熔、沸点相对高低可知,金刚石中的C—C
比晶体硅中的Si—Si强,D错误。]
6.A [金刚石和碳化硅都是共价晶体,在晶体中每个C原子或Si原子与相邻的4个原子形
成共价键,每个共价键为2个原子所共有,因此若晶体中含有1 mol原子,则物质含有共价
键的数目是2N ,故原子数相同的金刚石和碳化硅共价键个数之比为1∶1,A错误;在SiO
A 2
晶体中,每个Si原子与相邻的4个O原子形成Si—O,故Si原子与Si—O个数比为1∶4,
B正确;在石墨烯中,每个C原子为相邻的3个六元环所共有,则在六元环中含有的C原子
数为6×=2,因此石墨烯中碳原子和六元环个数比为2∶1,C正确;C 分子之间只有范
60
德华力,所以晶体是分子密堆积,D正确。]
7.C 8.D 9.B
10.A [Al和Ga均为第ⅢA族元素,N属于第ⅤA族元素,AlN、GaN的成键结构与金刚
石相似,则其均为共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的键长,
则N—Al的键能较大,故GaN的熔点低于AlN,A说法错误;不同元素的原子之间形成的
共价键为极性键,B说法正确;金刚石中每个C原子形成4个共价键(即C原子的价层电子
对数为4),无孤电子对,故C原子均采取sp3杂化,C原子的配位数是4,由于AlN、GaN
与金刚石结构相似,则其晶体中所有原子均采取sp3杂化,所有原子的配位数也均为4,C、
D说法正确。]
11.D [X为H元素,Y为O元素,Z为Si元素,W为C元素。XY晶体是冰,分子间存
2
在氢键,熔点高于CH ,A正确;固态XY 是HO ,属于分子晶体,B正确;SiC、晶体硅
4 2 2 2 2
为共价晶体,碳的原子半径小于硅,SiC的硬度比晶体硅的大,C正确;CO 、CO均是分子
2
晶体,D错误。]
12.(1)共价 小于 石墨中碳碳之间除σ键,还存在大π键,石墨中碳碳键的键长短于金
刚石,键能大于金刚石,沸点更高 (2)b (3)CH CHCHCHOH 能与水形成分子间氢键,
3 2 2 2
乙醚不能 (4)离子键 ②
13.(1)TiF 为离子晶体,熔点高,其他三种均为分子晶体,随相对分子质量的增大分子间作
4
用力增大,熔点逐渐升高
(2)NiO>CoO>FeO
(3)①正四面体形 分子晶体 ②NH 、AsH 、PH
3 3 3
14.(1)1s22s22p5 9 5 Cl->O2->F->Na+>Al3+
(2) 平面正三角形 共价晶体 (3)B
(4)AlF 是离子晶体,AlCl 是分子晶体 氧离子半径比氯离子半径小且氧离子带 2个电荷,
3 3
故NaO的离子键比NaCl强,熔点比NaCl高
2
解析 (1)题述涉及元素中最活泼非金属元素是 F元素,其基态原子核外电子排布式为
1s22s22p5,有9种不同运动状态的电子,能量最高且相同的电子为2p电子,有5个;电子层数越多,离子半径越大,电子层结构相同,核电荷数越小,离子半径越大,则能形成简单离
子的半径由大到小的顺序为Cl->O2->F->Na+>Al3+。(2)物质①NaO为离子化合物,其电
2
子式为 ;⑤BCl 中B原子的价层电子对数为3+0=3,空间结构为
3
平面正三角形;⑧SiO 熔点高达1 723 ℃,为共价晶体。(3)最高价氧化物对应水化物的碱
2
性越强,该元素的金属性越强,故 A正确;元素金属性强弱与最外层电子数无关,与得失
电子难易程度有关,故B错误;单质与HO反应的难易程度能判断其单质的还原性强弱,
2
从而确定元素金属性强弱,故C正确;比较同浓度NaCl和AlCl 溶液的pH来判断其金属元
3
素最高价氧化物对应水化物的碱性强弱,从而确定其金属性强弱,故D正确。
第 37 练 晶胞结构分析与计算
1.A 2.C
3.D [11B和10B互为同位素,形成的化合物在化学性质上无差异,但其物理性质不同,A
错误;该晶体结构中无自由移动的电子,不具有导电性,B错误;由图可知,该晶胞含4个
N原子,B原子位于晶胞的顶角和面心,故B原子的数目为8×+6×=4,C错误;由晶胞
示意图,1个N原子与4个B原子成键,1个B原子可以和4个N原子成键,除去该N原子
本身,则每个B原子周围有3个N原子与该N原子等距且最近,这些N原子距中心N原子
等距离且最近,总数为12,D正确。]
4.A [由晶胞结构可知,晶胞顶角上相邻的钛离子相距最近,则钛离子周围与它最接近且
距离相等的钛离子有6个,a=6;晶胞中钛原子个数为8×=1,氧原子个数为12×=3,钙
原子个数为1,则氧、钛、钙的原子个数比为 3∶1∶1,故选A。]
5.B 6.C
7.A [原子B在x、y、z轴上坐标分别为1、1、,则坐标参数为(1,1,),A错误;晶胞中
N、N之间的最近距离为面对角线长的,为a pm,则晶胞边长为a pm,B正确;该晶胞中,
Ti的个数为1+12×=4,N的个数为8×+6×=4,则该物质的化学式为TiN,C正确;以
体心Ti为例,与Ti距离相等且最近的N有6个,则Ti的配位数为6,D正确。]
8.C [晶胞参数为a pm,即a×10-10cm,则晶胞体积为a3×10-30cm3,A错误;晶胞中,
Au的个数为8×=1,Cu的个数为6×=3,则Au和Cu原子数之比为1∶3,B错误;由图
可知,Au和Cu之间的最短距离是面对角线长的一半,即a pm,D错误。]
9.C 10.C
11.B [由图甲知,砷化镓的化学式为GaAs,砷化镓中砷提供孤电子对,镓提供空轨道形
成配位键,则1 mol砷化镓中配位键的数目是N ,A正确;掺入Mn的晶体中Ga个数为7×
A
+5×=,As有4个位于体内,Mn个数为1×+1×=,Mn、Ga、As的原子个数比为∶∶4=5∶27∶32,B错误;由砷化镓晶胞结构可知,c位于侧面的面心,沿体对角线a→b方向
投影图如丙,则As的位置为7、9、11、13,C正确;由晶胞结构可知,距离最近的两个镓
原子之间的距离为面对角线长的一半,晶胞中含4个Ga和4个As,晶胞质量为 g,晶胞体
积为 cm3,则晶胞边长为×1010 pm,两个镓原子之间的最近距离为××1010 pm,D正确。]
12.A [根据晶胞结构可知CsPbBr 晶体中Cs+的配位数为12,Pb2+的配位数为6,A错误;
3
根据题干可知容忍因子其数值越接近1,晶体结构越稳定,Pb2+处于B位,t(CsPbBr )=
3
0.828,若用离子半径略小于Pb2+的离子取代Pb2+,容忍因子的分母减小、容忍因子数值增
大,越来越接近1,会提高晶体的稳定性,C正确;t=1说明(r +r )=r +r ,则A、B位
B C A C
的离子均恰好与C位的离子相切,D正确。]
13.2∶3 2∶1∶1 Zn2+
14.8 2-x
15.a a
解析 观察图(a)和图(b)知,4个铜原子相切并与面对角线平行,有(4x)2=2a2,x=a pm。镁
原子堆积方式类似金刚石,有y=a pm。晶胞体积为(a×10-10)3 cm3,代入密度公式计算即
可。
第十章 化学反应与能量
第 38 练 反应热 热化学方程式
1.B 2.C
3.D [A项,Ba(OH) ·8H O与NH Cl的反应属于吸热反应,错误;B项,铝片更换为等质
2 2 4
量的铝粉,没有改变反应物的本质,放出的热量不变,错误;C项,铁质搅拌器导热性好,
热量损失较大,错误;D项,NaOH固体溶于水时放热,使测定结果数值偏高,正确。]
4.C [能量越低越稳定,根据图示,等物质的量的HNC比HCN的能量高,HCN比HNC
更稳定,A错误;HCN转化为HNC是吸热反应,吸热反应的发生不一定需要加热,B错误;
加入催化剂,能降低反应的活化能,反应的热效应不变,D错误。]
5.C [2 mol SO 、1 mol O 充入恒容容器中,达平衡时,SO 的转化率为50%,则反应了的
3 2 2
SO 的物质的量为1 mol,放出热量98.3 kJ,故热化学方程式为2SO (g)+O(g)2SO (g)
2 2 2 3
ΔH=-196.6 kJ·mol-1或SO (g)+O(g)SO (g) ΔH=-98.3 kJ·mol-1。]
2 2 3
6.B [催化剂能改变反应途径,降低反应的活化能,加快化学反应速率。反应②的活化能
低,反应速率快,但反应①与②同时发生,不能确定反应②是否使用催化剂,B说法错
误。]7.D [由图像可知物质A、B的能量相对大小,A比B能量高,B更稳定,所以A→B释放
能量,是放热反应,A、B错误;催化剂能改变反应途径和活化能大小,但不能改变焓变,
C错误。]
8.D 9.D 10.D
11.D [甲图中反应物总能量高于生成物总能量,是放热反应,故 A错误;乙图体现的是
CO 转化成CO的能量变化,而碳的燃烧热是1 mol C全部转化成CO 放出的热量,故B错
2 2
误;丙图中V 为20 mL时,温度最高,说明此时酸碱反应完全,又因为实验中始终保持 V
2 1
+V =60 mL,则V =40 mL,由酸碱中和关系式:2NaOH~HSO 可知,HSO 和NaOH溶
2 1 2 4 2 4
液的浓度不同,故C错误。]
12.C [据反应物和生成物所具有的能量可以判断出,该反应为放热反应,故 A错误;根
据图示,过渡态1中Ni的成键数目为2,过渡态2中Ni的成键数目为3,反应过程中Ni的
成键数目发生了变化,故B错误;根据图示,中间体2到过渡态2的能垒(活化能)最大,为
204.32 kJ·
mol-1,故C正确;根据图示,Ni是反应物不是催化剂,故D错误。]
13.(1)< (2)2Cl (g)+2HO(g)+C(s)===4HCl(g)+CO(g) ΔH=-290.0 kJ·mol-1
2 2 2
(3)98.0 kJ (4)CO (g)+3H(g)===CHOH(g)+HO(g) ΔH=-46 kJ·mol-1
2 2 3 2
14.(1)B A→B是甲烷中的C—H断裂过程,断键吸热,A的能量小于B;B→C是形成化
学键的过程,成键放热,B 的能量大于 C (2)664.75 (3)271 (4)·CO +·H+
2
H(g)===·HOCO+H(g) -2.05N
2 2 A
解析 (3)反应Ⅰ中断裂2 mol C—H、形成1 mol碳碳π键和1 mol H—H,故416 kJ·mol-
1×2-E(碳碳π键)-436 kJ·mol-1=+125 kJ·mol-1,解得E(碳碳π键)=271 kJ·mol-1。
第 39 练 盖斯定律及应用
1.A
2.B [混合时浓硫酸在被稀释的过程中放热;浓、稀硫酸在与 Ba(OH) 溶液反应时还会形
2
成BaSO 沉淀,Ba2+、SO之间形成化学键的过程中也会放出热量。因放热反应的 ΔH取负
4
值,故ΔH<ΔH<ΔH。]
1 2 3
3.C
4.B [反应(ⅰ)放出能量,反应(ⅱ)吸收能量,故(ⅰ)中I 的能量高,为气态,(ⅱ)中I 为固
2 2
态,故A项错误;根据盖斯定律可知,(ⅱ)-(ⅰ)即得到I(s)I(g) ΔH=+35.96 kJ·mol-
2 2
1,说明1 mol固态碘与1 mol气态碘所含的能量相差35.96 kJ,故B项正确;两个反应的生
成物为相同状态的同种物质,其稳定性相同,故C项错误;254 g I (g)和2 g H (g)的物质的
2 2
量均为1 mol,因反应(ⅰ)是可逆反应,转化率达不到100%,则反应放热小于9.48 kJ,故D项错误。]
5.B [由图像可知,反应HCO(aq)+H+(aq)===CO(g)+HO(l)为吸热反应,A错误;由图
2 2
像可知,能量差值越大,反应热的绝对值越大,ΔH 、ΔH 都为放热反应,则ΔH <ΔH ,C
1 2 1 2
错误;加入催化剂,反应热不变,D错误。]
6.B
7.A [由题知表示各物质燃烧热的热化学方程式分别为①C(s)+O(g)===CO(g) ΔH=-
2 2
393.5 kJ·mol-1;② H(g)+O(g)===HO(l) ΔH=-285.8 kJ·mol-1;③ CHCOOH(l)+
2 2 2 3
2O(g)===2CO(g) + 2HO(l) ΔH = - 870.3 kJ·mol - 1 。 则 2C(s) + 2H(g) +
2 2 2 2
O(g)===CHCOOH(l)可由反应①×2+②×2-③得出,则反应热为(-393.5 kJ·mol-1)×2+
2 3
(-285.8 kJ·mol-1)×2-(-870.3 kJ·mol-1)=-488.3 kJ·mol-1。]
8.A 9.B
10.B [大多数化合反应为放热反应,而放热反应的反应热(ΔH)为负值,故A错误;铝热
反应为放热反应,故ΔH<0,而由④-③可得:2Al(s)+Fe O(s)===Al O(s)+2Fe(s)
5 2 3 2 3
ΔH =ΔH -ΔH<0,可得ΔH<ΔH 、ΔH =ΔH -ΔH ,故B正确、D错误;将(②+③)×可
5 4 3 4 3 3 4 5
得:2H(g)+O(g)===2HO(g) ΔH=(ΔH+ΔH),故C错误。]
2 2 2 1 2 3
11.C [根据盖斯定律可知,ΔH=ΔH+ΔH+ΔH+ΔH-ΔH,故A错误;原子失去电子
6 1 2 3 4 5
变为离子是吸热过程,Ca和Mg属于同主族元素,Ca的金属性强于Mg,Ca→Ca2+吸收的
热量小于Mg→Mg2+吸收的热量,即ΔH<ΔH,故B错误;气态卤素原子得电子生成气态卤
7 3
素离子是放热过程,Cl非金属性强于I,即Cl→Cl-放出的热量比I→I-放出的热量多,即
ΔH>ΔH ,故C正确;MgCl (s)===Mg2+(g)+2Cl-(g)属于吸热过程,即ΔH>0,Mg2+(g)、
8 4 2 5
2Cl-(g)转化成Mg2+(aq)、2Cl-(aq)要放出热量,发生MgCl (s)===Mg2+(aq)+2Cl-(aq)吸收热
2
量比MgCl (s)===Mg2+(g)+2Cl-(g)少,即ΔH<ΔH,故D错误。]
2 9 5
12.C [环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此,ΔH <0,
1
ΔH <0,A不正确;苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊
2
的共价键,因此,其与氢气完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生
的加成反应的反应热之和,即ΔH≠ΔH +ΔH ,B不正确;由于1 mol 1,3-环己二烯与氢气
3 1 2
完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量更多,则ΔH>ΔH;苯与氢气
1 2
发生加成反应生成1,3-环己二烯的反应为吸热反应(ΔH>0),根据盖斯定律可知,苯与氢气
4
完全加成的反应热:ΔH =ΔH +ΔH ,因此ΔH>ΔH ,ΔH =ΔH -ΔH ,C正确、D不正
3 4 2 3 2 2 3 4
确。]
13.(1)-307 (2)+6
14.(1)E-E+ΔH+E-E (2)-911.9
1 2 3 4
解析 (1)设反应过程中第一步的产物为M,第二步的产物为N,则X→M的ΔH =E -E ,
1 1 2
M→N的ΔH=ΔH,N→Y的ΔH=E-E,根据盖斯定律可知,X(g)→Y(g)的焓变为ΔH+
2 3 3 4 1ΔH+ΔH=E-E+ΔH+E-E。
2 3 1 2 3 4
(2)根据盖斯定律,①+②+2×③可得反应CaO(s)+2Al(s)+7HO(l)===Ca2+(aq)+2[Al(OH) ]-
2 4
(aq)+3H(g),则ΔH =ΔH +ΔH +2ΔH =(-65.17 kJ·mol-1)+(-16.73 kJ·mol-1)+2×(-
2 4 1 2 3
415.0 kJ·
mol-1)=-911.9 kJ·mol-1。
15.(1)2C H(g)+9O(g)===6CO(g)+6HO(g) ΔH=-3 854 kJ·mol-1 (2)2H S+
3 6 2 2 2 2
O=====2HO+2S↓[或2HS(g)+O(g)=====2HO(l)+2S(s)] 放出(a+) kJ热量 作催化剂
2 2 2 2 2
(或降低反应活化能)
第 40 练 原电池 常见化学电源
1.D [甲不是原电池,故A错误;甲中锌棒直接与稀HSO 接触,发生化学腐蚀,乙中构
2 4
成了原电池,负极失去电子速率加快,因此正极放出氢气的速率增大,故B错误。]
2.C
3.C [由题意可知,铝为负极,发生氧化反应,A项错误;原电池工作时,阳离子向正极
移动,阴离子向负极移动,B项错误;氧气在正极得电子,发生还原反应,C项正确;原电
池中,电流由正极流向负极,即由铂网经外电路流向铝板,D项错误。]
4.A 5.C
6.B [锂-海水电池的总反应为4Li+2HO+O===4LiOH,M极上Li失去电子发生氧化反
2 2
应,则M极为负极,电极反应为Li-e-===Li+,N极为正极,电极反应为O +2HO+4e-
2 2
===4OH-,故B错误;海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶
液,故A正确;Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和 Li反应,并传导
离子,故C正确;该电池不可充电,属于一次电池,故D正确。]
7.C [放电过程为原电池工作原理,所以钾离子均向正极移动,A错误;碱性环境下,
NH-O 清洁燃料电池总反应为NH +O===N +2HO,未消耗KOH,所以KOH的物质的
2 4 2 2 4 2 2 2
量不变,其他两种燃料电池根据总反应可知,KOH的物质的量均减小,B错误;理论放电
量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为 m g,则甲醇、NH 和
2 4
(CH)NNH 的放电量分别是×6、×4、×16,通过比较可知(CH)NNH 理论放电量最大,
3 2 2 3 2 2
C正确;根据转移电子数守恒和总反应式可知,消耗 1 mol O 生成氮气的物质的量为 1
2
mol,在标准状况下为22.4 L,D错误。]
8.B 9.C
10.C [装置①中现象说明浓硝酸具有强氧化性,能将Fe钝化,但形成的致密氧化膜的成
分复杂,不能仅用Fe O 表示,A错误;装置②中插入Cu并连接导线后,由于Fe表面已钝
2 3
化,此时Cu为负极,Fe为正极,Fe表面的氧化物得电子发生还原反应而溶解,待氧化膜完全溶解后,Fe为负极,Cu为正极,然后Fe表面再次发生钝化,如此往复多次,B错误;当
Fe为负极时,Fe发生钝化,钝化过程中会产生红棕色气泡,C正确;Cu表面与浓硝酸发生
氧化还原反应:Cu+4HNO(浓)===Cu(NO ) +2NO ↑+2HO,此外,当Cu作正极时,Cu
3 3 2 2 2
表面发生的电极反应为NO+2H++e-===NO ↑+HO,当Cu作负极时,Cu表面发生的电
2 2
极反应为Cu-2e-===Cu2+,D错误。]
11.C
12.D [放电时为原电池,质子向正极移动,Pt1电极为负极,则该电池放电时质子从Pt1
电极移向Pt2电极,A错误;Pt1电极为负极,发生氧化反应,SO 被氧化为硫酸,电极反应
2
式为SO +2HO-2e-===SO+4H+,B错误;酸性条件下,氧气得电子生成水,C错误;根
2 2
据转移电子数相等可知,放电过程中消耗的SO 和O 的体积比为2∶1,D正确。]
2 2
13.(1)SO -2e-+2HO===4H++SO (2)2 mol
2 2
解析 (1)由图可知,该装置为原电池,电极a为电池的负极,通入的二氧化硫气体在负极
失去电子发生氧化反应生成硫酸,电极反应式为SO -2e-+2HO===4H++SO。(2)由反应
2 2
HS+HSO ===SO ↑+S↓+2HO、S+O===SO 可知,1 mol H S参加反应时,负极上有2
2 2 4 2 2 2 2 2
mol二氧化硫参与放电,由得失电子守恒可得:2 mol×2=n(H )×2,解得n(H )=2 mol。
2 2
14.(1)①铂 ②14CO+12e-+8HO===HC==CH+12HCO ③16.8 L (2)C+xe-+xNa+
2 2 2 2
===NaC Na TMO+xe-+xNa+===NaTMO
x 1-x 2 2
第 41 练 新型化学电源分类突破
1.D 2.D
3.D [由题意知,放电时负极反应为Li-e-===Li+,正极反应为(2-x)O +4Li++4e-
2
===2LiO (x=0或1),电池总反应为(1-)O +2Li===LiO 。充电时的电池总反应与放电
2 2-x 2 2 2-x
时的电池总反应互为逆反应,故充电时电池总反应为LiO ===2Li+(1-)O ,D项正确;
2 2-x 2
该电池放电时,金属锂为负极,多孔碳材料为正极,A项错误;该电池放电时,外电路电子
由锂电极流向多孔碳材料电极,B项错误;该电池放电时,电解质溶液中Li+向多孔碳材料
区迁移,充电时电解质溶液中的Li+向锂电极区迁移,C项错误。]
4.B 5.C
6.C [充电时为电解池,由题目信息知,光照时,光催化电极产生电子和空穴,驱动阴极
反应(Li++e-===Li)和阳极反应(Li O +2h+===2Li++O),则充电时,电池的总反应为
2 2 2
LiO===2Li+O ,因此,充电效率与光照产生的电子和空穴量有关,A、B正确;放电时,
2 2 2
金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
放电时,电池总反应为 2Li+O===LiO ,则正极反应为 O +2Li++2e-===LiO ,D正
2 2 2 2 2 2
确。]7.A [由题图知,M极为负极,N极为正极,HN(CH )NH 在负极上失电子发生氧化反
2 2 2 2
应,电极反应式为HN(CH )NH +4HO-16e-===2CO +N +16H+,A正确;充电时二次
2 2 2 2 2 2 2
电池的正极应与外接电源的正极相连,即与N极相连,B错误;H+通过质子交换膜由M极
移向N极,C错误;当N电极消耗标况下2.24 L O 时,则转移× 4=0.4 mol电子,所以有
2
0.4 mol电子从M极流向N极,D错误。]
8.A [充电时为电解池装置,阳离子移向阴极,Na+由硫电极迁移至钠电极,A错误;放
电时Na在a电极失去电子,失去的电子经外电路流向 b电极,即电子在外电路的流向为
a→b,B正确;将题给硫电极发生的反应依次编号为①②③,由×①+×②+③可得正极的
反应式为2Na++S+2e-―→NaS,C正确;炭化纤维素纸中含有大量的炭,炭具有良好的
8 2 x
导电性,可以增强硫电极的导电性能,D正确。]
9.B 10.D
11.C [Zn是活泼金属,放电时,Zn为原电池的负极,发生氧化反应,A项正确;放电时,
Y电极是正极,发生还原反应,电极反应为PTO+Zn2++2e-===PTO-Zn,B项正确;充电
时,该装置为电解池,X电极与外加电源的负极相连,则Zn2+向X电极移动,C项错误,D
项正确。]
12.A [充电时n接电源的负极,作电解池的阴极,Zn2+通过阳离子交换膜向阴极定向迁移,
故由左侧流向右侧,A正确;放电时,负极Zn溶解生成Zn2+,Zn2+通过阳离子交换膜向正
极定向迁移,故负极区溶液质量不变,B错误;充电时阴极的电极反应式为 Zn2++2e-
===Zn,C错误;若将阳离子交换膜换成阴离子交换膜,放电时正、负极不会改变,D错
误。]
13.(1)阳 (2)NH+2O===NO+HO+2H+ (3)26
2 2
14.不变 18
解析 由题图可知,电子由M极流向N极,说明M极为负极,电极反应式为2HO-4e-
2
===O +4H+;N极为正极,电极反应式为CO +2H++2e-===CO+HO。导线中通过2 mol
2 2 2
电子后,则负极产生2 mol H+,此时有2 mol H+通过质子交换膜移向N极,即M极电解质
溶液中H+的量不变,电解质溶液的pH不变;由正极的电极反应式可知,每转移2 mol电子
N极电解质溶液中增加1 mol H O,则Δm=18 g。
2
第 42 练 电解池 金属的腐蚀与防护
1.B 2.C
3.B [用电解法精炼粗银,银单质失电子生成银离子,发生氧化反应,粗银与电源正极相
连,故A错误;由得电子能力:Ag+>Cu2+,阴极为Ag+得电子生成Ag,电极反应为Ag++e-===Ag,故B正确;粗银作阳极,Cu生成Cu2+,Pt成为阳极泥,故C错误;电解精炼银
时,粗银中比银活泼的铜会失电子形成离子进入溶液,则电解液中 c(Ag+)浓度不可能增大,
故D错误。]
4.C [金属M失电子,其活动性应比铁强,B错误;M失去的电子流入钢铁设施表面,因
积累大量电子而被保护,C正确;海水中所含电解质的浓度远大于河水中的,因此钢铁设施
在海水中腐蚀的速率快,D错误。]
5.B 6.B
7.D [①是密闭体系,NaCl溶液中溶解的O 较少,不足以使生铁片明显锈蚀,A项正确;
2
苯属于非电解质,②中无电解质溶液,不满足电化学腐蚀的条件,B项正确;根据③中现象,
铁在中性环境下发生吸氧腐蚀,正极反应式为O+4e-+2HO===4OH-,C项正确;根据现
2 2
象可知,③中发生吸氧腐蚀,③中观察到明显锈蚀,说明苯不能隔绝O,D项错误。]
2
8.A [M电极为正极,N电极为负极,电子从N电极经导线流向M电极,A错误;正极的
电极反应式为O+2HO+4e- ===4OH-,因此正极区附近溶液的pH增大,C正确;电路中
2 2
转移0.01 mol电子时,有=0.002 5 mol氧气反应,质量为0.002 5 mol×32 g·mol-1=0.08 g,
D正确。]
9.D 10.A
11.A [阶段Ⅰ中阴极上HO→H ,阳极上Na MnO →Na MnO ,则电源a为负极、b
2 2 0.44 2 0.44-x 2
为正极,A项错误;阶段Ⅰ中阴极生成H ,阶段Ⅱ中阳极生成Cl ,避免氢气和氯气混合,
2 2
且有利于提纯NaOH,C项正确;若阶段Ⅰ在饱和食盐水中进行,则阴极和阳极分别产生H
2
和Cl,达不到改进目的,D项正确。]
2
12.D [由图可知,在M电极I-转化为I,发生氧化反应,则M电极为阳极,N电极为阴
极,M接电源的正极,A错误;阳极反应式为3I--2e-===I,B错误;二氧化硫在电解池中
与溶液中的I反应,离子方程式为SO +I+2HO===3I-+SO+4H+,此时转移2个电子,
2 2
同时生成4个氢离子,而在阴极转移2个电子时消耗2个氢离子,则溶液中氢离子浓度增大,
pH减小,C错误;由关系式:SO ~I~2e-,电解消耗x库仑电量,则二氧化硫的体积分数
2
为×100%=×100%,D正确。]
13.(1)< (2)O +4e-+2HO===4OH- (3)H 1 1s22s22p63s23p5
2 2 2
14 . (1)①PbO X PbO + SO + 4H + + 2e - ===PbSO + 2HO ② Al - 3e - +
2 2 4 2
3HO===Al(OH) (胶体)+3H+、2HO-4e-===O↑+4H+ ③0.4
2 3 2 2
(2)①CO+2e-===CO+O2- ②6∶5
2
解析 (1)③消耗103.5 g(0.5 mol)Pb,转移电子的物质的量为 1 mol,装置的电流效率为
80%,故装置Ⅱ阴极上参与反应的电子为0.8 mol,阴极反应式为2HO+2e-===H↑+2OH
2 2
-,即产生0.4 mol H 。(2)①由图示可知,阴极上CO―→CO,且固体电解质能传导O2-,
2 2
则阴极反应式为CO +2e-===CO+O2-。②假设生成的乙烯和乙烷的物质的量分别为2 mol
2和1 mol,由2CH―→C H+2H、2CH―→C H+H 知,生成2 mol乙烯和1 mol乙烷时,
4 2 4 2 4 2 6 2
共脱去5 mol H ,转移10 mol e-,根据电子转移数目守恒可知,此时消耗的CO 为5 mol,
2 2
消耗的CH 为6 mol,即消耗的CH 和CO 的体积比为6∶5。
4 4 2
第 43 练 电解原理应用新拓展
1.C
2.B [根据图示可知,在b电极上产生N ,N元素失去电子化合价升高,所以b电极为阳
2
极,连接电源的正极,A错误;a电极上产生H ,a电极为阴极,电极反应式为2NH +2e-
2 3
===H↑+2NH,B正确;电解过程中,K+会向阴极区定向移动,最终导致阴极附近K+浓
2
度增大,C错误;每产生1 mol H ,转移2 mol电子,每产生1 mol N ,转移6 mol电子,故
2 2
阴极产生的H 与阳极产生的N 的物质的量之比是3∶1,D错误。]
2 2
3.D [在电解装置中,电子由电源的负极流入阴极,所以a极为负极,X极为阴极,Y极
为阳极,b极为正极,A正确;在电解池中,阴离子向阳极(Y极)迁移,B正确;Y极上钾汞
齐发生氧化反应,C正确;析出1 mol铝时转移3 mol电子,即转移1 mol电子理论上析出9
g Al,D错误。]
4.C
5.C [由(NH )SO →(NH )SO ,氧元素化合价升高被氧化,故右侧Pt电极为阳极,b为
4 2 4 4 2 2 8
外接电源正极,a为外接电源负极,左侧Pt电极为阴极。阴极氧气被还原,阳极硫酸根离子
被氧化,电解总反应正确,B正确;根据阳极产物可知,反应需要消耗硫酸根离子,阴离子
交换膜不可用阳离子交换膜替代,C错误;电解池工作时,Ⅰ室发生反应:O +2e-+2H+
2
===HO,同时SO移向阳极,故Ⅰ室溶液质量理论上逐渐减小,D正确。]
2 2
6.A [该电解池的总反应方程式为2CO +2HO===C H +3O ,多晶铜电极为阴极,该电
2 2 2 4 2
极的电极反应式为14CO +8HO+12e-===C H +12HCO,铂电极为阳极,该电极的反应式
2 2 2 4
为12HCO-12e-===12CO +3O +6HO。HCO在铂电极发生反应,并且电解前后电解液浓
2 2 2
度几乎不变,所以溶液中HCO通过阴离子交换膜向左槽移动,故C错误;由多晶铜电极电
极反应式分析可知,当电路中通过0.6 mol电子时,理论上能产生0.05 mol C H ,该题目没
2 4
有说明条件为标准状况,故D错误。]
7.A [A膜允许氢离子通过,是阳离子交换膜,故A错误;电极Y上是氢离子得电子生成
氢气,是阴极,发生还原反应,故B正确;阳极底物失去电子生成二氧化碳和氢离子,电
极反应:C H O+6HO-24e-===6CO↑+24H+,故C正确。]
6 12 6 2 2
8.C 9.B
10.D [a极区的稀氢氧化钠溶液变为浓氢氧化钠溶液,说明a极区生成了氢氧化钠,即钠离子通过膜1向a极区迁移,膜1为阳离子交换膜;同理,氯离子通过膜2向b极区迁移,
膜2为阴离子交换膜,A项正确;提纯蛋白质,不能让蛋白质(胶体粒子)通过膜1、膜2,所
以膜1、膜2的孔径应不大于半透膜的孔径,B项正确;a极为阴极,发生还原反应:2HO
2
+2e-===2OH-+H↑,C项正确;每转移2 mol电子,结合电极反应和电荷守恒可知,理
2
论上乳清减少的质量为2 mol NaCl的质量,即质量减少117 g,D项错误。]
11.C [M电极通入O ,发生反应生成自由基·OH,反应式为O +2e-+2H+===2·OH,M
2 2
作阴极,A正确;N为阳极,电解时阴离子向阳极移动,所以OH-透过膜a向N极移动,B
正确;1 mol甲醛生成1 mol CO 转移4 mol电子,1 mol苯酚生成6 mol CO 转移28 mol电
2 2
子,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7,D正确。]
2
12.Fe-2e-===Fe2+ 2NO+8H++6Fe2+===N↑+6Fe3++4HO
2 2
13.(1)Cu、Ag 减小 (2)c(H SiF)增大,电解液中c(H+)增大,阴极发生副反应:2H++2e
2 6
-===H↑,影响Pb2+放电,使铅产率减小
2
14.(1)使阴极表面尽可能被CO 附着,减少析氢反应的发生(减少氢离子在阴极上放电的几
2
率),提高含碳化合物的产率
(2)2.8 (3)为确定阴极上生成的含碳化合物源自CO 而非有机多孔电极材料
2
解析 (2)控制电压为0.8 V,产生0.2 mol氢气和0.2 mol乙醇,根据电极反应2H++2e-
===H↑,2CO +12e-+12H+===C HOH+3HO,故电解时转移电子的物质的量为0.4 mol
2 2 2 5 2
+2.4 mol=2.8 mol。
第十一章 化学反应速率与化学平衡
第 44 练 化学反应速率及影响因素
1.B 2.D 3.C
4.D [铁是固体,增加铁的量,浓度不变,反应速率不变,①与题意不符;将容器的体积
缩小一半,反应体系中气体物质的浓度增大,则化学反应速率增大,②符合题意;体积不变,
充入N 使体系压强增大,但各物质的浓度不变,所以反应速率不变,③与题意不符;保持
2
体积不变,充入水蒸气使体系压强增大,反应物浓度增大,反应速率增大,④符合题意。]
5.D [浓度和压强的变化是改变单位体积内活化分子的总数,活化分子的百分数不变;温
度、催化剂是改变活化分子的百分数,单位体积内分子总数不变。]
6.B [a的活化能更高,A错误;该反应为放热反应,反应物断键吸收的总能量小于生成
物成键释放的总能量,B正确;a与b相比,b的活化能小,b中活化分子的百分数更高,反
应速率更快,C、D错误。]7.C [由表中数据可计算,42~242 s,消耗CHCHO的平均反应速率为=1.02×10-2mol·L
3
-1·s-1,A项正确;随着反应的进行,c(CHCHO)减小,反应速率减慢,所以第384 s时的瞬
3
时速率大于第665 s时的瞬时速率,B项正确;由于CHCHO的初始浓度及气体体积未知,
3
故无法计算反应至105 s时,混合气体的体积,C项错误。]
8.D 9.C
10.D [由②③可知,温度相同时,pH越小,氧化率越大,由①②可知,pH相同时,温度
越高,氧化率越大,A、B错误;Fe2+的氧化率除受pH、温度影响外,还受其他因素影响,
如浓度等,C错误。]
11.C [由题中信息可知,瞬时速率与切线的斜率有关,切线的斜率越大瞬时速率越大,由
图知A、B、C三点斜率大小:A>B>C,即瞬时速率:A>B>C,故A错误、C正确;催
化剂只能改变化学反应的速率,不能改变化学反应本身,HO 本身可以发生分解反应,故
2 2
D错误。]
12.v(HCl)=2v(Cl )=2×=2× =1.8×10-3 mol·min-1
2
13.(1)2 (2)15 (3)0.45
解析 (1)控制CO 起始浓度为0.25 mol·L-1,根据CO的瞬时生成速率=kcm(H )·c(CO)和H
2 2 2 2
起始浓度呈直线关系可知,m=1,该反应的反应级数为1+1=2。(2)将图像上的点(0.4,1.5)
代入v=kc(H )·c(CO)中有1.5=0.4×k×0.25,解得k=15。(3)由于CO 起始浓度为0.25 mol·L
2 2 2
-1,反应进行到某一时刻时,测得CO 的浓度为0.2 mol·L-1,Δc(CO )=(0.25-0.2) mol·L-
2 2
1=0.05 mol·L-1,Δc(H )=Δc(CO)=0.05 mol·L-1,H 的瞬时浓度为 c(H )=(0.2-
2 2 2 2
0.05)mol·L-1=0.15 mol·L-1,此时CO的瞬时生成速率v=15×0.15×0.2 mol·L-1·s-1=0.45
mol·L-1·s-1。
14.(1)探究浓度对反应速率的影响 向反应物中加入等量同种催化剂(或升高相同温度)
(2)升高温度,反应速率加快 MnO 对过氧化氢分解的催化效果更好
2
(3)产生20 mL气体所需的时间
第 45 练 过渡态理论 催化剂对化学反应的影响
1.D 2.C 3.C
4.C [如图能量变化可知,生成物的总能量低于反应物的总能量,该反应为放热反应,
ΔH<0,A项正确;两步反应均为放热反应,总反应的化学反应速率由反应速率慢的基元反
应决定,即反应①决定,B项正确。]
5.B [整个过程中H+是催化剂,先参与第一步反应,在最后一步反应生成,故 A正确;
由图可知该历程中最小的能垒(基元反应活化能)为131 kJ·mol-1,故B错误;决定总反应速率的是活化能或能垒最高的基元反应,由图可知,该基元反应为 ―→CHOCH
3 3
+H+,故C正确。]
6.A [由于绝对值|E-E|<|E-E|,该值为负值,去掉绝对值后,E-E>E-E,A正确;
3 2 4 1 3 2 4 1
由图可知,反应Ⅰ的活化能较大,反应Ⅰ决定整个反应的速率,B错误;催化剂不改变焓变,
C错误;根据盖斯定律,反应Ⅰ+Ⅱ可得目标方程CHOH(g)+HO(g)===CO(g)+3H(g)
3 2 2 2
ΔH=ΔH+ΔH,D错误。]
1 2
7.C 8.A
9.D [第三步反应为慢反应,则反应的活化能较大,是决速反应,故 A错误;Cl和COCl
都是该总反应的中间产物,故B错误;从速率方程v=k (Cl )·c(CO)中可以看出,c(CO)、
2
c(Cl )分别增大相同的倍数,对总反应速率的影响程度c(CO)大,故C错误;升温可以提高
2
反应物中活化分子的百分数,使k增大导致反应速率加快,故D正确。]
10.D [由图b可知,随着pH减小,n(N )增大,n(氨态氮)变化不大,n(NO)减小,说明pH
2
越小,Pd对NO的吸附能力越强,A正确;由图b可知,pH不同还原产物也不同,pH为4
时还原产物主要为N ,pH为12时,还原产物几乎全是NO,故通过调节溶液的pH,可使
2
NO更多的转化为N ,B正确;由图b可知,pH=12时,还原产物几乎全是NO,则每处理
2
6.2 g NO转移电子×2=0.2 mol,根据得失电子守恒可知,理论上消耗标准状况下×22.4
L·mol-1=2.24 L H ,D错误。]
2
11.B [由表中数据可知,在0~20 min、20~40 min、40~60 min,X Y的浓度均减少了
2
0.02 mol·L-1,即该反应速率与起始浓度无关,为匀速反应,故a=0,v=k,A、D错误,
B正确;0~20 min内,k=v===1.0×10-3 mol·L-1·min-1,C错误。]
12.(1)温度升高,催化剂活性增强,反应速率加快 (2)> Ⅳ
13.迅速上升段是催化剂活性随温度升高而增大,与温度升高共同使 NO 去除反应速率迅
x
速增大;上升缓慢段主要是温度升高引起的 NO 去除反应速率增大 催化剂活性下降;
x
NH 与 O 反应生成了 NO
3 2
14.(1)Ⅰ 高 (2)随着H 体积分数的增加,NO反应完后,在Pt催化下,N 和H 反应生成
2 2 2
NH ,所以N 的体积分数呈下降趋势 (3)0.001 20%
3 2
解析 (3)由题给数据可知,0~20 min,反应速率为v(N O)==0.001 mol·L-1·min-1。由
2
题给数据可知,反应速率v(N O)与反应物NO的浓度无关,反应速率恒定为0.001 mol·L-
2 2
1·min-1,则反应至40 min时NO的转化率α=×100%=20%。
2第 46 练 化学平衡状态与化学平衡常数
1.B 2.A 3.D
4.A [若X 完全转化为Z,则X、Y、Z的浓度分别是0 mol·L-1、0.2 mol·L-1、0.4 mol·L-
2 2 2
1;若Z完全转化为X 、Y ,则X 、Y 、Z的浓度分别是0.2 mol·L-1、0.4 mol·L-1、0 mol·L
2 2 2 2
-1;反应为可逆反应,反应物不能完全转化,所以 00,为吸热反应,则平衡常数K
增大,C正确;加入催化剂,只能改变反应速率,平衡不移动,则不能提高合成气的平衡产
率,D错误。]
7.B 8.A
9.B [①反应中各物质均为气体,混合气体的总质量不变,且反应在恒容条件下进行,则
混合气体的密度始终不变,故不能据此判断反应2是否达到平衡,错误;②反应2的平衡建
立过程中,气体总物质的量不断变化,则气体压强不断变化,当气体压强保持不变时,反应
2达到平衡状态,正确;③平衡建立过程中,混合气体的总质量不变,但其总物质的量不断
变化,故当气体的平均摩尔质量保持不变时,反应2达到平衡状态,正确;④保持不变,则
c(NO )、c(N O)均保持不变,反应2达到平衡状态,正确;⑤反应1是不可逆反应,O 的物
2 2 4 2
质的量始终保持不变,不能据此判断反应2是否达到平衡,错误;⑥v (N O)∶v (NO )=
正 2 4 逆 2
1∶2,正、逆反应速率相等,反应2达到平衡状态,正确。]
10.C [达到平衡时消耗X的物质的量浓度为(0.1-0.05) mol·L-1=0.05 mol·L-1,因此X的
转化率为50%,A项正确;根据化学反应速率之比等于化学计量数之比,三种组分的系数之
比为(0.1-0.05)∶(0.2-0.05)∶0.1=1∶3∶2,因此反应方程式为X+3Y2Z,平衡常数K
==1 600,B项正确;化学平衡常数只受温度的影响,与浓度、压强无关,C项错误、D项
正确。]
11.C12.C [A项,因起始浓度相同,X、Y两点转化率相同,所以MTP的浓度也相等,正确;
B项,由图可知,X点曲线斜率大于Z点,且Z点转化率高,此时TOME的浓度只有0.02a
mol·L-1,所以瞬时速率:v(X)>v(Z),正确;C项,若Z点为平衡点,此时c(TOME)=0.02a
mol·L-1,c(MTP)= 0.98a mol·L-1,但因移出甲醇,甲醇浓度不为 0.98a mol·L-1,错误;
D项,0~150 min时间内,Δc(MTP)=0.67a mol·L-1,正确。]
13.(1)吸 0.20 (2)逆反应方向 不变 (3)升高温度
14.(1)B (2)
15.(1)放热 (2)< (3)2.7
解析 (1)根据数据可知,随着温度的升高,平衡常数减小,平衡逆向移动,逆反应为吸热
反应,则正反应为放热反应。(2)对于某时刻,浓度商Q===12.5,大于250 ℃的平衡常
数,反应逆向进行,正反应速率小于逆反应速率。(3)同温同体积的情况下,压强之比等于
物质的量之比,平衡时与起始时的气体压强比值为0.7,起始的物质的量为1 mol+2 mol=3
mol,则平衡时的物质的量为3 mol×0.7=2.1 mol。设CO转化的物质的量为x mol,列三段
式:
CO(g)+2H(g)CHOH(g)
2 3
起始/mol 1 2 0
转化/mol x 2x x
平衡/mol 1-x 2-2x x
1-x+2-2x+x=2.1,得x=0.45;体积为2 L,则有K==≈2.7。
第 47 练 化学平衡常数的综合计算
1.B
2.B [反应初始4 s内v(X)=0.005 mol·L-1·s-1,根据速率之比等于化学计量数之比,可知
v(Y)=0.005 mol·L-1·s-1,则4 s内Δc(Y)=0.005 mol·L-1·s-1×4 s=0.02 mol·L-1,Y的起始
浓度为=0.4 mol·L-1,故4 s时c(Y)=0.4 mol·L-1-0.02 mol·L-1=0.38 mol·L-1,A项错误;
设平衡时X的浓度转化量为x mol·L-1,则:
X(g)+ Y(g) R(g)+Q(g)
起始/(mol·L-1) 0.1 0.4 0 0
转化/(mol·L-1) x x x x
平衡/(mol·L-1) 0.1-x 0.4-x x x
故=1.0,解得x=0.08,所以平衡时X的转化率为×100%=80%,B项正确;由表格数据可知,温度升高,化学平衡常数减小,平衡逆向移动,C项错误;1 200 ℃时反应X(g)+Y(g)
R(g)+Q(g)的平衡常数为0.4,所以反应R(g)+Q(g) X(g)+Y(g)的平衡常数为=2.5,
D项错误。]
3.D
4.C [升高温度平衡右移,正反应为吸热反应,A项正确;25 ℃平衡时,p(NH )=12.0
3
kPa×=8 kPa,p(CO)=12.0 kPa×=4 kPa,K =(8 000 Pa)2×4 000 Pa=2.56×1011 Pa3,B
2 p
项正确;步骤Ⅰ中测压仪数值未稳定即关闭K ,说明未抽成真空状态,装置中留有空气,
1
最终测压仪所测压强偏大,K 测量值偏大,C项错误;步骤Ⅱ中读数时U形管左侧液面偏
p
高,说明U形管右侧压强较大,即所测压强偏大,K 测量值偏大,D项正确。]
p
5.D 6.B
7.C [从图像上可以看出温度越高,甲醇的体积分数越小,说明升温,平衡逆向移动,该
反应的ΔH<0,A项正确;B点与C点温度相同,平衡常数相等,B项正确;C点时,甲醇
的体积分数是50%,假设起始n(CO)=1 mol,n(H )=2 mol,消耗的CO的物质的量为x
2
mol,则列三段式:
2H(g)+CO(g)CHOH(g)
2 3
初始/mol 2 1 0
转化/mol 2x x x
平衡/mol 2-2x 1-x x
甲醇的体积分数为=50%,x=0.75,平衡常数K ==,D项正确。]
p
8.0.05p
0
9.9.1% 0.8p
10.(1)p
(2)p
解析 (1)设起始时C H 和H 的物质的量均为1 mol,列出三段式:
2 6 2
C H(g)C H(g)+H(g)
2 6 2 4 2
起始/mol 1 0 1
转化/mol α α α
平衡/mol 1-α α 1+α
平衡时C H 、C H 和H 对应的分压分别为p、p和p,则该反应的平衡常数K ==p。(2)设
2 6 2 4 2 p
通入的SO 、O 和N 共100 mol,利用三段式进行计算:
2 2 2
SO (g)+ O(g)SO (g)
2 2 3
起始/mol 2m m 0
转化/mol 2mα mα 2mα
平衡/mol 2m-2mα m-mα 2mα平衡时气体的总物质的量为(3m+q-mα) mol,则p(SO )=p×,p(O )=p×,p(SO )=p×,
2 2 3
因3m+q=100,K = ,代入计算得K =。
p p
11.0.4p
12.
解析 恒压反应器中,按照n(H )∶n(C H)=4∶1投料,设投入的苯的物质的量为1 mol,
2 6 6
发生Ⅰ、Ⅱ反应,总压为p,平衡时苯的转化率为α,环己烷的分压为p,则
0
(g)+3H(g) (g)
2
起始/mol 1 4 0
转化/mol α 3α α
平衡/mol 1-α 4-3α α
(g) (g)
起始/mol α 0
转化/mol x x
平衡/mol α-x x
反应后平衡体系中总的物质的量为1-α+4-3α+α-x+x=5-3α,故平衡时,苯的分压为
p,H 的分压为p,则反应Ⅰ的K ==。
0 2 0 p
13.(1)①0.12 mol·L-1·min-1 增大 ②F
(2)①K =K >K ②2
A B C
解析 (1)①=2,又n(CO)+n(H )=3 mol,则n(H )=2 mol,n(CO)=1 mol,0~5 min内转化
2 2
的n(CO)=0.6 mol,则有
CO(g)+2H(g)CHOH(g)
2 3
起始/(mol·L-1) 0.5 1 0
转化/(mol·L-1) 0.3 0.6 0.3
平衡/(mol·L-1) 0.2 0.4 0.3
v(H )==0.12 mol·L-1·min-1,K=>,所以平衡正向移动,v >v ,H 的转化率将增大。②
2 正 逆 2
反应物按方程式中各物质的化学计量数比投料时产物的体积分数最大,否则都会使产物的体
积分数减小,故应选F点。
(2)①平衡常数只与温度有关,CO与H 反应生成CHOH的反应为放热反应,则升高温度,
2 3
平衡常数减小,则 K K 。②达到平衡状态A时,容器的体积为10 L,状态A与B的平衡常数相同,状态A
B C时CO的转化率是0.5,则平衡时CO的物质的量是10 mol×(1-0.5)=5 mol,浓度是0.5
mol·L-1,c(H )=1 mol·L-1,生成甲醇的物质的量是5 mol,浓度是0.5 mol·L-1,所以平衡
2
常数K =1;设状态B时容器的体积是V L,状态B时CO的转化率是0.8,则平衡时,CO
A
的物质的量浓度为 mol·L-1,氢气的物质的量浓度是 mol·L-1,生成甲醇的物质的量浓度
是 mol·L-1,K ==1,解得V=2。
B
第 48 练 影响化学平衡的因素
1.B 2.B 3.D
4.C [向该溶液中加入过量浓NaOH溶液后,消耗氢离子,氢离子浓度减小,平衡正向移
动,溶液呈黄色,A错误;反应前后元素的化合价均不发生变化,该反应不是氧化还原反应,
B错误;向该溶液中滴加适量的浓硫酸,氢离子浓度增大,平衡向逆反应方向移动,由于只
能是减弱这种改变,所以再次达到平衡后,氢离子浓度比原溶液大,C正确;向体系中加入
少量水,相当于稀释,平衡正向移动,D错误。]
5.A
6.C [升高体系温度,正、逆反应速率都增大,故A错误;该反应气体总质量不变,容器
体积不变,根据ρ=可知该反应的气体密度始终不变,故B错误;平衡常数K=,K只与温
度有关,温度不变,K不变,故C正确;增大体系的压强,平衡逆移,NO 的平衡转化率
2 4
降低,故D错误。]
7.B [A项,充入B气体相当于增大压强,B的体积分数增大,故a>b;B项,使用催化剂,
平衡不移动,a=b;C项,升高温度,平衡正向移动,a>b;D项,相当于扩大容器容积,
减小压强,平衡逆向移动,a<b。]
8.B 9.C
10.D [温度不变,平衡常数不变,K=c(Cl ),因此反应 ⅰ 增大压强,达到新平衡后Cl
2 2
浓度不变,A错误;反应4HCl(g)+O(g)2Cl(g)+2HO(g)是放热反应,B错误;依据盖
2 2 2
斯定律,用[总反应-(反应ⅰ+反应ⅱ)]×得反应ⅲ:CuO(s)+2HCl(g)CuCl (s)+
2
HO(g),D正确;由反应 ⅰ、ⅱ、ⅲ 知,催化剂CuCl 参加反应,通过改变反应历程,从
2 2
而提高反应速率,但不影响平衡,改变不了平衡转化率,C错误。]
11.D [两室中发生反应2SO (g)+O(g)2SO (g),若右室的容积与左室相等,左室和
2 2 3
右室在相同条件下达到的平衡状态相同,含有的SO 物质的量相等,右室在此平衡状态时将
2
体积缩小为原来的,压强增大,平衡向生成SO 的方向移动,SO 物质的量减少,则第一次
3 2
平衡时,SO 的物质的量左室更多,A项正确;通入气体未反应前,左室气体总物质的量为
2
4 mol,右室气体总物质的量为2 mol,左室容积为右室的两倍,温度相同,则左室压强和右室一样大,B项正确;左室从正反应开始建立平衡,左室平衡时压强小于左室起始压强,右
室从逆反应开始建立平衡,右室平衡时压强大于右室起始压强,左室与右室起始压强相等,
则第一次平衡时左室内压强一定小于右室,C项正确;若在容积为2倍左室容积的容器中起
始充4 mol SO 、2 mol O ,相同条件下达到平衡时SO 的物质的量为左室SO 物质的量的2
2 2 2 2
倍,打开活塞相当于在容积为1.5倍左室容积的容器中起始充入2 mol SO 、1 mol O 、2 mol
2 2
SO (g)、1 mol Ar,相当于在容积为1.5倍左室容积的容器中起始充入4 mol SO 、2 mol O 、
3 2 2
1 mol Ar,相对于2倍左室容积的容器缩小了体积,压强增大,平衡向正反应方向移动,
SO 物质的量减小,即第二次平衡时,SO 的总物质的量比第一次平衡时左室SO 物质的量
2 2 2
的2倍要少,D项错误。]
12.(1)温度低于500 ℃,反应速率小;温度高于500 ℃,对副反应影响较大,化学平衡向
生成CO的方向移动程度增大,不利于甲烷的生成 (2)①C ②Ⅱ > ③45 kPa
13.(1)①Ⅱ ②< 该反应是放热反应,C H 与O 起始物质的量比相同时,升高温度,平
3 8 2
衡逆向移动,C H 体积分数增大,故横坐标向左是升高温度,所以TT>T 恒压条件下,HS的摩尔分数增大,平衡正向移动,最终
1 2 3 2
HS的转化率降低
2
(3)< 在 1 000 K,反应① ΔG>0,反应趋势小,反应③ ΔG<0,反应趋势大,占主导
(4)1.28×104
解析 (1)反应③等于反应①减去反应②,ΔH=+180 kJ·mol-1-(-81 kJ·mol-1)=+261 kJ·
3
mol-1;A项中都表示正反应,故A不符合题意;该反应是气体分子数变化的反应,恒容条
件下压强不变即达到平衡,故B符合题意;恒容条件又都是气体参与反应,故密度始终保
持不变,故C不符合题意。(2)反应①是吸热反应,温度升高,平衡正向移动,则HS的转
2
化率增大,故T>T>T 。(3)在1 000 K,反应①ΔG>0,不易自发,反应③ΔG<0,容易自发,
1 2 3
故反应自发趋势①<③。(4)设n(H S)=3 mol,列三段式
2
CH(g)+2HS(g)CS(g)+4H(g)
4 2 2 2
初始/mol 3 3 0 0转化/mol x 2x x 4x
平衡/mol 3-x 3-2x x 4x
达到平衡时,CS 分压与HS的分压相同即有3-2x=x,解得x=1,平衡后气体的总物质的
2 2
量为2 mol+1 mol+1 mol+4 mol+2 mol=10 mol,则K ==1.28×104。
p
第 49 练 化学反应的方向与调控
1.D 2.D
3.C [A(s)===B(g)+C(s)的ΔS>0,ΔH>0,在高温条件下能自发进行,故A错误;A(g)
+2B(g)===2C(g)+3D(g)的ΔS>0,所以当ΔH<0时,一定满足ΔH-TΔS<0,反应一定能
够自发进行,当ΔH>0时,高温下,ΔH-TΔS<0成立,也可以自发进行,故B错误;
M(s)+N(g)===2Q(s)的ΔS<0,当ΔH>0时,ΔH-TΔS>0,一定不能自发进行,故D错
误。]
4.C [由题图可知,NH 的体积分数随着温度的升高而显著下降,故要提高NH 的体积分
3 3
数,必须降低温度,但目前所用催化剂铁触媒的活性最高时的温度为 500 ℃,故最有前途
的研究方向为研制低温催化剂。]
5.A [图①到图③为氮气和氢气中的化学键断裂的过程,图⑤到图③为氨气中化学键断裂
的过程,故图①到图③的活化能减去图⑤到图③的活化能就是合成氨反应的反应热,A正确;
该反应过程中只有非极性键的断裂和极性键的形成,B错误;当温度、体积一定时,在原料
气中添加少量惰性气体不影响各组分的浓度,因此不影响平衡,不能提高平衡转化率,C错
误;合成氨的反应是气体总体积减小的放热反应,故高压是为了提高反应物的平衡转化率,
但高温不是为了提高转化率,D错误。]
6.C 7.A
8.A [根据题图,随着温度的升高,H 的平衡转化率降低,说明平衡向逆反应方向移动,
2
故正反应为放热反应,即ΔH<0,A项正确;N点压强大于M点,M点温度高于N点,因此
无法确定两点反应速率的快慢,B项错误;此反应是可逆反应,不能完全进行到底,C项错
误;采用更高的压强对设备的要求更高,增加经济成本,D项错误。]
9.C [在1.0×105 Pa,将TiO 、C、Cl 以物质的量之比为1∶2∶2进行反应:TiO +2C+
2 2 2
2Cl=====TiCl +2CO,三者完全反应时,生成TiCl 、CO的物质的量之比为1∶2,此时
2 4 4
TiCl 的物质的量分数约为33.3%,结合图像可知,200~1 600 ℃反应达到平衡时,TiCl 的
4 4
物质的量分数约为33.3%,则TiO 转化率均已接近100%,A正确;结合图像可知,将400
2
℃时的平衡体系加热至800 ℃,二氧化碳含量减小、一氧化碳含量增加,则平衡C(s)+
CO(g)2CO(g)向正反应方向移动,B正确;延长时间不能改变平衡时物质的转化率,C
2错误。]
10.(1)任何温度下都能自发进行,是因为ΔH<0、ΔS>0
(2)①+90.8 ②CD
11.(1)AD (2)
12.(2)0.975 该反应气体分子数减少,增大压强,α提高。5.0 MPa>2.5 MPa=p ,所以p
2 1
=5.0 MPa 反应物(N 和O)的起始浓度(组成)、温度、压强 (4)升高温度,k增大使v逐渐
2 2
提高,但α降低使v逐渐下降。当t<t ,k增大对v的提高大于α引起的降低;当t>t ,k
m m
增大对v的提高小于α引起的降低
13.(1)+124 (2)AD (3)①丙烷物质的量分数增大,相当于对平衡体系加压,平衡向逆反
应方向移动 ②16.7
解析 (1)设已知反应为反应Ⅲ根据盖斯定律,反应Ⅰ=(反应Ⅱ-反应Ⅲ)可得ΔH =+124
1
kJ·
mol-1。(3)②据图可知:在温度为T ℃时,当通入C H 的物质的量分数为0.4,C H 的平
1 3 8 3 8
衡转化率为50%,假设反应开始时通入气体物质的量为 a mol,则n(C H)=0.4a mol,
3 8
n(N )=0.6a mol,则平衡时n(C H)=0.2a mol,n(C H)=n(H )=0.2a mol,平衡时气体总
2 3 8 3 6 2
物质的量n(总)=0.2a mol+0.2a mol+0.2a mol+0.6a mol=1.2a mol,C H 、C H 、H 的
3 8 3 6 2
物质的量分数都是=,K ==≈16.7 kPa。
p
第 50 练 化学反应速率与化学平衡图像分类突破
1.C 2.C
3.D [由图可知,压强一定时,温度越高,CO的平衡转化率越低,说明升高温度,平衡
向逆反应方向移动,则正反应为放热反应,即ΔH<0,故A错误;正反应为气体体积减小
的反应,温度一定时,增大压强,平衡向正反应方向移动,CO的平衡转化率增大,故压强:
p >p ,故B错误;X点和Y点对应的温度相同,则化学平衡常数K(X)=K(Y),故C错误;
1 2
在p 和316 ℃时,若将6 mol H 和2 mol CO通入容器中,相当于在原平衡的基础上增大氢
2 2
气的浓度,平衡向正反应方向移动,CO的转化率增大,故CO的平衡转化率应大于50%,
故D正确。]
4.B [甲容器中,10~40 min内,氢气分压变化为(7.5-3.0) kPa=4.5 kPa,用氢气表示的
平均反应速率为=0.15 kPa·min-1,故A正确;根据题给反应方程式,反应前后气体系数之
和相等,增大起始时压强,平衡不移动,CoO的平衡转化率不变,故B错误;根据两个图
像可知,CO还原CoO的速率更快,达到平衡时间更短,CO还原CoO达到平衡时,CO 分
2
压为11.9 kPa,起始压强为12.0 kPa,说明CO还原CoO转化更彻底,因此选择CO还原
CoO的效率更高,故C正确;达到平衡时,CO 分压为11.9 kPa,该反应前后气体系数之和
2相等,总压强不变,即CO的分压为0.1 kPa,K ===119,故D正确。]
p
5.D 6.B
7.B [起始时刻NO 分压为40 kPa,发生反应①完全转化为二氧化氮和氧气,氧气分压为
2 5
20 kPa,二氧化氮发生反应②部分转化为四氧化二氮,平衡时二氧化氮分压为16 kPa,A、
B、C分别为NO、NO 、O 的分压随时间t的变化曲线,A错误;
2 5 2 2
2NO (g)NO(g)
2 2 4
起始分压/kPa 80 0
变化分压/kPa 64 32
平衡分压/kPa 16 32
K === kPa-1,B正确;某时刻O、NO 的分压相等为20 kPa时:
p 2 2 4
2NO (g)NO(g)
2 2 4
起始分压/kPa 80 0
变化分压/kPa 40 20
平衡分压/kPa 40 20
二氧化氮的转化率为50%,C错误;t min后,保持温度和体积不变,再充入NO (g)引起②
1 2
化学平衡发生移动,由勒夏特列原理知体系中总的物质的量依然增大,O(g)的物质的量不
2
变,氧气分压减小,D错误。]
8.A [当使用催化剂乙时,温度低于350 ℃时,催化剂的活性随温度升高逐渐增强,反应
速率加快,NO转化率也增大,温度高于350 ℃时,催化剂活性降低甚至失去活性,反应速
率下降,导致NO转化率下降,A错误;单位时间内,使用催化剂甲比使用催化剂乙反应速
率快,NO转化率高,则使用催化剂甲比使用催化剂乙正反应的活化能更低,B正确;设初
始一氧化氮和氢气的物质的量均为1 mol,容器体积为1 L,则初始一氧化氮和氢气的浓度
均为1 mol·L-1,v =k×1m×12=k,当H 转化率为60%时,c(H )=0.4 mol·L-1,c(NO)=0.4
0 2 2
mol·L-1,此时的反应速率为0.064v ,则有0.064v =k×0.4m×0.42=v×0.4m×0.42,解得m
0 0 0
=1,D正确。]
9.C
10.C [从图中可以看出,温度低于900 ℃时,CH 的相对体积基本上是100%,所以反应
4
Ⅰ基本不发生,所以工业生产上需要研发低温下CH 转化率高的催化剂,A、D正确;850
4
~900 ℃时,H 、CO的相对体积都增大,且增大的幅度相近,而CH 的相对体积变化不大,
2 4
所以主要发生反应Ⅳ,B正确;从图中可以看出,4个反应均为生成CO的反应,且都为吸
热反应,所以若想提高CO的相对体积,应选择升高温度,与增大焦炉煤气的流速无关,C
不正确。]
11.(1)d c 小于 (2)×
12.1 000 1 000解析 反应HN==C==O(g)+NH (g)CO(NH)(g)为放热反应,因为Tc(CHCOO-),故C正确;③点后,
3 3
溶液体积变大,溶液中离子浓度减小导致电导率减小,故D错误。]
8.D [次氯酸是弱电解质,电离方程式为HClOH++ClO-,故A错误;次氯酸是弱酸,
随着pH的增大,HClO逐渐减少,ClO-逐渐增多,故曲线a、b依次表示δ(HClO)、δ(ClO-)
的变化,故B错误;次氯酸的K=,在a、b的交点处,c(ClO-)=c(HClO),K=10-7.5,所
a a
以K 的数量级为10-8,故C错误;向次氯酸溶液中加NaOH溶液,随着碱性增强,HClO逐
a
渐减少,ClO-逐渐增多,故将减小,故D正确。]
9.C 10.A
11.B [B项,NH ·H O的电离常数K =,温度不变,K 不变,正确;C项,HCO 电离常
3 2 b b 2 3
数K =、K =,同一溶液中c(H+)相等,而K >K ,则>,错误;D项,0.1 mol·L-1的
a1 a2 a1 a2
HF溶液加水稀释,c(F-)趋近于0,而c(H+)趋于10-7 mol·L-1,故变小,错误。]
12.D [随着pH的增大,草酸分子的浓度逐渐减小,草酸氢根离子的浓度逐渐增大,pH
继续升高,草酸氢根离子的浓度又逐渐减小,而草酸根离子的浓度逐渐增大,因此曲线 a代
表HC O,曲线b代表C O,A正确;根据图像可知当草酸氢根离子和草酸根离子浓度相等
2 2 4 2
时,pH=4.30,所以草酸的第二步电离平衡常数K ==10-4.30,C正确;根据图像可知pH
a2
从1.30~4.30时,逐渐减小,D项错误。]
13.(1)①正盐 ②2 ③测NaH PO 溶液的pH,若pH>7,则证明次磷酸为弱酸 向等物
2 2
质的量浓度的盐酸、次磷酸溶液中各滴入2滴石蕊溶液,若次磷酸溶液中红色浅一些,则说
明次磷酸为弱酸 (2)1×10-3 (3)1 (4)>
14.(1)CH COOHH++CHCOO- α>α <
3 3 1 2
(2)由图像可知:a代表H+,b代表CHCOO-,c代表CHCOOH,d代表OH-,N点pH=
3 3
4.8,lg c(CHCOO-)=lg c(CHCOOH),即c(CHCOO-)=c(CHCOOH),K==1×10-4.8=
3 3 3 3 a
1.6×10-5
(3)0.038 mol·L-1解析 (3)pH=5时c(H+)=1×10-5 mol·L-1,相同温度下电离常数不变,K==10-4.8,=
a
=100.2=1.6,由于 c(CHCOO-)+c(CHCOOH)=0.1 mol·L-1,解得 c(CHCOOH)≈0.038
3 3 3
mol·L-1。
第 52 练 水的电离和溶液的 pH
1.D 2.C
3.D [该温度下蒸馏水中的c(H+)大于25 ℃时纯水中的c(H+),水的电离为吸热过程,A
项正确;此温度下K =1.0×10-12,故该NaHSO 溶液中c(OH-)= mol·L-1=1.0×10-10
w 4
mol·L-1,由水电离出的c(H+)与溶液中的c(OH-)相等,B项正确;NaHSO 电离出的H+抑
4
制了水的电离,C项正确;加水稀释时,溶液中c(H+)减小,而K 不变,故c(OH-)增大,D
w
项错误。]
4.C [该溶液c(H+)=10-10 mol·L-1,氢氧化钠是一元强碱,c(OH-)=0.01 mol·L-1,K =
w
0.01×10-10=10-12>10-14,因而溶液温度高于25 ℃,A、D错误;盐酸中n(H+)=V×10-
4mol,NaOH溶液中n(OH-)=V×10-2 mol,显然氢氧化钠过量,B错误;该温度下K =10
w
-12,则蒸馏水的pH=6,C正确。]
5.A [HSO 与Ba(OH) 抑制水的电离,NaS与NH NO 促进水的电离。25 ℃时,①pH=
2 4 2 2 4 3
0的HSO 溶液中:c (H O)=c(OH-)= mol·L-1=10-14 mol·L-1;同理可计算其余溶液
2 4 电离 2
中电离的水的浓度依次为②为10-13 mol·L-1,③为10-4 mol·L-1,④为10-5 mol·L-1,同
温同体积时,物质的量之比等于浓度之比,则物质的量之比为 10-14∶10-13∶10-4∶10-5=
1∶10∶1010∶109,故A正确。]
6.B 7.D
8.C [A项中,a=b,酸碱恰好完全反应生成正盐和水,由于酸碱强弱未知,不能确定溶
液的酸碱性;B项中未说明温度为25 ℃,故混合溶液的pH=7时不一定呈中性;C项混合
溶液中,c(H+)·c(OH-)=K ,因为c(H+)= mol·L-1,则c(H+)=c(OH-),故溶液呈中性;
w
D项中c(H+)+c(B+)=c(OH-)+c(A-),只能说明溶液中电荷守恒,无法判断溶液的酸碱
性。]
9.D
10.C [由b=6a>7得a>,由混合溶液的pH=7得n(H+)=n(OH-),即V×10-a=V×10b
a b
-14,得=10a+b-14;由于V<V ,即10a+b-14<1,得a+b-14<0,结合b=6a得a<2,综
a b
合知,<a<2,故选C项。]
11.A [T ℃时,水的离子积常数K =10-13,该温度下,V mL pH=12的Ba(OH) 稀溶液
w 1 2
中c(H+)=10-12 mol·L-1,则c(OH-)=10-1 mol·L-1;V mL pH=2的稀硫酸中c(H+)=10-2
2
mol·L-1,二者反应后恢复到T ℃,测得混合溶液的pH=3,c(H+)=10-3 mol·L-1,说明酸过量,
则c(H+)= mol·L-1=10-3 mol·L-1,解得V∶V=9∶101。]
1 2
12.D
13.C [根据图知,ROH加水稀释10倍,溶液的pH减小1,说明ROH完全电离,为强电
解质,则MOH为弱电解质。常温下浓度为c 的ROH溶液的pH=13,且ROH为强电解质,
0
则c =0.1 mol·L-1,A错误;lg=0时,MOH溶液的pH=12,c =0.1 mol·L-1,电离常数
0 0
K (MOH)==≈1.1×10-3,B错误;x点两种溶液的pH相等,所以二者抑制水的电离程度相
b
等,C正确;升高温度促进MOH的电离,所以lg相同时,升高温度c(R+)不变,c(M+)增大,
则减小,D错误。]
14.(1)10∶1 (2)a+b=14 (3)小于 (4)10
解析 (1)25 ℃时,pH=9的NaOH溶液,c(OH-)=10-5 mol·L-1;pH=4的HSO 溶液,
2 4
c(H+)=10-4 mol·L-1;若所得混合溶液的pH=7,则c(OH-)·V(NaOH)=c(H+)·V(H SO )。
2 4
故NaOH溶液与HSO 溶液的体积比为V(NaOH)∶V(H SO )=c(H+)∶c(OH-)=10∶1。
2 4 2 4
(2)100 ℃时,水的离子积常数K =1×10-12。100体积pH=a的某强酸溶液中n(H+)=
w
100×10-a mol=102-a mol,1体积pH=b的某强碱溶液中n(OH-)= mol=10b-12 mol。混
合后溶液呈中性,102-a mol=10b-12 mol,2-a=b-12,所以a+b=14。
(3)曲线A所对应的温度是25 ℃,pH=2的盐酸中c (H+)=10-12 mol·L-1;pH=11的某
水
BOH溶液中c (H+)=10-11 mol·L-1;水电离产生的H+的浓度越大,水的电离程度就越大,
水
则α<α。
1 2
(4)混合溶液中c(OH-)= mol·L-1=0.01 mol·L-1。由于该温度下水的离子积常数K =10-
w
12,所以c(H+)=10-10 mol·L-1,所得混合溶液的pH=10。
15.(1)①水的电离为吸热过程,升高温度有利于电离(压强对电离平衡影响不大) ②100
(2)H OH++HO、HOH++O 6
2 2
第 53 练 酸碱中和滴定及拓展应用
1.B 2.D
3.C [向容量瓶中转移溶液时需要用玻璃棒引流,故A错误;托盘天平的精确度为0.1 g,
故B错误;NaOH溶液应装在碱式滴定管中,故D错误。]
4.D [NaOH溶液和CHCOOH溶液恰好完全反应时生成CHCOONa,CHCOO-水解使溶
3 3 3
液显碱性,而酚酞的变色范围为8.2~10.0,比较接近。]
5.C [用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗后装入一定体积的NaOH溶液,会使
NaOH溶液的用量偏多,测定结果偏高,故B错误;取10.00 mL NaOH溶液放入锥形瓶后,
把碱式滴定管尖嘴处液滴吹去,会使得取用的NaOH溶液偏少,测定结果偏低,故D错误。]
6.C 7.D 8.B
9.C [步骤①中用NaOH溶液滴定甲酸,滴定终点时生成甲酸钠,溶液呈碱性,所以指示
剂可选用酚酞溶液,故A正确;步骤②若不静置,NH没有完全反应,会导致消耗标准液体
积偏小,测定结果偏低,故C错误;步骤③消耗NaOH溶液的体积为(V-V)mL,则饱和食
3 2
盐水中的c(NH)== mol·L-1,故D正确。]
10.C
11.D [滴定反应为碘单质与硫代硫酸钠反应,因为淀粉遇碘单质变蓝,则指示剂 X为淀
粉溶液,A项错误;滴定管装液之前最后一步操作是润洗,即用待装液润洗滴定管,C项错
误;根据关系式:2Cu2+~I~2SO可知,胆矾纯度为××100%=%,D项正确。]
2 2
12.A [据图可知,浓度均为0.1 mol·L-1的HX、HY溶液的pH都大于1,说明HX和HY
均为弱酸,N点加入NaOH溶液的体积为15 mL,NaOH与HY的物质的量之比为3∶2,则
根据元素守恒得2c(Na+)=3c(Y-)+3c(HY),A项错误;M点溶液中存在电荷守恒:c(Na+)
+c(H+)=c(OH-)+c(X-),由图知c(H+)>c(OH-),所以c(X-)>c(Na+),B项正确;据图可
知,浓度均为0.1 mol·L-1的HX、HY溶液的pH大小关系为pH(HX)<pH(HY),说明酸性:
HX>HY,所以滴至pH=7时,消耗NaOH溶液的体积:HX溶液>HY溶液,C项正确;
滴入10 mL NaOH溶液时,HX和HY均恰好完全反应分别得到NaX溶液和NaY溶液,因酸
性:HX>HY,则X-的水解程度小于Y-的水解程度,溶液中水的电离程度:HX溶液<HY
溶液,D项正确。]
13.(1)容量瓶 (2)酚酞溶液 (3)当滴入最后半滴标准液,溶液由无色恰好变为浅红色,且
在半分钟内不褪色 (4)0.75 4.5
14.浅蓝色至无色 ×100%
解析 达到滴定终点时I 完全反应,可观察到溶液颜色由浅蓝色变成无色,且半分钟内颜色
2
不再发生变化;根据滴定过量的I 消耗NaSO 溶液的体积和关系式I~2SO,可得n(I) =
2 2 2 3 2 2 2 过量
×0.100 0V×10-3mol,再根据关系式 S2-~I 可知,n(S2-)=0.100 0×25.00×10-3 mol-
2
×0.100 0V×10-3mol=(25.00-)×0.100 0×10-3mol,则样品中S2-的含量为×100%。
15.(1)SO +HO===HSO
2 2 2 2 4
(2)将胶管弯曲使玻璃尖嘴向上倾斜,用力捏挤玻璃球,使液体从尖嘴流出 (3)①酚酞 当
滴入最后半滴标准液,溶液由无色变为浅红色,且半分钟内不恢复原色
②甲基橙 当滴入最后半滴标准液,溶液由红色变为橙色,且半分钟内不恢复原色 (4)④
(5)n(NaOH)=0.090 0 mol·L-1×0.025 L=0.002 25 mol。根据反应关系 SO ~HSO ~
2 2 4
2NaOH,m(SO )==0.072 g,该葡萄酒中SO 的含量为=0.24 g·L-1
2 2
(6)盐酸具有挥发性,反应过程中挥发出的盐酸滴定时消耗了 NaOH标准液。改进措施:用
非挥发性的强酸硫酸代替盐酸第 54 练 盐类的水解
1.C 2.C
3.A [碳酸钠溶液显碱性,其加水稀释时,溶液中OH-浓度减小,由于温度不变,水的离
子积常数不变,所以溶液中c(H+)增大,A错误;加入NaOH固体会抑制CO水解,所以减
小,C正确;温度升高,促进CO的水解,因此水解平衡常数增大,D正确。]
4.D [根据表格中的酸的电离常数可知,酸性:CHCOOH>H CO>H S>HCO>HS-,根据
3 2 3 2
越弱越水解的规律可知,水解能力:S2->CO>HS->HCO>CHCOO-,故D正确。]
3
5.D 6.B
7.A [因硝酸铵晶体溶于水吸收热量,则不能说明盐的水解吸热,故 A错误;温度升高,
三价铁离子转化为氢氧化铁沉淀下来,说明升高温度有利于三价铁离子的水解平衡向右移动,
故B正确;温度升高,去油污效果好,说明温度升高有利于碳酸根离子的水解平衡正向移
动,故C正确;醋酸钠溶液中滴入酚酞溶液,加热后若红色加深,则说明升高温度促进水
解,即水解反应为吸热反应,故D正确。]
8.C [浓度均为 0.10 mol·L-1的 NaHCO 和 NaCO 溶液中都存在 Na+、HCO、CO、
3 2 3
HCO 、H+、OH-、HO,粒子种类相同,A错误;酸、碱抑制水的电离,某溶液由水电离
2 3 2
出的c(H+)为1.0×10-5 mol·L-1,水的电离受到促进,则该溶液不可能是酸,可能是盐,B
错误;1 L 0.50 mol·
L-1NH Cl溶液与2 L 0.25 mol·L-1NH Cl溶液中NH Cl的物质的量相等,由于NH Cl浓度不
4 4 4 4
同,NH水解程度不同,所以含NH物质的量不相同,C正确;测NaHA溶液的pH,若pH
>7,则HA是弱酸;若pH<7,HA可能是强酸也可能是弱酸,如亚硫酸是弱酸,但
2 2
NaHSO 溶液的pH<7,D错误。]
3
9.C
10.B [二乙胺是弱碱,其对应的盐酸盐溶液显酸性,水解是微弱的,所以0.01 mol·L-1
(C H)NH Cl水溶液的pH>2,故A错误;由于(C H)NH水解,(C H)NH Cl水溶液显酸性,
2 5 2 2 2 5 2 2 5 2 2
加热能促进水解的进行,所以(C H)NH Cl水溶液的pH随温度升高而减小,故B正确;
2 5 2 2
(C H)NH Cl水溶液显酸性,加水稀释,溶液酸性减弱,pH增大,故C错误;(C H)NH Cl
2 5 2 2 2 5 2 2
水溶液中存在电荷守恒:c(Cl-)+c(OH-)=c[(C H)NH]+c(H+),(C H)NH水解的方程式
2 5 2 2 5 2
为(C H)NH+HO(C H)NH +HO+,还存在着水的电离:HOH++OH-,所以c(H
2 5 2 2 2 5 2 3 2
+)>c[(C H)NH],故D错误。]
2 5 2
11.D [酸根离子水解程度越大,该盐溶液pH越大,酸根离子水解程度:AlO>HCO>
CHCOO-,所以等浓度的三种溶液pH由大到小的顺序是①>③>②,B正确;等浓度的盐溶
3
液中,铵根离子浓度与其系数成正比,当铵根离子系数相同时,酸根离子对应酸的酸性越弱,铵根离子水解程度越大,一水合氨是弱电解质,其电离程度很小,则c(NH)由大到小的顺序
是①>③>②>④,C正确;常温时,将等体积的盐酸和氨水混合后,pH=7,溶液呈中性,
则c(OH-)=c(H+),根据电荷守恒知c(NH)=c(Cl-),D不正确。]
12.B
13.(1)PO+HOHPO+OH-、
2
HPO+HOHPO+OH-、
2 2
HPO+HOHPO +OH-;
2 2 3 4
Fe3++3HOFe(OH) +3H+。
2 3
(2)[Al(OH)]2++HO[Al(OH) ]++H+
2 2
(3)NH Cl+2HO===NH ·H O+HClO
2 2 3 2
14.(1)①NaS ②大于 (2)B
2
第 55 练 盐类水解原理的应用、水解常数
1.D 2.A
3.A [根据盐类水解中越弱越水解的规律,可得酸性的强弱顺序是 CHCOOH>HCO >
3 2 3
HClO>HCN>C HOH>HCO;再利用较强酸制较弱酸原理进行判断。HClO可与CO发生
6 5
反应生 HCO,故CO 与NaClO溶液发生反应:CO +HO+NaClO===NaHCO +HClO,A
2 2 2 3
错误、B正确;酸性:HCO >C HOH>HCO,CO 通入C HONa溶液中发生反应生成
2 3 6 5 2 6 5
NaHCO 和C HOH,C正确;酸性:CHCOOH>HCN,CHCOOH与CN-发生反应生成
3 6 5 3 3
HCN,D正确。]
4.B 5.B
6.C [碳酸钠水解的离子方程式为CO+HOOH-+HCO,A错误;向沸水中滴入饱和
2
FeCl 溶液至液体呈红褐色是生成氢氧化铁胶体,其化学方程式为FeCl +3HO=====3HCl+
3 3 2
Fe(OH) (胶体),B错误;铝离子和碳酸氢根离子发生相互促进的水解反应,离子方程式为
3
3HCO+Al3+===3CO↑+Al(OH) ↓,D错误。]
2 3
7.C [K (HA-)==<K ,即说明HA-的电离程度大于其水解程度,故NaHA溶液中c(A2
h a2
-)>c(H A),A错误;HA为二元弱酸,将等浓度的HA溶液和硫酸溶液稀释10倍后,前
2 2 2
者溶液中H+浓度小于后者,即前者pH较大,B错误;HA+A2-2HA-的化学平衡常数
2
K===,C正确;向0.1 mol·L-1 HA溶液滴加NaOH溶液至中性时即c(H+)=10-7 mol·L
2
-1,K ==1.5×10-4,则=1.5×103,即c(HA-)<c(A2-),D错误。]
a2
8.B [A项,未加盐酸时,由于NH ·H O的部分电离,所以c(OH-)>c(Na+)>c(NH ·H O),
3 2 3 2
错误;B项,加入10 mL盐酸时,c(Cl-)=c(Na+),再由电荷守恒可知c(NH)+c(H+)=c(OH
-),正确;C项,由电荷守恒得c(Na+)+c(NH)+c(H+)=c(Cl-)+c(OH-),pH=7时,c(H+)=c(OH-) ,所以有c(Cl-)>c(Na+),错误;D项,当加入20 mL盐酸时,溶质为NaCl、
NH Cl,溶液呈酸性,即c(H+)>c(OH-),再根据电荷守恒可得c(Cl-)+c(OH-)=c(H+)+
4
c(NH)+c(Na+),则c(Cl-)>c(NH)+c(Na+),错误。]
9.D
10.B [A项,pH=4的CHCOOH溶液中,c(H+)=1.0×10-4 mol·L-1,根据电荷守恒可
3
得 c(H+)=c(CHCOO-)+c(OH-),故 c(H+)>c(CHCOO-),错误;B 项,CHCOOH 和
3 3 3
CHCOONa 的酸性混合溶液中,c(OH-)1.0×10-14,pH=
2 3 w
12,c(H+)=1.0×10-12 mol·
L-1,所以此时c(OH-)>1.0×10-2 mol·L-1,错误。]
11.D [A项,由K (CO)==可得0.5 mol·L-1的NaCO 溶液中c(OH-)≈= mol·L-1=
h 2 3
0.01 mol·L-1,则pH约为12,正确;B项,NaHCO 溶液中碳酸氢根离子的水解促进水的电
3
离,pH=8的NaHCO 溶液中c(H+)=10-8 mol·L-1,所以水电离产生的 c(OH-)=10-6
3
mol·L-1,正确;C项,NaHCO 溶液显碱性,说明HCO的水解程度大于其电离程度,所以
3
c(HCO)>c(H CO)>c(CO),正确;D项,由元素守恒可知,NaHCO 溶液中c(Na+)=c(CO)
2 3 3
+c(HCO)+c(H CO),NaCO 溶液中c(Na+)=2c(CO)+2c(HCO)+2c(H CO),则pH=10
2 3 2 3 2 3
的NaCO-NaHCO 缓冲溶液中c(Na+)>c(CO)+c(HCO)+c(H CO),错误。]
2 3 3 2 3
12.D
13.A [10c(H PO)=c(HPO)时,K ===10c(H+),则pH=pK +1,A正确;2pH=pK
2 a2 a2 a1
+pK 时,pH=,此时溶液中主要含有HPO,溶液显酸性,其电离程度大于水解程度,故
a2 2
c(H PO)>c(HPO)>c(H PO ),B错误;pH=pK 时,根据电荷守恒可知,c(H+)+c(Na+)=
2 3 4 a1
c(H PO)+2c(HPO)+3c(PO)+c(OH-),C错误;平衡常数只受温度的影响,故pK 不移动,
2 a1
D错误。]
14.(1)C (2)BC (3)< c(H+)+c(Na+)=c(CHCOO-)+c(OH-) (4)> <
3
第 56 练 溶液中的粒子平衡曲线分类突破
1.C
2.B [滴加10.00 mL盐酸时,溶质为NH Cl和NH ·H O,且物质的量相等,利用电荷守恒
4 3 2
和元素守恒,氨水中存在 c(NH)+c(H+)=c(Cl-)+c(OH-)和c(NH)+c(NH ·H O)=2c(Cl
3 2
-),所以有c(NH ·H O)+c(OH-)=c(Cl-)+c(H+),故A正确;分别滴加20.00 mL盐酸时,
3 2
恰好反应生成氯化钠和氯化铵,铵根离子能够水解,所以 NaOH溶液中水的电离程度小于
氨水,故B错误;若用甲基橙作指示剂,滴定终点时pH为3.1~4.4,若不考虑铵根离子水解,两份溶液消耗盐酸的量相等,铵根离子水解呈酸性,所以 NaOH溶液消耗盐酸的量略
大于氨水,故C正确;滴加10.00 mL盐酸时,氨水中存在等量的NH ·H O和NH Cl,此时
3 2 4
NH ·H O电离程度强于NH水解程度,所以存在c(NH)>c(Cl-)>c(OH-)>c(H+),故D正确。]
3 2
3.C 4.C
5.C [a点溶质为NaHCO ,此时溶液呈碱性,由此可知,NaHCO 溶液中HCO的水解程
3 3
度大于电离程度,故 A正确;由电荷守恒可知,a→b→c过程溶液中c(HCO)+2c(CO)+
c(OH-)=c(H+)+c(Na+),滴加NaOH溶液的过程中c(Na+)保持不变,c(H+)逐渐减小,因此
c(HCO)+2c(CO)+c(OH-)逐渐减小,故B正确;由元素守恒可知,a点溶液中c(Na+)=
c(HCO)+c(CO)+c(H CO),向NaHCO 溶液中滴加盐酸过程中有CO 逸出,因此a→d→e
2 3 3 2
过程中c(Na+)>c(HCO)+c(CO)+c(H CO),故C错误;c点溶液中c(Na+)+c(H+)=(0.05+
2 3
10-11.3)mol·L-1,e点溶液体积增大1倍,此时溶液中c(Na+)+c(H+)=(0.025+10-4.3)mol·L-
1,因此x>y,故D正确。]
6.A [曲线a显示,pH越大,该微粒的含量越高,表示的是CO,故A正确;根据碳酸钠
的性质可知,b表示HCO的变化,c表示HCO 的变化,由图像可知,HCO 、HCO、CO
2 3 2 3
不可大量共存于同一溶液中,故B错误;根据pH=11可求得碳酸钠的水解平衡常数,K =
h
=1.0×10-3,故D错误。]
7.B [0.1 mol·L-1 HA溶液中,-lg c (H+)=11,c (H+)=c (OH-)=10-11 mol·L-1,
水 水 水
c(H+)==10-3 mol·L-1,HAH++A-,K(HA)=≈=10-5,A项正确;N点水电离出的
a
H+浓度最大,说明HA与NaOH恰好完全反应生成NaA,则P点溶质为NaOH和NaA,溶
液显碱性,即P点溶液pH不等于7,且b=20.00,B项错误、C项正确;M点溶液的pH=
7,根据溶液呈电中性可知,c(Na+)=c(A-),则M点后,溶液呈碱性,c(Na+)>c(A-),D项
正确。]
8.D 9.B
10.B [二甲胺与盐酸恰好完全中和时放出热量最多,溶液温度最高,即 Y点表示酸碱恰
好完全反应。根据(CH)NH·HO+HCl===(CH)NH Cl+HO,可得10×10-3 L×c mol·L-1
3 2 2 3 2 2 2
=20×10-3 L×0.1 mol·L-1,c=0.2,A项正确;二甲胺是弱碱,Y点对应溶质是强酸弱碱
盐,其溶液呈酸性,X点对应的溶液中(CH)NH·HO、(CH)NH Cl的浓度相等,根据K 推
3 2 2 3 2 2 b
知,(CH)NH·HO的电离大于(CH)NH Cl的水解,其混合溶液呈碱性,故中性点应在X点
3 2 2 3 2 2
与Y点之间,B项错误;二甲胺是弱碱,Y点对应溶质是强酸弱碱盐,其溶液呈酸性,Y点
存在:c(Cl-)>c[(CH )NH]>c(H+)>c(OH-),C项正确;K ===6.25×10-11,D项正确。]
3 2 h
11.C [稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液pOH不断增大,OH-的浓度不断
2 4
减小,可知Ⅱ代表HFeO的变化曲线,故A错误;a、b、c三点溶液中微粒成分不同,溶液
pOH不同,对水的电离影响程度不同,故B错误;FeO+HOHFeO+OH-的平衡常数K
2 1
=,a点时c(FeO)=c(HFeO),pOH=1.6,则K =10-1.6,同理可知HFeO+HOHFeO
1 2 2 4+OH-的平衡常数K =10-5.2,HFeO+HOHFeO+OH-的平衡常数K =10-7.3,由此推
2 2 4 2 3 3
出<,故C正确;a点溶液中c(FeO)=c(HFeO),溶液中存在电荷守恒:c(Na+)+c(H+)+
c(H FeO)=c(OH-)+2c(FeO)+c(HFeO)+2c(SO),从O到a点溶液中发生反应:2NaFeO
3 2 4
+HSO ===2NaHFeO +NaSO ,溶液中c(SO)≠c(HFeO),则a点溶液中c(Na+)+c(H+)+
2 4 4 2 4
c(H FeO)≠c(OH-)+2c(FeO)+3c(HFeO),故D错误。]
3
12.D [a点时溶质成分为NaCl和CH COOH,c(CH COOH)≈0.010 0 mol·L-1,c(H+)=
3 3
10-3.38 mol·L-1,K(CHCOOH)=≈=10-4.76,故 A 正确;a 点溶液为等浓度的 NaCl 和
a 3
CHCOOH混合溶液,存在元素守恒:c(Na+)=c(Cl-)=c(CHCOOH)+c(CHCOO-),故B
3 3 3
正确;点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸
3 3
性,说明CHCOOH的电离程度大于CHCOO-的水解程度,则c(CHCOOH)d,故D错误。]
13.D [石蕊不能用作酸碱中和滴定的指示剂,根据图示滴定终点的 pH,可知第二反应终
点应用酚酞作指示剂,A项错误;X点对应的溶液中溶质主要是NaHA,W点到X点发生的
主要反应的离子方程式为HA+OH-===HA-+HO,B项错误;根据电荷守恒,c(Na+)+
2 2
c(H+)=c(OH-)+c(HA-)+2c(A2-),因为Y点对应的溶液中c(HA-)=c(A2-),所以c(Na+)+
c(H+)=c(OH-)+3c(A2-),C项错误;K =,由于W点c(HA-)=c(H A),故K =1.0×10-
a1 2 a1
2.3;K =,由于Y点对应的溶液中c(HA-)=c(A2-),故K =1.0×10-9.7;HAHA-+H+
a2 a2 2
与HA-A2-+H+相减即得HA+A2-2HA-,此时的平衡常数K===1.0×107.4,D项
2
正确。]
14.(1)2NH +HO+SO ===2NH+SO(或2NH ·H O+SO ===2NH+SO+HO) HSO
3 2 2 3 2 2 2
(2)ZnSO ZnSO+SO +HO===Zn2++2HSO(或ZnO+2SO +HO===Zn2++2HSO)
3 3 2 2 2 2
(3)随着pH降低,HSO浓度增大 减小
第 57 练 难溶电解质的沉淀溶解平衡
1.C 2.C 3.D
4.C [Ag+与氨分子结合生成二氨合银离子,导致银离子浓度减小,促使AgCl (s)Ag+
(aq)+Cl-(aq)正向移动,说明NH 结合Ag+能力比Cl-强,B正确;银镜反应后的试管壁上
3
是银单质,银离子能够与氨水反应,银单质不能,C错误;浓硝酸能够中和一水合氨,使
Ag++2NH ·H O[Ag(NH)]++2HO逆向移动,银离子与溶液中的氯离子结合生成沉淀,
3 2 3 2 2
所以加浓硝酸后生成的沉淀为AgCl,D正确。]
5.C [升高温度可以使HCO分解,海水中的CO浓度增加;当CO 浓度一定时,T 温度下
2 1的海水中CO浓度更高,因而T >T ,A正确、C错误;观察图像可知,随CO 浓度增加,
1 2 2
海水中的CO浓度下降,B正确;珊瑚礁的主要成分是CaCO ,存在平衡:CaCO (s)Ca2+
3 3
(aq)+CO (aq),若海水中的CO浓度下降,会导致平衡正向移动,珊瑚礁会逐渐溶解,D
正确。]
6.D [弱碱性的海水利于月桂酸形成月桂酸根离子,使得 Ca PO (OOCC H )(s)3Ca2+
3 4 11 23 3
(aq)+PO(aq)+3C H COO-(aq)平衡逆向移动,利于保护椰子蟹外壳,使其不易被腐蚀,B
11 23
正确;海水中 CO 浓度升高,溶液酸性增强,使得月桂酸根离子转化为月桂酸,促使
2
Ca PO (OOCC H )(s)3Ca2+(aq)+PO(aq)+3C H COO-(aq)平衡正向移动,导致腐蚀椰
3 4 11 23 3 11 23
子蟹的外壳,但不会使K 增大,D错误。]
sp
7.D 8.B
9.A [Mg(OH) 悬浊液中滴加几滴酚酞溶液后,溶液显红色,则溶液呈碱性,说明
2
Mg(OH) 能电离出OH-,是一种电解质,不能判断是否为弱电解质,A错误;Mg(OH) 溶解
2 2
产生的OH-与NH Cl溶液中的NH生成NH ·H O,能加快Mg(OH) 悬浊液的溶解,B正确;
4 3 2 2
因相同温度下,氢氧化镁比碳酸镁更难溶,碱过量时生成Mg(OH) ,D正确。]
2
10.B [常温下,K (NiCO)>K (PbCO ),故溶解度:NiCO>PbCO ,A项正确;逐滴加入
sp 3 sp 3 3 3
NaCO 溶液时,K (PbCO )较小,故先生成PbCO 沉淀,后生成NiCO 沉淀,B项错误;由
2 3 sp 3 3 3
于K (PbCO )1 mol·L-1,溶液pH>14,由图可知体系
中元素M主要以M(OH)存在,D错误。]
10.A
11.C [由图可知pH=4,即c(H+)=10×10-5 mol·L-1时,c2(M+)=7.5×10-8 mol2·L-2,
c(M+)=×10-4 mol·L-1<3.0×10-4 mol·L-1,A正确;由图可知,c(H+)=0时,可看作溶液
中有较大浓度的OH-,此时A-的水解极大地被抑制,溶液中c(M+)=c(A-),则K (MA)
sp
=c(M+)·c(A-)=c2(M+)=5.0×10-8,B正确;MA饱和溶液中,M+不发生水解,A-水解使
溶液呈碱性,若使pH=7,需加入酸,会引入其他阴离子,此时 c(M+)+c(H+)≠c(A-)+
c(OH-),C错误;K(HA)=,当c(A-)=c(HA)时,由元素守恒知c(A-)+c(HA)=c(M+),则
a
c(A-)=,K (MA)=c(M+)·c(A-)==5.0×10-8,则c2(M+)=10×10-8 mol2·L-2,对应图得此
sp
时溶液中c(H+)=2.0×10-4 mol·L-1,K(HA)==2.0×10-4,D正确。]
a
12.C
13.C [根据图像可知:横坐标代表pH,随着pH增大,溶液碱性增强,c(HCO)、c(CO)
增大,先生成HCO,再生成CO,所以曲线①代表HCO,曲线②代表CO,因为碳酸钙是难
溶物,因此随着c(CO)增大,溶液中c(Ca2+ )减小,推出曲线③代表Ca2+,A正确;电离平
衡常数只受温度的影响,曲线①和②的交点代表c(HCO)=c(CO),即K ==10-10.3,故
a2
K (H CO)的数量级为 10-11,B 正确;曲线②和③的交点代表 c(CO)=c(Ca2+),根据
a2 2 3
K (CaCO)=c(CO)·c(Ca2+)=10-8.7,则c(CO)== mol·L-1=10-4.35 mol·L-1,即a=-
sp 3
4.35;根据电离平衡常数K =,c(HCO)== mol·L-1=10-2.65 mol·L-1,即b=-2.65,C
a2
错误;当pH=10.3时,c(CO)=10-1.1 mol·L-1,c(Ca2+)== mol·L-1=10-7.6 mol·L-1,D
正确。]
14.(1)Li O·Al O·4SiO (2) 将矿石粉碎(搅拌、升高温度等) (3)4.7 (4)Mg(OH) 、CaCO
2 2 3 2 2 3
(5)Na CO(或其他合理答案) 净化 (6)6Li CO+4Co O+O=====12LiCoO +6CO
2 3 2 3 3 4 2 2 2
第 59 练 无机化工流程题的解题策略
1.(1)将Co3+还原为Co2+ (2)氧化浸出液中的Fe2+,便于调pH除去 Fe(OH) 除去Cu2+
3
(3)CaSO 、MgSO 10-10.8
4 4
2.(1)90 ℃ SiO 、CaSO c(SO)增大,使平衡Ca2+(aq)+SO(aq)CaSO(s)正向移动,
2 4 4促进CaSO 析出
4
(2)MnO +2Fe2++4H+===Mn2++2Fe3++2HO
2 2
(3)1.56×10-3
3.(1)做还原剂,将BaSO 还原 (2)S2-+Ca2+===CaS↓ (3)c (4)不可行 CaS也会与盐
4
酸反应生成有毒气体和可溶于水的CaCl ,影响产品纯度 (5)BaCl +TiCl +2(NH )C O +
2 2 4 4 2 2 4
HO===BaTiO(C O)↓+4NH Cl+2HCl (6)1∶1
2 2 4 2 4
解析 由流程和题中信息可知,BaSO 与过量的碳粉及过量的氯化钙在高温下焙烧得到
4
CO、BaCl 、易溶于水的BaS和微溶于水的CaS;烧渣经水浸取后过滤,滤渣中含碳粉和
2
CaS,滤液中有BaCl 和BaS;滤液经酸化后浓缩结晶得到BaCl 晶体,溶于水后,加入
2 2
TiCl 和(NH )C O 将钡离子充分沉淀得到 BaTiO(C O) ;BaTiO(C O) 经热分解得到
4 4 2 2 4 2 4 2 2 4 2
BaTiO 。(3)浸取后滤液中主要为BaCl 和BaS,为不引入杂质,“酸化”步骤应选用盐酸。
3 2
(6)“热分解”生成粉状钛酸钡,该反应的化学方程式为BaTiO(C O)=====BaTiO +2CO↑
2 4 2 3 2
+2CO↑,因此,产生的 ∶n =1∶1。
CO
4.(1)ab (2)2Bi S +9O=====2BiO +6SO (3)抑制金属离子水解 (4)SiO (5)Mn O +
2 3 2 2 3 2 2 2 3
6H++2Cl-===2Mn2++Cl↑+3HO (6)将Fe3+转化为Fe2+
2 2
5.(1)将废锌催化剂粉碎 温度升高,NH 挥发,使生成的[Zn(NH )]2+减少 (2)分液
3 3 4
(3)Mn2++2NH ·H O+HO===MnO ↓+2NH+2HO
3 2 2 2 2 2
(4)①[Zn(NH )]2++S2-===ZnS↓+4NH 2.16×1014
3 4 3
②C (5)0.01 mol·L-1
解析 废锌催化剂主要成分为ZnO及少量Fe O 、CuO、MnO、SiO ,加入过量NH -NH Cl
2 3 2 3 4
溶液,生成[Zn(NH )]2+、[Cu(NH )]2+,同时生成Fe(OH) 、Mn(OH) 等,SiO 不溶解,过
3 4 3 4 3 2 2
滤一起除去,再向滤液中加入 HO 溶液,进行深度除锰,反应的离子方程式为 Mn2++
2 2
2NH ·H O+HO===MnO ↓+2NH+2HO,再加入(NH )S,进行深度除铜,反应的离子方
3 2 2 2 2 2 4 2
程式为[Cu(NH )]2++S2-===CuS↓+4NH ,过滤,除去MnO 和CuS,向滤液中加入萃取剂,
3 4 3 2
使锌进入有机萃取剂中,分液后,再向有机萃取剂中加入硫酸进行反萃取,得到硫酸锌溶液,
然后进行电解,得到锌。(4)①当(NH )S加入量≥100%时,锌的回收率下降的可能原因是
4 2
[Zn(NH )]2+与S2-结合生成了硫化锌,离子方程式为[Zn(NH )]2++S2-===ZnS↓ +4NH
3 4 3 4 3
,该反应的平衡常数为K==·=×=×≈2.16×1014。②当(NH )S加入量为120%时,铜
4 2
锌比约为2.0×10-6,达到深度除铜标准,继续加大(NH )S加入量会导致锌的回收率下降且
4 2
不经济,故选C。(5)由滴定原理:Zn2++HY2-===ZnY2-+2H+,n(Zn2+)=n(H Y2-)=0.010
2 2
0 mol·L-1×
22.30×10-3 L=2.23×10-4 mol,反萃取水相中Zn2+的浓度为≈0.01 mol·L-1。第十三章 有机化合物的结构 烃
第 60 练 有机化合物的分类、命名及研究方法
1.D 2.C 3.A
4.D [乙烯的官能团为碳碳双键,属于烯烃,而聚乙烯结构中只有 C—C及C—H,不属于
烯烃,A错;B中物质名称为乙酸乙酯,属于酯,B错;C中给出的两种物质前者属于酚,
后者属于醇,C错;绝大多数有机物含有官能团,但烷烃等没有官能团,D对。]
5.C 6.D 7.D
8.D [根据质谱图得到X的相对分子质量为136,故A正确;6.8 g X(物质的量为0.05 mol)
完全燃烧生成3.6 g H O(物质的量为0.2 mol)和8.96 L(标准状况)CO(物质的量为0.4 mol),
2 2
根据原子守恒和相对分子质量得到X的分子式为C HO ,故B正确;根据红外光谱可知该
8 8 2
有机物只含一个苯环且苯环上只有一个取代基,含有 C==O、C—H、C—O—C,核磁共振
氢谱有4组峰且面积之比为3∶2∶2∶1,则X的结构简式为 ,则符合
题中X分子结构特征的有机物有1种,故C正确;与X属于同类化合物的同分异构体有
、 、 、 、
共5种,故D错误。]
9.B [SO 与NaOH溶液反应生成NaSO 和HO,乙烯与NaOH不反应,洗气可以分离,
2 2 3 2
A正确;乙酸与NaOH溶液反应,乙醇溶于水,不能进行分液,B错误;苯甲酸与NaOH溶
液反应生成苯甲酸钠和HO,苯与NaOH溶液不反应且不溶于NaOH溶液,混合液分层,可
2
进行分液,C正确;乙烯与溴水发生加成反应,乙烷不反应,可以通过盛有溴水的洗气瓶洗
气进行分离提纯,D正确。]
10.A 11.C
12.(1)2,4-二甲基-4-乙基庚烷 (2)甲酸乙酯 (3)苯甲醇 (4)3-甲基苯酚(或间甲基苯酚)
(5)邻羟基苯甲酸 (6)丁烯二酸
13.(1)5 (2)醛基 醚键 (3)(酚)羟基、酮羰基、酰胺基、碳溴键
14.(1)蒸馏烧瓶 仪器y
(2)①C HO ②88 C HO
2 4 4 8 2(3)羟基、酮羰基
解析 (1)球形冷凝管一般用于冷凝回流装置中,故虚线框内应选仪器y。
(2)①根据M中碳、氢元素的质量分数确定氧元素的质量分数为w(O)=100%-54.5%-9.1%
=36.4%,分子内各元素原子的个数比 N(C)∶N(H)∶N(O)=∶∶=2∶4∶1,其实验式为
C HO。②M的相对分子质量为2×44=88,设分子式为(C HO) ,则44n=88,n=2,则
2 4 2 4 n
M的分子式为C HO。
4 8 2
(3)根据核磁共振氢谱图中有4组峰,说明分子中含有4种不同化学环境的氢原子,且个数比
为1∶3∶1∶3,结合红外光谱图所示含有C—H、H—O、C==O等化学键,其结构简式为
,所含官能团为羟基、酮羰基。
第 61 练 有机化合物的空间结构 同系物 同分异构体
1.D 2.D
3.B [CH==CH为聚乙炔,可以制成导电塑料,A正确;甘油是丙三醇,属于三元醇,
乙醇是饱和一元醇,结构不相似,不互为同系物,B错误;同素异形体是指同一元素形成的
不同单质,则O 和O 互为同素异形体,C正确;有机物结构中单键可以旋转,
2 3
和 分子式相同,结构相同,是同一种物质,D正确。]
4.D [根据结构简式可知,K分子中含有苯环,属于芳香族化合物,A错误;K分子中碳
原子之间形成非极性键,B错误;K分子中的碳原子的杂化方式有sp2、sp3两种,氮原子的
杂化方式是sp3,C错误;K分子中含有苯环、双键和单键,因此含有大π键、π键和σ键,
含有氨基和羟基,分子间可以形成氢键,D正确。]
5.C [由结构简式可知,a、b、c的分子式均为C H ,三者的分子结构不同,互为同分异
7 8
构体,A正确;苯环上的碳原子及双键上的碳原子均采取sp2杂化,饱和碳原子采取sp3杂化,
B正确;a分子苯环上有3种氢原子,甲基上有1种氢原子,故其一氯代物有4种,C错误;
a分子含有苯环,苯是平面形结构,直接 与苯环相连的碳原子在苯环所在平面内,故a中所有碳原子共平面,b、c分子中两个环状结构均通过饱和碳原子连接,所有碳原子一定不共
平面,D正确。]
6.D 7.C
8.D [环己烷中所有C原子与其所连原子构成四面体结构,键角不是120°,A正确;
C H Cl的等效氢原子与C HCl 的等效氯原子数目相同,则同分异构体数目相同,B正
n 2n+1 n 2n+1
确;含有手性碳原子的饱和链烃中,碳原子数最少的可能是3-甲基己烷,也可能是2,3-二甲
基戊烷,D错误。]
9.A 10.C 11.B
12.A [分子式为 C HO 的酯可能是 HCOOC H 、CHCOOCH ,水解得到的醇分别是
3 6 2 2 5 3 3
C HOH、CHOH,得到的酸分别是HCOOH、CHCOOH,C HOH、CHOH与HCOOH、
2 5 3 3 2 5 3
CHCOOH 形成的酯共有 4 种,A 项错误;四联苯是具有两条对称轴的物质,即
3
,有5种不同化学环境的氢原子,故有5种一氯代物,B项正确;该
有机物含有4个环和1个碳碳双键,不饱和度为5,苯环的不饱和度为4,所以可能有属于
芳香族的同分异构体,D项正确。]
13.C [a含有碳碳双键,能够使溴的CCl 溶液褪色,而b不可以,A正确;b和d的分子
4
式均为C HO,结构不同,互为同分异构体,B正确;c的二氯代物有 、 、
4 8
、 ,共4种,C错误;d分子中含有羟基,可以发生取代反应,含有碳碳双
键,可以发生加聚反应,D正确。]
14.9 、 、
15.(1)2 2 4
(2) 、 、 、
、 、
第 62 练 烃 化石燃料
1.D 2.D
3.A [符合通式C H (n≥2)的烃可能是环烷烃,故B错误;烯烃和炔烃都能被酸性高锰酸
n 2n钾溶液氧化而使其褪色,故C错误;同碳原子数的炔烃和二烯烃分子式相同,结构不相似,
因此不互为同系物,故D错误。]
4.B 5.C
6.C [由流程可知乙烯与水发生加成反应生成乙醇,乙烯与氯气发生加成反应生成 1,2-二
氯乙烷,继续发生消去反应生成氯乙烯,乙烯发生加聚反应生成聚乙烯,乙烯氧化生成乙醛,
乙醛与新制氢氧化铜在加热条件下反应生成乙酸。]
7.C [丙烯含有碳碳双键,能被酸性高锰酸钾溶液氧化,能使其褪色,A正确;丙烯属于
烃,可燃烧生成二氧化碳和水,B正确;丙烯与溴发生加成反应的产物是CHBrCHBrCH ,
2 3
C错误。]
8.D 9.D 10.C
11.B [由二苯乙烯的结构简式可知,其分子式为C H ,A错误;二苯乙烯中含有碳碳双
14 12
键和苯环,能发生加聚反应、取代反应、氧化反应、加氢还原反应,B正确;苯环上的所有
原子均能与苯环共平面,双键连接的原子可以共平面,二苯乙烯中所有原子可能共平面,C
错误;1 mol二苯乙烯在一定条件下与足量H 反应最多消耗7 mol H ,D错误。]
2 2
12.C [双环戊二烯和环戊二烯中均含有碳碳双键,均能使酸性 KMnO 溶液褪色,B正确;
4
双环戊二烯的不饱和度为5,苯环的不饱和度为4,故双环戊二烯存在芳香烃类同分异构体,
C错误;环戊二烯中含有“—CH—”结构,所有原子不可能共平面,D正确。]
2
13.(1) 120°
(2)2CH CHOH+O――→2CHCHO+2HO
3 2 2 3 2
(3)碳碳双键、碳氯键
(4)一样多
(5)n ――→
(6)取代 液溴、铁粉、加热
(7)
14.(1)D (2)碳碳双键 取代反应 (3)保护碳碳双键,防止被氧化 丙烯酸甲酯
(4)nCH==CHCOOCH +n
2 3―――→
解析 A为烯烃,分子式为C H ,其结构简式为CHCH==CH ;结合反应②的生成物为
3 6 3 2
CH==CHCH OH及反应①的条件可知B为ClCH CH==CH ;生成D的反应物为CH==CH
2 2 2 2 2
—CN,由黏合剂 M 逆推可知 D 为 ,故 C 为 CH==CHCOOCH 。
2 3
(1)CH CH==CH 可发生加成反应和氧化反应,不能发生缩聚反应,A 项错误;C 为
3 2
CH==CHCOOCH ,其分子式应为C HO ,C项错误。(2)A为CHCH==CH ,其官能团为
2 3 4 6 2 3 2
碳碳双键,反应①是甲基在光照条件下的取代反应。(3)步骤③是CH==CHCH OH通过加成
2 2
反应,使碳碳双键得以保护,防止后续加入酸性KMnO 溶液时被氧化,待羟基被氧化后,
4
再通过步骤⑤的消去反应,得到原来的碳碳双键。
第十四章 烃的衍生物
第 63 练 卤代烃 醇 酚
1.C 2.C
3.D [将石油裂解后的气体通入溴的CCl 溶液中,溶液褪色,说明石油裂解后有不饱和烃
4
生成,但不一定是乙烯,故A错误;向废水中加入少量稀溴水,未见白色沉淀,可能是因
为生成的2,4,6-三溴苯酚的量太少而溶于苯酚,故B错误;向甲苯中滴加少量酸性KMnO
4
溶液,振荡后溶液褪色,甲苯被氧化为苯甲酸,甲基被氧化,苯环没有被酸性KMnO 氧化,
4
故C错误;某一卤代烃与NaOH水溶液共热后,卤代烃发生水解,加入过量硝酸酸化,再
滴入AgNO 溶液,有白色沉淀生成,说明沉淀是氯化银,证明该卤代烃为氯代烃,故 D正
3
确。]
4.D [烷烃 X分子中碳与氢的质量比为 36∶7,则 C、H原子数目之比为∶=3∶7=
6∶14,烷烃通式为C H ,故X的分子式为C H 。烷烃X萃取溴水中的溴,上层呈橙红
n 2n+2 6 14
色,说明X的密度比水小,故A错误;C H 的同分异构体有己烷、2-甲基戊烷、3-甲基戊
6 14
烷、2,3-二甲基丁烷、2,2-二甲基丁烷,共5种,故B错误;X为烷烃,不能与溴发生加成
反应使溴水褪色,故C错误;C H 能与溴发生取代反应得到溴代烃,溴代烃与水不互溶,
6 14
可以通过加水确定试管2中的有机层是上层还是下层,故D正确。]5.C 6.A 7.C
8.D [甲、丙、丁与NaOH的醇溶液共热不能发生消去反应,加入稀硝酸至溶液呈酸性,
再滴入AgNO 溶液,没有沉淀生成,故A错误;甲中加入NaOH的水溶液共热,没有进行
3
酸化,再滴入AgNO 溶液,溶液中的OH-会干扰卤素原子的检验,故B错误;乙发生消去
3
反应只能得到丙烯一种烯烃,故C错误;丙与NaOH的水溶液共热生成2,2-二甲基-1-丙醇,
能被氧化为2,2-二甲基丙醛,故D正确。]
9.B [该化合物含有氧元素,不属于烃类,A错误;该化合物含有酚羟基,能与FeCl 溶液
3
作用显紫色,B正确;该化合物含有酚羟基,溴可以取代2个酚羟基的4个邻位,则1 mol
双酚A最多消耗4 mol Br ,C错误;酚羟基的酸性小于碳酸,该化合物可以与NaCO 溶液
2 2 3
反应生成NaHCO ,不能放出CO 气体,D错误。]
3 2
10.C
11.A [由转化关系可知,X为 或 ,Y为 。 或 分子中
都含有饱和碳原子,饱和碳原子的空间结构为四面体形,所以 X分子中所有碳原子不能共
面,故A错误;X分子中的碳碳双键能与酸性高锰酸钾溶液发生反应,使溶液褪色,Y分子
中的 能被酸性高锰酸钾溶液氧化而使其褪色,故B正确;在浓硫酸、加热条
件下,Y能发生消去反应生成X,故C正确;含有 结构的Y的同分异构体的环上可能
连有乙基或2个甲基,其中连有乙基的有3种结构,连有2个甲基的有9种结构,共有12种,
故D正确。]
12.D
13.(1)碳碳双键 (2)取代
(3)①ClCH —CHOH—CH Cl ②B为CH==CH—CH Cl,Cl的电负性较大,使双键电子云
2 2 2 2
向中心碳原子偏移;HOCl中:HO—Cl,因此—OH易连在端基碳原子上
(4)ClCH —CHCl—CH OH+2NaOH――→HOCH —CHOH—CH OH+2NaCl
2 2 2 2
14.(1)CH ==CHCH Br (2)取代反应
2 2
(3) + HO― ― ― + ― ― ― ― →
2
CH==CHCH OH
2 2
(4)(5)ⅰ. ――→ ――――――――→
―――――――→CH==CHCOO-――→CH==CHCOOH
2 2
ⅱ.保护目标产物中的碳碳双键(或防止碳碳双键被氧化)
解析 B 的分子式为 C HBr,结合 B 和 A 反应生成产物的结构简式可知,B 为
3 5
CH==CHCH Br,A 为 ,根据已知信息①可知 C 的结构简式为
2 2
,由已知信息②可知佳味醇的结构简式为
。
(2)A 分 子 中 羟 基 上 的 氢 原 子 被 CH==CHCH Br 中 的 烃 基 取 代 生 成
2 2
和HBr,该反应的反应类型为取代反应。
(5)B的结构简式是CH==CHCH Br,B发生水解反应生成的 E为CH==CHCH OH,E和
2 2 2 2
HBr 发生加成反应生成 F,F 的结构简式是 CHCH(Br)CH OH,F 发生催化氧化生成
3 2
CHCH(Br)CHO,产物继续被氧化、酸化生成 CHCH(Br)COOH,最后通过消去反应生成
3 3
CH==CHCOOH;因为在氧化羟基的同时碳碳双键也易被氧化,所以为了保护碳碳双键才
2
设置反应②。
第 64 练 醛、酮
1.B
2.C [A项,CHCHO与HCN发生加成反应,H原子加在醛基带负电荷的O原子上,—
3
CN加在不饱和碳上,生成 ,故A正确;同理,CHCHO与NH 发生加成
3 3
反应生成 ,故 B 正确;CHCHO 与 CHOH 发生加成反应生成
3 3
,故C错误;丙酮与氢气发生加成反应生成2-丙醇,故D正确。]
3.A [油脂在碱性条件下发生水解反应,所以在做银镜实验准备洁净试管时,可用碱液煮
沸试管后再洗净,故A正确;银氨溶液久置会析出爆炸性沉淀物,必须现用现配,故 B错
误;在一支洁净的试管中加入少量的AgNO 溶液,然后滴加稀氨水,直到生成的沉淀刚好
3
溶解为止,得到的无色溶液称为银氨溶液,故C错误;水浴加热使反应容器内试剂受热均
匀,且易于控制反应温度,直接加热受热不均匀且温度太高,银镜反应需水浴,故 D错误。]
4.B 5.C
6.C [企鹅酮中含碳碳双键,能使酸性高锰酸钾溶液褪色,A正确;甲基碳原子上可发生
取代反应,B正确;1 mol企鹅酮含2 mol碳碳双键和1 mol酮羰基,都能和H 加成,加成
2
产物为C H OH,需消耗3 mol H ,C错误;环上有一个碳原子连有两个甲基,这个碳原子
10 19 2
以碳碳单键和四个碳原子相连,所有碳原子一定不可能共平面,D正确。]
7.D [单键均为σ键,双键中含有1个σ键、1个π键,X分子中σ键和π键数目之比为
9∶1,A错误;Y的名称为4-硝基苯甲醛,B错误;Z中羟基碳的相邻碳上有氢,能发生消
去反应,C错误; 分子中含有手性碳原子,存在对映异构现象,D正确。]
8.C 9.C
10.D [肉桂醛中苯环上能发生取代反应,碳碳双键、苯环和醛基能发生加成反应,碳碳
双键能发生聚合反应,A正确;肉桂醛含碳碳双键和醛基,苯甲醛含醛基,都能使酸性
KMnO 溶液褪色,B正确;苯环为平面结构,醛基为平面结构,两者通过单键相连,所有
4
原子可能共平面,C正确;肉桂醛含碳碳双键和醛基,苯甲醛含醛基,两者不互为同系物,
D错误。]
11.B [由结构简式可知,环己酮缩乙二醇不是高聚物,则生成环己酮缩乙二醇的反应不是
缩聚反应,故A错误;环己酮燃烧的反应属于氧化反应,一定条件下与氢气的加成反应属
于还原反应,故B正确;由结构简式可知,环己酮缩乙二醇的结构对称,分子中含有4种氢
原子,则一氯代物有4种,故C错误;由结构简式可知,环己酮分子中含有饱和碳原子,饱
和碳原子的空间结构为四面体形,则分子中所有碳原子不可能共平面,故D错误。]
12.(1)C H O 1-丁醇(或正丁醇)
4 10
(2)CH CHCHCHO+2Cu(OH) +NaOH――→CHCHCHCOONa+Cu O↓+3HO (3)2 银
3 2 2 2 3 2 2 2 2
氨溶液、稀盐酸、溴水 (4)还原反应(或加成反应) 羟基 (5)浓硫酸、加热
13.(1)对二甲苯 取代反应
(2) +NaOH――→ +NaCl
(3)O /Cu或Ag,加热
2
(4) 碳碳双键、醛基
(5)8 、(6)CH CHOH――→CHCHO―――――→ ――→CHCH==CHCHO
3 2 3 3
解析 由题给信息结合F的结构简式可知E为 ,则D为
, C 为 , 由 此 可 知 B 为
,A为对二甲苯。(5)D为 ,对应的同分异构
体如含有2个取代基,可以为—CH 、—CHO,则有邻、间2种,也可以为—CH==CH 、
3 2
—OH,有邻、间、对3种,如含有1个取代基,可以为 或—CHCHO或—O—
2
CH==CH ,则D的同分异构体有8种。(6)以乙醇为原料制备2-丁烯醛,乙醇可先氧化生成
2
乙醛,乙醛发生加成反应生成 CHCH(OH)CH CHO,然后发生消去反应可生成
3 2
CHCH==CHCHO,合成路线见答案。
3
第 65 练 羧酸 羧酸衍生物
1.D 2.C 3.B
4.B [苯甲酸的同系物中相对分子质量最小的是C HO ,A错误;C项中的醇可能是乙二
8 8 2
醇,C错误;苯甲酸钠是常用的食品防腐剂,不能用作奶粉中的抗氧化剂,D错误。]
5.D [A项,与足量的NaOH溶液共热,生成羧酸钠和酚钠结构,由于酸性:亚硫酸>
> ,则再通入SO 生成邻羟基苯甲酸,错误;B项,与稀HSO 共
2 2 4
热后,生成邻羟基苯甲酸,再加入足量的NaOH溶液,生成羧酸钠和酚钠结构,错误;C项,
加热溶液,通入足量的CO ,不发生反应,错误;D项,与稀HSO 共热后,生成邻羟基苯
2 2 4
甲酸,加入足量的NaHCO 溶液,—COOH反应生成羧酸钠,酚羟基不反应,正确。]
3
6.D 7.D
8.D [对苯二甲酸与乙二醇发生酯化反应可以制备该有机物,B正确;该有机物含有2个
醇羟基,能与二元羧酸发生缩聚反应,能发生氧化反应,C正确;采用“定一移一”的方法
可知,苯环上的二氯代物不止2种,D错误。]
9.D [解答本题时注意以下两点:①1 mol —OH或1 mol —COOH与足量金属钠反应分别
放出0.5 mol H ;②醇羟基不与NaHCO 反应,1 mol —COOH与足量NaHCO 反应放出1
2 3 3
mol CO。]
2
10.A 11.D 12.C13.(1)C H O
7 10 5
(2)
(3) +HO
2
(4)2.24 L (5)消去反应
14.(1)甲苯 (2)氢氧化钠水溶液,加热
(3)氧化反应
(4) +2Cu(OH) +NaOH――→
2
+Cu O↓+3HO
2 2
(5)H为酚类化合物,易被空气中的氧气氧化
(6)CH CHOH――→CHCHO――――――→CHCH==CHCHO――――――-―→
3 2 3 3
CHCH==CHCOOH
3
解析 A是相对分子质量为92的芳香烃,设该物质分子式是C H ,则14n-6=92,解得
n 2n-6
n=7,A是 ,名称为甲苯,结合C的结构简式逆推可知A与Cl 发生取代反
2
应生成B( ),C发生甲基上的取代反应生成D,D是C的一氯取代物,则
D的结构简式为 ,F能发生已知信息③的反应生成G,说明F中含
有醛基,则D发生水解反应生成E为 ,E发生催化氧化反应生
成F为 ,G的结构简式为 ,G发生氧化反应,然后酸化生成H为 。(6)利用已知信息③实现碳链变化,
乙醇发生催化氧化反应生成乙醛,2分子乙醛反应生成CHCH==CHCHO,再进一步氧化生
3
成CHCH==CHCOOH。
3
第 66 练 生物大分子 合成高分子
1.A 2.C
3.A [单位质量的H元素燃烧放出的热量大于C元素,甲烷为含氢量最高的烃,则相同条
件下,等质量的甲烷、汽油、氢气完全燃烧,氢气放出的热量最多,甲烷次之,汽油最少,
A项错误;油脂在碱性条件下的水解反应即为皂化反应,得到的高级脂肪酸盐是肥皂的主要
成分,B项正确。]
4.B [聚丙烯由丙烯(CH==CHCH )通过加聚反应制得,聚丙烯的结构简式为
2 3
,A正确、B错误;由聚丙烯的结构可知聚丙烯为线型结构,具有热塑性,
C正确;聚丙烯结构中的化学键为单键,不易被氧化、不能水解,因此聚丙烯在自然环境中
不容易降解,D正确。]
5.D 6.B 7.A
8.B [该高分子材料中含有酯基,能与碱溶液发生水解反应,则其所制容器不能用于盛放
碳酸钠溶液,故 A 正确;合成该高分子的两种单体分别为 CH==C(CH)COOCH 、
2 3 3
CH==CHCOOCH CHCHCH,乙酸乙酯只有酯基,没有碳碳双键,结构不相似,不互为同
2 2 2 2 3
系物,故B错误;由图可知,自修复过程中“—COOCH CHCHCH”基团之间没有化学键
2 2 2 3
的变化,故D正确。]
9.A 10.B 11.C
12.C [PLA 是聚酯类高聚物,链节为 ,该高聚物的单体为
,单体含羟基,可以发生消去、氧化、酯化等反应类型,故 A、B正确;PLA制取过程中可能生成副产物,两个单体( )之间相互发生酯化反应形
成环,结构简式为 ,故C错误;PLA结构中主要官能团为酯基,具有酯类
的性质,在碱性条件下易发生水解反应而降解,而聚氯乙烯塑料不易降解,故D正确。]
13.(1)酯基 CHBr
3
(2) 取代反应
(3) +2CHOH +2HO
3 2
(4)CH COOH+CH≡CH―→ 加成反应
3
(5)n + n ― ― →
+(2n-1)CHOH
3
14.(1) (2)还原反应 取代反应
(3)酰胺基 羧基
(4)
(5)解析 (1)由已知信息①可知, 与 反应时断键与成键位置为 ,由此可知A
的结构简式为 。
(2)A→B的反应过程中失去O原子,加入H原子,属于还原反应;D→E的反应过程中与醛
基相连的碳原子上的H原子被溴原子取代,属于取代反应。
(4) 丁 二 酸 酐 ( ) 和 乙 二 醇 (HOCHCHOH) 合 成 聚 丁 二 酸 乙 二 醇 酯 (
2 2
)的过程中,需先将 转化为丁二酸,可利用已
知信息②实现,然后利用B→C的反应类型合成聚丁二酸乙二醇酯。
(5)以乙烯和 为原料合成 的路线设计过程中,可利用E+F→G的反应类
型实现,因此需先利用乙烯合成 , 中醛基可通过羟基催化氧化
而得, 中溴原子可利用D→E的反应类型实现。
第十五章 有机化合物综合应用
第 67 练 官能团与有机物的性质 有机反应类型
1.C 2.C
3.C [A项,对比M、N的键线式,M生成N的反应为加成反应,错误;B项,N的分子
式为C HCl ,C HCl 为C H 的二氯代物,C H 有两种同分异构体:CHCHCHCH 和
4 8 2 4 8 2 4 10 4 10 3 2 2 3
, 采 用 定 一 移 一 法 , N 的 同 分 异 构 体 有 : CHCHCHCHCl 、
3 2 2 2
CHCHCHClCH Cl、
3 2 2CHCHClCH CHCl 、 CHCHCCl CH 、 CHCHClCHClCH 、 、
3 2 2 3 2 2 3 3 3
、 ,共8种,错误;C项,N中官能团为碳氯键,不能使酸
性KMnO 溶液褪色,Q中官能团为羟基,能使酸性KMnO 溶液褪色,正确;D项,由于H
4 4 2
所处温度和压强未知,不能使用22.4 L·mol-1计算H 的体积,错误。]
2
4.B [X的结构简式中含有碳碳双键,根据乙烯的空间结构为平面形,X中所有原子可能
位于同一平面,故A错误;麝香酮中含有烷基,能发生取代反应,多数有机物能够燃烧,
燃烧属于氧化反应,故B正确;麝香酮的分子式为C H O,与环十二酮分子式不同,它们
16 30
不互为同分异构体,故C错误。]
5.C [该有机物含有醚键、羟基、酰胺基、碳碳双键四种官能团,A正确;该有机物含有
酚羟基,能与FeCl 溶液发生显色反应,B正确;NaHCO 不能与酚羟基反应,故该有机物
3 3
不能与NaHCO 溶液反应生成CO ,C错误;1 mol该有机物最多能与2 mol NaOH发生反应,
3 2
酚羟基与酰胺基各消耗1 mol,D正确。]
6.D 7.C 8.D
9.B [该物质中含氧官能团只有酯基,A错误;含有碳碳双键,能与溴水发生加成反应,
也能被酸性高锰酸钾溶液氧化而使其褪色,B正确;该物质不含羧基和羟基,不能发生酯化
反应,C错误;该物质中只有酯基能消耗NaOH,1 mol该物质最多消耗1 mol NaOH,D错
误。]
10.D [c和HCl发生取代反应生成d,则d的结构简式为 ,B、C正确;
d→e是d分子中的氯原子被—CN取代,发生的是取代反应,D错误。]
11.D [A分子中含有2个酚羟基,处于苯环的间位,其系统名称是1,3-苯二酚,A错误;
反应①是A分子苯环上1个H原子被I原子代替,属于取代反应;反应②是B分子苯环上的
I原子被乙烯基代替,属于取代反应,B错误;酚羟基的邻、对位和溴发生取代反应,碳碳
双键和溴发生加成反应,1 mol C最多能与3 mol Br 反应,C错误;C中含有酚羟基,C遇
2
氯化铁溶液发生显色反应,D正确。]
12.(1)氧化反应 取代反应 取代反应(或酯化反应) 取代反应
(2) +3NaOH――→ +CHCOONa+CHOH+HO
3 3 2
13.(1)氯气/光照、取代反应(2)取代反应 加成反应 氧化反应
(3) +HO――→
2
(4) + ――→
14.(1)加成反应 HOOCCH CHCOOH
2 2
(2)碳碳三键、羟基 1,4-丁二醇
(3)
(4)nHOOCCH CHCOOH+nHOCH CHCHCHOH
2 2 2 2 2 2
+(2n-1)H O (5)ac
2
解析 (1)依据烯烃的性质知,A→B的反应是HOOCCH==CHCOOH与氢气发生的加成反应,
故B的结构简式为HOOCCH CHCOOH。(2)利用已知信息和合成路线可知,C的结构简式
2 2
为HOCH —C≡C—CHOH,其中所含官能团的名称为碳碳三键、羟基;D的碳链上1、4
2 2
号碳原子连有羟基,故 D的名称为 1,4-丁二醇。(5)物质A中含有碳碳双键,能使酸性
KMnO 溶液褪色,能与溴的CCl 溶液发生加成反应使其褪色,a项正确;物质A可与HBr
4 4
发生加成反应,b项错误;物质A含有羧基,可与新制的Cu(OH) 发生中和反应,c项正确;
2
1 mol A完全燃烧消耗3 mol O ,d项错误。
2
第 68 练 限定条件下同分异构体的判断与书写
1.102. 、
3. 12
解析 M为F的同分异构体,1 mol M最多能与3 mol NaOH发生反应,说明M中含有三个
酚羟基,同时苯环上连有4个取代基,则另一个取代基为—CHCHCH 或 ,苯
2 2 3
环上有4个取代基,其中3个取代基相同的同分异构体有6种,故满足条件的M的结构有
6×2=12种。
4.8
5.6 (或 或 )
6.
解析 C的同分异构体属于芳香族化合物,说明含有苯环,能发生银镜反应,也能发生水解
反应,分子式中有两个O原子,说明是甲酸酯,水解产物之一能与 FeCl 溶液发生显色反应,
3
说明是甲酸酚酯,即含有结构 ,结合核磁共振氢谱有四组峰,且峰面积之比为
1∶1∶2∶6可知,结构中还有两个甲基,且两个甲基的位置对称,所以满足条件的结构简
式为 、 。7.16
解析 C的分子式为C H O ,H满足下列条件:①分子中除苯环外不含其他环状结构;②
10 10 2
仅含有一种官能团,能与新制Cu(OH) 反应,生成砖红色沉淀,说明含有两个—CHO;③
2
苯环上有3个取代基,可以是—CHO、—CHO、—CHCH ,此时有6种结构;也可以是—
2 3
CHO、—CHCHO、—CH,此时有10种结构,所以符合条件的H有16种。
2 3
8. 、 、 、
9. 、 、
、
10. 、 、 、
解析 化合物C HNO 的同分异构体同时符合:①能与FeCl 溶液发生显色反应,说明含有
8 7 4 3
酚羟基,1 mol有机物能与足量银氨溶液反应生成4 mol Ag,说明含有2个醛基;②核磁共
振氢谱显示分子中有4种不同化学环境的氢原子,说明分子结构对称;③分子中无N—O,
符合条件的同分异构体的结构简式见答案。
11.32 (或 或
)
解析 B为 ,P为B的同系物,分子式为C HNO ,满足条件:①芳香环上只有
8 9 2
两个取代基,②能与FeCl 溶液发生显色反应说明含有酚羟基或羟基连接在吡啶环上,③能
3
发生银镜反应,说明含有醛基,同分异构体有 、 、
、 、 、 、
、 、 、 (数字表示—OH的位置),共32种,其中核磁共振氢谱有6组峰,且峰面积比为2∶2∶2∶1∶1∶1的
一种分子的结构简式为 、 或
。
第 69 练 有机合成
1.D [题干中强调的是最合理的方案,A项与D项相比,步骤多一步,且在乙醇发生消去
反应时,容易发生分子间脱水、氧化反应等副反应;B项步骤最少,但取代反应不会停留在
“CHBrCHBr”阶段,副产物多,分离困难,原料浪费;C项比D项多一步取代反应,显
2 2
然不合理;D项相对步骤少,操作简单,副产物少,较合理。]
2.B [由溴乙烷→乙醇,只需溴乙烷在碱性条件下水解即可,路线不合理,且由溴乙烷→
乙烯为消去反应。]
3.C [M和N发生加成反应生成O;对比O和P的结构简式,O到P为加成反应,P到Q
发生消去反应。]
4.B [该合成路线为 ――→CHCH==CH――→ ――→ 。]
3 2
5.D
6.D [CH==CH—CH==CH 与Cl 发生1,4-加成反应产生ClCH CH==CHCH Cl,该物质与
2 2 2 2 2
NaOH的水溶液发生水解反应产生 HOCH CH==CHCH OH,其与HCl发生加成反应产生
2 2
HOCH CHCHClCH OH,再与浓硫酸混合加热发生消去反应产生CH==CCl—CH==CH ,D
2 2 2 2 2
错误。]
7.B [以环戊烷为原料制备环戊二烯的合成路线如下:
A项,由上述分析可知,A可为氯代环戊烷;B项,反应①为光照条件下的取代反应,反应
②为在氢氧化钠醇溶液、加热条件下的消去反应;C项,反应②的反应试剂和反应条件为氢
氧化钠醇溶液、加热,反应③的条件为常温;D项,B为环戊烯,含碳碳双键,环戊二烯也
含碳碳双键,二者均能使KMnO 溶液褪色,所以酸性KMnO 溶液褪色不能证明环戊烷已完
4 4
全转化为环戊二烯。]
8.D [根据题意,要得到2-丙醇,则必须有CHCH(OMgX)CH 生成,必须有CHCHO和
3 3 3
CHMgX,分析选项中物质,则反应物为CHCHO和CHCl,答案选D。]
3 3 39 .
CH==CHCH OH―――→CHCHClCH OH―――→CHCHClCOOH―――→CH==CHCOONa――→CH=
2 2 3 2 3 2 2
=CHCOOH;选择合适的反应条件、要注意官能团的保护
10. ――→
―――――――――――→ ―――→ ――→
解析 由A+B―→C的原理是B中两酯基之间的碳原子取代A中的溴原子,构成四元环,
因而应先将 转化成卤代烃,之后完全类比C→D→E的变化即可。
11. ―――――→ ――――→
――――――――→
12. ―――――→ ――――→ ―――→
――――――→
13. ――――→ ――――→ ――→
14.(1) 浓硫酸、加热
(2)邻苯二甲醛(或1,2-苯二甲醛) 醚键
(3)氧化反应 取代反应(4)
(5)12
(6)
解析 由有机物的转化关系可知, 与酸性高锰酸钾溶液发生氧化反应生成 B(
);在浓硫酸作用下,B与甲醇共热发生酯化反应生成C( );
C与LiAlH 发生还原反应生成D( );在铜作催化剂条件下,D与氧气共热发
4
生催化氧化反应生成H( ),H与过氧化氢反应生成I( );I与甲醇发生
取代反应生成J;E与KCN发生取代反应后,酸化得到F,在催化剂作用下,F与D共热发
生缩聚反应生成 。(5)C的结构简式为 ,由C
的同分异构体M符合的条件可知,M的取代基可能为2个—CHCOOH或—COOH、—
2
CHCHCOOH或—COOH、—CH(CH )COOH或—CH 、—CH(COOH) ,每组取代基在苯
2 2 3 3 2
环上都有邻、间、对3种位置关系,则符合条件的同分异构体共有3×4=12种。
第 70 练 有机合成与推断综合突破
1.(1)对 (2)羧基(3)2 +O――→2 +2HO
2 2
(4)3 (5)取代反应
(6)
解析 (2)有机物C在酸性条件下发生水解,其含有的酯基发生水解生成羟基和羧基。(4)F
的同分异构体中不含有N—H,说明结构中含有 结构,又因红外光谱中显示有酚
羟基,说明结构中含有苯环和羟基,固定羟基的位置, 有邻、间、对三种情况,
故有3种同分异构体。(6)利用逆合成法分析,有机物N可以与NaBH 反应生成最终产物,
4
类似于题中有机物G与NaBH 反应生成有机物H,故有机物N的结构简式为 ,
4
有机物M可以发生已知条件②所给的反应生成有机物N,说明有机物M中含有C==O,结
合反应原料中含有羟基,说明原料发生反应生成有机物 M的反应是羟基的催化氧化,有机
物M的结构简式为 。
2 . (1)2,6- 二 氯 甲 苯 + 2KF― ― ― → + 2KCl 酰 胺 基
(2)2 ②④ 33.(1) (2)消去反应 加成反应
(3)醚键 碳碳双键 (4)
(5)③>①>② (6)4
(7) ――→ ――→
解析 (4)根据上述反应流程分析, 与呋喃反应生成 ,
继续与HCl反应生成有机物J( )。(5)-CH 是推
3
电子基团,使磺酸基团酸性减弱,-CF 是吸电子基团,使磺酸基团酸性增强。(6)呋喃是一
3
种重要的化工原料,其同分异构体中可以发生银镜反应,说明其同分异构体中含有醛基,这
样的同分异构体共有4种,分别为CH—C≡C—CHO、CH≡C—CH—CHO、 、
3 2
。
4.(1)CH BrCOOH+CHCHOHCHBrCOOCH CH +HO (2)醛基 (3)①羰基为强
2 3 2 2 2 3 2
吸电子基团,使得相邻碳原子上的电子偏向羰基上的碳原子,使得相邻碳原子上的C—H键
极性增强 ②
(4)ac (5)
(6)解析 (2)D的结构简式为 ,含有的官能团为醛基。(3)②2-戊酮的羰基相邻的两个碳
原子上均有C—H,均可以断裂与苯甲醛的醛基发生加成反应,如图所示 ,1号碳原
子上的C—H断裂与苯甲醛的醛基加成得到E,3号碳原子上的C—H也可以断裂与苯甲醛的
醛基加成得到副产物 。(4)F的结构简式为 ,存在顺反异构体,
a项正确;J的结构简式为 ,K中含有酮羰基,J中不含有酮羰基,二者
不互为同系物,b项错误;J中与羟基直接相连的碳原子上无H原子,在加热和Cu催化条件
下,J不能被O 氧化,c项正确。
2
5.(1)丙烯 取代反应
(2)ClCH CHCHCl 羟基
2 2 2
(3) +CHOH +
3
HO
2
(4)15 、
、 、
、 (任写一种即可)
(5)CH ==CCH――→ ――――→ ―――→
2 3 2
―――→ ―――→
解析 (2)根据 E 的结构简式、C→D→E 的反应条件、C 的分子式,可知 D 为
HOCH CHCHOH、C为ClCH CHCHCl。D中官能团的名称为羟基。
2 2 2 2 2 2
(4)I的同分异构体与I具有相同的官能团,则有碳碳双键、羧基、碳氯键,苯环上有两个取代基,可以为—Cl和—CCl==CHCOOH、—Cl和—CH==CClCOOH、—Cl和 、
—COOH和—CCl==CHCl、—COOH和—CH==CCl ,共5种情况,两个不同取代基在苯环
2
上有邻、间、对3种位置关系,则共有15种满足条件的同分异构体。核磁共振氢谱有4组
峰 , 则 有 4 种 不 同 化 学 环 境 的 H 原 子 , 符 合 条 件 的 同 分 异 构 体 为
、 、
、 、
。
第十六章 化学实验综合应用
第 71 练 简单实验方案的设计与评价
1.D [FeCl 溶液中加入Zn片,Fe2++Zn===Fe+Zn2+,溶液由浅绿色变为无色,Fe2+的氧
2
化能力比Zn2+强,A错误;溶液变成红色的原因为Fe3++3SCN-Fe(SCN) ,与SO和K+
3
无关,B错误;Fe3+可能先与单质铁反应生成Fe2+,则溶液呈浅绿色,C错误;向沸水中逐
滴滴加饱和氯化铁溶液,制取Fe(OH) 胶体,继续加热则胶体因聚沉变为沉淀,D正确。]
3
2.C [若Fe2+被氧化为Fe3+,Fe3+能与SCN-生成Fe(SCN) ,溶液变成红色,能达到实验
3
目的,故A不符合题意;实验室用浓盐酸和二氧化锰加热制氯气,先用饱和食盐水除去混
有的氯化氢,再通过盛有浓硫酸的洗气瓶干燥,能达到实验目的,故 B不符合题意;用pH
试纸测定NaOH溶液的pH,不能润湿pH试纸,否则会因浓度减小而影响测定结果,不能
达到实验目的,故C符合题意;制取无水乙醇时,通常把工业酒精和新制的生石灰混合,
加热蒸馏,能达到实验目的,故D不符合题意。]
3.D [根据实验操作和现象,说明反应产生I ,发生反应:2KI+Cl===2KCl+I ,证明氧
2 2 2
化性:Cl>I ,Br >I ,但不能比较Br 与Cl 的氧化性强弱,A错误;玻璃中含有Na元素,
2 2 2 2 2 2
因此灼烧时火焰呈黄色,不能证明溶液中含Na元素,B错误;应该采用对照方法进行实验,
但两种溶液的浓度未知,盐的种类也不同,因此不能通过测定溶液的pH来判断HCO 、
2 3
CHCOOH的酸性强弱,C错误;氧气有助燃性,木条复燃,可以证明NaO 与水反应产生
3 2 2了O,D正确。]
2
4.A [亚铁离子被硝酸氧化为铁离子,铁离子能使KSCN溶液变红色,若溶液变红,说明
菠菜中含有铁元素,故A符合题意;溶液中氯酸根离子不能和银离子反应生成氯化银沉淀,
故B不符合题意;碘单质能使淀粉溶液变蓝色,溶液颜色不变,说明该食盐不含碘单质,
不能说明不含碘元素,故C不符合题意;某些蛋白质遇浓硝酸变黄色,一段时间后鸡皮变
黄,说明鸡皮中含有蛋白质,故D不符合题意。]
5.C [观察钾元素的焰色需要透过蓝色钴玻璃,故A不符合题意;硫酸铜溶液可吸收硫化
氢而不吸收乙炔,从而能达到除杂的目的,故C符合题意;容量瓶不能直接溶解物质,故D
不符合题意。]
6.A [向盛有少量酸性KCr O 溶液的试管中滴加足量乙醇,充分振荡,若溶液由橙色变
2 2 7
为绿色,说明KCr O 被还原为Cr3+,则乙醇表现还原性,故A符合题意;焰色试验只能确
2 2 7
定金属元素是否存在,不能确定具体物质,故B不符合题意;锌比铁活泼,形成原电池时
Zn作负极,Fe作正极,铁钉不被腐蚀,故D不符合题意。]
7.C [铝片表面形成致密氧化膜后,与铜离子不反应,故A正确;CCl 层无色,说明氯气
4
未与溴离子反应,而是与亚铁离子反应,故B正确;产生的气体使带火星的木条复燃,可
能是铁离子的催化作用使双氧水分解,故C错误。]
8.B [硫酸铵溶液能使蛋白质发生盐析而不是变性,A错误;亚硫酸根离子和酸反应会生
成使品红褪色的二氧化硫气体,故该溶液中可能含有 SO,B正确;高锰酸钾发生还原反应
为氧化剂,过氧化氢发生氧化反应体现还原性,D错误。]
9.B [乙酸乙酯和乙醇互溶,不能采取分液的方法分离,A错误;加入稀盐酸,产生无色
无味且能使澄清石灰水变浑浊的气体,不能说明溶液中一定含有CO,也可能含有HCO,C
错误;将混有HCl的Cl 通过饱和食盐水,可以除去HCl,但是Cl 中还会混有水蒸气,得
2 2
不到纯净的Cl,D错误。]
2
10.A [反应中碘离子过量,充分反应后滴入5滴15% KSCN溶液,若溶液变红色,说明
KI与FeCl 的反应存在限度,故A符合题意;不能向浓硫酸中加水,会产生危险,应将反应
3
后的溶液加入水中,故B不符合题意;浓硝酸受热也会分解产生二氧化氮气体,故 C不符
合题意;浓硫酸溶解放出大量的热,应先加入乙醇,再沿器壁慢慢加入浓硫酸、乙酸,故D
不符合题意。]
11.B [向NaSO 溶液中滴加稀盐酸发生的反应为NaSO +2HCl===2NaCl+HO+S↓+
2 2 3 2 2 3 2
SO ↑,可观察到溶液变浑浊且有气体生成,但生成的气体是SO ,故A错误;饱和食盐水
2 2
中含有较多的 Na+,通入氨气至饱和后,再通入二氧化碳后产生较多的 HCO,析出
NaHCO 晶体,故B正确;加热无水乙醇和浓HSO 的混合液至170 ℃,产生的乙烯气体中
3 2 4
含有挥发出的乙醇,而乙烯、乙醇都能使酸性KMnO 溶液褪色,因此酸性KMnO 溶液褪色
4 4不能说明乙醇发生了消去反应,故C错误。]
12.B [“84”消毒液的有效成分是次氯酸钠,具有漂白性,能使pH试纸褪色,所以不能
用pH试纸测定“84”消毒液的pH,应该用pH计,故A不符合题意;加入稀硫酸后,溶液
中含有氢离子和硝酸根离子,相当于含有硝酸,硝酸能将亚铁离子氧化为铁离子,故C不
符合题意;盐酸为无氧酸,由碳酸、盐酸的酸性强弱不能比较C、Cl的非金属性强弱,故D
不符合题意。]
第 72 练 以物质制备为主的综合实验
1.(1)圆底烧瓶 b (2)干燥气体 (3)暴沸 (4)防止温度过高生成焦磷酸 (5)磷酸晶种
(6)B (7)磷酸可与水分子间形成氢键
解析 (1)由仪器构造可知,仪器A为圆底烧瓶,仪器B为直形冷凝管,冷凝水应从b口进、
a口出,形成逆流冷却,使冷却效果更好。(2)纯磷酸制备过程中要严格控制温度和水分,因
此五氧化二磷的作用为干燥气体。(5)过饱和溶液暂时处于亚稳态,当加入一些固体的晶体
或晃动时可使此状态失去平衡,过多的溶质就会结晶,因此可向磷酸的过饱和溶液中加入磷
酸晶种促进其结晶。(6)纯化过程中,温度低于21 ℃易形成2HPO ·H O(熔点为30 ℃),高
3 4 2
于100 ℃则发生分子间脱水生成焦磷酸,纯磷酸的熔点为42 ℃,因此过滤磷酸晶体时,除
了需要干燥的环境外,还需要控制温度为 30~42 ℃。(7)磷酸的结构式为 ,
分子中含羟基,可与水分子间形成氢键,因此磷酸中少量的水极难除去。
2.(1)A B (2)作催化剂 (3)③①③② 防止2-氯丁烷水解,减少2-氯丁烷挥发 (4)蒸馏
(5)80%
解析 (1)A为球形冷凝管,一般竖直放置,用于冷凝回流;B为直形冷凝管,倾斜放置,用
于 冷 凝 馏 分 。 (2) 甲 装 置 中 圆 底 烧 瓶 中 发 生 的 反 应 是 CHCHOHCH CH +
3 2 3
HCl―→CHCHClCH CH +HO,步骤1中加入的无水ZnCl 不作反应物,故其作催化剂,
3 2 3 2 2
加快化学反应速率。(3)步骤3进行系列操作的顺序是用蒸馏水洗去产品中含有的HCl、
ZnCl―→用10%Na CO 溶液洗去少量的HCl―→用蒸馏水洗去少量的NaCO―→用CaCl
2 2 3 2 3 2
固体干燥产品,放置一段时间后过滤;因为2-氯丁烷在碱性溶液中水解,为了防止2-氯丁
烷水解,同时减少2-氯丁烷(沸点较低)挥发,故用NaCO 溶液洗涤时操作要迅速。(4)蒸馏
2 3
可分离互溶的、有一定沸点差异的液体混合物,故步骤4进一步精制得产品所采用的操作方
法是蒸馏。(5)45.68 mL 2-丁醇的物质的量为≈0.50 mol,则理论上可得到0.50 mol 2-氯丁烷;
由 2-氯丁烷在测定实验中的反应可得关系式为 CHCHClCH CH ~NaCl~AgCl,
3 2 3n(CHCHClCH CH)=n(AgCl)==0.40 mol,则2-氯丁烷的产率是×100%=80%。
3 2 3
3.(1)c (2)吡咯中含有—NH—,可以形成分子间氢键 (3)
(4)将环氧乙烷溶液沿烧杯壁缓缓加入,并不断用玻璃棒搅拌 (5)与水解生成的OH-反应,
使水解更彻底 (6)球形冷凝管和分液漏斗 除去水 (7)70.0%
解析 (1)步骤 Ⅰ 制钠砂过程中,液体A不能和Na反应,而乙醇、水和液氨都能和金属
Na反应,故选c。(5)2-噻吩乙醇钠水解生成2-噻吩乙醇的过程中有NaOH生成,用盐酸调
节pH的目的是将NaOH中和,使平衡正向移动,增大反应物的转化率。(6)步骤Ⅴ中的操作
有过滤、蒸馏,蒸馏的过程中需要直形冷凝管、温度计、牛角管等,无需使用的是球形冷凝
管和分液漏斗。(7)步骤Ⅰ中向烧瓶中加入300 mL液体A和4.60 g金属钠,Na的物质的量
为=0.2 mol,步骤Ⅱ中Na完全反应,根据方程式可知,理论上可以生成0.2 mol 2-噻吩乙
醇,产品的产率为×100%=70.0%。
4.(1)检查装置的气密性 (2)MnO +4H++2Cl-=====Mn2++Cl↑+2HO (3)D (4)防止
2 2 2
PCl 与空气中的氧气和水蒸气反应 关闭 K 、打开K ,打开分液漏斗的旋塞和活塞,当看
3 2 3
到 B 装置中液面上方充满黄绿色气体时,打开 K 、关闭 K (5)3PCl +2P=====5PCl
2 3 5 3
(6)PCl +3HO===HPO +3HCl (7)碱式滴定管
3 2 3 3
(8)×100%
解析 (3)装置B的作用是除去氯气中混有的水蒸气,所以 B中所装试剂为浓硫酸,故选
D。(4)由题给信息知,PCl 易水解、易被空气中氧气氧化,所以实验开始前,打开K 通入
3 1
一段时间氮气来除去装置中的空气,防止PCl 与空气中的氧气和水蒸气反应;除去装置
3
A、B中空气,应通入Cl ,具体方法是关闭K 、打开K ,打开分液漏斗的旋塞和活塞,当
2 2 3
看到 B 装置中液面上方充满黄绿色气体时,打开 K 、关闭 K 。(7)H SO 是弱酸,则
2 3 2 2 3
NaSO 溶液呈碱性,使用的仪器是碱式滴定管。(8)依据反应,可建立关系式:PCl ~HPO
2 2 3 3 3 3
~I ~2NaSO ,则与HPO 反应的I 的物质的量为(cV -cV)×10-3mol,该产品中PCl 的
2 2 2 3 3 3 2 1 1 2 2 3
质量分数为×100%=×100%。
第 73 练 以物质含量或组成测定为主的综合实验
1.(1)d a b f (2) (3)固体由白色变为蓝色 由蓝色变为红色 (4)BaSO 、BaSO 否
4 3
铁元素的化合价升高,则必有硫元素的化合价降低,根据原子守恒和得失电子守恒可知,只
有一部分硫元素的化合价降低,则进入D中的气体为SO 和SO (5)FeSO ·4H O
3 2 4 2
解析 (1)测定晶体中结晶水含量时,需先排尽装置内的空气,再加热,依据固体颜色改变
确定结晶水全部失去后,停止加热、冷却称量,则实验操作步骤正确排序为
d→a→b→f→c→e。(2)根据实验记录,绿矾晶体的质量为(m -m)g,结晶水的质量为(m -
2 1 2m)g,硫酸亚铁的质量为(m -m)g,则绿矾化学式中结晶水数目x=。(3)在实验过程中,无
3 3 1
水硫酸铜吸收水,生成硫酸铜晶体,观察到B中的现象:固体由白色变为蓝色;SO 、SO
3 2
都是酸性气体,则C中试纸的颜色变化是由蓝色变为红色。(4)SO 、SO 都能与Ba(OH) 溶
3 2 2
液反应,则D中有白色沉淀生成,该沉淀的化学式为 BaSO 、BaSO 。(5)n(FeSO ·7H O)=
4 3 4 2
=0.03 mol,m(FeSO )=0.03 mol×152 g·mol-1=4.56 g,则在100 ℃时,FeSO ·7H O 只失
4 4 2
去部分结晶水,此时M的摩尔质量为=224 g·mol-1,设化学式为FeSO ·xHO,则152+18x
4 2
=224,x=4,M的化学式为FeSO ·4H O。
4 2
2.(1)Mg N+6HO===3Mg(OH) ↓+2NH ↑ 饱和食盐水可减缓生成氨气的速率
3 2 2 2 3
(2)三颈烧瓶
(3)分液漏斗的活塞与旋塞 沉淀恰好完全溶解时
(4)①打开K ,缓慢推动可滑动隔板,将气体全部推出,再关闭K 减小气体的通入速率,
2 2
使空气中的甲醛气体被完全吸收 ②0.037 5
解析 在仪器A中MgN 与HO反应产生Mg(OH) 和NH ,NH 通入AgNO 溶液中首先产
3 2 2 2 3 3 3
生AgOH白色沉淀,当氨气过量时,反应产生[Ag(NH)]OH,然后向溶液中通入甲醛,水
3 2
浴加热,发生银镜反应产生单质Ag和CO 气体,产生的Ag与加入的Fe3+定量反应生成Fe2
2
+,Fe2+与菲洛嗪形成有色物质,在562 nm处测定吸光度,测得生成1.12 mg Fe2+,据此结
合反应过程中电子守恒,可计算室内空气中甲醛的含量。
(4)②甲醛和银氨溶液加热反应生成银,银具有还原性,被Fe3+氧化,结合甲醛被氧化为
CO ,[Ag(NH)]OH被还原为银,甲醛中碳元素化合价由0价升高为+4价,银由+1价降
2 3 2
低为0价,生成的银又被铁离子氧化,铁离子被还原为亚铁离子,生成亚铁离子 1.12 mg,
则n(Fe)==2×10-5 mol,设消耗甲醛的物质的量为x,则4x=2×10-5 mol,x=5×10
-6 mol,因实验进行了4次操作,所以测得1 L空气中甲醛的含量为1.25×10-6 mol,空气
中甲醛的含量为=0.037 5 mg·L-1。
3.(1)不再有气泡产生时 (2)将甲装置中产生的CO 和水蒸气全部赶入乙、丙装置中
2
(3)D 活塞K前(或甲装置前)
(4)Co (OH) (CO) (5)饱和碳酸氢钠溶液会降低CO 的溶解度 将b向a倾斜,使稀硫酸流
3 4 3 2 2
入a中 不同 恢复至室温 C
解析 (4)n(H O)==0.02 mol,n(CO)==0.02 mol,由C元素守恒知,该样品物质的量为
2 2
0.01 mol,H元素物质的量为 0.04 mol,则 y为4,Co 元素质量为 3.65 g-0.04 mol×17
g·mol-1-0.02 mol×60 g·mol-1=1.77 g,Co的物质的量为0.03 mol,故碱式碳酸钴的化学式
为Co (OH) (CO) 。(5)实验 Ⅰ 中应该让样品完全反应,所以引发反应时应该将稀硫酸向样
3 4 3 2
品中倾斜;而实验 Ⅱ 中应该让稀硫酸完全反应,所以引发反应时应该将锌粒向稀硫酸中倾
斜。
4.(1)向上层清液中(或取上层清液少许于试管中)继续滴加BaCl 溶液,无白色沉淀生成,则
2SO已沉淀完全
(2)AgNO 溶液 (3)坩埚 (4) (5)偏低
3
(6)检查装置气密性 (7)b
(8) (9)偏高 (10)否
解析 (2)BaSO 沉淀表面附着的离子是Cu2+、Ba2+和Cl-,可向洗涤液中加入AgNO 溶液,
4 3
若没有沉淀生成,则证明BaSO 沉淀已洗净。
4
(3)步骤③灼烧的是BaSO 固体,灼烧固体选择的仪器是坩埚。
4
(4)BaSO 的质量为 w g,BaSO 的物质的量为 mol,由化学方程式:CuSO +
4 4 4
BaCl ===BaSO↓+CuCl 可知,CuSO 的物质的量等于BaSO 的物质的量,所以CuSO 溶液
2 4 2 4 4 4
的浓度为c(CuSO )== mol·L-1。
4
(5)若步骤①中,转移沉淀时未洗涤烧杯,会造成BaSO 沉淀的质量减少,所以使测得的
4
c(CuSO )偏低。
4
(7)步骤⑥中保证体系恢复到室温的原因是气体密度受温度影响较大,温度过高或过低都会
造成气体密度的改变。
(8)Zn粉的物质的量为 mol,反应产生H 的物质的量为= mol,由Zn+HSO ===ZnSO +
2 2 4 4
H↑知,与HSO 反应的Zn的物质的量等于产生H 的物质的量,为 mol,与CuSO 反应消
2 2 4 2 4
耗的Zn的物质的量为(-) mol,由化学方程式Zn+CuSO ===ZnSO +Cu可知,与CuSO
4 4 4
反应消耗的Zn的物质的量等于CuSO 的物质的量,所以c(CuSO )= mol·L-1。
4 4
(9)若步骤⑥E管液面高于D管,则D管内气体压强高于外界大气压,造成气体体积 b的数
值偏小,由c(CuSO )= mol·L-1可知,c(CuSO )会偏高。
4 4
(10)因为Zn和MgSO 溶液不反应,所以不能用同样的装置和方法测定MgSO 溶液的浓度。
4 4
第 74 练 以性质为主的探究类综合实验
1.(1)烧杯、量筒、托盘天平 (2)KCl
(3)石墨 (4)0.09 mol·L-1
(5)Fe3++e-===Fe2+ Fe-2e-===Fe2+ Fe3+ Fe
(6)取活化后溶液少许于试管中,加入KSCN溶液,若溶液不出现红色,说明活化反应完成
解析 (2)盐桥中阴、阳离子不与溶液中的物质发生化学反应,两烧杯溶液中含有 Fe2+、Fe3
+和SO,Ca2+与SO生成微溶于水的CaSO ,Fe2+、Fe3+均与HCO反应,酸性条件下NO与
4
Fe2+发生反应,故盐桥中不能含有Ca2+、HCO和NO。K+和Cl-的电迁移率(u∞)相差较小,
故盐桥中应选择KCl作为电解质。(4)假设两个烧杯中溶液体积均为V L,铁电极反应式为
Fe-2e-===Fe2+,一段时间后,铁电极溶液中c(Fe2+)增加了0.02 mol·L-1,则电路中通过的
电子为0.02 mol·L-1×V L×2=0.04V mol。石墨电极上未见Fe析出,则石墨电极反应式为Fe3++e-===Fe2+,据得失电子守恒可知,石墨电极生成的Fe2+为0.04V mol,故石墨电极
溶液中c(Fe2+)==0.09 mol·L-1。(6)铁电极表面发生活化反应:Fe+Fe (SO )===3FeSO ,
2 4 3 4
活化反应完成后,溶液中不含Fe3+。
2.(1)Cl MnO +2e-+4H+===2HO+Mn2+ (2)①10 20 ②φ<φ ③NaCl 又产生黄
2 2 2 1 3
绿色气体
解析 (2)①分析表格数据,实验1为对比实验,而实验3改变了MnSO 溶液的体积,实验
4
1和实验3组合研究Mn2+浓度对电极电势的影响。那么实验2和实验1组合可以研究H+浓
度的影响,所以改变HSO 溶液的体积而不改变MnSO 溶液的体积,同时保证总体积为40
2 4 4
mL,则 m=10、n=20。②随着 Mn2+浓度增大 MnO 氧化性减弱,电极电势降低,即
2
φ<φ 。③已知溶液中c(H+)减小、c(Mn2+)增大,MnO 氧化性减弱,保证单一变量,只改变
1 3 2
Cl-的量,可加入NaCl固体,若加热又产生黄绿色气体,说明Cl-的浓度增大其还原性增强。
3.(1)KMnO (2)①KOH < ②2 3 16OH- 2 6 8HO ③反应存在平衡16OH-+
4 2
2Fe3++3Cl2FeO+6Cl-+8HO,当为FeCl 时增加了Cl-浓度,使平衡逆向移动,产率
2 2 3
降低 (3)①吸入的HCl增加了Cl-浓度,使NaCl(s)Na+(aq)+Cl-(aq)平衡逆向移动,产
生NaCl晶体 ②HCl与KOH反应,溶液碱性减弱,+3价铁的还原性减弱,产率降低
(4)2OH-+Cl===Cl-+ClO-+HO (5)Fe(NO ) 溶液和过量KOH、适量Cl
2 2 3 3 2
解析 (2)①本实验探究碱性较强会增强Fe3+的还原性,只需改变Fe3+溶液的碱性即可,即
向右池中加入KOH,观察到电压增大。②Fe3+被Cl 氧化为FeO,而Cl 变为Cl-,按化合
2 2
价升降守恒配平,由于碱性环境需要加入OH-,该反应为16OH-+2Fe3++3Cl2FeO+
2
6Cl-+8HO。③对比两个实验的变量,结合平衡 16OH-+2Fe3++3Cl2FeO+6Cl-+
2 2
8HO分析,Cl-增加使平衡逆向移动,所以实验ⅱ产率较低。
2
(5)过量的Cl 和Cl-均会降低产率,而KOH会增加产率,所以所需的适宜条件是Fe(NO ) 溶
2 3 3
液和过量KOH、适量Cl。
2
4.(1)将湿润的红色石蕊试纸放在试管口,试纸变蓝
(2)Cl- Mg(OH)Cl
(3)NH+HONH ·H O+H+
2 3 2
(4)①5 mL 1.0 mol·L-1 CHCOONH 溶液 ②两试管反应剧烈程度相当
3 4
(5)取5 mL 无水乙醇,加入0.5 g Mg粉无明显变化
(6)NH Cl水解产生的H+对反应影响小,NH对反应影响大
4
解析 (2)向洗涤液中滴加AgNO 溶液后无明显浑浊,说明灰白色固体表面没有能使AgNO
3 3
溶液变浑浊的杂质,将洗涤后固体溶于稀HNO,再滴加AgNO 溶液,出现白色沉淀,说明
3 3
灰白色沉淀含有Cl-,结合已知灰白色沉淀中含有Mg2+、OH-和化合物中各元素化合价代
数和为0,可推测灰白色固体可能是Mg(OH)Cl。(4)①由题述(3)分析可知,NH Cl溶液因水
4
解呈酸性,故为了进行对照实验,必须找到一种含有相同阳离子即NH,且溶液显中性的试剂,由题干信息可知,试剂X是5 mL 1.0 mol·L-1 CHCOONH 溶液。②乙同学通过实验3
3 4
来证明甲同学的说法是不合理的,故由实验3获取的证据为两试管反应剧烈程度相当。 (5)
依据题述实验,可以得出Mg能与NH反应生成H,乙同学认为该方案不严谨,故需要补充
2
对照实验,在无NH的情况下是否也能与Mg反应放出H ,故实验方案为取5 mL无水乙醇,
2
加入0.5 g Mg粉无明显变化。