文档内容
专练 24 元素周期律及其应用
1.[2022·全国甲卷]Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电
子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子
内层电子数的2倍。下列说法正确的是( )
A.非金属性:X>Q
B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q
D.最高价含氧酸的酸性:Z>Y
2.[2021·浙江卷1月]现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,
其中Z、Q在同一周期。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为0
Z 单质为淡黄色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是 ( )
A.常温时,X单质能与水发生剧烈反应
B.Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C.Y、Z、Q的最高价氧化物对应水化物的酸性依次减弱
D.第五周期且与Q同主族元素的单质在常温常压下呈液态
3.[2021·广东卷]一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;
元素Y、Z、W原子序数依次增大,且均位于 X的下一周期;元素E的原子比W原子多8
个电子。下列说法不正确的是( )
A.XEZ 是一种强酸
4
B.非金属性:W>Z>Y
C.原子半径:Y>W>E
D.ZW 中,Z的化合价为+2价
2
4.[2021·福建卷]某种食品膨松剂由原子序数依次增大的R、W、X、Y、Z五种主族元
素组成。五种元素分处三个短周期,X、Z同主族,R、W、X的原子序数之和与Z的原子
序数相等,Y原子的最外层电子数是Z原子的一半。下列说法正确的是( )
A.简单氢化物的稳定性:W>X>Z
B.Y的氧化物是两性氧化物
C.R、W、X只能组成共价化合物
D.最高正价:YH SO >H SiO
4 2 3 2 3
B.碱性:KOH>NaOH>LiOH
C.热稳定性:HO>HS>PH
2 2 3D.非金属性:F>O>N
6.[2022·浙江卷1月]W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y
同族,Y的原子序数是W的2倍,X是地壳中含量最多的金属元素。下列说法正确的是(
)
A.非金属性:Y>W
B.XZ 是离子化合物
3
C.Y、Z的氧化物对应的水化物均为强酸
D.X与Y可形成化合物XY
2 3
7.[2021·全国甲卷]W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层
电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常
温下均为气体。下列叙述正确的是( )
A.原子半径:Z>Y>X>W
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
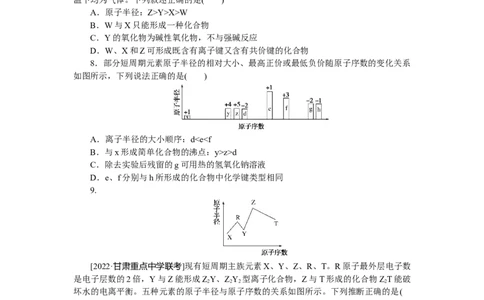
8.部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系
如图所示,下列说法正确的是( )
A.离子半径的大小顺序:dz>d
C.除去实验后残留的g可用热的氢氧化钠溶液
D.e、f分别与h所形成的化合物中化学键类型相同
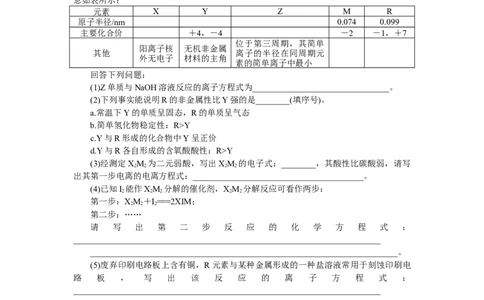
9.
[2022·甘肃重点中学联考]现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数
是电子层数的2倍,Y与Z能形成ZY、ZY 型离子化合物,Z与T形成的化合物ZT能破
2 2 2 2
坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是(
)
A.最简单氢化物的沸点排序:Y>T>R
B.原子半径和离子半径均满足:YR>T
10.[综合创新]短周期元素W、X、Y、Z、Q的原子序数依次增大,c、d、e、f、h是
由这些元素组成的二元化合物,自然界中硬度最大的单质和 a都由X组成,b由W、Y、Q
三种元素组成,d能使品红溶液褪色,e是液体,上述物质的转化关系如图所示(个别产物
略去)。下列说法错误的是( )A.二元化合物沸点:e>d>c
B.简单氢化物的热稳定性:Q>Y>X
C.元素的非金属性:Y>X>W
D.原子半径的大小:Z>Q>Y
11.[2022·安徽江淮十校月考]有X、Y、Z、M、R五种短周期主族元素,部分相关信
息如表所示:
元素 X Y Z M R
原子半径/nm 0.074 0.099
主要化合价 +4,-4 -2 -1,+7
位于第三周期,其简单
阳离子核 无机非金属
其他 离子的半径在同周期元
外无电子 材料的主角
素的简单离子中最小
回答下列问题:
(1)Z单质与NaOH溶液反应的离子方程式为________________________________。
(2)下列事实能说明R的非金属性比Y强的是________(填序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.简单氢化物稳定性:R>Y
c.Y与R形成的化合物中Y呈正价
d.Y与R各自形成的含氧酸酸性:R>Y
(3)经测定XM 为二元弱酸,写出XM 的电子式:________,其酸性比碳酸弱,请写
2 2 2 2
出其第一步电离的电离方程式:________________________________________。
(4)已知I 能作XM 分解的催化剂,XM 分解反应可看作两步:
2 2 2 2 2
第一步:XM+I===2XIM;
2 2 2
第二步:……
请 写 出 第 二 步 反 应 的 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
(5)废弃印刷电路板上含有铜,R元素与某种金属形成的一种盐溶液常用于刻蚀印刷电
路 板 , 写 出 该 反 应 的 离 子 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
12.位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、
D同主族,D、E同周期。A、B、C在周期表中相邻,且三种元素的原子最外层电子数之
和为 18。F是其所在周期中最活泼的金属元素。根据推断回答下列问题:
(1)A在周期表中的位置 ________;写出D与F形成的最简单离子化合物的电子式
________。
(2)用“>”或“<”填空:
离子半径 非金属性 酸性 沸点
D的最高价氧化物的
F+____D2- A____B 水化物____E 的最高 C的氢化物____E的氢化物
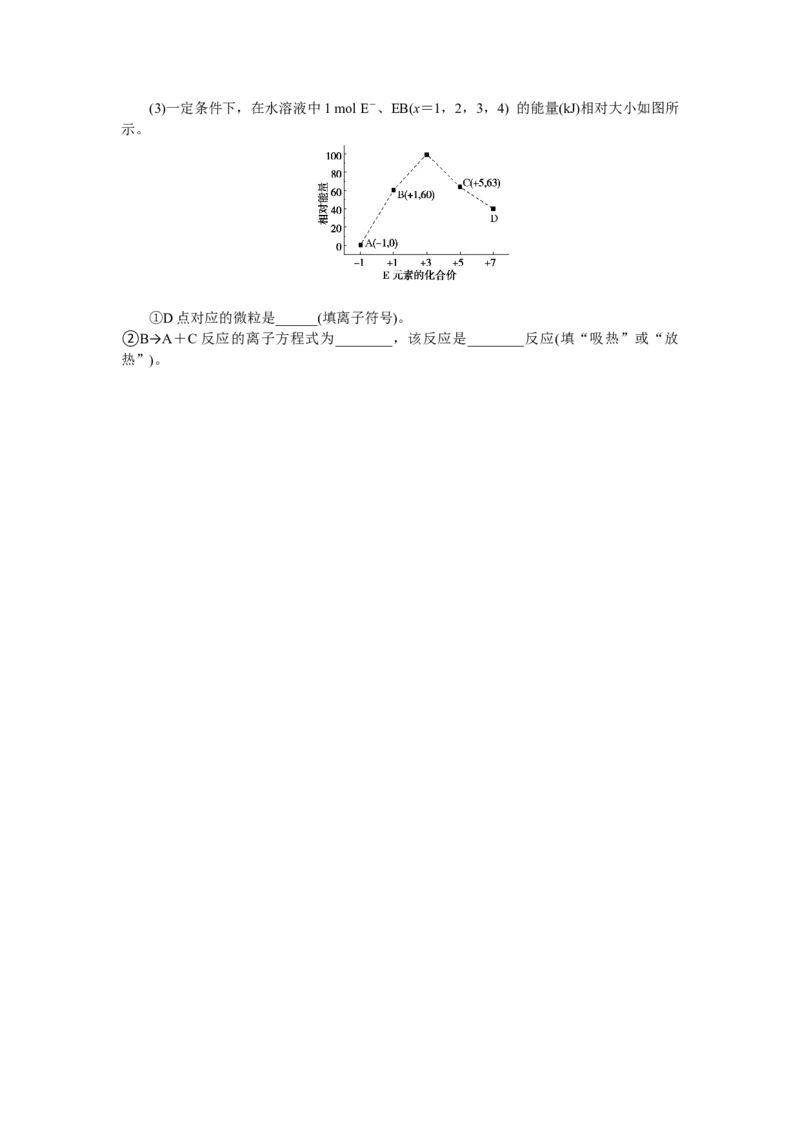
价氧化物的水化物(3)一定条件下,在水溶液中1 mol E-、EB(x=1,2,3,4) 的能量(kJ)相对大小如图所
示。
①D点对应的微粒是______(填离子符号)。
②B→A+C反应的离子方程式为________,该反应是________反应(填“吸热”或“放
热”)。