文档内容
专练 24 元素周期律及其应用
一、单项选择题
1.[2022·全国甲卷]Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电
子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子
内层电子数的2倍。下列说法正确的是( )
A.非金属性:X>Q
B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q
D.最高价含氧酸的酸性:Z>Y
2.[2021·浙江1月]现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中
Z、Q在同一周期。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为0
Z 单质为淡黄色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是 ( )
A.常温时,X单质能与水发生剧烈反应
B.Y与Q元素组成的YQ 分子,空间构型为正四面体
4
C.Y、Z、Q的最高价氧化物对应水化物的酸性依次减弱
D.第五周期且与Q同主族元素的单质在常温常压下呈液态
3.[2021·全国甲卷]W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层
电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常
温下均为气体。下列叙述正确的是( )
A.原子半径:Z>Y>X>W
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
4.[2021·北京卷]下列性质的比较,不能用元素周期律解释的是( )
A.酸性:HClO>HSO >HSiO
4 2 3 2 3
B.碱性:KOH>NaOH>LiOH
C.热稳定性:HO>HS>PH
2 2 3
D.非金属性:F>O>N
5.[2021·山东卷]X、Y为第三周期元素,Y最高正价与最低负价的代数和为6,二者形
成的一种化合物能以[XY ]+[XY ]-的形式存在,下列说法错误的是( )
4 6
A.原子半径:X>Y
B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强
D.同周期中第一电离能小于X的元素有4种
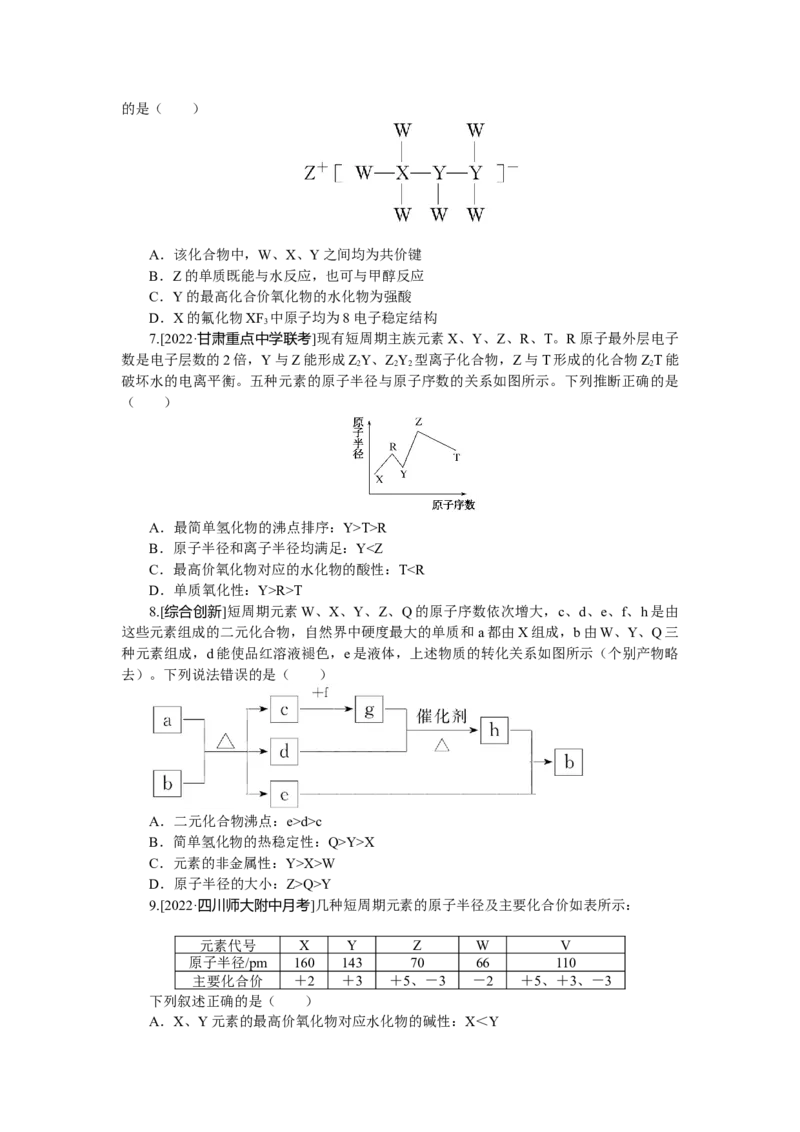
6.[2020·全国卷Ⅱ]一种由短周期主族元素组成的化合物(如图所示),具有良好的储
氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是( )
A.该化合物中,W、X、Y之间均为共价键
B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
7.[2022·甘肃重点中学联考]现有短周期主族元素X、Y、Z、R、T。R原子最外层电子
数是电子层数的2倍,Y与Z能形成ZY、ZY 型离子化合物,Z与T形成的化合物ZT能
2 2 2 2
破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
( )
A.最简单氢化物的沸点排序:Y>T>R
B.原子半径和离子半径均满足:YR>T
8.[综合创新]短周期元素W、X、Y、Z、Q的原子序数依次增大,c、d、e、f、h是由
这些元素组成的二元化合物,自然界中硬度最大的单质和a都由X组成,b由W、Y、Q三
种元素组成,d能使品红溶液褪色,e是液体,上述物质的转化关系如图所示(个别产物略
去)。下列说法错误的是( )
A.二元化合物沸点:e>d>c
B.简单氢化物的热稳定性:Q>Y>X
C.元素的非金属性:Y>X>W
D.原子半径的大小:Z>Q>Y
9.[2022·四川师大附中月考]几种短周期元素的原子半径及主要化合价如表所示:
元素代号 X Y Z W V
原子半径/pm 160 143 70 66 110
主要化合价 +2 +3 +5、-3 -2 +5、+3、-3
下列叙述正确的是( )
A.X、Y元素的最高价氧化物对应水化物的碱性:X<YB.简单离子半径:Z<W<X<Y
C.一定条件下,W的单质可以将Z的单质从其氢化物中置换出来
D.X与Z形成的化合物为共价化合物
二、不定项选择题
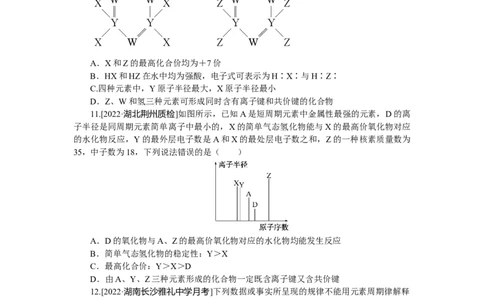
10.[2021·河北卷]如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中
W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价
电子数的3倍。下列说法正确的是( )
A.X和Z的最高化合价均为+7价
B.HX和HZ在水中均为强酸,电子式可表示为H∶X∶与H∶Z∶
C.四种元素中,Y原子半径最大,X原子半径最小
D.Z、W和氢三种元素可形成同时含有离子键和共价键的化合物
11.[2022·湖北荆州质检]如图所示,已知A是短周期元素中金属性最强的元素,D的离
子半径是同周期元素简单离子中最小的,X的简单气态氢化物能与X的最高价氧化物对应
的水化物反应,Y的最外层电子数是A和X的最处层电子数之和,Z的一种核素质量数为
35,中子数为18,下列说法错误的是( )
A.D的氧化物与A、Z的最高价氧化物对应的水化物均能发生反应
B.简单气态氢化物的稳定性:Y>X
C.最高化合价:Y>X>D
D.由A、Y、Z三种元素形成的化合物一定既含离子键又含共价键
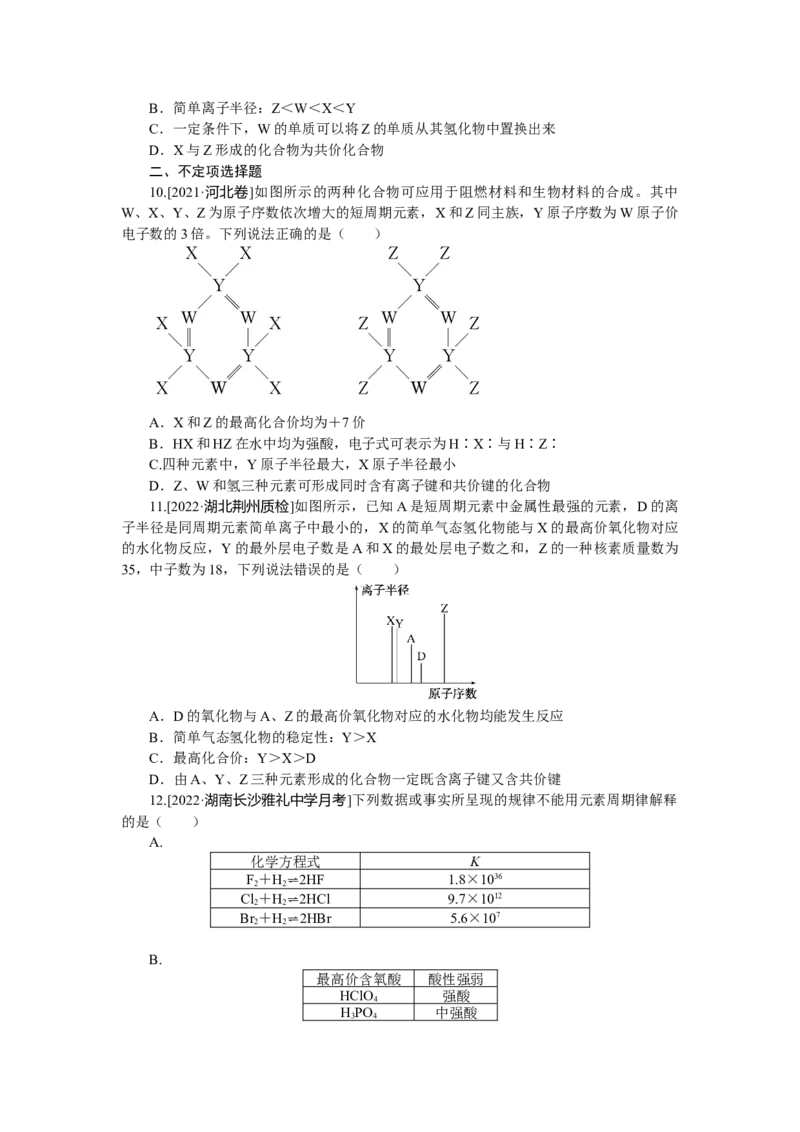
12.[2022·湖南长沙雅礼中学月考]下列数据或事实所呈现的规律不能用元素周期律解释
的是( )
A.
化学方程式 K
F
2
+H 2⇌2HF 1.8×1036
Cl
2
+H 2⇌2HCl 9.7×1012
Br
2
+H 2⇌2HBr 5.6×107
B.
最高价含氧酸 酸性强弱
HClO 强酸
4
HPO 中强酸
3 4HSiO 弱酸
2 3
C.
简单气态氢化物 分解温度/℃
HO >2 000
2
HS ≈300
2
HSe ≈160
2
D.
共价键 键能/(kJ·mol-1)
C—C 347
C===C 620
C≡C 812
13.[2022·河北武邑中学高三月考]W、X、Y、Z是原子半径依次增大的四种短周期主族
元素,已知25 ℃时,W、X形成的0.1 mol·L-1化合物的水溶液pH=1,Z的电子层数与最
外层电子数相等。下列说法错误的是( )
A.X、Y、Z一定位于同一周期
B.X与W形成的化合物中各原子都达到8电子稳定结构
C.Y、Z的最高价氧化物对应水化物之间一定能相互反应
D.W与X、Y形成的化合物的稳定性一定是前者大于后者
14.[2022·辽宁六校协作体上学期联考]X、Y、Z、W是短周期主族元素,X原子最外层
电子数是其内层电子数的3倍;Y的原子序数是其最外层电子数的6倍;Z的一种单质是自
然界中最硬的物质;自然界中,W的单质多出现在火山口附近,且为淡黄色晶体。下列叙
述正确的是( )
A.原子半径的大小:Y>Z>X
B.Z的氢化物的沸点一定比X 的低
C.W的最高价氧化物对应水化物的酸性在同主族中最强
D.Y的单质可通过铝热反应冶炼
15.[2022·河南南阳期中]短周期元素W、X、Y、Z的原子序数依次增大,浙江大学研
究团队以aYX·bZX (固态物质,a、b为系数)为载体,利用AuPb纳米颗粒催化气态单
2 3 2
质W、X 合成WX,其原理如图所示。下列说法错误的是( )
2 2 2 2
A.元素主要化合价(最高正价):Z>Y
B.地壳中元素含量:X>Z>Y
C.YX、ZX 均具有较高熔点
2 3 2
D.W与X形成的化合物只含极性键
三、非选择题
16.位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、D
同主族,D、E同周期。A、B、C在周期表中相邻,且三种元素的原子最外层电子数之和
为 18。F是其所在周期中最活泼的金属元素。根据推断回答下列问题:
(1)A在周期表中的位置 ;写出D与F形成的最简单离子化合物的电
子式 。
(2)用“>”或“<”填空:离子半径 非金属性 酸性 沸点
D的最高价氧化物的水化物
F+ D2- A B C的氢化物 E的氢化物
E的最高价氧化物的水化物
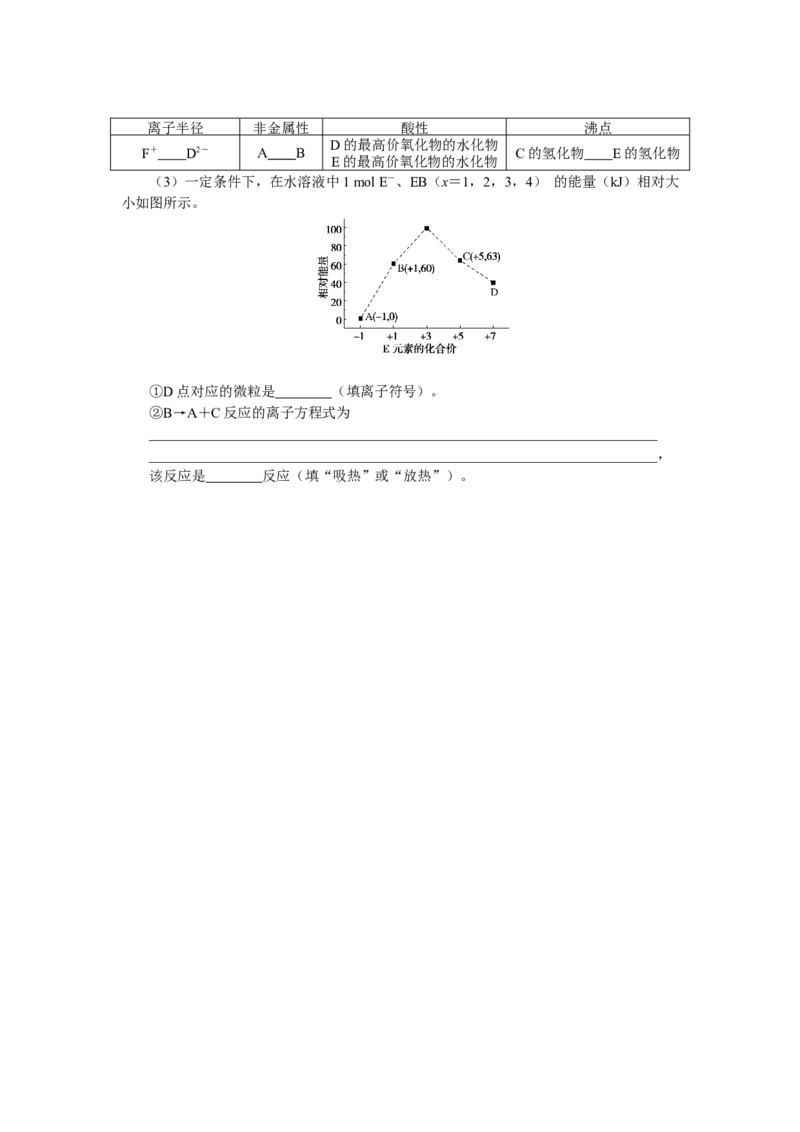
(3)一定条件下,在水溶液中1 mol E-、EB(x=1,2,3,4) 的能量(kJ)相对大
小如图所示。
①D点对应的微粒是 (填离子符号)。
②B→A+C反应的离子方程式为
________________________________________________________________________
________________________________________________________________________,
该反应是 反应(填“吸热”或“放热”)。