文档内容
专练 25 元素周期表及其应用
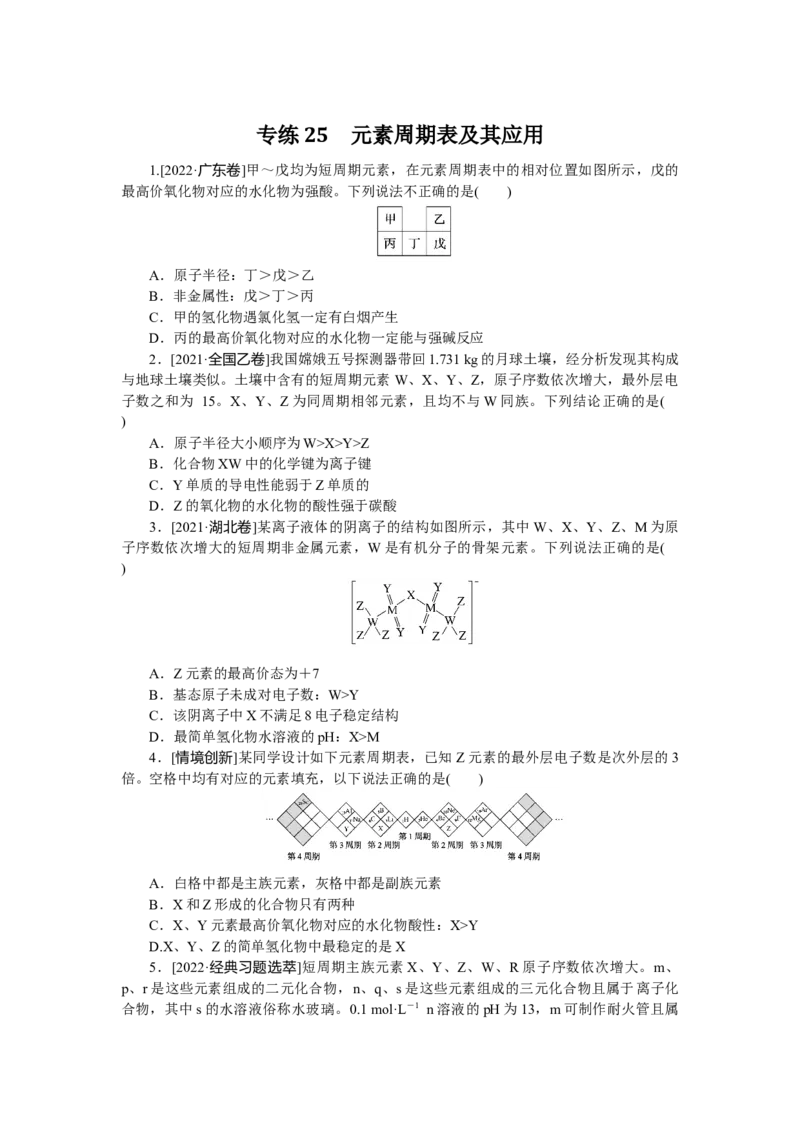
1.[2022·广东卷]甲~戊均为短周期元素,在元素周期表中的相对位置如图所示,戊的
最高价氧化物对应的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
2.[2021·全国乙卷]我国嫦娥五号探测器带回1.731 kg的月球土壤,经分析发现其构成
与地球土壤类似。土壤中含有的短周期元素 W、X、Y、Z,原子序数依次增大,最外层电
子数之和为 15。X、Y、Z为同周期相邻元素,且均不与W同族。下列结论正确的是(
)
A.原子半径大小顺序为W>X>Y>Z
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
3.[2021·湖北卷]某离子液体的阴离子的结构如图所示,其中 W、X、Y、Z、M为原
子序数依次增大的短周期非金属元素,W是有机分子的骨架元素。下列说法正确的是(
)
A.Z元素的最高价态为+7
B.基态原子未成对电子数:W>Y
C.该阴离子中X不满足8电子稳定结构
D.最简单氢化物水溶液的pH:X>M
4.[情境创新]某同学设计如下元素周期表,已知 Z元素的最外层电子数是次外层的3
倍。空格中均有对应的元素填充,以下说法正确的是( )
A.白格中都是主族元素,灰格中都是副族元素
B.X和Z形成的化合物只有两种
C.X、Y元素最高价氧化物对应的水化物酸性:X>Y
D.X、Y、Z的简单氢化物中最稳定的是X
5.[2022·经典习题选萃]短周期主族元素X、Y、Z、W、R原子序数依次增大。m、
p、r是这些元素组成的二元化合物,n、q、s是这些元素组成的三元化合物且属于离子化
合物,其中s的水溶液俗称水玻璃。0.1 mol·L-1 n溶液的pH为13,m可制作耐火管且属于两性物质。上述物质的转化关系如图所示。下列说法正确的是( )
A.简单气态氢化物的稳定性:R>Y
B.离子半径大小:Y>Z>W
C.W的最高价氧化物对应的水化物碱性比Z的强
D.单质的熔点:Z>R>X
6.[2022·安徽省江南片高三摸底考试]W、X、Y、Z均为短周期主族元素,原子序数
依次增加。W原子最外层电子数是其所在周期数的2倍;Y+和X2-的电子层结构相同;Z
的原子序数等于W和Y的核外电子数之和。下列说法正确的是( )
A.由化学键角度推断,能形成WXZ 这种共价化合物
2
B.离子半径大小:Z>Y>X
C.工业上用MnO 和Z的氢化物的浓溶液在加热的条件下制取Z的单质
2
D.Z的氢化物的水溶液酸性比WX 的水化物的酸性强,说明Z的非金属性比W的强
2
Y Z
X W
7.[2022·河南开封定位考试]W、X、Y、Z四种短周期元素,它们在元素周期表中的位
置如图所示,其中W元素的原子序数为Z元素原子序数的两倍,则下列说法正确的是(
)
A.X、Z、Y三种元素对应原子的半径依次减小
B.X位于元素周期表中的第三周期第ⅣA族
C.HYO 的酸性强于HWO,故W元素的非金属性弱于Y
3 2 3
D.X和Y可分别与Z形成XZ 和YZ,它们的结构和化学性质相似
2 2
8.[2022·河北邯郸开学考]已知X、Y、Z、M、N均为短周期主族元素。25 ℃时,各
元素最高价氧化物对应水化物的溶液(浓度均为0.01 mol·L-1)的pH和原子序数的关系如图
所示。下列说法正确的是( )
A.原子半径大小顺序:Z>Y>X
B.五种元素的氢化物均为共价化合物
C.最高价氧化物对应的水化物的酸性:M>N
D.Z的常见氧化物中阴、阳离子个数比均为1∶2
9.[2022·河北唐山期中]化合物A(结构式如图)是重要的药物中间体和分析试剂,化合
物A由原子序数依次增大的短周期元素 X、Y、Z、W组成,W是地壳中分布最广的元素,
下列说法正确的是( )A.Y的氢化物的沸点一定低于W的氢化物的沸点
B.原子半径大小顺序为W>Z>Y>X
C.非金属性强弱顺序为X>W>Y>Z
D.X、Y、Z、W四种元素可形成离子化合物
10.已知a、b、c、d是原子序数依次增大的短周期主族元素,a、c在周期表中的相对
位置如图所示。a元素最低负化合价的绝对值与其原子最外层电子数相等,b元素的简单离
子是同周期元素中半径最小的。下列说法错误的是( )
A.b离子发生水解使溶液呈酸性,c离子发生水解使溶液呈碱性
B.原子半径由小到大的顺序:dY>Z>M>X
B.N的一种氧化物可用作油漆和涂料
C.氢化物的沸点:Z小于M
D.工业上制备W单质的方法为电解熔融的W的氧化物
12.[2022·江西红色七校联考]短周期元素W、X、Y、Z、M原子序数依次增大,元素
W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2-
电子层结构与氖原子相同。
(1)M在元素周期表中的位置是________。
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl 溶液,溶液变
3
血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p
的化学式为______________。
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元素
的原子个数之比为1∶1∶1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双
键,但含极性键和非极性键,q分子的结构式为__________________。
(4)(XY) 的性质与 Cl 相似,(XY) 与 NaOH 溶液常温下反应的离子方程式为
2 2 2
________________________________________________________________________
________________________________________________________________________。
(5)常温下,1 mol Z 能与Y的最简单氢化物反应,生成一种常见的盐和1 mol Z,该反应的
3 2化学方程式为________________________________________________________________。